%ED%8E%A9%ED%83%80%EC%9D%B4%EB%93%9C
-
 카이랄 과학 혁신으로 암질환 치료제부터 인공효소까지
많은 약물은 카이랄 분자로 이루어져 있고 카이랄 분자의 두 거울상(이성질체)은 서로 다른 생물학적 효과를 가질 수 있다. 예를 들면, 하나의 형태는 의학적 효과를 가져올 수 있지만 다른 형태는 독성을 가져올 수 있다. 암 치료 사용 약물은 특정 암세포에만 작용되도록 설계되어 있는데 카이랄성을 활용하면 특정한 형태 약물을 선택적으로 전달할 수 있어 부작용을 줄이고 효과를 극대화할 수 있다. 이런 카이랄성 원리를 통해 암 질환 치료를 위한 약물 전달 등 다양한 분야에서 응용이 가능한 분자과학의 새로운 기술이 개발되었다.
우리 대학 화학과 이희승 교수 연구팀이 원자 수준의 정밀도 로 극미세 나선형 카이랄 통로를 만드는 방법을 발표했다고 19일 밝혔다. 이 통로는 인간 머리카락 직경의 약 5만분의 1에 해당하며, 그 특별한 나선 형태 때문에 특정 분자와만 세밀한 상호작용이 가능하다. 이 기술은 약물의 효율적인 개발부터 첨단 소재 설계에 이르기까지 혁신적인 응용을 가능하게 한다.
연구팀은 자연의 카이랄성 원리에 착안해, 짧은 비천연 펩타이드(아미노산으로 이뤄진 단백질 조각)와 구리 클러스터(다발)를 이용해 규칙적인 나선형 채널을 가진 금속-펩타이드 네트워크를 성공적으로 합성했다. 특히, 연구팀은 카이랄 채널의 세밀한 구조 조절로 이 금속-펩타이드 네트워크가 특정 카이랄성 분자에만 상호작용을 가능하게 만들었으며, 단결정 분석을 통해 이러한 복잡한 상호작용 원리를 명확히 규명했다.
이번 연구에서 연구팀은 기존에 알려진 금속-유기 프레임워크와는 달리, 폴대머(비천연 펩타이드) 기반의 방법을 도입해 3차원 구조 내에서 분자와의 상호작용을 더욱 세밀하게 제어할 수 있는 기술을 선보였다. 이는 분자 공학과 첨단 소재 분야에 새로운 지평을 열 것으로 전망된다.
원자 단위로 정의된 카이랄 채널의 제작은 다양한 분야, 특히 카이랄 촉매, 카이랄 광학센서, 암 질환 치료를 위한 약물 전달 등, 다양한 분야에서의 혁신적인 기술적 발전을 기대하게 한다.
연구를 주도한 이희승 교수는 “이번 연구는 세포막 채널 단백질 또는 효소의 활성부위에서 분자의 기질 특이적 상호작용을 인공적으로 재현하는 노력의 일환으로 시작되었으며, 복잡한 미세 상호작용이 가능하도록 다양한 기능기를 원하는 3차원 위치에 모듈식 치환을 통해 도입할 수 있는 청사진을 제시한 의의가 있다” 고 전하며 “앞으로 약물 전달, 고분자 및 나노기술에 응용이 가능하며 특정 카이랄 반응에 반응하는 인공효소 개발을 위한 핵심 기술로 간주될 것으로 기대된다”며 소감을 밝혔다.
화학과 김재욱 석박사통합과정이 제1 저자로 주도한 이번 연구는 화학소재 분야 최정상급 학술지인 `어드밴스드 머티리얼즈(Advanced Materials, ISSN: 0935-9648 print, 1521-4095 online, Impact Factor: 29.4)' 9월 18일 字 온라인판에 발표됐다.(논문명: Tailoring Enantiomeric Chiral Channels in Metal-Peptide Networks: A Novel Foldamer-Based Approach for Host-Guest Interactions, https://doi.org/10.1002/adma.202305753)
이번 연구는 한국연구재단의 선도연구센터사업(멀티스케일 카이랄구조체 연구센터, CMCA)의 지원으로 진행됐다.
2023.10.19 조회수 13551
카이랄 과학 혁신으로 암질환 치료제부터 인공효소까지
많은 약물은 카이랄 분자로 이루어져 있고 카이랄 분자의 두 거울상(이성질체)은 서로 다른 생물학적 효과를 가질 수 있다. 예를 들면, 하나의 형태는 의학적 효과를 가져올 수 있지만 다른 형태는 독성을 가져올 수 있다. 암 치료 사용 약물은 특정 암세포에만 작용되도록 설계되어 있는데 카이랄성을 활용하면 특정한 형태 약물을 선택적으로 전달할 수 있어 부작용을 줄이고 효과를 극대화할 수 있다. 이런 카이랄성 원리를 통해 암 질환 치료를 위한 약물 전달 등 다양한 분야에서 응용이 가능한 분자과학의 새로운 기술이 개발되었다.
우리 대학 화학과 이희승 교수 연구팀이 원자 수준의 정밀도 로 극미세 나선형 카이랄 통로를 만드는 방법을 발표했다고 19일 밝혔다. 이 통로는 인간 머리카락 직경의 약 5만분의 1에 해당하며, 그 특별한 나선 형태 때문에 특정 분자와만 세밀한 상호작용이 가능하다. 이 기술은 약물의 효율적인 개발부터 첨단 소재 설계에 이르기까지 혁신적인 응용을 가능하게 한다.
연구팀은 자연의 카이랄성 원리에 착안해, 짧은 비천연 펩타이드(아미노산으로 이뤄진 단백질 조각)와 구리 클러스터(다발)를 이용해 규칙적인 나선형 채널을 가진 금속-펩타이드 네트워크를 성공적으로 합성했다. 특히, 연구팀은 카이랄 채널의 세밀한 구조 조절로 이 금속-펩타이드 네트워크가 특정 카이랄성 분자에만 상호작용을 가능하게 만들었으며, 단결정 분석을 통해 이러한 복잡한 상호작용 원리를 명확히 규명했다.
이번 연구에서 연구팀은 기존에 알려진 금속-유기 프레임워크와는 달리, 폴대머(비천연 펩타이드) 기반의 방법을 도입해 3차원 구조 내에서 분자와의 상호작용을 더욱 세밀하게 제어할 수 있는 기술을 선보였다. 이는 분자 공학과 첨단 소재 분야에 새로운 지평을 열 것으로 전망된다.
원자 단위로 정의된 카이랄 채널의 제작은 다양한 분야, 특히 카이랄 촉매, 카이랄 광학센서, 암 질환 치료를 위한 약물 전달 등, 다양한 분야에서의 혁신적인 기술적 발전을 기대하게 한다.
연구를 주도한 이희승 교수는 “이번 연구는 세포막 채널 단백질 또는 효소의 활성부위에서 분자의 기질 특이적 상호작용을 인공적으로 재현하는 노력의 일환으로 시작되었으며, 복잡한 미세 상호작용이 가능하도록 다양한 기능기를 원하는 3차원 위치에 모듈식 치환을 통해 도입할 수 있는 청사진을 제시한 의의가 있다” 고 전하며 “앞으로 약물 전달, 고분자 및 나노기술에 응용이 가능하며 특정 카이랄 반응에 반응하는 인공효소 개발을 위한 핵심 기술로 간주될 것으로 기대된다”며 소감을 밝혔다.
화학과 김재욱 석박사통합과정이 제1 저자로 주도한 이번 연구는 화학소재 분야 최정상급 학술지인 `어드밴스드 머티리얼즈(Advanced Materials, ISSN: 0935-9648 print, 1521-4095 online, Impact Factor: 29.4)' 9월 18일 字 온라인판에 발표됐다.(논문명: Tailoring Enantiomeric Chiral Channels in Metal-Peptide Networks: A Novel Foldamer-Based Approach for Host-Guest Interactions, https://doi.org/10.1002/adma.202305753)
이번 연구는 한국연구재단의 선도연구센터사업(멀티스케일 카이랄구조체 연구센터, CMCA)의 지원으로 진행됐다.
2023.10.19 조회수 13551 -
 암과 치매 등 맞춤형 신약 발굴 플랫폼 개발
우리 대학 화학과 박희성 교수 연구팀이 질병을 유발하는 다양한 바이오마커들에 맞추어 재단하듯이 디자인이 가능한 고리형 펩타이드*기반 신약 발굴 플랫폼 기술을 개발했다고 21일 밝혔다.
*고리형 펩타이드: 기본 선형으로 이루어진 펩타이드를 약리 효과를 높일수 있도록 고리형태의 구조로 만들어진 아미노산 중합체를 지칭함
고리형 펩타이드는 낮은 독성과 뛰어난 약리 활성으로 인해 많은 주목을 받아왔지만 자유롭게 디자인하고 제조하기가 어려워 실제 신약 개발에 활용되기 어려운 단점이 있었다. 박 교수팀은 암을 포함한 다양한 질병들에 대한 치료제 후보물질 발굴에 매우 유용하게 활용될 수 있도록 이러한 고리형 펩타이드의 맞춤형 디자인을 가능하게 하는 신약 발굴 플랫폼 기술을 개발하는데 성공하였다.
우리 몸의 세포에서 만들어지는 단백질들은 다양한 변형을 통해 기능과 활성이 조절되며 이러한 변형은 생체 내에서 세포 신호 전달 등 우리 몸의 정상적인 신진대사 활동을 조절하는 매우 중요한 역할을 한다.
하지만 유전적 또는 환경적 요인으로 인해 단백질 변형이 비정상적으로 일어나면 세포의 신호 전달, 대사 활동 등이 손상되어 암, 치매, 당뇨를 포함한 다양한 중증 질환을 유발한다.
기존에는 이러한 비정상적 단백질 변형을 제어할 수 있는 후보물질의 탐색이 용이하지 않아서 질병의 원인 규명 및 신약 개발 연구에 어려움이 있었다.
박 교수팀은 지난 2016년 다양한 비정상 변형 단백질을 합성할 수 있는 단백질 변형기술을 개발해 `사이언스(Science)' 지에 논문을 발표한 바 있다.
*논문명: A chemical biology route to site-specific authenic protein modifications
연구팀은 기존 연구를 더 발전시켜 질병의 원인이 되는 비정상적인 단백질 변형을 제어할 수 있는 고리형 펩타이드를 효과적으로 디자인하고 탐색하는 스크리닝 플랫폼 기술을 개발했다.
연구팀은 이 기술을 활용해 비정상적인 단백질에 결합하여 다양한 종류의 암을 유발하는 원인으로 알려진 종양 바이오마커인 HDAC8(histone deaceytylase 8)의 활성을 저해하는 고리형 펩타이드를 효과적으로 발굴할 수 있음을 증명했다.
박희성 교수는 "이 기술이 실용화될 경우 다양한 질병에 대한 혁신신약 후보물질 탐색이 실질적으로 가능해질 것으로 전망된다ˮ며 "향후 맞춤형 표적 항암제 및 뇌 신경 치료제 개발 등 글로벌 신약 연구에 새 패러다임을 열 것이다ˮ고 말했다.
이번 연구는 과학기술정보통신부(장관 이종호)가 창의성 기초연구를 촉진하는 개인연구사업 중견연구와 미래 과학기술을 선도하는 연구자를 발굴하는 삼성미래기술육성사업재단(이사장 김성근)의 지원을 받아 수행됐다.
화학과 강덕희 박사와 김도욱 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지인 `앙게반테 케미(Angewandte Chemie International Edition)' 2023년 1월 16일 자 온라인판으로 게재됐다.
*논문명: A Versatile Strategy for Screening Cutson-Designed Warhead-Armed Cyclic Peptide Inhibitors
2023.02.21 조회수 8788
암과 치매 등 맞춤형 신약 발굴 플랫폼 개발
우리 대학 화학과 박희성 교수 연구팀이 질병을 유발하는 다양한 바이오마커들에 맞추어 재단하듯이 디자인이 가능한 고리형 펩타이드*기반 신약 발굴 플랫폼 기술을 개발했다고 21일 밝혔다.
*고리형 펩타이드: 기본 선형으로 이루어진 펩타이드를 약리 효과를 높일수 있도록 고리형태의 구조로 만들어진 아미노산 중합체를 지칭함
고리형 펩타이드는 낮은 독성과 뛰어난 약리 활성으로 인해 많은 주목을 받아왔지만 자유롭게 디자인하고 제조하기가 어려워 실제 신약 개발에 활용되기 어려운 단점이 있었다. 박 교수팀은 암을 포함한 다양한 질병들에 대한 치료제 후보물질 발굴에 매우 유용하게 활용될 수 있도록 이러한 고리형 펩타이드의 맞춤형 디자인을 가능하게 하는 신약 발굴 플랫폼 기술을 개발하는데 성공하였다.
우리 몸의 세포에서 만들어지는 단백질들은 다양한 변형을 통해 기능과 활성이 조절되며 이러한 변형은 생체 내에서 세포 신호 전달 등 우리 몸의 정상적인 신진대사 활동을 조절하는 매우 중요한 역할을 한다.
하지만 유전적 또는 환경적 요인으로 인해 단백질 변형이 비정상적으로 일어나면 세포의 신호 전달, 대사 활동 등이 손상되어 암, 치매, 당뇨를 포함한 다양한 중증 질환을 유발한다.
기존에는 이러한 비정상적 단백질 변형을 제어할 수 있는 후보물질의 탐색이 용이하지 않아서 질병의 원인 규명 및 신약 개발 연구에 어려움이 있었다.
박 교수팀은 지난 2016년 다양한 비정상 변형 단백질을 합성할 수 있는 단백질 변형기술을 개발해 `사이언스(Science)' 지에 논문을 발표한 바 있다.
*논문명: A chemical biology route to site-specific authenic protein modifications
연구팀은 기존 연구를 더 발전시켜 질병의 원인이 되는 비정상적인 단백질 변형을 제어할 수 있는 고리형 펩타이드를 효과적으로 디자인하고 탐색하는 스크리닝 플랫폼 기술을 개발했다.
연구팀은 이 기술을 활용해 비정상적인 단백질에 결합하여 다양한 종류의 암을 유발하는 원인으로 알려진 종양 바이오마커인 HDAC8(histone deaceytylase 8)의 활성을 저해하는 고리형 펩타이드를 효과적으로 발굴할 수 있음을 증명했다.
박희성 교수는 "이 기술이 실용화될 경우 다양한 질병에 대한 혁신신약 후보물질 탐색이 실질적으로 가능해질 것으로 전망된다ˮ며 "향후 맞춤형 표적 항암제 및 뇌 신경 치료제 개발 등 글로벌 신약 연구에 새 패러다임을 열 것이다ˮ고 말했다.
이번 연구는 과학기술정보통신부(장관 이종호)가 창의성 기초연구를 촉진하는 개인연구사업 중견연구와 미래 과학기술을 선도하는 연구자를 발굴하는 삼성미래기술육성사업재단(이사장 김성근)의 지원을 받아 수행됐다.
화학과 강덕희 박사와 김도욱 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지인 `앙게반테 케미(Angewandte Chemie International Edition)' 2023년 1월 16일 자 온라인판으로 게재됐다.
*논문명: A Versatile Strategy for Screening Cutson-Designed Warhead-Armed Cyclic Peptide Inhibitors
2023.02.21 조회수 8788 -
 암 면역치료를 위한 새로운 세포사멸 유도체 개발
우리 대학 생명화학공학과 김유천 교수와 한양대학교 생명공학과 윤채옥 교수 공동연구팀이 암 치료에 이용되는 면역항암제인 면역관문억제제와 협력 효과를 내는 *펩타이드 기반의 면역원성 세포사멸 유도체를 개발했다고 27일 밝혔다.
☞ 펩타이드(peptide): 아미노산이 2~50개 정도 결합된 물질을 뜻하며, 아미노산이 50개 이상 결합된 물질이 단백질이다.
연구팀이 개발한 펩타이드는 암세포 내의 미토콘드리아 외막을 붕괴시켜 활성산소 농도를 높이고, 이를 통해 형성된 산화적 스트레스가 소포체를 자극해 면역원성 세포사멸을 유도한다.
우리 대학 생명화학공학과 정성동 박사와 한양대학교 생명공학과 정보경 박사가 공동 제1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구 결과는 국제 학술지 `어드밴스드 사이언스 (Advanced Science)' 4월 7일 字 표지논문(Back cover)으로 게재됐다. (논문명 : Immunogenic Cell Death Inducing Fluorinated Mitochondria-Disrupting Helical Polypeptide Synergizes with PD-L1 Immune Checkpoint Blockade).
면역관문억제제는 T세포(CTLA-4, PD-1)나 암세포(PD-L1)에 발현된 면역세포의 활성을 저해하는 면역관문을 차단해서 면역세포의 작용을 활발하게 하는 치료제다. 2011년 미국 식품 의약국에 최초로 승인을 받은 후, 다양한 면역관문억제제가 환자들에게 이용되고 있다.
하지만 면역관문억제제도 몇 가지 한계점을 가지고 있다. 먼저 이 치료법은 모든 환자에게 효과가 있는 것이 아니라 10~40% 정도의 환자에게만 효과가 있다. 그리고 기존에 존재하는 항암 능력을 갖춘 T세포가 필요하다는 단점이 있다.
연구팀은 이러한 문제점들을 해결하기 위해 항암 면역반응을 유도하는 면역원성 세포사멸 유도체와 면역관문억제제를 병용투여 해 문제점을 해결하고자 했다.
연구팀은 펩타이드 기반의 면역원성 세포사멸 유도체가 미토콘드리아 외막 붕괴를 통해 세포 내의 활성산소를 과잉생산하고, 이렇게 생성된 산화적 스트레스가 소포체를 자극해 최종적으로 면역원성 세포사멸을 유도하는 것을 검증했다.
또한, 동물실험을 통해 펩타이드와 면역관문억제제인 anti-PD-L1을 병용 투여했을 때, 단독 투여에 비해 종양 억제 능력이 향상되고, 활성화된 면역반응을 통해 폐로의 전이가 줄어드는 것을 확인했다.
연구를 주도한 김유천 교수는 "이번 새로운 면역원성 세포사멸 유도체 개발을 통해, 기존 면역관문억제제의 낮은 반응률을 보이는 암에서 치료 효과를 높일 수 있는 다양한 방법을 제시할 것으로 기대한다ˮ고 말했다.
한편, 이번 연구는 한국연구재단 중견연구자사업과 기초연구실 사업을 통해 수행됐다.
2021.04.27 조회수 32209
암 면역치료를 위한 새로운 세포사멸 유도체 개발
우리 대학 생명화학공학과 김유천 교수와 한양대학교 생명공학과 윤채옥 교수 공동연구팀이 암 치료에 이용되는 면역항암제인 면역관문억제제와 협력 효과를 내는 *펩타이드 기반의 면역원성 세포사멸 유도체를 개발했다고 27일 밝혔다.
☞ 펩타이드(peptide): 아미노산이 2~50개 정도 결합된 물질을 뜻하며, 아미노산이 50개 이상 결합된 물질이 단백질이다.
연구팀이 개발한 펩타이드는 암세포 내의 미토콘드리아 외막을 붕괴시켜 활성산소 농도를 높이고, 이를 통해 형성된 산화적 스트레스가 소포체를 자극해 면역원성 세포사멸을 유도한다.
우리 대학 생명화학공학과 정성동 박사와 한양대학교 생명공학과 정보경 박사가 공동 제1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구 결과는 국제 학술지 `어드밴스드 사이언스 (Advanced Science)' 4월 7일 字 표지논문(Back cover)으로 게재됐다. (논문명 : Immunogenic Cell Death Inducing Fluorinated Mitochondria-Disrupting Helical Polypeptide Synergizes with PD-L1 Immune Checkpoint Blockade).
면역관문억제제는 T세포(CTLA-4, PD-1)나 암세포(PD-L1)에 발현된 면역세포의 활성을 저해하는 면역관문을 차단해서 면역세포의 작용을 활발하게 하는 치료제다. 2011년 미국 식품 의약국에 최초로 승인을 받은 후, 다양한 면역관문억제제가 환자들에게 이용되고 있다.
하지만 면역관문억제제도 몇 가지 한계점을 가지고 있다. 먼저 이 치료법은 모든 환자에게 효과가 있는 것이 아니라 10~40% 정도의 환자에게만 효과가 있다. 그리고 기존에 존재하는 항암 능력을 갖춘 T세포가 필요하다는 단점이 있다.
연구팀은 이러한 문제점들을 해결하기 위해 항암 면역반응을 유도하는 면역원성 세포사멸 유도체와 면역관문억제제를 병용투여 해 문제점을 해결하고자 했다.
연구팀은 펩타이드 기반의 면역원성 세포사멸 유도체가 미토콘드리아 외막 붕괴를 통해 세포 내의 활성산소를 과잉생산하고, 이렇게 생성된 산화적 스트레스가 소포체를 자극해 최종적으로 면역원성 세포사멸을 유도하는 것을 검증했다.
또한, 동물실험을 통해 펩타이드와 면역관문억제제인 anti-PD-L1을 병용 투여했을 때, 단독 투여에 비해 종양 억제 능력이 향상되고, 활성화된 면역반응을 통해 폐로의 전이가 줄어드는 것을 확인했다.
연구를 주도한 김유천 교수는 "이번 새로운 면역원성 세포사멸 유도체 개발을 통해, 기존 면역관문억제제의 낮은 반응률을 보이는 암에서 치료 효과를 높일 수 있는 다양한 방법을 제시할 것으로 기대한다ˮ고 말했다.
한편, 이번 연구는 한국연구재단 중견연구자사업과 기초연구실 사업을 통해 수행됐다.
2021.04.27 조회수 32209 -
 두뇌 인지 기능 조절하는 신경 펩타이드 발견
우리 대학 생명과학과 이승희 교수 연구팀이 두뇌에 존재하는 신경 펩타이드 중 하나인 소마토스타틴(somatostatin)이 두뇌 인지 기능을 높일 수 있음을 밝혔다.
이 교수 연구팀은 특정 가바(뇌세포 대사 기능을 억제 신경 안정 작용을 하는 신경 전달 억제 물질) 분비 신경 세포에서 분비되는 펩타이드 중 하나인 소마토스태틴이 시각 피질의 정보 처리 과정을 조절하고 높일 수 있음을 규명했다. 이번 연구 성과는 치매 등의 뇌 질환에서 인지 능력 회복을 위한 치료제 개발의 계기가 될 것으로 기대된다.
생명과학과 송유향 박사, 황양선 석사, 바이오및뇌공학과 김관수 박사과정, 서울대학교 의과학대학 이형로 박사과정이 공동 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘사이언스 어드밴시스 (Science Advances)’ 4월 22일 자 온라인판에 게재됐다(논문명 : Somatostatin enhances visual processing and perception by modulating excitatory inputs to the parvalbumin-positive interneurons in V1).
2019년 기준 국내 65세 이상 노인 중 10명 중 1명은 치매 질환을 갖고 있다. 치매는 기억력 손실, 인지 기능 및 운동기능 저하 등의 일상생활 장애를 유발해 그 심각성은 나날이 두드러지고 있다.
이승희 교수 연구팀은 치매의 한 종류인 알츠하이머 질환 환자의 뇌척수액에서 소마토스타틴의 발현율이 현저히 감소했다는 점에 주목해 소마토스타틴에 의한 인지 능력 회복 가능성을 밝히는 연구를 수행했다.
소마토스타틴은 인간을 포함한 포유류의 중추신경계에서 존재한다. 특히 정상적인 포유류의 대뇌 피질에서 소마토스타틴을 발현하는 신경 세포인 가바(GABA, γ-aminobutyric acid)를 신경전달물질로 분비해 흥분성 신경 세포의 활성을 억제함으로써 정보 처리 정도를 조율한다.
그러나 기존 연구는 가바의 효과에만 국한돼, 동시에 분비될 수 있는 신경 펩타이드인 소마토스타틴의 고유한 효과 관련 연구는 부족한 상황이다.
연구팀은 자유롭게 움직이는 실험용 생쥐에서 시각정보 인지 및 식별 능력을 측정할 수 있는 실험 장비를 개발 및 도입했다. 이를 통해 생쥐의 시각피질 또는 뇌척수액에 소마토스타틴을 직접 주입한 후 이를 관찰해 생쥐의 시각정보 인지 능력이 현저히 증가함을 발견했다.
나아가 소마토스타틴의 처리에 따른 생체 내 또는 뇌 절편에서의 신경 세포 간 신경전달 효율의 변화를 측정하고, 해당 신경망을 연속 볼록면 주사전자현미경(SBEM)으로 관찰해 소마토스타틴에 의한 시각인지 기능의 향상이 이루어지는 생체 내 신경 생리적 원리를 규명했다.
이러한 연구 성과는 향후 인간을 비롯한 포유류의 두뇌 인지 기능을 조절 가능할 수 있을 뿐 아니라 퇴행성 뇌 질환 등에서 나타나는 인지 기능 장애 치료에 폭넓게 응용 및 적용될 수 있을 것으로 기대된다.
이승희 교수는 “이번 연구는 두뇌 기능을 높이고, 뇌 질환을 치료할 수 있는 새로운 약물 개발로 이어질 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단 중견연구자 지원사업의 지원을 받아 수행됐다.
2020.04.23 조회수 17776
두뇌 인지 기능 조절하는 신경 펩타이드 발견
우리 대학 생명과학과 이승희 교수 연구팀이 두뇌에 존재하는 신경 펩타이드 중 하나인 소마토스타틴(somatostatin)이 두뇌 인지 기능을 높일 수 있음을 밝혔다.
이 교수 연구팀은 특정 가바(뇌세포 대사 기능을 억제 신경 안정 작용을 하는 신경 전달 억제 물질) 분비 신경 세포에서 분비되는 펩타이드 중 하나인 소마토스태틴이 시각 피질의 정보 처리 과정을 조절하고 높일 수 있음을 규명했다. 이번 연구 성과는 치매 등의 뇌 질환에서 인지 능력 회복을 위한 치료제 개발의 계기가 될 것으로 기대된다.
생명과학과 송유향 박사, 황양선 석사, 바이오및뇌공학과 김관수 박사과정, 서울대학교 의과학대학 이형로 박사과정이 공동 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘사이언스 어드밴시스 (Science Advances)’ 4월 22일 자 온라인판에 게재됐다(논문명 : Somatostatin enhances visual processing and perception by modulating excitatory inputs to the parvalbumin-positive interneurons in V1).
2019년 기준 국내 65세 이상 노인 중 10명 중 1명은 치매 질환을 갖고 있다. 치매는 기억력 손실, 인지 기능 및 운동기능 저하 등의 일상생활 장애를 유발해 그 심각성은 나날이 두드러지고 있다.
이승희 교수 연구팀은 치매의 한 종류인 알츠하이머 질환 환자의 뇌척수액에서 소마토스타틴의 발현율이 현저히 감소했다는 점에 주목해 소마토스타틴에 의한 인지 능력 회복 가능성을 밝히는 연구를 수행했다.
소마토스타틴은 인간을 포함한 포유류의 중추신경계에서 존재한다. 특히 정상적인 포유류의 대뇌 피질에서 소마토스타틴을 발현하는 신경 세포인 가바(GABA, γ-aminobutyric acid)를 신경전달물질로 분비해 흥분성 신경 세포의 활성을 억제함으로써 정보 처리 정도를 조율한다.
그러나 기존 연구는 가바의 효과에만 국한돼, 동시에 분비될 수 있는 신경 펩타이드인 소마토스타틴의 고유한 효과 관련 연구는 부족한 상황이다.
연구팀은 자유롭게 움직이는 실험용 생쥐에서 시각정보 인지 및 식별 능력을 측정할 수 있는 실험 장비를 개발 및 도입했다. 이를 통해 생쥐의 시각피질 또는 뇌척수액에 소마토스타틴을 직접 주입한 후 이를 관찰해 생쥐의 시각정보 인지 능력이 현저히 증가함을 발견했다.
나아가 소마토스타틴의 처리에 따른 생체 내 또는 뇌 절편에서의 신경 세포 간 신경전달 효율의 변화를 측정하고, 해당 신경망을 연속 볼록면 주사전자현미경(SBEM)으로 관찰해 소마토스타틴에 의한 시각인지 기능의 향상이 이루어지는 생체 내 신경 생리적 원리를 규명했다.
이러한 연구 성과는 향후 인간을 비롯한 포유류의 두뇌 인지 기능을 조절 가능할 수 있을 뿐 아니라 퇴행성 뇌 질환 등에서 나타나는 인지 기능 장애 치료에 폭넓게 응용 및 적용될 수 있을 것으로 기대된다.
이승희 교수는 “이번 연구는 두뇌 기능을 높이고, 뇌 질환을 치료할 수 있는 새로운 약물 개발로 이어질 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단 중견연구자 지원사업의 지원을 받아 수행됐다.
2020.04.23 조회수 17776 -
 산소 이용해 알츠하이머 유발 단백질 독성 개선
화학과 임미희 교수 연구팀이 공기 중의 산소를 이용해 알츠하이머 유발에 관여하는 단백질의 독성을 개선할 수 있는 화학적 도구를 설계하는 데 성공했다.
연구팀은 알츠하이머 발병에 관여한다고 알려진 구리-아밀로이드 베타 복합체의 응집과 이에 의한 발생한 세포 독성을 개선할 수 있는 화학적 도구를 설계하고, 구리 배위권 이중 변형을 통한 작용 원리를 분자적 수준에서 밝혀냈다.
한지연 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지인 미국 국립과학원회보(PNAS)에 2월 27일 자로 게재됐다.(논문명 : Mechanistic approaches for chemically modifying the coordination sphere of copper-amyloid-β complexes)
전이 금속 중 구리 이온은 항산화 작용과 신경전달물질 생성 등 신체에 필수적인 생리적 기능에 관여한다. 건강한 사람의 뇌와 달리 알츠하이머병 같은 퇴행성 뇌 질환 환자의 뇌에서는 이러한 구리 이온의 항상성이 완전히 무너져있다고 알려져 있다.
알츠하이머 발병에 밀접하게 관계가 있다고 알려진 아밀로이드 베타 펩타이드는 구리 이온과 강하게 결합할 수 있다. 구리 이온은 아밀로이드 베타의 응집을 촉진할 뿐만 아니라, 활성산소를 과다하게 생성해 신경독성을 일으킨다. 따라서 구리-아밀로이드 베타 복합체를 표적하고 그 배위 결합을 효과적으로 막을 수 있는 화학적 접근 기법이 최근 주목받고 있다.
연구팀은 알츠하이머 발병 원리에 직간접적으로 관여하는 구리 이온이 공기 중 산소와 반응할 수 있다는 점을 이용했다. 이에 구리-아밀로이드 베타 복합체와 상호작용할 수 있도록 화합물을 합리적으로 설계하고, 해당분자가 산소가 존재하는 환경에서 구리 배위권에 위치한 특정 아미노산에 결합 및 산화에 의한 이중 변형을 일으킨 것을 확인했다.
연구팀은 연구팀이 개발한 배위권 이중 변형 기법에 따라 구리-아밀로이드 베타의 응집 과정 및 섬유 형성 정도가 확연히 달라짐을 확인했다. 이 기법을 통해 구리 이온의 병리학적 특성 중 하나인 활성산소 생성 정도 또한 두드러지게 개선된 것을 관찰했다.
나아가 기존의 기법과 비교했을 때 구리-아밀로이드 베타 복합체에 의한 세포 독성을 더욱 효과적으로 회복시키는 것으로 나타났다.
이번 연구는 산소의 유무, 전이 금속의 종류, 산화 활성 금속의 산화수, 아밀로이드성 단백질의 종류 등 다양한 변수의 통제를 통해 해당 화합물이 아밀로이드 베타의 구리 배위권을 어떻게 변형시켰는지에 대한 작용 원리를 분자적 수준에서 제안했다는 의의가 있다.
임미희 교수는 “알츠하이머 발병에 관여한다고 알려진 구리 이온이 산소와 반응할 수 있다는 점을 역으로 이용했다”라며 “이번 연구에서 최초로 발표한 단백질 내 구리 배위권 이중 변형 기법을 바탕으로, 다른 퇴행성 뇌질환의 치료제 개발에도 더욱 박차를 가할 수 있을 것이다”라고 말했다.
이번 연구는 한국연구재단과 KAIST의 지원으로 수행됐다.
2020.03.03 조회수 17718
산소 이용해 알츠하이머 유발 단백질 독성 개선
화학과 임미희 교수 연구팀이 공기 중의 산소를 이용해 알츠하이머 유발에 관여하는 단백질의 독성을 개선할 수 있는 화학적 도구를 설계하는 데 성공했다.
연구팀은 알츠하이머 발병에 관여한다고 알려진 구리-아밀로이드 베타 복합체의 응집과 이에 의한 발생한 세포 독성을 개선할 수 있는 화학적 도구를 설계하고, 구리 배위권 이중 변형을 통한 작용 원리를 분자적 수준에서 밝혀냈다.
한지연 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지인 미국 국립과학원회보(PNAS)에 2월 27일 자로 게재됐다.(논문명 : Mechanistic approaches for chemically modifying the coordination sphere of copper-amyloid-β complexes)
전이 금속 중 구리 이온은 항산화 작용과 신경전달물질 생성 등 신체에 필수적인 생리적 기능에 관여한다. 건강한 사람의 뇌와 달리 알츠하이머병 같은 퇴행성 뇌 질환 환자의 뇌에서는 이러한 구리 이온의 항상성이 완전히 무너져있다고 알려져 있다.
알츠하이머 발병에 밀접하게 관계가 있다고 알려진 아밀로이드 베타 펩타이드는 구리 이온과 강하게 결합할 수 있다. 구리 이온은 아밀로이드 베타의 응집을 촉진할 뿐만 아니라, 활성산소를 과다하게 생성해 신경독성을 일으킨다. 따라서 구리-아밀로이드 베타 복합체를 표적하고 그 배위 결합을 효과적으로 막을 수 있는 화학적 접근 기법이 최근 주목받고 있다.
연구팀은 알츠하이머 발병 원리에 직간접적으로 관여하는 구리 이온이 공기 중 산소와 반응할 수 있다는 점을 이용했다. 이에 구리-아밀로이드 베타 복합체와 상호작용할 수 있도록 화합물을 합리적으로 설계하고, 해당분자가 산소가 존재하는 환경에서 구리 배위권에 위치한 특정 아미노산에 결합 및 산화에 의한 이중 변형을 일으킨 것을 확인했다.
연구팀은 연구팀이 개발한 배위권 이중 변형 기법에 따라 구리-아밀로이드 베타의 응집 과정 및 섬유 형성 정도가 확연히 달라짐을 확인했다. 이 기법을 통해 구리 이온의 병리학적 특성 중 하나인 활성산소 생성 정도 또한 두드러지게 개선된 것을 관찰했다.
나아가 기존의 기법과 비교했을 때 구리-아밀로이드 베타 복합체에 의한 세포 독성을 더욱 효과적으로 회복시키는 것으로 나타났다.
이번 연구는 산소의 유무, 전이 금속의 종류, 산화 활성 금속의 산화수, 아밀로이드성 단백질의 종류 등 다양한 변수의 통제를 통해 해당 화합물이 아밀로이드 베타의 구리 배위권을 어떻게 변형시켰는지에 대한 작용 원리를 분자적 수준에서 제안했다는 의의가 있다.
임미희 교수는 “알츠하이머 발병에 관여한다고 알려진 구리 이온이 산소와 반응할 수 있다는 점을 역으로 이용했다”라며 “이번 연구에서 최초로 발표한 단백질 내 구리 배위권 이중 변형 기법을 바탕으로, 다른 퇴행성 뇌질환의 치료제 개발에도 더욱 박차를 가할 수 있을 것이다”라고 말했다.
이번 연구는 한국연구재단과 KAIST의 지원으로 수행됐다.
2020.03.03 조회수 17718 -
 김유천 교수, 암세포 사멸 유도하는 새 방식의 항암제 개발
〈 김유천 교수, 이대용 박사 〉
우리 대학 생명화학공학과 김유천 교수 공동 연구팀이 세포의 이온 항상성을 교란하는 새로운 원리로 암세포 자가사멸을 유도하는 항암제를 개발했다.
연구팀이 개발한 이온 교란 펩타이드는 세포의 활성산소 농도를 급격하게 높이고 소포체에 강력한 스트레스를 부여해 최종적으로 자가사멸을 유도할 수 있다. 또한, 물에 대한 용해성이 좋아 향후 임상에 적용 가능할 것으로 기대된다.
생명화학공학과 이대용 박사와 한양대학교 생명공학과 이수환 박사과정이 공동 1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구결과는 국제 학술지 ‘어드밴스드 사이언스(Advanced Science)’ 7월 17일 자 표지논문(Back cover)으로 게재됐다. (논문명 : A helical polypeptide-based potassium ionophore induces endoplasmic reticulum stress-mediated apoptosis by perturbing ion homeostasis)
세포 안팎의 이온 기울기는 세포 성장 및 대사과정에 중요한 역할을 해, 세포 이온 항상성을 교란하게 되면 세포의 중요한 기능이 억제돼 자가사멸(Apoptosis)을 촉진할 수 있다.
기존의 이온 항상성 교란 물질은 물에 대한 용해도가 낮아 동물 실험에 적용하기 매우 어렵고 이온 항상성 교란을 통한 자가사멸 원리가 구체적으로 밝혀지지 않아 실제 적용에 한계가 있다.
연구팀은 수용성을 지니고 칼륨 이온을 운반할 수 있는 알파나선 펩타이드 기반 항암물질을 개발했다. 펩타이드 끝에 양이온성을 지니며 물에 잘 녹는 친수성이 강한 그룹과 칼륨 이온 운반이 가능한 그룹을 결합해 이온 수송 능력과 친수성을 동시에 지니게 했다.
이 항암 펩타이드는 세포 내의 칼륨 농도를 낮추는 동시에 세포 내 칼슘 농도를 증가시킨다. 증가한 세포 내 칼슘 농도는 세포 내의 활성산소 농도를 크게 높여, 소포체 스트레스를 일으키며 최종적으로 자가사멸을 유도한다.
연구팀은 종양을 이식한 실험용 동물 모델에 새로운 항암물질을 투여해 높은 항암 효과와 소포체 스트레스를 통한 자가사멸 신호를 확인해 암 성장을 저해할 수 있음을 증명했다.
연구를 주도한 이대용 박사는“이온 교란 펩타이드는 세포 내의 활성산소 농도를 크게 높여 세포 자가사멸을 유도하기 때문에 기존의 항암 치료보다 더 효과적일 것으로 기대한다”라고 말했다.
김유천 교수는 “새로운 기작으로 암세포를 사멸하는 항암 펩타이드는 기존 항암요법의 한계점을 대체할 수 있는 새로운 방법으로 사용될 것이라 기대한다”라고 말했다.
이번 연구는 한국연구재단의 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. Advanced Science 표지
그림2. 동물 실험을 통한 소포체 스트레스를 통한 자가사멸 신호 규명
2019.08.01 조회수 19357
김유천 교수, 암세포 사멸 유도하는 새 방식의 항암제 개발
〈 김유천 교수, 이대용 박사 〉
우리 대학 생명화학공학과 김유천 교수 공동 연구팀이 세포의 이온 항상성을 교란하는 새로운 원리로 암세포 자가사멸을 유도하는 항암제를 개발했다.
연구팀이 개발한 이온 교란 펩타이드는 세포의 활성산소 농도를 급격하게 높이고 소포체에 강력한 스트레스를 부여해 최종적으로 자가사멸을 유도할 수 있다. 또한, 물에 대한 용해성이 좋아 향후 임상에 적용 가능할 것으로 기대된다.
생명화학공학과 이대용 박사와 한양대학교 생명공학과 이수환 박사과정이 공동 1 저자로 참여하고, 한양대학교 생명공학과 윤채옥 교수가 공동 교신저자로 참여한 이번 연구결과는 국제 학술지 ‘어드밴스드 사이언스(Advanced Science)’ 7월 17일 자 표지논문(Back cover)으로 게재됐다. (논문명 : A helical polypeptide-based potassium ionophore induces endoplasmic reticulum stress-mediated apoptosis by perturbing ion homeostasis)
세포 안팎의 이온 기울기는 세포 성장 및 대사과정에 중요한 역할을 해, 세포 이온 항상성을 교란하게 되면 세포의 중요한 기능이 억제돼 자가사멸(Apoptosis)을 촉진할 수 있다.
기존의 이온 항상성 교란 물질은 물에 대한 용해도가 낮아 동물 실험에 적용하기 매우 어렵고 이온 항상성 교란을 통한 자가사멸 원리가 구체적으로 밝혀지지 않아 실제 적용에 한계가 있다.
연구팀은 수용성을 지니고 칼륨 이온을 운반할 수 있는 알파나선 펩타이드 기반 항암물질을 개발했다. 펩타이드 끝에 양이온성을 지니며 물에 잘 녹는 친수성이 강한 그룹과 칼륨 이온 운반이 가능한 그룹을 결합해 이온 수송 능력과 친수성을 동시에 지니게 했다.
이 항암 펩타이드는 세포 내의 칼륨 농도를 낮추는 동시에 세포 내 칼슘 농도를 증가시킨다. 증가한 세포 내 칼슘 농도는 세포 내의 활성산소 농도를 크게 높여, 소포체 스트레스를 일으키며 최종적으로 자가사멸을 유도한다.
연구팀은 종양을 이식한 실험용 동물 모델에 새로운 항암물질을 투여해 높은 항암 효과와 소포체 스트레스를 통한 자가사멸 신호를 확인해 암 성장을 저해할 수 있음을 증명했다.
연구를 주도한 이대용 박사는“이온 교란 펩타이드는 세포 내의 활성산소 농도를 크게 높여 세포 자가사멸을 유도하기 때문에 기존의 항암 치료보다 더 효과적일 것으로 기대한다”라고 말했다.
김유천 교수는 “새로운 기작으로 암세포를 사멸하는 항암 펩타이드는 기존 항암요법의 한계점을 대체할 수 있는 새로운 방법으로 사용될 것이라 기대한다”라고 말했다.
이번 연구는 한국연구재단의 중견연구자지원사업을 통해 수행됐다.
□ 그림 설명
그림1. Advanced Science 표지
그림2. 동물 실험을 통한 소포체 스트레스를 통한 자가사멸 신호 규명
2019.08.01 조회수 19357 -
 전상용 교수, 펩타이드-항체 하이브리드 항암제 기반기술 개발
〈 전상용 교수, 유병준 박사과정 〉
우리 대학 생명과학과 전상용 교수와 서울대학교 의과대학 정준호 교수 공동 연구팀이 암 치료를 위한 새로운 펩타이드-항체 복합체(하이브리드) 기술을 개발했다.
연구팀은 두 가지 암 표적에 결합하는 펩타이드를 니코틴의 대사체인 코티닌에 항체와 복합체 형태로 형성함으로써 항암 펩타이드의 약효 지속기간을 늘리는 동시에 암 조직 침투 효능을 높여 효과적으로 암 치료가 가능함을 증명했다.
유병준 박사과정이 1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 ‘앙게반테 케미(Angewandte chemi)’ 1월 26일자 온라인판에 게재됐다 (논문명 : A Hybrid Platform Based on a Bispecific Peptide–Antibody Complex for Targeted Cancer Therapy).
펩타이드 의약품은 상대적으로 크기가 작아 신장을 통해 빠르게 제거돼 혈중 반감기가 짧다. 이로 인해 약효가 반감되거나 약을 자주 투여해야 하는 한계가 있다. 항체 의약품은 혈중 반감기는 길지만 크기가 커 암 조직의 깊은 곳까지 전달되지 않아서 약효가 충분히 발휘하지 못한다.
연구팀은 문제 해결을 위해 새로운 형태의 펩타이드-항체 복합체를 개발했다. 암 조직에 특이적으로 발현되는 표적에 결합하는 펩타이드와 혈관 형성 물질을 억제하는 펩타이드, 그리고 코티닌의 결합체를 합성했다. 이를 항 코티닌 항체와 함께 섞어 두 가지 표적에 특이적인 펩타이드-항원 복합체를 만들었다.
이 결합체는 펩타이드의 암 조직 특이적 결합 및 혈관 형성 물질을 저해하는 특성을 보존하면서도 펩타이드 형태 대비 약 20배 증가한 혈중 반감기를 보였다.
연구팀은 쥐를 이용한 암 동물모델에 투여했을 때 암 조직에 특이적으로 축적되고 표적 부위에서 펩타이드가 항체에서 분리돼 나와 암 조직의 깊은 곳까지 분포하는 것을 확인했다. 이러한 특징을 통해 효과적으로 암의 성장을 억제할 수 있음을 증명했다.
전상용 교수는 “암 치료를 위한 새로운 형태의 펩타이드-항원 복합체 플랫폼을 개발했다”라며 “기존 펩타이드와 항체 의약품이 가지는 한계를 극복할 수 있는 하나의 새로운 플랫폼으로서 향후 다양한 펩타이드 의약품에 적용해 효과적인 암 치료제를 개발하는데 기여할 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단의 리더연구사업 및 글로벌박사펠로우십의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 두 가지 표적에 특이적인 펩타이드-항체 복합체의 모식도
2019.02.18 조회수 11721
전상용 교수, 펩타이드-항체 하이브리드 항암제 기반기술 개발
〈 전상용 교수, 유병준 박사과정 〉
우리 대학 생명과학과 전상용 교수와 서울대학교 의과대학 정준호 교수 공동 연구팀이 암 치료를 위한 새로운 펩타이드-항체 복합체(하이브리드) 기술을 개발했다.
연구팀은 두 가지 암 표적에 결합하는 펩타이드를 니코틴의 대사체인 코티닌에 항체와 복합체 형태로 형성함으로써 항암 펩타이드의 약효 지속기간을 늘리는 동시에 암 조직 침투 효능을 높여 효과적으로 암 치료가 가능함을 증명했다.
유병준 박사과정이 1 저자로 참여한 이번 연구는 화학 분야 국제 학술지 ‘앙게반테 케미(Angewandte chemi)’ 1월 26일자 온라인판에 게재됐다 (논문명 : A Hybrid Platform Based on a Bispecific Peptide–Antibody Complex for Targeted Cancer Therapy).
펩타이드 의약품은 상대적으로 크기가 작아 신장을 통해 빠르게 제거돼 혈중 반감기가 짧다. 이로 인해 약효가 반감되거나 약을 자주 투여해야 하는 한계가 있다. 항체 의약품은 혈중 반감기는 길지만 크기가 커 암 조직의 깊은 곳까지 전달되지 않아서 약효가 충분히 발휘하지 못한다.
연구팀은 문제 해결을 위해 새로운 형태의 펩타이드-항체 복합체를 개발했다. 암 조직에 특이적으로 발현되는 표적에 결합하는 펩타이드와 혈관 형성 물질을 억제하는 펩타이드, 그리고 코티닌의 결합체를 합성했다. 이를 항 코티닌 항체와 함께 섞어 두 가지 표적에 특이적인 펩타이드-항원 복합체를 만들었다.
이 결합체는 펩타이드의 암 조직 특이적 결합 및 혈관 형성 물질을 저해하는 특성을 보존하면서도 펩타이드 형태 대비 약 20배 증가한 혈중 반감기를 보였다.
연구팀은 쥐를 이용한 암 동물모델에 투여했을 때 암 조직에 특이적으로 축적되고 표적 부위에서 펩타이드가 항체에서 분리돼 나와 암 조직의 깊은 곳까지 분포하는 것을 확인했다. 이러한 특징을 통해 효과적으로 암의 성장을 억제할 수 있음을 증명했다.
전상용 교수는 “암 치료를 위한 새로운 형태의 펩타이드-항원 복합체 플랫폼을 개발했다”라며 “기존 펩타이드와 항체 의약품이 가지는 한계를 극복할 수 있는 하나의 새로운 플랫폼으로서 향후 다양한 펩타이드 의약품에 적용해 효과적인 암 치료제를 개발하는데 기여할 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단의 리더연구사업 및 글로벌박사펠로우십의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 두 가지 표적에 특이적인 펩타이드-항체 복합체의 모식도
2019.02.18 조회수 11721 -
 전상용 교수, 건선,아토피 치료용 펩타이드 개발
우리 대학 생명과학과 전상용 교수 연구팀이 피부 전달을 통해 건선을 치료할 수 있는 펩타이드 치료제를 개발했다.
연구팀은 수 년 전 발견한 펩타이드를 나노입자로 제작해 피부를 통해 전달함으로써 동물 모델에서 건선을 치료하는 데 성공했다.
김진용 박사가 1저자로 참여한 이번 연구는 나노분야 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 6월 27일자 온라인 판에 게재됐다.(논문명 :Nanoparticle-Assisted Transcutaneous Delivery of a Signal Transducer and Activator of Transcription 3-Inhibiting Peptide Ameliorates Psoriasis-like Skin Inflammation)
건선은 대표적인 만성 염증성 피부질환으로 전 세계 성인의 약 3%가 앓고 있는 자가 면역질환 중 하나이다. 최근 건선의 원인에 STAT3라는 단백질이 핵심 역할을 한다는 사실이 밝혀졌다.
연구팀은 수 년 전 STAT3라는 단백질의 기능을 저하시킬 수 있는 펩타이드를 최초로 발견해 항암 치료제로 개발한 바 있다. 그러나 건선 피부는 각질층이 매우 두껍기 때문에 피부를 통해 펩타이드를 투과시켜 표적 약물 치료를 하는 데에는 기술적인 한계가 존재했다.
연구팀은 이번 연구에서 길이가 서로 다른 두 개의 인지질과 STAT3 억제 펩타이드가 특정 조건에서 약 30나노미터 크기의 매우 작은 원반 모양의 나노입자를 안정적으로 형성함을 발견했다.
연구팀은 특수 지질성분으로 이뤄진 제형(劑形)을 통해 수십 나노미터 크기의 원판형 나노입자로 이뤄진 STAT3 억제용 펩타이드를 제조했다.
연구팀이 개발한 STAT3 억제 펩타이드는 건선 피부를 가진 동물 모델에 투여했을 때 뛰어난 항염증 효과를 보였고, 건선 발병의 핵심 요소인 각질세포의 과증식과 염증성 싸이토카인인 IL-17 등의 분비를 막는 역할을 했다.
연구팀은 의과학대학원 김필한 교수와의 공동 연구를 통해 펩타이드가 피부 속으로 얼마나 깊이 투과되는지 관찰했고, 이를 통해 나노입자가 각질층을 통과해 진피층 상부까지 전달됨을 확인했다.
전상용 교수는 “STAT3 억제 앱타이드가 난치성 염증성 피부질환인 건선에 대해 우수한 치료 효과를 보이는 바이오 신약 후보물질이 될 수 있음을 확인했다.”며 “효율적인 피부 전달이 가능한 시스템을 구축했다는 점에서 큰 의미가 있으며 향후 임상 적용이 될 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 글로벌연구실사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 앱타이드-지질 나노복합체의 건선 유발 생쥐 귀 모델에서의 치료효능 평가
그림2. 앱타이드-지질 나노복합체의 건선 유발 생쥐모델에서의 피부투과 효능 평가
2018.07.17 조회수 19374
전상용 교수, 건선,아토피 치료용 펩타이드 개발
우리 대학 생명과학과 전상용 교수 연구팀이 피부 전달을 통해 건선을 치료할 수 있는 펩타이드 치료제를 개발했다.
연구팀은 수 년 전 발견한 펩타이드를 나노입자로 제작해 피부를 통해 전달함으로써 동물 모델에서 건선을 치료하는 데 성공했다.
김진용 박사가 1저자로 참여한 이번 연구는 나노분야 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 6월 27일자 온라인 판에 게재됐다.(논문명 :Nanoparticle-Assisted Transcutaneous Delivery of a Signal Transducer and Activator of Transcription 3-Inhibiting Peptide Ameliorates Psoriasis-like Skin Inflammation)
건선은 대표적인 만성 염증성 피부질환으로 전 세계 성인의 약 3%가 앓고 있는 자가 면역질환 중 하나이다. 최근 건선의 원인에 STAT3라는 단백질이 핵심 역할을 한다는 사실이 밝혀졌다.
연구팀은 수 년 전 STAT3라는 단백질의 기능을 저하시킬 수 있는 펩타이드를 최초로 발견해 항암 치료제로 개발한 바 있다. 그러나 건선 피부는 각질층이 매우 두껍기 때문에 피부를 통해 펩타이드를 투과시켜 표적 약물 치료를 하는 데에는 기술적인 한계가 존재했다.
연구팀은 이번 연구에서 길이가 서로 다른 두 개의 인지질과 STAT3 억제 펩타이드가 특정 조건에서 약 30나노미터 크기의 매우 작은 원반 모양의 나노입자를 안정적으로 형성함을 발견했다.
연구팀은 특수 지질성분으로 이뤄진 제형(劑形)을 통해 수십 나노미터 크기의 원판형 나노입자로 이뤄진 STAT3 억제용 펩타이드를 제조했다.
연구팀이 개발한 STAT3 억제 펩타이드는 건선 피부를 가진 동물 모델에 투여했을 때 뛰어난 항염증 효과를 보였고, 건선 발병의 핵심 요소인 각질세포의 과증식과 염증성 싸이토카인인 IL-17 등의 분비를 막는 역할을 했다.
연구팀은 의과학대학원 김필한 교수와의 공동 연구를 통해 펩타이드가 피부 속으로 얼마나 깊이 투과되는지 관찰했고, 이를 통해 나노입자가 각질층을 통과해 진피층 상부까지 전달됨을 확인했다.
전상용 교수는 “STAT3 억제 앱타이드가 난치성 염증성 피부질환인 건선에 대해 우수한 치료 효과를 보이는 바이오 신약 후보물질이 될 수 있음을 확인했다.”며 “효율적인 피부 전달이 가능한 시스템을 구축했다는 점에서 큰 의미가 있으며 향후 임상 적용이 될 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 글로벌연구실사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 앱타이드-지질 나노복합체의 건선 유발 생쥐 귀 모델에서의 치료효능 평가
그림2. 앱타이드-지질 나노복합체의 건선 유발 생쥐모델에서의 피부투과 효능 평가
2018.07.17 조회수 19374 -
 이상엽 특훈교수, 대장균 이용한 나노재료 생물학적 합성법 개발
〈 최 유 진 박사과정, 이 상 엽 특훈교수 〉
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 대장균을 이용해 다양한 나노재료를 생물학적으로 합성할 수 있는 기술을 개발했다.
이번 연구를 통해 기존의 물리, 화학적 방법으로 합성되지 않는 새로운 나노재료도 생물학적으로 합성할 수 있는 가능성을 제시했다.
중앙대학교 박태정 교수 팀과 공동으로 진행하고 우리 대학 최유진 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘미국 국립과학원 회보(PNAS)’ 5월 22일자 온라인 판에 게재됐다.
기존의 생물학적 나노재료는 주로 고온, 고압의 조건에서 합성되고 유독한 유기용매와 값비싼 촉매를 사용하기 때문에 환경오염과 높은 에너지 소모의 문제가 있었다.
대안으로 친환경적이고 경제적인 미생물을 활용한 생물 공학적 나노재료 합성법에 대한 연구가 진행되고 있다. 그러나 현재까지 보고된 합성기술은 나노재료의 종류가 다양하지 않고 결정질과 비결정질 나노재료의 합성 원리가 규명되지 않아 다양한 결정질의 나노재료를 만드는 데 어려움이 있다.
이 교수 연구팀은 유전자 재조합 대장균을 이용해 주기율표 기반의 35개 원소로 이뤄진 60가지의 다양한 나노재료를 친환경적으로 생물학적 합성하는 기술을 개발했다.
다양한 금속 이온과 결합할 수 있는 단백질인 메탈로싸이오닌(metallothionein)과 펩타이드인 파이로킬레틴(phytochelatin)을 합성하는 파이오킬레틴 합성효소(phytochelatin synthase)를 대장균 내에서 동시에 발현해 다양한 나노재료를 합성하는 데 성공했다.
연구팀은 각 원소별 푸베 다이어그램(pourbaix diagram)을 분석해 생물학적 나노재료의 합성 과정에서 열역학적 안정성을 갖는 화학종의 상태를 파악했다. 이를 기반으로 생물학적으로 합성 가능한 물질을 예측 및 생산하는 데 성공했다.
또한 용액의 pH를 조절해 기존 생물학적 합성 조건에서 합성이 불가능하거나 비결정질 나노재료로 합성되는 물질을 합성이 가능하게 만들었다.
연구팀의 이번 연구는 화학적 방법으로 합성하기 어렵거나 아직 보고되지 않은 다양한 나노소재의 종류를 확장시켰다는 의의를 갖는다.
이상엽 특훈교수는 “기존의 물리, 화학적인 공정을 통한 나노재료 합성이 아닌 박테리아를 대사공학적으로 개량한 뒤 생물 공학적 배양을 통해 원하는 나노입자를 쉽고 효율적으로 합성 가능한 기술이다”고 말했다.
또한 “생물공학적 방법으로 합성된 60개의 나노재료들은 나노입자, 나노막대, 나노 판상형 등의 모양을 가지며 향후 에너지, 의료, 환경 분야 등 다양한 산업적 응용이 가능하다”고 말했다.
이번 연구는 과학기술정보통신부 기후변화대응사업의 ‘바이오리파이너리를 위한 시스템대사공학 연구과제’의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 재조합 대장균을 이용한 다양한 나노재료들의 생물학적 합성 기술의 전체 모식도 및 이미지
2018.05.23 조회수 18033
이상엽 특훈교수, 대장균 이용한 나노재료 생물학적 합성법 개발
〈 최 유 진 박사과정, 이 상 엽 특훈교수 〉
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 대장균을 이용해 다양한 나노재료를 생물학적으로 합성할 수 있는 기술을 개발했다.
이번 연구를 통해 기존의 물리, 화학적 방법으로 합성되지 않는 새로운 나노재료도 생물학적으로 합성할 수 있는 가능성을 제시했다.
중앙대학교 박태정 교수 팀과 공동으로 진행하고 우리 대학 최유진 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘미국 국립과학원 회보(PNAS)’ 5월 22일자 온라인 판에 게재됐다.
기존의 생물학적 나노재료는 주로 고온, 고압의 조건에서 합성되고 유독한 유기용매와 값비싼 촉매를 사용하기 때문에 환경오염과 높은 에너지 소모의 문제가 있었다.
대안으로 친환경적이고 경제적인 미생물을 활용한 생물 공학적 나노재료 합성법에 대한 연구가 진행되고 있다. 그러나 현재까지 보고된 합성기술은 나노재료의 종류가 다양하지 않고 결정질과 비결정질 나노재료의 합성 원리가 규명되지 않아 다양한 결정질의 나노재료를 만드는 데 어려움이 있다.
이 교수 연구팀은 유전자 재조합 대장균을 이용해 주기율표 기반의 35개 원소로 이뤄진 60가지의 다양한 나노재료를 친환경적으로 생물학적 합성하는 기술을 개발했다.
다양한 금속 이온과 결합할 수 있는 단백질인 메탈로싸이오닌(metallothionein)과 펩타이드인 파이로킬레틴(phytochelatin)을 합성하는 파이오킬레틴 합성효소(phytochelatin synthase)를 대장균 내에서 동시에 발현해 다양한 나노재료를 합성하는 데 성공했다.
연구팀은 각 원소별 푸베 다이어그램(pourbaix diagram)을 분석해 생물학적 나노재료의 합성 과정에서 열역학적 안정성을 갖는 화학종의 상태를 파악했다. 이를 기반으로 생물학적으로 합성 가능한 물질을 예측 및 생산하는 데 성공했다.
또한 용액의 pH를 조절해 기존 생물학적 합성 조건에서 합성이 불가능하거나 비결정질 나노재료로 합성되는 물질을 합성이 가능하게 만들었다.
연구팀의 이번 연구는 화학적 방법으로 합성하기 어렵거나 아직 보고되지 않은 다양한 나노소재의 종류를 확장시켰다는 의의를 갖는다.
이상엽 특훈교수는 “기존의 물리, 화학적인 공정을 통한 나노재료 합성이 아닌 박테리아를 대사공학적으로 개량한 뒤 생물 공학적 배양을 통해 원하는 나노입자를 쉽고 효율적으로 합성 가능한 기술이다”고 말했다.
또한 “생물공학적 방법으로 합성된 60개의 나노재료들은 나노입자, 나노막대, 나노 판상형 등의 모양을 가지며 향후 에너지, 의료, 환경 분야 등 다양한 산업적 응용이 가능하다”고 말했다.
이번 연구는 과학기술정보통신부 기후변화대응사업의 ‘바이오리파이너리를 위한 시스템대사공학 연구과제’의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 재조합 대장균을 이용한 다양한 나노재료들의 생물학적 합성 기술의 전체 모식도 및 이미지
2018.05.23 조회수 18033 -
 이해신 교수, 와인성분 통해 심장에 정맥주사로 약물 전달 기술 개발
〈 이 해 신 교수 〉
우리 대학 화학과 이해신 교수 연구팀이 와인의 떫은맛을 내는 성분인 탄닌산(tannic acid)을 이용해 간단한 정맥주사만으로도 약물을 심장 조직에 전달할 수 있는 기술을 개발했다.
연구팀은 탄닌산을 단백질, 펩타이드 등의 약물과 혼합시켜 입자화 하는 방법을 통해 심장조직을 표적할 수 있음을 규명했다. 연구팀의 심장 질환의 효율적 치료를 위한 표적화 약물전달 기술은 단백질 기반의 다양한 신약에 적용 가능할 것으로 기대된다.
안전성평가연구소의 예측모델 연구센터 김기석 박사 연구팀과 공동으로 수행된 이번 연구는 네이처 자매지 ‘네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)’ 4월 30일자 온라인 판에 게재됐다.
심장은 인체 내 가장 중요한 기관으로 분당 60~100회의 박동을 하는 동안 약 5리터의 혈액을 뇌를 포함한 전신에 공급하는 역할을 한다. 심장은 심근이라는 근육을 이용해 끊임없이 박동하는 운동성이 높은 기관이다.
심장 및 관련 혈관 질병을 심혈관계-순환계 질환이라고 하는데 이는 우리나라 사망 원인 2위를 차지한다. 고혈압, 당뇨, 고지혈증, 흡연, 비만 등 현대인의 불규칙한 식습관 및 생활습관으로 인해 나타날 수 있다. 대표적으로 심장으로 가는 관상동맥이나 미세한 혈류들이 좁아져 산소 및 영양분 공급이 원활하지 못해 발생하는 심근경색이 있다.
많은 연구자들이 심혈관계 질환 극복을 위한 화학약물요법이나 치료용 단백질 등을 개발하고 있다. 그러나 여전히 직접적인 수술, 카테터 및 스텐트 삽입 등에 의존하고 있으며 일반 정맥주사로 개발된 약물을 심장에 효율적으로 전달하는 기술은 개발되지 않았다.
심장의 강한 운동성으로 인해 정맥으로 주사된 약물이 순환하는 동안 심장으로의 전달 효율이 급격하게 저하되기 때문이다.
문제 해결을 위해 연구팀은 과일 껍질, 견과류, 카카오, 와인 등에 다량으로 존재하는 탄닌산이라는 물질을 이용했다. 탄닌산은 와인의 떫은맛을 내는 폴리페놀 분자의 일종으로 혀에 존재하는 점막 단백질과 결합해 떫은맛을 낸다고 알려져 있다.
연구팀은 탄닌산과 단백질 사이의 강한 분자 간 결합력을 이용해 치료용 단백질, 유전자 전달체인 바이러스 또는 기능성 펩타이드 약물 등을 간단하게 섞어주는 방법으로 입자화에 성공했다. 그리고 이를 주사했을 때 심장을 표적화할 수 있다는 사실을 발견했다.
탄닌산을 이용한 단백질 입자화 기술의 원리는 일종의 ‘분자 수준에서의 코팅’ 기술이다. 입자화된 단백질 복합체 표면에 코팅된 탄닌산이 심장의 기능을 유지하기 위해 밀집돼 있는 엘라스틴 및 콜라겐 단백질과 부가적으로 강한 상호작용을 하며 심장 조직에 부착된 상태로 오랜 시간 머무는 심장 표적화 기술이다.
이러한 탄닌산-단백질 복합체는 단백질만을 주사했을 때와 비교하면 5일 이상 장기적으로 혈관 내에서 순환됨을 확인했다.
이 교수 연구팀은 예전부터 탄닌산을 비롯한 접착성, 코팅성을 갖는 다양한 폴리페놀 재료를 응용해 의료용 생체 재료를 개발해 왔다. 실제로 심근경색 동물 모델에 탄닌산과 섬유아세포 증식인자를 섞어서 만든 약품을 주입하고 4주가 지난 뒤 심근경색이 일어난 크기가 감소했을 뿐 아니라 좌심실 압력 및 심박출량 등이 정상에 가깝게 호전되는 것을 확인했다.
이해신 교수는 “지금까지 심장질환 관련한 많은 약물들이 개발됐음에도 불구하고 상대적으로 약물을 심장에 효율적으로 전달하는 방법은 개발되지 않았다”며 “이번 기술은 기존 약물들을 새롭게 공식화해 개량신약으로 만들 수 있는 원천기술이다”고 말했다.
이번 연구는 연구재단 중견연구자 도약연구, 보건복지부 암정복프로그램, 산업통상자원부의 바이오산업핵심기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 탄닌산으로 제조한 단백질 복합체가 심장 조직에 전달되는 모식도
그림2. 바이러스 유전자 발현 효율 및 치료기능성을 보여주는 연구결과
2018.05.16 조회수 21209
이해신 교수, 와인성분 통해 심장에 정맥주사로 약물 전달 기술 개발
〈 이 해 신 교수 〉
우리 대학 화학과 이해신 교수 연구팀이 와인의 떫은맛을 내는 성분인 탄닌산(tannic acid)을 이용해 간단한 정맥주사만으로도 약물을 심장 조직에 전달할 수 있는 기술을 개발했다.
연구팀은 탄닌산을 단백질, 펩타이드 등의 약물과 혼합시켜 입자화 하는 방법을 통해 심장조직을 표적할 수 있음을 규명했다. 연구팀의 심장 질환의 효율적 치료를 위한 표적화 약물전달 기술은 단백질 기반의 다양한 신약에 적용 가능할 것으로 기대된다.
안전성평가연구소의 예측모델 연구센터 김기석 박사 연구팀과 공동으로 수행된 이번 연구는 네이처 자매지 ‘네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)’ 4월 30일자 온라인 판에 게재됐다.
심장은 인체 내 가장 중요한 기관으로 분당 60~100회의 박동을 하는 동안 약 5리터의 혈액을 뇌를 포함한 전신에 공급하는 역할을 한다. 심장은 심근이라는 근육을 이용해 끊임없이 박동하는 운동성이 높은 기관이다.
심장 및 관련 혈관 질병을 심혈관계-순환계 질환이라고 하는데 이는 우리나라 사망 원인 2위를 차지한다. 고혈압, 당뇨, 고지혈증, 흡연, 비만 등 현대인의 불규칙한 식습관 및 생활습관으로 인해 나타날 수 있다. 대표적으로 심장으로 가는 관상동맥이나 미세한 혈류들이 좁아져 산소 및 영양분 공급이 원활하지 못해 발생하는 심근경색이 있다.
많은 연구자들이 심혈관계 질환 극복을 위한 화학약물요법이나 치료용 단백질 등을 개발하고 있다. 그러나 여전히 직접적인 수술, 카테터 및 스텐트 삽입 등에 의존하고 있으며 일반 정맥주사로 개발된 약물을 심장에 효율적으로 전달하는 기술은 개발되지 않았다.
심장의 강한 운동성으로 인해 정맥으로 주사된 약물이 순환하는 동안 심장으로의 전달 효율이 급격하게 저하되기 때문이다.
문제 해결을 위해 연구팀은 과일 껍질, 견과류, 카카오, 와인 등에 다량으로 존재하는 탄닌산이라는 물질을 이용했다. 탄닌산은 와인의 떫은맛을 내는 폴리페놀 분자의 일종으로 혀에 존재하는 점막 단백질과 결합해 떫은맛을 낸다고 알려져 있다.
연구팀은 탄닌산과 단백질 사이의 강한 분자 간 결합력을 이용해 치료용 단백질, 유전자 전달체인 바이러스 또는 기능성 펩타이드 약물 등을 간단하게 섞어주는 방법으로 입자화에 성공했다. 그리고 이를 주사했을 때 심장을 표적화할 수 있다는 사실을 발견했다.
탄닌산을 이용한 단백질 입자화 기술의 원리는 일종의 ‘분자 수준에서의 코팅’ 기술이다. 입자화된 단백질 복합체 표면에 코팅된 탄닌산이 심장의 기능을 유지하기 위해 밀집돼 있는 엘라스틴 및 콜라겐 단백질과 부가적으로 강한 상호작용을 하며 심장 조직에 부착된 상태로 오랜 시간 머무는 심장 표적화 기술이다.
이러한 탄닌산-단백질 복합체는 단백질만을 주사했을 때와 비교하면 5일 이상 장기적으로 혈관 내에서 순환됨을 확인했다.
이 교수 연구팀은 예전부터 탄닌산을 비롯한 접착성, 코팅성을 갖는 다양한 폴리페놀 재료를 응용해 의료용 생체 재료를 개발해 왔다. 실제로 심근경색 동물 모델에 탄닌산과 섬유아세포 증식인자를 섞어서 만든 약품을 주입하고 4주가 지난 뒤 심근경색이 일어난 크기가 감소했을 뿐 아니라 좌심실 압력 및 심박출량 등이 정상에 가깝게 호전되는 것을 확인했다.
이해신 교수는 “지금까지 심장질환 관련한 많은 약물들이 개발됐음에도 불구하고 상대적으로 약물을 심장에 효율적으로 전달하는 방법은 개발되지 않았다”며 “이번 기술은 기존 약물들을 새롭게 공식화해 개량신약으로 만들 수 있는 원천기술이다”고 말했다.
이번 연구는 연구재단 중견연구자 도약연구, 보건복지부 암정복프로그램, 산업통상자원부의 바이오산업핵심기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 탄닌산으로 제조한 단백질 복합체가 심장 조직에 전달되는 모식도
그림2. 바이러스 유전자 발현 효율 및 치료기능성을 보여주는 연구결과
2018.05.16 조회수 21209 -
 인공 펩타이드를 이용한 3차원 자기조립 분자구조체 개발
- 조각품 같은 유기물 구조체 최초로 구현 -
유기물질로도 다양한 3차원 구조체를 합성할 수 있는 새로운 길이 열려, ‘기능성 인공단백질 개발’의 기초가 될 것으로 전망된다.
우리학교 화학과 이희승 교수팀은 분자의 자기조립 과정에서 서로 다른 세 방향(x, y, z)의 분자간 인력의 미세한 조절이 가능하도록 분자를 디자인하면, 이제까지 만들 수 없었던 다양한 모양의 3차원 유기물 구조체들을 자유자재로 합성할 수 있다는 가설을 실험적으로 구현하는데 성공했다고 28일 밝혔다.
이 연구결과는 생체적합성이 요구되는 의공학이나 재료과학에 광범위하게 응용 가능한 다양한 유기물 소자 개발에 기술적 전기가 마련된 것으로 평가받고 있으며, 미세한 분자기계 개발을 위한 빌딩 블록(building blocks)으로도 활용될 수 있다.
이 교수팀은 베타-펩타이드라는 비천연 펩타이드의 구조적 특징에서 착안한 새로운 자기조립 원리를 개발해 기존 방법으로는 불가능했던 풍차, 꽃잎, 사각막대와 같은 다양한 모양의 새로운 3차원 구조의 유기물 구조체를 합성했다.
아울러 마치 top-down 방식으로 깎아놓은 조각품과 같은 분자구조체들을 bottom-up 방식으로 자유자재로 만들어 낼 수 있는 새로운 길을 열고, 자기조립 과정을 자유자재로 조절할 수 있는 방법론을 확립해 같은 분자로부터 다양한 구조체를 합성할 수 있는 방법을 개발하는데 성공했다.
그동안 무기물 나노물질의 경우 다양한 크기와 모양의 구조를 만드는 방법들이 이미 잘 알려져 있지만, 펩타이드를 비롯한 유기물의 경우에는 자기조립체의 크기와 모양을 제어하는 일은 난제로 인식되어 왔다.
특히, 펩타이드의 경우 원형모양(구, 튜브, 원통형 막대 등)의 구조체 이외에는 만들 수가 없었다.
이 교수는 “이번 기초연구 결과를 바탕으로 기능성 인공 단백질 개발과 응용에 관한 연구를 계속 수행하고 있다”며, “분자기계를 설계하거나 자연계에서 일어나는 자기조립 현상에 대한 이해를 촉진할 수 있는 기폭제가 될 것으로 전망된다”고 말했다.
이번 연구는 한국연구재단(이사장 박찬모) 인터페이스 분자제어 연구센터(선도연구센터, 센터장 김세훈)와 일반연구자 지원사업의 공동지원을 받아 수행됐다. 또한, 연구초기에 KAIST의 고위험고수익(High Risk High Return) Project의 연구지원을 통해 연구초기 아이디어 검증이 가능했다는 점이 주목할 만하다.
한편, 화학과 이희승 교수와 권선범 박사과정 학생이 주도한 이번 연구결과는 화학분야의 세계적인 학술지인 ‘안게반테 케미(Angewante Chemie International Edition)’지 온라인 판 8월 23일자에 게재됐다.
또한, 연구의 중요성을 인정받아 표지논문 및 중요논문으로 동시에 선정됐으며, 미국화학회(American Chemical Society)에서 발간하는 ‘C&EN (Chemical & Engineering News)’지 9월 6일자에 연구결과가 소개됐고, 현재 특허출원 중이다.
2010.09.28 조회수 20581
인공 펩타이드를 이용한 3차원 자기조립 분자구조체 개발
- 조각품 같은 유기물 구조체 최초로 구현 -
유기물질로도 다양한 3차원 구조체를 합성할 수 있는 새로운 길이 열려, ‘기능성 인공단백질 개발’의 기초가 될 것으로 전망된다.
우리학교 화학과 이희승 교수팀은 분자의 자기조립 과정에서 서로 다른 세 방향(x, y, z)의 분자간 인력의 미세한 조절이 가능하도록 분자를 디자인하면, 이제까지 만들 수 없었던 다양한 모양의 3차원 유기물 구조체들을 자유자재로 합성할 수 있다는 가설을 실험적으로 구현하는데 성공했다고 28일 밝혔다.
이 연구결과는 생체적합성이 요구되는 의공학이나 재료과학에 광범위하게 응용 가능한 다양한 유기물 소자 개발에 기술적 전기가 마련된 것으로 평가받고 있으며, 미세한 분자기계 개발을 위한 빌딩 블록(building blocks)으로도 활용될 수 있다.
이 교수팀은 베타-펩타이드라는 비천연 펩타이드의 구조적 특징에서 착안한 새로운 자기조립 원리를 개발해 기존 방법으로는 불가능했던 풍차, 꽃잎, 사각막대와 같은 다양한 모양의 새로운 3차원 구조의 유기물 구조체를 합성했다.
아울러 마치 top-down 방식으로 깎아놓은 조각품과 같은 분자구조체들을 bottom-up 방식으로 자유자재로 만들어 낼 수 있는 새로운 길을 열고, 자기조립 과정을 자유자재로 조절할 수 있는 방법론을 확립해 같은 분자로부터 다양한 구조체를 합성할 수 있는 방법을 개발하는데 성공했다.
그동안 무기물 나노물질의 경우 다양한 크기와 모양의 구조를 만드는 방법들이 이미 잘 알려져 있지만, 펩타이드를 비롯한 유기물의 경우에는 자기조립체의 크기와 모양을 제어하는 일은 난제로 인식되어 왔다.
특히, 펩타이드의 경우 원형모양(구, 튜브, 원통형 막대 등)의 구조체 이외에는 만들 수가 없었다.
이 교수는 “이번 기초연구 결과를 바탕으로 기능성 인공 단백질 개발과 응용에 관한 연구를 계속 수행하고 있다”며, “분자기계를 설계하거나 자연계에서 일어나는 자기조립 현상에 대한 이해를 촉진할 수 있는 기폭제가 될 것으로 전망된다”고 말했다.
이번 연구는 한국연구재단(이사장 박찬모) 인터페이스 분자제어 연구센터(선도연구센터, 센터장 김세훈)와 일반연구자 지원사업의 공동지원을 받아 수행됐다. 또한, 연구초기에 KAIST의 고위험고수익(High Risk High Return) Project의 연구지원을 통해 연구초기 아이디어 검증이 가능했다는 점이 주목할 만하다.
한편, 화학과 이희승 교수와 권선범 박사과정 학생이 주도한 이번 연구결과는 화학분야의 세계적인 학술지인 ‘안게반테 케미(Angewante Chemie International Edition)’지 온라인 판 8월 23일자에 게재됐다.
또한, 연구의 중요성을 인정받아 표지논문 및 중요논문으로 동시에 선정됐으며, 미국화학회(American Chemical Society)에서 발간하는 ‘C&EN (Chemical & Engineering News)’지 9월 6일자에 연구결과가 소개됐고, 현재 특허출원 중이다.
2010.09.28 조회수 20581 -
 최성민교수, 세포막의 탄성특성 변화현상 규명
- 피지컬 리뷰 레터스 7월16일자 게제 -- 새로운 의약품 개발에 중요한 역할을 할 것으로 기대-
우리학교 원자력 및 양자공학과 최성민 교수 연구팀은 세포막을 형성하는 인지질 이중막과 향균 펩타이드의 상호작용에 따른 세포막의 탄성특성 변화 현상을 첨단 중성자 산란 측정을 이용하여 세계 최초로 규명했다.
이번 연구결과는 지난 16일 물리학 분야의 세계적 권위지인 피지컬 리뷰 레터스(Physical Review Letters)에 발표됐다.
최성민 교수와 박사과정 이지환 씨가 주도한 이번 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 원자력연구기반확충사업(원자력기초공동연구소)의 지원을 받아 수행됐다.
세포막은 인지질 분자의 이중막으로 구성되어 있으며, 세포 내부의 물질을 유지하는 방어막 역할과 다양한 기능의 단백질을 함유하고 있는 등 매우 중요한 역할을 담당한다.
세포막을 통한 물질전달, 세포 분열 등 세포에서 일어나는 여러 가지 현상은 세포막과 단백질의 상호작용에 의해 지배되며 세포막은 이러한 과정에서 다양한 형태의 구조적 변화를 겪게 된다.
세포막의 탄성특성, 즉 탄성계수는 세포막이 얼마나 부드럽거나 단단한가를 나타내는 것으로 세포막과 단백질의 상호작용에 따른 탄성특성 변화에 대한 이해는 세포에서 일어나는 여러 가지 과정과 이에 따른 구조적 변화를 이해하는데 매우 중요한 사안이다.
최 교수팀은 펩타이드라는 작은 단백질들이 세포막을 구성하는 인지질 이중막에 흡착되어 인지질 이중막의 구조적 변화를 일으키는 과정에서 인지질 이중막의 탄성특성이 어떻게 변하는가를 중성자 스핀에코 분광법이라는 최첨단 비탄성 중성자 산란 기법을 이용하여 규명했다.
이번 연구결과에 의하면 멜리틴이라는 펩타이드는 그 양이 적을 때는 인지질 이중막 표면에 흡착되어 이중막을 형성하고 있는 인지질 분자들의 정렬도를 저해함으로써 인지질 이중막을 부드럽게 만드는 효과를 보인다.
반대로, 멜리틴의 양이 일정량보다 많아지게 되면 인지질 이중막을 통과하는 구멍을 형성하고 동시에 이중막을 단단하게 만들기 시작하며, 멜리틴에 의해 형성된 인지질 이중막의 구멍이 더욱 많아지게 되면 구멍들이 서로 상호작용을 일으켜 인지질 이중막이 급격하게 단단해짐을 밝혔다.
현재 여타 단백질과 인지질 이중막의 상호작용에 대한 추가적인 연구가 진행되고 있으며, 이러한 현상에 대한 이해는 세포에서의 생명현상에 대한 근본적인 이해와 향후 새로운 의약품 개발에 중요한 역할을 할 것으로 기대된다.
최 교수팀은 최근 중성자 및 X-선 산란을 이용하여 탄소나노튜브 및 나노입자의 자기조립 초구조체 개발 연구를 수행하여 신소재 및 화학분야의 세계적 권위지인 어드밴스드 메터리얼즈(Advanced Materials), 미국화학회지(Journal of the American Chemical Society) 등에 연속적으로 논문을 게재하는 등 연성나노물질 연구에서도 우수한 연구성과를 거두고 있다.
최 교수는 중성자를 이용한 연성나노물질 연구분야에서 국제적 전문성을 인정받고 있으며 대표적인 국제 중성자 협회인 아시아-오세아니아 중성자 산란협회(AONSA)의 총무이사를 담당하고 있다. 또한 최성민 교수와 한국원자력연구원이 공동으로 개발한 하나로 냉중성자 연구시설의 40m 소각중성자산란 장치는 세계 최고수준의 나노구조 측정능력을 갖추고 있어 우리나라 나노소재 연구분야의 발전에 새로운 기회를 제공할 것으로 기대되고 있다.
<용어설명>
❶ 세포막(cell membrane)
세포와 세포 외부의 경계를 짓는 막으로 세포 내의 물질들을 보호하고 세포간 물질 이동을 조절한다. 세포막은 인지질 및 단백질 분자로 구성된 얇고 구조적인 인지질 이중층으로 되어 있으며, 선택적인 투과성을 지닌다.
❷ 펩타이드(Peptide)
아미노산의 중합체이다. 보통 소수의 아미노산이 연결된 형태를 펩타이드라 부르고 많은 아미노산이 연결되면 단백질로 부른다.
❸ 멜리틴(melittin)벌 독에서 분리한 26개의 아미노산으로 구성된 단백질로 10∼20년 전에 그 성분과 역할이 알려져 항균물질로 사용된다.
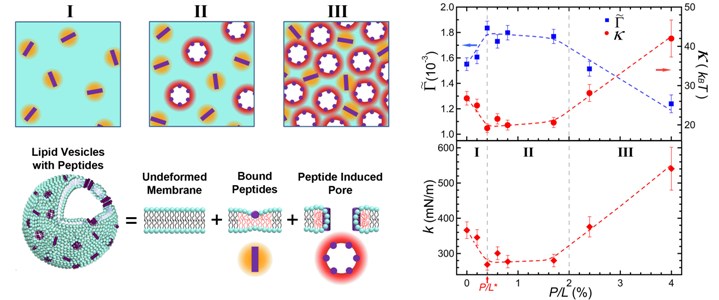
[그림]세포막을 구성하는 인지질 이중막에 멜리틴 펩타이드가 흡착되어 형성하는 구조의 각 단계별 모식도 (왼쪽). 멜리틴 펩타이드 양의 증가에 따른 인지질 이중막의 각 단계별 탄성특성 변화 (오른쪽).
2010.07.19 조회수 22340
최성민교수, 세포막의 탄성특성 변화현상 규명
- 피지컬 리뷰 레터스 7월16일자 게제 -- 새로운 의약품 개발에 중요한 역할을 할 것으로 기대-
우리학교 원자력 및 양자공학과 최성민 교수 연구팀은 세포막을 형성하는 인지질 이중막과 향균 펩타이드의 상호작용에 따른 세포막의 탄성특성 변화 현상을 첨단 중성자 산란 측정을 이용하여 세계 최초로 규명했다.
이번 연구결과는 지난 16일 물리학 분야의 세계적 권위지인 피지컬 리뷰 레터스(Physical Review Letters)에 발표됐다.
최성민 교수와 박사과정 이지환 씨가 주도한 이번 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 원자력연구기반확충사업(원자력기초공동연구소)의 지원을 받아 수행됐다.
세포막은 인지질 분자의 이중막으로 구성되어 있으며, 세포 내부의 물질을 유지하는 방어막 역할과 다양한 기능의 단백질을 함유하고 있는 등 매우 중요한 역할을 담당한다.
세포막을 통한 물질전달, 세포 분열 등 세포에서 일어나는 여러 가지 현상은 세포막과 단백질의 상호작용에 의해 지배되며 세포막은 이러한 과정에서 다양한 형태의 구조적 변화를 겪게 된다.
세포막의 탄성특성, 즉 탄성계수는 세포막이 얼마나 부드럽거나 단단한가를 나타내는 것으로 세포막과 단백질의 상호작용에 따른 탄성특성 변화에 대한 이해는 세포에서 일어나는 여러 가지 과정과 이에 따른 구조적 변화를 이해하는데 매우 중요한 사안이다.
최 교수팀은 펩타이드라는 작은 단백질들이 세포막을 구성하는 인지질 이중막에 흡착되어 인지질 이중막의 구조적 변화를 일으키는 과정에서 인지질 이중막의 탄성특성이 어떻게 변하는가를 중성자 스핀에코 분광법이라는 최첨단 비탄성 중성자 산란 기법을 이용하여 규명했다.
이번 연구결과에 의하면 멜리틴이라는 펩타이드는 그 양이 적을 때는 인지질 이중막 표면에 흡착되어 이중막을 형성하고 있는 인지질 분자들의 정렬도를 저해함으로써 인지질 이중막을 부드럽게 만드는 효과를 보인다.
반대로, 멜리틴의 양이 일정량보다 많아지게 되면 인지질 이중막을 통과하는 구멍을 형성하고 동시에 이중막을 단단하게 만들기 시작하며, 멜리틴에 의해 형성된 인지질 이중막의 구멍이 더욱 많아지게 되면 구멍들이 서로 상호작용을 일으켜 인지질 이중막이 급격하게 단단해짐을 밝혔다.
현재 여타 단백질과 인지질 이중막의 상호작용에 대한 추가적인 연구가 진행되고 있으며, 이러한 현상에 대한 이해는 세포에서의 생명현상에 대한 근본적인 이해와 향후 새로운 의약품 개발에 중요한 역할을 할 것으로 기대된다.
최 교수팀은 최근 중성자 및 X-선 산란을 이용하여 탄소나노튜브 및 나노입자의 자기조립 초구조체 개발 연구를 수행하여 신소재 및 화학분야의 세계적 권위지인 어드밴스드 메터리얼즈(Advanced Materials), 미국화학회지(Journal of the American Chemical Society) 등에 연속적으로 논문을 게재하는 등 연성나노물질 연구에서도 우수한 연구성과를 거두고 있다.
최 교수는 중성자를 이용한 연성나노물질 연구분야에서 국제적 전문성을 인정받고 있으며 대표적인 국제 중성자 협회인 아시아-오세아니아 중성자 산란협회(AONSA)의 총무이사를 담당하고 있다. 또한 최성민 교수와 한국원자력연구원이 공동으로 개발한 하나로 냉중성자 연구시설의 40m 소각중성자산란 장치는 세계 최고수준의 나노구조 측정능력을 갖추고 있어 우리나라 나노소재 연구분야의 발전에 새로운 기회를 제공할 것으로 기대되고 있다.
<용어설명>
❶ 세포막(cell membrane)
세포와 세포 외부의 경계를 짓는 막으로 세포 내의 물질들을 보호하고 세포간 물질 이동을 조절한다. 세포막은 인지질 및 단백질 분자로 구성된 얇고 구조적인 인지질 이중층으로 되어 있으며, 선택적인 투과성을 지닌다.
❷ 펩타이드(Peptide)
아미노산의 중합체이다. 보통 소수의 아미노산이 연결된 형태를 펩타이드라 부르고 많은 아미노산이 연결되면 단백질로 부른다.
❸ 멜리틴(melittin)벌 독에서 분리한 26개의 아미노산으로 구성된 단백질로 10∼20년 전에 그 성분과 역할이 알려져 항균물질로 사용된다.
[그림]세포막을 구성하는 인지질 이중막에 멜리틴 펩타이드가 흡착되어 형성하는 구조의 각 단계별 모식도 (왼쪽). 멜리틴 펩타이드 양의 증가에 따른 인지질 이중막의 각 단계별 탄성특성 변화 (오른쪽).
2010.07.19 조회수 22340