%EB%87%8C%EC%A2%85%EC%96%91
-
 장내 미생물로 난치성 뇌종양 면역치료 효과 높인다
우리 몸의 면역세포인 T세포를 활성화시켜 암세포를 제거하도록 유도하는 첨단 치료법인 ‘면역항암제’는 가장 치명적인 뇌종양 ‘교모세포종(Glioblastoma)’에는 거의 반응하지 않고, 치료에 대한 저항성이 높아 단독 치료로는 효과가 매우 제한적이라는 한계가 있었다. 이에 우리 연구진이 장내 미생물과 그 대사산물을 활용해 뇌종양의 면역치료 효과를 높일 수 있는 새로운 치료 전략을 세계 최초로 입증했다. 향후 미생물을 기반으로 한 면역치료 보완제 개발에 대한 가능성도 보여줬다.
우리 대학 생명과학과 이흥규 교수 연구팀이 장내 미생물 생태계 변화에 주목해 교모세포종 면역치료의 효율을 크게 높이는 방법을 발굴하고 이를 입증했다고 1일 밝혔다.
연구팀은 교모세포종이 진행되면서 장내에서 중요한 아미노산인 ‘트립토판(tryptophan)’의 농도가 급격히 줄어들고, 이로 인해 장내 미생물 생태계가 변화한다는 점에 주목했다. 그리고 트립토판을 보충해 미생물 다양성을 회복시키면, 특정 유익한 균주가 면역세포 중 하나인 CD8 T세포를 활성화하고 종양 조직으로 다시 유도하는 역할을 한다는 사실을 밝혀냈다.
연구팀은 생쥐 교모세포종 모델을 통해, 트립토판을 보충하면 암을 공격하는 T세포(특히 CD8 T세포)의 반응이 향상되고, 이들이 림프절과 뇌 등 종양이 있는 부위로 더 많이 이동한다는 사실을 확인했다.
이 과정에서 장내에 존재하는 유익한 공생균인 ‘던카니엘라 두보시(Duncaniella dubosii)’가 핵심적인 역할을 한다는 점도 밝혀냈다. 해당 균주는 T세포가 몸 안에서 효과적으로 재분포하도록 도와줬고, 면역항암제(anti-PD-1)와 함께 사용할 때 생존율이 유의미하게 향상됐다.
또한, 장내 미생물이 전혀 없는 무균 생쥐에게 위 공생균을 단독으로 투입해도 교모세포종에 대한 생존율이 높아졌으며, 이는 이 균주가 트립토판을 활용해 장내 환경을 조절하고, 그 과정에서 생성되는 대사산물이 CD8 T세포의 암세포 공격 능력을 강화하기 때문임이 입증됐다.
이흥규 교수는 “이번 연구는 면역관문억제제가 효과를 보이지 않았던 난치성 뇌종양에서도, 장내 미생물을 활용한 병용 전략을 통해 치료 반응을 유의하게 높일 수 있음을 보여준 의미 있는 성과”라고 설명했다.
우리 대학 김현철 박사(現, 생명과학연구소 박사후연구원)가 제1 저자로 참여했고 연구 결과는 생명과학 분야 국제 학술지‘셀 리포츠(Cell Reports)’에 지난 6월 26 일자 온라인판에 게재됐다.
(논문명: Gut microbiota dysbiosis induced by brain tumor modulates the efficacy of immunotherapy, https://doi.org/10.1016/j.celrep.2025.115825)
한편, 이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
2025.07.01 조회수 177
장내 미생물로 난치성 뇌종양 면역치료 효과 높인다
우리 몸의 면역세포인 T세포를 활성화시켜 암세포를 제거하도록 유도하는 첨단 치료법인 ‘면역항암제’는 가장 치명적인 뇌종양 ‘교모세포종(Glioblastoma)’에는 거의 반응하지 않고, 치료에 대한 저항성이 높아 단독 치료로는 효과가 매우 제한적이라는 한계가 있었다. 이에 우리 연구진이 장내 미생물과 그 대사산물을 활용해 뇌종양의 면역치료 효과를 높일 수 있는 새로운 치료 전략을 세계 최초로 입증했다. 향후 미생물을 기반으로 한 면역치료 보완제 개발에 대한 가능성도 보여줬다.
우리 대학 생명과학과 이흥규 교수 연구팀이 장내 미생물 생태계 변화에 주목해 교모세포종 면역치료의 효율을 크게 높이는 방법을 발굴하고 이를 입증했다고 1일 밝혔다.
연구팀은 교모세포종이 진행되면서 장내에서 중요한 아미노산인 ‘트립토판(tryptophan)’의 농도가 급격히 줄어들고, 이로 인해 장내 미생물 생태계가 변화한다는 점에 주목했다. 그리고 트립토판을 보충해 미생물 다양성을 회복시키면, 특정 유익한 균주가 면역세포 중 하나인 CD8 T세포를 활성화하고 종양 조직으로 다시 유도하는 역할을 한다는 사실을 밝혀냈다.
연구팀은 생쥐 교모세포종 모델을 통해, 트립토판을 보충하면 암을 공격하는 T세포(특히 CD8 T세포)의 반응이 향상되고, 이들이 림프절과 뇌 등 종양이 있는 부위로 더 많이 이동한다는 사실을 확인했다.
이 과정에서 장내에 존재하는 유익한 공생균인 ‘던카니엘라 두보시(Duncaniella dubosii)’가 핵심적인 역할을 한다는 점도 밝혀냈다. 해당 균주는 T세포가 몸 안에서 효과적으로 재분포하도록 도와줬고, 면역항암제(anti-PD-1)와 함께 사용할 때 생존율이 유의미하게 향상됐다.
또한, 장내 미생물이 전혀 없는 무균 생쥐에게 위 공생균을 단독으로 투입해도 교모세포종에 대한 생존율이 높아졌으며, 이는 이 균주가 트립토판을 활용해 장내 환경을 조절하고, 그 과정에서 생성되는 대사산물이 CD8 T세포의 암세포 공격 능력을 강화하기 때문임이 입증됐다.
이흥규 교수는 “이번 연구는 면역관문억제제가 효과를 보이지 않았던 난치성 뇌종양에서도, 장내 미생물을 활용한 병용 전략을 통해 치료 반응을 유의하게 높일 수 있음을 보여준 의미 있는 성과”라고 설명했다.
우리 대학 김현철 박사(現, 생명과학연구소 박사후연구원)가 제1 저자로 참여했고 연구 결과는 생명과학 분야 국제 학술지‘셀 리포츠(Cell Reports)’에 지난 6월 26 일자 온라인판에 게재됐다.
(논문명: Gut microbiota dysbiosis induced by brain tumor modulates the efficacy of immunotherapy, https://doi.org/10.1016/j.celrep.2025.115825)
한편, 이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
2025.07.01 조회수 177 -
 짠 음식의 뇌종양 악화 유발 원인 세계 최초 밝혀
짠 음식을 자주 섭취하는 식습관이 건강에 해롭다는 것은 널리 알려진 사실이다. 그런데 최근 KAIST 연구진은 짠 음식이 뇌종양까지 악화시킬 수 있다는 사실을 세계 최초로, “왜 나빠지는지", "무엇이 그 과정을 유도하는지", "어떤 유전자가, 어떤 단백질이 작용하는지"까지 분자적 인과관계를 입증해 주목받고 있다.
우리 대학 생명과학과 이흥규 교수 연구팀이 고염식이 장내 미생물 구성을 변화시키고, 이로 인해 증식이 증대된 미생물에 의해 분비되는 대사물질인‘프로피오네이트(propionate)‘가 장내에 과도하게 축적되어 뇌종양을 악화시킨다는 사실을 밝혀냈다.
연구팀은 뇌종양 마우스 모델을 이용한 실험에서 이 같은 사실을 입증했다. 마우스에게 4주간 짠 사료를 섭취하게 한 뒤 종양세포를 주입하자 일반식이 그룹에 비해 생존율이 크게 낮아지고 종양 크기가 증가하는 것을 확인했다. 이어 항생제로 장내 미생물을 제거하거나, 무균 마우스에 분변(고염사료 섭취한 사람의 대변에 해당되는 마우스 분변 샘플) 미생물을 이식하는 실험에서도 유사한 뇌종양 악화 반응이 관찰되었다. 이는 장내 미생물 변화가 뇌종양 악화의 핵심 요인임을 보여주는 증거이다.
특히, 연구팀은 장내 미생물 중 박테로이드 불가투스(Bacteroides vulgatus)라는 균이 고염식이에 따라 증가하고, 이 균이 프로피오네이트(propionate)라는 효소(Pccb)의 발현을 높인다는 사실을 발견했다.
그 결과, 장내에서 프로피오네이트 농도가 비정상적으로 상승했으며, 이 물질은 뇌종양 세포에서 산소가 충분한데도 마치 부족한 것처럼 ‘저산소유도인자-1알파(HIF-1α)’를 활성화시켰다. 이는 다시 ‘형질전환성장인자-베타(TGF-β)’를 증가시켜 제1형 콜라겐(COL1A1)을 과하게 만들게 하여 종양 세포가 더 쉽게 퍼지고 악성도를 높이게 하였다.
이러한 분자적 기전은 실제 뇌종양 중 가장 악성도가 높은 교모세포종(Glioblastoma) 환자의 암세포 데이터 분석을 통해서 임상 적용 가능성을 제시하였다. 마우스와 인간 종양세포에서 공통적으로 발현된 관련 유전자들로 인해 환자의 생존율이 낮아짐을 보여주었다.
이흥규 교수는 “이번 연구는 짠 음식 섭취가 장내 미생물 생태계를 변화시키고, 그 결과 생성된 대사산물이 뇌종양을 악화시킬 수 있음을 세계 최초로 분자 수준에서 규명한 것”이라며, “향후 뇌종양 환자를 대상으로 한 식이 조절 연구와 장내 미생물 기반 치료 전략 개발의 기초 자료로 활용될 수 있을 것”이라고 밝혔다.
공동 제1 저자로는 KAIST 김채원 박사(현. 미국 하버드 의과대학 부속 보스턴 어린이병원 박사후연구원)와 김현진 박사(KAIST 생명과학연구소 박사후연구원)가 참여했으며, 연구 결과는 생의학 분야 권위 학술지인 저널 어브 익스페리멘탈 메디슨(Journal of Experimental Medicine)에 5월 22일 자에 게재됐다.
논문 : Gut dysbiosis from high-salt diet promotes glioma via propionate-mediated TGF-β activation https://doi.org/10.1084/jem.20241135
이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
2025.06.02 조회수 1112
짠 음식의 뇌종양 악화 유발 원인 세계 최초 밝혀
짠 음식을 자주 섭취하는 식습관이 건강에 해롭다는 것은 널리 알려진 사실이다. 그런데 최근 KAIST 연구진은 짠 음식이 뇌종양까지 악화시킬 수 있다는 사실을 세계 최초로, “왜 나빠지는지", "무엇이 그 과정을 유도하는지", "어떤 유전자가, 어떤 단백질이 작용하는지"까지 분자적 인과관계를 입증해 주목받고 있다.
우리 대학 생명과학과 이흥규 교수 연구팀이 고염식이 장내 미생물 구성을 변화시키고, 이로 인해 증식이 증대된 미생물에 의해 분비되는 대사물질인‘프로피오네이트(propionate)‘가 장내에 과도하게 축적되어 뇌종양을 악화시킨다는 사실을 밝혀냈다.
연구팀은 뇌종양 마우스 모델을 이용한 실험에서 이 같은 사실을 입증했다. 마우스에게 4주간 짠 사료를 섭취하게 한 뒤 종양세포를 주입하자 일반식이 그룹에 비해 생존율이 크게 낮아지고 종양 크기가 증가하는 것을 확인했다. 이어 항생제로 장내 미생물을 제거하거나, 무균 마우스에 분변(고염사료 섭취한 사람의 대변에 해당되는 마우스 분변 샘플) 미생물을 이식하는 실험에서도 유사한 뇌종양 악화 반응이 관찰되었다. 이는 장내 미생물 변화가 뇌종양 악화의 핵심 요인임을 보여주는 증거이다.
특히, 연구팀은 장내 미생물 중 박테로이드 불가투스(Bacteroides vulgatus)라는 균이 고염식이에 따라 증가하고, 이 균이 프로피오네이트(propionate)라는 효소(Pccb)의 발현을 높인다는 사실을 발견했다.
그 결과, 장내에서 프로피오네이트 농도가 비정상적으로 상승했으며, 이 물질은 뇌종양 세포에서 산소가 충분한데도 마치 부족한 것처럼 ‘저산소유도인자-1알파(HIF-1α)’를 활성화시켰다. 이는 다시 ‘형질전환성장인자-베타(TGF-β)’를 증가시켜 제1형 콜라겐(COL1A1)을 과하게 만들게 하여 종양 세포가 더 쉽게 퍼지고 악성도를 높이게 하였다.
이러한 분자적 기전은 실제 뇌종양 중 가장 악성도가 높은 교모세포종(Glioblastoma) 환자의 암세포 데이터 분석을 통해서 임상 적용 가능성을 제시하였다. 마우스와 인간 종양세포에서 공통적으로 발현된 관련 유전자들로 인해 환자의 생존율이 낮아짐을 보여주었다.
이흥규 교수는 “이번 연구는 짠 음식 섭취가 장내 미생물 생태계를 변화시키고, 그 결과 생성된 대사산물이 뇌종양을 악화시킬 수 있음을 세계 최초로 분자 수준에서 규명한 것”이라며, “향후 뇌종양 환자를 대상으로 한 식이 조절 연구와 장내 미생물 기반 치료 전략 개발의 기초 자료로 활용될 수 있을 것”이라고 밝혔다.
공동 제1 저자로는 KAIST 김채원 박사(현. 미국 하버드 의과대학 부속 보스턴 어린이병원 박사후연구원)와 김현진 박사(KAIST 생명과학연구소 박사후연구원)가 참여했으며, 연구 결과는 생의학 분야 권위 학술지인 저널 어브 익스페리멘탈 메디슨(Journal of Experimental Medicine)에 5월 22일 자에 게재됐다.
논문 : Gut dysbiosis from high-salt diet promotes glioma via propionate-mediated TGF-β activation https://doi.org/10.1084/jem.20241135
이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
2025.06.02 조회수 1112 -
 교모세포종 암의 씨앗‘전암 세포’첫 규명·정조준했다
교모세포종(Glioblastoma)은 가장 공격적이고 예후가 나쁜 대표적 악성 뇌종양으로, 광범위한 뇌 절제술을 포함한 표준 치료 후에도 1년 이내 대부분 재발하며 생존률이 매우 낮은 치명적인 질환이다. KAIST 연구진이 교모세포종에 암세포로 발전하는 가능성을 가진 전암세포가 있다는 것을 최초로 밝혔다.
우리 대학 의과학대학원 이정호 교수 연구팀은 세계 최초로 교모세포종의 진화와 재발 및 치료 저항성의 근원이 되는 ‘전암세포(Precancerous cell)’를 규명했다.
이정호 교수 연구팀은 2018년 교모세포종이 뇌 깊은 곳에 있는 돌연변이 줄기세포로부터 시작된다는 것을 최초로 밝혀내며 ‘네이쳐(Nature)’지에 게재한 바 있다. 이번 연구에서는 암의 씨앗과 같은 ‘전암 세포’가 어디서 유래하는지, 즉, 돌연변이 기원 세포가 어떻게 분화되는지를 규명하였고 이 전암 세포가 종양 내 세부 유형의 암세포들을 만들어 암이 재발하는 중심축 역할을 한다는 사실도 밝혔다.
특히, 교모세포종 같은 악성 뇌종양에서는 암세포들이 매우 다양한 형태로 공존하고, 각각이 치료에 다르게 반응하는데, 이를 ‘종양 내 이질성’(intratumoral heterogeneity)이라고 한다. 이 이질성은 교모세포종 치료의 가장 큰 걸림돌로 꼽히는데, 이번 연구는 종양 내 이질성 현상을 일으키는 뿌리가 전암세포 때문이라는 것을 세계 최초로 밝혀낸 것이다.
이번 연구를 통해 교모세포종의 전암세포를 표적으로 삼아 암 진화와 재발을 효과적으로 억제할 수 있는 새로운 치료 패러다임의 기초를 마련할 것으로 예상된다. 이는 기존의 암 세포 자체를 겨냥한 치료에서 벗어나 악성 뇌종양의 근원인 전암 세포를 선제적으로 제거함으로써 암의 진화와 재발을 막는 정밀 맞춤형 치료가 가능할 것으로 평가된다.
이를 바탕으로, 교원창업기업 소바젠(주) (대표이사 박철원)은 암 진화와 재발을 억제하는 교모세포종 RNA 치료제 혁신 신약을 연구 개발하고 있다.
여성 의사 과학자이자 논문의 단독 제1 저자인 KAIST 의과학대학원 김현정 박사(현, 고려대학교 의과대학 교수)는 “전암세포는 종양을 더욱 복잡하고 공격적인 형태로 진화시키는 ‘암 이질성의 씨앗’과 같은 존재이다”라며, “이 전암세포를 이해하고 표적화하는 것이 교모세포종을 근본적으로 극복할 열쇠가 될 수 있다”라고 설명했다.
해당 논문은 암 분야 세계적 권위지인 ‘캔서 디스커버리(Cancer Discovery, IF=30.6)’지에 4월 16일 字로 게재됐다.
※ 논문명: Precancerous cells initiate glioblastoma evolution and contribute to intratumoral heterogeneity DOI: https://doi.org/10.1158/2159-8290.CD-24-0234
※ 저자정보: 김현정(카이스트 의과학대학원, 현 고려대학교 의과대학, 제1 저자), 이정호(카이스트 의과학대학원, 소바젠, 교신저자)
한편, 이번 연구는 한국연구재단, 서경배과학재단 등의 지원을 받아 수행됐다.
2025.04.21 조회수 3541
교모세포종 암의 씨앗‘전암 세포’첫 규명·정조준했다
교모세포종(Glioblastoma)은 가장 공격적이고 예후가 나쁜 대표적 악성 뇌종양으로, 광범위한 뇌 절제술을 포함한 표준 치료 후에도 1년 이내 대부분 재발하며 생존률이 매우 낮은 치명적인 질환이다. KAIST 연구진이 교모세포종에 암세포로 발전하는 가능성을 가진 전암세포가 있다는 것을 최초로 밝혔다.
우리 대학 의과학대학원 이정호 교수 연구팀은 세계 최초로 교모세포종의 진화와 재발 및 치료 저항성의 근원이 되는 ‘전암세포(Precancerous cell)’를 규명했다.
이정호 교수 연구팀은 2018년 교모세포종이 뇌 깊은 곳에 있는 돌연변이 줄기세포로부터 시작된다는 것을 최초로 밝혀내며 ‘네이쳐(Nature)’지에 게재한 바 있다. 이번 연구에서는 암의 씨앗과 같은 ‘전암 세포’가 어디서 유래하는지, 즉, 돌연변이 기원 세포가 어떻게 분화되는지를 규명하였고 이 전암 세포가 종양 내 세부 유형의 암세포들을 만들어 암이 재발하는 중심축 역할을 한다는 사실도 밝혔다.
특히, 교모세포종 같은 악성 뇌종양에서는 암세포들이 매우 다양한 형태로 공존하고, 각각이 치료에 다르게 반응하는데, 이를 ‘종양 내 이질성’(intratumoral heterogeneity)이라고 한다. 이 이질성은 교모세포종 치료의 가장 큰 걸림돌로 꼽히는데, 이번 연구는 종양 내 이질성 현상을 일으키는 뿌리가 전암세포 때문이라는 것을 세계 최초로 밝혀낸 것이다.
이번 연구를 통해 교모세포종의 전암세포를 표적으로 삼아 암 진화와 재발을 효과적으로 억제할 수 있는 새로운 치료 패러다임의 기초를 마련할 것으로 예상된다. 이는 기존의 암 세포 자체를 겨냥한 치료에서 벗어나 악성 뇌종양의 근원인 전암 세포를 선제적으로 제거함으로써 암의 진화와 재발을 막는 정밀 맞춤형 치료가 가능할 것으로 평가된다.
이를 바탕으로, 교원창업기업 소바젠(주) (대표이사 박철원)은 암 진화와 재발을 억제하는 교모세포종 RNA 치료제 혁신 신약을 연구 개발하고 있다.
여성 의사 과학자이자 논문의 단독 제1 저자인 KAIST 의과학대학원 김현정 박사(현, 고려대학교 의과대학 교수)는 “전암세포는 종양을 더욱 복잡하고 공격적인 형태로 진화시키는 ‘암 이질성의 씨앗’과 같은 존재이다”라며, “이 전암세포를 이해하고 표적화하는 것이 교모세포종을 근본적으로 극복할 열쇠가 될 수 있다”라고 설명했다.
해당 논문은 암 분야 세계적 권위지인 ‘캔서 디스커버리(Cancer Discovery, IF=30.6)’지에 4월 16일 字로 게재됐다.
※ 논문명: Precancerous cells initiate glioblastoma evolution and contribute to intratumoral heterogeneity DOI: https://doi.org/10.1158/2159-8290.CD-24-0234
※ 저자정보: 김현정(카이스트 의과학대학원, 현 고려대학교 의과대학, 제1 저자), 이정호(카이스트 의과학대학원, 소바젠, 교신저자)
한편, 이번 연구는 한국연구재단, 서경배과학재단 등의 지원을 받아 수행됐다.
2025.04.21 조회수 3541 -
 난치성 뇌종양 치료의 새로운 가능성 열다
면역항암제는 암세포를 제거하는 T세포의 항암 면역작용을 강화하는 가장 주목받는 항암치료 요법이다. 하지만 난치성 뇌종양인 교모세포종의 경우 면역관문억제제를 활용한 수차례 임상시험에서 그 효과를 확인할 수 없었다. 우리 연구진이 난치성 암종에서 T세포가 만성적 항원에 노출되어 기능이 상실되거나 약화된 원인을 분석하여 T세포 활성 제어 인자를 발굴하고 치료 효능 증진 원리를 규명했다.
우리 대학 생명과학과 이흥규 교수 연구팀이 한국화학연구원(원장 이영국) 감염병예방진단기술연구센터와 협력하여, 교모세포종 실험 쥐 모델에서 억제성 Fc 감마수용체(FcγRIIB)의 결손을 통한 면역관문억제제의 세포독성 T세포 불응성을 회복해, 항암 작용 증대를 유도함으로 생존율 개선 효능을 확인했다고 6일 밝혔다.
연구팀은 최근 세포독성 T세포에서 발견된 억제 수용체(FcγRIIB)가 종양 침윤 세포독성 T세포의 특성과 면역관문억제제(항 PD-1)의 치료 효능에 미치는 영향을 확인했다.
연구 결과, 억제 수용체(FcγRIIB)가 결손되었을때 종양항원 특이적 기억 T세포의 증가를 유도했다. 이 같은 T세포 아형은 탈진화를 억제하고 줄기세포 특성을 강화했고, 이를 통한 항 PD-1 치료의 회복된 T세포 항암 면역반응을 이끌었다. 또한, 연구팀은 항원 특이적 기억 T세포가 FcγRIIB 결손 시 상대적으로 높은 수의 증가와 함께 지속적인 종양 조직 내 T세포 침투를 이끈다는 결과를 확인했다.
해당 연구는 면역관문억제제에 불응성을 보이는 종양에 대한 새로운 치료 타깃을 제시했으며, 특히 교모세포종과 같은 항 PD-1 치료에 반응하지 않는 종양에 FcγRIIB 억제와 항 PD-1 치료를 병행함으로써 시너지 효과를 발휘할 수 있음을 증명했다.
연구팀은 이러한 FcγRIIB 억제를 통한 항암 면역작용 증진 전략이 면역관문억제제의 효능을 높이는 데 중요한 기여를 할 것으로 기대하고 있다.
생명과학과 이흥규 교수는 “면역관문 치료제를 이용한 뇌종양 치료 임상 실패를 극복할 가능성과 다른 난치성 종양으로의 범용적 적용 가능성을 제시한 결과로 추후 세포독성 T 세포의 종양 세포치료 활용과 접근 가능성도 확인한 결과”라고 소개했다.
우리 대학 구근본 박사(現, 한국화학연구원 감염병예방진단기술연구센터 선임연구원)가 제1 저자로 참여한 이번 연구는 암 면역치료 학회(Society for Immunotherapy of Cancer)에서 발간하는 종양면역 및 치료 분야 국제 학술지 `Journal for ImmunoTherapy of Cancer'에 10월 26일 온라인판에 게재됐다. (논문명: Inhibitory Fcγ receptor deletion enhances CD8 T cell stemness increasing anti-PD-1 therapy responsiveness against glioblastoma, http://dx.doi.org/10.1136/jitc-2024-009449)
한편 이번 연구는 한국연구재단 개인기초연구사업, 바이오의료기술개발사업 및 삼성미래육성재단의 지원을 받아 수행됐다.
2024.11.06 조회수 5780
난치성 뇌종양 치료의 새로운 가능성 열다
면역항암제는 암세포를 제거하는 T세포의 항암 면역작용을 강화하는 가장 주목받는 항암치료 요법이다. 하지만 난치성 뇌종양인 교모세포종의 경우 면역관문억제제를 활용한 수차례 임상시험에서 그 효과를 확인할 수 없었다. 우리 연구진이 난치성 암종에서 T세포가 만성적 항원에 노출되어 기능이 상실되거나 약화된 원인을 분석하여 T세포 활성 제어 인자를 발굴하고 치료 효능 증진 원리를 규명했다.
우리 대학 생명과학과 이흥규 교수 연구팀이 한국화학연구원(원장 이영국) 감염병예방진단기술연구센터와 협력하여, 교모세포종 실험 쥐 모델에서 억제성 Fc 감마수용체(FcγRIIB)의 결손을 통한 면역관문억제제의 세포독성 T세포 불응성을 회복해, 항암 작용 증대를 유도함으로 생존율 개선 효능을 확인했다고 6일 밝혔다.
연구팀은 최근 세포독성 T세포에서 발견된 억제 수용체(FcγRIIB)가 종양 침윤 세포독성 T세포의 특성과 면역관문억제제(항 PD-1)의 치료 효능에 미치는 영향을 확인했다.
연구 결과, 억제 수용체(FcγRIIB)가 결손되었을때 종양항원 특이적 기억 T세포의 증가를 유도했다. 이 같은 T세포 아형은 탈진화를 억제하고 줄기세포 특성을 강화했고, 이를 통한 항 PD-1 치료의 회복된 T세포 항암 면역반응을 이끌었다. 또한, 연구팀은 항원 특이적 기억 T세포가 FcγRIIB 결손 시 상대적으로 높은 수의 증가와 함께 지속적인 종양 조직 내 T세포 침투를 이끈다는 결과를 확인했다.
해당 연구는 면역관문억제제에 불응성을 보이는 종양에 대한 새로운 치료 타깃을 제시했으며, 특히 교모세포종과 같은 항 PD-1 치료에 반응하지 않는 종양에 FcγRIIB 억제와 항 PD-1 치료를 병행함으로써 시너지 효과를 발휘할 수 있음을 증명했다.
연구팀은 이러한 FcγRIIB 억제를 통한 항암 면역작용 증진 전략이 면역관문억제제의 효능을 높이는 데 중요한 기여를 할 것으로 기대하고 있다.
생명과학과 이흥규 교수는 “면역관문 치료제를 이용한 뇌종양 치료 임상 실패를 극복할 가능성과 다른 난치성 종양으로의 범용적 적용 가능성을 제시한 결과로 추후 세포독성 T 세포의 종양 세포치료 활용과 접근 가능성도 확인한 결과”라고 소개했다.
우리 대학 구근본 박사(現, 한국화학연구원 감염병예방진단기술연구센터 선임연구원)가 제1 저자로 참여한 이번 연구는 암 면역치료 학회(Society for Immunotherapy of Cancer)에서 발간하는 종양면역 및 치료 분야 국제 학술지 `Journal for ImmunoTherapy of Cancer'에 10월 26일 온라인판에 게재됐다. (논문명: Inhibitory Fcγ receptor deletion enhances CD8 T cell stemness increasing anti-PD-1 therapy responsiveness against glioblastoma, http://dx.doi.org/10.1136/jitc-2024-009449)
한편 이번 연구는 한국연구재단 개인기초연구사업, 바이오의료기술개발사업 및 삼성미래육성재단의 지원을 받아 수행됐다.
2024.11.06 조회수 5780 -
 뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
2023.10.16 조회수 7048
뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
2023.10.16 조회수 7048 -
 악성 뇌종양 탐지 대식세포 발견 및 기능 규명
뇌에서 발생하는 악성 종양인 교모세포종은 미국에서만 매년 1만 명 이상의 환자가 발생하지만 최근 주목받는 면역치료제도 유의미한 효과를 보지 못한, 치료가 매우 어려운 암 중 하나다. 국내 연구진은 이러한 교모세포종에 대한 면역반응을 증가시키는 *대식세포와 그 작용 기전을 밝혀 새로운 면역치료법의 가능성을 열었다.
☞ 대식세포: 세포 찌꺼기, 이물질, 미생물, 암세포 등을 집어삼켜서 분해하는 식세포작용을 하는 백혈구의 한 유형
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 내에서 항암 면역반응에 중요한 대식세포를 찾고, 이 세포가 *세포독성 T 세포를 활성화하고 *포식작용으로 암세포를 제거할 수 있다는 것을 발견했다고 4일 밝혔다.
☞ 세포독성 T 세포: 바이러스에 감염된 체세포나 종양 세포를 파괴하는, 흉선에서 유래한 림프구
☞ 포식작용: 세균이나 죽은 세포 등 체내의 이물질을 섭취하여 제거하는 작용
교모세포종 환자는 진단 후 평균 생존 기간이 8개월에 불과하며 5년 이상 생존율은 6.8%로 매우 낮은 수준이다. 종양 치료를 위한 활발한 연구로 면역관문 치료제 등 다양한 치료법이 개발돼 지난 30년간 전체 암 환자의 생존율이 20% 가까이 증가했지만, 교모세포종 환자의 생존율 증가는 2%에 그쳤다.
종양 내 면역세포의 상당수를 차지하는 대식세포는 일반적으로 종양을 제거하는 대신 종양 환경에 적응해 종양세포의 성장 및 전이를 돕고 다른 면역세포들의 활성 및 작용을 억제해 항암 면역반응을 감소시킨다고 알려져 있다. 최근 흑색종 등에서 큰 효과를 나타내는 면역관문 치료제가 교모세포종 치료에서는 효과가 거의 없다는 것이 보고됐는데, 그 이유 중 하나로 손꼽히는 것이 이러한 면역 억제성 대식세포의 과다한 유입이다. 하지만 최근 보고된 연구 결과들은 종양 내 대식세포는 매우 다양한 표현형을 나타내는 여러 대식세포 아형으로 나눌 수 있으며, 이 세포들이 면역관문 치료제 등이 효과를 나타내는 데에 중요하다고 밝혔다.
이 교수 연구팀은 미국 국립암연구소(National Cancer Institute, NCI)와 국립인간유전체연구소(National Human Genome Research Institute, NHGRI)에서 운영하는 암 유전체 아틀라스(The Cancer Genome Atlas, TCGA)에 공개된 교모세포종 환자의 유전자 발현을 비교해 교모세포종 내에서 항암 면역반응을 증가시키는 대식세포의 마커로 CD169 유전자를 발굴하고, 마우스 교모세포종 모델을 사용해 CD169 단백질을 발현하는 대식세포가 없으면 항암 면역반응이 감소해 마우스의 생존이 감소하는 것을 밝혔다.
특히 연구팀은 CD169를 발현하는 대식세포가 세포독성 T 세포의 종양 내 유입에 중요한 CXCL10과 같은 *케모카인을 증가시켜 활성화된 T 세포의 종양 내 유입을 증가시킨다는 것을 밝혔다. 또한, CD169는 이 대식세포의 마커일 뿐 아니라 암세포에 대한 포식작용을 증가시키는 기능을 하며, CD169로 인해 포식작용이 증가한 대식세포는 암세포 특이적인 세포독성 T 세포의 활성을 직접 증가시키는 것을 밝혔다.
☞ 케모카인(chemokine): 백혈구 유주작용, 활성화 작용을 하는 단백질
이 교수는 "이번 연구 결과는 교모세포종에 대한 항암 면역반응에 중요한 대식세포의 마커를 발굴한 것뿐만 아니라, 이들 대식세포가 항암 면역반응을 증가시키는 기전을 확인해 면역관문 치료제의 효과를 높이는 복합치료제 개발에 실마리를 제공할 수 있을 것으로 기대한다ˮ고 밝혔다.
의과학대학원 연수연구원 김현진 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)' 10월 20일 字 온라인판에 게재됐다. (논문명: Blood monocyte-derived CD169⁺ macrophages contribute to antitumor immunity against glioblastoma)
한편 이번 연구는 삼성미래기술육성재단 및 한국연구재단의 지원을 받아 수행됐다.
2022.11.04 조회수 10813
악성 뇌종양 탐지 대식세포 발견 및 기능 규명
뇌에서 발생하는 악성 종양인 교모세포종은 미국에서만 매년 1만 명 이상의 환자가 발생하지만 최근 주목받는 면역치료제도 유의미한 효과를 보지 못한, 치료가 매우 어려운 암 중 하나다. 국내 연구진은 이러한 교모세포종에 대한 면역반응을 증가시키는 *대식세포와 그 작용 기전을 밝혀 새로운 면역치료법의 가능성을 열었다.
☞ 대식세포: 세포 찌꺼기, 이물질, 미생물, 암세포 등을 집어삼켜서 분해하는 식세포작용을 하는 백혈구의 한 유형
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 내에서 항암 면역반응에 중요한 대식세포를 찾고, 이 세포가 *세포독성 T 세포를 활성화하고 *포식작용으로 암세포를 제거할 수 있다는 것을 발견했다고 4일 밝혔다.
☞ 세포독성 T 세포: 바이러스에 감염된 체세포나 종양 세포를 파괴하는, 흉선에서 유래한 림프구
☞ 포식작용: 세균이나 죽은 세포 등 체내의 이물질을 섭취하여 제거하는 작용
교모세포종 환자는 진단 후 평균 생존 기간이 8개월에 불과하며 5년 이상 생존율은 6.8%로 매우 낮은 수준이다. 종양 치료를 위한 활발한 연구로 면역관문 치료제 등 다양한 치료법이 개발돼 지난 30년간 전체 암 환자의 생존율이 20% 가까이 증가했지만, 교모세포종 환자의 생존율 증가는 2%에 그쳤다.
종양 내 면역세포의 상당수를 차지하는 대식세포는 일반적으로 종양을 제거하는 대신 종양 환경에 적응해 종양세포의 성장 및 전이를 돕고 다른 면역세포들의 활성 및 작용을 억제해 항암 면역반응을 감소시킨다고 알려져 있다. 최근 흑색종 등에서 큰 효과를 나타내는 면역관문 치료제가 교모세포종 치료에서는 효과가 거의 없다는 것이 보고됐는데, 그 이유 중 하나로 손꼽히는 것이 이러한 면역 억제성 대식세포의 과다한 유입이다. 하지만 최근 보고된 연구 결과들은 종양 내 대식세포는 매우 다양한 표현형을 나타내는 여러 대식세포 아형으로 나눌 수 있으며, 이 세포들이 면역관문 치료제 등이 효과를 나타내는 데에 중요하다고 밝혔다.
이 교수 연구팀은 미국 국립암연구소(National Cancer Institute, NCI)와 국립인간유전체연구소(National Human Genome Research Institute, NHGRI)에서 운영하는 암 유전체 아틀라스(The Cancer Genome Atlas, TCGA)에 공개된 교모세포종 환자의 유전자 발현을 비교해 교모세포종 내에서 항암 면역반응을 증가시키는 대식세포의 마커로 CD169 유전자를 발굴하고, 마우스 교모세포종 모델을 사용해 CD169 단백질을 발현하는 대식세포가 없으면 항암 면역반응이 감소해 마우스의 생존이 감소하는 것을 밝혔다.
특히 연구팀은 CD169를 발현하는 대식세포가 세포독성 T 세포의 종양 내 유입에 중요한 CXCL10과 같은 *케모카인을 증가시켜 활성화된 T 세포의 종양 내 유입을 증가시킨다는 것을 밝혔다. 또한, CD169는 이 대식세포의 마커일 뿐 아니라 암세포에 대한 포식작용을 증가시키는 기능을 하며, CD169로 인해 포식작용이 증가한 대식세포는 암세포 특이적인 세포독성 T 세포의 활성을 직접 증가시키는 것을 밝혔다.
☞ 케모카인(chemokine): 백혈구 유주작용, 활성화 작용을 하는 단백질
이 교수는 "이번 연구 결과는 교모세포종에 대한 항암 면역반응에 중요한 대식세포의 마커를 발굴한 것뿐만 아니라, 이들 대식세포가 항암 면역반응을 증가시키는 기전을 확인해 면역관문 치료제의 효과를 높이는 복합치료제 개발에 실마리를 제공할 수 있을 것으로 기대한다ˮ고 밝혔다.
의과학대학원 연수연구원 김현진 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)' 10월 20일 字 온라인판에 게재됐다. (논문명: Blood monocyte-derived CD169⁺ macrophages contribute to antitumor immunity against glioblastoma)
한편 이번 연구는 삼성미래기술육성재단 및 한국연구재단의 지원을 받아 수행됐다.
2022.11.04 조회수 10813 -
 의과학대학원 이흥규 교수팀, 새로운 뇌종양 면역반응 규명
뇌종양 세포가 주변의 산소를 먹어 치우며 면역세포를 무력화시키는 과정이 밝혀졌다. 후천성 면역세포에 의해 인식될 표지도 만들지 않는 뇌종양 세포가 선천성 면역세포조차 회피하는 비결이 밝혀진 것이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 악성 뇌종양 세포의 과도한 산소소비로 인한 감마델타 T 세포의 면역반응 저하 과정을 규명했다고 16일 밝혔다.
이번 연구 결과로 왕성하게 증식하며 주변 산소를 빠르게 소비하는 뇌종양 세포로의 산소유입을 막는 방식이 면역항암치료제의 낮은 반응성을 보완할 실마리가 될 것으로 기대된다.
연구팀은 뇌종양의 악성도가 높을수록 감마델타 T 세포의 종양 내 유입이 적고 저산소 환경은 심한 것을 알아냈다. 반면 감마델타 T 세포가 많이 유입될수록 환자의 예후가 좋은 것으로 나타났다. 종양에 대항하는 면역세포로 잘 알려진 후천성 T 세포가 아닌 선천성 T 세포인 감마델타 T 세포의 활성에 주목하게 된 이유다.
이에 연구팀은 저산소 환경을 해소해 감마델타 T 세포에 적절한 산소를 공급, 세포의 생존을 도우면 면역반응이 정상화 될 것이라는 가설을 세웠다.
실제 감마델타 T 세포는 스트레스에 노출된 뇌종양 세포 표면에 많이 생기는 리간드(NKG2DL)를 직접 인식하는 수용체(NKG2D)가 있어 종양에 대항한 면역반응의 새로운 주체로 주목받았지만 기대만큼의 효과를 내지 못하고 있었다.
연구팀이 실제 뇌종양 생쥐모델에 뇌종양의 과도한 산소대사를 막을 화합물(메트포르민)을 감마델타 T 세포와 함께 투여하자, 면역세포의 종양조직 내 침투가 늘고 생존률이 향상됐다. 감마델타 T세포의 저산소 환경을 해소하자, 항종양 면역반응이 개선된 것이다.
한편 감마델타 T 세포의 항 뇌종양 면역반응 기전을 규명하고 감마델타 T 세포의 면역반응을 증대시킬 방안을 제시한 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오의료기술개발사업(차세대바이오사업) 및 삼성미래기술육성재단의 지원으로 수행됐으며 면역학 분야 국제학술지 ‘네이처 이뮤놀로지(Nature Immunology)’ 2월 11일 자에 게재됐다.
2021.02.16 조회수 80061
의과학대학원 이흥규 교수팀, 새로운 뇌종양 면역반응 규명
뇌종양 세포가 주변의 산소를 먹어 치우며 면역세포를 무력화시키는 과정이 밝혀졌다. 후천성 면역세포에 의해 인식될 표지도 만들지 않는 뇌종양 세포가 선천성 면역세포조차 회피하는 비결이 밝혀진 것이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 악성 뇌종양 세포의 과도한 산소소비로 인한 감마델타 T 세포의 면역반응 저하 과정을 규명했다고 16일 밝혔다.
이번 연구 결과로 왕성하게 증식하며 주변 산소를 빠르게 소비하는 뇌종양 세포로의 산소유입을 막는 방식이 면역항암치료제의 낮은 반응성을 보완할 실마리가 될 것으로 기대된다.
연구팀은 뇌종양의 악성도가 높을수록 감마델타 T 세포의 종양 내 유입이 적고 저산소 환경은 심한 것을 알아냈다. 반면 감마델타 T 세포가 많이 유입될수록 환자의 예후가 좋은 것으로 나타났다. 종양에 대항하는 면역세포로 잘 알려진 후천성 T 세포가 아닌 선천성 T 세포인 감마델타 T 세포의 활성에 주목하게 된 이유다.
이에 연구팀은 저산소 환경을 해소해 감마델타 T 세포에 적절한 산소를 공급, 세포의 생존을 도우면 면역반응이 정상화 될 것이라는 가설을 세웠다.
실제 감마델타 T 세포는 스트레스에 노출된 뇌종양 세포 표면에 많이 생기는 리간드(NKG2DL)를 직접 인식하는 수용체(NKG2D)가 있어 종양에 대항한 면역반응의 새로운 주체로 주목받았지만 기대만큼의 효과를 내지 못하고 있었다.
연구팀이 실제 뇌종양 생쥐모델에 뇌종양의 과도한 산소대사를 막을 화합물(메트포르민)을 감마델타 T 세포와 함께 투여하자, 면역세포의 종양조직 내 침투가 늘고 생존률이 향상됐다. 감마델타 T세포의 저산소 환경을 해소하자, 항종양 면역반응이 개선된 것이다.
한편 감마델타 T 세포의 항 뇌종양 면역반응 기전을 규명하고 감마델타 T 세포의 면역반응을 증대시킬 방안을 제시한 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오의료기술개발사업(차세대바이오사업) 및 삼성미래기술육성재단의 지원으로 수행됐으며 면역학 분야 국제학술지 ‘네이처 이뮤놀로지(Nature Immunology)’ 2월 11일 자에 게재됐다.
2021.02.16 조회수 80061 -
 고현용 연구원, 뇌전증 동반하는 소아 뇌종양 근본원인 밝혀
〈 고 현 용 연구원 〉
우리 대학 의과학대학원 고현용 연구원(지도교수 : 이정호 교수)이 난치성 뇌전증(간질 발작)을 일으키는 소아 뇌종양의 근본 원인과 뇌전증 발생의 원리를 규명해 새로운 치료법을 제시했다.
이번 연구 결과를 통해 수술 치료에 어려움이 있는 소아 뇌종양 기반의 난치성 뇌전증 치료에 큰 기여를 할 수 있을 것으로 기대된다.
고현용 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 메디슨(Nature Medicine)’ 9월 17일자 온라인 판에 게재됐다. (논문명: 비라프 체성 돌연변이가 소아뇌종양의 본질적 뇌전증 발생에 기여함; BRAF somatic mutation contributes to intrinsic epileptogenicity in pediatric brain tumors)
소아 뇌종양은 성인 뇌종양에 비해 난치성 뇌전증이 빈번하게 동반되는 특징을 갖고 있다. 그러나 소아 뇌종양에서 특이적으로 난치성 뇌전증이 발생하는 원인에 대해서는 밝혀진 바가 없으며 현존하는 항 뇌전증 약물에 반응하지 않기 때문에 환자의 치료에 많은 어려움을 겪고 있다.
연구팀은 소아 뇌종양 환지 뇌 조직 및 동물 모델의 분자 유전학적 분석을 통해 태아의 뇌 발달과정 중 신경 줄기 세포에 ‘비라프 (BRAF V600E)’라는 돌연변이가 발생하면서 난치성 뇌전증이 동반된 소아 뇌종양이 발생하는 것을 규명했다.
연구팀은 뇌전증이 동반된 소아 뇌종양 중 하나인 신경절 교세포종 환자의 종양 조직을 분자 유전학적으로 분석한 결과 비라프 유전변이가 태아 뇌 발달 과정 중 발생함을 확인했다.
이 변이를 동물 모델에서 구현해 신경절 교세포종의 병리 양상을 재현하고 발작을 관찰해 소아 뇌종양 기반의 뇌전증 치료용 동물 모델을 최초로 확립했다.
이를 이용해 면역 염색 분석과 전사체 분석을 실시했다. 소아 뇌종양에서 발생하는 난치성 뇌전증이 신경세포에 존재하는 비라프 변이로 인해 발생하고, 교세포에 존재하는 변이는 종양 덩어리를 형성하는데 중요한 역할을 하는 것을 확인했다.
특히 현재 임상에서 항암제로 사용되고 있는 비라프의 저해제를 동물 모델에 주입해 난치성 뇌전증 치료 효과를 확인했다.
1저자인 고현용 연구원은 “소아 뇌종양 환자의 경 줄기 세포에서 발생한 특정 돌연변이가 난치성 뇌전증 발생에 핵심적 역할을 한다는 것을 국내 연구진이 최초로 발견해냈다는 것에 큰 의미가 있다”며 “소아 뇌종양으로 인해 발생한 난치성 뇌전증의 근본 원인을 규명해 과적 치료의 가능성을 처음으로 보여준 것이다”고 말했다.
연구팀은 교원창업기업(소바젠, 대표 김병태)을 통해 소아 뇌종양 기반의 난치성 뇌전증 치료약 개발에 나설 예정이다.
이번 연구는 연세대학교 의과대학 세브란스 병원 김동석, 김세훈, 강훈철 교수 연구팀과 공동 연구 및 서경배과학재단, 보건복지부 세계선도과학자육성사업의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 수술전 (PreOP) 과 수술후 (PostOP) 의 신경절 교세포종의 MRI사진과 이형성이 동반된 신경세포가 있는 병리 조직 사진
그림2. BRAF V600E 돌연변이가 발생하여 뇌전증 동반 소아 뇌종양을 유발하는 과정 모식도
2018.09.18 조회수 13400
고현용 연구원, 뇌전증 동반하는 소아 뇌종양 근본원인 밝혀
〈 고 현 용 연구원 〉
우리 대학 의과학대학원 고현용 연구원(지도교수 : 이정호 교수)이 난치성 뇌전증(간질 발작)을 일으키는 소아 뇌종양의 근본 원인과 뇌전증 발생의 원리를 규명해 새로운 치료법을 제시했다.
이번 연구 결과를 통해 수술 치료에 어려움이 있는 소아 뇌종양 기반의 난치성 뇌전증 치료에 큰 기여를 할 수 있을 것으로 기대된다.
고현용 박사과정이 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처 메디슨(Nature Medicine)’ 9월 17일자 온라인 판에 게재됐다. (논문명: 비라프 체성 돌연변이가 소아뇌종양의 본질적 뇌전증 발생에 기여함; BRAF somatic mutation contributes to intrinsic epileptogenicity in pediatric brain tumors)
소아 뇌종양은 성인 뇌종양에 비해 난치성 뇌전증이 빈번하게 동반되는 특징을 갖고 있다. 그러나 소아 뇌종양에서 특이적으로 난치성 뇌전증이 발생하는 원인에 대해서는 밝혀진 바가 없으며 현존하는 항 뇌전증 약물에 반응하지 않기 때문에 환자의 치료에 많은 어려움을 겪고 있다.
연구팀은 소아 뇌종양 환지 뇌 조직 및 동물 모델의 분자 유전학적 분석을 통해 태아의 뇌 발달과정 중 신경 줄기 세포에 ‘비라프 (BRAF V600E)’라는 돌연변이가 발생하면서 난치성 뇌전증이 동반된 소아 뇌종양이 발생하는 것을 규명했다.
연구팀은 뇌전증이 동반된 소아 뇌종양 중 하나인 신경절 교세포종 환자의 종양 조직을 분자 유전학적으로 분석한 결과 비라프 유전변이가 태아 뇌 발달 과정 중 발생함을 확인했다.
이 변이를 동물 모델에서 구현해 신경절 교세포종의 병리 양상을 재현하고 발작을 관찰해 소아 뇌종양 기반의 뇌전증 치료용 동물 모델을 최초로 확립했다.
이를 이용해 면역 염색 분석과 전사체 분석을 실시했다. 소아 뇌종양에서 발생하는 난치성 뇌전증이 신경세포에 존재하는 비라프 변이로 인해 발생하고, 교세포에 존재하는 변이는 종양 덩어리를 형성하는데 중요한 역할을 하는 것을 확인했다.
특히 현재 임상에서 항암제로 사용되고 있는 비라프의 저해제를 동물 모델에 주입해 난치성 뇌전증 치료 효과를 확인했다.
1저자인 고현용 연구원은 “소아 뇌종양 환자의 경 줄기 세포에서 발생한 특정 돌연변이가 난치성 뇌전증 발생에 핵심적 역할을 한다는 것을 국내 연구진이 최초로 발견해냈다는 것에 큰 의미가 있다”며 “소아 뇌종양으로 인해 발생한 난치성 뇌전증의 근본 원인을 규명해 과적 치료의 가능성을 처음으로 보여준 것이다”고 말했다.
연구팀은 교원창업기업(소바젠, 대표 김병태)을 통해 소아 뇌종양 기반의 난치성 뇌전증 치료약 개발에 나설 예정이다.
이번 연구는 연세대학교 의과대학 세브란스 병원 김동석, 김세훈, 강훈철 교수 연구팀과 공동 연구 및 서경배과학재단, 보건복지부 세계선도과학자육성사업의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 수술전 (PreOP) 과 수술후 (PostOP) 의 신경절 교세포종의 MRI사진과 이형성이 동반된 신경세포가 있는 병리 조직 사진
그림2. BRAF V600E 돌연변이가 발생하여 뇌전증 동반 소아 뇌종양을 유발하는 과정 모식도
2018.09.18 조회수 13400 -
 이정호 교수, 이주호 박사, 악성 뇌종양의 근본적 원인 밝혀
〈 이 주 호 박사 〉
악성 뇌종양인 교모세포종은 미디어에서 주요 소재로 나올 만큼 인간에게 치명적인 질병으로 일반 대중에게 낯설지 않은 질병이다. 실제로 악성 뇌종양으로 인한 미국 암 관련 사망률은 4위에 달하며 미국의 에드워드 케네디, 존 매케인 상원의원 등이 이 질병으로 사망했거나 투병 중이다.
우리 대학 의과학대학원 이정호 교수 연구팀이 세브란스병원 신경외과 강석구 교수와의 공동 연구를 통해 악성 뇌종양인 교모세포종 돌연변이 발생이 암 부위가 아닌 암에서 멀리 떨어진 뇌실하영역에서 발생한다는 사실을 규명했다.
이는 교모세포종 발병의 원인이 암 발생 부위일 것이라는 기존의 학설을 뒤집는 연구 결과로, 악성도가 가장 높은 종양인 교모세포종의 치료법 개발에 새로운 방향을 제시할 것으로 기대된다.
또한 그동안 암 조직만을 대상으로 이뤄진 암 연구가 암의 기원이 되는 조직에 대한 연구로 발전하면서 교모세포종 뿐 아니라 다른 암에 대해서도 치료의 실마리를 찾을 수 있는 기반이 될 것으로 보인다.
의과학대학원 졸업생 이주호 박사가 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처(Nature)’ 8월 1일자 온라인 판에 게재됐다.
교모세포종은 가장 예후가 좋지 않은 종양이다. 암 발생의 근본적인 원인에 대한 이해가 부족해 수술을 하더라도 재발 가능성이 매우 높기 때문이다. 수술만으로 치료가 불가능해 항암치료, 방사선치료, 표적항암제 등을 병행하지만 아직도 그 치료법이 명확하지 않다.
이정호 교수 연구팀은 암 발생 부위가 아닌 종양과 떨어져 있는 뇌실하영역이라는 곳에 주목했다. 교모세포종이 수술 이후에도 재발률이 높다는 점에서 원인이 다른 곳에 있을 것이라고 판단한 것이다.
이 교수는“교모세포종은 종양을 떼어내도 1~2년 후에 재발률이 높다. 암은 돌연변이인데 돌연변이가 발생하는 곳이 종양이 아닌 다른 부위라고 생각했고 그곳이 바로 뇌실하영역(subventricular zone : SVZ)이라는 사실을 밝혀냈다”고 말했다.
연구팀은 2013년부터 2017년 사이에 수술을 한 뇌종양 환자 28명을 대상으로 종양조직 외에 수술 중 제거되는 종양조직, 정상조직, 뇌실주변의 조직 3가지를 조합해 분석했다. 딥 시퀀싱, 단일세포시퀀싱 등을 통해 교모세포종의 시작이 뇌실하영역에서 발생한 낮은 빈도의 종양을 유발하는 돌연변이에 의한 것임을 밝혔다.
특히 유전자 편집 동물 모델을 통해 뇌실하영역에서 돌연변이가 생기면 이 돌연변이를 가진 세포가 뇌실하영역을 떠나 뇌의 다른 부위로 이동해 교모세포종이 되는 사실 또한 확인했다. 돌연변이 세포가 마치 불꽃놀이처럼 곳곳으로 퍼진 뒤 시간이 지나자 다른 부위에서 종양으로 진화한 것이다.
연구팀은 KAIST 교원창업(소바젠, 대표 김병태)을 통해 이번 연구결과를 바탕으로 뇌실하영역의 세포가 교모세포종으로 진화되는 과정을 막기 위한 치료약 개발에 나설 예정이다.
1저자인 이주호 박사는 “암 중 예후가 가장 좋지 않은 교모세포종에 대한 발암의 비밀을 국내 연구진이 풀어냈다는 것에 큰 의미가 있다”며 “악성 뇌종양의 연구와 치료의 획기적 전환점을 최초로 증명하고 제시한 것이다”고 말했다.
이정호 교수는 “암 중 가장 예후가 좋지 않은 교모세포종의 원인을 파악하고 동물 모델 제작까지 성공했다는 점에서 큰 의미가 있다. 환자에게서 찾은 것을 동물에 그대로 반영했기 때문에 여기서 치료를 할 수 있다면 임상까지 가능할 것이다.”고 말했다.
이정호 교수 연구팀은 후천성 뇌 돌연변이에 의한 난치성 뇌전증의 원리와 치료법을 최초로 규명한 바 있다. 이를 토대로 글로벌 제약회사와 함께 임상 2상이 진행될 정도로 난치성 뇌질환의 진단 및 치료법 개발을 세계적으로 리드하고 있다.
이 교수는 한국인으로서는 처음으로 난치성 뇌전증의 유전 병리학적 진단 기준을 세우는 세계 뇌전증학회 핵심 위원으로 참여해 국제 기준을 제정 중이다.
이번 연구는 서경배과학재단, 보건복지부 세계선도의과학자육성사업, 한국연구재단, 보건산업진흥원 사업을 통해 수행됐다.
□ 그림 설명
그림1. 교모세포종의 발암의 시작을 불꽃놀이에 비유한 그림
그림2. 동물 실험을 통해 뇌실하영역이 발암의 시발점임을 증명
2018.08.02 조회수 19712
이정호 교수, 이주호 박사, 악성 뇌종양의 근본적 원인 밝혀
〈 이 주 호 박사 〉
악성 뇌종양인 교모세포종은 미디어에서 주요 소재로 나올 만큼 인간에게 치명적인 질병으로 일반 대중에게 낯설지 않은 질병이다. 실제로 악성 뇌종양으로 인한 미국 암 관련 사망률은 4위에 달하며 미국의 에드워드 케네디, 존 매케인 상원의원 등이 이 질병으로 사망했거나 투병 중이다.
우리 대학 의과학대학원 이정호 교수 연구팀이 세브란스병원 신경외과 강석구 교수와의 공동 연구를 통해 악성 뇌종양인 교모세포종 돌연변이 발생이 암 부위가 아닌 암에서 멀리 떨어진 뇌실하영역에서 발생한다는 사실을 규명했다.
이는 교모세포종 발병의 원인이 암 발생 부위일 것이라는 기존의 학설을 뒤집는 연구 결과로, 악성도가 가장 높은 종양인 교모세포종의 치료법 개발에 새로운 방향을 제시할 것으로 기대된다.
또한 그동안 암 조직만을 대상으로 이뤄진 암 연구가 암의 기원이 되는 조직에 대한 연구로 발전하면서 교모세포종 뿐 아니라 다른 암에 대해서도 치료의 실마리를 찾을 수 있는 기반이 될 것으로 보인다.
의과학대학원 졸업생 이주호 박사가 1저자로 참여한 이번 연구 결과는 국제 학술지 ‘네이처(Nature)’ 8월 1일자 온라인 판에 게재됐다.
교모세포종은 가장 예후가 좋지 않은 종양이다. 암 발생의 근본적인 원인에 대한 이해가 부족해 수술을 하더라도 재발 가능성이 매우 높기 때문이다. 수술만으로 치료가 불가능해 항암치료, 방사선치료, 표적항암제 등을 병행하지만 아직도 그 치료법이 명확하지 않다.
이정호 교수 연구팀은 암 발생 부위가 아닌 종양과 떨어져 있는 뇌실하영역이라는 곳에 주목했다. 교모세포종이 수술 이후에도 재발률이 높다는 점에서 원인이 다른 곳에 있을 것이라고 판단한 것이다.
이 교수는“교모세포종은 종양을 떼어내도 1~2년 후에 재발률이 높다. 암은 돌연변이인데 돌연변이가 발생하는 곳이 종양이 아닌 다른 부위라고 생각했고 그곳이 바로 뇌실하영역(subventricular zone : SVZ)이라는 사실을 밝혀냈다”고 말했다.
연구팀은 2013년부터 2017년 사이에 수술을 한 뇌종양 환자 28명을 대상으로 종양조직 외에 수술 중 제거되는 종양조직, 정상조직, 뇌실주변의 조직 3가지를 조합해 분석했다. 딥 시퀀싱, 단일세포시퀀싱 등을 통해 교모세포종의 시작이 뇌실하영역에서 발생한 낮은 빈도의 종양을 유발하는 돌연변이에 의한 것임을 밝혔다.
특히 유전자 편집 동물 모델을 통해 뇌실하영역에서 돌연변이가 생기면 이 돌연변이를 가진 세포가 뇌실하영역을 떠나 뇌의 다른 부위로 이동해 교모세포종이 되는 사실 또한 확인했다. 돌연변이 세포가 마치 불꽃놀이처럼 곳곳으로 퍼진 뒤 시간이 지나자 다른 부위에서 종양으로 진화한 것이다.
연구팀은 KAIST 교원창업(소바젠, 대표 김병태)을 통해 이번 연구결과를 바탕으로 뇌실하영역의 세포가 교모세포종으로 진화되는 과정을 막기 위한 치료약 개발에 나설 예정이다.
1저자인 이주호 박사는 “암 중 예후가 가장 좋지 않은 교모세포종에 대한 발암의 비밀을 국내 연구진이 풀어냈다는 것에 큰 의미가 있다”며 “악성 뇌종양의 연구와 치료의 획기적 전환점을 최초로 증명하고 제시한 것이다”고 말했다.
이정호 교수는 “암 중 가장 예후가 좋지 않은 교모세포종의 원인을 파악하고 동물 모델 제작까지 성공했다는 점에서 큰 의미가 있다. 환자에게서 찾은 것을 동물에 그대로 반영했기 때문에 여기서 치료를 할 수 있다면 임상까지 가능할 것이다.”고 말했다.
이정호 교수 연구팀은 후천성 뇌 돌연변이에 의한 난치성 뇌전증의 원리와 치료법을 최초로 규명한 바 있다. 이를 토대로 글로벌 제약회사와 함께 임상 2상이 진행될 정도로 난치성 뇌질환의 진단 및 치료법 개발을 세계적으로 리드하고 있다.
이 교수는 한국인으로서는 처음으로 난치성 뇌전증의 유전 병리학적 진단 기준을 세우는 세계 뇌전증학회 핵심 위원으로 참여해 국제 기준을 제정 중이다.
이번 연구는 서경배과학재단, 보건복지부 세계선도의과학자육성사업, 한국연구재단, 보건산업진흥원 사업을 통해 수행됐다.
□ 그림 설명
그림1. 교모세포종의 발암의 시작을 불꽃놀이에 비유한 그림
그림2. 동물 실험을 통해 뇌실하영역이 발암의 시발점임을 증명
2018.08.02 조회수 19712 -
 김필남 교수, 악성 뇌종양의 내성 발생 원리 밝혀
〈 김 필 남 교수 〉
우리 대학 바이오및뇌공학과 김필남 교수 연구팀이 3차원 체외 종양 모델을 제작해 악성 뇌종양의 약물 저항성(내성) 발생 원리를 밝혔다.이번에 제작된 뇌종양 3차원 모델은 실제로 중요한 영향을 미치는 종양의 미세환경(tumor microenvironment)을 고려해 제작함으로써 실질적 암 치료에 적용 가능할 것으로 기대된다.
이번 연구는 네이처 자매지인 ‘사이언티픽 리포트(Scientific Reports)’ 4월 26일자 온라인 판에 게재됐다. (논문명: Strategies of Mesenchymal Invasion of Patient-derived Brain Tumors: Microenvironmental Adaptation)
악성 뇌종양은 주변 조직으로 침윤하는 특성이 매우 강해 치료하기 힘든 질병 중 하나이다. 수술을 통해 종양을 절제해도 주변 조직에 넓게 침윤한 잔여 세포들이 재발하는 경우가 많다.
따라서 악성 뇌종양의 치료 효율 및 생존율을 높이기 위해서는 남아있는 침윤 세포를 표적으로 한 치료법을 개발해야 한다.
그러나 종양의 악성화 및 침윤 특성의 주요 원인인 주변 미세환경(tumor microenvironment)을 고려하지 않은 항암제 개발이 주로 이뤄졌기 때문에 종양의 침윤 및 약물 저항의 원리를 밝히기 어려웠다.
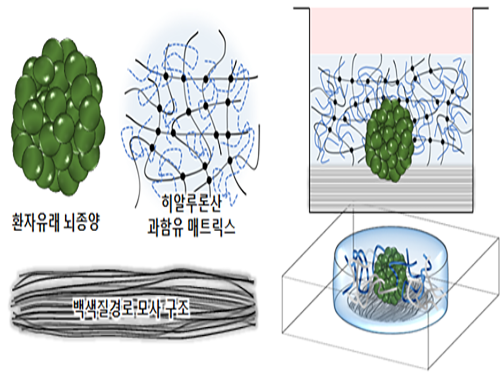
연구팀은 문제 해결을 위해 체외에서 종양 주변 미세환경의 특성을 반영한 3차원 암 모델을 구현했다. 이는 뇌종양 미세환경의 주요 구성요소인 과함유 히알루론산(hyaluronic acid) 기질과 백색질 경로(white matter tract)를 모사한 생체모방체외종양 모델이다.
연구팀은 체내에 존재하는 악성 뇌종양의 특성을 체외에서도 유사하게 유지시켜 환자를 대체할 수 있는 종양 모델로 활용 가능함을 확인했다.
연구팀은 뇌종양 세포가 침윤하는 데 중요한 역할을 하는 히알루론산 합성 단백질을 억제하는 약물을 투입했다. 초기에는 뇌종양 침윤이 억제됐지만 시간이 흐르며 미세환경 적응(microenvironmental adaptation) 과정에서 뇌종양이 새 기전을 통해 약물에 대한 내성이 생기는 현상을 발견했다.
이 모든 과정을 체외 종양 모델을 통해 진행함으로써 동물실험을 대체하여 다양한 항암제를 조합하고 검증할 수 있어 실질적인 암 치료에 도움이 될 것으로 기대된다.
연구팀이 제시한 3차원 체외 암 모델은 기존 약물의 저항 원인을 규명하는 기반이 될 것으로 예상된다. 또한 추후 정밀 암 치료를 위한 핵심 기반 기술로 환자맞춤 약물 검증 및 신약 발굴 모델 등으로 다각적 활용이 가능할 것으로 기대된다.
김 교수는 “뇌종양의 체외 종양모델로서 공학적 기술 기반의 3차원 미세환경 암 모델을 제시했다”며 “이를 바탕으로 뇌종양 환자 개별 치료의 가능성을 높여 생존율 개선에 힘이 되겠다”고 말했다.
바이오및뇌공학과 차정화 박사과정 학생이 1저자로 참여한 이번 연구는 한국연구재단 신진연구자지원사업 및 보건복지부 중개중점 연구사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 악성 뇌종양 주변 미세환경
그림2. 환자 대체치료용 3차원 체외뇌암모델의 모식도
그림3. 환자유래 뇌종양 세포의 미세환경 적응 과정에 의한 약물 저항 메커니즘
2016.05.11 조회수 16502
김필남 교수, 악성 뇌종양의 내성 발생 원리 밝혀
〈 김 필 남 교수 〉
우리 대학 바이오및뇌공학과 김필남 교수 연구팀이 3차원 체외 종양 모델을 제작해 악성 뇌종양의 약물 저항성(내성) 발생 원리를 밝혔다.이번에 제작된 뇌종양 3차원 모델은 실제로 중요한 영향을 미치는 종양의 미세환경(tumor microenvironment)을 고려해 제작함으로써 실질적 암 치료에 적용 가능할 것으로 기대된다.
이번 연구는 네이처 자매지인 ‘사이언티픽 리포트(Scientific Reports)’ 4월 26일자 온라인 판에 게재됐다. (논문명: Strategies of Mesenchymal Invasion of Patient-derived Brain Tumors: Microenvironmental Adaptation)
악성 뇌종양은 주변 조직으로 침윤하는 특성이 매우 강해 치료하기 힘든 질병 중 하나이다. 수술을 통해 종양을 절제해도 주변 조직에 넓게 침윤한 잔여 세포들이 재발하는 경우가 많다.
따라서 악성 뇌종양의 치료 효율 및 생존율을 높이기 위해서는 남아있는 침윤 세포를 표적으로 한 치료법을 개발해야 한다.
그러나 종양의 악성화 및 침윤 특성의 주요 원인인 주변 미세환경(tumor microenvironment)을 고려하지 않은 항암제 개발이 주로 이뤄졌기 때문에 종양의 침윤 및 약물 저항의 원리를 밝히기 어려웠다.
연구팀은 문제 해결을 위해 체외에서 종양 주변 미세환경의 특성을 반영한 3차원 암 모델을 구현했다. 이는 뇌종양 미세환경의 주요 구성요소인 과함유 히알루론산(hyaluronic acid) 기질과 백색질 경로(white matter tract)를 모사한 생체모방체외종양 모델이다.
연구팀은 체내에 존재하는 악성 뇌종양의 특성을 체외에서도 유사하게 유지시켜 환자를 대체할 수 있는 종양 모델로 활용 가능함을 확인했다.
연구팀은 뇌종양 세포가 침윤하는 데 중요한 역할을 하는 히알루론산 합성 단백질을 억제하는 약물을 투입했다. 초기에는 뇌종양 침윤이 억제됐지만 시간이 흐르며 미세환경 적응(microenvironmental adaptation) 과정에서 뇌종양이 새 기전을 통해 약물에 대한 내성이 생기는 현상을 발견했다.
이 모든 과정을 체외 종양 모델을 통해 진행함으로써 동물실험을 대체하여 다양한 항암제를 조합하고 검증할 수 있어 실질적인 암 치료에 도움이 될 것으로 기대된다.
연구팀이 제시한 3차원 체외 암 모델은 기존 약물의 저항 원인을 규명하는 기반이 될 것으로 예상된다. 또한 추후 정밀 암 치료를 위한 핵심 기반 기술로 환자맞춤 약물 검증 및 신약 발굴 모델 등으로 다각적 활용이 가능할 것으로 기대된다.
김 교수는 “뇌종양의 체외 종양모델로서 공학적 기술 기반의 3차원 미세환경 암 모델을 제시했다”며 “이를 바탕으로 뇌종양 환자 개별 치료의 가능성을 높여 생존율 개선에 힘이 되겠다”고 말했다.
바이오및뇌공학과 차정화 박사과정 학생이 1저자로 참여한 이번 연구는 한국연구재단 신진연구자지원사업 및 보건복지부 중개중점 연구사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 악성 뇌종양 주변 미세환경
그림2. 환자 대체치료용 3차원 체외뇌암모델의 모식도
그림3. 환자유래 뇌종양 세포의 미세환경 적응 과정에 의한 약물 저항 메커니즘
2016.05.11 조회수 16502