%EC%8A%A4%EB%84%A4%EC%96%B4
-
 신경세포 전달 후 분해 원리 30년 만에 규명
윤태영 교수
2013년도의 노벨 생리의학상은 제임스 로스먼, 랜디 셰크먼, 토마스 쥐트호프에게 돌아갔다. 그들은 신경전달물질, 호르몬 등의 주요 물질이 자루 모양의 지질막인 소포(vesicles)에 담겨 택배처럼 전달되는 과정을 발생시키는 단백질을 발견한 공로를 인정받았다.
수상자들은 소포의 막을 열어 세포막과 융합해 물질을 분출하는 방식으로 에너지를 전달하는 역할인 스네어(SNARE)라는 단백질과, 물질을 분출한 후의 스네어 단백질 재활용을 위해 기능하는 NSF라는 단백질을 발견했다.
우리에게 잘 알려진 보톡스도 스네어 단백질의 작용 과정을 역으로 이용한 것이다. 보톡스가 스네어를 절단해 소포가 세포막과 융합하지 못하게 만들어 신경전달물질의 방출을 막고, 그로인해 근육의 수축을 방해하는 것이다.
이런 운송 업무가 있기 때문에 우리 세포는 신체 곳곳에 단백질과 같은 물질이 공급돼 정상적인 기능을 할 수 있다.
우리 대학 물리학과 윤태영 교수 연구팀은 그간 명확하지 않았던 NSF가 스네어 결합체를 분해해 세포수송을 지속시키는 원리를 규명했다고 밝혔다.
이번 연구 결과는 저명 학술지 사이언스지 3월 27일자에 게재됐다.
NSF와 스네어 단백질은 30여 년 전에 발견됐지만 각각의 물질이 작용하는 방식은 명확히 규명되지 않았다. 특히 세포막과 결합한 스네어 결합체를 NSF가 어떤 방법으로 분해해 재활용하는지에 대해선 의견이 분분했다.
지금까지 과학자들은 NSF가 스네어 결합체를 분해할 때 끈을 조금씩 푸는 것처럼 점진적인 과정을 통해 분해가 이뤄지고, 하나의 스네어 결합체를 분해하는 데 ATP라는 연료 역할을 하는 유기화합물 수십 개가 필요하다는 가설을 주장했다.
하지만 윤 교수팀의 연구는 단분자 형광 기법과 자기집게 기술(magnetic tweezers)을 사용해 가설을 반박했다. 마치 매듭의 양 끝을 잡고 당기면 한 번에 풀리듯, ATP를 주입하면 NSF가 스프링처럼 에너지를 저장했다가 스네어 결합체 전체를 단번에 폭발적으로 풀어냄을 증명한 것이다.
이번에 규명된 NSF는 근육의 이동, 단백질 분해, DNA의 복제 및 이동 등 신체에서 중요한 역할을 하는 AAA+ 단백질 그룹에 속해있다. 따라서 NSF와 비슷한 구조의 AAA+ 단백질 그룹은 함께 동작할 것으로 예상되며, 앞으로 많은 생물 현상 이해의 주춧돌이 될 것으로 보인다.
스네어 단백질은 신경세포 통신과 인슐린 분비 등에 중추적 역할을 하고 있어 윤 교수팀의 성과는 알츠하이머와 같은 퇴행성 뇌질환, 당뇨병과 같은 대사질환 관련 연구 뿐 아니라 피부미용 연구에도 이바지 할 것으로 기대된다.
윤 교수는 “생물 물리 분야에서 우리나라가 최고수준의 기초과학 연구력을 보유하고 있음을 증명했다”며 “이번 연구결과는 여러 대사질환을 분자수준에서 이해할 수 있는 토대가 될 것”이라고 말했다.
이번 연구는 고등과학원의 현창봉 교수팀, 독일 막스 플랑크 연구소 라인하르트 얀(Reinhard Jahn) 교수팀, 우리 대학 의과학대학원 김호민 교수팀과의 공동 연구로 진행됐으며, 윤 교수 연구팀의 류제경, 민두영 박사, 나상현 학생의 주도로 이뤄졌다.
□ 그림 설명
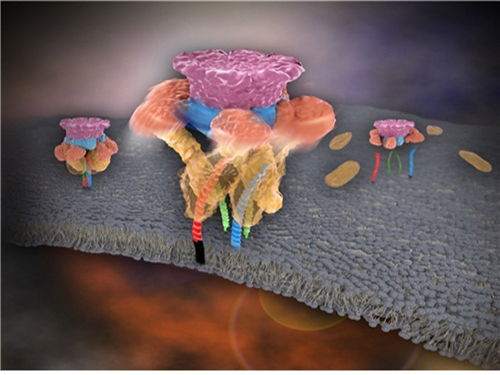
그림 1. 신경전달물질의 분비가 끝난 후 NSF가 SNARE 단백질 복합체를 한 번에 분해하는 모습
그림 2. NSF 가 SNARE 복합체를 풀어내는 모습
2015.03.27 조회수 14883
신경세포 전달 후 분해 원리 30년 만에 규명
윤태영 교수
2013년도의 노벨 생리의학상은 제임스 로스먼, 랜디 셰크먼, 토마스 쥐트호프에게 돌아갔다. 그들은 신경전달물질, 호르몬 등의 주요 물질이 자루 모양의 지질막인 소포(vesicles)에 담겨 택배처럼 전달되는 과정을 발생시키는 단백질을 발견한 공로를 인정받았다.
수상자들은 소포의 막을 열어 세포막과 융합해 물질을 분출하는 방식으로 에너지를 전달하는 역할인 스네어(SNARE)라는 단백질과, 물질을 분출한 후의 스네어 단백질 재활용을 위해 기능하는 NSF라는 단백질을 발견했다.
우리에게 잘 알려진 보톡스도 스네어 단백질의 작용 과정을 역으로 이용한 것이다. 보톡스가 스네어를 절단해 소포가 세포막과 융합하지 못하게 만들어 신경전달물질의 방출을 막고, 그로인해 근육의 수축을 방해하는 것이다.
이런 운송 업무가 있기 때문에 우리 세포는 신체 곳곳에 단백질과 같은 물질이 공급돼 정상적인 기능을 할 수 있다.
우리 대학 물리학과 윤태영 교수 연구팀은 그간 명확하지 않았던 NSF가 스네어 결합체를 분해해 세포수송을 지속시키는 원리를 규명했다고 밝혔다.
이번 연구 결과는 저명 학술지 사이언스지 3월 27일자에 게재됐다.
NSF와 스네어 단백질은 30여 년 전에 발견됐지만 각각의 물질이 작용하는 방식은 명확히 규명되지 않았다. 특히 세포막과 결합한 스네어 결합체를 NSF가 어떤 방법으로 분해해 재활용하는지에 대해선 의견이 분분했다.
지금까지 과학자들은 NSF가 스네어 결합체를 분해할 때 끈을 조금씩 푸는 것처럼 점진적인 과정을 통해 분해가 이뤄지고, 하나의 스네어 결합체를 분해하는 데 ATP라는 연료 역할을 하는 유기화합물 수십 개가 필요하다는 가설을 주장했다.
하지만 윤 교수팀의 연구는 단분자 형광 기법과 자기집게 기술(magnetic tweezers)을 사용해 가설을 반박했다. 마치 매듭의 양 끝을 잡고 당기면 한 번에 풀리듯, ATP를 주입하면 NSF가 스프링처럼 에너지를 저장했다가 스네어 결합체 전체를 단번에 폭발적으로 풀어냄을 증명한 것이다.
이번에 규명된 NSF는 근육의 이동, 단백질 분해, DNA의 복제 및 이동 등 신체에서 중요한 역할을 하는 AAA+ 단백질 그룹에 속해있다. 따라서 NSF와 비슷한 구조의 AAA+ 단백질 그룹은 함께 동작할 것으로 예상되며, 앞으로 많은 생물 현상 이해의 주춧돌이 될 것으로 보인다.
스네어 단백질은 신경세포 통신과 인슐린 분비 등에 중추적 역할을 하고 있어 윤 교수팀의 성과는 알츠하이머와 같은 퇴행성 뇌질환, 당뇨병과 같은 대사질환 관련 연구 뿐 아니라 피부미용 연구에도 이바지 할 것으로 기대된다.
윤 교수는 “생물 물리 분야에서 우리나라가 최고수준의 기초과학 연구력을 보유하고 있음을 증명했다”며 “이번 연구결과는 여러 대사질환을 분자수준에서 이해할 수 있는 토대가 될 것”이라고 말했다.
이번 연구는 고등과학원의 현창봉 교수팀, 독일 막스 플랑크 연구소 라인하르트 얀(Reinhard Jahn) 교수팀, 우리 대학 의과학대학원 김호민 교수팀과의 공동 연구로 진행됐으며, 윤 교수 연구팀의 류제경, 민두영 박사, 나상현 학생의 주도로 이뤄졌다.
□ 그림 설명
그림 1. 신경전달물질의 분비가 끝난 후 NSF가 SNARE 단백질 복합체를 한 번에 분해하는 모습
그림 2. NSF 가 SNARE 복합체를 풀어내는 모습
2015.03.27 조회수 14883 -
 뇌신경전달 단백질의 구조와 작동원리 규명
- 생체막 융합 단백질의 구조변화 실시간 측정 -- 퇴행성 뇌질환 연구에 실마리 제공 -
우리 학교 물리학과 윤태영 교수 연구팀이 자기력 나노집게를 이용해 뇌신경세포사이의 신경물질전달에 가장 중추적인 역할을 하는 스네어(SNARE) 단백질의 숨겨진 구조와 작동원리를 단분자 수준에서 밝히는데 성공했다.
스네어 단백질의 세포막 융합기능은 알츠하이머병 같은 퇴행성 뇌질환이나 신경질환과 밀접하게 연관되어 있어 이 같은 질병의 예방과 치료법 개발에 새로운 실마리가 될 것으로 기대된다.
뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 가장 핵심적인 역할을 하는 세포막 융합 단백질이다.
지금까지 학계에서는 스네어 단백질이 신경물질을 주고받는 과정을 조절할 것이라고 추정해 왔지만 그 구조와 기능을 명확하게 밝혀내지 못했다.
연구팀은 자기력 나노집게를 이용해 피코 뉴턴(pN, 1조분의 1뉴턴) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하는 실험기법을 개발했다.
이를 통해 스네어 단백질에 숨겨진 중간구조가 존재하며, 이 구조에 대한 정밀한 측정결과 중간상태가 어떤 구조를 갖는지 정확하게 예측했다.
이와 함께 생체막 사이에 있는 스네어 단백질의 중간구조가 생체막이 서로 밀어내는 힘을 견디고 유지하면서 신경물질을 주고받는 과정을 조절하는 역할을 할 수 있음을 밝혔다.
윤태영 교수는 “생체단백질이 갖는 숨겨진 구조와 작동원리를 힘을 정교하게 조절하는 실험만으로 직접 관찰하는 것과 동일한 획기적 연구 결과를 일궈냈다”며 “이 기술은 생물학의 연구대상을 물리학적인 방법 연구하는데 매우 중요한 기술로 향후 학제적 융합연구에 매우 중요한 기반이 될 것”이라고 말했다.
한편, 이번 연구는 KAIST 물리학과 윤태영 교수와 김기범 연구교수의 주도 아래 KIST 의공학연구소 신연균 교수와 공동연구로 진행됐고, KAIST 물리학과 조용훈 교수, 민두영 박사과정, KIAS 계산과학부 현창봉 교수가 참여했으며, 이번 세계적 과학학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 4월 16일자에 게재됐다.
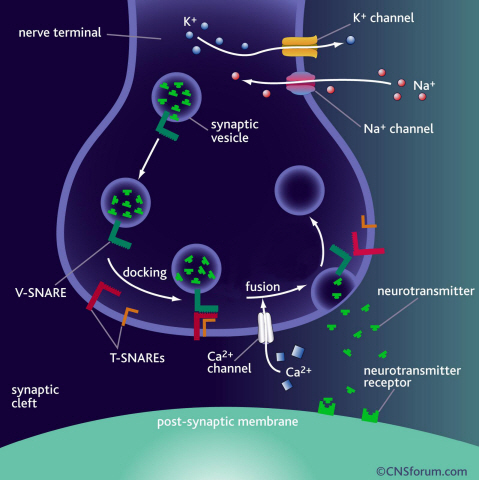
(a) 뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 핵심적인 역할을 한다.
(b) 자기력 나노집게를 이용하여 단분자 수준에서 단백질 구조 변화를 실시간으로 측정방법의 개략도. 피코 뉴톤(pN) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하여 생체막 융합 단백질의 숨겨진 중간구조와 작동원리를 단분자 수준에서 관찰한다.
2013.05.09 조회수 19652
뇌신경전달 단백질의 구조와 작동원리 규명
- 생체막 융합 단백질의 구조변화 실시간 측정 -- 퇴행성 뇌질환 연구에 실마리 제공 -
우리 학교 물리학과 윤태영 교수 연구팀이 자기력 나노집게를 이용해 뇌신경세포사이의 신경물질전달에 가장 중추적인 역할을 하는 스네어(SNARE) 단백질의 숨겨진 구조와 작동원리를 단분자 수준에서 밝히는데 성공했다.
스네어 단백질의 세포막 융합기능은 알츠하이머병 같은 퇴행성 뇌질환이나 신경질환과 밀접하게 연관되어 있어 이 같은 질병의 예방과 치료법 개발에 새로운 실마리가 될 것으로 기대된다.
뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 가장 핵심적인 역할을 하는 세포막 융합 단백질이다.
지금까지 학계에서는 스네어 단백질이 신경물질을 주고받는 과정을 조절할 것이라고 추정해 왔지만 그 구조와 기능을 명확하게 밝혀내지 못했다.
연구팀은 자기력 나노집게를 이용해 피코 뉴턴(pN, 1조분의 1뉴턴) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하는 실험기법을 개발했다.
이를 통해 스네어 단백질에 숨겨진 중간구조가 존재하며, 이 구조에 대한 정밀한 측정결과 중간상태가 어떤 구조를 갖는지 정확하게 예측했다.
이와 함께 생체막 사이에 있는 스네어 단백질의 중간구조가 생체막이 서로 밀어내는 힘을 견디고 유지하면서 신경물질을 주고받는 과정을 조절하는 역할을 할 수 있음을 밝혔다.
윤태영 교수는 “생체단백질이 갖는 숨겨진 구조와 작동원리를 힘을 정교하게 조절하는 실험만으로 직접 관찰하는 것과 동일한 획기적 연구 결과를 일궈냈다”며 “이 기술은 생물학의 연구대상을 물리학적인 방법 연구하는데 매우 중요한 기술로 향후 학제적 융합연구에 매우 중요한 기반이 될 것”이라고 말했다.
한편, 이번 연구는 KAIST 물리학과 윤태영 교수와 김기범 연구교수의 주도 아래 KIST 의공학연구소 신연균 교수와 공동연구로 진행됐고, KAIST 물리학과 조용훈 교수, 민두영 박사과정, KIAS 계산과학부 현창봉 교수가 참여했으며, 이번 세계적 과학학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 4월 16일자에 게재됐다.
(a) 뇌의 신경전달은 신경세포 말단 시냅스에서 신경전달물질을 저장하는 포낭 주머니가 세포막에 융합되면서 일어난다. 이 과정에서 스네어 단백질은 신경전달물질 분출에 핵심적인 역할을 한다.
(b) 자기력 나노집게를 이용하여 단분자 수준에서 단백질 구조 변화를 실시간으로 측정방법의 개략도. 피코 뉴톤(pN) 수준의 힘으로 단백질 하나를 정교하게 당겼다 놓으면서 나노 미터수준의 물리적 변화를 실시간으로 측정하여 생체막 융합 단백질의 숨겨진 중간구조와 작동원리를 단분자 수준에서 관찰한다.
2013.05.09 조회수 19652