%EC%97%AD%EB%B6%84%ED%99%94
-
 인공지능으로 파킨슨병 맞춤형 치료 가능
파킨슨병 같은 만성 퇴행성 뇌 질환의 경우, 생존 환자의 뇌세포에 직접 접근이 제한적이기 때문에, 뇌 질환 환자의 세포 데이터를 토대로 환자 질병의 메커니즘 하위 유형을 인공지능으로 예측하는 것은 시도된 바가 없다.
우리 대학 뇌인지과학과 최민이 교수 연구팀이 영국 프랜시스 크릭 연구소(Francis Crick Institute)와의 공동 연구로 파킨슨병 환자의 개인별 질병 하위 유형을 예측하는 인공지능 기반의 플랫폼을 개발했다고 15일 밝혔다.
최민이 교수 연구팀이 개발한 플랫폼은 파킨슨병 환자의 역분화 만능 줄기세포(hiPSC)에서 분화된 신경 세포의 핵, 미토콘드리아, 리보솜 이미지 정보만 학습해 파킨슨 환자의 병리적 하위 유형을 정확하게 예측한다.
이 기술을 활용하면 환자별로 다르게 나타나는 파킨슨병 양상을 겉으로 보이는 발현형이 아닌 생물학적 메커니즘별로 분류할 수 있다. 이를 통해 원인 미상의 파킨슨병 환자가 속한 분자 세포적 하위 유형별로 진단이 가능해져 환자 맞춤형 치료의 길을 열 수 있다. 또 이 플랫폼은 고속의 대량 스크리닝 시스템을 사용하기 때문에 병리적 하위 유형에 적합한 맞춤형 약물 개발 파이프라인으로도 활용될 수 있다.
지금까지 파킨슨병의 치료는 환자 개별의 병리 상태를 고려하지 않고 확률에 기댄 ‘일률적 접근’ 방식을 사용해 왔다. 이러한 접근 방식은 병리적 원인과 치료 방법 사이의 불일치로 인해 치료 효과를 향상하기 어려웠다.
최민이 교수 연구팀이 개발한 플랫폼을 사용하면 개별 환자 뇌세포의 분자 및 세포 정보를 정밀하게 프로파일링할 수 있다. 이를 토대로 환자들의 질병 하위 유형을 정확히 진단할 수 있어서 궁극적으로 ‘정밀 의학 (Precise medicine)’이 가능해진다. 이는 각 개인에게 맞춤화된 치료 (Personalized medicine)로 이어져 치료 효과를 크게 향상할 수 있을 것으로 기대된다.
이 플랫폼은 2012년 노벨의학상 수상 기술인 유도만능줄기세포(iPSC: 성인 피부세포나 혈액에서 얻은 체세포를 태아기의 미분화 상태로 리프로그래밍한 세포. 어떤 장기 세포로도 분화가 가능)를 분화시켜 얻은 뇌세포를 사용하는 ‘접시 속 질병(disease in a dish)’ 패러다임이다. 이는 퇴행성 뇌 질환처럼 병변을 직접 얻을 수 없거나, 인간의 뇌를 정확하게 모사할 수 없는 동물 모델의 한계점을 극복할 수 있는 기술 중 하나로 주목받고 있다. 특히, 접시 속에 배양한 자신의 표적 질병 세포를 순차적으로 이미징하면 일련의 병리적 사건을 추적할 수 있어 질병 진행에 따른 약물 반응 결과를 예측할 수 있다는 이점이 있다.
교신 저자인 최민이 교수는 "이번 연구는 실험실에서 얻은 생물학적 데이터를 인공지능에 효과적으로 학습시켜, 정확도가 높은 질병 하위 유형 분류 모델을 생성하는 방법을 구체적으로 소개했다”며, "이 플랫폼은 자폐 스펙트럼과 같이 환자 개인별 증상이 뚜렷하게 다른 뇌 질환의 하위 유형을 분류하는 데에도 유용할 것이며, 이를 통해 효과적인 치료법 개발도 가능해질 것이다”라고 연구의 의의를 설명했다.
이번 논문은 영국 Medical Research Council (MRC)와 대교-KAIST 인지 향상 연구센터의 지원으로 수행됐으며, 국제 학술지 ‘네이처 머신 인텔리젼스 (Nature Machine Intelligence, IF = 25.8) 8월호에 출판됐다 (논문명: Prediction of mechanistic subtypes of Parkinson’s using patient-derived stem cell model)
2023.08.16 조회수 9490
인공지능으로 파킨슨병 맞춤형 치료 가능
파킨슨병 같은 만성 퇴행성 뇌 질환의 경우, 생존 환자의 뇌세포에 직접 접근이 제한적이기 때문에, 뇌 질환 환자의 세포 데이터를 토대로 환자 질병의 메커니즘 하위 유형을 인공지능으로 예측하는 것은 시도된 바가 없다.
우리 대학 뇌인지과학과 최민이 교수 연구팀이 영국 프랜시스 크릭 연구소(Francis Crick Institute)와의 공동 연구로 파킨슨병 환자의 개인별 질병 하위 유형을 예측하는 인공지능 기반의 플랫폼을 개발했다고 15일 밝혔다.
최민이 교수 연구팀이 개발한 플랫폼은 파킨슨병 환자의 역분화 만능 줄기세포(hiPSC)에서 분화된 신경 세포의 핵, 미토콘드리아, 리보솜 이미지 정보만 학습해 파킨슨 환자의 병리적 하위 유형을 정확하게 예측한다.
이 기술을 활용하면 환자별로 다르게 나타나는 파킨슨병 양상을 겉으로 보이는 발현형이 아닌 생물학적 메커니즘별로 분류할 수 있다. 이를 통해 원인 미상의 파킨슨병 환자가 속한 분자 세포적 하위 유형별로 진단이 가능해져 환자 맞춤형 치료의 길을 열 수 있다. 또 이 플랫폼은 고속의 대량 스크리닝 시스템을 사용하기 때문에 병리적 하위 유형에 적합한 맞춤형 약물 개발 파이프라인으로도 활용될 수 있다.
지금까지 파킨슨병의 치료는 환자 개별의 병리 상태를 고려하지 않고 확률에 기댄 ‘일률적 접근’ 방식을 사용해 왔다. 이러한 접근 방식은 병리적 원인과 치료 방법 사이의 불일치로 인해 치료 효과를 향상하기 어려웠다.
최민이 교수 연구팀이 개발한 플랫폼을 사용하면 개별 환자 뇌세포의 분자 및 세포 정보를 정밀하게 프로파일링할 수 있다. 이를 토대로 환자들의 질병 하위 유형을 정확히 진단할 수 있어서 궁극적으로 ‘정밀 의학 (Precise medicine)’이 가능해진다. 이는 각 개인에게 맞춤화된 치료 (Personalized medicine)로 이어져 치료 효과를 크게 향상할 수 있을 것으로 기대된다.
이 플랫폼은 2012년 노벨의학상 수상 기술인 유도만능줄기세포(iPSC: 성인 피부세포나 혈액에서 얻은 체세포를 태아기의 미분화 상태로 리프로그래밍한 세포. 어떤 장기 세포로도 분화가 가능)를 분화시켜 얻은 뇌세포를 사용하는 ‘접시 속 질병(disease in a dish)’ 패러다임이다. 이는 퇴행성 뇌 질환처럼 병변을 직접 얻을 수 없거나, 인간의 뇌를 정확하게 모사할 수 없는 동물 모델의 한계점을 극복할 수 있는 기술 중 하나로 주목받고 있다. 특히, 접시 속에 배양한 자신의 표적 질병 세포를 순차적으로 이미징하면 일련의 병리적 사건을 추적할 수 있어 질병 진행에 따른 약물 반응 결과를 예측할 수 있다는 이점이 있다.
교신 저자인 최민이 교수는 "이번 연구는 실험실에서 얻은 생물학적 데이터를 인공지능에 효과적으로 학습시켜, 정확도가 높은 질병 하위 유형 분류 모델을 생성하는 방법을 구체적으로 소개했다”며, "이 플랫폼은 자폐 스펙트럼과 같이 환자 개인별 증상이 뚜렷하게 다른 뇌 질환의 하위 유형을 분류하는 데에도 유용할 것이며, 이를 통해 효과적인 치료법 개발도 가능해질 것이다”라고 연구의 의의를 설명했다.
이번 논문은 영국 Medical Research Council (MRC)와 대교-KAIST 인지 향상 연구센터의 지원으로 수행됐으며, 국제 학술지 ‘네이처 머신 인텔리젼스 (Nature Machine Intelligence, IF = 25.8) 8월호에 출판됐다 (논문명: Prediction of mechanistic subtypes of Parkinson’s using patient-derived stem cell model)
2023.08.16 조회수 9490 -
 시스템생물학 이용 세계 최초 알츠하이머성 치매 환자 맞춤형 치료 효능 예측 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀 (장소영 박사과정(제1저자), 강의룡 박사과정, 장홍준 박사과정)은 서울대학교 의과대학 묵인희 교수 연구팀과 공동연구를 통해 시스템생물학*과 알츠하이머 환자 유래 뇌 오가노이드** 모델의 융합으로 환자 맞춤형 약물 효능평가 플랫폼(Drug-screening platform)을 세계 최초로 개발했다고 13일 밝혔다.
* 시스템생물학: IT의 수학모델링 및 컴퓨터시뮬레이션과 BT의 분자세포생물학 실험을 융합하여 복잡한 생명현상을 규명하고 설명하는 연구 패러다임
** 뇌 오가노이드: 환자의 역분화 줄기세포(iPSC) 유래 인공 미니 뇌
알츠하이머병은 치매의 약 70%를 차지하는 대표적 치매 질환이나 현재까지 발병 원인이 불명확하며, 근본적인 치료제도 없는 인류가 극복하지 못한 질병 중 하나다.
알츠하이머병 치료제 개발 난제 중 하나는 실제 살아있는 환자의 뇌를 직접 실험 샘플로 사용할 수 없다는 것이었다. 이는 수많은 치료제 후보군의 약물 효능을 정확히 평가하기가 어려워 치료제 개발의 걸림돌로 작용해왔다.
조광현 교수 공동 연구팀은 실제 치매환자에서 유래한 뇌 오가노이드 기반으로 생물학적 메커니즘에 대한 수학 모델링을 융합하여 약물효능 예측이 가능한 플랫폼을 세계 최초로 개발했다. 환자 혈액으로부터 역분화줄기세포(Induced-pluripotent stem cell)*를 구축 후 이를 이용하여 3D 뇌 오가노이드를 제작해 실제 환자의 뇌와 유사한 환경 구축을 통해 실험적 한계를 극복했다.
* 역분화줄기세포: 다능성이 없는 혈액 면역세포에 역분화를 일으키는 4가지 특정 유전자를 도입하여 배아 줄기세포와 같이 모든 종류의 세포로 분화할 수 있는 성질(다능성)을 가진 줄기세포
또한, 시스템생물학 기반 수학 모델링 기법으로 알츠하이머병의 신경세포 특이적 네트워크망을 구축하고, 이를 실제 알츠하이머병 환자 및 정상군 유래 뇌 오가노이드를 통하여 신경세포 컴퓨터 모델의 실효성을 검증했다.
이 연구결과는 알츠하이머병의 시스템생물학 기반 신경세포 컴퓨터 모델을 실제 환자 유래 뇌 오가노이드로 검증한 세계 최초의 사례이다. 이는 환자 맞춤형 치료(Precision medicine)의 불모지로 여겨졌던 뇌 질환분야에서도 알츠하이머병 환자의 유전형에 따른 최적의 약물 효능 예측이 가능하게 됨을 의미하며 향후 약물 타겟 발굴에 기여할 것으로 기대된다.
조광현 교수는 “이번에 개발한 시스템생물학 기반 알츠하이머성 치매환자 약물 효능평가 플랫폼을 통해 향후 치매 치료제 개발 경쟁에서 우리나라가 국가적 우위를 선점할 수 있을 것으로 기대한다”고 밝혔다.
이번 연구는 보건복지부 한국보건산업진흥원의 국가치매극복기술개발 사업 및 한국연구재단의 중견연구자지원사업으로 수행됐으며, 연구성과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications)의 2021년 1월 12일자 논문으로 게재됐다.
(https://www.nature.com/articles/s41467-020-20440-5)
2021.01.13 조회수 75541
시스템생물학 이용 세계 최초 알츠하이머성 치매 환자 맞춤형 치료 효능 예측 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀 (장소영 박사과정(제1저자), 강의룡 박사과정, 장홍준 박사과정)은 서울대학교 의과대학 묵인희 교수 연구팀과 공동연구를 통해 시스템생물학*과 알츠하이머 환자 유래 뇌 오가노이드** 모델의 융합으로 환자 맞춤형 약물 효능평가 플랫폼(Drug-screening platform)을 세계 최초로 개발했다고 13일 밝혔다.
* 시스템생물학: IT의 수학모델링 및 컴퓨터시뮬레이션과 BT의 분자세포생물학 실험을 융합하여 복잡한 생명현상을 규명하고 설명하는 연구 패러다임
** 뇌 오가노이드: 환자의 역분화 줄기세포(iPSC) 유래 인공 미니 뇌
알츠하이머병은 치매의 약 70%를 차지하는 대표적 치매 질환이나 현재까지 발병 원인이 불명확하며, 근본적인 치료제도 없는 인류가 극복하지 못한 질병 중 하나다.
알츠하이머병 치료제 개발 난제 중 하나는 실제 살아있는 환자의 뇌를 직접 실험 샘플로 사용할 수 없다는 것이었다. 이는 수많은 치료제 후보군의 약물 효능을 정확히 평가하기가 어려워 치료제 개발의 걸림돌로 작용해왔다.
조광현 교수 공동 연구팀은 실제 치매환자에서 유래한 뇌 오가노이드 기반으로 생물학적 메커니즘에 대한 수학 모델링을 융합하여 약물효능 예측이 가능한 플랫폼을 세계 최초로 개발했다. 환자 혈액으로부터 역분화줄기세포(Induced-pluripotent stem cell)*를 구축 후 이를 이용하여 3D 뇌 오가노이드를 제작해 실제 환자의 뇌와 유사한 환경 구축을 통해 실험적 한계를 극복했다.
* 역분화줄기세포: 다능성이 없는 혈액 면역세포에 역분화를 일으키는 4가지 특정 유전자를 도입하여 배아 줄기세포와 같이 모든 종류의 세포로 분화할 수 있는 성질(다능성)을 가진 줄기세포
또한, 시스템생물학 기반 수학 모델링 기법으로 알츠하이머병의 신경세포 특이적 네트워크망을 구축하고, 이를 실제 알츠하이머병 환자 및 정상군 유래 뇌 오가노이드를 통하여 신경세포 컴퓨터 모델의 실효성을 검증했다.
이 연구결과는 알츠하이머병의 시스템생물학 기반 신경세포 컴퓨터 모델을 실제 환자 유래 뇌 오가노이드로 검증한 세계 최초의 사례이다. 이는 환자 맞춤형 치료(Precision medicine)의 불모지로 여겨졌던 뇌 질환분야에서도 알츠하이머병 환자의 유전형에 따른 최적의 약물 효능 예측이 가능하게 됨을 의미하며 향후 약물 타겟 발굴에 기여할 것으로 기대된다.
조광현 교수는 “이번에 개발한 시스템생물학 기반 알츠하이머성 치매환자 약물 효능평가 플랫폼을 통해 향후 치매 치료제 개발 경쟁에서 우리나라가 국가적 우위를 선점할 수 있을 것으로 기대한다”고 밝혔다.
이번 연구는 보건복지부 한국보건산업진흥원의 국가치매극복기술개발 사업 및 한국연구재단의 중견연구자지원사업으로 수행됐으며, 연구성과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications)의 2021년 1월 12일자 논문으로 게재됐다.
(https://www.nature.com/articles/s41467-020-20440-5)
2021.01.13 조회수 75541 -
 노화된 세포를 젊은 세포로 되돌리는 초기 원천기술 개발
우리 연구진이 노화된 세포를 젊은 세포로 되돌리는 역 노화 원천기술을 개발했다. 이를 활용하면 노화 현상을 막고 각종 노인성 질환을 사전 억제할 수 있는 치료제를 개발할 단서를 찾을 수 있을 것으로 기대된다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌리는 역 노화의 초기 원천기술을 개발했다고 26일 밝혔다.
조광현 교수팀의 이번 연구 결과는 ㈜아모레퍼시픽 기술연구원과의 산학 공동연구를 통해 최초로 개발된 노화 인공피부 모델에서 이 기술을 적용함으로써 입증하는 데 성공했다.
조 교수팀은 이번 연구를 위해 인간 진피 섬유아세포의 세포노화 신호전달 네트워크의 컴퓨터 모델을 개발한 후 시뮬레이션 분석을 통해 노화된 인간 진피 섬유아세포를 젊은 세포로 되돌리는데 필요한 핵심 인자를 찾아냈다. 이후 노화 인공피부 모델에서 핵심 인자를 조절함으로써 노화된 피부조직에서 감소된 콜라겐의 합성을 증가시키고 재생 능력을 회복시켜 젊은 피부조직의 특성을 보이게 하는 역 노화 기술을 개발했다.
연구팀 관계자는 이러한 역 노화 기술은 노화된 피부 등을 포함한 노화 현상 및 많은 노인성 질환의 발생을 사전에 억제할 수 있도록 근본적인 치료전략을 제시한 것으로 건강 수명을 오랫동안 유지하고 싶은 인류의 꿈을 실현하는데 한 걸음 다가선 결과라고 의미를 부여했다.
바이오및뇌공학과 안수균 박사과정 학생, 강준수 연구원, 이수범 연구원과 ㈜아모레퍼시픽의 바이오사이언스랩이 참여한 이번 연구 결과는 국제저명학술지인 `미국국립과학원회보(PNAS)'에 게재됐다.(논문명: Inhibition of 3-phosphoinositide-dependent protein kinase 1 (PDK1) can revert cellular senescence in human dermal fibroblasts)
현재 널리 연구되고 있는 회춘 전략은 이미 분화된 세포를 역분화시키는 4개의 `OSKM(Oct4, Sox2, Klf4, c-Myc) 야마나카 전사인자'를 일시적으로 발현시켜 후성유전학적 리모델링(epigenetic remodeling)을 일으킴으로써 노화된 세포를 젊은 상태로 되돌리는 부분적 역분화(partial reprogramming) 전략이다.
이 기술은 노화된 세포가 젊은 세포로 되돌아갈 수 있다는 것을 증명했지만 종양의 형성과 암의 진행을 유발하는 부작용이 생긴다. 따라서 이와 같은 부작용을 배제할 수 있는 정교한 제어 전략이 과학 난제로 남아있었다.
조 교수팀은 이러한 난제 해결을 위해 시스템생물학 연구 방법을 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌릴 수 있는 핵심 조절인자를 오래전부터 탐구하기 시작했다. 4년에 걸친 연구 끝에 단백질 합성, 세포의 성장 등을 조절하는 mTOR와 면역 물질 사이토카인의 생성에 관여하는 NF-kB를 동시에 제어하고 있는 상위 조절 인자인 `PDK1(3-phosphoinositide-dependent protein kinase 1)'을 찾아냈다.
연구팀은 PDK1을 억제함으로써 노화된 인간 진피 섬유아세포를 다시 정상적인 젊은 세포로 되돌릴 수 있음을 분자 세포실험 및 노화 인공피부 모델 실험을 통해 입증했다. 연구를 통해 노화된 인간 진피 섬유아세포에서 PDK1을 억제했을 때 세포노화 표지 인자들이 사라지고 주변 환경에 적절하게 반응하는 정상 세포로서 기능을 회복하는 현상을 확인했다.
연구 결과 노화된 인간 진피 섬유아세포에서는 PDK1이 mTOR와 NF-kB를 활성화해 노화와 관련된 분비 표현형(SASP: Senescence Associated Secretary Phenotype)을 유발하고 노화 형질을 유지하는 것과 연관돼 있음을 밝혀냈다. 즉, PDK1을 억제함으로써 다시 원래의 정상적인 젊은 세포 상태로 안전하게 되돌릴 수 있음을 증명한 것이다.
조 교수팀이 연구 과정에서 찾아낸 표적 단백질의 활성을 억제할 수 있는 저분자화합물과 관련된 신약개발과 그리고 전임상실험을 통해 노화된 세포의 정상 세포화라는 연구 결과는 새로운 노인성 질환의 치료 기술과 회춘 기술에 관한 연구를 본 궤도에 올려놓은 초석을 다진 획기적인 연구로 평가받고 있다.
실제 ㈜아모레퍼시픽 기술연구원은 이번 연구 결과로부터 동백추출물에서 PDK1 억제 성분을 추출해 노화된 피부의 주름을 개선하는 화장품을 개발중이다.
조광현 교수는 "그동안 비가역적 생명현상이라고 인식돼왔던 노화를 가역화할 가능성을 보여줬다ˮ라며 "이번 연구는 노화를 가역적 생명현상으로 인식하고 이에 적극적으로 대처해 건강 수명을 연장하는 한편 노인성 질환을 예방할 수 있는 새로운 시대의 서막을 열었다ˮ라고 의미를 부여했다.
이번 연구는 조광현 교수 연구팀의 시스템생물학 기반 가역화 기술 개발의 일환으로 이뤄졌으며, 연구팀은 지난 1월 같은 기술을 적용해 대장암세포를 다시 정상 대장 세포로 되돌리는 연구에 성공한 바 있다.
한편 이번 연구는 한국연구재단의 중견연구자지원사업과 KAIST 그랜드챌린지 30 (KC30) 프로젝트 및 아모레퍼시픽 R&D 센터의 지원으로 수행됐다.
2020.11.26 조회수 48583
노화된 세포를 젊은 세포로 되돌리는 초기 원천기술 개발
우리 연구진이 노화된 세포를 젊은 세포로 되돌리는 역 노화 원천기술을 개발했다. 이를 활용하면 노화 현상을 막고 각종 노인성 질환을 사전 억제할 수 있는 치료제를 개발할 단서를 찾을 수 있을 것으로 기대된다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌리는 역 노화의 초기 원천기술을 개발했다고 26일 밝혔다.
조광현 교수팀의 이번 연구 결과는 ㈜아모레퍼시픽 기술연구원과의 산학 공동연구를 통해 최초로 개발된 노화 인공피부 모델에서 이 기술을 적용함으로써 입증하는 데 성공했다.
조 교수팀은 이번 연구를 위해 인간 진피 섬유아세포의 세포노화 신호전달 네트워크의 컴퓨터 모델을 개발한 후 시뮬레이션 분석을 통해 노화된 인간 진피 섬유아세포를 젊은 세포로 되돌리는데 필요한 핵심 인자를 찾아냈다. 이후 노화 인공피부 모델에서 핵심 인자를 조절함으로써 노화된 피부조직에서 감소된 콜라겐의 합성을 증가시키고 재생 능력을 회복시켜 젊은 피부조직의 특성을 보이게 하는 역 노화 기술을 개발했다.
연구팀 관계자는 이러한 역 노화 기술은 노화된 피부 등을 포함한 노화 현상 및 많은 노인성 질환의 발생을 사전에 억제할 수 있도록 근본적인 치료전략을 제시한 것으로 건강 수명을 오랫동안 유지하고 싶은 인류의 꿈을 실현하는데 한 걸음 다가선 결과라고 의미를 부여했다.
바이오및뇌공학과 안수균 박사과정 학생, 강준수 연구원, 이수범 연구원과 ㈜아모레퍼시픽의 바이오사이언스랩이 참여한 이번 연구 결과는 국제저명학술지인 `미국국립과학원회보(PNAS)'에 게재됐다.(논문명: Inhibition of 3-phosphoinositide-dependent protein kinase 1 (PDK1) can revert cellular senescence in human dermal fibroblasts)
현재 널리 연구되고 있는 회춘 전략은 이미 분화된 세포를 역분화시키는 4개의 `OSKM(Oct4, Sox2, Klf4, c-Myc) 야마나카 전사인자'를 일시적으로 발현시켜 후성유전학적 리모델링(epigenetic remodeling)을 일으킴으로써 노화된 세포를 젊은 상태로 되돌리는 부분적 역분화(partial reprogramming) 전략이다.
이 기술은 노화된 세포가 젊은 세포로 되돌아갈 수 있다는 것을 증명했지만 종양의 형성과 암의 진행을 유발하는 부작용이 생긴다. 따라서 이와 같은 부작용을 배제할 수 있는 정교한 제어 전략이 과학 난제로 남아있었다.
조 교수팀은 이러한 난제 해결을 위해 시스템생물학 연구 방법을 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌릴 수 있는 핵심 조절인자를 오래전부터 탐구하기 시작했다. 4년에 걸친 연구 끝에 단백질 합성, 세포의 성장 등을 조절하는 mTOR와 면역 물질 사이토카인의 생성에 관여하는 NF-kB를 동시에 제어하고 있는 상위 조절 인자인 `PDK1(3-phosphoinositide-dependent protein kinase 1)'을 찾아냈다.
연구팀은 PDK1을 억제함으로써 노화된 인간 진피 섬유아세포를 다시 정상적인 젊은 세포로 되돌릴 수 있음을 분자 세포실험 및 노화 인공피부 모델 실험을 통해 입증했다. 연구를 통해 노화된 인간 진피 섬유아세포에서 PDK1을 억제했을 때 세포노화 표지 인자들이 사라지고 주변 환경에 적절하게 반응하는 정상 세포로서 기능을 회복하는 현상을 확인했다.
연구 결과 노화된 인간 진피 섬유아세포에서는 PDK1이 mTOR와 NF-kB를 활성화해 노화와 관련된 분비 표현형(SASP: Senescence Associated Secretary Phenotype)을 유발하고 노화 형질을 유지하는 것과 연관돼 있음을 밝혀냈다. 즉, PDK1을 억제함으로써 다시 원래의 정상적인 젊은 세포 상태로 안전하게 되돌릴 수 있음을 증명한 것이다.
조 교수팀이 연구 과정에서 찾아낸 표적 단백질의 활성을 억제할 수 있는 저분자화합물과 관련된 신약개발과 그리고 전임상실험을 통해 노화된 세포의 정상 세포화라는 연구 결과는 새로운 노인성 질환의 치료 기술과 회춘 기술에 관한 연구를 본 궤도에 올려놓은 초석을 다진 획기적인 연구로 평가받고 있다.
실제 ㈜아모레퍼시픽 기술연구원은 이번 연구 결과로부터 동백추출물에서 PDK1 억제 성분을 추출해 노화된 피부의 주름을 개선하는 화장품을 개발중이다.
조광현 교수는 "그동안 비가역적 생명현상이라고 인식돼왔던 노화를 가역화할 가능성을 보여줬다ˮ라며 "이번 연구는 노화를 가역적 생명현상으로 인식하고 이에 적극적으로 대처해 건강 수명을 연장하는 한편 노인성 질환을 예방할 수 있는 새로운 시대의 서막을 열었다ˮ라고 의미를 부여했다.
이번 연구는 조광현 교수 연구팀의 시스템생물학 기반 가역화 기술 개발의 일환으로 이뤄졌으며, 연구팀은 지난 1월 같은 기술을 적용해 대장암세포를 다시 정상 대장 세포로 되돌리는 연구에 성공한 바 있다.
한편 이번 연구는 한국연구재단의 중견연구자지원사업과 KAIST 그랜드챌린지 30 (KC30) 프로젝트 및 아모레퍼시픽 R&D 센터의 지원으로 수행됐다.
2020.11.26 조회수 48583 -
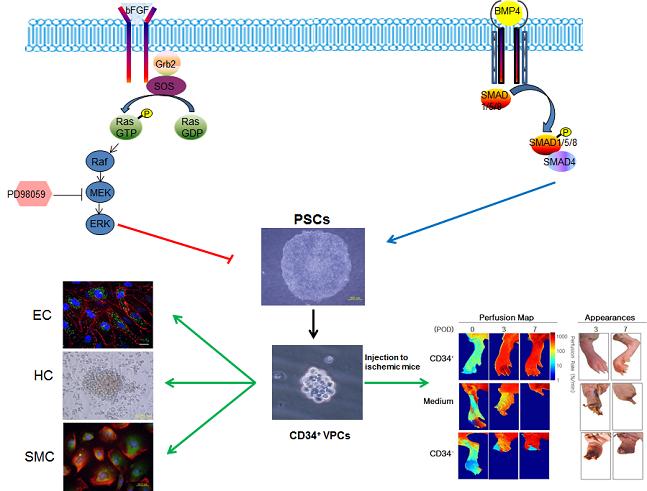 기능성 혈관전구세포 분화 성공
- 배아줄기세포 및 역분화줄기세포로 부터 기능성 혈관전구세포 분화 성공
- Blood誌 표지논문 게재, 줄기세포를 이용한 혈관질환의 세포치료 가능성 열어
우리학교 한용만 교수팀이 인간배아줄기세포 및 역분화줄기세포로부터 혈관전구세포로의 분화를 성공하였다.
이번 연구에서는 기존에 알려진 배아체형성이나 생쥐세포공배양 방식을 뛰어넘어, 인간배아줄기세포의 신호전달체계의 조절을 통해 혈관전구세포를 분화 유도하였다.
연구팀은 인간배아줄기세포를 분화하기 위해, 인간배아줄기세포의 자가재생산에 매우 중요한 역할을 하는 MEK/ERK 및 BMP 신호전달체계를 조절하여 혈관전구세포를 약 20%가량 분화 유도하였다.
이러한 방식으로 생산된 혈관전구세포는 체외에서 혈관계를 구성하는 혈관내피세포, 혈관평활근세포 및 조혈세포로의 분화가 이뤄졌고, 체내에서도 역시 혈관을 형성함을 누드마우스모델을 통해 확인하였다.
또한, 인간배아줄기세포 유래의 혈관전구세포는 하지허혈성질환동물에 주입하였을 때, 직접 혈관을 형성하거나 혈관형성에 관여하는 성장인자등을 분비하여, 하지허혈성질환동물의 혈류량이 증가한 반면 허혈성 부위의 괴사는 감소하였다.
이번 연구는 교육과학기술부(장관 이주호) 21세기프론티어연구개발사업인 세포응용연구사업단의 연구비 지원으로 수행되었으며, 고규영 교수(KAIST), 최철희 교수(KAIST), 정형민 교수(차의과대학교), 조이숙 박사(한국생명공학연구원) 등이 참여하였다.
연구결과는 올해 9월 美혈액학회지인 "Blood(IF:10.55)"에 표지논문으로 최종 게재되었으며, 국내특허 등록 및 해외 PCT출원을 마친 상태이다.
이 실험결과를 바탕으로, 향후 혈관질환분야에 줄기세포를 이용한 환자맞춤형 세포치료의 가능성을 열어줄 것으로 기대된다.
[그림] 신호전달체계의 조절을 통한 배아 및 역분화 줄기세포의 혈관전구세포의 분화
2010.12.27 조회수 19611
기능성 혈관전구세포 분화 성공
- 배아줄기세포 및 역분화줄기세포로 부터 기능성 혈관전구세포 분화 성공
- Blood誌 표지논문 게재, 줄기세포를 이용한 혈관질환의 세포치료 가능성 열어
우리학교 한용만 교수팀이 인간배아줄기세포 및 역분화줄기세포로부터 혈관전구세포로의 분화를 성공하였다.
이번 연구에서는 기존에 알려진 배아체형성이나 생쥐세포공배양 방식을 뛰어넘어, 인간배아줄기세포의 신호전달체계의 조절을 통해 혈관전구세포를 분화 유도하였다.
연구팀은 인간배아줄기세포를 분화하기 위해, 인간배아줄기세포의 자가재생산에 매우 중요한 역할을 하는 MEK/ERK 및 BMP 신호전달체계를 조절하여 혈관전구세포를 약 20%가량 분화 유도하였다.
이러한 방식으로 생산된 혈관전구세포는 체외에서 혈관계를 구성하는 혈관내피세포, 혈관평활근세포 및 조혈세포로의 분화가 이뤄졌고, 체내에서도 역시 혈관을 형성함을 누드마우스모델을 통해 확인하였다.
또한, 인간배아줄기세포 유래의 혈관전구세포는 하지허혈성질환동물에 주입하였을 때, 직접 혈관을 형성하거나 혈관형성에 관여하는 성장인자등을 분비하여, 하지허혈성질환동물의 혈류량이 증가한 반면 허혈성 부위의 괴사는 감소하였다.
이번 연구는 교육과학기술부(장관 이주호) 21세기프론티어연구개발사업인 세포응용연구사업단의 연구비 지원으로 수행되었으며, 고규영 교수(KAIST), 최철희 교수(KAIST), 정형민 교수(차의과대학교), 조이숙 박사(한국생명공학연구원) 등이 참여하였다.
연구결과는 올해 9월 美혈액학회지인 "Blood(IF:10.55)"에 표지논문으로 최종 게재되었으며, 국내특허 등록 및 해외 PCT출원을 마친 상태이다.
이 실험결과를 바탕으로, 향후 혈관질환분야에 줄기세포를 이용한 환자맞춤형 세포치료의 가능성을 열어줄 것으로 기대된다.
[그림] 신호전달체계의 조절을 통한 배아 및 역분화 줄기세포의 혈관전구세포의 분화
2010.12.27 조회수 19611