%EC%97%B0%EA%B5%AC%EC%8B%A4
-
 하운드(Hound) 로봇, 100m를 19.87초 주파, 기네스 기록
우리 대학 기계공학과의 박해원 교수 연구팀이 제작한 사족 로봇 하운드(Hound)의 사족 보행 로봇의 100m 달리기 기록이 기네스 세계 기록으로 인정받았다고 15일 밝혔다.
하운드(Hound)는 KAIST 동적 로봇 설계 및 제어 연구실(Dynamic Robot Control and Design Laboratory)에서 제작된 로봇으로, 지난 2023년 10월 26일에 측정된 실험을 통해 정지 상태에서 출발해 100미터 선을 19.87초 만에 통과한 후 완전히 멈추는 데 성공했다. 이 성과는 AI 방법론 중 하나인 강화학습을 이용해 시뮬레이션 가상환경에서 훈련된 단일 제어기를 통해 달성됐다.
연구팀은 하운드(Hound) 로봇이 고속으로 달릴 수 있도록, 액추에이터 출력의 한계를 최대한 이용하기 위해, 모터가 최대로 낼 수 있는 한계 토크와 속도 특성을 강화학습에 활용했다. 또한, 대칭적인 걸음새를 통해 모터의 출력을 고르게 분배하고, 로봇의 빠른 움직임을 위해 경량 발바닥을 설계했다. 이러한 종합적인 설계와 제어에 대한 접근방식을 통해 하운드(Hound)는 빠른 속도로 100미터를 주파할 수 있었다.
하운드(Hound)의 100미터 달리기 기록은 우리 대학 대운동장의 실외 육상 트랙에서 공식적으로 측정됐다.
하운드(Hound)는 실외뿐만 아니라 실내 러닝머신 위에서 6.5m/s (시속 23.4km)의 주행 속도를 기록했다. 이는 전기 모터 기반 사족 로봇의 최고속도이며, 기존 메사추세츠 공과대학교(MIT)의 치타 2(Cheetah 2)의 6.4m/s를 뛰어넘는 기록이다. 박해원 교수 연구팀은 이 성과 또한 기네스 기록 인증을 신청 중이다.
연구 책임자인 기계공학과 박해원 교수는 “KAIST의 기술로 직접 설계 제작된 사족 보행 로봇과 AI 학습 기반 제어기로 보행 로봇 세계 최고속도를 세움으로써 우리나라의 로봇 하드웨어 기술 및 로봇제어 AI 기술이 세계 최고 수준을 보여줬다는 데 의의가 있다”이라고 소감을 전했다.
한편 이번 연구는 2019년 국방과학연구소 미래도전국방기술 연구개발사업(912768601)의 지원을 받아 수행됐다.
기네스 기록 홈페이지 링크 : https://www.guinnessworldrecords.com/world-records/625586-fastest-100-m-by-a-quadrupedal-robot
기네스 Youtube 계정에 올라온 영상 : https://www.youtube.com/shorts/sdF1cn7iX0g
2023.12.15 조회수 4022
하운드(Hound) 로봇, 100m를 19.87초 주파, 기네스 기록
우리 대학 기계공학과의 박해원 교수 연구팀이 제작한 사족 로봇 하운드(Hound)의 사족 보행 로봇의 100m 달리기 기록이 기네스 세계 기록으로 인정받았다고 15일 밝혔다.
하운드(Hound)는 KAIST 동적 로봇 설계 및 제어 연구실(Dynamic Robot Control and Design Laboratory)에서 제작된 로봇으로, 지난 2023년 10월 26일에 측정된 실험을 통해 정지 상태에서 출발해 100미터 선을 19.87초 만에 통과한 후 완전히 멈추는 데 성공했다. 이 성과는 AI 방법론 중 하나인 강화학습을 이용해 시뮬레이션 가상환경에서 훈련된 단일 제어기를 통해 달성됐다.
연구팀은 하운드(Hound) 로봇이 고속으로 달릴 수 있도록, 액추에이터 출력의 한계를 최대한 이용하기 위해, 모터가 최대로 낼 수 있는 한계 토크와 속도 특성을 강화학습에 활용했다. 또한, 대칭적인 걸음새를 통해 모터의 출력을 고르게 분배하고, 로봇의 빠른 움직임을 위해 경량 발바닥을 설계했다. 이러한 종합적인 설계와 제어에 대한 접근방식을 통해 하운드(Hound)는 빠른 속도로 100미터를 주파할 수 있었다.
하운드(Hound)의 100미터 달리기 기록은 우리 대학 대운동장의 실외 육상 트랙에서 공식적으로 측정됐다.
하운드(Hound)는 실외뿐만 아니라 실내 러닝머신 위에서 6.5m/s (시속 23.4km)의 주행 속도를 기록했다. 이는 전기 모터 기반 사족 로봇의 최고속도이며, 기존 메사추세츠 공과대학교(MIT)의 치타 2(Cheetah 2)의 6.4m/s를 뛰어넘는 기록이다. 박해원 교수 연구팀은 이 성과 또한 기네스 기록 인증을 신청 중이다.
연구 책임자인 기계공학과 박해원 교수는 “KAIST의 기술로 직접 설계 제작된 사족 보행 로봇과 AI 학습 기반 제어기로 보행 로봇 세계 최고속도를 세움으로써 우리나라의 로봇 하드웨어 기술 및 로봇제어 AI 기술이 세계 최고 수준을 보여줬다는 데 의의가 있다”이라고 소감을 전했다.
한편 이번 연구는 2019년 국방과학연구소 미래도전국방기술 연구개발사업(912768601)의 지원을 받아 수행됐다.
기네스 기록 홈페이지 링크 : https://www.guinnessworldrecords.com/world-records/625586-fastest-100-m-by-a-quadrupedal-robot
기네스 Youtube 계정에 올라온 영상 : https://www.youtube.com/shorts/sdF1cn7iX0g
2023.12.15 조회수 4022 -
 성형진 교수 연구팀, 랩온어칩(Lab on a Chip)지 표지논문 게재
우리 대학 기계공학과 성형진 교수 연구팀(초세대협업연구실)이 고주파수 표면탄성파 기반 마이크로스케일 음향흐름유동을 이용해 나노리터급 액적 내 화학적 농도 제어 기술을 개발했다.
동전 크기의 초소형 미세유체칩 내에 서로 섞이지 않는 두 유체로 조성된 마이크로스케일 액적을 기반으로 하는 액적 기반 미세유체역학 분야에서 개별 액적 내 화학적 농도를 제어하기 위해 그동안 많은 노력이 기울여져 왔다. 하지만 지금까지 개발된 액적 내 화학적 농도 제어 기술은 복잡한 미세유로 혹은 별도의 외부 구동시스템이 필요하거나, 만들어진 액적의 병합 혹은 희석을 통해 액적 내 화학적 농도를 제어하기 때문에 동적 제어가 불가능하고 액적 간 화학적 농도 구배를 형성하기 어렵다는 한계를 지니고 있었다.
이번 연구에서 성형진 교수 연구팀은 고주파수 표면탄성파를 미세유체칩 내 유동에 집속하여 음향흐름유동을 발생시켜 농도 제어가 필요한 액상 화학 시료와 완충용액을 혼합한 후, 혼합된 액상 시료를 분산상으로 하는 나노리터급 액적을 생성함으로써 액적 내 화학적 농도의 정밀 제어할 수 있음을 보였다. 개발된 기술을 활용하여 미세유체칩 내 고속으로 생성되는 개별 액적의 화학적 농도를 동적으로 제어할 수 있으며, 더 나아가 액적라이브러리 내 액적 간 화학적 농도 구배를 자유롭게 형성할 수 있는 최초의 기술이라는 점에서 기존 기술보다 진일보한 기술이라는 평가를 받았다.
아울러 평면파 각스펙트럼 이론과 등가 구경 이론을 이용해 원형 빗살무늬전극에서 생성되는 집속 표면탄성파의 집속점 위치가 기하학적 중심이 아니라는 점을 밝혔다. 또한 MHz 대역의 초음파 대역의 압전기판 위 표면탄성파 및 유체 내 종파의 감쇄에 의해 생성되는 마이크로스케일 음향흐름유동 및 와류를 전산유체역학적으로 가시화하여 인가되는 표면탄성파의 진폭과 생성되는 음향흐름유동장 사이의 관계를 규명해 효율적인 마이크로스케일 유동 혼합을 위한 조건을 제시했다.
이번 연구는 영국왕립화학회(Royal Society of Chemistry)에서 발간하는 미세유체역학 및 마이크로타스(microTAS) 분야의 세계적 권위 국제학술지인 랩온어칩(Lab on a Chip)지 2020년 21호의 표지논문으로 선정됐다 (논문명: Acoustofluidic generation of droplets with tunable chemical concentrations). 이는 성형진 교수의 Lab on a Chip 학술지 2016년 4호, 17호, 2017년 6호, 2018년 3호, 19호에 이은 여섯 번째 표지논문으로 미세유체역학 분야의 선도적 연구 성과다.
성형진 교수 연구팀은 그동안 미세유체역학, 난류, 고체-유체 상호작용 연구 분야에서 탁월한 연구 성과를 내 SCI급 국제학술지에 380여편의 논문을 게재했으며, 이번 연구는 과학기술정보통신부의 재원으로 한국연구재단의 중견연구와 초세대협업연구실의 지원으로 수행됐다.
박진수 박사 (현 전남대 교수)와 성형진 교수는 “이번 연구에서 개발된 음향미세유체역학 기술을 통해 마이크로스케일 액적 내 화학적 농도를 칩 내에서 정밀·동적 제어하고 액적 간 농도 구배를 형성할 수 있는 최초의 기술로서, 개발된 기술이 약물스크리닝, 단일 세포 및 입자 기반 분석, 기능성 마이크로캡슐 합성 등 액적 기반 미세유체역학 시스템이 사용되는 다양한 분야에서 핵심 원천기술로 널리 활용될 수 있을 것으로 기대된다”라며 연구 의의를 밝혔다.
2020.11.10 조회수 31075
성형진 교수 연구팀, 랩온어칩(Lab on a Chip)지 표지논문 게재
우리 대학 기계공학과 성형진 교수 연구팀(초세대협업연구실)이 고주파수 표면탄성파 기반 마이크로스케일 음향흐름유동을 이용해 나노리터급 액적 내 화학적 농도 제어 기술을 개발했다.
동전 크기의 초소형 미세유체칩 내에 서로 섞이지 않는 두 유체로 조성된 마이크로스케일 액적을 기반으로 하는 액적 기반 미세유체역학 분야에서 개별 액적 내 화학적 농도를 제어하기 위해 그동안 많은 노력이 기울여져 왔다. 하지만 지금까지 개발된 액적 내 화학적 농도 제어 기술은 복잡한 미세유로 혹은 별도의 외부 구동시스템이 필요하거나, 만들어진 액적의 병합 혹은 희석을 통해 액적 내 화학적 농도를 제어하기 때문에 동적 제어가 불가능하고 액적 간 화학적 농도 구배를 형성하기 어렵다는 한계를 지니고 있었다.
이번 연구에서 성형진 교수 연구팀은 고주파수 표면탄성파를 미세유체칩 내 유동에 집속하여 음향흐름유동을 발생시켜 농도 제어가 필요한 액상 화학 시료와 완충용액을 혼합한 후, 혼합된 액상 시료를 분산상으로 하는 나노리터급 액적을 생성함으로써 액적 내 화학적 농도의 정밀 제어할 수 있음을 보였다. 개발된 기술을 활용하여 미세유체칩 내 고속으로 생성되는 개별 액적의 화학적 농도를 동적으로 제어할 수 있으며, 더 나아가 액적라이브러리 내 액적 간 화학적 농도 구배를 자유롭게 형성할 수 있는 최초의 기술이라는 점에서 기존 기술보다 진일보한 기술이라는 평가를 받았다.
아울러 평면파 각스펙트럼 이론과 등가 구경 이론을 이용해 원형 빗살무늬전극에서 생성되는 집속 표면탄성파의 집속점 위치가 기하학적 중심이 아니라는 점을 밝혔다. 또한 MHz 대역의 초음파 대역의 압전기판 위 표면탄성파 및 유체 내 종파의 감쇄에 의해 생성되는 마이크로스케일 음향흐름유동 및 와류를 전산유체역학적으로 가시화하여 인가되는 표면탄성파의 진폭과 생성되는 음향흐름유동장 사이의 관계를 규명해 효율적인 마이크로스케일 유동 혼합을 위한 조건을 제시했다.
이번 연구는 영국왕립화학회(Royal Society of Chemistry)에서 발간하는 미세유체역학 및 마이크로타스(microTAS) 분야의 세계적 권위 국제학술지인 랩온어칩(Lab on a Chip)지 2020년 21호의 표지논문으로 선정됐다 (논문명: Acoustofluidic generation of droplets with tunable chemical concentrations). 이는 성형진 교수의 Lab on a Chip 학술지 2016년 4호, 17호, 2017년 6호, 2018년 3호, 19호에 이은 여섯 번째 표지논문으로 미세유체역학 분야의 선도적 연구 성과다.
성형진 교수 연구팀은 그동안 미세유체역학, 난류, 고체-유체 상호작용 연구 분야에서 탁월한 연구 성과를 내 SCI급 국제학술지에 380여편의 논문을 게재했으며, 이번 연구는 과학기술정보통신부의 재원으로 한국연구재단의 중견연구와 초세대협업연구실의 지원으로 수행됐다.
박진수 박사 (현 전남대 교수)와 성형진 교수는 “이번 연구에서 개발된 음향미세유체역학 기술을 통해 마이크로스케일 액적 내 화학적 농도를 칩 내에서 정밀·동적 제어하고 액적 간 농도 구배를 형성할 수 있는 최초의 기술로서, 개발된 기술이 약물스크리닝, 단일 세포 및 입자 기반 분석, 기능성 마이크로캡슐 합성 등 액적 기반 미세유체역학 시스템이 사용되는 다양한 분야에서 핵심 원천기술로 널리 활용될 수 있을 것으로 기대된다”라며 연구 의의를 밝혔다.
2020.11.10 조회수 31075 -
 중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
2020.07.14 조회수 27723
중증 코로나19 환자의 사이토카인 폭풍 원인 찾았다
우리 대학 의과학대학원 신의철 교수와 생명과학과 정인경 교수 연구팀이 서울아산병원 김성한 교수·연세대 세브란스병원 최준용·안진영 교수, 충북대병원 정혜원 교수와의 공동연구를 통해 중증 코로나19 환자에서 나타나는 과잉 염증반응을 일으키는 원인을 발견했다.
과잉 염증반응이란 흔히 '사이토카인 폭풍'이라고도 불리는 증상인데 면역 물질인 사이토카인(cytokine)이 과다하게 분비돼 이 물질이 정상 세포를 공격하는 현상이다.
☞ 사이토카인(cytokine): 면역세포로부터 분비되는 단백질 면역조절제로서 자가분비형 신호전달(autocrine signaling), 측분비 신호전달(paracrine signaling), 내분비 신호전달(endocrine signaling) 과정에서 특정 수용체와 결합하여 면역반응에 관여한다. 세포의 증식, 분화, 세포사멸 또는 상처 치료 등에 관여하는 다양한 종류의 사이토카인이 존재하며, 특히 면역과 염증에 관여하는 것이 많다. 세포를 의미하는 접두어인 ‘cyto’와 그리스어로 ‘움직이다’를 의미하는 ‘kinein’으로부터 cytokine이 명명됐다.
☞ 사이토카인 폭풍(cytokine storm): 인체에 바이러스가 침투하였을 때 면역 물질인 사이토카인이 과다하게 분비되어 정상 세포를 공격하는 현상
빠르게 확산하고 있는 코로나19 바이러스는 전 세계적으로 이미 1,300만 명 이상이 감염됐고 이 중 50만 명 이상이 사망했다. 코로나19 바이러스에 감염된 환자들은 경증 질환만을 앓고 자연적으로 회복되는 경우가 많으나, 어떤 환자들은 중증 질환으로 발전해 심한 경우 사망하기도 한다. 흔히 사이토카인 폭풍 때문에 중증 코로나19가 유발된다는 사실이 널리 알려져 있다. 하지만 어떤 이유에서 과잉 염증반응이 일어나는지 구체적인 원인은 아직도 알려지지 않아 중증 코로나19 환자의 치료에 많은 어려움을 겪고 있다.
우리 대학 의과학대학원 이정석 연구원 및 생명과학과 박성완 연구원이 주도한 이번 연구에서 공동연구팀은 중증 및 경증 코로나19 환자로부터 혈액을 얻은 후 면역세포들을 분리하고 단일 세포 유전자발현 분석이라는 최신 연구기법을 적용해 그 특성을 상세히 분석했다. 그 결과, 중증 또는 경증을 막론하고 코로나19 환자의 면역세포에서 염증성 사이토카인의 일종인 종양괴사인자(TNF)와 인터류킨-1(IL-1)이 공통으로 나타나는 현상을 발견했다. 연구팀은 특히 중증과 경증 환자를 비교 분석한 결과, 인터페론이라는 사이토카인 반응이 중증 환자에게서만 특징적으로 강하게 나타남을 확인했다.
☞ 인터페론(interferon): 사이토카인(cytokine)의 일종으로 숙주 세포가 바이러스, 세균, 기생균 등 다양한 병원체에 감염되거나 혹은 암세포 존재 하에서 합성되고 분비되는 당단백질이다. 일반적으로 바이러스에 감염된 세포에서 분비되는 제 1형 인터페론이 많이 알려져 있으며 주변 세포들이 항바이러스 방어 효과를 나타낼 수 있도록 돕는다.
지금까지 인터페론은 항바이러스 작용을 하는 착한(?) 사이토카인으로 알려져 있으나, 공동연구팀은 인터페론 반응이 코로나19 환자에서는 오히려 과도한 염증반응을 촉발하는 원인이 될 수 있다는 사실을 다양한 방법을 통해 이를 증명했다.
삼성미래기술육성재단과 서경배과학재단의 지원을 받아 수행한 공동연구팀의 이번 연구결과는 면역학 분야 국제 학술지인 사이언스 면역학(Science Immunology)誌 7월 10일 字에 게재됐다(논문명: Immunophenotyping of COVID-19 and Influenza Highlights the Role of Type I Interferons in Development of Severe COVID-19).
연구팀은 중증 코로나19 환자의 과잉 염증반응 완화를 위해 현재에는 스테로이드제와 같은 비특이적 항염증 약물이 사용하고 있는데 이번 연구 성과를 계기로 인터페론을 표적으로 하는 새로운 치료방법도 고려할 수 있음을 보여준다며 중증 코로나19 환자 치료에 새로운 패러다임을 제시한 획기적인 연구라고 이 연구에 대한 의미를 부여했다.
관련 학계와 의료계에서도 코로나19의 재확산 등 팬데믹이 지속되는 현 상황에서 KAIST와 대학병원 연구팀이 긴밀한 협력을 통해 코로나19의 면역학적 원리를 밝히고 새로운 치료전략을 제시한 이번 연구를 중개 연구(translational research)의 주요 성과로 높게 평가했다.
공동연구팀은 현재 중증 코로나19 환자의 과잉 염증반응을 완화해 환자 생존율을 높일 수 있는 약물을 시험관 내에서 효율적으로 검색하고 발굴하는 방법을 개발하는 후속연구를 진행중에 있다.
이번 연구를 주도한 이정석 연구원은 내과 전문의로서 의과학대학원 박사과정에 재학 중인데 "중증 코로나19 환자의 의료적 문제를 해결하기 위해 정인경 교수 연구팀과 함께 이번 연구를 긴박하게 시작했는데 서울아산병원과 연세대 세브란스병원·충북대병원의 적극적인 지원에 힘입어 불과 3개월 만에 마칠 수 있게 됐다ˮ고 말했다.
정인경 교수는 "코로나19와 같은 신규 질환의 특성을 신속하게 규명하는데 있어 최신 단일세포 전사체 빅데이터 분석법이 매우 효과적ˮ이었음을 밝혔다.
신의철 교수도 "이번 연구는 코로나19 환자의 면역세포에서 어떤 일이 벌어지는지 상세히 연구함으로써 향후 치료전략을 설계할 수 있는 토대를 마련했다는 점에서 매우 중요하고 의미가 있는 연구ˮ라고 평가했다.
신의철 교수와 정인경 교수는 이와 함께 "중증 코로나19 환자의 생존율을 높일 수 있도록 새로운 면역기전 연구 및 환자 맞춤 항염증 약물 사용에 관한 연구를 지속적으로 수행할 것ˮ이라고 강조했다.
2020.07.14 조회수 27723 -
 인공신경망 기반 핵융합플라즈마 자기장 재구성 기술 개발
우리 대학 원자력및양자공학과 김영철 교수 연구팀(핵융합및플라즈마연구실)이 국가핵융합연구소, ㈜모비스 연구진과 공동으로 인공신경망 기반 핵융합플라즈마 자기장의 재구성 기법을 개발했다.
김 교수 연구팀은 비실시간으로 엄밀히 계산된 자기장 구조와의 오차를 최소화함과 동시에 실시간으로 해당 정보를 제공할 수 있는 인공신경망을 개발해 핵융합플라즈마 제어 성능을 높이는 데 기여할 것으로 기대된다.
정세민 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘뉴클리어 퓨전(Nuclear Fusion)’ 2019년 12월 3일 자에 게재됐다. (논문명: Deep neural network Grad-Shafranov solver constrained with measured magnetic signals)
핵융합 연구에 널리 사용되는 토카막은 실시간으로 재구성된 자기장 구조를 바탕으로 초고온(약 1억도) 핵융합 플라즈마의 운전과 제어를 가능하게 만든다. 따라서 재구성된 자기장 구조의 정확도는 토카막 운전 성능과 밀접한 관계가 있다.
2계 비선형 미분방정식을 따르는 토카막의 내부 자기장은 일반적으로 수치해석 기법과 외부에서 측정된 자기장 값을 이용하여 재구성된다. 실시간과 비실시간 재구성 기법이 존재하며, 비실시간 기법의 정확도가 실시간보다 높다고 알려졌지만 이름에서도 확인할 수 있듯 실시간 운전에 활용하기 어렵다는 아쉬움이 있다.
연구팀은 비실시간 기법의 정확도를 유지하되 실시간으로 해당 정보를 확보할 수 있는 알고리즘을 인공신경망을 활용해 개발했다. 측정된 외부 자기장과 토카막 내부 공간 정보를 입력값으로 하고 비실시간 기법을 활용해 재구성된 자기장을 출력값으로 신경망을 훈련했다.
또한, 신경망의 출력값은 앞서 언급된 2계 비선형 미분방정식을 만족해야 하므로 이 역시 신경망의 훈련 조건으로 둬 단순한 자기장 재구성을 넘어서 해당 문제의 지배방정식 역시 만족하도록 했다.
연구팀이 개발한 기법은 그 성능의 우수성과 더불어 토카막의 고성능 운전 달성에 큰 영향을 미칠 것을 인정받았다. 세계적으로 활발히 진행 중인 토카막 연구에 가장 기초적이며 중추적인 토카막 내부 자기장 정보를 최소화된 오차 내에서 실시간으로 제공할 수 있다는 점에서 토카막을 활용한 핵융합발전의 가능성을 제고할 수 있을 것으로 기대된다.
이번 연구는 과학기술정보통신부 한국연구재단의 핵융합기초연구사업과 개인연구사업(신진연구) 및 기관고유과제 KAI-NEET의 지원을 받아 수행됐다.
타기관 참여연구진
국가핵융합연구소(공저자순): 박준교, 이상곤, 한현선, 김현석 ㈜모비스(공저자순): 이근호, 권대호
□ 그림 설명
그림1. 토카막 내부 재구성된 자기장 구조
2020.02.05 조회수 10432
인공신경망 기반 핵융합플라즈마 자기장 재구성 기술 개발
우리 대학 원자력및양자공학과 김영철 교수 연구팀(핵융합및플라즈마연구실)이 국가핵융합연구소, ㈜모비스 연구진과 공동으로 인공신경망 기반 핵융합플라즈마 자기장의 재구성 기법을 개발했다.
김 교수 연구팀은 비실시간으로 엄밀히 계산된 자기장 구조와의 오차를 최소화함과 동시에 실시간으로 해당 정보를 제공할 수 있는 인공신경망을 개발해 핵융합플라즈마 제어 성능을 높이는 데 기여할 것으로 기대된다.
정세민 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘뉴클리어 퓨전(Nuclear Fusion)’ 2019년 12월 3일 자에 게재됐다. (논문명: Deep neural network Grad-Shafranov solver constrained with measured magnetic signals)
핵융합 연구에 널리 사용되는 토카막은 실시간으로 재구성된 자기장 구조를 바탕으로 초고온(약 1억도) 핵융합 플라즈마의 운전과 제어를 가능하게 만든다. 따라서 재구성된 자기장 구조의 정확도는 토카막 운전 성능과 밀접한 관계가 있다.
2계 비선형 미분방정식을 따르는 토카막의 내부 자기장은 일반적으로 수치해석 기법과 외부에서 측정된 자기장 값을 이용하여 재구성된다. 실시간과 비실시간 재구성 기법이 존재하며, 비실시간 기법의 정확도가 실시간보다 높다고 알려졌지만 이름에서도 확인할 수 있듯 실시간 운전에 활용하기 어렵다는 아쉬움이 있다.
연구팀은 비실시간 기법의 정확도를 유지하되 실시간으로 해당 정보를 확보할 수 있는 알고리즘을 인공신경망을 활용해 개발했다. 측정된 외부 자기장과 토카막 내부 공간 정보를 입력값으로 하고 비실시간 기법을 활용해 재구성된 자기장을 출력값으로 신경망을 훈련했다.
또한, 신경망의 출력값은 앞서 언급된 2계 비선형 미분방정식을 만족해야 하므로 이 역시 신경망의 훈련 조건으로 둬 단순한 자기장 재구성을 넘어서 해당 문제의 지배방정식 역시 만족하도록 했다.
연구팀이 개발한 기법은 그 성능의 우수성과 더불어 토카막의 고성능 운전 달성에 큰 영향을 미칠 것을 인정받았다. 세계적으로 활발히 진행 중인 토카막 연구에 가장 기초적이며 중추적인 토카막 내부 자기장 정보를 최소화된 오차 내에서 실시간으로 제공할 수 있다는 점에서 토카막을 활용한 핵융합발전의 가능성을 제고할 수 있을 것으로 기대된다.
이번 연구는 과학기술정보통신부 한국연구재단의 핵융합기초연구사업과 개인연구사업(신진연구) 및 기관고유과제 KAI-NEET의 지원을 받아 수행됐다.
타기관 참여연구진
국가핵융합연구소(공저자순): 박준교, 이상곤, 한현선, 김현석 ㈜모비스(공저자순): 이근호, 권대호
□ 그림 설명
그림1. 토카막 내부 재구성된 자기장 구조
2020.02.05 조회수 10432 -
 정재웅 교수, 스마트폰으로 뇌 신경회로 무선 제어 기술 개발
〈 김충연, 변상혁 박사과정, 정재웅 교수〉
우리 대학 전기및전자공학부 정재웅 교수와 미국 워싱턴대(University of Washington) 마이클 브루카스(Michael Bruchas) 교수 공동 연구팀이 스마트폰 앱 조작을 통해 약물과 빛을 뇌 특정 부위에 전달함으로써 신경회로를 정교하게 조절할 수 있는 뇌 이식용 무선 기기를 개발했다.
이번 기술 개발을 통해 장기간의 동물 실험이 필요한 신약 개발뿐 아니라 치매, 파킨슨병 등 뇌 질환 치료에도 적용할 수 있을 것으로 기대된다.
라자 콰지(Raza Qazi, 1저자), 김충연, 변상혁 연구원이 개발하고 워싱턴대 신경과학 연구원들이 공동으로 참여한 이번 연구는 의공학 분야 국제 학술지 ‘네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)’ 8월 6일 자에 게재됐다. (논문명 : Wireless optofluidic brain probes for chronic neuropharmacology and photostimulation).
광유전학과 신경약물학은 주변 신경회로에 영향을 주지 않고 목표로 하는 뉴런이나 신경회로만을 빛 또는 약물, 혹은 그 둘의 조합을 이용해 정교하게 제어할 수 있다. 기존의 전기자극을 활용한 방법에 비해 훨씬 더 높은 시공간적 해상도를 가져 최근 뇌 연구 및 뇌 질병 치료 목적으로 주목받고 있다.
하지만 현재 뇌 연구에 일반적으로 쓰는 기기는 상대적으로 크기가 커 뇌 조직 손상, 정교한 선택적 신경회로 제어 불가, 하나의 다기능성 프로브(probe) 형태로 구현이 어렵다. 또한, 기존 기기는 실리카(silica)와 금속 등 고강성 재료로 제작돼 부드러운 뇌 조직과의 기계 특성적 간극이 있다. 이러한 특성으로 인해 염증반응을 악화시켜 장기간 이식용으로 적합하지 않다.
무엇보다 일반적으로 연구실에서 쓰이고 있는 광섬유, 약물주입관 등은 뇌 이식 후 외부기기에 선이 연결된 형태로 사용해야 해 자유로운 행동을 크게 제약하게 된다.
연구팀은 중합체(polymer) 미세유체관과 마이크로 LED를 결합해 머리카락 두께의 유연한 탐침을 만들고, 이를 소형 블루투스 기반 제어 회로와 교체 가능한 약물 카트리지와 결합했다. 이를 통해 스마트폰 앱을 통해 무선으로 마이크로 LED와 약물 전달을 제어할 수 있는 무게 2g의 뇌 이식용 기기를 구현했다.
특히 약물 카트리지는 레고의 원리를 모사해 탐침 부분과 쉽게 조립 및 분리할 수 있도록 제작해, 필요할 때마다 새로운 약물 카트리지를 결합함으로써 원하는 약물을 장기간에 걸쳐 뇌의 특정 부위에 반복 전달할 수 있도록 만들었다.
연구팀은 이 기기를 쥐의 뇌 보상회로에 이식한 후 도파민 활성 약물과 억제 약물이 든 카트리지를 기기와 결합했다. 그 후 간단한 스마트폰 앱 제어와 도파민 활성 약물을 이용해 원하는 타이밍에 자유롭게 움직이는 쥐의 행동을 증가, 억제하는 데 성공했다.
또한, 연구팀은 쥐의 뇌에서 장소 선호도를 유도할 수 있는 부위에 빛에 반응하는 단백질을 주입해 신경세포가 빛에 반응하도록 처리했다.
그 후 쥐가 특정 장소로 이동했을 때 마이크로 LED를 켜 빛 자극을 통해 쥐가 그 장소에 계속 머물고 싶게 만들었다. 반대로 약물 전달을 통해 뇌 신경회로를 제어함으로써 쥐의 특정 장소 선호도를 없애는 데도 성공했다.
정 교수는 “빛과 약물을 이용한 신경회로 제어는 기존의 전기자극 방법보다 훨씬 더 정교해 부작용 없는 뇌 제어가 가능하다”라며 “개발된 기기는 간단한 스마트폰 조작으로 뇌의 특정 회로를 빛과 약물을 이용해 반복적, 장기적으로 무선 제어가 가능해 뇌 기능을 밝혀내기 위한 연구나 향후 뇌 질환의 치료에도 유용하게 적용할 수 있을 것이다”라고 말했다.
연구팀은 이 기술을 인체에 적용하기 위해 두개골 내에 완전히 이식할 수 있고 반영구적 사용이 가능한 형태로 디자인을 발전시키는 확장 연구를 계획하고 있다.
이번 연구는 한국연구재단 신진연구자지원사업(완전 이식 가능한 무선 유연성 광유체 뉴럴 임플랜트 개발 및 뇌 연구를 위한 광유전학/광약물학에의 적용) 및 기초연구실 지원사업(유전자 및 신경회로 조절 기반 중독 행동 제어 기초연구실)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 디바이스가 이식된 쥐의 사진
그림2. 스마트폰앱을 이용한 마이크로 LED 컨트롤
그림3. 개발된 뇌 이식용 무선 디바이스
2019.08.08 조회수 21112
정재웅 교수, 스마트폰으로 뇌 신경회로 무선 제어 기술 개발
〈 김충연, 변상혁 박사과정, 정재웅 교수〉
우리 대학 전기및전자공학부 정재웅 교수와 미국 워싱턴대(University of Washington) 마이클 브루카스(Michael Bruchas) 교수 공동 연구팀이 스마트폰 앱 조작을 통해 약물과 빛을 뇌 특정 부위에 전달함으로써 신경회로를 정교하게 조절할 수 있는 뇌 이식용 무선 기기를 개발했다.
이번 기술 개발을 통해 장기간의 동물 실험이 필요한 신약 개발뿐 아니라 치매, 파킨슨병 등 뇌 질환 치료에도 적용할 수 있을 것으로 기대된다.
라자 콰지(Raza Qazi, 1저자), 김충연, 변상혁 연구원이 개발하고 워싱턴대 신경과학 연구원들이 공동으로 참여한 이번 연구는 의공학 분야 국제 학술지 ‘네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)’ 8월 6일 자에 게재됐다. (논문명 : Wireless optofluidic brain probes for chronic neuropharmacology and photostimulation).
광유전학과 신경약물학은 주변 신경회로에 영향을 주지 않고 목표로 하는 뉴런이나 신경회로만을 빛 또는 약물, 혹은 그 둘의 조합을 이용해 정교하게 제어할 수 있다. 기존의 전기자극을 활용한 방법에 비해 훨씬 더 높은 시공간적 해상도를 가져 최근 뇌 연구 및 뇌 질병 치료 목적으로 주목받고 있다.
하지만 현재 뇌 연구에 일반적으로 쓰는 기기는 상대적으로 크기가 커 뇌 조직 손상, 정교한 선택적 신경회로 제어 불가, 하나의 다기능성 프로브(probe) 형태로 구현이 어렵다. 또한, 기존 기기는 실리카(silica)와 금속 등 고강성 재료로 제작돼 부드러운 뇌 조직과의 기계 특성적 간극이 있다. 이러한 특성으로 인해 염증반응을 악화시켜 장기간 이식용으로 적합하지 않다.
무엇보다 일반적으로 연구실에서 쓰이고 있는 광섬유, 약물주입관 등은 뇌 이식 후 외부기기에 선이 연결된 형태로 사용해야 해 자유로운 행동을 크게 제약하게 된다.
연구팀은 중합체(polymer) 미세유체관과 마이크로 LED를 결합해 머리카락 두께의 유연한 탐침을 만들고, 이를 소형 블루투스 기반 제어 회로와 교체 가능한 약물 카트리지와 결합했다. 이를 통해 스마트폰 앱을 통해 무선으로 마이크로 LED와 약물 전달을 제어할 수 있는 무게 2g의 뇌 이식용 기기를 구현했다.
특히 약물 카트리지는 레고의 원리를 모사해 탐침 부분과 쉽게 조립 및 분리할 수 있도록 제작해, 필요할 때마다 새로운 약물 카트리지를 결합함으로써 원하는 약물을 장기간에 걸쳐 뇌의 특정 부위에 반복 전달할 수 있도록 만들었다.
연구팀은 이 기기를 쥐의 뇌 보상회로에 이식한 후 도파민 활성 약물과 억제 약물이 든 카트리지를 기기와 결합했다. 그 후 간단한 스마트폰 앱 제어와 도파민 활성 약물을 이용해 원하는 타이밍에 자유롭게 움직이는 쥐의 행동을 증가, 억제하는 데 성공했다.
또한, 연구팀은 쥐의 뇌에서 장소 선호도를 유도할 수 있는 부위에 빛에 반응하는 단백질을 주입해 신경세포가 빛에 반응하도록 처리했다.
그 후 쥐가 특정 장소로 이동했을 때 마이크로 LED를 켜 빛 자극을 통해 쥐가 그 장소에 계속 머물고 싶게 만들었다. 반대로 약물 전달을 통해 뇌 신경회로를 제어함으로써 쥐의 특정 장소 선호도를 없애는 데도 성공했다.
정 교수는 “빛과 약물을 이용한 신경회로 제어는 기존의 전기자극 방법보다 훨씬 더 정교해 부작용 없는 뇌 제어가 가능하다”라며 “개발된 기기는 간단한 스마트폰 조작으로 뇌의 특정 회로를 빛과 약물을 이용해 반복적, 장기적으로 무선 제어가 가능해 뇌 기능을 밝혀내기 위한 연구나 향후 뇌 질환의 치료에도 유용하게 적용할 수 있을 것이다”라고 말했다.
연구팀은 이 기술을 인체에 적용하기 위해 두개골 내에 완전히 이식할 수 있고 반영구적 사용이 가능한 형태로 디자인을 발전시키는 확장 연구를 계획하고 있다.
이번 연구는 한국연구재단 신진연구자지원사업(완전 이식 가능한 무선 유연성 광유체 뉴럴 임플랜트 개발 및 뇌 연구를 위한 광유전학/광약물학에의 적용) 및 기초연구실 지원사업(유전자 및 신경회로 조절 기반 중독 행동 제어 기초연구실)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 디바이스가 이식된 쥐의 사진
그림2. 스마트폰앱을 이용한 마이크로 LED 컨트롤
그림3. 개발된 뇌 이식용 무선 디바이스
2019.08.08 조회수 21112 -
 이상엽 특훈교수, 김현욱 교수, 인공지능 이용한 효소기능 예측 기술 개발
우리 대학 생명화학공학과 이상엽 특훈교수와 김현욱 교수의 초세대 협업연구실 공동연구팀이 딥러닝(deep learning) 기술을 이용해 효소의 기능을 신속하고 정확하게 예측할 수 있는 컴퓨터 방법론 DeepEC를 개발했다.
공동연구팀의 류재용 박사가 1 저자로 참여한 이번 연구결과는 국제학술지 ‘미국 국립과학원 회보(PNAS)’ 6월 20일 자 온라인판에 게재됐다. (논문명 : Deep learning enables high-quality and high-throughput prediction of enzyme commission numbers)
효소는 세포 내의 생화학반응들을 촉진하는 단백질 촉매로 이들의 기능을 정확히 이해하는 것은 세포의 대사(metabolism) 과정을 이해하는 데에 매우 중요하다.
특히 효소들은 다양한 질병 발생 원리 및 산업 생명공학과 밀접한 연관이 있어 방대한 게놈 정보에서 효소들의 기능을 빠르고 정확하게 예측하는 기술은 응용기술 측면에서도 중요하다.
효소의 기능을 표기하는 시스템 중 대표적인 것이 EC 번호(enzyme commission number)이다. EC 번호는 ‘EC 3.4.11.4’처럼 효소가 매개하는 생화학반응들의 종류에 따라 총 4개의 숫자로 구성돼 있다.
중요한 것은 특정 효소에 주어진 EC 번호를 통해서 해당 효소가 어떠한 종류의 생화학반응을 매개하는지 알 수 있다는 것이다. 따라서 게놈으로부터 얻을 수 있는 효소 단백질 서열의 EC 번호를 빠르고 정확하게 예측할 수 있는 기술은 효소 및 대사 관련 문제를 해결하는 데 중요한 역할을 한다.
작년까지 여러 해에 걸쳐 EC 번호를 예측해주는 컴퓨터 방법론들이 최소 10개 이상 개발됐다. 그러나 이들 모두 예측 속도, 예측 정확성 및 예측 가능 범위 측면에서 발전 필요성이 있었다. 특히 현대 생명과학 및 생명공학에서 이뤄지는 연구의 속도와 규모를 고려했을 때 이러한 방법론의 성능은 충분하지 않았다.
공동연구팀은 1,388,606개의 단백질 서열과 이들에게 신뢰성 있게 부여된 EC 번호를 담고 있는 바이오 빅데이터에 딥러닝 기술을 적용해 EC 번호를 빠르고 정확하게 예측할 수 있는 DeepEC를 개발했다.
DeepEC는 주어진 단백질 서열의 EC 번호를 예측하기 위해서 3개의 합성곱 신경망(Convolutional neural network)을 주요 예측기술로 사용하며, 합성곱 신경망으로 EC 번호를 예측하지 못했을 경우 서열정렬(sequence alignment)을 통해서 EC 번호를 예측한다.
연구팀은 더 나아가 단백질 서열의 도메인(domain)과 기질 결합 부위 잔기(binding site residue)에 변이를 인위적으로 주었을 때, DeepEC가 가장 민감하게 해당 변이의 영향을 감지하는 것을 확인했다.
김현욱 교수는 “DeepEC의 성능을 평가하기 위해서 이전에 발표된 5개의 대표적인 EC 번호 예측 방법론과 비교해보니 DeepEC가 가장 빠르고 정확하게 주어진 단백질의 EC 번호를 예측하는 것으로 나타났다”라며 “효소 기능 연구에 크게 이바지할 것으로 기대한다”라고 말했다.
이상엽 특훈교수는 “이번에 개발한 DeepEC를 통해서 지속해서 재생되는 게놈 및 메타 게놈에 존재하는 방대한 효소 단백질 서열의 기능을 보다 효율적이고 정확하게 알아내는 것이 가능해졌다”라고 말했다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제 및 바이오·의료기술 개발 Korea Bio Grand Challenge 사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 인공지능 기반의 DeepEC를 이용한 효소 기능 EC 번호 예측
2019.07.03 조회수 19165
이상엽 특훈교수, 김현욱 교수, 인공지능 이용한 효소기능 예측 기술 개발
우리 대학 생명화학공학과 이상엽 특훈교수와 김현욱 교수의 초세대 협업연구실 공동연구팀이 딥러닝(deep learning) 기술을 이용해 효소의 기능을 신속하고 정확하게 예측할 수 있는 컴퓨터 방법론 DeepEC를 개발했다.
공동연구팀의 류재용 박사가 1 저자로 참여한 이번 연구결과는 국제학술지 ‘미국 국립과학원 회보(PNAS)’ 6월 20일 자 온라인판에 게재됐다. (논문명 : Deep learning enables high-quality and high-throughput prediction of enzyme commission numbers)
효소는 세포 내의 생화학반응들을 촉진하는 단백질 촉매로 이들의 기능을 정확히 이해하는 것은 세포의 대사(metabolism) 과정을 이해하는 데에 매우 중요하다.
특히 효소들은 다양한 질병 발생 원리 및 산업 생명공학과 밀접한 연관이 있어 방대한 게놈 정보에서 효소들의 기능을 빠르고 정확하게 예측하는 기술은 응용기술 측면에서도 중요하다.
효소의 기능을 표기하는 시스템 중 대표적인 것이 EC 번호(enzyme commission number)이다. EC 번호는 ‘EC 3.4.11.4’처럼 효소가 매개하는 생화학반응들의 종류에 따라 총 4개의 숫자로 구성돼 있다.
중요한 것은 특정 효소에 주어진 EC 번호를 통해서 해당 효소가 어떠한 종류의 생화학반응을 매개하는지 알 수 있다는 것이다. 따라서 게놈으로부터 얻을 수 있는 효소 단백질 서열의 EC 번호를 빠르고 정확하게 예측할 수 있는 기술은 효소 및 대사 관련 문제를 해결하는 데 중요한 역할을 한다.
작년까지 여러 해에 걸쳐 EC 번호를 예측해주는 컴퓨터 방법론들이 최소 10개 이상 개발됐다. 그러나 이들 모두 예측 속도, 예측 정확성 및 예측 가능 범위 측면에서 발전 필요성이 있었다. 특히 현대 생명과학 및 생명공학에서 이뤄지는 연구의 속도와 규모를 고려했을 때 이러한 방법론의 성능은 충분하지 않았다.
공동연구팀은 1,388,606개의 단백질 서열과 이들에게 신뢰성 있게 부여된 EC 번호를 담고 있는 바이오 빅데이터에 딥러닝 기술을 적용해 EC 번호를 빠르고 정확하게 예측할 수 있는 DeepEC를 개발했다.
DeepEC는 주어진 단백질 서열의 EC 번호를 예측하기 위해서 3개의 합성곱 신경망(Convolutional neural network)을 주요 예측기술로 사용하며, 합성곱 신경망으로 EC 번호를 예측하지 못했을 경우 서열정렬(sequence alignment)을 통해서 EC 번호를 예측한다.
연구팀은 더 나아가 단백질 서열의 도메인(domain)과 기질 결합 부위 잔기(binding site residue)에 변이를 인위적으로 주었을 때, DeepEC가 가장 민감하게 해당 변이의 영향을 감지하는 것을 확인했다.
김현욱 교수는 “DeepEC의 성능을 평가하기 위해서 이전에 발표된 5개의 대표적인 EC 번호 예측 방법론과 비교해보니 DeepEC가 가장 빠르고 정확하게 주어진 단백질의 EC 번호를 예측하는 것으로 나타났다”라며 “효소 기능 연구에 크게 이바지할 것으로 기대한다”라고 말했다.
이상엽 특훈교수는 “이번에 개발한 DeepEC를 통해서 지속해서 재생되는 게놈 및 메타 게놈에 존재하는 방대한 효소 단백질 서열의 기능을 보다 효율적이고 정확하게 알아내는 것이 가능해졌다”라고 말했다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제 및 바이오·의료기술 개발 Korea Bio Grand Challenge 사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 인공지능 기반의 DeepEC를 이용한 효소 기능 EC 번호 예측
2019.07.03 조회수 19165 -
 김용대 교수, 대테러 방지용 안티 드론 기술 개발
〈 (오른쪽 위부터 시계방향으로) 김용대 교수, 권유진, 노주환, 신호철, 김도현 박사과정 〉
우리 대학 전기및전자공학부 김용대 교수 연구팀이 위조 GPS 신호를 이용해 드론의 위치를 속이는 방식으로 드론을 납치할 수 있는 안티 드론 기술을 개발했다.
이 기술은 긴급 상황에서 급격한 방향 변화 없이도 드론이 원하는 방향으로 안전하게 움직이도록 유도할 수 있어 테러 등의 목적을 가진 위험한 드론에 효과적으로 대응할 수 있다.
이번 연구성과는 ‘ACM 트랜잭션 온 프라이버시 & 시큐리티(ACM Transactions on Privacy and Security, TOPS)’ 저널 4월 9일 자에 게재됐다. (논문명 : Tractor Beam: Safe-hijacking of Consumer Drones with Adaptive GPS Spoofing)
드론 산업이 발전하며 수색, 구조, 방재 및 재해 대응, 택배와 정찰 등 다양한 영역에서 드론이 활용되면서 한편으로는 사유지와 주요시설 무단 침입, 안전과 보안 위협, 사생활 침해 등의 우려 또한 커지고 있다.
이에 따라 드론 침투를 탐지하고 대응하는 안티 드론 산업 급성장하고 있다. 현재 공항 등 주요시설에 구축되고 있는 안티 드론 시스템들은 방해 전파나 고출력 레이저를 쏘거나 그물로 포획해 드론을 무력화시키는 방식이다.
그러나 테러를 목적으로 폭발물이나 무기를 장착한 드론은 사람들과 주요시설로부터 즉시 안전거리를 확보한 뒤 무력화해야 피해가 최소화될 수 있다. 예를 들어 공항에서 무단 침입한 드론을 단순 방해 전파로 대응하면 드론을 못 움직이게 할 수는 있지만 한 자리에 계속 떠 있게 돼 비행기의 이착륙이 긴 시간 중단될 수 있다.
이렇듯 위험한 드론을 발견하는 즉시 안전하게 원하는 방향으로 격리할 수 있는 새로운 안티 드론 기술의 필요성이 커지고 있다.
김 교수 연구팀은 위조 GPS 신호를 이용해 드론의 위치를 속이는 방식으로 드론을 납치할 수 있는 안티 드론 기술을 개발했다.
위조 GPS 신호를 통해 드론이 자신의 위치를 착각하게 만들어서 정해진 위치나 경로로부터 드론을 이탈시키는 공격 기법은 기존 연구를 통해 알려진 바 있다. 그러나 이러한 공격 기법은 GPS 안전모드가 활성화되면 적용할 수 없다는 문제가 있다.
GPS 안전모드는 드론이 위조 GPS 신호로 인해 신호가 끊기거나 위치 정확도가 낮아지면 드론의 안전을 보장하기 위해 발동되는 일종의 비상 모드로 모델이나 제조사에 따라 제각각이기 때문이다.
연구팀은 디제이아이(DJI), 패롯(Parrot) 등 주요 드론 제조업체의 드론 GPS 안전모드를 분석하고 이를 기준으로 드론의 분류 체계를 만들어 각 드론 유형에 따른 드론 납치 기법을 설계했다.
이 분류 체계는 거의 모든 형태의 드론 GPS 안전모드를 다루고 있어 모델, 제조사와 관계없이 GPS를 사용하고 있는 드론이라면 보편적으로 적용할 수 있다. 연구팀은 실제 총 4종의 드론에 개발한 기법을 적용했고, 그 결과 작은 오차범위 안에서 의도한 납치 방향으로 드론을 안전하게 유도할 수 있음을 입증했다.
김 교수는 “기존 컨슈머 드론들은 GPS 안전모드를 갖추고 있어 위조 GPS 공격으로부터 안전한 것처럼 보이나 초보적인 방법으로 GPS 오류를 감지하고 있어 대부분 우회가 가능하다”라며 “특히 드론 불법 비행으로 발생하는 항공업계와 공항의 피해를 줄이는데 기여할 수 있을 것이다”라고 말했다.
연구팀은 기술이전을 통해 기존 안티 드론 솔루션에 연구팀이 개발한 기술을 적용하는 방식으로 상용화에 나설 계획이다.
이번 연구는 방위사업청의 광운대학교 초소형무인기 전술신호처리 특화연구실과 국방과학연구소의 지원을 통해 수행됐다.
□ 그림 설명
그림1. PC로 부터 위조 GPS 전파를 생성하여 지향성 안테나를 이용해 드론에 신호를 주입하는 실험환경
2019.06.05 조회수 14795
김용대 교수, 대테러 방지용 안티 드론 기술 개발
〈 (오른쪽 위부터 시계방향으로) 김용대 교수, 권유진, 노주환, 신호철, 김도현 박사과정 〉
우리 대학 전기및전자공학부 김용대 교수 연구팀이 위조 GPS 신호를 이용해 드론의 위치를 속이는 방식으로 드론을 납치할 수 있는 안티 드론 기술을 개발했다.
이 기술은 긴급 상황에서 급격한 방향 변화 없이도 드론이 원하는 방향으로 안전하게 움직이도록 유도할 수 있어 테러 등의 목적을 가진 위험한 드론에 효과적으로 대응할 수 있다.
이번 연구성과는 ‘ACM 트랜잭션 온 프라이버시 & 시큐리티(ACM Transactions on Privacy and Security, TOPS)’ 저널 4월 9일 자에 게재됐다. (논문명 : Tractor Beam: Safe-hijacking of Consumer Drones with Adaptive GPS Spoofing)
드론 산업이 발전하며 수색, 구조, 방재 및 재해 대응, 택배와 정찰 등 다양한 영역에서 드론이 활용되면서 한편으로는 사유지와 주요시설 무단 침입, 안전과 보안 위협, 사생활 침해 등의 우려 또한 커지고 있다.
이에 따라 드론 침투를 탐지하고 대응하는 안티 드론 산업 급성장하고 있다. 현재 공항 등 주요시설에 구축되고 있는 안티 드론 시스템들은 방해 전파나 고출력 레이저를 쏘거나 그물로 포획해 드론을 무력화시키는 방식이다.
그러나 테러를 목적으로 폭발물이나 무기를 장착한 드론은 사람들과 주요시설로부터 즉시 안전거리를 확보한 뒤 무력화해야 피해가 최소화될 수 있다. 예를 들어 공항에서 무단 침입한 드론을 단순 방해 전파로 대응하면 드론을 못 움직이게 할 수는 있지만 한 자리에 계속 떠 있게 돼 비행기의 이착륙이 긴 시간 중단될 수 있다.
이렇듯 위험한 드론을 발견하는 즉시 안전하게 원하는 방향으로 격리할 수 있는 새로운 안티 드론 기술의 필요성이 커지고 있다.
김 교수 연구팀은 위조 GPS 신호를 이용해 드론의 위치를 속이는 방식으로 드론을 납치할 수 있는 안티 드론 기술을 개발했다.
위조 GPS 신호를 통해 드론이 자신의 위치를 착각하게 만들어서 정해진 위치나 경로로부터 드론을 이탈시키는 공격 기법은 기존 연구를 통해 알려진 바 있다. 그러나 이러한 공격 기법은 GPS 안전모드가 활성화되면 적용할 수 없다는 문제가 있다.
GPS 안전모드는 드론이 위조 GPS 신호로 인해 신호가 끊기거나 위치 정확도가 낮아지면 드론의 안전을 보장하기 위해 발동되는 일종의 비상 모드로 모델이나 제조사에 따라 제각각이기 때문이다.
연구팀은 디제이아이(DJI), 패롯(Parrot) 등 주요 드론 제조업체의 드론 GPS 안전모드를 분석하고 이를 기준으로 드론의 분류 체계를 만들어 각 드론 유형에 따른 드론 납치 기법을 설계했다.
이 분류 체계는 거의 모든 형태의 드론 GPS 안전모드를 다루고 있어 모델, 제조사와 관계없이 GPS를 사용하고 있는 드론이라면 보편적으로 적용할 수 있다. 연구팀은 실제 총 4종의 드론에 개발한 기법을 적용했고, 그 결과 작은 오차범위 안에서 의도한 납치 방향으로 드론을 안전하게 유도할 수 있음을 입증했다.
김 교수는 “기존 컨슈머 드론들은 GPS 안전모드를 갖추고 있어 위조 GPS 공격으로부터 안전한 것처럼 보이나 초보적인 방법으로 GPS 오류를 감지하고 있어 대부분 우회가 가능하다”라며 “특히 드론 불법 비행으로 발생하는 항공업계와 공항의 피해를 줄이는데 기여할 수 있을 것이다”라고 말했다.
연구팀은 기술이전을 통해 기존 안티 드론 솔루션에 연구팀이 개발한 기술을 적용하는 방식으로 상용화에 나설 계획이다.
이번 연구는 방위사업청의 광운대학교 초소형무인기 전술신호처리 특화연구실과 국방과학연구소의 지원을 통해 수행됐다.
□ 그림 설명
그림1. PC로 부터 위조 GPS 전파를 생성하여 지향성 안테나를 이용해 드론에 신호를 주입하는 실험환경
2019.06.05 조회수 14795 -
 김용훈 교수, 페로브스카이트 나노선 기반 소자 구현방안 제시
〈 이주호 박사과정, 무하메드 칸 박사후 연구원, 김용훈 교수 〉
우리 대학 전기및전자공학부 김용훈 교수 연구팀이 저차원 페로브스카이트 나노소재의 새 물성을 밝히고 이를 이용한 새로운 비선형 소자 구현 방법을 제시했다.
연구팀은 최근 태양전지, 발광다이오드(LED) 등 광소자 응용의 핵심 요소로 주목받는 페로브스카이트 나노소재가 차세대 전자 소자 구현에도 유망함을 증명했다. 또한 초절전, 다진법 전자 소자 구현에 필요한 부성 미분 저항 소자를 구현하는 새로운 이론적 청사진을 제시했다.
무하메드 칸(Muhammad Ejaz Khan) 박사후연구원과 이주호 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘어드밴스드 펑셔널 머티리얼즈(Advanced Functional Materials)’ 1월 7일자 온라인판에 게재됐고, 표지논문으로 선정돼 출간될 예정이다.(논문명 : Semimetallicity and negative differential resistance from hybrid halide perovskite nanowires, 하이브리드 할로겐화 페로브스카이트 나노선에서의 준금속성과 부성미분저항 발현)
유무기 하이브리드 할로겐화 페로브스카이트 물질은 우수한 광학적 성능뿐만 아니라 저비용의 간편한 공정으로 제작할 수 있어 최근 태양전지 및 LED 등 다양한 광소자 응용 분야에서 주목받고 있다. 그러나 할로겐화 페로브스카이트의 전자 소자 응용에 관한 연구는 세계적으로도 아직 부족한 상황이다.
김 교수 연구팀은 최근 새롭게 제조 기술이 개발되고 양자효과가 극대화되는 특성을 가진 저차원 유무기 할로겐화 페로브스카이트 물질에 주목했다.
연구팀은 슈퍼컴퓨터를 활용해 우선 1차원 페로브스카이트 나노선의 유기물을 벗겨내면 기존에 보고되지 않은 준 금속성 특성을 발현할 수 있다는 것을 발견했다.
이 1차원 무기 틀을 전극으로 활용해 단일 페로브스카이트 나노선 기반의 터널링 접합 소자를 제작하면 매우 우수한 비선형 부성미분저항(negative differential resistance, NDR) 소자를 구현할 수 있음을 확인했다.
부성미분저항은 일반적인 특성과는 반대로 특정 구간에서 전압이 증가할 때 전류는 오히려 감소해 전류-전압 특성 곡성이 마치 알파벳 ‘N’모양처럼 비선형적으로 나타나는 현상을 말한다. 차세대 소자 개발의 원천기술 이 되는 매우 중요한 특성이다.
연구팀은 나아가 이 부성미분저항 특성은 기존에 보고된 바 없는 양자 역학적 혼성화(quantum-mechanical hybridization)에 기반을 둔 새로운 부성미분저항 원리에 기반함을 밝혀냈다.
연구팀은 저차원 할로겐화 페로브스카이트의 새로운 구조적, 전기적 특성을 규명했을 뿐 아니라 페로브스카이트 기반의 터널링 소자를 이용하면 획기적으로 향상된 부성미분저항 소자 특성을 유도할 수 있음을 증명했다.
김 교수는 “양자역학에 기반한 전산모사가 첨단 나노소재 및 나노소자의 개발을 선도할 수 있음을 보여준 연구이다”라며 “특히 1973년 일본의 에사키(Esaki) 박사의 노벨상 수상 주제였던 양자역학적 터널링 소자 개발의 새로운 방향을 제시한 연구이다”라고 말했다.
이번 연구는 미래창조과학부 중견연구자지원사업, 나노소재원천기술개발사업, 기초연구실지원사업, 글로벌프론티어사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 어드밴스드 펑셔널 머티리얼즈 표지
그림2. 연구개요
2019.02.21 조회수 18676
김용훈 교수, 페로브스카이트 나노선 기반 소자 구현방안 제시
〈 이주호 박사과정, 무하메드 칸 박사후 연구원, 김용훈 교수 〉
우리 대학 전기및전자공학부 김용훈 교수 연구팀이 저차원 페로브스카이트 나노소재의 새 물성을 밝히고 이를 이용한 새로운 비선형 소자 구현 방법을 제시했다.
연구팀은 최근 태양전지, 발광다이오드(LED) 등 광소자 응용의 핵심 요소로 주목받는 페로브스카이트 나노소재가 차세대 전자 소자 구현에도 유망함을 증명했다. 또한 초절전, 다진법 전자 소자 구현에 필요한 부성 미분 저항 소자를 구현하는 새로운 이론적 청사진을 제시했다.
무하메드 칸(Muhammad Ejaz Khan) 박사후연구원과 이주호 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘어드밴스드 펑셔널 머티리얼즈(Advanced Functional Materials)’ 1월 7일자 온라인판에 게재됐고, 표지논문으로 선정돼 출간될 예정이다.(논문명 : Semimetallicity and negative differential resistance from hybrid halide perovskite nanowires, 하이브리드 할로겐화 페로브스카이트 나노선에서의 준금속성과 부성미분저항 발현)
유무기 하이브리드 할로겐화 페로브스카이트 물질은 우수한 광학적 성능뿐만 아니라 저비용의 간편한 공정으로 제작할 수 있어 최근 태양전지 및 LED 등 다양한 광소자 응용 분야에서 주목받고 있다. 그러나 할로겐화 페로브스카이트의 전자 소자 응용에 관한 연구는 세계적으로도 아직 부족한 상황이다.
김 교수 연구팀은 최근 새롭게 제조 기술이 개발되고 양자효과가 극대화되는 특성을 가진 저차원 유무기 할로겐화 페로브스카이트 물질에 주목했다.
연구팀은 슈퍼컴퓨터를 활용해 우선 1차원 페로브스카이트 나노선의 유기물을 벗겨내면 기존에 보고되지 않은 준 금속성 특성을 발현할 수 있다는 것을 발견했다.
이 1차원 무기 틀을 전극으로 활용해 단일 페로브스카이트 나노선 기반의 터널링 접합 소자를 제작하면 매우 우수한 비선형 부성미분저항(negative differential resistance, NDR) 소자를 구현할 수 있음을 확인했다.
부성미분저항은 일반적인 특성과는 반대로 특정 구간에서 전압이 증가할 때 전류는 오히려 감소해 전류-전압 특성 곡성이 마치 알파벳 ‘N’모양처럼 비선형적으로 나타나는 현상을 말한다. 차세대 소자 개발의 원천기술 이 되는 매우 중요한 특성이다.
연구팀은 나아가 이 부성미분저항 특성은 기존에 보고된 바 없는 양자 역학적 혼성화(quantum-mechanical hybridization)에 기반을 둔 새로운 부성미분저항 원리에 기반함을 밝혀냈다.
연구팀은 저차원 할로겐화 페로브스카이트의 새로운 구조적, 전기적 특성을 규명했을 뿐 아니라 페로브스카이트 기반의 터널링 소자를 이용하면 획기적으로 향상된 부성미분저항 소자 특성을 유도할 수 있음을 증명했다.
김 교수는 “양자역학에 기반한 전산모사가 첨단 나노소재 및 나노소자의 개발을 선도할 수 있음을 보여준 연구이다”라며 “특히 1973년 일본의 에사키(Esaki) 박사의 노벨상 수상 주제였던 양자역학적 터널링 소자 개발의 새로운 방향을 제시한 연구이다”라고 말했다.
이번 연구는 미래창조과학부 중견연구자지원사업, 나노소재원천기술개발사업, 기초연구실지원사업, 글로벌프론티어사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 어드밴스드 펑셔널 머티리얼즈 표지
그림2. 연구개요
2019.02.21 조회수 18676 -
 김학성 교수, 세포 내 단백질 전달 효율 높이는 DNA 기반 나노구조체 개발
우리 대학 생명과학과 김학성 교수, 류이슬 박사 연구팀이 강원대 이중재 교수, 한국원자력연구원 강정애 박사와의 공동 연구를 통해 DNA를 기반으로 나노 구조체를 개발해 세포 속으로의 단백질 전달 효율을 높이는 기술을 개발했다.
이번 연구 결과는 국제 학술지 ‘스몰(Small)’에 2018년 12월 28일일자 표지논문으로 게재됐다.
단백질 치료제는 저분자 화합물에 비해 반응 부위를 구별해내는 특이성이 우수해 차세대 의약품으로 활발히 개발되고 있다. 단백질 치료제가 탁월한 효과를 내기 위해서는 치료용 단백질이 세포 내로 효율적으로 전달되는 기술이 선행돼야 한다.
지금까지는 화학적 합성법 등으로 단백질 전달체를 제작해 왔지만 생체 독성, 낮은 전달 효율, 복잡한 제조공정과 효과가 일관적이지 않은 재현성 등이 해결돼야 할 과제로 남아있다.
연구팀은 생체 분자인 DNA를 기반으로 나노 구조체를 제작해 생체 친화적이면서 특정 세포로의 높은 전달 효율을 보였다. 특히 다양한 단백질을 전달할 수 있는 범용적인 기술로서 폐암 동물 모델에서도 항암 물질을 전달해 높은 항암 효과를 입증했다.
제조공정도 복잡하지 않다. 먼저 금 나노입자 표면에 DNA를 부착한다. 다음으로 징크 핑거를 이용해 각 DNA 가닥에 암세포를 표적하는 생체 분자와 항암 단백질을 결합해 제작했다.
DNA와 징크 핑거 간의 상호작용을 이용하므로 DNA 서열과 길이를 조절해 나노 구조체에 탑재되는 단백질의 양을 손쉽게 조절할 수 있다.
김학성 교수는 “생체 적합한 소재인 DNA와 단백질의 상호작용을 이용해 세포 내로 단백질을 효율적으로 전달하는 새로운 나노 구조체를 개발한 것이다”라며, “세포 내 단백질 치료제의 전달뿐 아니라 동반 진단용으로 광범위하게 활용될 것으로 기대된다”라고 말했다.
이번 연구 성과는 과학기술정보통신부‧한국연구재단 기초연구사업(글로벌연구실, 중견연구, 생애첫연구) 지원으로 수행됐다.
□ 그림 설명
그림1. small 표지
그림2. 나노 구조체 제조 과정 모식도
그림3. 나노 구조체의 세포 내 단백질 전달 효과
그림4. 나노 구조체의 현미경 관찰 사진
2019.01.21 조회수 11839
김학성 교수, 세포 내 단백질 전달 효율 높이는 DNA 기반 나노구조체 개발
우리 대학 생명과학과 김학성 교수, 류이슬 박사 연구팀이 강원대 이중재 교수, 한국원자력연구원 강정애 박사와의 공동 연구를 통해 DNA를 기반으로 나노 구조체를 개발해 세포 속으로의 단백질 전달 효율을 높이는 기술을 개발했다.
이번 연구 결과는 국제 학술지 ‘스몰(Small)’에 2018년 12월 28일일자 표지논문으로 게재됐다.
단백질 치료제는 저분자 화합물에 비해 반응 부위를 구별해내는 특이성이 우수해 차세대 의약품으로 활발히 개발되고 있다. 단백질 치료제가 탁월한 효과를 내기 위해서는 치료용 단백질이 세포 내로 효율적으로 전달되는 기술이 선행돼야 한다.
지금까지는 화학적 합성법 등으로 단백질 전달체를 제작해 왔지만 생체 독성, 낮은 전달 효율, 복잡한 제조공정과 효과가 일관적이지 않은 재현성 등이 해결돼야 할 과제로 남아있다.
연구팀은 생체 분자인 DNA를 기반으로 나노 구조체를 제작해 생체 친화적이면서 특정 세포로의 높은 전달 효율을 보였다. 특히 다양한 단백질을 전달할 수 있는 범용적인 기술로서 폐암 동물 모델에서도 항암 물질을 전달해 높은 항암 효과를 입증했다.
제조공정도 복잡하지 않다. 먼저 금 나노입자 표면에 DNA를 부착한다. 다음으로 징크 핑거를 이용해 각 DNA 가닥에 암세포를 표적하는 생체 분자와 항암 단백질을 결합해 제작했다.
DNA와 징크 핑거 간의 상호작용을 이용하므로 DNA 서열과 길이를 조절해 나노 구조체에 탑재되는 단백질의 양을 손쉽게 조절할 수 있다.
김학성 교수는 “생체 적합한 소재인 DNA와 단백질의 상호작용을 이용해 세포 내로 단백질을 효율적으로 전달하는 새로운 나노 구조체를 개발한 것이다”라며, “세포 내 단백질 치료제의 전달뿐 아니라 동반 진단용으로 광범위하게 활용될 것으로 기대된다”라고 말했다.
이번 연구 성과는 과학기술정보통신부‧한국연구재단 기초연구사업(글로벌연구실, 중견연구, 생애첫연구) 지원으로 수행됐다.
□ 그림 설명
그림1. small 표지
그림2. 나노 구조체 제조 과정 모식도
그림3. 나노 구조체의 세포 내 단백질 전달 효과
그림4. 나노 구조체의 현미경 관찰 사진
2019.01.21 조회수 11839 -
 김신현 교수, 달걀 속 살충제 성분, 현장 즉시 검출 기술 개발
〈 김신현 교수, 김동재 박사과정 〉
우리 대학 생명화학공학과 김신현 교수 연구팀과 재료연구소(소장 이정환) 김동호 박사 공동 연구팀이 생체 시료에 들어있는 미량의 분자를 직접 검출할 수 있는 센서를 개발했다.
연구팀은 개발한 센서를 통해 다양한 종류의 살충제 성분을 검출하는데 성공했다. 특히 국내 및 유럽에서 문제가 됐던 달걀 속 살충제 성분인 피프로닐 술폰(Fipronil sulfone)을 시료 전처리 없이 검출할 수 있음을 증명했다.
연구팀의 센서는 전하를 띠는 하이드로젤 미세입자 내부에 금 나노입자 응집체를 캡슐화한 형태로 생체 시료 내에 존재하는 분자를 직접 분석해야 하는 광범위한 분야에 적용 가능할 것으로 기대된다.
김동재 박사과정이 1저자로 참여한 이번 연구는 나노분야의 국제 학술지 ‘스몰(Small)’ 10월 4일자 내부표지 논문으로 게재됐다.(논문명 : SERS-Active Charged Microgels for Size- and Charge-Selective Molecular Analysis of Complex Biological Samples, 생체 시료의 분자 크기 및 전하 선택적 분석을 위한 표면증강라만산란용 마이크로젤)
분자가 레이저에 노출되면 ‘분자 지문’이라고 불리는 고유의 라만(Raman) 신호를 보인다. 하지만 일반적으로 라만 신호의 세기는 매우 낮아 실질적인 분자 감지에 사용이 어렵다.
연구팀은 금속 나노구조의 표면에서 발생하는 표면 플라즈몬 공명 현상이 강한 세기의 기장을 형성하는 점을 이용해 라만신호를 현저히 증가시켰다. 이를 표면증강라만산란 현상이라고 한다.
이 표면증강라만산란 현상에 의해 금속 나노구조 표면에 존재하는 분자의 라만신호는 크게 증가시킬 수 있지만 이를 일반적인 생체 시료에 직접 적용하는 것은 어렵다. 생체 시료에 존재하는 다양한 크기의 단백질들이 금속 표면에 비가역적으로 흡착해 실제 분석이 필요한 분자의 접근을 막기 때문이다.
일반적으로 사용되는 생체 시료 분석법은 대형 장비를 이용한 시료 전처리 과정이 필수이다. 하지만 이로 인해 시료의 신속한 현장 분석이 어려워 시간과 비용을 증가시킨다.
연구팀은 시료의 정제 과정 없이 분자를 직접 검출하기 위해 하이드로젤에 주목했다. 하이드로젤은 친수성(親水性) 나노 그물 구조를 이루고 있어 단백질처럼 크기가 큰 분자는 배제하고 작은 크기의 분자만을 내부로 확산시킨다. 또한 하이드로젤이 전하를 띠는 경우 반대 전하를 띠고 있는 분자를 선택적으로 흡착시켜 농축할 수 있다.
연구팀은 이러한 원리를 센서 구현에 적용시키기 위해 미세유체기술을 이용했다. 이를 통해 금 나노입자 응집체를 형성하는 동시에 전하를 띠는 하이드로젤 미세입자 안에 캡슐화 하는데 성공했다.
하이드로젤 미세 입자는 생체 시료에 도입돼 단백질로부터 금 나노입자 응집체를 보호하고, 동시에 반대 전하를 띠는 표적 분자를 응집체 표면에 선택적으로 농축시킨다. 이를 통해 표적 분자의 라만 신호는 단백질의 방해 없이 증대되며 시료의 전처리 과정 없이 빠르고 정확한 분자 검출이 가능해진다.
김신현 교수는 “새롭게 개발한 라만 센서는 식품 내 살충제 성분 검출 뿐 아니라 혈액과 소변, 땀 등 인체 속 시료에 들어있는 약물, 마약 성분 등 다양한 바이오마커의 직접 검출에도 사용 가능하다”고 말했다.
재료연구소 김동호 박사는 “시료 전처리가 필요없기 때문에 현장에서 시료의 직접 분석이 가능해 시간과 비용의 혁신적 절감이 가능해질 것이다”고 말했다.
이번 연구결과는 재료연구소의 기관 주요사업과 한국연구재단의 중견연구자지원사업 및 글로벌연구실사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. small 저널 내부표지
그림2. 시료 전처리 없이 분자 선택적 라만 분석이 가능한 하이드로젤 기반 라만 센서의 원리
그림3. 분자 전하 선택적 농축 및 배제를 보여주는 현미경 사진
2018.10.18 조회수 12349
김신현 교수, 달걀 속 살충제 성분, 현장 즉시 검출 기술 개발
〈 김신현 교수, 김동재 박사과정 〉
우리 대학 생명화학공학과 김신현 교수 연구팀과 재료연구소(소장 이정환) 김동호 박사 공동 연구팀이 생체 시료에 들어있는 미량의 분자를 직접 검출할 수 있는 센서를 개발했다.
연구팀은 개발한 센서를 통해 다양한 종류의 살충제 성분을 검출하는데 성공했다. 특히 국내 및 유럽에서 문제가 됐던 달걀 속 살충제 성분인 피프로닐 술폰(Fipronil sulfone)을 시료 전처리 없이 검출할 수 있음을 증명했다.
연구팀의 센서는 전하를 띠는 하이드로젤 미세입자 내부에 금 나노입자 응집체를 캡슐화한 형태로 생체 시료 내에 존재하는 분자를 직접 분석해야 하는 광범위한 분야에 적용 가능할 것으로 기대된다.
김동재 박사과정이 1저자로 참여한 이번 연구는 나노분야의 국제 학술지 ‘스몰(Small)’ 10월 4일자 내부표지 논문으로 게재됐다.(논문명 : SERS-Active Charged Microgels for Size- and Charge-Selective Molecular Analysis of Complex Biological Samples, 생체 시료의 분자 크기 및 전하 선택적 분석을 위한 표면증강라만산란용 마이크로젤)
분자가 레이저에 노출되면 ‘분자 지문’이라고 불리는 고유의 라만(Raman) 신호를 보인다. 하지만 일반적으로 라만 신호의 세기는 매우 낮아 실질적인 분자 감지에 사용이 어렵다.
연구팀은 금속 나노구조의 표면에서 발생하는 표면 플라즈몬 공명 현상이 강한 세기의 기장을 형성하는 점을 이용해 라만신호를 현저히 증가시켰다. 이를 표면증강라만산란 현상이라고 한다.
이 표면증강라만산란 현상에 의해 금속 나노구조 표면에 존재하는 분자의 라만신호는 크게 증가시킬 수 있지만 이를 일반적인 생체 시료에 직접 적용하는 것은 어렵다. 생체 시료에 존재하는 다양한 크기의 단백질들이 금속 표면에 비가역적으로 흡착해 실제 분석이 필요한 분자의 접근을 막기 때문이다.
일반적으로 사용되는 생체 시료 분석법은 대형 장비를 이용한 시료 전처리 과정이 필수이다. 하지만 이로 인해 시료의 신속한 현장 분석이 어려워 시간과 비용을 증가시킨다.
연구팀은 시료의 정제 과정 없이 분자를 직접 검출하기 위해 하이드로젤에 주목했다. 하이드로젤은 친수성(親水性) 나노 그물 구조를 이루고 있어 단백질처럼 크기가 큰 분자는 배제하고 작은 크기의 분자만을 내부로 확산시킨다. 또한 하이드로젤이 전하를 띠는 경우 반대 전하를 띠고 있는 분자를 선택적으로 흡착시켜 농축할 수 있다.
연구팀은 이러한 원리를 센서 구현에 적용시키기 위해 미세유체기술을 이용했다. 이를 통해 금 나노입자 응집체를 형성하는 동시에 전하를 띠는 하이드로젤 미세입자 안에 캡슐화 하는데 성공했다.
하이드로젤 미세 입자는 생체 시료에 도입돼 단백질로부터 금 나노입자 응집체를 보호하고, 동시에 반대 전하를 띠는 표적 분자를 응집체 표면에 선택적으로 농축시킨다. 이를 통해 표적 분자의 라만 신호는 단백질의 방해 없이 증대되며 시료의 전처리 과정 없이 빠르고 정확한 분자 검출이 가능해진다.
김신현 교수는 “새롭게 개발한 라만 센서는 식품 내 살충제 성분 검출 뿐 아니라 혈액과 소변, 땀 등 인체 속 시료에 들어있는 약물, 마약 성분 등 다양한 바이오마커의 직접 검출에도 사용 가능하다”고 말했다.
재료연구소 김동호 박사는 “시료 전처리가 필요없기 때문에 현장에서 시료의 직접 분석이 가능해 시간과 비용의 혁신적 절감이 가능해질 것이다”고 말했다.
이번 연구결과는 재료연구소의 기관 주요사업과 한국연구재단의 중견연구자지원사업 및 글로벌연구실사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. small 저널 내부표지
그림2. 시료 전처리 없이 분자 선택적 라만 분석이 가능한 하이드로젤 기반 라만 센서의 원리
그림3. 분자 전하 선택적 농축 및 배제를 보여주는 현미경 사진
2018.10.18 조회수 12349 -
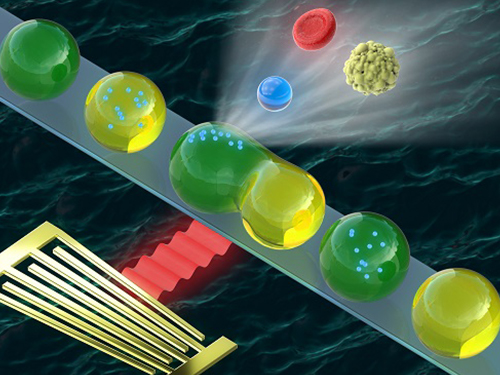 성형진 교수, 마이크로스케일 액적 내 입자의 세정 및 집속기술 개발
우리 대학 기계공학과 성형진 석좌교수 연구팀(유동제어연구실)이 고주파수 표면탄성파 기반 음향방사현상을 이용해 마이크로스케일 액적 내 입자의 세정 및 집속 기술을 개발했다.
박진수 박사과정이 제 1저자로 참여한 이번 연구는 영국왕립화학회에서 발간하는 미세유체역학 및 마이크로타스 분야의 국제학술지 랩온어칩(Lab on a Chip)지 2018년 19호의 표지논문으로 선정됐다 (논문명: In-droplet microparticle washing and enrichment using surface acoustic wave-driven acoustic radiation force).
이는 같은 학술지 2016년 4호, 17호, 2017년 6호, 2018년 3호에 이은 다섯 번째 표지논문으로 미세유체역학 분야의 선도적 연구 성과이다.
동전 크기의 초소형 미세유체칩 내에 서로 섞이지 않는 두 유체로 조성된 마이크로스케일 액적을 기반으로 하는 액적 기반 미세유체역학 분야에서 액적 내 입자, 세포, 생체분자 등의 샘플을 제어하기 위해 많은 노력이 기울여져 왔다.
하지만 지금까지 개발된 액적 내 샘플 세정 및 집속 기술은 복잡한 시스템이 요구되고 자성 혹은 극성을 띈 샘플만 제어할 수 있다는 한계를 지니고 있었다.
이번 연구에서 성 석좌교수 연구팀은 고주파수 표면탄성파를 이용해 마이크로스케일 액적과 액적 내 입자에 음향방사력을 인가해 입자의 위치를 음향장 내에 고정시켰다.
그리고 액적을 포획, 분할, 병합, 방출함으로써 액적 내 입자의 매개 용액을 교체하고 더 나아가 입자의 개체수를 원하는 수준까지 농축할 수 있음을 증명했다.
개발된 기술은 액적 내 입자를 비접촉·비표지 방식으로 세정할 수 있으며 액적 내 샘플의 개체수를 증가시킬 수 있는 기술이라는 점에서 기존보다 진일보했다는 평을 받았다.
아울러 음파와 탄성 고체 입자의 상호작용 이론을 바탕으로 표면탄성파의 주파수와 액적 내 입자 크기 사이의 관계를 규명해 효율적인 음향영동 현상 유발을 위한 조건을 제시했다.
박진수 박사과정은 “개발된 음향미세유체역학 기술을 통해 마이크로스케일 액적 내 샘플의 매개용액을 자유롭게 교체할 수 있음은 물론 액적 내 샘플을 원하는 수준으로 농축할 수 있다”고 말했다.
성형진 석좌교수는 “이 기술이 다양한 액적 기반 미세유체역학 시스템에서 액적 내 입자, 세포, 생체분자 등 다양한 샘플의 전처리를 위한 핵심 기술로 널리 활용될 수 있을 것으로 기대된다”고 말했다.
성형진 석좌교수 연구팀은 그동안 광력과 음향력 기반의 미세유체역학, 난류, 고체-유체 상호작용 연구 분야에서 탁월한 연구 성과를 내 SCI급 국제학술지에 320여편의 논문을 게재한 바 있다.
특히 이번 연구는 올해 우리 대학에서 국내 최초로 시행된 초세대 협업연구실(헬스케어 음향미세유체 연구실)의 공동 연구 성과로, 헬스케어 음향미세유체 연구실은 기계공학과 성형진 석좌교수가 책임을 맡고 같은 학과 조연우 교수, 김형수 교수가 참여하고 있다.
이번 연구는 KAIST-KUSTAR, 한국연구재단의 창의연구지원사업과 글로벌박사펠로우십, 극지연구소, KAIST 초세대 협엽연구실(헬스케어 음향미세유체 연구실)의 지원으로 수행됐다.
□ 그림 설명
그림1. 논문 대표 이미지
그림2. 표지논문 이미지
2018.10.05 조회수 13772
성형진 교수, 마이크로스케일 액적 내 입자의 세정 및 집속기술 개발
우리 대학 기계공학과 성형진 석좌교수 연구팀(유동제어연구실)이 고주파수 표면탄성파 기반 음향방사현상을 이용해 마이크로스케일 액적 내 입자의 세정 및 집속 기술을 개발했다.
박진수 박사과정이 제 1저자로 참여한 이번 연구는 영국왕립화학회에서 발간하는 미세유체역학 및 마이크로타스 분야의 국제학술지 랩온어칩(Lab on a Chip)지 2018년 19호의 표지논문으로 선정됐다 (논문명: In-droplet microparticle washing and enrichment using surface acoustic wave-driven acoustic radiation force).
이는 같은 학술지 2016년 4호, 17호, 2017년 6호, 2018년 3호에 이은 다섯 번째 표지논문으로 미세유체역학 분야의 선도적 연구 성과이다.
동전 크기의 초소형 미세유체칩 내에 서로 섞이지 않는 두 유체로 조성된 마이크로스케일 액적을 기반으로 하는 액적 기반 미세유체역학 분야에서 액적 내 입자, 세포, 생체분자 등의 샘플을 제어하기 위해 많은 노력이 기울여져 왔다.
하지만 지금까지 개발된 액적 내 샘플 세정 및 집속 기술은 복잡한 시스템이 요구되고 자성 혹은 극성을 띈 샘플만 제어할 수 있다는 한계를 지니고 있었다.
이번 연구에서 성 석좌교수 연구팀은 고주파수 표면탄성파를 이용해 마이크로스케일 액적과 액적 내 입자에 음향방사력을 인가해 입자의 위치를 음향장 내에 고정시켰다.
그리고 액적을 포획, 분할, 병합, 방출함으로써 액적 내 입자의 매개 용액을 교체하고 더 나아가 입자의 개체수를 원하는 수준까지 농축할 수 있음을 증명했다.
개발된 기술은 액적 내 입자를 비접촉·비표지 방식으로 세정할 수 있으며 액적 내 샘플의 개체수를 증가시킬 수 있는 기술이라는 점에서 기존보다 진일보했다는 평을 받았다.
아울러 음파와 탄성 고체 입자의 상호작용 이론을 바탕으로 표면탄성파의 주파수와 액적 내 입자 크기 사이의 관계를 규명해 효율적인 음향영동 현상 유발을 위한 조건을 제시했다.
박진수 박사과정은 “개발된 음향미세유체역학 기술을 통해 마이크로스케일 액적 내 샘플의 매개용액을 자유롭게 교체할 수 있음은 물론 액적 내 샘플을 원하는 수준으로 농축할 수 있다”고 말했다.
성형진 석좌교수는 “이 기술이 다양한 액적 기반 미세유체역학 시스템에서 액적 내 입자, 세포, 생체분자 등 다양한 샘플의 전처리를 위한 핵심 기술로 널리 활용될 수 있을 것으로 기대된다”고 말했다.
성형진 석좌교수 연구팀은 그동안 광력과 음향력 기반의 미세유체역학, 난류, 고체-유체 상호작용 연구 분야에서 탁월한 연구 성과를 내 SCI급 국제학술지에 320여편의 논문을 게재한 바 있다.
특히 이번 연구는 올해 우리 대학에서 국내 최초로 시행된 초세대 협업연구실(헬스케어 음향미세유체 연구실)의 공동 연구 성과로, 헬스케어 음향미세유체 연구실은 기계공학과 성형진 석좌교수가 책임을 맡고 같은 학과 조연우 교수, 김형수 교수가 참여하고 있다.
이번 연구는 KAIST-KUSTAR, 한국연구재단의 창의연구지원사업과 글로벌박사펠로우십, 극지연구소, KAIST 초세대 협엽연구실(헬스케어 음향미세유체 연구실)의 지원으로 수행됐다.
□ 그림 설명
그림1. 논문 대표 이미지
그림2. 표지논문 이미지
2018.10.05 조회수 13772 -
 김준 교수, 난치성 유전질환인 섬모병증 치료제 후보 발굴
〈 김준 교수, 김용준 박사과정 〉
우리 대학 의과학대학원 김준 교수가 연세대학교 생명공학과 권호정 교수 연구팀과의 공동 연구를 통해 난치성 유전질환인 섬모병증의 치료제 후보를 개발했다.
이번 연구 결과는 섬모병증 치료제 개발을 위한 기반이 될 것으로 기대되며 유사한 난치성 유전질환에 대한 저분자 화합물 약물 개발 플랫폼으로도 활용 가능할 것으로 예상된다.
김용준 박사과정이 1저자로 참여하고 정인지, 김성수, 정유주 연구원이 공동 저자로 참여한 이번 연구는 의, 과학 분야 국제 학술지 ‘저널 오브 클리니컬 인베스티게이션(Journal of Clinical Investigation)’ 7월 23일자 온라인 판에 게재됐다.(논문명 Eupatilin rescues ciliary transition zone defects to ameliorate ciliopathy-related phenotypes)
세포 소기관인 일차섬모는 배아가 발생하는 과정에서 세포 간 신호전달에 관여하고 망막 광수용체 세포가 기능하는 역할을 하는 등 인체에 중요한 기관이다.
섬모병증은 이러한 섬모의 형성에 필수적인 유전자들의 돌연변이로 인해 발생되며 소뇌발달 및 신장 이상, 망막 퇴행 등의 증상을 보인다.
현재 섬모병증을 치료하는 약물은 개발되지 않았다. 섬모병증 뿐 아니라 기능손실 유전자 돌연변이가 원인이 되는 대부분의 희귀유전질환은 유전자 치료를 제외하고는 치료 약물의 개발이 이뤄지지 않았다.
연구팀은 문제 해결을 위해 섬모병증 원인의 하나인 CEP290 유전자 돌연변이를 유전자 편집기법으로 모사한 세포를 구축한 뒤 화합물 라이브러리 스크리닝 기법을 통해 섬모병증에서 나타나는 섬모형성 부진 현상을 극복할 수 있는 천연 저분자 화합물을 발굴했다.
발굴된 화합물은 CEP290 단백질과 복합체를 이뤄 섬모형성과 기능에 관여하는 단백질(NPHP5)에 작용하는 것으로 밝혀졌다. CEP290 단백질이 유전자 돌연변이로 인해 만들어지지 않는 경우 NPHP5 단백질도 정상적으로 작용하지 못하는데 이 화합물은 NPHP5의 기능을 정상화시켜 복합체가 담당하던 기능의 일부를 회복함을 확인했다.
또한 연구팀은 발굴한 화합물을 섬모병증 증상을 갖는 동물 모델에 주입했고 망막 퇴행 현상을 지연시키는 효과를 입증했다.
1저자인 김용준 박사과정은 “이번 연구는 기능손실 유전자 돌연변이로 인해 발생하는 유전질환도 저분자 화합물 약물로 치료가 가능함을 규명했다는 의미를 갖는다”고 말했다.
김준 교수는 “발굴된 후보약물의 효과를 동물실험을 통해 확인했기 때문에 인체에서의 효과 또한 증명하는 후속 연구를 진행할 예정이다”고 말했다.
이번 연구는 보건복지부 희귀질환연구센터지원사업, 한국연구재단 바이오의료기술개발사업, 글로벌연구실 사업의 지원으로 수행됐다.
□ 그림 설명
그림1.섬모형성 이상을 회복시키는 약물 발굴
그림2. 발굴된 약물에 의해 섬모병증 모델 생쥐의 망막퇴행이 지연되는 효과 확인
2018.07.30 조회수 12249
김준 교수, 난치성 유전질환인 섬모병증 치료제 후보 발굴
〈 김준 교수, 김용준 박사과정 〉
우리 대학 의과학대학원 김준 교수가 연세대학교 생명공학과 권호정 교수 연구팀과의 공동 연구를 통해 난치성 유전질환인 섬모병증의 치료제 후보를 개발했다.
이번 연구 결과는 섬모병증 치료제 개발을 위한 기반이 될 것으로 기대되며 유사한 난치성 유전질환에 대한 저분자 화합물 약물 개발 플랫폼으로도 활용 가능할 것으로 예상된다.
김용준 박사과정이 1저자로 참여하고 정인지, 김성수, 정유주 연구원이 공동 저자로 참여한 이번 연구는 의, 과학 분야 국제 학술지 ‘저널 오브 클리니컬 인베스티게이션(Journal of Clinical Investigation)’ 7월 23일자 온라인 판에 게재됐다.(논문명 Eupatilin rescues ciliary transition zone defects to ameliorate ciliopathy-related phenotypes)
세포 소기관인 일차섬모는 배아가 발생하는 과정에서 세포 간 신호전달에 관여하고 망막 광수용체 세포가 기능하는 역할을 하는 등 인체에 중요한 기관이다.
섬모병증은 이러한 섬모의 형성에 필수적인 유전자들의 돌연변이로 인해 발생되며 소뇌발달 및 신장 이상, 망막 퇴행 등의 증상을 보인다.
현재 섬모병증을 치료하는 약물은 개발되지 않았다. 섬모병증 뿐 아니라 기능손실 유전자 돌연변이가 원인이 되는 대부분의 희귀유전질환은 유전자 치료를 제외하고는 치료 약물의 개발이 이뤄지지 않았다.
연구팀은 문제 해결을 위해 섬모병증 원인의 하나인 CEP290 유전자 돌연변이를 유전자 편집기법으로 모사한 세포를 구축한 뒤 화합물 라이브러리 스크리닝 기법을 통해 섬모병증에서 나타나는 섬모형성 부진 현상을 극복할 수 있는 천연 저분자 화합물을 발굴했다.
발굴된 화합물은 CEP290 단백질과 복합체를 이뤄 섬모형성과 기능에 관여하는 단백질(NPHP5)에 작용하는 것으로 밝혀졌다. CEP290 단백질이 유전자 돌연변이로 인해 만들어지지 않는 경우 NPHP5 단백질도 정상적으로 작용하지 못하는데 이 화합물은 NPHP5의 기능을 정상화시켜 복합체가 담당하던 기능의 일부를 회복함을 확인했다.
또한 연구팀은 발굴한 화합물을 섬모병증 증상을 갖는 동물 모델에 주입했고 망막 퇴행 현상을 지연시키는 효과를 입증했다.
1저자인 김용준 박사과정은 “이번 연구는 기능손실 유전자 돌연변이로 인해 발생하는 유전질환도 저분자 화합물 약물로 치료가 가능함을 규명했다는 의미를 갖는다”고 말했다.
김준 교수는 “발굴된 후보약물의 효과를 동물실험을 통해 확인했기 때문에 인체에서의 효과 또한 증명하는 후속 연구를 진행할 예정이다”고 말했다.
이번 연구는 보건복지부 희귀질환연구센터지원사업, 한국연구재단 바이오의료기술개발사업, 글로벌연구실 사업의 지원으로 수행됐다.
□ 그림 설명
그림1.섬모형성 이상을 회복시키는 약물 발굴
그림2. 발굴된 약물에 의해 섬모병증 모델 생쥐의 망막퇴행이 지연되는 효과 확인
2018.07.30 조회수 12249