-
 김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27
조회수 22014
-
 연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
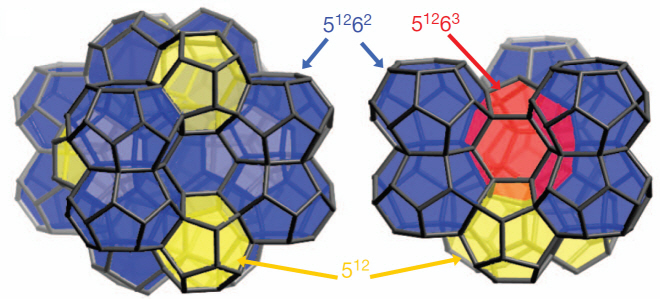
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
2012.07.24
조회수 22827
 김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 22014
김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 22014 연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
2012.07.24 조회수 22827
연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
2012.07.24 조회수 22827