-
 최정우 교수팀, 세계 최고 음향 AI 챌린지 세계 1위 쾌거
‘음향 분리 및 분류 기술’은 드론, 공장 배관, 국경 감시 시스템 등에서 이상 음향을 조기에 탐지하거나, AR/VR 콘텐츠 제작 시 공간 음향(Spatial Audio)을 음원별로 분리해 편집할 수 있도록 하는 차세대 인공지능(AI) 핵심 기술이다.
우리 대학 전기및전자공학부 최정우 교수 연구팀이 세계 최고 권위의 음향 탐지 및 분석 대회인 ‘IEEE DCASE 챌린지 2025’에서 ‘공간 의미 기반 음향 장면 분할(Spatial Semantic Segmentation of Sound Scenes)’ 분야에서 우승을 차지했다고 11일 밝혔다.
이번 대회에서 연구팀은 전 세계 86개 참가팀과 총 6개 분야에서 경쟁 끝에 최초 참가임에도 세계 1위 성과를 거두었다. KAIST 최정우 교수 연구팀은 이동헌 박사, 권영후 석박통합과정생, 김도환 석사과정생으로 구성되었다.
연구팀이 참가한 ‘공간 의미 기반 음향 장면 분할’의 ‘태스크(Task) 4’분야는 여러 음원이 혼합된 다채널 신호의 공간 정보를 분석해 개별 소리를 분리하고 18종으로의 분류를 수행해야 하는 기술 난이도가 매우 높은 분야이다. 연구팀은 오는 10월, 바르셀로나에서 열리는 DCASE 워크숍에서 기술을 발표할 예정이다.
연구팀의 이동헌 박사는 올해 초 트랜스포머(Transformer)와 맘바(Mamba) 아키텍처를 결합한 세계 최고 성능의 음원 분리 인공지능을 개발했으며, 챌린지 기간 동안 권영후 연구원을 중심으로 1차로 분리된 음원의 파형과 종류를 단서로 해 다시 음원 분리와 분류를 수행하는‘단계적 추론 방식’의 AI 모델을 완성했다.
이는 사람이 복잡한 소리를 들을 때 소리의 종류나 리듬, 방향 등 특정 단서에 기반해 개별 소리를 분리해 듣는 방식을 AI가 모방한 모델이다.
이를 통해, 순위를 결정하는 척도인 AI가 소리를 얼마나 잘 분리하고 분류했는지 평가하는‘음원의 신호대 왜곡비 향상도(CA-SDRi)*’에서 참가팀 중 유일하게 두 자릿수 대의 성능(11 dB)을 보여, 기술적인 우수성을 입증하였다.
*음원의 신호대 왜곡비 향상도(CA-SDRi): 기존의 오디오와 비교해 얼마나 더 선명하게(덜 왜곡되게) 원하는 소리를 분리했는지를 dB(데시벨) 단위로 측정하고 숫자가 클수록 더 정확하고 깔끔하게 소리를 분리했다는 뜻임
최정우 교수는 "연구팀은 최근 3년간 세계 최고의 음향 분리 AI 모델을 선보여 왔으며, 그 결과를 공식적으로 인정받는 계기가 되어 기쁘다”면서 “난이도가 대폭 향상되고, 타 학회 일정과 기말고사로 불과 몇 주간만 개발이 가능했음에도 집중력 있는 연구를 통해 1위를 차지한 연구팀 개개인이 자랑스럽다”고 소감을 밝혔다.
‘IEEE DCASE 챌린지 2025’는 온라인으로 진행됐으며, 4월 1일부터 시작해 6월 15일 인공지능 모델 투고를 마감했고 지난 6월 30일 결과가 발표됐다. 각종 음향 관련 탐지 및 분류 기술을 평가하는 IEEE 신호처리학회(Signal Processing Society) 산하 국제대회인 본 챌린지는 2013년 개최된 이래 음향 분야 인공지능 모델의 세계적인 경연의 장으로 자리매김해 왔다.
https://dcase.community/challenge2025/task-spatial-semantic-segmentation-of-sound-scenes
한편, 해당 연구는 교육과학기술부의 재원으로 한국연구재단 중견연구자지원사업, STEAM 연구사업 지원 및 방위사업청 및 국방과학연구소 재원으로 미래국방연구센터 지원을 받아 수행됐다.
최정우 교수팀, 세계 최고 음향 AI 챌린지 세계 1위 쾌거
‘음향 분리 및 분류 기술’은 드론, 공장 배관, 국경 감시 시스템 등에서 이상 음향을 조기에 탐지하거나, AR/VR 콘텐츠 제작 시 공간 음향(Spatial Audio)을 음원별로 분리해 편집할 수 있도록 하는 차세대 인공지능(AI) 핵심 기술이다.
우리 대학 전기및전자공학부 최정우 교수 연구팀이 세계 최고 권위의 음향 탐지 및 분석 대회인 ‘IEEE DCASE 챌린지 2025’에서 ‘공간 의미 기반 음향 장면 분할(Spatial Semantic Segmentation of Sound Scenes)’ 분야에서 우승을 차지했다고 11일 밝혔다.
이번 대회에서 연구팀은 전 세계 86개 참가팀과 총 6개 분야에서 경쟁 끝에 최초 참가임에도 세계 1위 성과를 거두었다. KAIST 최정우 교수 연구팀은 이동헌 박사, 권영후 석박통합과정생, 김도환 석사과정생으로 구성되었다.
연구팀이 참가한 ‘공간 의미 기반 음향 장면 분할’의 ‘태스크(Task) 4’분야는 여러 음원이 혼합된 다채널 신호의 공간 정보를 분석해 개별 소리를 분리하고 18종으로의 분류를 수행해야 하는 기술 난이도가 매우 높은 분야이다. 연구팀은 오는 10월, 바르셀로나에서 열리는 DCASE 워크숍에서 기술을 발표할 예정이다.
연구팀의 이동헌 박사는 올해 초 트랜스포머(Transformer)와 맘바(Mamba) 아키텍처를 결합한 세계 최고 성능의 음원 분리 인공지능을 개발했으며, 챌린지 기간 동안 권영후 연구원을 중심으로 1차로 분리된 음원의 파형과 종류를 단서로 해 다시 음원 분리와 분류를 수행하는‘단계적 추론 방식’의 AI 모델을 완성했다.
이는 사람이 복잡한 소리를 들을 때 소리의 종류나 리듬, 방향 등 특정 단서에 기반해 개별 소리를 분리해 듣는 방식을 AI가 모방한 모델이다.
이를 통해, 순위를 결정하는 척도인 AI가 소리를 얼마나 잘 분리하고 분류했는지 평가하는‘음원의 신호대 왜곡비 향상도(CA-SDRi)*’에서 참가팀 중 유일하게 두 자릿수 대의 성능(11 dB)을 보여, 기술적인 우수성을 입증하였다.
*음원의 신호대 왜곡비 향상도(CA-SDRi): 기존의 오디오와 비교해 얼마나 더 선명하게(덜 왜곡되게) 원하는 소리를 분리했는지를 dB(데시벨) 단위로 측정하고 숫자가 클수록 더 정확하고 깔끔하게 소리를 분리했다는 뜻임
최정우 교수는 "연구팀은 최근 3년간 세계 최고의 음향 분리 AI 모델을 선보여 왔으며, 그 결과를 공식적으로 인정받는 계기가 되어 기쁘다”면서 “난이도가 대폭 향상되고, 타 학회 일정과 기말고사로 불과 몇 주간만 개발이 가능했음에도 집중력 있는 연구를 통해 1위를 차지한 연구팀 개개인이 자랑스럽다”고 소감을 밝혔다.
‘IEEE DCASE 챌린지 2025’는 온라인으로 진행됐으며, 4월 1일부터 시작해 6월 15일 인공지능 모델 투고를 마감했고 지난 6월 30일 결과가 발표됐다. 각종 음향 관련 탐지 및 분류 기술을 평가하는 IEEE 신호처리학회(Signal Processing Society) 산하 국제대회인 본 챌린지는 2013년 개최된 이래 음향 분야 인공지능 모델의 세계적인 경연의 장으로 자리매김해 왔다.
https://dcase.community/challenge2025/task-spatial-semantic-segmentation-of-sound-scenes
한편, 해당 연구는 교육과학기술부의 재원으로 한국연구재단 중견연구자지원사업, STEAM 연구사업 지원 및 방위사업청 및 국방과학연구소 재원으로 미래국방연구센터 지원을 받아 수행됐다.
2025.07.11
조회수 282
-
 뇌는 포도당을 구별한다..비만·당뇨 치료의 단서 찾아
‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해낼까?’ 우리 대학 연구진은 이 질문에서 출발해, 뇌가 단순히 총열량(칼로리)을 감지하는 수준을 넘어 특정 영양소, 특히 포도당을 선택적으로 인식할 수 있다는 사실을 입증했다. 이번 연구는 향후 식욕 조절 및 대사성 질환 치료 전략에 새로운 패러다임을 제시할 수 있을 것으로 기대된다.
우리 대학 생명과학과 서성배 교수 연구팀이 바이오및뇌공학과 박영균 교수팀, 생명과학과 이승희 교수팀, 뉴욕 알버트 아인슈타인 의과대학과의 협력을 통해, 배고픔 상태에서 포도당이 결핍된 동물이 장내의 포도당을 선택적으로 인식하고 선호하도록 유도하는 장-뇌 회로의 존재를 규명했다고 9일 밝혔다.
생물은 당, 단백질, 지방 등 다양한 영양소로부터 에너지를 얻는다. 기존 연구들은 장내 총열량 정보가 시상하부의 배고픔 뉴런(hunger neurons)을 억제함으로써 식욕을 조절한다는 사실을 밝혀왔으나, 특정 포도당에 특이적으로 반응하는 장-뇌 회로와 이에 반응하는 특정 뇌세포의 존재는 규명되지 않았다.
연구팀은 이번 연구를 통해 뇌의 기능에 필수적인 포도당을 감지하고 필요한 영양소에 대한 섭취 행동을 조절하는 ‘장-뇌 회로’를 밝혀내는 데 성공했다.
또한, 이 회로는 뇌의 ‘스트레스 반응 세포(CRF 뉴런*)’가 배고픔이나 외부 자극뿐만 아니라, 소장에 직접 유입된 특정 열량 영양소에 대해서도 초 단위로 반응하며, 특히 ‘포도당(D-glucose)’에 선택적으로 반응한다는 점을 처음으로 입증했다.
*CRF 뉴런: 우리 몸이 심리적·물리적 스트레스에 대응하는 핵심 생리 시스템은 시상하부-뇌하수체-부신 축(Hypothalamus-Pituitary-Adrenal Axis, HPA axis)이다. 이 축의 중심에는 시상하부에서 CRF(부신피질호르몬 방출인자)를 분비하는 뉴런이 있으며, 이들은 다양한 스트레스 자극에 반응해 코르티솔 분비를 유도하고, 생리 및 대사 균형을 유지하는 신경 내분비 조절의 중추로 알려져 있다.
연구팀은 실시간 뇌 속을 정밀하게 추적할 수 있는 광유전학 기반 신경 활성 조절 및 회로 추적 기법을 활용해서, 포도당(D-글루코스, L-글루코스,) 아미노산, 지방 등 다양한 영양소의 쥐의 소장 내 직접 주입하고 관찰했다.
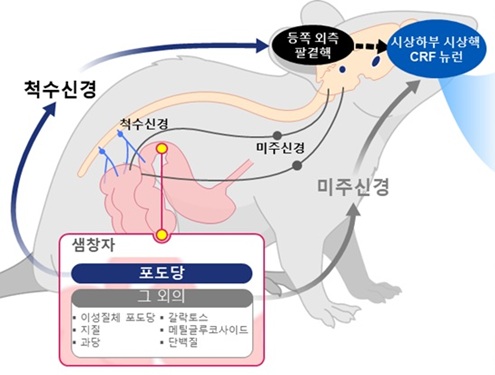
그 결과, 뇌 시상하부의 ‘시상하부 시상핵(PVN)* 부위’에 있는 CRF 뉴런 중 D-글루코스(glucose) 포도당에만 선택적으로 반응하며, 다른 당류나 단백질·지방류에는 반응하지 않거나 반대 방향의 반응을 보이는 것을 확인했다. 이는 뇌가 장내 영양소가 유입 시 반응에 대해 단일 뇌세포 수준에서 어떤 방향성을 유도한다는 것을 처음 확인한 것을 의미한다.
* 시상하부 시상핵(paraventricular nucleus, PVN): 뇌의 시상하부(hypothalamus) 안에 있는 매우 중요한 신경핵(뉴런 무리)으로, 신체 항상성(몸의 균형 유지)을 조절하는 핵심 구조
또한, 연구팀은 소장의 포도당 감지 신호가 ‘척수신경’을 거쳐 뇌의 특정 부위(등쪽 외측 팔곁핵,parabrachial nucleus, PBNdl)을 통해 PVN의 CRF 뉴런으로 전달되는 특징적인 회로를 밝혀냈다. 반면, 아미노산이나 지방 등 기타 영양소는 미주신경(vagus nerve)이란 다른 통로로 뇌에 전달된다는 사실도 확인했다.
광유전학적 억제 실험에서도, 공복 상태의 생쥐에서 CRF 뉴런을 억제하면 동물은 더 이상 포도당을 선호하지 않게 됐으며, 이 회로가 영양소 선택에 있어 포도당 특이적 선호를 유도하는 데 필수적임이 드러났다.
이 연구는 서 교수가 뉴욕대(NYU) 재직 시절 초파리를 모델로, 장내 포도당(글루코스) 및 당을 선택적으로 감지하는 ‘DH44 뉴런’을 발견했던 점을 착안해, 포유류에서도 시상하부 뉴런이 포도당 특이적 반응에 있어 기능적 유사성을 보일 것이라는 가설에서 시작되었다.
이 가설을 입증하기 위해 서 교수 연구팀 김진은 박사(KAIST 박사 졸, 現 캘리포니아공과대학교 연수연구원)가 학위과정 중 생쥐 실험을 통해 배고픈 쥐는 장에 주입된 다양한 영양소 중 열량을 지닌 포도당을 선호하며, CRF 뉴런이 빠르고 특이적인 반응을 보인다는 사실을 확인했다.
또한, 같은 팀 정원교 연구원(KAIST 학사 졸, 現 캘리포니아공과대학교 박사과정)과 함께 실험과 모델링을 통해 CRF 뉴런의 중요성을 규명했고, 김신혜 박사는 협업을 통해 장-뇌 회로 중 특정 척추 신경세포가 장의 정보를 뇌로 전달 한다는 놀라운 발견을 입증했다.
김진은 박사와 김신혜 박사는 “이 연구는 ‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해내는가?’라는 단순하지만, 본질적인 질문에서 시작됐고, 이번 연구에서 장-뇌 연결 회로의 핵심 축인 척수신경의 역할을 규명하고 장내 특정 영양소를 감지한 후 이를 뇌에 전달하는 척수 기반 신경 회로가 우리 몸의 에너지 대사 조절과 항상성 유지에 핵심적일 것이라는 것을 밝혀냈다”고 말했다.
서성배 교수는 “이번 연구는 포도당에 특화된 장-뇌 신호 경로를 규명함으로써, 비만·당뇨병 등 대사 질환의 새로운 치료 표적을 제시할 수 있다”며 “향후 아미노산, 지방 등 다른 필수 영양소를 감지하는 유사 회로의 존재와 그 상호작용 메커니즘을 밝히는 연구로 확장될 예정”이라고 밝혔다.
우리 대학 김진은 박사, 김신혜 박사, 정원교 학생이 공동 제1 저자로 참여한 이번 연구의 결과는 국제 학술지 ‘뉴런(Neuron)’에 2025년 6월 20일 온라인 게재됐다.
※논문명: Encoding the glucose identity by discrete hypothalamic neurons via the gut-brain axis
※DOI: https://doi.org/10.1016/j.neuron.2025.05.024
이번 연구는 삼성미래기술육성사업, 한국연구재단 리더과제, 포스코 청암재단 사이언스 펠로십, 아산재단 의생명과학 장학사업, 기초과학연구원, KAIST KAIX 사업의 지원을 통해 수행됐다.
뇌는 포도당을 구별한다..비만·당뇨 치료의 단서 찾아
‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해낼까?’ 우리 대학 연구진은 이 질문에서 출발해, 뇌가 단순히 총열량(칼로리)을 감지하는 수준을 넘어 특정 영양소, 특히 포도당을 선택적으로 인식할 수 있다는 사실을 입증했다. 이번 연구는 향후 식욕 조절 및 대사성 질환 치료 전략에 새로운 패러다임을 제시할 수 있을 것으로 기대된다.
우리 대학 생명과학과 서성배 교수 연구팀이 바이오및뇌공학과 박영균 교수팀, 생명과학과 이승희 교수팀, 뉴욕 알버트 아인슈타인 의과대학과의 협력을 통해, 배고픔 상태에서 포도당이 결핍된 동물이 장내의 포도당을 선택적으로 인식하고 선호하도록 유도하는 장-뇌 회로의 존재를 규명했다고 9일 밝혔다.
생물은 당, 단백질, 지방 등 다양한 영양소로부터 에너지를 얻는다. 기존 연구들은 장내 총열량 정보가 시상하부의 배고픔 뉴런(hunger neurons)을 억제함으로써 식욕을 조절한다는 사실을 밝혀왔으나, 특정 포도당에 특이적으로 반응하는 장-뇌 회로와 이에 반응하는 특정 뇌세포의 존재는 규명되지 않았다.
연구팀은 이번 연구를 통해 뇌의 기능에 필수적인 포도당을 감지하고 필요한 영양소에 대한 섭취 행동을 조절하는 ‘장-뇌 회로’를 밝혀내는 데 성공했다.
또한, 이 회로는 뇌의 ‘스트레스 반응 세포(CRF 뉴런*)’가 배고픔이나 외부 자극뿐만 아니라, 소장에 직접 유입된 특정 열량 영양소에 대해서도 초 단위로 반응하며, 특히 ‘포도당(D-glucose)’에 선택적으로 반응한다는 점을 처음으로 입증했다.
*CRF 뉴런: 우리 몸이 심리적·물리적 스트레스에 대응하는 핵심 생리 시스템은 시상하부-뇌하수체-부신 축(Hypothalamus-Pituitary-Adrenal Axis, HPA axis)이다. 이 축의 중심에는 시상하부에서 CRF(부신피질호르몬 방출인자)를 분비하는 뉴런이 있으며, 이들은 다양한 스트레스 자극에 반응해 코르티솔 분비를 유도하고, 생리 및 대사 균형을 유지하는 신경 내분비 조절의 중추로 알려져 있다.
연구팀은 실시간 뇌 속을 정밀하게 추적할 수 있는 광유전학 기반 신경 활성 조절 및 회로 추적 기법을 활용해서, 포도당(D-글루코스, L-글루코스,) 아미노산, 지방 등 다양한 영양소의 쥐의 소장 내 직접 주입하고 관찰했다.
그 결과, 뇌 시상하부의 ‘시상하부 시상핵(PVN)* 부위’에 있는 CRF 뉴런 중 D-글루코스(glucose) 포도당에만 선택적으로 반응하며, 다른 당류나 단백질·지방류에는 반응하지 않거나 반대 방향의 반응을 보이는 것을 확인했다. 이는 뇌가 장내 영양소가 유입 시 반응에 대해 단일 뇌세포 수준에서 어떤 방향성을 유도한다는 것을 처음 확인한 것을 의미한다.
* 시상하부 시상핵(paraventricular nucleus, PVN): 뇌의 시상하부(hypothalamus) 안에 있는 매우 중요한 신경핵(뉴런 무리)으로, 신체 항상성(몸의 균형 유지)을 조절하는 핵심 구조
또한, 연구팀은 소장의 포도당 감지 신호가 ‘척수신경’을 거쳐 뇌의 특정 부위(등쪽 외측 팔곁핵,parabrachial nucleus, PBNdl)을 통해 PVN의 CRF 뉴런으로 전달되는 특징적인 회로를 밝혀냈다. 반면, 아미노산이나 지방 등 기타 영양소는 미주신경(vagus nerve)이란 다른 통로로 뇌에 전달된다는 사실도 확인했다.
광유전학적 억제 실험에서도, 공복 상태의 생쥐에서 CRF 뉴런을 억제하면 동물은 더 이상 포도당을 선호하지 않게 됐으며, 이 회로가 영양소 선택에 있어 포도당 특이적 선호를 유도하는 데 필수적임이 드러났다.
이 연구는 서 교수가 뉴욕대(NYU) 재직 시절 초파리를 모델로, 장내 포도당(글루코스) 및 당을 선택적으로 감지하는 ‘DH44 뉴런’을 발견했던 점을 착안해, 포유류에서도 시상하부 뉴런이 포도당 특이적 반응에 있어 기능적 유사성을 보일 것이라는 가설에서 시작되었다.
이 가설을 입증하기 위해 서 교수 연구팀 김진은 박사(KAIST 박사 졸, 現 캘리포니아공과대학교 연수연구원)가 학위과정 중 생쥐 실험을 통해 배고픈 쥐는 장에 주입된 다양한 영양소 중 열량을 지닌 포도당을 선호하며, CRF 뉴런이 빠르고 특이적인 반응을 보인다는 사실을 확인했다.
또한, 같은 팀 정원교 연구원(KAIST 학사 졸, 現 캘리포니아공과대학교 박사과정)과 함께 실험과 모델링을 통해 CRF 뉴런의 중요성을 규명했고, 김신혜 박사는 협업을 통해 장-뇌 회로 중 특정 척추 신경세포가 장의 정보를 뇌로 전달 한다는 놀라운 발견을 입증했다.
김진은 박사와 김신혜 박사는 “이 연구는 ‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해내는가?’라는 단순하지만, 본질적인 질문에서 시작됐고, 이번 연구에서 장-뇌 연결 회로의 핵심 축인 척수신경의 역할을 규명하고 장내 특정 영양소를 감지한 후 이를 뇌에 전달하는 척수 기반 신경 회로가 우리 몸의 에너지 대사 조절과 항상성 유지에 핵심적일 것이라는 것을 밝혀냈다”고 말했다.
서성배 교수는 “이번 연구는 포도당에 특화된 장-뇌 신호 경로를 규명함으로써, 비만·당뇨병 등 대사 질환의 새로운 치료 표적을 제시할 수 있다”며 “향후 아미노산, 지방 등 다른 필수 영양소를 감지하는 유사 회로의 존재와 그 상호작용 메커니즘을 밝히는 연구로 확장될 예정”이라고 밝혔다.
우리 대학 김진은 박사, 김신혜 박사, 정원교 학생이 공동 제1 저자로 참여한 이번 연구의 결과는 국제 학술지 ‘뉴런(Neuron)’에 2025년 6월 20일 온라인 게재됐다.
※논문명: Encoding the glucose identity by discrete hypothalamic neurons via the gut-brain axis
※DOI: https://doi.org/10.1016/j.neuron.2025.05.024
이번 연구는 삼성미래기술육성사업, 한국연구재단 리더과제, 포스코 청암재단 사이언스 펠로십, 아산재단 의생명과학 장학사업, 기초과학연구원, KAIST KAIX 사업의 지원을 통해 수행됐다.
2025.07.09
조회수 407
-
 부작용·내성 극복한 신개념 칸디다증 치료제 개발
칸디다증은 곰팡이균(진균)의 일종인 칸디다(Candida)가 혈액을 통해 전신으로 퍼지며 장기 손상과 패혈증을 유발할 수 있는 치명적인 감염 질환이다. 최근 면역 저하 치료, 장기 이식, 의료기기 사용 등이 증가함에 따라 칸디다증 발병이 급증하고 있다. 한국 연구진이 기존 항진균제와 달리, 칸디다균에만 선택적으로 작용해 높은 치료 효능과 낮은 부작용을 동시에 갖춘 차세대 치료제를 개발하는데 성공했다.
우리 대학 생명과학과 정현정 교수 연구팀이 서울아산병원 정용필 교수팀과의 협력을 통해, 칸디다 세포벽의 두 핵심 효소를 동시에 저해하는 유전자 기반 나노치료제(FTNx)를 개발했다고 8일 밝혔다.
현재 사용 중인 칸디다의 항진균제들은 표적 선택성이 낮아 인체 세포에도 영향을 미칠 수 있으며, 이에 내성을 가지는 새로운 균의 출현으로 인해 치료 효과가 점차 떨어지고 있다. 특히 면역력이 저하된 환자들에게는 감염의 진행이 빠르고 예후도 좋지 않아, 기존 치료제의 한계를 극복할 수 있는 새로운 치료법의 개발이 시급한 상황이다.
이에 연구팀이 개발한 치료제는 전신 투여가 가능하며, 유전자 억제 기술과 나노소재 기술을 융합함으로써 기존 화합물 기반의 약물들이 가지는 구조적 한계를 효과적으로 극복하고, 칸디다균에만 선택적으로 치료하는데 성공했다.
연구팀은 칸디다라는 곰팡이균의 세포벽을 만드는 데 중요한 두 가지 효소 — β‑1,3‑글루칸 합성효소(FKS1)와 키틴 합성효소(CHS3)를 동시에 표적하는 짧은 DNA 조각(antisense oligonucleotide, ASO)을 탑재한 금 나노입자 기반의 복합체를 제작했다.
여기에 칸디다 세포벽의 특정 당지질 구조(당과 지방이 결합된 구조)와 결합하는 표면 코팅 기술을 적용하여 표적유도장치를 장착함으로써, 인체 세포에는 아예 전달되지 않고 칸디다에만 선택적으로 작용하는 정밀 타겟팅 효과를 구현하는 데 성공했다.
이 복합체는 칸디다 세포 내로 진입한 후, FKS1 및 CHS3의 유전자가 만들어내는 mRNA를 잘라버려서 번역을 억제해 세포벽 성분인 β‑1,3‑글루칸과 키틴의 합성을 동시에 차단한다. 이로 인해 칸디다 세포벽은 구조적 안정성을 유지하지 못하고 붕괴되며, 세균의 생존과 증식이 억제된다.
실제로 쥐에서 전신 칸디다증 모델 실험을 통해 치료 효과를 검증한 결과, 치료군에서 칸디다의 장기 내 균 수 감소, 면역 반응 정상화, 그리고 생존율의 유의미한 증가가 관찰됐다.
연구를 주도한 정현정 교수는 “이번 연구는 기존 치료제가 인체 독성과 약제내성 확산 문제를 극복하는 방법을 제시하며, 유전자 치료의 전신 감염 적용 가능성을 보여주는 중요한 전환점”이라며, “향후 임상 적용을 위한 투여 방식 최적화 및 독성 검증 연구를 지속적으로 진행할 계획”이라고 밝혔다.
해당 연구는 생명과학과 정주연 학생 및 서울아산병원 홍윤경 박사가 제1 저자로 참여했으며, 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 7월 1일 자로 게재됐다.
※ 논문명 : Effective treatment of systemic candidiasis by synergistic targeting of cell wall synthesis
※ DOI : 10.1038/s41467-025-60684-7
이번 연구는 보건복지부 및 한국연구재단의 지원을 받아 수행됐다.
부작용·내성 극복한 신개념 칸디다증 치료제 개발
칸디다증은 곰팡이균(진균)의 일종인 칸디다(Candida)가 혈액을 통해 전신으로 퍼지며 장기 손상과 패혈증을 유발할 수 있는 치명적인 감염 질환이다. 최근 면역 저하 치료, 장기 이식, 의료기기 사용 등이 증가함에 따라 칸디다증 발병이 급증하고 있다. 한국 연구진이 기존 항진균제와 달리, 칸디다균에만 선택적으로 작용해 높은 치료 효능과 낮은 부작용을 동시에 갖춘 차세대 치료제를 개발하는데 성공했다.
우리 대학 생명과학과 정현정 교수 연구팀이 서울아산병원 정용필 교수팀과의 협력을 통해, 칸디다 세포벽의 두 핵심 효소를 동시에 저해하는 유전자 기반 나노치료제(FTNx)를 개발했다고 8일 밝혔다.
현재 사용 중인 칸디다의 항진균제들은 표적 선택성이 낮아 인체 세포에도 영향을 미칠 수 있으며, 이에 내성을 가지는 새로운 균의 출현으로 인해 치료 효과가 점차 떨어지고 있다. 특히 면역력이 저하된 환자들에게는 감염의 진행이 빠르고 예후도 좋지 않아, 기존 치료제의 한계를 극복할 수 있는 새로운 치료법의 개발이 시급한 상황이다.
이에 연구팀이 개발한 치료제는 전신 투여가 가능하며, 유전자 억제 기술과 나노소재 기술을 융합함으로써 기존 화합물 기반의 약물들이 가지는 구조적 한계를 효과적으로 극복하고, 칸디다균에만 선택적으로 치료하는데 성공했다.
연구팀은 칸디다라는 곰팡이균의 세포벽을 만드는 데 중요한 두 가지 효소 — β‑1,3‑글루칸 합성효소(FKS1)와 키틴 합성효소(CHS3)를 동시에 표적하는 짧은 DNA 조각(antisense oligonucleotide, ASO)을 탑재한 금 나노입자 기반의 복합체를 제작했다.
여기에 칸디다 세포벽의 특정 당지질 구조(당과 지방이 결합된 구조)와 결합하는 표면 코팅 기술을 적용하여 표적유도장치를 장착함으로써, 인체 세포에는 아예 전달되지 않고 칸디다에만 선택적으로 작용하는 정밀 타겟팅 효과를 구현하는 데 성공했다.
이 복합체는 칸디다 세포 내로 진입한 후, FKS1 및 CHS3의 유전자가 만들어내는 mRNA를 잘라버려서 번역을 억제해 세포벽 성분인 β‑1,3‑글루칸과 키틴의 합성을 동시에 차단한다. 이로 인해 칸디다 세포벽은 구조적 안정성을 유지하지 못하고 붕괴되며, 세균의 생존과 증식이 억제된다.
실제로 쥐에서 전신 칸디다증 모델 실험을 통해 치료 효과를 검증한 결과, 치료군에서 칸디다의 장기 내 균 수 감소, 면역 반응 정상화, 그리고 생존율의 유의미한 증가가 관찰됐다.
연구를 주도한 정현정 교수는 “이번 연구는 기존 치료제가 인체 독성과 약제내성 확산 문제를 극복하는 방법을 제시하며, 유전자 치료의 전신 감염 적용 가능성을 보여주는 중요한 전환점”이라며, “향후 임상 적용을 위한 투여 방식 최적화 및 독성 검증 연구를 지속적으로 진행할 계획”이라고 밝혔다.
해당 연구는 생명과학과 정주연 학생 및 서울아산병원 홍윤경 박사가 제1 저자로 참여했으며, 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 7월 1일 자로 게재됐다.
※ 논문명 : Effective treatment of systemic candidiasis by synergistic targeting of cell wall synthesis
※ DOI : 10.1038/s41467-025-60684-7
이번 연구는 보건복지부 및 한국연구재단의 지원을 받아 수행됐다.
2025.07.08
조회수 779
-
 항암제 내성 없앤다! 당뇨병 등 난치성 질환 치료도 기대
암 치료의 큰 걸림돌 중 하나는 항암제에 대한 암세포의 내성이다. 기존에는 내성 암세포를 제거할 수 있는 새로운 표적을 찾는 방식이 주를 이뤘지만, 오히려 더 강한 내성을 유도할 수 있다는 한계가 있었다. 이에 우리 연구진이 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 자동으로 예측하는 컴퓨터 기반 방법론을 개발했다. 이 기술은 다양한 암 치료뿐 아니라 당뇨병 등 난치성 대사 질환에도 활용될 수 있어 주목된다.
우리 대학 생명화학공학과 김현욱 교수와 김유식 교수 연구팀이 인체 대사를 시뮬레이션할 수 있는 컴퓨터 모델인 대사 네트워크 모델을 활용해, 항암제에 내성을 가진 유방암 세포를 약물에 민감화시킬 수 있는 새로운 약물 표적을 예측하는 컴퓨터 기반 방법론을 개발했다고 7일 밝혔다.
연구진은 암세포의 대사 변형이 약물 내성 형성에 관여하는 주요한 특징으로 주목하고, 항암제 내성 유방암 세포의 대사를 조절해 약물 반응성을 높일 유전자 표적을 예측하는 대사 네트워크 모델 기반 방법론을 개발했다.
연구진은 먼저 독소루비신(doxorubicin)과 파클리탁셀(paclitaxel)에 각각 내성을 지닌 MCF7 유방암 세포주에서 얻은 단백체 데이터를 통합해 세포별 대사 네트워크 모델을 구축했다. 이어 모든 대사 유전자에 대해서 유전자 낙아웃(결실) 시뮬레이션*을 수행하고, 그 결과를 분석했다.
*유전자 낙아웃 시뮬레이션: 특정 유전자를 가상으로 제거한 상태에서 생물학적 네트워크의 변화를 계산적으로 예측하는 방법
그 결과, 특정 유전자의 단백질을 억제하면, 항암제에 잘 듣지 않던 내성 암세포가 다시 항암제에 반응하도록 만들 수 있다는 것을 알아냈다. 독소루비신 내성 세포에서는 GOT1 유전자를, 파클리탁셀 내성 세포에서는 GPI 유전자를 선별했으며, 두 약물 공통으로는 SLC1A5 유전자를 표적으로 선별했다.
예측하여 선별한 유전자를 실제로 억제해 본 결과, 내성 암세포가 항암제에 다시 반응하게 됨을 실험적으로 검증했다.
나아가 같은 항암제에 내성을 갖는 다른 종류의 유방암 세포에서도 같은 유전자를 억제했을 때 항암제에 다시 민감해지는 효과가 일관되게 나타나는 것을 확인할 수 있었다.
김유식 교수는 “세포 대사는 감염병, 퇴행성 질환 등 다양한 난치성 질환에서 중요한 역할을 한다”며, “이번에 개발된 대사 조절 스위치 예측 기술은 약물 내성 유방암 치료를 넘어, 치료제가 없는 다양한 대사 질환에도 적용될 수 있는 기반 기술이 될 것”이라고 말했다.
연구를 총괄한 김현욱 교수는 “이번 연구의 가장 큰 의의는 컴퓨터 시뮬레이션만과 최소한의 실험 데이터만으로 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 정밀하게 예측할 수 있다는 점”이라며, “이 방법론은 다양한 암종과 대사 관련 난치성 질환의 새로운 치료 표적 발굴에도 폭넓게 활용될 수 있을 것”이라고 강조했다.
우리 대학 생명화학공학과 임진아 박사과정생과 정해덕 박사과정생이 공동 제1 저자로 참여한 이번 연구는 생명과학·물리·공학·사회과학 등 다양한 분야의 최고 수준 연구를 다루는 다학제 국제 학술지인 미국국립과학원회보(PNAS) 6월 25일 자 온라인에 게재됐다.
※ 논문명 : Genome-scale knockout simulation and clustering analysis of drug-resistant breast cancer cells reveal drug sensitization targets
※ 저자 정보 : 임진아(한국과학기술원, 공동 제1 저자), 정해덕(한국과학기술원, 공동 제1 저자), 유한석(서울대학교병원, 교신저자), 김유식(한국과학기술원, 교신저자), 김현욱(한국과학기술원, 교신저자) 포함 총 10명
※ DOI: https://doi.org/10.1073/pnas.2425384122
이번 연구는 과학기술정보통신부 한국전자통신연구원 및 한국연구재단의 지원을 받아 수행됐다.
항암제 내성 없앤다! 당뇨병 등 난치성 질환 치료도 기대
암 치료의 큰 걸림돌 중 하나는 항암제에 대한 암세포의 내성이다. 기존에는 내성 암세포를 제거할 수 있는 새로운 표적을 찾는 방식이 주를 이뤘지만, 오히려 더 강한 내성을 유도할 수 있다는 한계가 있었다. 이에 우리 연구진이 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 자동으로 예측하는 컴퓨터 기반 방법론을 개발했다. 이 기술은 다양한 암 치료뿐 아니라 당뇨병 등 난치성 대사 질환에도 활용될 수 있어 주목된다.
우리 대학 생명화학공학과 김현욱 교수와 김유식 교수 연구팀이 인체 대사를 시뮬레이션할 수 있는 컴퓨터 모델인 대사 네트워크 모델을 활용해, 항암제에 내성을 가진 유방암 세포를 약물에 민감화시킬 수 있는 새로운 약물 표적을 예측하는 컴퓨터 기반 방법론을 개발했다고 7일 밝혔다.
연구진은 암세포의 대사 변형이 약물 내성 형성에 관여하는 주요한 특징으로 주목하고, 항암제 내성 유방암 세포의 대사를 조절해 약물 반응성을 높일 유전자 표적을 예측하는 대사 네트워크 모델 기반 방법론을 개발했다.
연구진은 먼저 독소루비신(doxorubicin)과 파클리탁셀(paclitaxel)에 각각 내성을 지닌 MCF7 유방암 세포주에서 얻은 단백체 데이터를 통합해 세포별 대사 네트워크 모델을 구축했다. 이어 모든 대사 유전자에 대해서 유전자 낙아웃(결실) 시뮬레이션*을 수행하고, 그 결과를 분석했다.
*유전자 낙아웃 시뮬레이션: 특정 유전자를 가상으로 제거한 상태에서 생물학적 네트워크의 변화를 계산적으로 예측하는 방법
그 결과, 특정 유전자의 단백질을 억제하면, 항암제에 잘 듣지 않던 내성 암세포가 다시 항암제에 반응하도록 만들 수 있다는 것을 알아냈다. 독소루비신 내성 세포에서는 GOT1 유전자를, 파클리탁셀 내성 세포에서는 GPI 유전자를 선별했으며, 두 약물 공통으로는 SLC1A5 유전자를 표적으로 선별했다.
예측하여 선별한 유전자를 실제로 억제해 본 결과, 내성 암세포가 항암제에 다시 반응하게 됨을 실험적으로 검증했다.
나아가 같은 항암제에 내성을 갖는 다른 종류의 유방암 세포에서도 같은 유전자를 억제했을 때 항암제에 다시 민감해지는 효과가 일관되게 나타나는 것을 확인할 수 있었다.
김유식 교수는 “세포 대사는 감염병, 퇴행성 질환 등 다양한 난치성 질환에서 중요한 역할을 한다”며, “이번에 개발된 대사 조절 스위치 예측 기술은 약물 내성 유방암 치료를 넘어, 치료제가 없는 다양한 대사 질환에도 적용될 수 있는 기반 기술이 될 것”이라고 말했다.
연구를 총괄한 김현욱 교수는 “이번 연구의 가장 큰 의의는 컴퓨터 시뮬레이션만과 최소한의 실험 데이터만으로 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 정밀하게 예측할 수 있다는 점”이라며, “이 방법론은 다양한 암종과 대사 관련 난치성 질환의 새로운 치료 표적 발굴에도 폭넓게 활용될 수 있을 것”이라고 강조했다.
우리 대학 생명화학공학과 임진아 박사과정생과 정해덕 박사과정생이 공동 제1 저자로 참여한 이번 연구는 생명과학·물리·공학·사회과학 등 다양한 분야의 최고 수준 연구를 다루는 다학제 국제 학술지인 미국국립과학원회보(PNAS) 6월 25일 자 온라인에 게재됐다.
※ 논문명 : Genome-scale knockout simulation and clustering analysis of drug-resistant breast cancer cells reveal drug sensitization targets
※ 저자 정보 : 임진아(한국과학기술원, 공동 제1 저자), 정해덕(한국과학기술원, 공동 제1 저자), 유한석(서울대학교병원, 교신저자), 김유식(한국과학기술원, 교신저자), 김현욱(한국과학기술원, 교신저자) 포함 총 10명
※ DOI: https://doi.org/10.1073/pnas.2425384122
이번 연구는 과학기술정보통신부 한국전자통신연구원 및 한국연구재단의 지원을 받아 수행됐다.
2025.07.07
조회수 663
-
 마이크로 OLED로 난치성 뇌질환 치료 '게임 체인저' 기술 제시
광유전학 기술은 빛에 반응하는 광 단백질이 발현된 뉴런에 특정 파장의 빛 자극을 통해 뉴런의 활성을 조절하는 기술로 다양한 뇌질환의 원인을 규명하며 난치성 뇌질환의 새로운 치료 방법을 개발할 가능성을 열고 있다. 이 기술은 인체의 뇌에 삽입하여 자극을 주는 의료 기기인 ‘뉴럴 프로브’를 통해 정확하게 자극하고 무른 뇌 조직의 손상을 최소화해야 한다. 이에 우리 연구진이 마이크로 OLED를 활용해 얇고 유연한 인체 삽입형 의료기기로 구현함으로써 뉴럴 프로브의 새로운 패러다임을 제시했다.
우리 대학 전기및전자공학부 최경철 교수와 이현주 연구팀이 공동 연구를 통해, 유연한 마이크로 OLED가 집적된 광유전학용 뉴럴 프로브 개발에 성공했다고 6일 밝혔다.
광유전학 연구에서 주요 기술은 광원의 빛을 뇌로 전달하는 방식으로 외부 광원으로부터의 깊은 뇌 영역까지 빛을 전달하기 위해 수십 년간 광섬유를 사용해 왔다. 하지만 단일 뉴런을 자극하기 위한 유연 광섬유, 초미세 광원 집적 뉴럴 프로브 등 관련 연구가 이뤄지고 있다.
연구팀은 마이크로 OLED는 높은 공간적 해상도와 유연성을 가져, 매우 작은 영역의 뉴런에서도 정확하게 빛을 조사할 수 있어 세밀한 뇌 회로 분석이 가능하고 동물의 움직임에 불편함을 주지 않으면서 부작용을 최소화하는 장점에 주목했다. 그뿐만 아니라, 미세한 파장 조절을 통해 정밀한 빛 조절이 가능하며 다중 자극을 통한 복잡한 뇌 기능 연구가 가능하다.
하지만, 체내 수분이나 물에 의해 전기적 특성이 쉽게 열화되기 때문에 생체 삽입형 전자장치로 활용되는데 한계가 있었고, 얇고 유연한 탐침 위 고해상도 집적 공정에 대한 세부적인 최적화도 필요했다.
공동연구팀은 수분과 산소가 많은 생체 내 환경에서 OLED의 구동 신뢰성을 높이며 생체 삽입 시 조직 손상을 최소화하고자, 산화알루미늄/파릴렌-C(Al2O3/parylene-C)로 구성된 초박막 유연 봉지막*을 얇은 탐침 형태인 260~600마이크로미터(μm) 너비로 패터닝해 생체친화성을 유지했다.
* 봉지막: 소자를 외부 환경요인인 산소와 물 분자로부터 완전히 차단하는 막 기술로 소자의 수명을 유지시키고 신뢰성을 줌
또한, 고해상도 마이크로 OLED를 집적함에 있어 전체 소자의 유연성과 생체친화성을 유지하기 위해, 봉지막과 동일한 생체친화 재료인 파릴렌-C(parylene-C)를 활용하였다. 아울러, 인접한 OLED 픽셀 간 전기적 간섭 현상을 제거하고 각 픽셀을 공간적으로 분리하기 위해 구조적 레이어인 ‘화소 정의막(pixel define layer)’을 도입함으로써, 8개의 마이크로 OLED를 독립적으로 개별 구동할 수 있도록 구현했다.
마지막으로, 소자 내 다중 박막층의 잔류 응력과 두께를 정밀하게 조절함으로써, 생체 내 환경에서도 소자의 유연성을 유지할 수 있도록 하였다. 이를 통해 외부 셔틀이나 바늘과 같은 보조 장치 없이도 단일 탐침만으로 휘어짐 없이 삽입이 가능하도록, 소자의 기계적 스트레스를 최적화해 설계했다.
결론적으로 연구팀은 채널로돕신2의 활성화에 적합한 470나노미터(nm) 파장에서 1밀리와트/제곱밀리미터(mW/mm2)이상의 광 파워 밀도를 가지는 즉, 광유전학 및 생체조직 자극 응용에서 상당히 높은 수준의 광출력을 가진 마이크로 OLED 집적 유연 뉴럴 프로브를 개발했다.
또한, 초박막 유연 봉지막은 2.66×10⁻⁵ g/m²/day의 낮은 수분 투습률을 보이며 소자 수명은 10년 이상 유지할 수 있고, 패릴렌-C(parylene-C)를 기반으로 생체 내 높은 봉지막 성능을 발휘하며, 전기적 간섭과 휨 이슈 없이 집적된 OLED의 개별 구동을 성공적으로 시연했다.
이번 연구를 주도한 최경철 교수 연구팀의 이소민 박사는 “고유연·고해상도의 마이크로 OLED를 얇은 유연 탐침 위에 집적하는 세부 공정 및 생체 적용성, 친화성 향상에 집중했다”며 “이번 연구는 기존 연구를 넘어 유연 프로브 형태에 최초로 개발해 보고된 사례로, 유연 OLED가 인체 삽입형 측정 및 치료 의료기기로서의 새로운 패러다임을 제시할 것으로 기대된다”고 말했다.
이번 연구는 전기및전자공학부 이소민 박사가 제1 저자로 나노 분야의 권위 있는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials, IF 18.5)'에 지난 3월 26일 字로 온라인 게재됐으며, 전면 표지 논문으로 이번 7월에 선정됐다.
※ 논문명: Advanced Micro-OLED Integration on Thin and Flexible Polymer Neural Probes for Targeted Optogenetic Stimulation
※ DOI: https://doi.org/10.1002/adfm.202420758
한편, 이번 연구는 과학기술정보통신부 한국연구재단의 전자약 기술개발사업(연구 과제명: 뇌인지-정서 향상 빛 자극 전자약의 핵심원천기술 개발 및 생체 적용가능성 검증)의 지원을 받아 수행됐다.
마이크로 OLED로 난치성 뇌질환 치료 '게임 체인저' 기술 제시
광유전학 기술은 빛에 반응하는 광 단백질이 발현된 뉴런에 특정 파장의 빛 자극을 통해 뉴런의 활성을 조절하는 기술로 다양한 뇌질환의 원인을 규명하며 난치성 뇌질환의 새로운 치료 방법을 개발할 가능성을 열고 있다. 이 기술은 인체의 뇌에 삽입하여 자극을 주는 의료 기기인 ‘뉴럴 프로브’를 통해 정확하게 자극하고 무른 뇌 조직의 손상을 최소화해야 한다. 이에 우리 연구진이 마이크로 OLED를 활용해 얇고 유연한 인체 삽입형 의료기기로 구현함으로써 뉴럴 프로브의 새로운 패러다임을 제시했다.
우리 대학 전기및전자공학부 최경철 교수와 이현주 연구팀이 공동 연구를 통해, 유연한 마이크로 OLED가 집적된 광유전학용 뉴럴 프로브 개발에 성공했다고 6일 밝혔다.
광유전학 연구에서 주요 기술은 광원의 빛을 뇌로 전달하는 방식으로 외부 광원으로부터의 깊은 뇌 영역까지 빛을 전달하기 위해 수십 년간 광섬유를 사용해 왔다. 하지만 단일 뉴런을 자극하기 위한 유연 광섬유, 초미세 광원 집적 뉴럴 프로브 등 관련 연구가 이뤄지고 있다.
연구팀은 마이크로 OLED는 높은 공간적 해상도와 유연성을 가져, 매우 작은 영역의 뉴런에서도 정확하게 빛을 조사할 수 있어 세밀한 뇌 회로 분석이 가능하고 동물의 움직임에 불편함을 주지 않으면서 부작용을 최소화하는 장점에 주목했다. 그뿐만 아니라, 미세한 파장 조절을 통해 정밀한 빛 조절이 가능하며 다중 자극을 통한 복잡한 뇌 기능 연구가 가능하다.
하지만, 체내 수분이나 물에 의해 전기적 특성이 쉽게 열화되기 때문에 생체 삽입형 전자장치로 활용되는데 한계가 있었고, 얇고 유연한 탐침 위 고해상도 집적 공정에 대한 세부적인 최적화도 필요했다.
공동연구팀은 수분과 산소가 많은 생체 내 환경에서 OLED의 구동 신뢰성을 높이며 생체 삽입 시 조직 손상을 최소화하고자, 산화알루미늄/파릴렌-C(Al2O3/parylene-C)로 구성된 초박막 유연 봉지막*을 얇은 탐침 형태인 260~600마이크로미터(μm) 너비로 패터닝해 생체친화성을 유지했다.
* 봉지막: 소자를 외부 환경요인인 산소와 물 분자로부터 완전히 차단하는 막 기술로 소자의 수명을 유지시키고 신뢰성을 줌
또한, 고해상도 마이크로 OLED를 집적함에 있어 전체 소자의 유연성과 생체친화성을 유지하기 위해, 봉지막과 동일한 생체친화 재료인 파릴렌-C(parylene-C)를 활용하였다. 아울러, 인접한 OLED 픽셀 간 전기적 간섭 현상을 제거하고 각 픽셀을 공간적으로 분리하기 위해 구조적 레이어인 ‘화소 정의막(pixel define layer)’을 도입함으로써, 8개의 마이크로 OLED를 독립적으로 개별 구동할 수 있도록 구현했다.
마지막으로, 소자 내 다중 박막층의 잔류 응력과 두께를 정밀하게 조절함으로써, 생체 내 환경에서도 소자의 유연성을 유지할 수 있도록 하였다. 이를 통해 외부 셔틀이나 바늘과 같은 보조 장치 없이도 단일 탐침만으로 휘어짐 없이 삽입이 가능하도록, 소자의 기계적 스트레스를 최적화해 설계했다.
결론적으로 연구팀은 채널로돕신2의 활성화에 적합한 470나노미터(nm) 파장에서 1밀리와트/제곱밀리미터(mW/mm2)이상의 광 파워 밀도를 가지는 즉, 광유전학 및 생체조직 자극 응용에서 상당히 높은 수준의 광출력을 가진 마이크로 OLED 집적 유연 뉴럴 프로브를 개발했다.
또한, 초박막 유연 봉지막은 2.66×10⁻⁵ g/m²/day의 낮은 수분 투습률을 보이며 소자 수명은 10년 이상 유지할 수 있고, 패릴렌-C(parylene-C)를 기반으로 생체 내 높은 봉지막 성능을 발휘하며, 전기적 간섭과 휨 이슈 없이 집적된 OLED의 개별 구동을 성공적으로 시연했다.
이번 연구를 주도한 최경철 교수 연구팀의 이소민 박사는 “고유연·고해상도의 마이크로 OLED를 얇은 유연 탐침 위에 집적하는 세부 공정 및 생체 적용성, 친화성 향상에 집중했다”며 “이번 연구는 기존 연구를 넘어 유연 프로브 형태에 최초로 개발해 보고된 사례로, 유연 OLED가 인체 삽입형 측정 및 치료 의료기기로서의 새로운 패러다임을 제시할 것으로 기대된다”고 말했다.
이번 연구는 전기및전자공학부 이소민 박사가 제1 저자로 나노 분야의 권위 있는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials, IF 18.5)'에 지난 3월 26일 字로 온라인 게재됐으며, 전면 표지 논문으로 이번 7월에 선정됐다.
※ 논문명: Advanced Micro-OLED Integration on Thin and Flexible Polymer Neural Probes for Targeted Optogenetic Stimulation
※ DOI: https://doi.org/10.1002/adfm.202420758
한편, 이번 연구는 과학기술정보통신부 한국연구재단의 전자약 기술개발사업(연구 과제명: 뇌인지-정서 향상 빛 자극 전자약의 핵심원천기술 개발 및 생체 적용가능성 검증)의 지원을 받아 수행됐다.
2025.07.07
조회수 534
-
 60% 이상 챗GPT 추론 성능 향상할 NPU 핵심기술 개발
오픈AI 챗GPT4, 구글 Gemnini 2.5 등 최신 생성형AI 모델들은 높은 메모리 대역폭(Bandwidth) 뿐만 아니라 많은 메모리 용량(Capacity)를 필요로 한다. 마이크로소프트, 구글 등 생성형AI 클라우드 운영 기업들이 엔비디아 GPU를 수십만 장씩 구매하는 이유다. 이런 고성능 AI 인프라 구축의 핵심 난제를 해소할 방안으로, 한국 연구진이 최신 GPU 대비 약 44% 낮은 전력 소모에도 평균 60% 이상 생성형 AI 모델의 추론 성능을 향상할 NPU(신경망처리장치)* 핵심 기술을 개발하는데 성공했다.
*NPU(Neural Processing Unit): 인공신경망(Neural Network)을 빠르게 처리하기 위해 만든 AI 전용 반도체 칩
우리 대학 전산학부 박종세 교수 연구팀과 (주)하이퍼엑셀(전기및전자공학부 김주영 교수 창업기업)이 연구 협력을 통해, 챗GPT와 같은 생성형AI 클라우드에 특화된 고성능·저전력의 NPU(신경망처리장치) 핵심기술을 개발했다고 4일 밝혔다.
연구팀이 제안한 기술은 컴퓨터 아키텍처 분야에서 최고 권위를 자랑하는 국제 학회인 ‘2025 국제 컴퓨터구조 심포지엄(International Symposium on Computer Architecture, ISCA 2025)’에 채택됐다.
이번 연구의 핵심은 추론 과정에서 경량화를 통해 정확도 손실을 최소화하면서도 메모리 병목 문제를 해결해 대규모 생성형AI 서비스의 성능을 개선하는 것이다. 이번 연구는 AI인프라의 핵심 구성요소인 AI반도체와 AI시스템SW를 통합 설계했다는 점에서 그 가치를 높게 인정받았다.
기존 GPU 기반 AI 인프라는 높은 메모리 대역폭과 메모리 용량 요구를 충족하기 위해 다수의 GPU 디바이스가 필요한 반면, 이번 기술은 메모리 사용의 대부분을 차지하는 KV 캐시의 양자화*를 통해 적은 수의 NPU 디바이스만으로 동일 수준의 AI 인프라를 구성할 수 있어, 생성형 AI 클라우드 구축 비용을 크게 절감할 수 있다.
*KV 캐시(Key-Value Cache)의 양자화: 생성형 AI 모델을 작동할 때 성능을 높이기 위해 사용하는 일종의 임시 저장 공간에 데이터 크기를 줄이는 것을 의미(32비트로 저장된 수를 4비트로 바꾸면, 데이터 크기는 1/8로 줄어듬)
연구팀은 기존 NPU 아키텍처의 연산 로직을 변경하지 않으면서 메모리 인터페이스와 통합될 수 있도록 설계했다. 이번 하드웨어 아키텍처 기술은 제안된 양자화 알고리즘을 구현할 뿐만 아니라, 제한된 메모리 대역폭 및 용량을 효율적으로 활용하기 위한 페이지 단위 메모리 관리 기법*과 양자화된 KV 캐시에 최적화된 새로운 인코딩 기법 등을 개발했다.
*페이지 단위 메모리 관리 기법: CPU처럼 메모리 주소를 가상화하여 NPU 내부에서 일관된 방식으로 접근할 수 있게 함
또한, 최신 GPU 대비 비용·전력 효율성이 우수한 NPU 기반 AI 클라우드를 구성할 경우, NPU의 고성능, 저전력 특성을 활용해 운영 비용 역시 크게 절감할 수 있을 것으로 기대된다.
박종세 교수는 “이 연구는 (주)하이퍼엑셀과의 공동연구를 통해 생성형AI 추론 경량화 알고리즘에서 그 해법을 찾았고 ‘메모리 문제’를 해결할 수 있는 NPU 핵심기술 개발에 성공했다. 이 기술을 통해 추론의 정확도를 유지하면서 메모리 요구량을 줄이는 경량화 기법과, 이에 최적화된 하드웨어 설계를 결합해 최신 GPU 대비 평균 60% 이상 성능이 향상된 NPU를 구현했다” 고 말했다.
이어 “이 기술은 생성형AI에 특화된 고성능·저전력 인프라 구현 가능성을 입증했으며, AI클라우드 데이터센터뿐 아니라 능동적인 실행형 AI인 ‘에이전틱 AI ’등으로 대표되는 AI 대전환(AX) 환경에서도 핵심 역할이 기대된다”고 강조했다.
이 연구는 김민수 박사과정 학생과 ㈜하이퍼엑셀 홍성민 박사가 공동 제1 저자로 지난 6월 21일부터 6월 25일까지 일본 도쿄에서 열린 ‘2025 국제 컴퓨터구조 심포지엄(ISCA)’에 발표됐다. 국제적 저명학회인 ISCA는 올해는 570편의 논문이 제출됐으며 그중 127편 만이 채택됐다. (채택률 22.7%).
※논문 제목: Oaken: Fast and Efficient LLM Serving with Online-Offline Hybrid KV Cache Quantization
※DOI: https://doi.org/10.1145/3695053.3731019
한편 이번 연구는 한국연구재단 우수신진연구자지원사업, 정보통신기획평가원(IITP), 인공지능반도체대학원지원사업의 지원을 받아 수행됐다.
60% 이상 챗GPT 추론 성능 향상할 NPU 핵심기술 개발
오픈AI 챗GPT4, 구글 Gemnini 2.5 등 최신 생성형AI 모델들은 높은 메모리 대역폭(Bandwidth) 뿐만 아니라 많은 메모리 용량(Capacity)를 필요로 한다. 마이크로소프트, 구글 등 생성형AI 클라우드 운영 기업들이 엔비디아 GPU를 수십만 장씩 구매하는 이유다. 이런 고성능 AI 인프라 구축의 핵심 난제를 해소할 방안으로, 한국 연구진이 최신 GPU 대비 약 44% 낮은 전력 소모에도 평균 60% 이상 생성형 AI 모델의 추론 성능을 향상할 NPU(신경망처리장치)* 핵심 기술을 개발하는데 성공했다.
*NPU(Neural Processing Unit): 인공신경망(Neural Network)을 빠르게 처리하기 위해 만든 AI 전용 반도체 칩
우리 대학 전산학부 박종세 교수 연구팀과 (주)하이퍼엑셀(전기및전자공학부 김주영 교수 창업기업)이 연구 협력을 통해, 챗GPT와 같은 생성형AI 클라우드에 특화된 고성능·저전력의 NPU(신경망처리장치) 핵심기술을 개발했다고 4일 밝혔다.
연구팀이 제안한 기술은 컴퓨터 아키텍처 분야에서 최고 권위를 자랑하는 국제 학회인 ‘2025 국제 컴퓨터구조 심포지엄(International Symposium on Computer Architecture, ISCA 2025)’에 채택됐다.
이번 연구의 핵심은 추론 과정에서 경량화를 통해 정확도 손실을 최소화하면서도 메모리 병목 문제를 해결해 대규모 생성형AI 서비스의 성능을 개선하는 것이다. 이번 연구는 AI인프라의 핵심 구성요소인 AI반도체와 AI시스템SW를 통합 설계했다는 점에서 그 가치를 높게 인정받았다.
기존 GPU 기반 AI 인프라는 높은 메모리 대역폭과 메모리 용량 요구를 충족하기 위해 다수의 GPU 디바이스가 필요한 반면, 이번 기술은 메모리 사용의 대부분을 차지하는 KV 캐시의 양자화*를 통해 적은 수의 NPU 디바이스만으로 동일 수준의 AI 인프라를 구성할 수 있어, 생성형 AI 클라우드 구축 비용을 크게 절감할 수 있다.
*KV 캐시(Key-Value Cache)의 양자화: 생성형 AI 모델을 작동할 때 성능을 높이기 위해 사용하는 일종의 임시 저장 공간에 데이터 크기를 줄이는 것을 의미(32비트로 저장된 수를 4비트로 바꾸면, 데이터 크기는 1/8로 줄어듬)
연구팀은 기존 NPU 아키텍처의 연산 로직을 변경하지 않으면서 메모리 인터페이스와 통합될 수 있도록 설계했다. 이번 하드웨어 아키텍처 기술은 제안된 양자화 알고리즘을 구현할 뿐만 아니라, 제한된 메모리 대역폭 및 용량을 효율적으로 활용하기 위한 페이지 단위 메모리 관리 기법*과 양자화된 KV 캐시에 최적화된 새로운 인코딩 기법 등을 개발했다.
*페이지 단위 메모리 관리 기법: CPU처럼 메모리 주소를 가상화하여 NPU 내부에서 일관된 방식으로 접근할 수 있게 함
또한, 최신 GPU 대비 비용·전력 효율성이 우수한 NPU 기반 AI 클라우드를 구성할 경우, NPU의 고성능, 저전력 특성을 활용해 운영 비용 역시 크게 절감할 수 있을 것으로 기대된다.
박종세 교수는 “이 연구는 (주)하이퍼엑셀과의 공동연구를 통해 생성형AI 추론 경량화 알고리즘에서 그 해법을 찾았고 ‘메모리 문제’를 해결할 수 있는 NPU 핵심기술 개발에 성공했다. 이 기술을 통해 추론의 정확도를 유지하면서 메모리 요구량을 줄이는 경량화 기법과, 이에 최적화된 하드웨어 설계를 결합해 최신 GPU 대비 평균 60% 이상 성능이 향상된 NPU를 구현했다” 고 말했다.
이어 “이 기술은 생성형AI에 특화된 고성능·저전력 인프라 구현 가능성을 입증했으며, AI클라우드 데이터센터뿐 아니라 능동적인 실행형 AI인 ‘에이전틱 AI ’등으로 대표되는 AI 대전환(AX) 환경에서도 핵심 역할이 기대된다”고 강조했다.
이 연구는 김민수 박사과정 학생과 ㈜하이퍼엑셀 홍성민 박사가 공동 제1 저자로 지난 6월 21일부터 6월 25일까지 일본 도쿄에서 열린 ‘2025 국제 컴퓨터구조 심포지엄(ISCA)’에 발표됐다. 국제적 저명학회인 ISCA는 올해는 570편의 논문이 제출됐으며 그중 127편 만이 채택됐다. (채택률 22.7%).
※논문 제목: Oaken: Fast and Efficient LLM Serving with Online-Offline Hybrid KV Cache Quantization
※DOI: https://doi.org/10.1145/3695053.3731019
한편 이번 연구는 한국연구재단 우수신진연구자지원사업, 정보통신기획평가원(IITP), 인공지능반도체대학원지원사업의 지원을 받아 수행됐다.
2025.07.04
조회수 927
-
 정확도·효율성 높인 생명과학 데이터 분석 도구 'scICE' 개발
기존보다 최대 30배 빠른 속도로 안정적인 결과만을 자동으로 선별하여 대규모 생명과학 데이터 분석의 정확도와 효율성을 획기적으로 향상하는 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀은 세포 분류(클러스터링) 결과의 안정성을 수학적으로 평가해 불안정한 결과를 걸러내는 새로운 분석 도구인 ‘scICE(single-cell Inconsistency Clustering Estimator)’를 개발했다.
단일세포 수준에서 유전자 발현을 분석하는 기술인 단일세포 전사체 분석법(scRNA-seq)은 현대 생명과학 연구의 핵심 도구로 자리 잡았다. 이 과정에서 클러스터링은 유사한 유전자 발현 특성을 가진 세포들을 그룹으로 묶는 작업으로, 암세포와 정상 세포를 구분하거나 새로운 세포 유형을 발견하는 데 중요한 첫걸음이다. 하지만 클러스터링 알고리즘은 무작위로 세포를 분류해 같은 데이터를 분석해도 결과가 달라지는 경우가 많다.
제1 저자인 김현 선임연구원은 “일부 정상 세포가 암세포로 잘못 분류되거나 중요한 세포 유형이 누락되는 불안정성으로 인해 연구자들은 다시 분석하거나 복잡한 계산을 통해 신뢰도가 높은 결과를 선별해야 했다”며, “기존 방법들은 분석을 여러 번 반복해 합의된 결과를 도출하는 방식으로, 계산량이 방대하고 수만 개 이상의 세포가 포함된 대용량 데이터에는 적합하지 않다”고 말했다.
연구팀이 개발한 scICE는 한 번의 분석만으로도 얼마나 일관성 있게 결과가 도출됐는지를 수학적으로 평가한다. 새로 도입한 ‘불일치 계수(Inconsistency Coefficient, IC)’를 통해 많은 계산량이 요구되는 연산 없이도 클러스터 간 안정성을 정량적으로 판단할 수 있다. 모든 세포를 일일이 비교하던 기존 방식과 달리, 불일치 계수를 활용한 안정성 평가는 클러스터 구조 간 유사성만 평가해 비교 대상을 획기적으로 줄일 수 있어 분석 시간을 크게 단축한다.
연구팀은 뇌, 폐, 혈액 등 다양한 조직에서 수집된 48개의 실제 및 모의 scRNA-seq 데이터에 scICE를 적용하여 그 유효성을 입증했다. 그 결과, 기존 분석 결과 중 약 3분의 2는 통계적으로 불안정하며 신뢰하기 어렵다는 사실을 밝혀냈다. 반면, scICE는 신뢰할 수 있는 결과만을 선별해 연구자의 시간과 계산 자원을 절약하면서도 정확도를 한층 높였다.
또한, scICE는 일반적인 클러스터링으로는 놓치기 쉬운 희귀한 세포 유형을 효과적으로 탐지했다. 실제로 일부 데이터에서 찾기 어려웠던 희귀 면역세포들을 scICE 기반의 서브클러스터링을 통해 안정적으로 식별해냈다. 예를 들어, 매우 복잡한 분석을 거쳐야만 식별할 수 있던 여러 대식세포(macrophage) 아형들을 훨씬 간편하고 정확하게 구분해냈다.
scICE에 관심 있는 연구자는 누구나 깃허브 사이트(https://github.com/Mathbiomed/scICE)를 통해 쉽게 활용해볼 수 있다.
김재경 교수는 “이번 연구는 수학적 아이디어가 어떻게 생명과학의 핵심 문제를 해결하고 분석 과정을 혁신할 수 있는지를 보여주는 성과”라며, “클러스터링 신뢰도의 중요성이 간과되어 온 측면이 있는데, 이번 기회로 scICE가 생명과학 분야에서 신뢰도 높은 데이터 해석을 가능케 하는 표준 도구로 자리 잡기를 기대한다”고 전했다.
우리 대학 박종은 교수 연구팀, POSTECH 김종경 교수 연구팀, 고려대 서민석 교수 연구팀과 공동으로 참여한 이번 연구결과는 세계적인 국제학술지 네이처 커뮤니케이션즈(Nature Communications, IF 14.7)에 7월 2일 온라인 게재됐다.
정확도·효율성 높인 생명과학 데이터 분석 도구 'scICE' 개발
기존보다 최대 30배 빠른 속도로 안정적인 결과만을 자동으로 선별하여 대규모 생명과학 데이터 분석의 정확도와 효율성을 획기적으로 향상하는 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀은 세포 분류(클러스터링) 결과의 안정성을 수학적으로 평가해 불안정한 결과를 걸러내는 새로운 분석 도구인 ‘scICE(single-cell Inconsistency Clustering Estimator)’를 개발했다.
단일세포 수준에서 유전자 발현을 분석하는 기술인 단일세포 전사체 분석법(scRNA-seq)은 현대 생명과학 연구의 핵심 도구로 자리 잡았다. 이 과정에서 클러스터링은 유사한 유전자 발현 특성을 가진 세포들을 그룹으로 묶는 작업으로, 암세포와 정상 세포를 구분하거나 새로운 세포 유형을 발견하는 데 중요한 첫걸음이다. 하지만 클러스터링 알고리즘은 무작위로 세포를 분류해 같은 데이터를 분석해도 결과가 달라지는 경우가 많다.
제1 저자인 김현 선임연구원은 “일부 정상 세포가 암세포로 잘못 분류되거나 중요한 세포 유형이 누락되는 불안정성으로 인해 연구자들은 다시 분석하거나 복잡한 계산을 통해 신뢰도가 높은 결과를 선별해야 했다”며, “기존 방법들은 분석을 여러 번 반복해 합의된 결과를 도출하는 방식으로, 계산량이 방대하고 수만 개 이상의 세포가 포함된 대용량 데이터에는 적합하지 않다”고 말했다.
연구팀이 개발한 scICE는 한 번의 분석만으로도 얼마나 일관성 있게 결과가 도출됐는지를 수학적으로 평가한다. 새로 도입한 ‘불일치 계수(Inconsistency Coefficient, IC)’를 통해 많은 계산량이 요구되는 연산 없이도 클러스터 간 안정성을 정량적으로 판단할 수 있다. 모든 세포를 일일이 비교하던 기존 방식과 달리, 불일치 계수를 활용한 안정성 평가는 클러스터 구조 간 유사성만 평가해 비교 대상을 획기적으로 줄일 수 있어 분석 시간을 크게 단축한다.
연구팀은 뇌, 폐, 혈액 등 다양한 조직에서 수집된 48개의 실제 및 모의 scRNA-seq 데이터에 scICE를 적용하여 그 유효성을 입증했다. 그 결과, 기존 분석 결과 중 약 3분의 2는 통계적으로 불안정하며 신뢰하기 어렵다는 사실을 밝혀냈다. 반면, scICE는 신뢰할 수 있는 결과만을 선별해 연구자의 시간과 계산 자원을 절약하면서도 정확도를 한층 높였다.
또한, scICE는 일반적인 클러스터링으로는 놓치기 쉬운 희귀한 세포 유형을 효과적으로 탐지했다. 실제로 일부 데이터에서 찾기 어려웠던 희귀 면역세포들을 scICE 기반의 서브클러스터링을 통해 안정적으로 식별해냈다. 예를 들어, 매우 복잡한 분석을 거쳐야만 식별할 수 있던 여러 대식세포(macrophage) 아형들을 훨씬 간편하고 정확하게 구분해냈다.
scICE에 관심 있는 연구자는 누구나 깃허브 사이트(https://github.com/Mathbiomed/scICE)를 통해 쉽게 활용해볼 수 있다.
김재경 교수는 “이번 연구는 수학적 아이디어가 어떻게 생명과학의 핵심 문제를 해결하고 분석 과정을 혁신할 수 있는지를 보여주는 성과”라며, “클러스터링 신뢰도의 중요성이 간과되어 온 측면이 있는데, 이번 기회로 scICE가 생명과학 분야에서 신뢰도 높은 데이터 해석을 가능케 하는 표준 도구로 자리 잡기를 기대한다”고 전했다.
우리 대학 박종은 교수 연구팀, POSTECH 김종경 교수 연구팀, 고려대 서민석 교수 연구팀과 공동으로 참여한 이번 연구결과는 세계적인 국제학술지 네이처 커뮤니케이션즈(Nature Communications, IF 14.7)에 7월 2일 온라인 게재됐다.
2025.07.03
조회수 846
-
 24시간 말하는 AI비서 가능성 여는 '스피치SSM' 개발
최근 음성 언어 모델(Spoken Language Model, SLM)은 텍스트 없이 인간의 음성을 학습해 음성의 언어적, 비언어적 정보를 이해 및 생성하는 기술로 텍스트 기반 언어 모델의 한계를 넘어서는 차세대 기술로 각광받고 있다. 하지만 기존 모델은 장시간 콘텐츠 생성이 요구되는 팟캐스트, 오디오북, 음성비서 등에서 한계가 두드러졌는데, 우리 연구진이 이런 한계를 뛰어넘어, 시간 제약 없이 일관되고 자연스러운 음성 생성을 실현한 ‘스피치SSM’을 개발하는데 성공했다.
우리 대학 전기및전자공학부 노용만 교수 연구팀의 박세진 연구원(박사과정)이 장시간 음성 생성이 가능한 음성 언어 모델 ‘스피치SSM(SpeechSSM)’을 개발했다고 3일 밝혔다.
이번 연구는 국제 최고 권위 머신러닝 학회인 ICML(International Conference on Machine Learning) 2025에 전체 제출된 논문 중 약 1%만이 선정되는 구두 논문 발표에 확정돼 뛰어난 연구 역량을 입증할 뿐만 아니라 우리 대학의 인공지능 연구 능력이 세계 최고 수준임을 다시 한번 보여주는 계기가 될 전망이다.
음성 언어 모델(SLM)은 중간에 텍스트로 변환하지 않고 음성을 직접 처리함으로써, 인간 화자 고유의 음향적 특성을 활용할 수 있어 대규모 모델에서도 고품질의 음성을 빠르게 생성할 수 있다는 점이 큰 강점이다.
그러나 기존 모델은 음성을 아주 세밀하게 잘게 쪼개서 아주 자세한 정보까지 담는 경우, ‘음성 토큰 해상도’가 높아지고 사용하는 메모리 소비도 증가하는 문제로 인해 장시간 음성의 의미적, 화자적 일관성을 유지하기 어려웠다.
연구팀은 이러한 문제를 해결하기 위해 하이브리드 상태공간 모델(Hybrid State-Space Model)을 사용한 음성 언어 모델인‘스피치SSM’를 개발해 긴 음성 시퀀스를 효율적으로 처리하고 생성할 수 있게 설계했다.
이 모델은 최근 정보에 집중하는 ‘어텐션 레이어(attention layer)’와 전체 이야기 흐름(장기적인 맥락)을 오래 기억하는 ‘순환 레이어(recurrent layer)’를 교차 배치한 ‘하이브리드 구조’를 통해 긴 시간 동안 음성을 생성해도 흐름을 잃지 않고 이야기를 잘 이어간다. 또한, 메모리 사용량과 연산량이 입력 길이에 따라 급격히 증가하지 않아, 장시간의 음성을 안정적이고 효율적으로 학습하고 생성할 수 있다.
스피치SSM은 음성 데이터를 짧은 고정된 단위(윈도우)로 나눠 각 단위별로 독립적으로 처리하고, 전체 긴 음성을 만들 경우에는 다시 붙이는 방식을 활용해 쉽게 긴 음성을 만들 수 있어 무한한 길이의 음성 시퀀스(unbounded speech sequence)를 효과적으로 처리할 수 있게 했다.
또한 음성 생성 단계에서는 한 글자, 한 단어 차례대로 천천히 만들어내지 않고, 여러 부분을 한꺼번에 빠르게 만들어내는 ‘비자기회귀(Non-Autoregressive)’방식의 오디오 합성 모델(SoundStorm)을 사용해, 고품질의 음성을 빠르게 생성할 수 있게 했다.
기존은 10초 정도 짧은 음성 모델을 평가했지만, 연구팀은 16분까지 생성할 수 있도록 자체 구축한 새로운 벤치마크 데이터셋인 ‘LibriSpeech-Long'을 기반으로 음성을 생성하는 평가 태스크를 새롭게 만들었다.
기존 음성 모델 평가 지표인 말이 문법적으로 맞는지 정도만 알려주는 PPL(Perplexity)에 비해, 연구팀은 시간이 지나면서도 내용이 잘 이어지는지 보는 'SC-L(semantic coherence over time)', 자연스럽게 들리는 정도를 시간 따라 보는 'N-MOS-T(naturalness mean opinion score over time)' 등 새로운 평가 지표들을 제안해 보다 효과적이고 정밀하게 평가했다.
새로운 평가를 통해 스피치SSM 음성 언어 모델로 생성된 음성은 긴 시간 생성에도 불구하고 초기 프롬프트에서 언급된 특정 인물이 지속적으로 등장하며, 맥락적으로 일관된 새로운 인물과 사건들이 자연스럽게 전개되는 모습을 확인했다. 이는 기존 모델들이 장시간 생성 시 쉽게 주제를 잃고 반복되는 현상을 보였던 것과 크게 대조적이다.
박세진 박사과정생은 “기존 음성 언어 모델은 장시간 생성에 한계가 있어, 실제 인간이 사용하도록 장시간 음성 생성이 가능한 음성 언어 모델을 개발하는 것이 목표였다”며 “이번 연구 성과를 통해 긴 문맥에서도 일관된 내용을 유지하면서, 기존 방식보다 더 효율적이고 빠르게 실시간으로 응답할 수 있어, 다양한 음성 콘텐츠 제작과 음성비서 등 음성 AI 분야에 크게 기여할 것으로 기대한다”라고 밝혔다.
이 연구는 제1 저자인 우리 대학 박세진 박사과정 학생이 구글 딥마인드(Google DeepMind)와 협력해, ICML(국제 머신러닝 학회) 2025에서 7월 16일 구두 발표로 소개될 예정이다.
※ 논문제목: Long-Form Speech Generation with Spoken Language Models
※ DOI: 10.48550/arXiv.2412.18603
한편, 박세진 박사과정생은 비전, 음성, 언어를 통합하는 연구를 수행하며 CVPR(컴퓨터 비전 분야 최고 학회) 2024 하이라이트 논문 발표, 2024년 ACL(자연어 처리 분야 최고 학회)에서 우수논문상(Outstanding Paper Award) 수상 등을 통해 우수한 연구 역량을 입증한 바 있다.
[데모 페이지 링크]
https://google.github.io/tacotron/publications/speechssm/
24시간 말하는 AI비서 가능성 여는 '스피치SSM' 개발
최근 음성 언어 모델(Spoken Language Model, SLM)은 텍스트 없이 인간의 음성을 학습해 음성의 언어적, 비언어적 정보를 이해 및 생성하는 기술로 텍스트 기반 언어 모델의 한계를 넘어서는 차세대 기술로 각광받고 있다. 하지만 기존 모델은 장시간 콘텐츠 생성이 요구되는 팟캐스트, 오디오북, 음성비서 등에서 한계가 두드러졌는데, 우리 연구진이 이런 한계를 뛰어넘어, 시간 제약 없이 일관되고 자연스러운 음성 생성을 실현한 ‘스피치SSM’을 개발하는데 성공했다.
우리 대학 전기및전자공학부 노용만 교수 연구팀의 박세진 연구원(박사과정)이 장시간 음성 생성이 가능한 음성 언어 모델 ‘스피치SSM(SpeechSSM)’을 개발했다고 3일 밝혔다.
이번 연구는 국제 최고 권위 머신러닝 학회인 ICML(International Conference on Machine Learning) 2025에 전체 제출된 논문 중 약 1%만이 선정되는 구두 논문 발표에 확정돼 뛰어난 연구 역량을 입증할 뿐만 아니라 우리 대학의 인공지능 연구 능력이 세계 최고 수준임을 다시 한번 보여주는 계기가 될 전망이다.
음성 언어 모델(SLM)은 중간에 텍스트로 변환하지 않고 음성을 직접 처리함으로써, 인간 화자 고유의 음향적 특성을 활용할 수 있어 대규모 모델에서도 고품질의 음성을 빠르게 생성할 수 있다는 점이 큰 강점이다.
그러나 기존 모델은 음성을 아주 세밀하게 잘게 쪼개서 아주 자세한 정보까지 담는 경우, ‘음성 토큰 해상도’가 높아지고 사용하는 메모리 소비도 증가하는 문제로 인해 장시간 음성의 의미적, 화자적 일관성을 유지하기 어려웠다.
연구팀은 이러한 문제를 해결하기 위해 하이브리드 상태공간 모델(Hybrid State-Space Model)을 사용한 음성 언어 모델인‘스피치SSM’를 개발해 긴 음성 시퀀스를 효율적으로 처리하고 생성할 수 있게 설계했다.
이 모델은 최근 정보에 집중하는 ‘어텐션 레이어(attention layer)’와 전체 이야기 흐름(장기적인 맥락)을 오래 기억하는 ‘순환 레이어(recurrent layer)’를 교차 배치한 ‘하이브리드 구조’를 통해 긴 시간 동안 음성을 생성해도 흐름을 잃지 않고 이야기를 잘 이어간다. 또한, 메모리 사용량과 연산량이 입력 길이에 따라 급격히 증가하지 않아, 장시간의 음성을 안정적이고 효율적으로 학습하고 생성할 수 있다.
스피치SSM은 음성 데이터를 짧은 고정된 단위(윈도우)로 나눠 각 단위별로 독립적으로 처리하고, 전체 긴 음성을 만들 경우에는 다시 붙이는 방식을 활용해 쉽게 긴 음성을 만들 수 있어 무한한 길이의 음성 시퀀스(unbounded speech sequence)를 효과적으로 처리할 수 있게 했다.
또한 음성 생성 단계에서는 한 글자, 한 단어 차례대로 천천히 만들어내지 않고, 여러 부분을 한꺼번에 빠르게 만들어내는 ‘비자기회귀(Non-Autoregressive)’방식의 오디오 합성 모델(SoundStorm)을 사용해, 고품질의 음성을 빠르게 생성할 수 있게 했다.
기존은 10초 정도 짧은 음성 모델을 평가했지만, 연구팀은 16분까지 생성할 수 있도록 자체 구축한 새로운 벤치마크 데이터셋인 ‘LibriSpeech-Long'을 기반으로 음성을 생성하는 평가 태스크를 새롭게 만들었다.
기존 음성 모델 평가 지표인 말이 문법적으로 맞는지 정도만 알려주는 PPL(Perplexity)에 비해, 연구팀은 시간이 지나면서도 내용이 잘 이어지는지 보는 'SC-L(semantic coherence over time)', 자연스럽게 들리는 정도를 시간 따라 보는 'N-MOS-T(naturalness mean opinion score over time)' 등 새로운 평가 지표들을 제안해 보다 효과적이고 정밀하게 평가했다.
새로운 평가를 통해 스피치SSM 음성 언어 모델로 생성된 음성은 긴 시간 생성에도 불구하고 초기 프롬프트에서 언급된 특정 인물이 지속적으로 등장하며, 맥락적으로 일관된 새로운 인물과 사건들이 자연스럽게 전개되는 모습을 확인했다. 이는 기존 모델들이 장시간 생성 시 쉽게 주제를 잃고 반복되는 현상을 보였던 것과 크게 대조적이다.
박세진 박사과정생은 “기존 음성 언어 모델은 장시간 생성에 한계가 있어, 실제 인간이 사용하도록 장시간 음성 생성이 가능한 음성 언어 모델을 개발하는 것이 목표였다”며 “이번 연구 성과를 통해 긴 문맥에서도 일관된 내용을 유지하면서, 기존 방식보다 더 효율적이고 빠르게 실시간으로 응답할 수 있어, 다양한 음성 콘텐츠 제작과 음성비서 등 음성 AI 분야에 크게 기여할 것으로 기대한다”라고 밝혔다.
이 연구는 제1 저자인 우리 대학 박세진 박사과정 학생이 구글 딥마인드(Google DeepMind)와 협력해, ICML(국제 머신러닝 학회) 2025에서 7월 16일 구두 발표로 소개될 예정이다.
※ 논문제목: Long-Form Speech Generation with Spoken Language Models
※ DOI: 10.48550/arXiv.2412.18603
한편, 박세진 박사과정생은 비전, 음성, 언어를 통합하는 연구를 수행하며 CVPR(컴퓨터 비전 분야 최고 학회) 2024 하이라이트 논문 발표, 2024년 ACL(자연어 처리 분야 최고 학회)에서 우수논문상(Outstanding Paper Award) 수상 등을 통해 우수한 연구 역량을 입증한 바 있다.
[데모 페이지 링크]
https://google.github.io/tacotron/publications/speechssm/
2025.07.03
조회수 1007
-
 AI로 방사성 오염 '아이오딘' 제거용 최적 신소재 발굴
원자력 에너지 활용에 있어 방사성 폐기물 관리는 핵심적인 과제 중 하나다. 특히 방사성 ‘아이오딘(요오드)’는 반감기가 길고(I-129의 경우 1,570만 년), 이동성 및 생체 유독성이 높아 환경 및 인체에 심각한 위험을 초래할 수 있다. 한국 연구진이 인공지능을 활용해 아이오딘을 제거할 원자력 환경 정화용 신소재 발굴에 성공했다. 연구팀은 향후 방사성 오염 흡착용 분말부터 오염수 처리 필터까지 다양한 산학협력을 통해 상용화를 추진할 예정이다.
우리 대학 원자력및양자공학과 류호진 교수 연구팀이 한국화학연구원 디지털화학연구센터 노주환 박사가 협력하여, 인공지능을 활용해 방사성 오염 물질이 될 수 있는 아이오딘을 효과적으로 제거하는 신소재를 발굴하는 기술을 개발했다고 2일 밝혔다.
최근 보고에 따르면 방사능 오염 물질인 아이오딘이 수용액 환경에서 아이오딘산염(IO3-) 형태로 존재하는 것으로 밝혀졌으나, 기존의 은 기반 흡착제는 이에 대해 낮은 화학적 흡착력을 가져 비효율적이었다. 따라서 아이오딘산염을 효과적으로 제거할 수 있는 새로운 흡착제 신소재 개발이 시급한 실정이다.
류호진 교수 연구팀은 기계학습을 활용한 실험 전략을 통해 다양한 금속원소를 함유한 ‘이중층 수산화물(Layered Double Hydroxide, 이하 LDH)’이라는 화합물 중 최적의 아이오딘산염 흡착제를 발굴했다.
이번 연구에서 개발된 구리-크롬-철-알루미늄 기반의 다중금속 이중층 수산화물 Cu3(CrFeAl)은 아이오딘산염에 대해 90% 이상의 뛰어난 흡착 성능을 보였다. 이는 기존의 시행착오 실험 방식으로는 탐색이 어려운 방대한 물질 조성 공간을 인공지능 기반의 능동학습법을 통해 효율적으로 탐색해 얻어낸 성과다.
연구팀은 이중층 수산화물(이하 LDH)이 고엔트로피 재료와 같이 다양한 금속 조성을 가질 수 있고 음이온 흡착에 유리한 구조를 지녔다는 점에 주목했다. 그러나 다중금속 LDH의 경우 가능한 금속 조합이 너무 많아 기존의 실험 방식으로는 최적의 조합을 찾기 어려웠다.
이를 해결하기 위해 연구팀은 인공지능(기계학습)을 도입했다. 초기 24개의 2원계 및 96개의 3원계 LDH 실험 데이터로 학습을 시작해, 4원계 및 5원계 후보 물질로 탐색을 확장했다. 이 결과 전체 후보 물질 중 단 16%에 대해서만 실험을 수행하고도 아이오딘산염 제거에 최적인 신소재 물질을 찾아낼 수 있었다.
류호진 교수는 “인공지능을 활용하면 방대한 신소재 후보 물질 군에서 방사성 오염 제거용 물질을 효율적으로 찾아낼 가능성을 보여, 원자력 환경 정화용 신소재 개발에 필요한 연구를 가속화하는데 기여할 것으로 기대된다”고 말했다.
류 교수 연구팀은 개발된 분말 기술에 대한 국내 특허를 출원했으며 이를 기반으로 해외 특허 출원을 진행 중이다. 연구팀은 향후 방사성 오염 흡착용 분말의 다양한 사용 환경에서의 성능을 고도화하고, 오염수 처리 필터 개발 분야에서 산학 협력을 통한 상용화 방안을 추진할 예정이다.
우리 대학 신소재공학과를 졸업한 이수정 박사와 한국화학연구원 디지털화학연구센터 노주환 박사가 제1 저자로 참여한 이번 연구는 이번 연구 결과는 환경 분야 국제 저명 학술지인 ‘위험물질 저널(Journal of Hazardous Materials)'에 5월 26일 온라인 게재됐다.
※논문명: Discovery of multi-metal-layered double hydroxides for decontamination of iodate by machine learning-assisted experiments
※DOI: https://doi.org/10.1016/j.jhazmat.2025.138735
이번 연구는 과학기술정보통신부 한국연구재단의 원자력기초연구지원사업과 나노·소재기술개발사업의 지원으로 수행됐다.
AI로 방사성 오염 '아이오딘' 제거용 최적 신소재 발굴
원자력 에너지 활용에 있어 방사성 폐기물 관리는 핵심적인 과제 중 하나다. 특히 방사성 ‘아이오딘(요오드)’는 반감기가 길고(I-129의 경우 1,570만 년), 이동성 및 생체 유독성이 높아 환경 및 인체에 심각한 위험을 초래할 수 있다. 한국 연구진이 인공지능을 활용해 아이오딘을 제거할 원자력 환경 정화용 신소재 발굴에 성공했다. 연구팀은 향후 방사성 오염 흡착용 분말부터 오염수 처리 필터까지 다양한 산학협력을 통해 상용화를 추진할 예정이다.
우리 대학 원자력및양자공학과 류호진 교수 연구팀이 한국화학연구원 디지털화학연구센터 노주환 박사가 협력하여, 인공지능을 활용해 방사성 오염 물질이 될 수 있는 아이오딘을 효과적으로 제거하는 신소재를 발굴하는 기술을 개발했다고 2일 밝혔다.
최근 보고에 따르면 방사능 오염 물질인 아이오딘이 수용액 환경에서 아이오딘산염(IO3-) 형태로 존재하는 것으로 밝혀졌으나, 기존의 은 기반 흡착제는 이에 대해 낮은 화학적 흡착력을 가져 비효율적이었다. 따라서 아이오딘산염을 효과적으로 제거할 수 있는 새로운 흡착제 신소재 개발이 시급한 실정이다.
류호진 교수 연구팀은 기계학습을 활용한 실험 전략을 통해 다양한 금속원소를 함유한 ‘이중층 수산화물(Layered Double Hydroxide, 이하 LDH)’이라는 화합물 중 최적의 아이오딘산염 흡착제를 발굴했다.
이번 연구에서 개발된 구리-크롬-철-알루미늄 기반의 다중금속 이중층 수산화물 Cu3(CrFeAl)은 아이오딘산염에 대해 90% 이상의 뛰어난 흡착 성능을 보였다. 이는 기존의 시행착오 실험 방식으로는 탐색이 어려운 방대한 물질 조성 공간을 인공지능 기반의 능동학습법을 통해 효율적으로 탐색해 얻어낸 성과다.
연구팀은 이중층 수산화물(이하 LDH)이 고엔트로피 재료와 같이 다양한 금속 조성을 가질 수 있고 음이온 흡착에 유리한 구조를 지녔다는 점에 주목했다. 그러나 다중금속 LDH의 경우 가능한 금속 조합이 너무 많아 기존의 실험 방식으로는 최적의 조합을 찾기 어려웠다.
이를 해결하기 위해 연구팀은 인공지능(기계학습)을 도입했다. 초기 24개의 2원계 및 96개의 3원계 LDH 실험 데이터로 학습을 시작해, 4원계 및 5원계 후보 물질로 탐색을 확장했다. 이 결과 전체 후보 물질 중 단 16%에 대해서만 실험을 수행하고도 아이오딘산염 제거에 최적인 신소재 물질을 찾아낼 수 있었다.
류호진 교수는 “인공지능을 활용하면 방대한 신소재 후보 물질 군에서 방사성 오염 제거용 물질을 효율적으로 찾아낼 가능성을 보여, 원자력 환경 정화용 신소재 개발에 필요한 연구를 가속화하는데 기여할 것으로 기대된다”고 말했다.
류 교수 연구팀은 개발된 분말 기술에 대한 국내 특허를 출원했으며 이를 기반으로 해외 특허 출원을 진행 중이다. 연구팀은 향후 방사성 오염 흡착용 분말의 다양한 사용 환경에서의 성능을 고도화하고, 오염수 처리 필터 개발 분야에서 산학 협력을 통한 상용화 방안을 추진할 예정이다.
우리 대학 신소재공학과를 졸업한 이수정 박사와 한국화학연구원 디지털화학연구센터 노주환 박사가 제1 저자로 참여한 이번 연구는 이번 연구 결과는 환경 분야 국제 저명 학술지인 ‘위험물질 저널(Journal of Hazardous Materials)'에 5월 26일 온라인 게재됐다.
※논문명: Discovery of multi-metal-layered double hydroxides for decontamination of iodate by machine learning-assisted experiments
※DOI: https://doi.org/10.1016/j.jhazmat.2025.138735
이번 연구는 과학기술정보통신부 한국연구재단의 원자력기초연구지원사업과 나노·소재기술개발사업의 지원으로 수행됐다.
2025.07.02
조회수 868
-
 장내 미생물로 난치성 뇌종양 면역치료 효과 높인다
우리 몸의 면역세포인 T세포를 활성화시켜 암세포를 제거하도록 유도하는 첨단 치료법인 ‘면역항암제’는 가장 치명적인 뇌종양 ‘교모세포종(Glioblastoma)’에는 거의 반응하지 않고, 치료에 대한 저항성이 높아 단독 치료로는 효과가 매우 제한적이라는 한계가 있었다. 이에 우리 연구진이 장내 미생물과 그 대사산물을 활용해 뇌종양의 면역치료 효과를 높일 수 있는 새로운 치료 전략을 세계 최초로 입증했다. 향후 미생물을 기반으로 한 면역치료 보완제 개발에 대한 가능성도 보여줬다.
우리 대학 생명과학과 이흥규 교수 연구팀이 장내 미생물 생태계 변화에 주목해 교모세포종 면역치료의 효율을 크게 높이는 방법을 발굴하고 이를 입증했다고 1일 밝혔다.
연구팀은 교모세포종이 진행되면서 장내에서 중요한 아미노산인 ‘트립토판(tryptophan)’의 농도가 급격히 줄어들고, 이로 인해 장내 미생물 생태계가 변화한다는 점에 주목했다. 그리고 트립토판을 보충해 미생물 다양성을 회복시키면, 특정 유익한 균주가 면역세포 중 하나인 CD8 T세포를 활성화하고 종양 조직으로 다시 유도하는 역할을 한다는 사실을 밝혀냈다.
연구팀은 생쥐 교모세포종 모델을 통해, 트립토판을 보충하면 암을 공격하는 T세포(특히 CD8 T세포)의 반응이 향상되고, 이들이 림프절과 뇌 등 종양이 있는 부위로 더 많이 이동한다는 사실을 확인했다.
이 과정에서 장내에 존재하는 유익한 공생균인 ‘던카니엘라 두보시(Duncaniella dubosii)’가 핵심적인 역할을 한다는 점도 밝혀냈다. 해당 균주는 T세포가 몸 안에서 효과적으로 재분포하도록 도와줬고, 면역항암제(anti-PD-1)와 함께 사용할 때 생존율이 유의미하게 향상됐다.
또한, 장내 미생물이 전혀 없는 무균 생쥐에게 위 공생균을 단독으로 투입해도 교모세포종에 대한 생존율이 높아졌으며, 이는 이 균주가 트립토판을 활용해 장내 환경을 조절하고, 그 과정에서 생성되는 대사산물이 CD8 T세포의 암세포 공격 능력을 강화하기 때문임이 입증됐다.
이흥규 교수는 “이번 연구는 면역관문억제제가 효과를 보이지 않았던 난치성 뇌종양에서도, 장내 미생물을 활용한 병용 전략을 통해 치료 반응을 유의하게 높일 수 있음을 보여준 의미 있는 성과”라고 설명했다.
우리 대학 김현철 박사(現, 생명과학연구소 박사후연구원)가 제1 저자로 참여했고 연구 결과는 생명과학 분야 국제 학술지‘셀 리포츠(Cell Reports)’에 지난 6월 26 일자 온라인판에 게재됐다.
(논문명: Gut microbiota dysbiosis induced by brain tumor modulates the efficacy of immunotherapy, https://doi.org/10.1016/j.celrep.2025.115825)
한편, 이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
장내 미생물로 난치성 뇌종양 면역치료 효과 높인다
우리 몸의 면역세포인 T세포를 활성화시켜 암세포를 제거하도록 유도하는 첨단 치료법인 ‘면역항암제’는 가장 치명적인 뇌종양 ‘교모세포종(Glioblastoma)’에는 거의 반응하지 않고, 치료에 대한 저항성이 높아 단독 치료로는 효과가 매우 제한적이라는 한계가 있었다. 이에 우리 연구진이 장내 미생물과 그 대사산물을 활용해 뇌종양의 면역치료 효과를 높일 수 있는 새로운 치료 전략을 세계 최초로 입증했다. 향후 미생물을 기반으로 한 면역치료 보완제 개발에 대한 가능성도 보여줬다.
우리 대학 생명과학과 이흥규 교수 연구팀이 장내 미생물 생태계 변화에 주목해 교모세포종 면역치료의 효율을 크게 높이는 방법을 발굴하고 이를 입증했다고 1일 밝혔다.
연구팀은 교모세포종이 진행되면서 장내에서 중요한 아미노산인 ‘트립토판(tryptophan)’의 농도가 급격히 줄어들고, 이로 인해 장내 미생물 생태계가 변화한다는 점에 주목했다. 그리고 트립토판을 보충해 미생물 다양성을 회복시키면, 특정 유익한 균주가 면역세포 중 하나인 CD8 T세포를 활성화하고 종양 조직으로 다시 유도하는 역할을 한다는 사실을 밝혀냈다.
연구팀은 생쥐 교모세포종 모델을 통해, 트립토판을 보충하면 암을 공격하는 T세포(특히 CD8 T세포)의 반응이 향상되고, 이들이 림프절과 뇌 등 종양이 있는 부위로 더 많이 이동한다는 사실을 확인했다.
이 과정에서 장내에 존재하는 유익한 공생균인 ‘던카니엘라 두보시(Duncaniella dubosii)’가 핵심적인 역할을 한다는 점도 밝혀냈다. 해당 균주는 T세포가 몸 안에서 효과적으로 재분포하도록 도와줬고, 면역항암제(anti-PD-1)와 함께 사용할 때 생존율이 유의미하게 향상됐다.
또한, 장내 미생물이 전혀 없는 무균 생쥐에게 위 공생균을 단독으로 투입해도 교모세포종에 대한 생존율이 높아졌으며, 이는 이 균주가 트립토판을 활용해 장내 환경을 조절하고, 그 과정에서 생성되는 대사산물이 CD8 T세포의 암세포 공격 능력을 강화하기 때문임이 입증됐다.
이흥규 교수는 “이번 연구는 면역관문억제제가 효과를 보이지 않았던 난치성 뇌종양에서도, 장내 미생물을 활용한 병용 전략을 통해 치료 반응을 유의하게 높일 수 있음을 보여준 의미 있는 성과”라고 설명했다.
우리 대학 김현철 박사(現, 생명과학연구소 박사후연구원)가 제1 저자로 참여했고 연구 결과는 생명과학 분야 국제 학술지‘셀 리포츠(Cell Reports)’에 지난 6월 26 일자 온라인판에 게재됐다.
(논문명: Gut microbiota dysbiosis induced by brain tumor modulates the efficacy of immunotherapy, https://doi.org/10.1016/j.celrep.2025.115825)
한편, 이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
2025.07.01
조회수 986
-
 기계공학과 윤국진 교수 연구팀, 세계 최고 권위 컴퓨터비전 국제학술대회 ICCV 2025에 논문 12편 채택
우리 대학 기계공학과 윤국진 교수 연구팀의 논문 12편이 세계 최고 권위 컴퓨터비전 국제 학술 대회 중 하나인 IEEE/CVF International Conference on Computer Vision 2025(ICCV 2025)에 채택되어, 연구팀의 독보적인 연구 역량을 다시 한번 국제적으로 인정받았다.
ICCV는 CVPR, ECCV와 함께 컴퓨터비전 및 인공지능 분야에서 가장 영향력 있는 국제 학술대회 중 하나로, 1987년부터 격년으로 개최되어 왔다. 이번 ICCV 2025에는 총 11,152편의 논문이 제출되었고, 이 중 2,698편이 채택되어 약 24.19%의 낮은 채택률을 기록하였다. 학술대회에 제출할 수 있는 논문 편수에 대한 제한이 있음에도 불구하고 단일 연구실에서 12편의 논문이 동시 채택되는 것은 매우 드문 성과다.
윤국진 교수 연구팀은 학습 기반의 시각 지능 구현을 목표로 연구를 진행하고 있으며, 이번에 발표된 12편의 논문들은 3D 객체 탐지 및 재구성, 동작 예측 및 계획, 악천후나 모션 블러와 같은 극한 환경에서의 영상 인식 및 개선, 테스트 시점 적응 및 멀티태스크 학습, 4D 맵을 활용한 재구성과 같은 컴퓨터비전 분야의 핵심 주제들에 대한 논문들이다.
특히 연구팀은 지난해 CVPR 2024와 ECCV 2024에서도 각각 9편과 12편의 논문을 발표하여 학계의 주목을 받은 바 있는데, 이번 ICCV 2025에서의 성과를 통해 전 세계 컴퓨터 비전 분야의 선두 연구실로서 입지를 더욱 확고히 했다. 연구팀은 앞으로도 도전적인 연구를 이어가며 학문적·기술적 한계를 확장해 나갈 계획이다.
ICCV 2025는 오는 10월 19일부터 23일까지 미국 하와이 호놀룰루에서 개최될 예정이다.
기계공학과 윤국진 교수 연구팀, 세계 최고 권위 컴퓨터비전 국제학술대회 ICCV 2025에 논문 12편 채택
우리 대학 기계공학과 윤국진 교수 연구팀의 논문 12편이 세계 최고 권위 컴퓨터비전 국제 학술 대회 중 하나인 IEEE/CVF International Conference on Computer Vision 2025(ICCV 2025)에 채택되어, 연구팀의 독보적인 연구 역량을 다시 한번 국제적으로 인정받았다.
ICCV는 CVPR, ECCV와 함께 컴퓨터비전 및 인공지능 분야에서 가장 영향력 있는 국제 학술대회 중 하나로, 1987년부터 격년으로 개최되어 왔다. 이번 ICCV 2025에는 총 11,152편의 논문이 제출되었고, 이 중 2,698편이 채택되어 약 24.19%의 낮은 채택률을 기록하였다. 학술대회에 제출할 수 있는 논문 편수에 대한 제한이 있음에도 불구하고 단일 연구실에서 12편의 논문이 동시 채택되는 것은 매우 드문 성과다.
윤국진 교수 연구팀은 학습 기반의 시각 지능 구현을 목표로 연구를 진행하고 있으며, 이번에 발표된 12편의 논문들은 3D 객체 탐지 및 재구성, 동작 예측 및 계획, 악천후나 모션 블러와 같은 극한 환경에서의 영상 인식 및 개선, 테스트 시점 적응 및 멀티태스크 학습, 4D 맵을 활용한 재구성과 같은 컴퓨터비전 분야의 핵심 주제들에 대한 논문들이다.
특히 연구팀은 지난해 CVPR 2024와 ECCV 2024에서도 각각 9편과 12편의 논문을 발표하여 학계의 주목을 받은 바 있는데, 이번 ICCV 2025에서의 성과를 통해 전 세계 컴퓨터 비전 분야의 선두 연구실로서 입지를 더욱 확고히 했다. 연구팀은 앞으로도 도전적인 연구를 이어가며 학문적·기술적 한계를 확장해 나갈 계획이다.
ICCV 2025는 오는 10월 19일부터 23일까지 미국 하와이 호놀룰루에서 개최될 예정이다.
2025.06.30
조회수 806
-
 ‘슝’ 스스로 움직이는 생명체 세포로봇 개발
현재 전 세계적으로 마이크로 및 나노급의 작은 입자 기반의 비생명체 자가 추진 로봇 기술은 활발하게 연구되고 있는 반면에, 세포와 같은 생명체 구성 요소를 직접 활용한 세포로봇 연구는 아직 초기 단계에 머물러 있다. 우리 연구진이 세포 기반 시스템의 자율적으로 이동하는 세포로봇을 개발하는데 성공했다. 향후 정밀 약물 전달이나 차세대 세포 기반 치료법의 원천기술로 활용될 수 있을 것으로 기대된다.
우리 대학 화학과 최인성 교수 연구팀이 외부 동력 장치나 복잡한 기계 구조 없이, 생체 부산물인 ‘요소(urea)’*를 연료로 사용하는 자가 추진 세포로봇을 개발했다고 30일 밝혔다.
*요소(urea): 사람을 포함한 대부분의 동물 체내에서 단백질을 분해하면서 생기는 노폐물로 생명체 안에서는 단백질 대사 과정에서 암모니아를 독성이 낮은 형태로 전환하여 배출하는 중요한 역할을 함
연구팀이 구현한 세포로봇은 방향성을 갖고 스스로 이동할 수 있으며, 원하는 물질을 운반하거나 주변 환경 제어 기능을 탑재할 수 있는 다기능성 플랫폼으로 설계됐다.
연구팀은 쉽고 안정적으로 얻을 수 있는 생명체이면서 부산물로 생성된 에탄올 활용 가능성이 있고, 인공적인 복잡한 외부 장치 없이 생명체 스스로 만들어내는 물질을 활용할 수 있는 ‘효모’에 주목했다.
제빵과 막걸리 발효에 사용되는 효모(이스트, yeast)는 포도당을 분해해 에너지를 얻는 대사 과정에서 알코올(에탄올)을 부산물로 생성하는데, 연구팀은 이때 생성된 에탄올을 활용해 효모 표면에 생체친화적인 방식으로 나노 껍질을 형성할 수 있는 원천기술을 개발했다.
이를 위해, 알코올산화효소(AOx)와 겨자무과산화효소(HRP)로 구성된 효소 시스템을 도입했다. 이 효소 시스템은 효모의 포도당 분해 반응과 연계된 연쇄적 효소 반응을 유도하며, 그 결과로 멜라닌 계열의 나노껍질이 효모 표면에 형성된다.
특히, 이번에 개발된 화학적 방법론은 효모가 성장하고 분열하는 동안에도 나노껍질 형성이 지속적으로 일어나도록 설계돼 있어서, 세포의 형태 변화에 따라 비대칭적인 세포-껍질 구조가 자연스럽게 생성된다.
예를 들어, 분열 중인 세포 전체를 감싸는 껍질이 형성되기도 하지만, 모세포 부분에는 껍질이 생성되고 딸세포 부분에는 형성되지 않는 구조도 만들어진다.
연구팀은 세포를 감싸는 나노껍질에 우레아제(urease)*를 부착하고 세포로봇의 움직임을 관찰했다. 우레아제는 요소를 분해하는 촉매 역할을 하며 세포로봇이 스스로 움직일 수 있도록 구동력을 만들어내는 핵심 역할을 수행하며 비대칭 구조를 가진 세포로봇이 보다 명확한 방향성을 갖고 자가 추진하는 현상을 확인했다.
*우레아제(urease): 요소를 분해해 암모니아와 이산화탄소를 만드는 효소
이번에 개발된 세포로봇은 세포 주위에 존재하는 물질만으로 자가 추진이 가능하고, 자석이나 레이저 등 복잡한 외부 제어 장치에 의존하지 않아 구동 메커니즘이 훨씬 간단하고 생체친화적이다. 또한, 나노껍질에 다양한 효소를 화학적으로 접합할 수 있어, 다양한 생체 물질을 연료로 활용하는 세포로봇의 확장 개발도 가능하다.
이번 연구의 제1 저자인 화학과 김나영 박사과정은 “자가 추진 세포로봇은 스스로 환경을 감지하고 반응하며 움직이는 능력을 지닌 새로운 개념의 플랫폼으로, 향후 암세포 표적 치료나 정밀 약물전달시스템 등에서 중요한 역할을 할 수 있을 것”이라고 말했다.
이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’에 지난 6월 25일 오후 2시(미국 동부시각) 온라인판에 게재됐다.
※ 논문명 : Autonomous Chemo-Metabolic Construction of Anisotropic Cell-in-Shell Nanobiohybrids in Enzyme-Powered Cell Microrobots; 국문 번역 : 효소 구동 세포 마이크로로봇 구축에서의 자율적인 화학-대사 반응을 통해 형성된 비등방성 세포내껍질 나노바이오하이브리드
※ DOI: https://doi.org/10.1126/sciadv.adu5451
한편, 이번 연구는 한국연구재단 기초연구사업 중견연구과제(제목: 세포대사 연계형 단일세포나노피포화)의 지원을 받아 수행됐다.
‘슝’ 스스로 움직이는 생명체 세포로봇 개발
현재 전 세계적으로 마이크로 및 나노급의 작은 입자 기반의 비생명체 자가 추진 로봇 기술은 활발하게 연구되고 있는 반면에, 세포와 같은 생명체 구성 요소를 직접 활용한 세포로봇 연구는 아직 초기 단계에 머물러 있다. 우리 연구진이 세포 기반 시스템의 자율적으로 이동하는 세포로봇을 개발하는데 성공했다. 향후 정밀 약물 전달이나 차세대 세포 기반 치료법의 원천기술로 활용될 수 있을 것으로 기대된다.
우리 대학 화학과 최인성 교수 연구팀이 외부 동력 장치나 복잡한 기계 구조 없이, 생체 부산물인 ‘요소(urea)’*를 연료로 사용하는 자가 추진 세포로봇을 개발했다고 30일 밝혔다.
*요소(urea): 사람을 포함한 대부분의 동물 체내에서 단백질을 분해하면서 생기는 노폐물로 생명체 안에서는 단백질 대사 과정에서 암모니아를 독성이 낮은 형태로 전환하여 배출하는 중요한 역할을 함
연구팀이 구현한 세포로봇은 방향성을 갖고 스스로 이동할 수 있으며, 원하는 물질을 운반하거나 주변 환경 제어 기능을 탑재할 수 있는 다기능성 플랫폼으로 설계됐다.
연구팀은 쉽고 안정적으로 얻을 수 있는 생명체이면서 부산물로 생성된 에탄올 활용 가능성이 있고, 인공적인 복잡한 외부 장치 없이 생명체 스스로 만들어내는 물질을 활용할 수 있는 ‘효모’에 주목했다.
제빵과 막걸리 발효에 사용되는 효모(이스트, yeast)는 포도당을 분해해 에너지를 얻는 대사 과정에서 알코올(에탄올)을 부산물로 생성하는데, 연구팀은 이때 생성된 에탄올을 활용해 효모 표면에 생체친화적인 방식으로 나노 껍질을 형성할 수 있는 원천기술을 개발했다.
이를 위해, 알코올산화효소(AOx)와 겨자무과산화효소(HRP)로 구성된 효소 시스템을 도입했다. 이 효소 시스템은 효모의 포도당 분해 반응과 연계된 연쇄적 효소 반응을 유도하며, 그 결과로 멜라닌 계열의 나노껍질이 효모 표면에 형성된다.
특히, 이번에 개발된 화학적 방법론은 효모가 성장하고 분열하는 동안에도 나노껍질 형성이 지속적으로 일어나도록 설계돼 있어서, 세포의 형태 변화에 따라 비대칭적인 세포-껍질 구조가 자연스럽게 생성된다.
예를 들어, 분열 중인 세포 전체를 감싸는 껍질이 형성되기도 하지만, 모세포 부분에는 껍질이 생성되고 딸세포 부분에는 형성되지 않는 구조도 만들어진다.
연구팀은 세포를 감싸는 나노껍질에 우레아제(urease)*를 부착하고 세포로봇의 움직임을 관찰했다. 우레아제는 요소를 분해하는 촉매 역할을 하며 세포로봇이 스스로 움직일 수 있도록 구동력을 만들어내는 핵심 역할을 수행하며 비대칭 구조를 가진 세포로봇이 보다 명확한 방향성을 갖고 자가 추진하는 현상을 확인했다.
*우레아제(urease): 요소를 분해해 암모니아와 이산화탄소를 만드는 효소
이번에 개발된 세포로봇은 세포 주위에 존재하는 물질만으로 자가 추진이 가능하고, 자석이나 레이저 등 복잡한 외부 제어 장치에 의존하지 않아 구동 메커니즘이 훨씬 간단하고 생체친화적이다. 또한, 나노껍질에 다양한 효소를 화학적으로 접합할 수 있어, 다양한 생체 물질을 연료로 활용하는 세포로봇의 확장 개발도 가능하다.
이번 연구의 제1 저자인 화학과 김나영 박사과정은 “자가 추진 세포로봇은 스스로 환경을 감지하고 반응하며 움직이는 능력을 지닌 새로운 개념의 플랫폼으로, 향후 암세포 표적 치료나 정밀 약물전달시스템 등에서 중요한 역할을 할 수 있을 것”이라고 말했다.
이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’에 지난 6월 25일 오후 2시(미국 동부시각) 온라인판에 게재됐다.
※ 논문명 : Autonomous Chemo-Metabolic Construction of Anisotropic Cell-in-Shell Nanobiohybrids in Enzyme-Powered Cell Microrobots; 국문 번역 : 효소 구동 세포 마이크로로봇 구축에서의 자율적인 화학-대사 반응을 통해 형성된 비등방성 세포내껍질 나노바이오하이브리드
※ DOI: https://doi.org/10.1126/sciadv.adu5451
한편, 이번 연구는 한국연구재단 기초연구사업 중견연구과제(제목: 세포대사 연계형 단일세포나노피포화)의 지원을 받아 수행됐다.
2025.06.30
조회수 1212
 최정우 교수팀, 세계 최고 음향 AI 챌린지 세계 1위 쾌거
‘음향 분리 및 분류 기술’은 드론, 공장 배관, 국경 감시 시스템 등에서 이상 음향을 조기에 탐지하거나, AR/VR 콘텐츠 제작 시 공간 음향(Spatial Audio)을 음원별로 분리해 편집할 수 있도록 하는 차세대 인공지능(AI) 핵심 기술이다.
우리 대학 전기및전자공학부 최정우 교수 연구팀이 세계 최고 권위의 음향 탐지 및 분석 대회인 ‘IEEE DCASE 챌린지 2025’에서 ‘공간 의미 기반 음향 장면 분할(Spatial Semantic Segmentation of Sound Scenes)’ 분야에서 우승을 차지했다고 11일 밝혔다.
이번 대회에서 연구팀은 전 세계 86개 참가팀과 총 6개 분야에서 경쟁 끝에 최초 참가임에도 세계 1위 성과를 거두었다. KAIST 최정우 교수 연구팀은 이동헌 박사, 권영후 석박통합과정생, 김도환 석사과정생으로 구성되었다.
연구팀이 참가한 ‘공간 의미 기반 음향 장면 분할’의 ‘태스크(Task) 4’분야는 여러 음원이 혼합된 다채널 신호의 공간 정보를 분석해 개별 소리를 분리하고 18종으로의 분류를 수행해야 하는 기술 난이도가 매우 높은 분야이다. 연구팀은 오는 10월, 바르셀로나에서 열리는 DCASE 워크숍에서 기술을 발표할 예정이다.
연구팀의 이동헌 박사는 올해 초 트랜스포머(Transformer)와 맘바(Mamba) 아키텍처를 결합한 세계 최고 성능의 음원 분리 인공지능을 개발했으며, 챌린지 기간 동안 권영후 연구원을 중심으로 1차로 분리된 음원의 파형과 종류를 단서로 해 다시 음원 분리와 분류를 수행하는‘단계적 추론 방식’의 AI 모델을 완성했다.
이는 사람이 복잡한 소리를 들을 때 소리의 종류나 리듬, 방향 등 특정 단서에 기반해 개별 소리를 분리해 듣는 방식을 AI가 모방한 모델이다.
이를 통해, 순위를 결정하는 척도인 AI가 소리를 얼마나 잘 분리하고 분류했는지 평가하는‘음원의 신호대 왜곡비 향상도(CA-SDRi)*’에서 참가팀 중 유일하게 두 자릿수 대의 성능(11 dB)을 보여, 기술적인 우수성을 입증하였다.
*음원의 신호대 왜곡비 향상도(CA-SDRi): 기존의 오디오와 비교해 얼마나 더 선명하게(덜 왜곡되게) 원하는 소리를 분리했는지를 dB(데시벨) 단위로 측정하고 숫자가 클수록 더 정확하고 깔끔하게 소리를 분리했다는 뜻임
최정우 교수는 "연구팀은 최근 3년간 세계 최고의 음향 분리 AI 모델을 선보여 왔으며, 그 결과를 공식적으로 인정받는 계기가 되어 기쁘다”면서 “난이도가 대폭 향상되고, 타 학회 일정과 기말고사로 불과 몇 주간만 개발이 가능했음에도 집중력 있는 연구를 통해 1위를 차지한 연구팀 개개인이 자랑스럽다”고 소감을 밝혔다.
‘IEEE DCASE 챌린지 2025’는 온라인으로 진행됐으며, 4월 1일부터 시작해 6월 15일 인공지능 모델 투고를 마감했고 지난 6월 30일 결과가 발표됐다. 각종 음향 관련 탐지 및 분류 기술을 평가하는 IEEE 신호처리학회(Signal Processing Society) 산하 국제대회인 본 챌린지는 2013년 개최된 이래 음향 분야 인공지능 모델의 세계적인 경연의 장으로 자리매김해 왔다.
https://dcase.community/challenge2025/task-spatial-semantic-segmentation-of-sound-scenes
한편, 해당 연구는 교육과학기술부의 재원으로 한국연구재단 중견연구자지원사업, STEAM 연구사업 지원 및 방위사업청 및 국방과학연구소 재원으로 미래국방연구센터 지원을 받아 수행됐다.
2025.07.11 조회수 282
최정우 교수팀, 세계 최고 음향 AI 챌린지 세계 1위 쾌거
‘음향 분리 및 분류 기술’은 드론, 공장 배관, 국경 감시 시스템 등에서 이상 음향을 조기에 탐지하거나, AR/VR 콘텐츠 제작 시 공간 음향(Spatial Audio)을 음원별로 분리해 편집할 수 있도록 하는 차세대 인공지능(AI) 핵심 기술이다.
우리 대학 전기및전자공학부 최정우 교수 연구팀이 세계 최고 권위의 음향 탐지 및 분석 대회인 ‘IEEE DCASE 챌린지 2025’에서 ‘공간 의미 기반 음향 장면 분할(Spatial Semantic Segmentation of Sound Scenes)’ 분야에서 우승을 차지했다고 11일 밝혔다.
이번 대회에서 연구팀은 전 세계 86개 참가팀과 총 6개 분야에서 경쟁 끝에 최초 참가임에도 세계 1위 성과를 거두었다. KAIST 최정우 교수 연구팀은 이동헌 박사, 권영후 석박통합과정생, 김도환 석사과정생으로 구성되었다.
연구팀이 참가한 ‘공간 의미 기반 음향 장면 분할’의 ‘태스크(Task) 4’분야는 여러 음원이 혼합된 다채널 신호의 공간 정보를 분석해 개별 소리를 분리하고 18종으로의 분류를 수행해야 하는 기술 난이도가 매우 높은 분야이다. 연구팀은 오는 10월, 바르셀로나에서 열리는 DCASE 워크숍에서 기술을 발표할 예정이다.
연구팀의 이동헌 박사는 올해 초 트랜스포머(Transformer)와 맘바(Mamba) 아키텍처를 결합한 세계 최고 성능의 음원 분리 인공지능을 개발했으며, 챌린지 기간 동안 권영후 연구원을 중심으로 1차로 분리된 음원의 파형과 종류를 단서로 해 다시 음원 분리와 분류를 수행하는‘단계적 추론 방식’의 AI 모델을 완성했다.
이는 사람이 복잡한 소리를 들을 때 소리의 종류나 리듬, 방향 등 특정 단서에 기반해 개별 소리를 분리해 듣는 방식을 AI가 모방한 모델이다.
이를 통해, 순위를 결정하는 척도인 AI가 소리를 얼마나 잘 분리하고 분류했는지 평가하는‘음원의 신호대 왜곡비 향상도(CA-SDRi)*’에서 참가팀 중 유일하게 두 자릿수 대의 성능(11 dB)을 보여, 기술적인 우수성을 입증하였다.
*음원의 신호대 왜곡비 향상도(CA-SDRi): 기존의 오디오와 비교해 얼마나 더 선명하게(덜 왜곡되게) 원하는 소리를 분리했는지를 dB(데시벨) 단위로 측정하고 숫자가 클수록 더 정확하고 깔끔하게 소리를 분리했다는 뜻임
최정우 교수는 "연구팀은 최근 3년간 세계 최고의 음향 분리 AI 모델을 선보여 왔으며, 그 결과를 공식적으로 인정받는 계기가 되어 기쁘다”면서 “난이도가 대폭 향상되고, 타 학회 일정과 기말고사로 불과 몇 주간만 개발이 가능했음에도 집중력 있는 연구를 통해 1위를 차지한 연구팀 개개인이 자랑스럽다”고 소감을 밝혔다.
‘IEEE DCASE 챌린지 2025’는 온라인으로 진행됐으며, 4월 1일부터 시작해 6월 15일 인공지능 모델 투고를 마감했고 지난 6월 30일 결과가 발표됐다. 각종 음향 관련 탐지 및 분류 기술을 평가하는 IEEE 신호처리학회(Signal Processing Society) 산하 국제대회인 본 챌린지는 2013년 개최된 이래 음향 분야 인공지능 모델의 세계적인 경연의 장으로 자리매김해 왔다.
https://dcase.community/challenge2025/task-spatial-semantic-segmentation-of-sound-scenes
한편, 해당 연구는 교육과학기술부의 재원으로 한국연구재단 중견연구자지원사업, STEAM 연구사업 지원 및 방위사업청 및 국방과학연구소 재원으로 미래국방연구센터 지원을 받아 수행됐다.
2025.07.11 조회수 282 뇌는 포도당을 구별한다..비만·당뇨 치료의 단서 찾아
‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해낼까?’ 우리 대학 연구진은 이 질문에서 출발해, 뇌가 단순히 총열량(칼로리)을 감지하는 수준을 넘어 특정 영양소, 특히 포도당을 선택적으로 인식할 수 있다는 사실을 입증했다. 이번 연구는 향후 식욕 조절 및 대사성 질환 치료 전략에 새로운 패러다임을 제시할 수 있을 것으로 기대된다.
우리 대학 생명과학과 서성배 교수 연구팀이 바이오및뇌공학과 박영균 교수팀, 생명과학과 이승희 교수팀, 뉴욕 알버트 아인슈타인 의과대학과의 협력을 통해, 배고픔 상태에서 포도당이 결핍된 동물이 장내의 포도당을 선택적으로 인식하고 선호하도록 유도하는 장-뇌 회로의 존재를 규명했다고 9일 밝혔다.
생물은 당, 단백질, 지방 등 다양한 영양소로부터 에너지를 얻는다. 기존 연구들은 장내 총열량 정보가 시상하부의 배고픔 뉴런(hunger neurons)을 억제함으로써 식욕을 조절한다는 사실을 밝혀왔으나, 특정 포도당에 특이적으로 반응하는 장-뇌 회로와 이에 반응하는 특정 뇌세포의 존재는 규명되지 않았다.
연구팀은 이번 연구를 통해 뇌의 기능에 필수적인 포도당을 감지하고 필요한 영양소에 대한 섭취 행동을 조절하는 ‘장-뇌 회로’를 밝혀내는 데 성공했다.
또한, 이 회로는 뇌의 ‘스트레스 반응 세포(CRF 뉴런*)’가 배고픔이나 외부 자극뿐만 아니라, 소장에 직접 유입된 특정 열량 영양소에 대해서도 초 단위로 반응하며, 특히 ‘포도당(D-glucose)’에 선택적으로 반응한다는 점을 처음으로 입증했다.
*CRF 뉴런: 우리 몸이 심리적·물리적 스트레스에 대응하는 핵심 생리 시스템은 시상하부-뇌하수체-부신 축(Hypothalamus-Pituitary-Adrenal Axis, HPA axis)이다. 이 축의 중심에는 시상하부에서 CRF(부신피질호르몬 방출인자)를 분비하는 뉴런이 있으며, 이들은 다양한 스트레스 자극에 반응해 코르티솔 분비를 유도하고, 생리 및 대사 균형을 유지하는 신경 내분비 조절의 중추로 알려져 있다.
연구팀은 실시간 뇌 속을 정밀하게 추적할 수 있는 광유전학 기반 신경 활성 조절 및 회로 추적 기법을 활용해서, 포도당(D-글루코스, L-글루코스,) 아미노산, 지방 등 다양한 영양소의 쥐의 소장 내 직접 주입하고 관찰했다.
그 결과, 뇌 시상하부의 ‘시상하부 시상핵(PVN)* 부위’에 있는 CRF 뉴런 중 D-글루코스(glucose) 포도당에만 선택적으로 반응하며, 다른 당류나 단백질·지방류에는 반응하지 않거나 반대 방향의 반응을 보이는 것을 확인했다. 이는 뇌가 장내 영양소가 유입 시 반응에 대해 단일 뇌세포 수준에서 어떤 방향성을 유도한다는 것을 처음 확인한 것을 의미한다.
* 시상하부 시상핵(paraventricular nucleus, PVN): 뇌의 시상하부(hypothalamus) 안에 있는 매우 중요한 신경핵(뉴런 무리)으로, 신체 항상성(몸의 균형 유지)을 조절하는 핵심 구조
또한, 연구팀은 소장의 포도당 감지 신호가 ‘척수신경’을 거쳐 뇌의 특정 부위(등쪽 외측 팔곁핵,parabrachial nucleus, PBNdl)을 통해 PVN의 CRF 뉴런으로 전달되는 특징적인 회로를 밝혀냈다. 반면, 아미노산이나 지방 등 기타 영양소는 미주신경(vagus nerve)이란 다른 통로로 뇌에 전달된다는 사실도 확인했다.
광유전학적 억제 실험에서도, 공복 상태의 생쥐에서 CRF 뉴런을 억제하면 동물은 더 이상 포도당을 선호하지 않게 됐으며, 이 회로가 영양소 선택에 있어 포도당 특이적 선호를 유도하는 데 필수적임이 드러났다.
이 연구는 서 교수가 뉴욕대(NYU) 재직 시절 초파리를 모델로, 장내 포도당(글루코스) 및 당을 선택적으로 감지하는 ‘DH44 뉴런’을 발견했던 점을 착안해, 포유류에서도 시상하부 뉴런이 포도당 특이적 반응에 있어 기능적 유사성을 보일 것이라는 가설에서 시작되었다.
이 가설을 입증하기 위해 서 교수 연구팀 김진은 박사(KAIST 박사 졸, 現 캘리포니아공과대학교 연수연구원)가 학위과정 중 생쥐 실험을 통해 배고픈 쥐는 장에 주입된 다양한 영양소 중 열량을 지닌 포도당을 선호하며, CRF 뉴런이 빠르고 특이적인 반응을 보인다는 사실을 확인했다.
또한, 같은 팀 정원교 연구원(KAIST 학사 졸, 現 캘리포니아공과대학교 박사과정)과 함께 실험과 모델링을 통해 CRF 뉴런의 중요성을 규명했고, 김신혜 박사는 협업을 통해 장-뇌 회로 중 특정 척추 신경세포가 장의 정보를 뇌로 전달 한다는 놀라운 발견을 입증했다.
김진은 박사와 김신혜 박사는 “이 연구는 ‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해내는가?’라는 단순하지만, 본질적인 질문에서 시작됐고, 이번 연구에서 장-뇌 연결 회로의 핵심 축인 척수신경의 역할을 규명하고 장내 특정 영양소를 감지한 후 이를 뇌에 전달하는 척수 기반 신경 회로가 우리 몸의 에너지 대사 조절과 항상성 유지에 핵심적일 것이라는 것을 밝혀냈다”고 말했다.
서성배 교수는 “이번 연구는 포도당에 특화된 장-뇌 신호 경로를 규명함으로써, 비만·당뇨병 등 대사 질환의 새로운 치료 표적을 제시할 수 있다”며 “향후 아미노산, 지방 등 다른 필수 영양소를 감지하는 유사 회로의 존재와 그 상호작용 메커니즘을 밝히는 연구로 확장될 예정”이라고 밝혔다.
우리 대학 김진은 박사, 김신혜 박사, 정원교 학생이 공동 제1 저자로 참여한 이번 연구의 결과는 국제 학술지 ‘뉴런(Neuron)’에 2025년 6월 20일 온라인 게재됐다.
※논문명: Encoding the glucose identity by discrete hypothalamic neurons via the gut-brain axis
※DOI: https://doi.org/10.1016/j.neuron.2025.05.024
이번 연구는 삼성미래기술육성사업, 한국연구재단 리더과제, 포스코 청암재단 사이언스 펠로십, 아산재단 의생명과학 장학사업, 기초과학연구원, KAIST KAIX 사업의 지원을 통해 수행됐다.
2025.07.09 조회수 407
뇌는 포도당을 구별한다..비만·당뇨 치료의 단서 찾아
‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해낼까?’ 우리 대학 연구진은 이 질문에서 출발해, 뇌가 단순히 총열량(칼로리)을 감지하는 수준을 넘어 특정 영양소, 특히 포도당을 선택적으로 인식할 수 있다는 사실을 입증했다. 이번 연구는 향후 식욕 조절 및 대사성 질환 치료 전략에 새로운 패러다임을 제시할 수 있을 것으로 기대된다.
우리 대학 생명과학과 서성배 교수 연구팀이 바이오및뇌공학과 박영균 교수팀, 생명과학과 이승희 교수팀, 뉴욕 알버트 아인슈타인 의과대학과의 협력을 통해, 배고픔 상태에서 포도당이 결핍된 동물이 장내의 포도당을 선택적으로 인식하고 선호하도록 유도하는 장-뇌 회로의 존재를 규명했다고 9일 밝혔다.
생물은 당, 단백질, 지방 등 다양한 영양소로부터 에너지를 얻는다. 기존 연구들은 장내 총열량 정보가 시상하부의 배고픔 뉴런(hunger neurons)을 억제함으로써 식욕을 조절한다는 사실을 밝혀왔으나, 특정 포도당에 특이적으로 반응하는 장-뇌 회로와 이에 반응하는 특정 뇌세포의 존재는 규명되지 않았다.
연구팀은 이번 연구를 통해 뇌의 기능에 필수적인 포도당을 감지하고 필요한 영양소에 대한 섭취 행동을 조절하는 ‘장-뇌 회로’를 밝혀내는 데 성공했다.
또한, 이 회로는 뇌의 ‘스트레스 반응 세포(CRF 뉴런*)’가 배고픔이나 외부 자극뿐만 아니라, 소장에 직접 유입된 특정 열량 영양소에 대해서도 초 단위로 반응하며, 특히 ‘포도당(D-glucose)’에 선택적으로 반응한다는 점을 처음으로 입증했다.
*CRF 뉴런: 우리 몸이 심리적·물리적 스트레스에 대응하는 핵심 생리 시스템은 시상하부-뇌하수체-부신 축(Hypothalamus-Pituitary-Adrenal Axis, HPA axis)이다. 이 축의 중심에는 시상하부에서 CRF(부신피질호르몬 방출인자)를 분비하는 뉴런이 있으며, 이들은 다양한 스트레스 자극에 반응해 코르티솔 분비를 유도하고, 생리 및 대사 균형을 유지하는 신경 내분비 조절의 중추로 알려져 있다.
연구팀은 실시간 뇌 속을 정밀하게 추적할 수 있는 광유전학 기반 신경 활성 조절 및 회로 추적 기법을 활용해서, 포도당(D-글루코스, L-글루코스,) 아미노산, 지방 등 다양한 영양소의 쥐의 소장 내 직접 주입하고 관찰했다.
그 결과, 뇌 시상하부의 ‘시상하부 시상핵(PVN)* 부위’에 있는 CRF 뉴런 중 D-글루코스(glucose) 포도당에만 선택적으로 반응하며, 다른 당류나 단백질·지방류에는 반응하지 않거나 반대 방향의 반응을 보이는 것을 확인했다. 이는 뇌가 장내 영양소가 유입 시 반응에 대해 단일 뇌세포 수준에서 어떤 방향성을 유도한다는 것을 처음 확인한 것을 의미한다.
* 시상하부 시상핵(paraventricular nucleus, PVN): 뇌의 시상하부(hypothalamus) 안에 있는 매우 중요한 신경핵(뉴런 무리)으로, 신체 항상성(몸의 균형 유지)을 조절하는 핵심 구조
또한, 연구팀은 소장의 포도당 감지 신호가 ‘척수신경’을 거쳐 뇌의 특정 부위(등쪽 외측 팔곁핵,parabrachial nucleus, PBNdl)을 통해 PVN의 CRF 뉴런으로 전달되는 특징적인 회로를 밝혀냈다. 반면, 아미노산이나 지방 등 기타 영양소는 미주신경(vagus nerve)이란 다른 통로로 뇌에 전달된다는 사실도 확인했다.
광유전학적 억제 실험에서도, 공복 상태의 생쥐에서 CRF 뉴런을 억제하면 동물은 더 이상 포도당을 선호하지 않게 됐으며, 이 회로가 영양소 선택에 있어 포도당 특이적 선호를 유도하는 데 필수적임이 드러났다.
이 연구는 서 교수가 뉴욕대(NYU) 재직 시절 초파리를 모델로, 장내 포도당(글루코스) 및 당을 선택적으로 감지하는 ‘DH44 뉴런’을 발견했던 점을 착안해, 포유류에서도 시상하부 뉴런이 포도당 특이적 반응에 있어 기능적 유사성을 보일 것이라는 가설에서 시작되었다.
이 가설을 입증하기 위해 서 교수 연구팀 김진은 박사(KAIST 박사 졸, 現 캘리포니아공과대학교 연수연구원)가 학위과정 중 생쥐 실험을 통해 배고픈 쥐는 장에 주입된 다양한 영양소 중 열량을 지닌 포도당을 선호하며, CRF 뉴런이 빠르고 특이적인 반응을 보인다는 사실을 확인했다.
또한, 같은 팀 정원교 연구원(KAIST 학사 졸, 現 캘리포니아공과대학교 박사과정)과 함께 실험과 모델링을 통해 CRF 뉴런의 중요성을 규명했고, 김신혜 박사는 협업을 통해 장-뇌 회로 중 특정 척추 신경세포가 장의 정보를 뇌로 전달 한다는 놀라운 발견을 입증했다.
김진은 박사와 김신혜 박사는 “이 연구는 ‘우리의 뇌는 어떻게 장내에서 흡수된 다양한 영양소 중 포도당을 구별해내는가?’라는 단순하지만, 본질적인 질문에서 시작됐고, 이번 연구에서 장-뇌 연결 회로의 핵심 축인 척수신경의 역할을 규명하고 장내 특정 영양소를 감지한 후 이를 뇌에 전달하는 척수 기반 신경 회로가 우리 몸의 에너지 대사 조절과 항상성 유지에 핵심적일 것이라는 것을 밝혀냈다”고 말했다.
서성배 교수는 “이번 연구는 포도당에 특화된 장-뇌 신호 경로를 규명함으로써, 비만·당뇨병 등 대사 질환의 새로운 치료 표적을 제시할 수 있다”며 “향후 아미노산, 지방 등 다른 필수 영양소를 감지하는 유사 회로의 존재와 그 상호작용 메커니즘을 밝히는 연구로 확장될 예정”이라고 밝혔다.
우리 대학 김진은 박사, 김신혜 박사, 정원교 학생이 공동 제1 저자로 참여한 이번 연구의 결과는 국제 학술지 ‘뉴런(Neuron)’에 2025년 6월 20일 온라인 게재됐다.
※논문명: Encoding the glucose identity by discrete hypothalamic neurons via the gut-brain axis
※DOI: https://doi.org/10.1016/j.neuron.2025.05.024
이번 연구는 삼성미래기술육성사업, 한국연구재단 리더과제, 포스코 청암재단 사이언스 펠로십, 아산재단 의생명과학 장학사업, 기초과학연구원, KAIST KAIX 사업의 지원을 통해 수행됐다.
2025.07.09 조회수 407 부작용·내성 극복한 신개념 칸디다증 치료제 개발
칸디다증은 곰팡이균(진균)의 일종인 칸디다(Candida)가 혈액을 통해 전신으로 퍼지며 장기 손상과 패혈증을 유발할 수 있는 치명적인 감염 질환이다. 최근 면역 저하 치료, 장기 이식, 의료기기 사용 등이 증가함에 따라 칸디다증 발병이 급증하고 있다. 한국 연구진이 기존 항진균제와 달리, 칸디다균에만 선택적으로 작용해 높은 치료 효능과 낮은 부작용을 동시에 갖춘 차세대 치료제를 개발하는데 성공했다.
우리 대학 생명과학과 정현정 교수 연구팀이 서울아산병원 정용필 교수팀과의 협력을 통해, 칸디다 세포벽의 두 핵심 효소를 동시에 저해하는 유전자 기반 나노치료제(FTNx)를 개발했다고 8일 밝혔다.
현재 사용 중인 칸디다의 항진균제들은 표적 선택성이 낮아 인체 세포에도 영향을 미칠 수 있으며, 이에 내성을 가지는 새로운 균의 출현으로 인해 치료 효과가 점차 떨어지고 있다. 특히 면역력이 저하된 환자들에게는 감염의 진행이 빠르고 예후도 좋지 않아, 기존 치료제의 한계를 극복할 수 있는 새로운 치료법의 개발이 시급한 상황이다.
이에 연구팀이 개발한 치료제는 전신 투여가 가능하며, 유전자 억제 기술과 나노소재 기술을 융합함으로써 기존 화합물 기반의 약물들이 가지는 구조적 한계를 효과적으로 극복하고, 칸디다균에만 선택적으로 치료하는데 성공했다.
연구팀은 칸디다라는 곰팡이균의 세포벽을 만드는 데 중요한 두 가지 효소 — β‑1,3‑글루칸 합성효소(FKS1)와 키틴 합성효소(CHS3)를 동시에 표적하는 짧은 DNA 조각(antisense oligonucleotide, ASO)을 탑재한 금 나노입자 기반의 복합체를 제작했다.
여기에 칸디다 세포벽의 특정 당지질 구조(당과 지방이 결합된 구조)와 결합하는 표면 코팅 기술을 적용하여 표적유도장치를 장착함으로써, 인체 세포에는 아예 전달되지 않고 칸디다에만 선택적으로 작용하는 정밀 타겟팅 효과를 구현하는 데 성공했다.
이 복합체는 칸디다 세포 내로 진입한 후, FKS1 및 CHS3의 유전자가 만들어내는 mRNA를 잘라버려서 번역을 억제해 세포벽 성분인 β‑1,3‑글루칸과 키틴의 합성을 동시에 차단한다. 이로 인해 칸디다 세포벽은 구조적 안정성을 유지하지 못하고 붕괴되며, 세균의 생존과 증식이 억제된다.
실제로 쥐에서 전신 칸디다증 모델 실험을 통해 치료 효과를 검증한 결과, 치료군에서 칸디다의 장기 내 균 수 감소, 면역 반응 정상화, 그리고 생존율의 유의미한 증가가 관찰됐다.
연구를 주도한 정현정 교수는 “이번 연구는 기존 치료제가 인체 독성과 약제내성 확산 문제를 극복하는 방법을 제시하며, 유전자 치료의 전신 감염 적용 가능성을 보여주는 중요한 전환점”이라며, “향후 임상 적용을 위한 투여 방식 최적화 및 독성 검증 연구를 지속적으로 진행할 계획”이라고 밝혔다.
해당 연구는 생명과학과 정주연 학생 및 서울아산병원 홍윤경 박사가 제1 저자로 참여했으며, 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 7월 1일 자로 게재됐다.
※ 논문명 : Effective treatment of systemic candidiasis by synergistic targeting of cell wall synthesis
※ DOI : 10.1038/s41467-025-60684-7
이번 연구는 보건복지부 및 한국연구재단의 지원을 받아 수행됐다.
2025.07.08 조회수 779
부작용·내성 극복한 신개념 칸디다증 치료제 개발
칸디다증은 곰팡이균(진균)의 일종인 칸디다(Candida)가 혈액을 통해 전신으로 퍼지며 장기 손상과 패혈증을 유발할 수 있는 치명적인 감염 질환이다. 최근 면역 저하 치료, 장기 이식, 의료기기 사용 등이 증가함에 따라 칸디다증 발병이 급증하고 있다. 한국 연구진이 기존 항진균제와 달리, 칸디다균에만 선택적으로 작용해 높은 치료 효능과 낮은 부작용을 동시에 갖춘 차세대 치료제를 개발하는데 성공했다.
우리 대학 생명과학과 정현정 교수 연구팀이 서울아산병원 정용필 교수팀과의 협력을 통해, 칸디다 세포벽의 두 핵심 효소를 동시에 저해하는 유전자 기반 나노치료제(FTNx)를 개발했다고 8일 밝혔다.
현재 사용 중인 칸디다의 항진균제들은 표적 선택성이 낮아 인체 세포에도 영향을 미칠 수 있으며, 이에 내성을 가지는 새로운 균의 출현으로 인해 치료 효과가 점차 떨어지고 있다. 특히 면역력이 저하된 환자들에게는 감염의 진행이 빠르고 예후도 좋지 않아, 기존 치료제의 한계를 극복할 수 있는 새로운 치료법의 개발이 시급한 상황이다.
이에 연구팀이 개발한 치료제는 전신 투여가 가능하며, 유전자 억제 기술과 나노소재 기술을 융합함으로써 기존 화합물 기반의 약물들이 가지는 구조적 한계를 효과적으로 극복하고, 칸디다균에만 선택적으로 치료하는데 성공했다.
연구팀은 칸디다라는 곰팡이균의 세포벽을 만드는 데 중요한 두 가지 효소 — β‑1,3‑글루칸 합성효소(FKS1)와 키틴 합성효소(CHS3)를 동시에 표적하는 짧은 DNA 조각(antisense oligonucleotide, ASO)을 탑재한 금 나노입자 기반의 복합체를 제작했다.
여기에 칸디다 세포벽의 특정 당지질 구조(당과 지방이 결합된 구조)와 결합하는 표면 코팅 기술을 적용하여 표적유도장치를 장착함으로써, 인체 세포에는 아예 전달되지 않고 칸디다에만 선택적으로 작용하는 정밀 타겟팅 효과를 구현하는 데 성공했다.
이 복합체는 칸디다 세포 내로 진입한 후, FKS1 및 CHS3의 유전자가 만들어내는 mRNA를 잘라버려서 번역을 억제해 세포벽 성분인 β‑1,3‑글루칸과 키틴의 합성을 동시에 차단한다. 이로 인해 칸디다 세포벽은 구조적 안정성을 유지하지 못하고 붕괴되며, 세균의 생존과 증식이 억제된다.
실제로 쥐에서 전신 칸디다증 모델 실험을 통해 치료 효과를 검증한 결과, 치료군에서 칸디다의 장기 내 균 수 감소, 면역 반응 정상화, 그리고 생존율의 유의미한 증가가 관찰됐다.
연구를 주도한 정현정 교수는 “이번 연구는 기존 치료제가 인체 독성과 약제내성 확산 문제를 극복하는 방법을 제시하며, 유전자 치료의 전신 감염 적용 가능성을 보여주는 중요한 전환점”이라며, “향후 임상 적용을 위한 투여 방식 최적화 및 독성 검증 연구를 지속적으로 진행할 계획”이라고 밝혔다.
해당 연구는 생명과학과 정주연 학생 및 서울아산병원 홍윤경 박사가 제1 저자로 참여했으며, 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 7월 1일 자로 게재됐다.
※ 논문명 : Effective treatment of systemic candidiasis by synergistic targeting of cell wall synthesis
※ DOI : 10.1038/s41467-025-60684-7
이번 연구는 보건복지부 및 한국연구재단의 지원을 받아 수행됐다.
2025.07.08 조회수 779 항암제 내성 없앤다! 당뇨병 등 난치성 질환 치료도 기대
암 치료의 큰 걸림돌 중 하나는 항암제에 대한 암세포의 내성이다. 기존에는 내성 암세포를 제거할 수 있는 새로운 표적을 찾는 방식이 주를 이뤘지만, 오히려 더 강한 내성을 유도할 수 있다는 한계가 있었다. 이에 우리 연구진이 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 자동으로 예측하는 컴퓨터 기반 방법론을 개발했다. 이 기술은 다양한 암 치료뿐 아니라 당뇨병 등 난치성 대사 질환에도 활용될 수 있어 주목된다.
우리 대학 생명화학공학과 김현욱 교수와 김유식 교수 연구팀이 인체 대사를 시뮬레이션할 수 있는 컴퓨터 모델인 대사 네트워크 모델을 활용해, 항암제에 내성을 가진 유방암 세포를 약물에 민감화시킬 수 있는 새로운 약물 표적을 예측하는 컴퓨터 기반 방법론을 개발했다고 7일 밝혔다.
연구진은 암세포의 대사 변형이 약물 내성 형성에 관여하는 주요한 특징으로 주목하고, 항암제 내성 유방암 세포의 대사를 조절해 약물 반응성을 높일 유전자 표적을 예측하는 대사 네트워크 모델 기반 방법론을 개발했다.
연구진은 먼저 독소루비신(doxorubicin)과 파클리탁셀(paclitaxel)에 각각 내성을 지닌 MCF7 유방암 세포주에서 얻은 단백체 데이터를 통합해 세포별 대사 네트워크 모델을 구축했다. 이어 모든 대사 유전자에 대해서 유전자 낙아웃(결실) 시뮬레이션*을 수행하고, 그 결과를 분석했다.
*유전자 낙아웃 시뮬레이션: 특정 유전자를 가상으로 제거한 상태에서 생물학적 네트워크의 변화를 계산적으로 예측하는 방법
그 결과, 특정 유전자의 단백질을 억제하면, 항암제에 잘 듣지 않던 내성 암세포가 다시 항암제에 반응하도록 만들 수 있다는 것을 알아냈다. 독소루비신 내성 세포에서는 GOT1 유전자를, 파클리탁셀 내성 세포에서는 GPI 유전자를 선별했으며, 두 약물 공통으로는 SLC1A5 유전자를 표적으로 선별했다.
예측하여 선별한 유전자를 실제로 억제해 본 결과, 내성 암세포가 항암제에 다시 반응하게 됨을 실험적으로 검증했다.
나아가 같은 항암제에 내성을 갖는 다른 종류의 유방암 세포에서도 같은 유전자를 억제했을 때 항암제에 다시 민감해지는 효과가 일관되게 나타나는 것을 확인할 수 있었다.
김유식 교수는 “세포 대사는 감염병, 퇴행성 질환 등 다양한 난치성 질환에서 중요한 역할을 한다”며, “이번에 개발된 대사 조절 스위치 예측 기술은 약물 내성 유방암 치료를 넘어, 치료제가 없는 다양한 대사 질환에도 적용될 수 있는 기반 기술이 될 것”이라고 말했다.
연구를 총괄한 김현욱 교수는 “이번 연구의 가장 큰 의의는 컴퓨터 시뮬레이션만과 최소한의 실험 데이터만으로 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 정밀하게 예측할 수 있다는 점”이라며, “이 방법론은 다양한 암종과 대사 관련 난치성 질환의 새로운 치료 표적 발굴에도 폭넓게 활용될 수 있을 것”이라고 강조했다.
우리 대학 생명화학공학과 임진아 박사과정생과 정해덕 박사과정생이 공동 제1 저자로 참여한 이번 연구는 생명과학·물리·공학·사회과학 등 다양한 분야의 최고 수준 연구를 다루는 다학제 국제 학술지인 미국국립과학원회보(PNAS) 6월 25일 자 온라인에 게재됐다.
※ 논문명 : Genome-scale knockout simulation and clustering analysis of drug-resistant breast cancer cells reveal drug sensitization targets
※ 저자 정보 : 임진아(한국과학기술원, 공동 제1 저자), 정해덕(한국과학기술원, 공동 제1 저자), 유한석(서울대학교병원, 교신저자), 김유식(한국과학기술원, 교신저자), 김현욱(한국과학기술원, 교신저자) 포함 총 10명
※ DOI: https://doi.org/10.1073/pnas.2425384122
이번 연구는 과학기술정보통신부 한국전자통신연구원 및 한국연구재단의 지원을 받아 수행됐다.
2025.07.07 조회수 663
항암제 내성 없앤다! 당뇨병 등 난치성 질환 치료도 기대
암 치료의 큰 걸림돌 중 하나는 항암제에 대한 암세포의 내성이다. 기존에는 내성 암세포를 제거할 수 있는 새로운 표적을 찾는 방식이 주를 이뤘지만, 오히려 더 강한 내성을 유도할 수 있다는 한계가 있었다. 이에 우리 연구진이 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 자동으로 예측하는 컴퓨터 기반 방법론을 개발했다. 이 기술은 다양한 암 치료뿐 아니라 당뇨병 등 난치성 대사 질환에도 활용될 수 있어 주목된다.
우리 대학 생명화학공학과 김현욱 교수와 김유식 교수 연구팀이 인체 대사를 시뮬레이션할 수 있는 컴퓨터 모델인 대사 네트워크 모델을 활용해, 항암제에 내성을 가진 유방암 세포를 약물에 민감화시킬 수 있는 새로운 약물 표적을 예측하는 컴퓨터 기반 방법론을 개발했다고 7일 밝혔다.
연구진은 암세포의 대사 변형이 약물 내성 형성에 관여하는 주요한 특징으로 주목하고, 항암제 내성 유방암 세포의 대사를 조절해 약물 반응성을 높일 유전자 표적을 예측하는 대사 네트워크 모델 기반 방법론을 개발했다.
연구진은 먼저 독소루비신(doxorubicin)과 파클리탁셀(paclitaxel)에 각각 내성을 지닌 MCF7 유방암 세포주에서 얻은 단백체 데이터를 통합해 세포별 대사 네트워크 모델을 구축했다. 이어 모든 대사 유전자에 대해서 유전자 낙아웃(결실) 시뮬레이션*을 수행하고, 그 결과를 분석했다.
*유전자 낙아웃 시뮬레이션: 특정 유전자를 가상으로 제거한 상태에서 생물학적 네트워크의 변화를 계산적으로 예측하는 방법
그 결과, 특정 유전자의 단백질을 억제하면, 항암제에 잘 듣지 않던 내성 암세포가 다시 항암제에 반응하도록 만들 수 있다는 것을 알아냈다. 독소루비신 내성 세포에서는 GOT1 유전자를, 파클리탁셀 내성 세포에서는 GPI 유전자를 선별했으며, 두 약물 공통으로는 SLC1A5 유전자를 표적으로 선별했다.
예측하여 선별한 유전자를 실제로 억제해 본 결과, 내성 암세포가 항암제에 다시 반응하게 됨을 실험적으로 검증했다.
나아가 같은 항암제에 내성을 갖는 다른 종류의 유방암 세포에서도 같은 유전자를 억제했을 때 항암제에 다시 민감해지는 효과가 일관되게 나타나는 것을 확인할 수 있었다.
김유식 교수는 “세포 대사는 감염병, 퇴행성 질환 등 다양한 난치성 질환에서 중요한 역할을 한다”며, “이번에 개발된 대사 조절 스위치 예측 기술은 약물 내성 유방암 치료를 넘어, 치료제가 없는 다양한 대사 질환에도 적용될 수 있는 기반 기술이 될 것”이라고 말했다.
연구를 총괄한 김현욱 교수는 “이번 연구의 가장 큰 의의는 컴퓨터 시뮬레이션만과 최소한의 실험 데이터만으로 내성 암세포를 다시 약물에 반응하게 만들 수 있는 핵심 유전자를 정밀하게 예측할 수 있다는 점”이라며, “이 방법론은 다양한 암종과 대사 관련 난치성 질환의 새로운 치료 표적 발굴에도 폭넓게 활용될 수 있을 것”이라고 강조했다.
우리 대학 생명화학공학과 임진아 박사과정생과 정해덕 박사과정생이 공동 제1 저자로 참여한 이번 연구는 생명과학·물리·공학·사회과학 등 다양한 분야의 최고 수준 연구를 다루는 다학제 국제 학술지인 미국국립과학원회보(PNAS) 6월 25일 자 온라인에 게재됐다.
※ 논문명 : Genome-scale knockout simulation and clustering analysis of drug-resistant breast cancer cells reveal drug sensitization targets
※ 저자 정보 : 임진아(한국과학기술원, 공동 제1 저자), 정해덕(한국과학기술원, 공동 제1 저자), 유한석(서울대학교병원, 교신저자), 김유식(한국과학기술원, 교신저자), 김현욱(한국과학기술원, 교신저자) 포함 총 10명
※ DOI: https://doi.org/10.1073/pnas.2425384122
이번 연구는 과학기술정보통신부 한국전자통신연구원 및 한국연구재단의 지원을 받아 수행됐다.
2025.07.07 조회수 663 마이크로 OLED로 난치성 뇌질환 치료 '게임 체인저' 기술 제시
광유전학 기술은 빛에 반응하는 광 단백질이 발현된 뉴런에 특정 파장의 빛 자극을 통해 뉴런의 활성을 조절하는 기술로 다양한 뇌질환의 원인을 규명하며 난치성 뇌질환의 새로운 치료 방법을 개발할 가능성을 열고 있다. 이 기술은 인체의 뇌에 삽입하여 자극을 주는 의료 기기인 ‘뉴럴 프로브’를 통해 정확하게 자극하고 무른 뇌 조직의 손상을 최소화해야 한다. 이에 우리 연구진이 마이크로 OLED를 활용해 얇고 유연한 인체 삽입형 의료기기로 구현함으로써 뉴럴 프로브의 새로운 패러다임을 제시했다.
우리 대학 전기및전자공학부 최경철 교수와 이현주 연구팀이 공동 연구를 통해, 유연한 마이크로 OLED가 집적된 광유전학용 뉴럴 프로브 개발에 성공했다고 6일 밝혔다.
광유전학 연구에서 주요 기술은 광원의 빛을 뇌로 전달하는 방식으로 외부 광원으로부터의 깊은 뇌 영역까지 빛을 전달하기 위해 수십 년간 광섬유를 사용해 왔다. 하지만 단일 뉴런을 자극하기 위한 유연 광섬유, 초미세 광원 집적 뉴럴 프로브 등 관련 연구가 이뤄지고 있다.
연구팀은 마이크로 OLED는 높은 공간적 해상도와 유연성을 가져, 매우 작은 영역의 뉴런에서도 정확하게 빛을 조사할 수 있어 세밀한 뇌 회로 분석이 가능하고 동물의 움직임에 불편함을 주지 않으면서 부작용을 최소화하는 장점에 주목했다. 그뿐만 아니라, 미세한 파장 조절을 통해 정밀한 빛 조절이 가능하며 다중 자극을 통한 복잡한 뇌 기능 연구가 가능하다.
하지만, 체내 수분이나 물에 의해 전기적 특성이 쉽게 열화되기 때문에 생체 삽입형 전자장치로 활용되는데 한계가 있었고, 얇고 유연한 탐침 위 고해상도 집적 공정에 대한 세부적인 최적화도 필요했다.
공동연구팀은 수분과 산소가 많은 생체 내 환경에서 OLED의 구동 신뢰성을 높이며 생체 삽입 시 조직 손상을 최소화하고자, 산화알루미늄/파릴렌-C(Al2O3/parylene-C)로 구성된 초박막 유연 봉지막*을 얇은 탐침 형태인 260~600마이크로미터(μm) 너비로 패터닝해 생체친화성을 유지했다.
* 봉지막: 소자를 외부 환경요인인 산소와 물 분자로부터 완전히 차단하는 막 기술로 소자의 수명을 유지시키고 신뢰성을 줌
또한, 고해상도 마이크로 OLED를 집적함에 있어 전체 소자의 유연성과 생체친화성을 유지하기 위해, 봉지막과 동일한 생체친화 재료인 파릴렌-C(parylene-C)를 활용하였다. 아울러, 인접한 OLED 픽셀 간 전기적 간섭 현상을 제거하고 각 픽셀을 공간적으로 분리하기 위해 구조적 레이어인 ‘화소 정의막(pixel define layer)’을 도입함으로써, 8개의 마이크로 OLED를 독립적으로 개별 구동할 수 있도록 구현했다.
마지막으로, 소자 내 다중 박막층의 잔류 응력과 두께를 정밀하게 조절함으로써, 생체 내 환경에서도 소자의 유연성을 유지할 수 있도록 하였다. 이를 통해 외부 셔틀이나 바늘과 같은 보조 장치 없이도 단일 탐침만으로 휘어짐 없이 삽입이 가능하도록, 소자의 기계적 스트레스를 최적화해 설계했다.
결론적으로 연구팀은 채널로돕신2의 활성화에 적합한 470나노미터(nm) 파장에서 1밀리와트/제곱밀리미터(mW/mm2)이상의 광 파워 밀도를 가지는 즉, 광유전학 및 생체조직 자극 응용에서 상당히 높은 수준의 광출력을 가진 마이크로 OLED 집적 유연 뉴럴 프로브를 개발했다.
또한, 초박막 유연 봉지막은 2.66×10⁻⁵ g/m²/day의 낮은 수분 투습률을 보이며 소자 수명은 10년 이상 유지할 수 있고, 패릴렌-C(parylene-C)를 기반으로 생체 내 높은 봉지막 성능을 발휘하며, 전기적 간섭과 휨 이슈 없이 집적된 OLED의 개별 구동을 성공적으로 시연했다.
이번 연구를 주도한 최경철 교수 연구팀의 이소민 박사는 “고유연·고해상도의 마이크로 OLED를 얇은 유연 탐침 위에 집적하는 세부 공정 및 생체 적용성, 친화성 향상에 집중했다”며 “이번 연구는 기존 연구를 넘어 유연 프로브 형태에 최초로 개발해 보고된 사례로, 유연 OLED가 인체 삽입형 측정 및 치료 의료기기로서의 새로운 패러다임을 제시할 것으로 기대된다”고 말했다.
이번 연구는 전기및전자공학부 이소민 박사가 제1 저자로 나노 분야의 권위 있는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials, IF 18.5)'에 지난 3월 26일 字로 온라인 게재됐으며, 전면 표지 논문으로 이번 7월에 선정됐다.
※ 논문명: Advanced Micro-OLED Integration on Thin and Flexible Polymer Neural Probes for Targeted Optogenetic Stimulation
※ DOI: https://doi.org/10.1002/adfm.202420758
한편, 이번 연구는 과학기술정보통신부 한국연구재단의 전자약 기술개발사업(연구 과제명: 뇌인지-정서 향상 빛 자극 전자약의 핵심원천기술 개발 및 생체 적용가능성 검증)의 지원을 받아 수행됐다.
2025.07.07 조회수 534
마이크로 OLED로 난치성 뇌질환 치료 '게임 체인저' 기술 제시
광유전학 기술은 빛에 반응하는 광 단백질이 발현된 뉴런에 특정 파장의 빛 자극을 통해 뉴런의 활성을 조절하는 기술로 다양한 뇌질환의 원인을 규명하며 난치성 뇌질환의 새로운 치료 방법을 개발할 가능성을 열고 있다. 이 기술은 인체의 뇌에 삽입하여 자극을 주는 의료 기기인 ‘뉴럴 프로브’를 통해 정확하게 자극하고 무른 뇌 조직의 손상을 최소화해야 한다. 이에 우리 연구진이 마이크로 OLED를 활용해 얇고 유연한 인체 삽입형 의료기기로 구현함으로써 뉴럴 프로브의 새로운 패러다임을 제시했다.
우리 대학 전기및전자공학부 최경철 교수와 이현주 연구팀이 공동 연구를 통해, 유연한 마이크로 OLED가 집적된 광유전학용 뉴럴 프로브 개발에 성공했다고 6일 밝혔다.
광유전학 연구에서 주요 기술은 광원의 빛을 뇌로 전달하는 방식으로 외부 광원으로부터의 깊은 뇌 영역까지 빛을 전달하기 위해 수십 년간 광섬유를 사용해 왔다. 하지만 단일 뉴런을 자극하기 위한 유연 광섬유, 초미세 광원 집적 뉴럴 프로브 등 관련 연구가 이뤄지고 있다.
연구팀은 마이크로 OLED는 높은 공간적 해상도와 유연성을 가져, 매우 작은 영역의 뉴런에서도 정확하게 빛을 조사할 수 있어 세밀한 뇌 회로 분석이 가능하고 동물의 움직임에 불편함을 주지 않으면서 부작용을 최소화하는 장점에 주목했다. 그뿐만 아니라, 미세한 파장 조절을 통해 정밀한 빛 조절이 가능하며 다중 자극을 통한 복잡한 뇌 기능 연구가 가능하다.
하지만, 체내 수분이나 물에 의해 전기적 특성이 쉽게 열화되기 때문에 생체 삽입형 전자장치로 활용되는데 한계가 있었고, 얇고 유연한 탐침 위 고해상도 집적 공정에 대한 세부적인 최적화도 필요했다.
공동연구팀은 수분과 산소가 많은 생체 내 환경에서 OLED의 구동 신뢰성을 높이며 생체 삽입 시 조직 손상을 최소화하고자, 산화알루미늄/파릴렌-C(Al2O3/parylene-C)로 구성된 초박막 유연 봉지막*을 얇은 탐침 형태인 260~600마이크로미터(μm) 너비로 패터닝해 생체친화성을 유지했다.
* 봉지막: 소자를 외부 환경요인인 산소와 물 분자로부터 완전히 차단하는 막 기술로 소자의 수명을 유지시키고 신뢰성을 줌
또한, 고해상도 마이크로 OLED를 집적함에 있어 전체 소자의 유연성과 생체친화성을 유지하기 위해, 봉지막과 동일한 생체친화 재료인 파릴렌-C(parylene-C)를 활용하였다. 아울러, 인접한 OLED 픽셀 간 전기적 간섭 현상을 제거하고 각 픽셀을 공간적으로 분리하기 위해 구조적 레이어인 ‘화소 정의막(pixel define layer)’을 도입함으로써, 8개의 마이크로 OLED를 독립적으로 개별 구동할 수 있도록 구현했다.
마지막으로, 소자 내 다중 박막층의 잔류 응력과 두께를 정밀하게 조절함으로써, 생체 내 환경에서도 소자의 유연성을 유지할 수 있도록 하였다. 이를 통해 외부 셔틀이나 바늘과 같은 보조 장치 없이도 단일 탐침만으로 휘어짐 없이 삽입이 가능하도록, 소자의 기계적 스트레스를 최적화해 설계했다.
결론적으로 연구팀은 채널로돕신2의 활성화에 적합한 470나노미터(nm) 파장에서 1밀리와트/제곱밀리미터(mW/mm2)이상의 광 파워 밀도를 가지는 즉, 광유전학 및 생체조직 자극 응용에서 상당히 높은 수준의 광출력을 가진 마이크로 OLED 집적 유연 뉴럴 프로브를 개발했다.
또한, 초박막 유연 봉지막은 2.66×10⁻⁵ g/m²/day의 낮은 수분 투습률을 보이며 소자 수명은 10년 이상 유지할 수 있고, 패릴렌-C(parylene-C)를 기반으로 생체 내 높은 봉지막 성능을 발휘하며, 전기적 간섭과 휨 이슈 없이 집적된 OLED의 개별 구동을 성공적으로 시연했다.
이번 연구를 주도한 최경철 교수 연구팀의 이소민 박사는 “고유연·고해상도의 마이크로 OLED를 얇은 유연 탐침 위에 집적하는 세부 공정 및 생체 적용성, 친화성 향상에 집중했다”며 “이번 연구는 기존 연구를 넘어 유연 프로브 형태에 최초로 개발해 보고된 사례로, 유연 OLED가 인체 삽입형 측정 및 치료 의료기기로서의 새로운 패러다임을 제시할 것으로 기대된다”고 말했다.
이번 연구는 전기및전자공학부 이소민 박사가 제1 저자로 나노 분야의 권위 있는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials, IF 18.5)'에 지난 3월 26일 字로 온라인 게재됐으며, 전면 표지 논문으로 이번 7월에 선정됐다.
※ 논문명: Advanced Micro-OLED Integration on Thin and Flexible Polymer Neural Probes for Targeted Optogenetic Stimulation
※ DOI: https://doi.org/10.1002/adfm.202420758
한편, 이번 연구는 과학기술정보통신부 한국연구재단의 전자약 기술개발사업(연구 과제명: 뇌인지-정서 향상 빛 자극 전자약의 핵심원천기술 개발 및 생체 적용가능성 검증)의 지원을 받아 수행됐다.
2025.07.07 조회수 534 60% 이상 챗GPT 추론 성능 향상할 NPU 핵심기술 개발
오픈AI 챗GPT4, 구글 Gemnini 2.5 등 최신 생성형AI 모델들은 높은 메모리 대역폭(Bandwidth) 뿐만 아니라 많은 메모리 용량(Capacity)를 필요로 한다. 마이크로소프트, 구글 등 생성형AI 클라우드 운영 기업들이 엔비디아 GPU를 수십만 장씩 구매하는 이유다. 이런 고성능 AI 인프라 구축의 핵심 난제를 해소할 방안으로, 한국 연구진이 최신 GPU 대비 약 44% 낮은 전력 소모에도 평균 60% 이상 생성형 AI 모델의 추론 성능을 향상할 NPU(신경망처리장치)* 핵심 기술을 개발하는데 성공했다.
*NPU(Neural Processing Unit): 인공신경망(Neural Network)을 빠르게 처리하기 위해 만든 AI 전용 반도체 칩
우리 대학 전산학부 박종세 교수 연구팀과 (주)하이퍼엑셀(전기및전자공학부 김주영 교수 창업기업)이 연구 협력을 통해, 챗GPT와 같은 생성형AI 클라우드에 특화된 고성능·저전력의 NPU(신경망처리장치) 핵심기술을 개발했다고 4일 밝혔다.
연구팀이 제안한 기술은 컴퓨터 아키텍처 분야에서 최고 권위를 자랑하는 국제 학회인 ‘2025 국제 컴퓨터구조 심포지엄(International Symposium on Computer Architecture, ISCA 2025)’에 채택됐다.
이번 연구의 핵심은 추론 과정에서 경량화를 통해 정확도 손실을 최소화하면서도 메모리 병목 문제를 해결해 대규모 생성형AI 서비스의 성능을 개선하는 것이다. 이번 연구는 AI인프라의 핵심 구성요소인 AI반도체와 AI시스템SW를 통합 설계했다는 점에서 그 가치를 높게 인정받았다.
기존 GPU 기반 AI 인프라는 높은 메모리 대역폭과 메모리 용량 요구를 충족하기 위해 다수의 GPU 디바이스가 필요한 반면, 이번 기술은 메모리 사용의 대부분을 차지하는 KV 캐시의 양자화*를 통해 적은 수의 NPU 디바이스만으로 동일 수준의 AI 인프라를 구성할 수 있어, 생성형 AI 클라우드 구축 비용을 크게 절감할 수 있다.
*KV 캐시(Key-Value Cache)의 양자화: 생성형 AI 모델을 작동할 때 성능을 높이기 위해 사용하는 일종의 임시 저장 공간에 데이터 크기를 줄이는 것을 의미(32비트로 저장된 수를 4비트로 바꾸면, 데이터 크기는 1/8로 줄어듬)
연구팀은 기존 NPU 아키텍처의 연산 로직을 변경하지 않으면서 메모리 인터페이스와 통합될 수 있도록 설계했다. 이번 하드웨어 아키텍처 기술은 제안된 양자화 알고리즘을 구현할 뿐만 아니라, 제한된 메모리 대역폭 및 용량을 효율적으로 활용하기 위한 페이지 단위 메모리 관리 기법*과 양자화된 KV 캐시에 최적화된 새로운 인코딩 기법 등을 개발했다.
*페이지 단위 메모리 관리 기법: CPU처럼 메모리 주소를 가상화하여 NPU 내부에서 일관된 방식으로 접근할 수 있게 함
또한, 최신 GPU 대비 비용·전력 효율성이 우수한 NPU 기반 AI 클라우드를 구성할 경우, NPU의 고성능, 저전력 특성을 활용해 운영 비용 역시 크게 절감할 수 있을 것으로 기대된다.
박종세 교수는 “이 연구는 (주)하이퍼엑셀과의 공동연구를 통해 생성형AI 추론 경량화 알고리즘에서 그 해법을 찾았고 ‘메모리 문제’를 해결할 수 있는 NPU 핵심기술 개발에 성공했다. 이 기술을 통해 추론의 정확도를 유지하면서 메모리 요구량을 줄이는 경량화 기법과, 이에 최적화된 하드웨어 설계를 결합해 최신 GPU 대비 평균 60% 이상 성능이 향상된 NPU를 구현했다” 고 말했다.
이어 “이 기술은 생성형AI에 특화된 고성능·저전력 인프라 구현 가능성을 입증했으며, AI클라우드 데이터센터뿐 아니라 능동적인 실행형 AI인 ‘에이전틱 AI ’등으로 대표되는 AI 대전환(AX) 환경에서도 핵심 역할이 기대된다”고 강조했다.
이 연구는 김민수 박사과정 학생과 ㈜하이퍼엑셀 홍성민 박사가 공동 제1 저자로 지난 6월 21일부터 6월 25일까지 일본 도쿄에서 열린 ‘2025 국제 컴퓨터구조 심포지엄(ISCA)’에 발표됐다. 국제적 저명학회인 ISCA는 올해는 570편의 논문이 제출됐으며 그중 127편 만이 채택됐다. (채택률 22.7%).
※논문 제목: Oaken: Fast and Efficient LLM Serving with Online-Offline Hybrid KV Cache Quantization
※DOI: https://doi.org/10.1145/3695053.3731019
한편 이번 연구는 한국연구재단 우수신진연구자지원사업, 정보통신기획평가원(IITP), 인공지능반도체대학원지원사업의 지원을 받아 수행됐다.
2025.07.04 조회수 927
60% 이상 챗GPT 추론 성능 향상할 NPU 핵심기술 개발
오픈AI 챗GPT4, 구글 Gemnini 2.5 등 최신 생성형AI 모델들은 높은 메모리 대역폭(Bandwidth) 뿐만 아니라 많은 메모리 용량(Capacity)를 필요로 한다. 마이크로소프트, 구글 등 생성형AI 클라우드 운영 기업들이 엔비디아 GPU를 수십만 장씩 구매하는 이유다. 이런 고성능 AI 인프라 구축의 핵심 난제를 해소할 방안으로, 한국 연구진이 최신 GPU 대비 약 44% 낮은 전력 소모에도 평균 60% 이상 생성형 AI 모델의 추론 성능을 향상할 NPU(신경망처리장치)* 핵심 기술을 개발하는데 성공했다.
*NPU(Neural Processing Unit): 인공신경망(Neural Network)을 빠르게 처리하기 위해 만든 AI 전용 반도체 칩
우리 대학 전산학부 박종세 교수 연구팀과 (주)하이퍼엑셀(전기및전자공학부 김주영 교수 창업기업)이 연구 협력을 통해, 챗GPT와 같은 생성형AI 클라우드에 특화된 고성능·저전력의 NPU(신경망처리장치) 핵심기술을 개발했다고 4일 밝혔다.
연구팀이 제안한 기술은 컴퓨터 아키텍처 분야에서 최고 권위를 자랑하는 국제 학회인 ‘2025 국제 컴퓨터구조 심포지엄(International Symposium on Computer Architecture, ISCA 2025)’에 채택됐다.
이번 연구의 핵심은 추론 과정에서 경량화를 통해 정확도 손실을 최소화하면서도 메모리 병목 문제를 해결해 대규모 생성형AI 서비스의 성능을 개선하는 것이다. 이번 연구는 AI인프라의 핵심 구성요소인 AI반도체와 AI시스템SW를 통합 설계했다는 점에서 그 가치를 높게 인정받았다.
기존 GPU 기반 AI 인프라는 높은 메모리 대역폭과 메모리 용량 요구를 충족하기 위해 다수의 GPU 디바이스가 필요한 반면, 이번 기술은 메모리 사용의 대부분을 차지하는 KV 캐시의 양자화*를 통해 적은 수의 NPU 디바이스만으로 동일 수준의 AI 인프라를 구성할 수 있어, 생성형 AI 클라우드 구축 비용을 크게 절감할 수 있다.
*KV 캐시(Key-Value Cache)의 양자화: 생성형 AI 모델을 작동할 때 성능을 높이기 위해 사용하는 일종의 임시 저장 공간에 데이터 크기를 줄이는 것을 의미(32비트로 저장된 수를 4비트로 바꾸면, 데이터 크기는 1/8로 줄어듬)
연구팀은 기존 NPU 아키텍처의 연산 로직을 변경하지 않으면서 메모리 인터페이스와 통합될 수 있도록 설계했다. 이번 하드웨어 아키텍처 기술은 제안된 양자화 알고리즘을 구현할 뿐만 아니라, 제한된 메모리 대역폭 및 용량을 효율적으로 활용하기 위한 페이지 단위 메모리 관리 기법*과 양자화된 KV 캐시에 최적화된 새로운 인코딩 기법 등을 개발했다.
*페이지 단위 메모리 관리 기법: CPU처럼 메모리 주소를 가상화하여 NPU 내부에서 일관된 방식으로 접근할 수 있게 함
또한, 최신 GPU 대비 비용·전력 효율성이 우수한 NPU 기반 AI 클라우드를 구성할 경우, NPU의 고성능, 저전력 특성을 활용해 운영 비용 역시 크게 절감할 수 있을 것으로 기대된다.
박종세 교수는 “이 연구는 (주)하이퍼엑셀과의 공동연구를 통해 생성형AI 추론 경량화 알고리즘에서 그 해법을 찾았고 ‘메모리 문제’를 해결할 수 있는 NPU 핵심기술 개발에 성공했다. 이 기술을 통해 추론의 정확도를 유지하면서 메모리 요구량을 줄이는 경량화 기법과, 이에 최적화된 하드웨어 설계를 결합해 최신 GPU 대비 평균 60% 이상 성능이 향상된 NPU를 구현했다” 고 말했다.
이어 “이 기술은 생성형AI에 특화된 고성능·저전력 인프라 구현 가능성을 입증했으며, AI클라우드 데이터센터뿐 아니라 능동적인 실행형 AI인 ‘에이전틱 AI ’등으로 대표되는 AI 대전환(AX) 환경에서도 핵심 역할이 기대된다”고 강조했다.
이 연구는 김민수 박사과정 학생과 ㈜하이퍼엑셀 홍성민 박사가 공동 제1 저자로 지난 6월 21일부터 6월 25일까지 일본 도쿄에서 열린 ‘2025 국제 컴퓨터구조 심포지엄(ISCA)’에 발표됐다. 국제적 저명학회인 ISCA는 올해는 570편의 논문이 제출됐으며 그중 127편 만이 채택됐다. (채택률 22.7%).
※논문 제목: Oaken: Fast and Efficient LLM Serving with Online-Offline Hybrid KV Cache Quantization
※DOI: https://doi.org/10.1145/3695053.3731019
한편 이번 연구는 한국연구재단 우수신진연구자지원사업, 정보통신기획평가원(IITP), 인공지능반도체대학원지원사업의 지원을 받아 수행됐다.
2025.07.04 조회수 927 정확도·효율성 높인 생명과학 데이터 분석 도구 'scICE' 개발
기존보다 최대 30배 빠른 속도로 안정적인 결과만을 자동으로 선별하여 대규모 생명과학 데이터 분석의 정확도와 효율성을 획기적으로 향상하는 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀은 세포 분류(클러스터링) 결과의 안정성을 수학적으로 평가해 불안정한 결과를 걸러내는 새로운 분석 도구인 ‘scICE(single-cell Inconsistency Clustering Estimator)’를 개발했다.
단일세포 수준에서 유전자 발현을 분석하는 기술인 단일세포 전사체 분석법(scRNA-seq)은 현대 생명과학 연구의 핵심 도구로 자리 잡았다. 이 과정에서 클러스터링은 유사한 유전자 발현 특성을 가진 세포들을 그룹으로 묶는 작업으로, 암세포와 정상 세포를 구분하거나 새로운 세포 유형을 발견하는 데 중요한 첫걸음이다. 하지만 클러스터링 알고리즘은 무작위로 세포를 분류해 같은 데이터를 분석해도 결과가 달라지는 경우가 많다.
제1 저자인 김현 선임연구원은 “일부 정상 세포가 암세포로 잘못 분류되거나 중요한 세포 유형이 누락되는 불안정성으로 인해 연구자들은 다시 분석하거나 복잡한 계산을 통해 신뢰도가 높은 결과를 선별해야 했다”며, “기존 방법들은 분석을 여러 번 반복해 합의된 결과를 도출하는 방식으로, 계산량이 방대하고 수만 개 이상의 세포가 포함된 대용량 데이터에는 적합하지 않다”고 말했다.
연구팀이 개발한 scICE는 한 번의 분석만으로도 얼마나 일관성 있게 결과가 도출됐는지를 수학적으로 평가한다. 새로 도입한 ‘불일치 계수(Inconsistency Coefficient, IC)’를 통해 많은 계산량이 요구되는 연산 없이도 클러스터 간 안정성을 정량적으로 판단할 수 있다. 모든 세포를 일일이 비교하던 기존 방식과 달리, 불일치 계수를 활용한 안정성 평가는 클러스터 구조 간 유사성만 평가해 비교 대상을 획기적으로 줄일 수 있어 분석 시간을 크게 단축한다.
연구팀은 뇌, 폐, 혈액 등 다양한 조직에서 수집된 48개의 실제 및 모의 scRNA-seq 데이터에 scICE를 적용하여 그 유효성을 입증했다. 그 결과, 기존 분석 결과 중 약 3분의 2는 통계적으로 불안정하며 신뢰하기 어렵다는 사실을 밝혀냈다. 반면, scICE는 신뢰할 수 있는 결과만을 선별해 연구자의 시간과 계산 자원을 절약하면서도 정확도를 한층 높였다.
또한, scICE는 일반적인 클러스터링으로는 놓치기 쉬운 희귀한 세포 유형을 효과적으로 탐지했다. 실제로 일부 데이터에서 찾기 어려웠던 희귀 면역세포들을 scICE 기반의 서브클러스터링을 통해 안정적으로 식별해냈다. 예를 들어, 매우 복잡한 분석을 거쳐야만 식별할 수 있던 여러 대식세포(macrophage) 아형들을 훨씬 간편하고 정확하게 구분해냈다.
scICE에 관심 있는 연구자는 누구나 깃허브 사이트(https://github.com/Mathbiomed/scICE)를 통해 쉽게 활용해볼 수 있다.
김재경 교수는 “이번 연구는 수학적 아이디어가 어떻게 생명과학의 핵심 문제를 해결하고 분석 과정을 혁신할 수 있는지를 보여주는 성과”라며, “클러스터링 신뢰도의 중요성이 간과되어 온 측면이 있는데, 이번 기회로 scICE가 생명과학 분야에서 신뢰도 높은 데이터 해석을 가능케 하는 표준 도구로 자리 잡기를 기대한다”고 전했다.
우리 대학 박종은 교수 연구팀, POSTECH 김종경 교수 연구팀, 고려대 서민석 교수 연구팀과 공동으로 참여한 이번 연구결과는 세계적인 국제학술지 네이처 커뮤니케이션즈(Nature Communications, IF 14.7)에 7월 2일 온라인 게재됐다.
2025.07.03 조회수 846
정확도·효율성 높인 생명과학 데이터 분석 도구 'scICE' 개발
기존보다 최대 30배 빠른 속도로 안정적인 결과만을 자동으로 선별하여 대규모 생명과학 데이터 분석의 정확도와 효율성을 획기적으로 향상하는 방법이 나왔다. 우리 대학 수리과학과 김재경 교수 연구팀은 세포 분류(클러스터링) 결과의 안정성을 수학적으로 평가해 불안정한 결과를 걸러내는 새로운 분석 도구인 ‘scICE(single-cell Inconsistency Clustering Estimator)’를 개발했다.
단일세포 수준에서 유전자 발현을 분석하는 기술인 단일세포 전사체 분석법(scRNA-seq)은 현대 생명과학 연구의 핵심 도구로 자리 잡았다. 이 과정에서 클러스터링은 유사한 유전자 발현 특성을 가진 세포들을 그룹으로 묶는 작업으로, 암세포와 정상 세포를 구분하거나 새로운 세포 유형을 발견하는 데 중요한 첫걸음이다. 하지만 클러스터링 알고리즘은 무작위로 세포를 분류해 같은 데이터를 분석해도 결과가 달라지는 경우가 많다.
제1 저자인 김현 선임연구원은 “일부 정상 세포가 암세포로 잘못 분류되거나 중요한 세포 유형이 누락되는 불안정성으로 인해 연구자들은 다시 분석하거나 복잡한 계산을 통해 신뢰도가 높은 결과를 선별해야 했다”며, “기존 방법들은 분석을 여러 번 반복해 합의된 결과를 도출하는 방식으로, 계산량이 방대하고 수만 개 이상의 세포가 포함된 대용량 데이터에는 적합하지 않다”고 말했다.
연구팀이 개발한 scICE는 한 번의 분석만으로도 얼마나 일관성 있게 결과가 도출됐는지를 수학적으로 평가한다. 새로 도입한 ‘불일치 계수(Inconsistency Coefficient, IC)’를 통해 많은 계산량이 요구되는 연산 없이도 클러스터 간 안정성을 정량적으로 판단할 수 있다. 모든 세포를 일일이 비교하던 기존 방식과 달리, 불일치 계수를 활용한 안정성 평가는 클러스터 구조 간 유사성만 평가해 비교 대상을 획기적으로 줄일 수 있어 분석 시간을 크게 단축한다.
연구팀은 뇌, 폐, 혈액 등 다양한 조직에서 수집된 48개의 실제 및 모의 scRNA-seq 데이터에 scICE를 적용하여 그 유효성을 입증했다. 그 결과, 기존 분석 결과 중 약 3분의 2는 통계적으로 불안정하며 신뢰하기 어렵다는 사실을 밝혀냈다. 반면, scICE는 신뢰할 수 있는 결과만을 선별해 연구자의 시간과 계산 자원을 절약하면서도 정확도를 한층 높였다.
또한, scICE는 일반적인 클러스터링으로는 놓치기 쉬운 희귀한 세포 유형을 효과적으로 탐지했다. 실제로 일부 데이터에서 찾기 어려웠던 희귀 면역세포들을 scICE 기반의 서브클러스터링을 통해 안정적으로 식별해냈다. 예를 들어, 매우 복잡한 분석을 거쳐야만 식별할 수 있던 여러 대식세포(macrophage) 아형들을 훨씬 간편하고 정확하게 구분해냈다.
scICE에 관심 있는 연구자는 누구나 깃허브 사이트(https://github.com/Mathbiomed/scICE)를 통해 쉽게 활용해볼 수 있다.
김재경 교수는 “이번 연구는 수학적 아이디어가 어떻게 생명과학의 핵심 문제를 해결하고 분석 과정을 혁신할 수 있는지를 보여주는 성과”라며, “클러스터링 신뢰도의 중요성이 간과되어 온 측면이 있는데, 이번 기회로 scICE가 생명과학 분야에서 신뢰도 높은 데이터 해석을 가능케 하는 표준 도구로 자리 잡기를 기대한다”고 전했다.
우리 대학 박종은 교수 연구팀, POSTECH 김종경 교수 연구팀, 고려대 서민석 교수 연구팀과 공동으로 참여한 이번 연구결과는 세계적인 국제학술지 네이처 커뮤니케이션즈(Nature Communications, IF 14.7)에 7월 2일 온라인 게재됐다.
2025.07.03 조회수 846 24시간 말하는 AI비서 가능성 여는 '스피치SSM' 개발
최근 음성 언어 모델(Spoken Language Model, SLM)은 텍스트 없이 인간의 음성을 학습해 음성의 언어적, 비언어적 정보를 이해 및 생성하는 기술로 텍스트 기반 언어 모델의 한계를 넘어서는 차세대 기술로 각광받고 있다. 하지만 기존 모델은 장시간 콘텐츠 생성이 요구되는 팟캐스트, 오디오북, 음성비서 등에서 한계가 두드러졌는데, 우리 연구진이 이런 한계를 뛰어넘어, 시간 제약 없이 일관되고 자연스러운 음성 생성을 실현한 ‘스피치SSM’을 개발하는데 성공했다.
우리 대학 전기및전자공학부 노용만 교수 연구팀의 박세진 연구원(박사과정)이 장시간 음성 생성이 가능한 음성 언어 모델 ‘스피치SSM(SpeechSSM)’을 개발했다고 3일 밝혔다.
이번 연구는 국제 최고 권위 머신러닝 학회인 ICML(International Conference on Machine Learning) 2025에 전체 제출된 논문 중 약 1%만이 선정되는 구두 논문 발표에 확정돼 뛰어난 연구 역량을 입증할 뿐만 아니라 우리 대학의 인공지능 연구 능력이 세계 최고 수준임을 다시 한번 보여주는 계기가 될 전망이다.
음성 언어 모델(SLM)은 중간에 텍스트로 변환하지 않고 음성을 직접 처리함으로써, 인간 화자 고유의 음향적 특성을 활용할 수 있어 대규모 모델에서도 고품질의 음성을 빠르게 생성할 수 있다는 점이 큰 강점이다.
그러나 기존 모델은 음성을 아주 세밀하게 잘게 쪼개서 아주 자세한 정보까지 담는 경우, ‘음성 토큰 해상도’가 높아지고 사용하는 메모리 소비도 증가하는 문제로 인해 장시간 음성의 의미적, 화자적 일관성을 유지하기 어려웠다.
연구팀은 이러한 문제를 해결하기 위해 하이브리드 상태공간 모델(Hybrid State-Space Model)을 사용한 음성 언어 모델인‘스피치SSM’를 개발해 긴 음성 시퀀스를 효율적으로 처리하고 생성할 수 있게 설계했다.
이 모델은 최근 정보에 집중하는 ‘어텐션 레이어(attention layer)’와 전체 이야기 흐름(장기적인 맥락)을 오래 기억하는 ‘순환 레이어(recurrent layer)’를 교차 배치한 ‘하이브리드 구조’를 통해 긴 시간 동안 음성을 생성해도 흐름을 잃지 않고 이야기를 잘 이어간다. 또한, 메모리 사용량과 연산량이 입력 길이에 따라 급격히 증가하지 않아, 장시간의 음성을 안정적이고 효율적으로 학습하고 생성할 수 있다.
스피치SSM은 음성 데이터를 짧은 고정된 단위(윈도우)로 나눠 각 단위별로 독립적으로 처리하고, 전체 긴 음성을 만들 경우에는 다시 붙이는 방식을 활용해 쉽게 긴 음성을 만들 수 있어 무한한 길이의 음성 시퀀스(unbounded speech sequence)를 효과적으로 처리할 수 있게 했다.
또한 음성 생성 단계에서는 한 글자, 한 단어 차례대로 천천히 만들어내지 않고, 여러 부분을 한꺼번에 빠르게 만들어내는 ‘비자기회귀(Non-Autoregressive)’방식의 오디오 합성 모델(SoundStorm)을 사용해, 고품질의 음성을 빠르게 생성할 수 있게 했다.
기존은 10초 정도 짧은 음성 모델을 평가했지만, 연구팀은 16분까지 생성할 수 있도록 자체 구축한 새로운 벤치마크 데이터셋인 ‘LibriSpeech-Long'을 기반으로 음성을 생성하는 평가 태스크를 새롭게 만들었다.
기존 음성 모델 평가 지표인 말이 문법적으로 맞는지 정도만 알려주는 PPL(Perplexity)에 비해, 연구팀은 시간이 지나면서도 내용이 잘 이어지는지 보는 'SC-L(semantic coherence over time)', 자연스럽게 들리는 정도를 시간 따라 보는 'N-MOS-T(naturalness mean opinion score over time)' 등 새로운 평가 지표들을 제안해 보다 효과적이고 정밀하게 평가했다.
새로운 평가를 통해 스피치SSM 음성 언어 모델로 생성된 음성은 긴 시간 생성에도 불구하고 초기 프롬프트에서 언급된 특정 인물이 지속적으로 등장하며, 맥락적으로 일관된 새로운 인물과 사건들이 자연스럽게 전개되는 모습을 확인했다. 이는 기존 모델들이 장시간 생성 시 쉽게 주제를 잃고 반복되는 현상을 보였던 것과 크게 대조적이다.
박세진 박사과정생은 “기존 음성 언어 모델은 장시간 생성에 한계가 있어, 실제 인간이 사용하도록 장시간 음성 생성이 가능한 음성 언어 모델을 개발하는 것이 목표였다”며 “이번 연구 성과를 통해 긴 문맥에서도 일관된 내용을 유지하면서, 기존 방식보다 더 효율적이고 빠르게 실시간으로 응답할 수 있어, 다양한 음성 콘텐츠 제작과 음성비서 등 음성 AI 분야에 크게 기여할 것으로 기대한다”라고 밝혔다.
이 연구는 제1 저자인 우리 대학 박세진 박사과정 학생이 구글 딥마인드(Google DeepMind)와 협력해, ICML(국제 머신러닝 학회) 2025에서 7월 16일 구두 발표로 소개될 예정이다.
※ 논문제목: Long-Form Speech Generation with Spoken Language Models
※ DOI: 10.48550/arXiv.2412.18603
한편, 박세진 박사과정생은 비전, 음성, 언어를 통합하는 연구를 수행하며 CVPR(컴퓨터 비전 분야 최고 학회) 2024 하이라이트 논문 발표, 2024년 ACL(자연어 처리 분야 최고 학회)에서 우수논문상(Outstanding Paper Award) 수상 등을 통해 우수한 연구 역량을 입증한 바 있다.
[데모 페이지 링크]
https://google.github.io/tacotron/publications/speechssm/
2025.07.03 조회수 1007
24시간 말하는 AI비서 가능성 여는 '스피치SSM' 개발
최근 음성 언어 모델(Spoken Language Model, SLM)은 텍스트 없이 인간의 음성을 학습해 음성의 언어적, 비언어적 정보를 이해 및 생성하는 기술로 텍스트 기반 언어 모델의 한계를 넘어서는 차세대 기술로 각광받고 있다. 하지만 기존 모델은 장시간 콘텐츠 생성이 요구되는 팟캐스트, 오디오북, 음성비서 등에서 한계가 두드러졌는데, 우리 연구진이 이런 한계를 뛰어넘어, 시간 제약 없이 일관되고 자연스러운 음성 생성을 실현한 ‘스피치SSM’을 개발하는데 성공했다.
우리 대학 전기및전자공학부 노용만 교수 연구팀의 박세진 연구원(박사과정)이 장시간 음성 생성이 가능한 음성 언어 모델 ‘스피치SSM(SpeechSSM)’을 개발했다고 3일 밝혔다.
이번 연구는 국제 최고 권위 머신러닝 학회인 ICML(International Conference on Machine Learning) 2025에 전체 제출된 논문 중 약 1%만이 선정되는 구두 논문 발표에 확정돼 뛰어난 연구 역량을 입증할 뿐만 아니라 우리 대학의 인공지능 연구 능력이 세계 최고 수준임을 다시 한번 보여주는 계기가 될 전망이다.
음성 언어 모델(SLM)은 중간에 텍스트로 변환하지 않고 음성을 직접 처리함으로써, 인간 화자 고유의 음향적 특성을 활용할 수 있어 대규모 모델에서도 고품질의 음성을 빠르게 생성할 수 있다는 점이 큰 강점이다.
그러나 기존 모델은 음성을 아주 세밀하게 잘게 쪼개서 아주 자세한 정보까지 담는 경우, ‘음성 토큰 해상도’가 높아지고 사용하는 메모리 소비도 증가하는 문제로 인해 장시간 음성의 의미적, 화자적 일관성을 유지하기 어려웠다.
연구팀은 이러한 문제를 해결하기 위해 하이브리드 상태공간 모델(Hybrid State-Space Model)을 사용한 음성 언어 모델인‘스피치SSM’를 개발해 긴 음성 시퀀스를 효율적으로 처리하고 생성할 수 있게 설계했다.
이 모델은 최근 정보에 집중하는 ‘어텐션 레이어(attention layer)’와 전체 이야기 흐름(장기적인 맥락)을 오래 기억하는 ‘순환 레이어(recurrent layer)’를 교차 배치한 ‘하이브리드 구조’를 통해 긴 시간 동안 음성을 생성해도 흐름을 잃지 않고 이야기를 잘 이어간다. 또한, 메모리 사용량과 연산량이 입력 길이에 따라 급격히 증가하지 않아, 장시간의 음성을 안정적이고 효율적으로 학습하고 생성할 수 있다.
스피치SSM은 음성 데이터를 짧은 고정된 단위(윈도우)로 나눠 각 단위별로 독립적으로 처리하고, 전체 긴 음성을 만들 경우에는 다시 붙이는 방식을 활용해 쉽게 긴 음성을 만들 수 있어 무한한 길이의 음성 시퀀스(unbounded speech sequence)를 효과적으로 처리할 수 있게 했다.
또한 음성 생성 단계에서는 한 글자, 한 단어 차례대로 천천히 만들어내지 않고, 여러 부분을 한꺼번에 빠르게 만들어내는 ‘비자기회귀(Non-Autoregressive)’방식의 오디오 합성 모델(SoundStorm)을 사용해, 고품질의 음성을 빠르게 생성할 수 있게 했다.
기존은 10초 정도 짧은 음성 모델을 평가했지만, 연구팀은 16분까지 생성할 수 있도록 자체 구축한 새로운 벤치마크 데이터셋인 ‘LibriSpeech-Long'을 기반으로 음성을 생성하는 평가 태스크를 새롭게 만들었다.
기존 음성 모델 평가 지표인 말이 문법적으로 맞는지 정도만 알려주는 PPL(Perplexity)에 비해, 연구팀은 시간이 지나면서도 내용이 잘 이어지는지 보는 'SC-L(semantic coherence over time)', 자연스럽게 들리는 정도를 시간 따라 보는 'N-MOS-T(naturalness mean opinion score over time)' 등 새로운 평가 지표들을 제안해 보다 효과적이고 정밀하게 평가했다.
새로운 평가를 통해 스피치SSM 음성 언어 모델로 생성된 음성은 긴 시간 생성에도 불구하고 초기 프롬프트에서 언급된 특정 인물이 지속적으로 등장하며, 맥락적으로 일관된 새로운 인물과 사건들이 자연스럽게 전개되는 모습을 확인했다. 이는 기존 모델들이 장시간 생성 시 쉽게 주제를 잃고 반복되는 현상을 보였던 것과 크게 대조적이다.
박세진 박사과정생은 “기존 음성 언어 모델은 장시간 생성에 한계가 있어, 실제 인간이 사용하도록 장시간 음성 생성이 가능한 음성 언어 모델을 개발하는 것이 목표였다”며 “이번 연구 성과를 통해 긴 문맥에서도 일관된 내용을 유지하면서, 기존 방식보다 더 효율적이고 빠르게 실시간으로 응답할 수 있어, 다양한 음성 콘텐츠 제작과 음성비서 등 음성 AI 분야에 크게 기여할 것으로 기대한다”라고 밝혔다.
이 연구는 제1 저자인 우리 대학 박세진 박사과정 학생이 구글 딥마인드(Google DeepMind)와 협력해, ICML(국제 머신러닝 학회) 2025에서 7월 16일 구두 발표로 소개될 예정이다.
※ 논문제목: Long-Form Speech Generation with Spoken Language Models
※ DOI: 10.48550/arXiv.2412.18603
한편, 박세진 박사과정생은 비전, 음성, 언어를 통합하는 연구를 수행하며 CVPR(컴퓨터 비전 분야 최고 학회) 2024 하이라이트 논문 발표, 2024년 ACL(자연어 처리 분야 최고 학회)에서 우수논문상(Outstanding Paper Award) 수상 등을 통해 우수한 연구 역량을 입증한 바 있다.
[데모 페이지 링크]
https://google.github.io/tacotron/publications/speechssm/
2025.07.03 조회수 1007 AI로 방사성 오염 '아이오딘' 제거용 최적 신소재 발굴
원자력 에너지 활용에 있어 방사성 폐기물 관리는 핵심적인 과제 중 하나다. 특히 방사성 ‘아이오딘(요오드)’는 반감기가 길고(I-129의 경우 1,570만 년), 이동성 및 생체 유독성이 높아 환경 및 인체에 심각한 위험을 초래할 수 있다. 한국 연구진이 인공지능을 활용해 아이오딘을 제거할 원자력 환경 정화용 신소재 발굴에 성공했다. 연구팀은 향후 방사성 오염 흡착용 분말부터 오염수 처리 필터까지 다양한 산학협력을 통해 상용화를 추진할 예정이다.
우리 대학 원자력및양자공학과 류호진 교수 연구팀이 한국화학연구원 디지털화학연구센터 노주환 박사가 협력하여, 인공지능을 활용해 방사성 오염 물질이 될 수 있는 아이오딘을 효과적으로 제거하는 신소재를 발굴하는 기술을 개발했다고 2일 밝혔다.
최근 보고에 따르면 방사능 오염 물질인 아이오딘이 수용액 환경에서 아이오딘산염(IO3-) 형태로 존재하는 것으로 밝혀졌으나, 기존의 은 기반 흡착제는 이에 대해 낮은 화학적 흡착력을 가져 비효율적이었다. 따라서 아이오딘산염을 효과적으로 제거할 수 있는 새로운 흡착제 신소재 개발이 시급한 실정이다.
류호진 교수 연구팀은 기계학습을 활용한 실험 전략을 통해 다양한 금속원소를 함유한 ‘이중층 수산화물(Layered Double Hydroxide, 이하 LDH)’이라는 화합물 중 최적의 아이오딘산염 흡착제를 발굴했다.
이번 연구에서 개발된 구리-크롬-철-알루미늄 기반의 다중금속 이중층 수산화물 Cu3(CrFeAl)은 아이오딘산염에 대해 90% 이상의 뛰어난 흡착 성능을 보였다. 이는 기존의 시행착오 실험 방식으로는 탐색이 어려운 방대한 물질 조성 공간을 인공지능 기반의 능동학습법을 통해 효율적으로 탐색해 얻어낸 성과다.
연구팀은 이중층 수산화물(이하 LDH)이 고엔트로피 재료와 같이 다양한 금속 조성을 가질 수 있고 음이온 흡착에 유리한 구조를 지녔다는 점에 주목했다. 그러나 다중금속 LDH의 경우 가능한 금속 조합이 너무 많아 기존의 실험 방식으로는 최적의 조합을 찾기 어려웠다.
이를 해결하기 위해 연구팀은 인공지능(기계학습)을 도입했다. 초기 24개의 2원계 및 96개의 3원계 LDH 실험 데이터로 학습을 시작해, 4원계 및 5원계 후보 물질로 탐색을 확장했다. 이 결과 전체 후보 물질 중 단 16%에 대해서만 실험을 수행하고도 아이오딘산염 제거에 최적인 신소재 물질을 찾아낼 수 있었다.
류호진 교수는 “인공지능을 활용하면 방대한 신소재 후보 물질 군에서 방사성 오염 제거용 물질을 효율적으로 찾아낼 가능성을 보여, 원자력 환경 정화용 신소재 개발에 필요한 연구를 가속화하는데 기여할 것으로 기대된다”고 말했다.
류 교수 연구팀은 개발된 분말 기술에 대한 국내 특허를 출원했으며 이를 기반으로 해외 특허 출원을 진행 중이다. 연구팀은 향후 방사성 오염 흡착용 분말의 다양한 사용 환경에서의 성능을 고도화하고, 오염수 처리 필터 개발 분야에서 산학 협력을 통한 상용화 방안을 추진할 예정이다.
우리 대학 신소재공학과를 졸업한 이수정 박사와 한국화학연구원 디지털화학연구센터 노주환 박사가 제1 저자로 참여한 이번 연구는 이번 연구 결과는 환경 분야 국제 저명 학술지인 ‘위험물질 저널(Journal of Hazardous Materials)'에 5월 26일 온라인 게재됐다.
※논문명: Discovery of multi-metal-layered double hydroxides for decontamination of iodate by machine learning-assisted experiments
※DOI: https://doi.org/10.1016/j.jhazmat.2025.138735
이번 연구는 과학기술정보통신부 한국연구재단의 원자력기초연구지원사업과 나노·소재기술개발사업의 지원으로 수행됐다.
2025.07.02 조회수 868
AI로 방사성 오염 '아이오딘' 제거용 최적 신소재 발굴
원자력 에너지 활용에 있어 방사성 폐기물 관리는 핵심적인 과제 중 하나다. 특히 방사성 ‘아이오딘(요오드)’는 반감기가 길고(I-129의 경우 1,570만 년), 이동성 및 생체 유독성이 높아 환경 및 인체에 심각한 위험을 초래할 수 있다. 한국 연구진이 인공지능을 활용해 아이오딘을 제거할 원자력 환경 정화용 신소재 발굴에 성공했다. 연구팀은 향후 방사성 오염 흡착용 분말부터 오염수 처리 필터까지 다양한 산학협력을 통해 상용화를 추진할 예정이다.
우리 대학 원자력및양자공학과 류호진 교수 연구팀이 한국화학연구원 디지털화학연구센터 노주환 박사가 협력하여, 인공지능을 활용해 방사성 오염 물질이 될 수 있는 아이오딘을 효과적으로 제거하는 신소재를 발굴하는 기술을 개발했다고 2일 밝혔다.
최근 보고에 따르면 방사능 오염 물질인 아이오딘이 수용액 환경에서 아이오딘산염(IO3-) 형태로 존재하는 것으로 밝혀졌으나, 기존의 은 기반 흡착제는 이에 대해 낮은 화학적 흡착력을 가져 비효율적이었다. 따라서 아이오딘산염을 효과적으로 제거할 수 있는 새로운 흡착제 신소재 개발이 시급한 실정이다.
류호진 교수 연구팀은 기계학습을 활용한 실험 전략을 통해 다양한 금속원소를 함유한 ‘이중층 수산화물(Layered Double Hydroxide, 이하 LDH)’이라는 화합물 중 최적의 아이오딘산염 흡착제를 발굴했다.
이번 연구에서 개발된 구리-크롬-철-알루미늄 기반의 다중금속 이중층 수산화물 Cu3(CrFeAl)은 아이오딘산염에 대해 90% 이상의 뛰어난 흡착 성능을 보였다. 이는 기존의 시행착오 실험 방식으로는 탐색이 어려운 방대한 물질 조성 공간을 인공지능 기반의 능동학습법을 통해 효율적으로 탐색해 얻어낸 성과다.
연구팀은 이중층 수산화물(이하 LDH)이 고엔트로피 재료와 같이 다양한 금속 조성을 가질 수 있고 음이온 흡착에 유리한 구조를 지녔다는 점에 주목했다. 그러나 다중금속 LDH의 경우 가능한 금속 조합이 너무 많아 기존의 실험 방식으로는 최적의 조합을 찾기 어려웠다.
이를 해결하기 위해 연구팀은 인공지능(기계학습)을 도입했다. 초기 24개의 2원계 및 96개의 3원계 LDH 실험 데이터로 학습을 시작해, 4원계 및 5원계 후보 물질로 탐색을 확장했다. 이 결과 전체 후보 물질 중 단 16%에 대해서만 실험을 수행하고도 아이오딘산염 제거에 최적인 신소재 물질을 찾아낼 수 있었다.
류호진 교수는 “인공지능을 활용하면 방대한 신소재 후보 물질 군에서 방사성 오염 제거용 물질을 효율적으로 찾아낼 가능성을 보여, 원자력 환경 정화용 신소재 개발에 필요한 연구를 가속화하는데 기여할 것으로 기대된다”고 말했다.
류 교수 연구팀은 개발된 분말 기술에 대한 국내 특허를 출원했으며 이를 기반으로 해외 특허 출원을 진행 중이다. 연구팀은 향후 방사성 오염 흡착용 분말의 다양한 사용 환경에서의 성능을 고도화하고, 오염수 처리 필터 개발 분야에서 산학 협력을 통한 상용화 방안을 추진할 예정이다.
우리 대학 신소재공학과를 졸업한 이수정 박사와 한국화학연구원 디지털화학연구센터 노주환 박사가 제1 저자로 참여한 이번 연구는 이번 연구 결과는 환경 분야 국제 저명 학술지인 ‘위험물질 저널(Journal of Hazardous Materials)'에 5월 26일 온라인 게재됐다.
※논문명: Discovery of multi-metal-layered double hydroxides for decontamination of iodate by machine learning-assisted experiments
※DOI: https://doi.org/10.1016/j.jhazmat.2025.138735
이번 연구는 과학기술정보통신부 한국연구재단의 원자력기초연구지원사업과 나노·소재기술개발사업의 지원으로 수행됐다.
2025.07.02 조회수 868 장내 미생물로 난치성 뇌종양 면역치료 효과 높인다
우리 몸의 면역세포인 T세포를 활성화시켜 암세포를 제거하도록 유도하는 첨단 치료법인 ‘면역항암제’는 가장 치명적인 뇌종양 ‘교모세포종(Glioblastoma)’에는 거의 반응하지 않고, 치료에 대한 저항성이 높아 단독 치료로는 효과가 매우 제한적이라는 한계가 있었다. 이에 우리 연구진이 장내 미생물과 그 대사산물을 활용해 뇌종양의 면역치료 효과를 높일 수 있는 새로운 치료 전략을 세계 최초로 입증했다. 향후 미생물을 기반으로 한 면역치료 보완제 개발에 대한 가능성도 보여줬다.
우리 대학 생명과학과 이흥규 교수 연구팀이 장내 미생물 생태계 변화에 주목해 교모세포종 면역치료의 효율을 크게 높이는 방법을 발굴하고 이를 입증했다고 1일 밝혔다.
연구팀은 교모세포종이 진행되면서 장내에서 중요한 아미노산인 ‘트립토판(tryptophan)’의 농도가 급격히 줄어들고, 이로 인해 장내 미생물 생태계가 변화한다는 점에 주목했다. 그리고 트립토판을 보충해 미생물 다양성을 회복시키면, 특정 유익한 균주가 면역세포 중 하나인 CD8 T세포를 활성화하고 종양 조직으로 다시 유도하는 역할을 한다는 사실을 밝혀냈다.
연구팀은 생쥐 교모세포종 모델을 통해, 트립토판을 보충하면 암을 공격하는 T세포(특히 CD8 T세포)의 반응이 향상되고, 이들이 림프절과 뇌 등 종양이 있는 부위로 더 많이 이동한다는 사실을 확인했다.
이 과정에서 장내에 존재하는 유익한 공생균인 ‘던카니엘라 두보시(Duncaniella dubosii)’가 핵심적인 역할을 한다는 점도 밝혀냈다. 해당 균주는 T세포가 몸 안에서 효과적으로 재분포하도록 도와줬고, 면역항암제(anti-PD-1)와 함께 사용할 때 생존율이 유의미하게 향상됐다.
또한, 장내 미생물이 전혀 없는 무균 생쥐에게 위 공생균을 단독으로 투입해도 교모세포종에 대한 생존율이 높아졌으며, 이는 이 균주가 트립토판을 활용해 장내 환경을 조절하고, 그 과정에서 생성되는 대사산물이 CD8 T세포의 암세포 공격 능력을 강화하기 때문임이 입증됐다.
이흥규 교수는 “이번 연구는 면역관문억제제가 효과를 보이지 않았던 난치성 뇌종양에서도, 장내 미생물을 활용한 병용 전략을 통해 치료 반응을 유의하게 높일 수 있음을 보여준 의미 있는 성과”라고 설명했다.
우리 대학 김현철 박사(現, 생명과학연구소 박사후연구원)가 제1 저자로 참여했고 연구 결과는 생명과학 분야 국제 학술지‘셀 리포츠(Cell Reports)’에 지난 6월 26 일자 온라인판에 게재됐다.
(논문명: Gut microbiota dysbiosis induced by brain tumor modulates the efficacy of immunotherapy, https://doi.org/10.1016/j.celrep.2025.115825)
한편, 이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
2025.07.01 조회수 986
장내 미생물로 난치성 뇌종양 면역치료 효과 높인다
우리 몸의 면역세포인 T세포를 활성화시켜 암세포를 제거하도록 유도하는 첨단 치료법인 ‘면역항암제’는 가장 치명적인 뇌종양 ‘교모세포종(Glioblastoma)’에는 거의 반응하지 않고, 치료에 대한 저항성이 높아 단독 치료로는 효과가 매우 제한적이라는 한계가 있었다. 이에 우리 연구진이 장내 미생물과 그 대사산물을 활용해 뇌종양의 면역치료 효과를 높일 수 있는 새로운 치료 전략을 세계 최초로 입증했다. 향후 미생물을 기반으로 한 면역치료 보완제 개발에 대한 가능성도 보여줬다.
우리 대학 생명과학과 이흥규 교수 연구팀이 장내 미생물 생태계 변화에 주목해 교모세포종 면역치료의 효율을 크게 높이는 방법을 발굴하고 이를 입증했다고 1일 밝혔다.
연구팀은 교모세포종이 진행되면서 장내에서 중요한 아미노산인 ‘트립토판(tryptophan)’의 농도가 급격히 줄어들고, 이로 인해 장내 미생물 생태계가 변화한다는 점에 주목했다. 그리고 트립토판을 보충해 미생물 다양성을 회복시키면, 특정 유익한 균주가 면역세포 중 하나인 CD8 T세포를 활성화하고 종양 조직으로 다시 유도하는 역할을 한다는 사실을 밝혀냈다.
연구팀은 생쥐 교모세포종 모델을 통해, 트립토판을 보충하면 암을 공격하는 T세포(특히 CD8 T세포)의 반응이 향상되고, 이들이 림프절과 뇌 등 종양이 있는 부위로 더 많이 이동한다는 사실을 확인했다.
이 과정에서 장내에 존재하는 유익한 공생균인 ‘던카니엘라 두보시(Duncaniella dubosii)’가 핵심적인 역할을 한다는 점도 밝혀냈다. 해당 균주는 T세포가 몸 안에서 효과적으로 재분포하도록 도와줬고, 면역항암제(anti-PD-1)와 함께 사용할 때 생존율이 유의미하게 향상됐다.
또한, 장내 미생물이 전혀 없는 무균 생쥐에게 위 공생균을 단독으로 투입해도 교모세포종에 대한 생존율이 높아졌으며, 이는 이 균주가 트립토판을 활용해 장내 환경을 조절하고, 그 과정에서 생성되는 대사산물이 CD8 T세포의 암세포 공격 능력을 강화하기 때문임이 입증됐다.
이흥규 교수는 “이번 연구는 면역관문억제제가 효과를 보이지 않았던 난치성 뇌종양에서도, 장내 미생물을 활용한 병용 전략을 통해 치료 반응을 유의하게 높일 수 있음을 보여준 의미 있는 성과”라고 설명했다.
우리 대학 김현철 박사(現, 생명과학연구소 박사후연구원)가 제1 저자로 참여했고 연구 결과는 생명과학 분야 국제 학술지‘셀 리포츠(Cell Reports)’에 지난 6월 26 일자 온라인판에 게재됐다.
(논문명: Gut microbiota dysbiosis induced by brain tumor modulates the efficacy of immunotherapy, https://doi.org/10.1016/j.celrep.2025.115825)
한편, 이번 연구는 과학기술정보통신부와 한국연구재단이 지원하는 개인기초연구사업 및 바이오의료기술개발사업의 일환으로 수행됐다.
2025.07.01 조회수 986 기계공학과 윤국진 교수 연구팀, 세계 최고 권위 컴퓨터비전 국제학술대회 ICCV 2025에 논문 12편 채택
우리 대학 기계공학과 윤국진 교수 연구팀의 논문 12편이 세계 최고 권위 컴퓨터비전 국제 학술 대회 중 하나인 IEEE/CVF International Conference on Computer Vision 2025(ICCV 2025)에 채택되어, 연구팀의 독보적인 연구 역량을 다시 한번 국제적으로 인정받았다.
ICCV는 CVPR, ECCV와 함께 컴퓨터비전 및 인공지능 분야에서 가장 영향력 있는 국제 학술대회 중 하나로, 1987년부터 격년으로 개최되어 왔다. 이번 ICCV 2025에는 총 11,152편의 논문이 제출되었고, 이 중 2,698편이 채택되어 약 24.19%의 낮은 채택률을 기록하였다. 학술대회에 제출할 수 있는 논문 편수에 대한 제한이 있음에도 불구하고 단일 연구실에서 12편의 논문이 동시 채택되는 것은 매우 드문 성과다.
윤국진 교수 연구팀은 학습 기반의 시각 지능 구현을 목표로 연구를 진행하고 있으며, 이번에 발표된 12편의 논문들은 3D 객체 탐지 및 재구성, 동작 예측 및 계획, 악천후나 모션 블러와 같은 극한 환경에서의 영상 인식 및 개선, 테스트 시점 적응 및 멀티태스크 학습, 4D 맵을 활용한 재구성과 같은 컴퓨터비전 분야의 핵심 주제들에 대한 논문들이다.
특히 연구팀은 지난해 CVPR 2024와 ECCV 2024에서도 각각 9편과 12편의 논문을 발표하여 학계의 주목을 받은 바 있는데, 이번 ICCV 2025에서의 성과를 통해 전 세계 컴퓨터 비전 분야의 선두 연구실로서 입지를 더욱 확고히 했다. 연구팀은 앞으로도 도전적인 연구를 이어가며 학문적·기술적 한계를 확장해 나갈 계획이다.
ICCV 2025는 오는 10월 19일부터 23일까지 미국 하와이 호놀룰루에서 개최될 예정이다.
2025.06.30 조회수 806
기계공학과 윤국진 교수 연구팀, 세계 최고 권위 컴퓨터비전 국제학술대회 ICCV 2025에 논문 12편 채택
우리 대학 기계공학과 윤국진 교수 연구팀의 논문 12편이 세계 최고 권위 컴퓨터비전 국제 학술 대회 중 하나인 IEEE/CVF International Conference on Computer Vision 2025(ICCV 2025)에 채택되어, 연구팀의 독보적인 연구 역량을 다시 한번 국제적으로 인정받았다.
ICCV는 CVPR, ECCV와 함께 컴퓨터비전 및 인공지능 분야에서 가장 영향력 있는 국제 학술대회 중 하나로, 1987년부터 격년으로 개최되어 왔다. 이번 ICCV 2025에는 총 11,152편의 논문이 제출되었고, 이 중 2,698편이 채택되어 약 24.19%의 낮은 채택률을 기록하였다. 학술대회에 제출할 수 있는 논문 편수에 대한 제한이 있음에도 불구하고 단일 연구실에서 12편의 논문이 동시 채택되는 것은 매우 드문 성과다.
윤국진 교수 연구팀은 학습 기반의 시각 지능 구현을 목표로 연구를 진행하고 있으며, 이번에 발표된 12편의 논문들은 3D 객체 탐지 및 재구성, 동작 예측 및 계획, 악천후나 모션 블러와 같은 극한 환경에서의 영상 인식 및 개선, 테스트 시점 적응 및 멀티태스크 학습, 4D 맵을 활용한 재구성과 같은 컴퓨터비전 분야의 핵심 주제들에 대한 논문들이다.
특히 연구팀은 지난해 CVPR 2024와 ECCV 2024에서도 각각 9편과 12편의 논문을 발표하여 학계의 주목을 받은 바 있는데, 이번 ICCV 2025에서의 성과를 통해 전 세계 컴퓨터 비전 분야의 선두 연구실로서 입지를 더욱 확고히 했다. 연구팀은 앞으로도 도전적인 연구를 이어가며 학문적·기술적 한계를 확장해 나갈 계획이다.
ICCV 2025는 오는 10월 19일부터 23일까지 미국 하와이 호놀룰루에서 개최될 예정이다.
2025.06.30 조회수 806 ‘슝’ 스스로 움직이는 생명체 세포로봇 개발
현재 전 세계적으로 마이크로 및 나노급의 작은 입자 기반의 비생명체 자가 추진 로봇 기술은 활발하게 연구되고 있는 반면에, 세포와 같은 생명체 구성 요소를 직접 활용한 세포로봇 연구는 아직 초기 단계에 머물러 있다. 우리 연구진이 세포 기반 시스템의 자율적으로 이동하는 세포로봇을 개발하는데 성공했다. 향후 정밀 약물 전달이나 차세대 세포 기반 치료법의 원천기술로 활용될 수 있을 것으로 기대된다.
우리 대학 화학과 최인성 교수 연구팀이 외부 동력 장치나 복잡한 기계 구조 없이, 생체 부산물인 ‘요소(urea)’*를 연료로 사용하는 자가 추진 세포로봇을 개발했다고 30일 밝혔다.
*요소(urea): 사람을 포함한 대부분의 동물 체내에서 단백질을 분해하면서 생기는 노폐물로 생명체 안에서는 단백질 대사 과정에서 암모니아를 독성이 낮은 형태로 전환하여 배출하는 중요한 역할을 함
연구팀이 구현한 세포로봇은 방향성을 갖고 스스로 이동할 수 있으며, 원하는 물질을 운반하거나 주변 환경 제어 기능을 탑재할 수 있는 다기능성 플랫폼으로 설계됐다.
연구팀은 쉽고 안정적으로 얻을 수 있는 생명체이면서 부산물로 생성된 에탄올 활용 가능성이 있고, 인공적인 복잡한 외부 장치 없이 생명체 스스로 만들어내는 물질을 활용할 수 있는 ‘효모’에 주목했다.
제빵과 막걸리 발효에 사용되는 효모(이스트, yeast)는 포도당을 분해해 에너지를 얻는 대사 과정에서 알코올(에탄올)을 부산물로 생성하는데, 연구팀은 이때 생성된 에탄올을 활용해 효모 표면에 생체친화적인 방식으로 나노 껍질을 형성할 수 있는 원천기술을 개발했다.
이를 위해, 알코올산화효소(AOx)와 겨자무과산화효소(HRP)로 구성된 효소 시스템을 도입했다. 이 효소 시스템은 효모의 포도당 분해 반응과 연계된 연쇄적 효소 반응을 유도하며, 그 결과로 멜라닌 계열의 나노껍질이 효모 표면에 형성된다.
특히, 이번에 개발된 화학적 방법론은 효모가 성장하고 분열하는 동안에도 나노껍질 형성이 지속적으로 일어나도록 설계돼 있어서, 세포의 형태 변화에 따라 비대칭적인 세포-껍질 구조가 자연스럽게 생성된다.
예를 들어, 분열 중인 세포 전체를 감싸는 껍질이 형성되기도 하지만, 모세포 부분에는 껍질이 생성되고 딸세포 부분에는 형성되지 않는 구조도 만들어진다.
연구팀은 세포를 감싸는 나노껍질에 우레아제(urease)*를 부착하고 세포로봇의 움직임을 관찰했다. 우레아제는 요소를 분해하는 촉매 역할을 하며 세포로봇이 스스로 움직일 수 있도록 구동력을 만들어내는 핵심 역할을 수행하며 비대칭 구조를 가진 세포로봇이 보다 명확한 방향성을 갖고 자가 추진하는 현상을 확인했다.
*우레아제(urease): 요소를 분해해 암모니아와 이산화탄소를 만드는 효소
이번에 개발된 세포로봇은 세포 주위에 존재하는 물질만으로 자가 추진이 가능하고, 자석이나 레이저 등 복잡한 외부 제어 장치에 의존하지 않아 구동 메커니즘이 훨씬 간단하고 생체친화적이다. 또한, 나노껍질에 다양한 효소를 화학적으로 접합할 수 있어, 다양한 생체 물질을 연료로 활용하는 세포로봇의 확장 개발도 가능하다.
이번 연구의 제1 저자인 화학과 김나영 박사과정은 “자가 추진 세포로봇은 스스로 환경을 감지하고 반응하며 움직이는 능력을 지닌 새로운 개념의 플랫폼으로, 향후 암세포 표적 치료나 정밀 약물전달시스템 등에서 중요한 역할을 할 수 있을 것”이라고 말했다.
이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’에 지난 6월 25일 오후 2시(미국 동부시각) 온라인판에 게재됐다.
※ 논문명 : Autonomous Chemo-Metabolic Construction of Anisotropic Cell-in-Shell Nanobiohybrids in Enzyme-Powered Cell Microrobots; 국문 번역 : 효소 구동 세포 마이크로로봇 구축에서의 자율적인 화학-대사 반응을 통해 형성된 비등방성 세포내껍질 나노바이오하이브리드
※ DOI: https://doi.org/10.1126/sciadv.adu5451
한편, 이번 연구는 한국연구재단 기초연구사업 중견연구과제(제목: 세포대사 연계형 단일세포나노피포화)의 지원을 받아 수행됐다.
2025.06.30 조회수 1212
‘슝’ 스스로 움직이는 생명체 세포로봇 개발
현재 전 세계적으로 마이크로 및 나노급의 작은 입자 기반의 비생명체 자가 추진 로봇 기술은 활발하게 연구되고 있는 반면에, 세포와 같은 생명체 구성 요소를 직접 활용한 세포로봇 연구는 아직 초기 단계에 머물러 있다. 우리 연구진이 세포 기반 시스템의 자율적으로 이동하는 세포로봇을 개발하는데 성공했다. 향후 정밀 약물 전달이나 차세대 세포 기반 치료법의 원천기술로 활용될 수 있을 것으로 기대된다.
우리 대학 화학과 최인성 교수 연구팀이 외부 동력 장치나 복잡한 기계 구조 없이, 생체 부산물인 ‘요소(urea)’*를 연료로 사용하는 자가 추진 세포로봇을 개발했다고 30일 밝혔다.
*요소(urea): 사람을 포함한 대부분의 동물 체내에서 단백질을 분해하면서 생기는 노폐물로 생명체 안에서는 단백질 대사 과정에서 암모니아를 독성이 낮은 형태로 전환하여 배출하는 중요한 역할을 함
연구팀이 구현한 세포로봇은 방향성을 갖고 스스로 이동할 수 있으며, 원하는 물질을 운반하거나 주변 환경 제어 기능을 탑재할 수 있는 다기능성 플랫폼으로 설계됐다.
연구팀은 쉽고 안정적으로 얻을 수 있는 생명체이면서 부산물로 생성된 에탄올 활용 가능성이 있고, 인공적인 복잡한 외부 장치 없이 생명체 스스로 만들어내는 물질을 활용할 수 있는 ‘효모’에 주목했다.
제빵과 막걸리 발효에 사용되는 효모(이스트, yeast)는 포도당을 분해해 에너지를 얻는 대사 과정에서 알코올(에탄올)을 부산물로 생성하는데, 연구팀은 이때 생성된 에탄올을 활용해 효모 표면에 생체친화적인 방식으로 나노 껍질을 형성할 수 있는 원천기술을 개발했다.
이를 위해, 알코올산화효소(AOx)와 겨자무과산화효소(HRP)로 구성된 효소 시스템을 도입했다. 이 효소 시스템은 효모의 포도당 분해 반응과 연계된 연쇄적 효소 반응을 유도하며, 그 결과로 멜라닌 계열의 나노껍질이 효모 표면에 형성된다.
특히, 이번에 개발된 화학적 방법론은 효모가 성장하고 분열하는 동안에도 나노껍질 형성이 지속적으로 일어나도록 설계돼 있어서, 세포의 형태 변화에 따라 비대칭적인 세포-껍질 구조가 자연스럽게 생성된다.
예를 들어, 분열 중인 세포 전체를 감싸는 껍질이 형성되기도 하지만, 모세포 부분에는 껍질이 생성되고 딸세포 부분에는 형성되지 않는 구조도 만들어진다.
연구팀은 세포를 감싸는 나노껍질에 우레아제(urease)*를 부착하고 세포로봇의 움직임을 관찰했다. 우레아제는 요소를 분해하는 촉매 역할을 하며 세포로봇이 스스로 움직일 수 있도록 구동력을 만들어내는 핵심 역할을 수행하며 비대칭 구조를 가진 세포로봇이 보다 명확한 방향성을 갖고 자가 추진하는 현상을 확인했다.
*우레아제(urease): 요소를 분해해 암모니아와 이산화탄소를 만드는 효소
이번에 개발된 세포로봇은 세포 주위에 존재하는 물질만으로 자가 추진이 가능하고, 자석이나 레이저 등 복잡한 외부 제어 장치에 의존하지 않아 구동 메커니즘이 훨씬 간단하고 생체친화적이다. 또한, 나노껍질에 다양한 효소를 화학적으로 접합할 수 있어, 다양한 생체 물질을 연료로 활용하는 세포로봇의 확장 개발도 가능하다.
이번 연구의 제1 저자인 화학과 김나영 박사과정은 “자가 추진 세포로봇은 스스로 환경을 감지하고 반응하며 움직이는 능력을 지닌 새로운 개념의 플랫폼으로, 향후 암세포 표적 치료나 정밀 약물전달시스템 등에서 중요한 역할을 할 수 있을 것”이라고 말했다.
이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’에 지난 6월 25일 오후 2시(미국 동부시각) 온라인판에 게재됐다.
※ 논문명 : Autonomous Chemo-Metabolic Construction of Anisotropic Cell-in-Shell Nanobiohybrids in Enzyme-Powered Cell Microrobots; 국문 번역 : 효소 구동 세포 마이크로로봇 구축에서의 자율적인 화학-대사 반응을 통해 형성된 비등방성 세포내껍질 나노바이오하이브리드
※ DOI: https://doi.org/10.1126/sciadv.adu5451
한편, 이번 연구는 한국연구재단 기초연구사업 중견연구과제(제목: 세포대사 연계형 단일세포나노피포화)의 지원을 받아 수행됐다.
2025.06.30 조회수 1212