%EC%86%90%EC%A2%85%EC%9A%B0
-
 비정형 항정신병 약물에 의한 비만의 원인 규명
우리 대학 생명과학과 손종우 교수 연구팀이 *비정형 항정신병 약물로 인해 발생하는 비만의 원인을 규명하는 데 성공했다고 17일 밝혔다.
☞ 비정형 항정신병 약물: 중추신경계의 도파민 수용체 및 세로토닌 수용체에 결합해 뇌 신경 전달물질의 작용을 차단함으로써 조현병 치료에 사용된다. 약리작용이 한 가지에 국한되지 않았다는 뜻으로 비정형 항정신병 약물이라 부르며, 비교적 최근에 개발된 약물이다.
이번 연구를 통해 향후 비정형 항정신병 약물을 처방받는 환자들에게 발생하는 비만을 예방할 수 있는 전략 수립에 도움을 줌으로써, 환자들의 약물 순응도를 높이고 질병 치료에 집중할 수 있도록 할 것으로 기대된다.
생명과학과 유은선 석박사통합과정 학생이 공동 제1 저자로 참여하고, 미국 텍사스 주립대학 사우스웨스턴 메디컬센터 첸 리우(Chen Liu) 교수와의 공동연구로 진행한 이번 연구 결과는 국제 학술지 `실험의학저널 (Journal of Experimental Medicine)' 218권 7호에 12일 字 온라인 게재됐다. (논문명 : The Atypical Antipsychotic Risperidone Targets Hypothalamic Melanocortin 4 Receptors to Cause Weight Gain)
`리스페리돈', `올란자핀'과 같은 비정형 항정신병 약물은 조현병, 양극성 장애 및 자폐 스펙트럼 장애 등 다양한 신경정신질환을 치료하기 위해 널리 처방되고 있다. 비정형 항정신병 약물은 정형 항정신병 약물과 비교해 운동계 부작용이 적으나 과도한 식욕과 비만을 유발하는 문제점이 있는데, 기존 동물 모델에서는 환자에게서 나타나는 비만이 재현되지 않아 비정형 항정신병 약물이 비만을 유발하는 원인을 알아내는 데 한계가 있었다.
손 교수와 리우 교수 연구팀은 리스페리돈을 먹이에 포함해 생쥐에게 먹임으로써 동물 모델을 이용해 이들 약물에 의한 식욕 증가와 비만을 재현하는 데 성공했다. 연구팀은 이 모델을 이용해 리스페리돈이 우리 몸의 항상성을 조절하는 뇌 부위인 시상하부에서 식욕을 억제하는 중요한 신경 전달물질 중 하나인 멜라노코르틴에 대한 반응성을 감소시킨다는 사실을 확인했다.
또한, 연구팀은 조현병 모델 생쥐에서 리스페리돈과 함께 멜라노코르틴 반응성 신경 세포 활성도를 높여 작용하는 식욕 억제제인 세트멜라노티드를 처치하면 리스페리돈의 항정신병 효과를 보존하면서도 비만을 예방할 수 있음을 확인했다. 세트멜라노티드(상품명: 임시브리)는 작년 11월 미국 FDA의 승인을 받고 현재 몇 가지 유전적 요인에 의한 비만 치료에 이용되고 있는 약물이다.
손종우 교수는 "비정형 항정신병 약물에 의한 식욕 증가와 비만의 원인을 신경 세포와 분자 수준에서 처음 규명한 것으로 향후 이들 약물을 이용한 신경정신질환 치료에 도움이 될 것으로 기대된다ˮ라고 말했다.
또한, "리스페리돈이 시상하부 멜라노코르틴 반응성을 저하한다는 사실을 확인했으나, 이 현상이 다른 비정형 항정신병 약물에도 적용되는지 아직 밝혀지지 않아 이 부분에 관한 연구에 집중할 계획이다ˮ라고 밝혔다.
이번 연구는 한국연구재단 중견연구자지원사업의 지원을 통해 수행됐다.
2021.05.17 조회수 45579
비정형 항정신병 약물에 의한 비만의 원인 규명
우리 대학 생명과학과 손종우 교수 연구팀이 *비정형 항정신병 약물로 인해 발생하는 비만의 원인을 규명하는 데 성공했다고 17일 밝혔다.
☞ 비정형 항정신병 약물: 중추신경계의 도파민 수용체 및 세로토닌 수용체에 결합해 뇌 신경 전달물질의 작용을 차단함으로써 조현병 치료에 사용된다. 약리작용이 한 가지에 국한되지 않았다는 뜻으로 비정형 항정신병 약물이라 부르며, 비교적 최근에 개발된 약물이다.
이번 연구를 통해 향후 비정형 항정신병 약물을 처방받는 환자들에게 발생하는 비만을 예방할 수 있는 전략 수립에 도움을 줌으로써, 환자들의 약물 순응도를 높이고 질병 치료에 집중할 수 있도록 할 것으로 기대된다.
생명과학과 유은선 석박사통합과정 학생이 공동 제1 저자로 참여하고, 미국 텍사스 주립대학 사우스웨스턴 메디컬센터 첸 리우(Chen Liu) 교수와의 공동연구로 진행한 이번 연구 결과는 국제 학술지 `실험의학저널 (Journal of Experimental Medicine)' 218권 7호에 12일 字 온라인 게재됐다. (논문명 : The Atypical Antipsychotic Risperidone Targets Hypothalamic Melanocortin 4 Receptors to Cause Weight Gain)
`리스페리돈', `올란자핀'과 같은 비정형 항정신병 약물은 조현병, 양극성 장애 및 자폐 스펙트럼 장애 등 다양한 신경정신질환을 치료하기 위해 널리 처방되고 있다. 비정형 항정신병 약물은 정형 항정신병 약물과 비교해 운동계 부작용이 적으나 과도한 식욕과 비만을 유발하는 문제점이 있는데, 기존 동물 모델에서는 환자에게서 나타나는 비만이 재현되지 않아 비정형 항정신병 약물이 비만을 유발하는 원인을 알아내는 데 한계가 있었다.
손 교수와 리우 교수 연구팀은 리스페리돈을 먹이에 포함해 생쥐에게 먹임으로써 동물 모델을 이용해 이들 약물에 의한 식욕 증가와 비만을 재현하는 데 성공했다. 연구팀은 이 모델을 이용해 리스페리돈이 우리 몸의 항상성을 조절하는 뇌 부위인 시상하부에서 식욕을 억제하는 중요한 신경 전달물질 중 하나인 멜라노코르틴에 대한 반응성을 감소시킨다는 사실을 확인했다.
또한, 연구팀은 조현병 모델 생쥐에서 리스페리돈과 함께 멜라노코르틴 반응성 신경 세포 활성도를 높여 작용하는 식욕 억제제인 세트멜라노티드를 처치하면 리스페리돈의 항정신병 효과를 보존하면서도 비만을 예방할 수 있음을 확인했다. 세트멜라노티드(상품명: 임시브리)는 작년 11월 미국 FDA의 승인을 받고 현재 몇 가지 유전적 요인에 의한 비만 치료에 이용되고 있는 약물이다.
손종우 교수는 "비정형 항정신병 약물에 의한 식욕 증가와 비만의 원인을 신경 세포와 분자 수준에서 처음 규명한 것으로 향후 이들 약물을 이용한 신경정신질환 치료에 도움이 될 것으로 기대된다ˮ라고 말했다.
또한, "리스페리돈이 시상하부 멜라노코르틴 반응성을 저하한다는 사실을 확인했으나, 이 현상이 다른 비정형 항정신병 약물에도 적용되는지 아직 밝혀지지 않아 이 부분에 관한 연구에 집중할 계획이다ˮ라고 밝혔다.
이번 연구는 한국연구재단 중견연구자지원사업의 지원을 통해 수행됐다.
2021.05.17 조회수 45579 -
 소금 섭취 제어할 수 있는 신체 메커니즘 규명
우리 대학 생명과학과 손종우 교수 연구팀이 각종 성인병의 원인으로 알려진 과도한 소금 섭취를 제어할 수 있는 메커니즘을 규명하는 데 성공했다.
이번 연구를 통해 향후 소금의 섭취를 적절하게 제한하는 전략 수립에 도움을 줌으로써 고혈압, 신부전 등 소금 섭취와 밀접하게 관련된 각종 질병 치료에 이바지할 수 있을 것으로 기대된다.
박시형 박사과정이 1 저자로 참여하고, 미국 텍사스 주립대학 사우스웨스턴 메디컬 센터 첸 리우(Chen Liu) 교수와의 공동연구로 진행한 이번 연구 결과는 국제 학술지 ‘네이처 뉴로사이언스(Nature Neuroscience)’ 1월 20일 자 온라인판에 게재됐다. (논문명 : A Neural Basis for Tonic Suppression of Sodium Appetite)
우리 몸의 체액은 혈액, 간질액 등을 포함하는 세포외액과 세포내액으로 구성돼 있다. 소금의 주요 성분인 나트륨 이온은 세포외액에 분포돼 삼투 현상에 의해 세포내액에 있는 수분을 끌어당긴다.
체내에 나트륨 이온이 과량 존재하면 혈액과 간질액의 부피가 증가해 혈압 상승, 부종 발생 등이 일어날 수 있어 적정한 수준으로 소금을 섭취하는 것이 중요하다.
특히 신부전 등과 같이 체액량 조절이 중요한 질병이 있는 환자의 경우 과도한 소금 섭취가 치명적임에도 적절한 조절이 어려운 것이 현실이다. 따라서 많은 의사와 과학자들이 소금 섭취를 효과적으로 제어할 방법에 대해 고민해 왔다.
손종우 교수 연구팀은 중요한 신경 전달 물질 중 하나인 세로토닌의 기능에 주목했다. 뇌줄기 안에 있는 세로토닌 반응성 신경 세포가 평상시에도 활성화돼 있어 이 세포가 소금의 섭취를 억제한다는 사실을 밝혀냈다. 그리고 세로토닌에 반응하는 현상을 재현하면 이 신경 세포의 활성이 억제돼 소금 섭취가 증가하는 현상을 확인했다.
최근 미국의 연구팀 등이 체액량이 감소했을 때 활성화돼 소금의 섭취를 증가시키는 신경 회로를 제시한 바 있으나, 평상시에 소금 섭취를 억제하는 메커니즘이 존재하고 이를 활용해 소금 섭취를 제어할 수 있다는 것은 손 교수 연구팀이 최초로 발견했다.
손종우 교수는 "소금 섭취를 제어할 수 있는 메커니즘을 분자 수준에서 규명한 것으로 향후 고혈압, 신부전 등 과도한 소금 섭취와 관련된 각종 질환 치료에 도움이 될 것으로 기대된다"라고 말했다.
또한, "소금 섭취 욕구와 세로토닌 신경회로 간의 상관관계를 규명했으나, 어떤 상황에서 세로토닌이 분비되는지는 아직 밝혀지지 않아 이 부분에 대한 연구에 집중할 계획이다"라고 밝혔다.
이번 연구는 삼성미래기술육성재단과 KAIST 시스템헬스케어사업 및 석박사모험연구사업의 지원을 통해 수행됐다.
□ 그림 설명
2020.02.12 조회수 10173
소금 섭취 제어할 수 있는 신체 메커니즘 규명
우리 대학 생명과학과 손종우 교수 연구팀이 각종 성인병의 원인으로 알려진 과도한 소금 섭취를 제어할 수 있는 메커니즘을 규명하는 데 성공했다.
이번 연구를 통해 향후 소금의 섭취를 적절하게 제한하는 전략 수립에 도움을 줌으로써 고혈압, 신부전 등 소금 섭취와 밀접하게 관련된 각종 질병 치료에 이바지할 수 있을 것으로 기대된다.
박시형 박사과정이 1 저자로 참여하고, 미국 텍사스 주립대학 사우스웨스턴 메디컬 센터 첸 리우(Chen Liu) 교수와의 공동연구로 진행한 이번 연구 결과는 국제 학술지 ‘네이처 뉴로사이언스(Nature Neuroscience)’ 1월 20일 자 온라인판에 게재됐다. (논문명 : A Neural Basis for Tonic Suppression of Sodium Appetite)
우리 몸의 체액은 혈액, 간질액 등을 포함하는 세포외액과 세포내액으로 구성돼 있다. 소금의 주요 성분인 나트륨 이온은 세포외액에 분포돼 삼투 현상에 의해 세포내액에 있는 수분을 끌어당긴다.
체내에 나트륨 이온이 과량 존재하면 혈액과 간질액의 부피가 증가해 혈압 상승, 부종 발생 등이 일어날 수 있어 적정한 수준으로 소금을 섭취하는 것이 중요하다.
특히 신부전 등과 같이 체액량 조절이 중요한 질병이 있는 환자의 경우 과도한 소금 섭취가 치명적임에도 적절한 조절이 어려운 것이 현실이다. 따라서 많은 의사와 과학자들이 소금 섭취를 효과적으로 제어할 방법에 대해 고민해 왔다.
손종우 교수 연구팀은 중요한 신경 전달 물질 중 하나인 세로토닌의 기능에 주목했다. 뇌줄기 안에 있는 세로토닌 반응성 신경 세포가 평상시에도 활성화돼 있어 이 세포가 소금의 섭취를 억제한다는 사실을 밝혀냈다. 그리고 세로토닌에 반응하는 현상을 재현하면 이 신경 세포의 활성이 억제돼 소금 섭취가 증가하는 현상을 확인했다.
최근 미국의 연구팀 등이 체액량이 감소했을 때 활성화돼 소금의 섭취를 증가시키는 신경 회로를 제시한 바 있으나, 평상시에 소금 섭취를 억제하는 메커니즘이 존재하고 이를 활용해 소금 섭취를 제어할 수 있다는 것은 손 교수 연구팀이 최초로 발견했다.
손종우 교수는 "소금 섭취를 제어할 수 있는 메커니즘을 분자 수준에서 규명한 것으로 향후 고혈압, 신부전 등 과도한 소금 섭취와 관련된 각종 질환 치료에 도움이 될 것으로 기대된다"라고 말했다.
또한, "소금 섭취 욕구와 세로토닌 신경회로 간의 상관관계를 규명했으나, 어떤 상황에서 세로토닌이 분비되는지는 아직 밝혀지지 않아 이 부분에 대한 연구에 집중할 계획이다"라고 밝혔다.
이번 연구는 삼성미래기술육성재단과 KAIST 시스템헬스케어사업 및 석박사모험연구사업의 지원을 통해 수행됐다.
□ 그림 설명
2020.02.12 조회수 10173 -
 전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
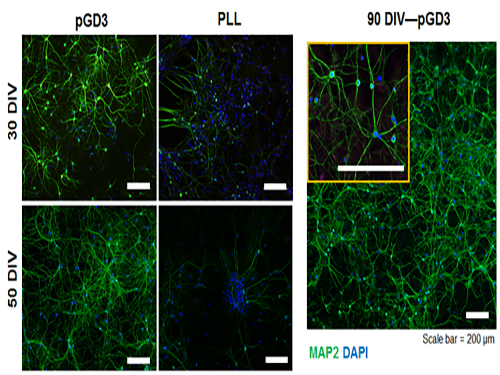
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
2016.11.17 조회수 26541
전상용, 임성갑 교수, 신경세포의 안정적 배양 가능한 플랫폼 개발
우리 대학 생명과학과 전상용 교수와 생명화학공학과 임성갑 교수 공동 연구팀이 신경세포를 장기적, 안정적으로 배양할 수 있는 아세틸콜린 유사 고분자 박막 소재를 개발했다.
특히 이 연구는 KAIST의 ‘학부생 연구 참여 프로그램(URP : Undergraduate research program)’을 통해 유승윤 학부생이 참여해 더욱 큰 의미를 갖는다.
유승윤 학부생을 포함해 백지응 박사과정, 최민석 박사가 공동 1저자로 참여한 이번 연구 성과는 나노분야 학술지 ‘에이시에스 나노(ACS Nano)’ 10월 28일자 온라인 판에 게재됐다.
신경세포는 알츠하이머, 파킨슨병, 헌팅턴병 등의 신경퇴행성 질환 및 신경 기반 바이오센서 등 전반적인 신경관련 응용연구에 꼭 필요한 요소이다.
대부분의 신경 질환이 노인성, 퇴행성이기 때문에 신경세포가 오래됐을 때 어떤 현상이 발생하는지 관찰할 수 있어야 한다. 하지만 신경세포는 장기 배양이 어려워 퇴행 상태가 되기 전에 세포가 죽게 돼 관찰이 어려웠다.
기존에는 특정 수용성 고분자(PLL)를 배양접시 위에 코팅하는 방법을 통해 신경세포를 배양했다. 그러나 이 방법은 장기적, 안정적인 세포 배양이 불가능하기 때문에 신경세포를 안정적으로 장기 배양할 수 있는 새로운 플랫폼이 필요하다.
연구팀은 문제 해결을 위해 ‘개시제를 이용한 화학 기상 증착법(iCVD : initiated chemical vapor deposition)’을 이용했다. iCVD는 기체 상태의 반응물을 이용해 고분자를 박막 형태로 합성하는 방법으로, 기존 세포 배양 기판 위에 손쉽게 얇고 안정적인 박막을 형성시킬 수 있다.
연구팀은 이러한 기체상 공정의 장점을 이용해 신경세포를 장기적으로 배양할 수 있는 기능을 가진 공중합체 고분자 박막을 합성하는 데 성공했다. 새로 합성된 이 고분자 박막은 신경전달물질로 알려진 아세틸콜린과 유사한 물질로 이뤄져 있다.
또한 신경세포가 고분자 박막에서 배양될 수 있는 최적화된 조건을 발견했고, 이 조건에서 생존에 관여하는 여러 신경관련 유전자를 확인했다.
연구팀은 생명과학과 손종우 교수 연구팀의 도움을 통해 새로 배양된 신경세포가 기존의 신경세포보다 전기생리학적 측면 및 신경전달 기능적 측면에서 안정화됨을 확인했다.
연구팀은 “신경세포를 장기적으로 배양할 수 있는 이 기술은 향후 신경세포를 이용한 바이오센서와 신경세포 칩 개발의 핵심 소재로 활용될 것이다”며 “다양한 신경 관련 질병의 원리를 이해할 수 있는 역할을 할 것으로 기대된다”고 말했다.
이번 연구는 한국보건산업진흥원과 한국연구재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 본 연구에서 개발된 표면(pGD3) 및 폴리라이신 코팅 위에서 장시간 배양된 신경세포
그림2. 신경전달물질 유사 작용기를 도입한 표면 형성 과정
2016.11.17 조회수 26541