-
 5단 수직 적층 반도체 트랜지스터 개발
우리 대학 전기 및 전자공학부 이병현 연구원(지도교수 최양규)과 나노종합기술원(원장 이재영) 강민호 박사가 실리콘 기반의 5단 수직 적층 반도체 트랜지스터를 개발했다.
그리고 반도체 트랜지스터를 이용한 비휘발성 메모리 개발에 성공했다.
이번 연구는 나노 분야 학술지 ‘나노 레터스(Nano letters)’ 11월 6일자 온라인판에 게재됐다.
반도체 트랜지스터 분야는 모든 전자기기의 핵심 구성요소로 국내 산업과 경제 발전에 큰 영향을 끼쳤다.
세계적 추세에 따라 치열한 소형화를 통해 생산성과 성능의 향상을 거듭했으나 최근 10나노미터 시대에 접어들며 제작 공정의 한계 및 누설전류로 인한 전력소모 문제가 커지고 있다.
학계 및 산업계는 문제 해결을 위해 전면-게이트 실리콘 나노선 구조를 개발했다. 이는 누설전류 제어에 가장 효과적인 구조로 저전력 트랜지스터 개발에 이용됐다. 그러나 이 역시 소형화에 따른 나노선 면적 감소로 성능 저하의 한계가 있었다.
연구팀은 전면-게이트 실리콘 나노선을 수직으로 5단으로 쌓아 문제를 해결했다. 이 5단 적층 실리콘 나노선 채널을 보유한 반도체 트랜지스터는 단일 나노선 기반의 트랜지스터보다 5배의 향상된 성능을 보였다.
또한 수직 적층 나노선 구조는 말 그대로 위로 쌓기 때문에 단일 구조와 달리 면적이 증가되지 않아 집적도 향상에도 기여할 수 있다.
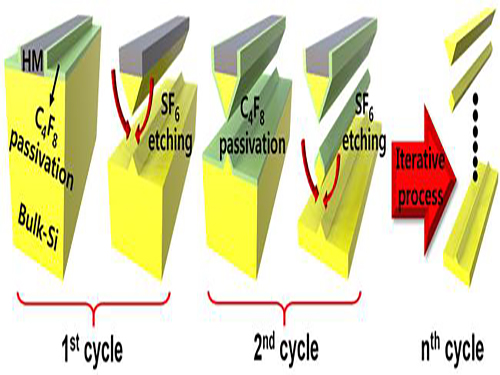
나노선 수직 적층은 개발된 ‘일괄 플라즈마 건식 식각 공정’ 방식을 통해 이뤄졌다. 이 공정은 고분자 중합체를 이용해 패턴이 형성될 영역에 미리 보호막을 친 뒤 등방성 건식 식각을 통해 나노선 구조를 형성하는 기술이다. 수직 적층 나노선 구조는 이 기술의 연속 작용을 통해 확보한 결과물이다.
이 기술은 지속적 소형화로 인해 기술적 한계에 부딪힌 반도체 트랜지스터 분야에 새로운 돌파구를 제시할 것으로 기대된다.
관련 연구가 이전부터 진행됐지만 더 간단한 공정기술을 이용해 가장 많은 나노선 채널의 적층에 성공했기 때문에 비용절감 및 제작 시간 단축, 반도체 트랜지스터의 성능 향상으로 인한 상용화 등에 크게 기여할 것으로 예상된다.
연구팀은 건식 식각 공정 기술이 기존 방법보다 간단하고 안정적으로 수직 적층 실리콘나노선 구조 제작을 가능하게 함으로써 고성능 트랜지스터 개발에 응용 가능할 것이라고 밝혔다.
이병현 연구원과 강민호 박사는 “이번 기술 개발은 미래창조 국가 나노기술 인프라 기관 나노종합기술원의 훌륭한 반도체 연구 기반과 김진수 부장 포함 관련 연구진들의 우수한 공정 능력이 뒷받침돼 가능했다”고 소감을 말했다.
이번 연구는 글로벌프론티어사업 스마트IT융합시스템 연구단의 지원을 받아 수행됐다.
연구를 주도한 이병현 연구원은 우리 대학 최양규 교수 지도하에 박사과정을 수행 중이며, 삼성전자 메모리 사업부의 책임 연구원으로 재직 중이다.
□ 그림 설명
그림1. 일괄 플라즈마 건식 식각 공정 과정의 모식도.
그림2. 서로 다른 방향에서 단면을 관찰한 주사 전자 현미경 사진 및 투과 전자 현미경 사진
5단 수직 적층 반도체 트랜지스터 개발
우리 대학 전기 및 전자공학부 이병현 연구원(지도교수 최양규)과 나노종합기술원(원장 이재영) 강민호 박사가 실리콘 기반의 5단 수직 적층 반도체 트랜지스터를 개발했다.
그리고 반도체 트랜지스터를 이용한 비휘발성 메모리 개발에 성공했다.
이번 연구는 나노 분야 학술지 ‘나노 레터스(Nano letters)’ 11월 6일자 온라인판에 게재됐다.
반도체 트랜지스터 분야는 모든 전자기기의 핵심 구성요소로 국내 산업과 경제 발전에 큰 영향을 끼쳤다.
세계적 추세에 따라 치열한 소형화를 통해 생산성과 성능의 향상을 거듭했으나 최근 10나노미터 시대에 접어들며 제작 공정의 한계 및 누설전류로 인한 전력소모 문제가 커지고 있다.
학계 및 산업계는 문제 해결을 위해 전면-게이트 실리콘 나노선 구조를 개발했다. 이는 누설전류 제어에 가장 효과적인 구조로 저전력 트랜지스터 개발에 이용됐다. 그러나 이 역시 소형화에 따른 나노선 면적 감소로 성능 저하의 한계가 있었다.
연구팀은 전면-게이트 실리콘 나노선을 수직으로 5단으로 쌓아 문제를 해결했다. 이 5단 적층 실리콘 나노선 채널을 보유한 반도체 트랜지스터는 단일 나노선 기반의 트랜지스터보다 5배의 향상된 성능을 보였다.
또한 수직 적층 나노선 구조는 말 그대로 위로 쌓기 때문에 단일 구조와 달리 면적이 증가되지 않아 집적도 향상에도 기여할 수 있다.
나노선 수직 적층은 개발된 ‘일괄 플라즈마 건식 식각 공정’ 방식을 통해 이뤄졌다. 이 공정은 고분자 중합체를 이용해 패턴이 형성될 영역에 미리 보호막을 친 뒤 등방성 건식 식각을 통해 나노선 구조를 형성하는 기술이다. 수직 적층 나노선 구조는 이 기술의 연속 작용을 통해 확보한 결과물이다.
이 기술은 지속적 소형화로 인해 기술적 한계에 부딪힌 반도체 트랜지스터 분야에 새로운 돌파구를 제시할 것으로 기대된다.
관련 연구가 이전부터 진행됐지만 더 간단한 공정기술을 이용해 가장 많은 나노선 채널의 적층에 성공했기 때문에 비용절감 및 제작 시간 단축, 반도체 트랜지스터의 성능 향상으로 인한 상용화 등에 크게 기여할 것으로 예상된다.
연구팀은 건식 식각 공정 기술이 기존 방법보다 간단하고 안정적으로 수직 적층 실리콘나노선 구조 제작을 가능하게 함으로써 고성능 트랜지스터 개발에 응용 가능할 것이라고 밝혔다.
이병현 연구원과 강민호 박사는 “이번 기술 개발은 미래창조 국가 나노기술 인프라 기관 나노종합기술원의 훌륭한 반도체 연구 기반과 김진수 부장 포함 관련 연구진들의 우수한 공정 능력이 뒷받침돼 가능했다”고 소감을 말했다.
이번 연구는 글로벌프론티어사업 스마트IT융합시스템 연구단의 지원을 받아 수행됐다.
연구를 주도한 이병현 연구원은 우리 대학 최양규 교수 지도하에 박사과정을 수행 중이며, 삼성전자 메모리 사업부의 책임 연구원으로 재직 중이다.
□ 그림 설명
그림1. 일괄 플라즈마 건식 식각 공정 과정의 모식도.
그림2. 서로 다른 방향에서 단면을 관찰한 주사 전자 현미경 사진 및 투과 전자 현미경 사진
2015.11.24
조회수 16500
-
 광섬유로 300조분의 1초 오차의 클럭 개발
〈김 정 원 교수〉
우리 대학 기계항공공학부 김정원 교수 연구팀이 광섬유 광학 기술로 수백조분의 1초 오차를 가지는 클럭(clock) 원천기술을 개발했다.
이는 클럭 발진기(oscillator)의 성능을 획기적으로 향상시킬 수 있는 원천 기술로 성과를 인정받아 국제학술지 ‘사이언티픽 리포트(Scientific Reports)’ 11월 4일자 온라인 판에 게재됐다.
클럭 발진기는 일정한 시간 간격의 주기적 신호를 발생시켜 전자시스템이 신호에 맞춰 정확하게 동작하도록 만드는 장치이다. 음악 연주에서 메트로놈과 같은 역할을 한다.
이 클럭 발진기는 오늘날 각종 정보통신 시스템 뿐 아니라 입자가속기나 천체관측장치 같은 거대 과학시설, 초정밀 계측 장비, 레이더, GPS 및 위성항법 시스템 등 전 분야에 걸쳐 핵심적 역할을 하고 있다. 따라서 클럭 발진기에서 발생하는 주기적 신호의 시간 오차를 줄인다면 각종 시스템들의 획기적인 성능 향상과 이전에는 불가능했던 기술 개발도 가능해진다.
기존에는 특수 제작된 공진 회로를 이용한 라디오파 혹은 마이크로파 발진기를 사용하거나 광공진기의 주파수 나눔을 이용한 방식의 기술을 사용했으나, 이 방식은 크기가 클 뿐 아니라 기계적 안정도가 떨어지고 수억 원 이상의 고가였기 때문에 실험실 밖에서의 응용 등에 한계가 있었다.
연구팀은 문제 해결을 위해 신뢰성이 높고 가격경쟁력이 확보된 광통신용 광섬유 부품을 활용한 새로운 방식의 클럭 발진기를 개발했다.
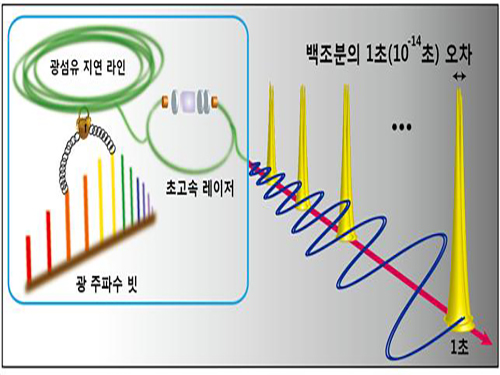
기술의 핵심은 초고속 광섬유 레이저에서 발생하는 넓은 스펙트럼 내의 두 광주파수(optical frequency) 차이를 이용한 것이다. 기존 전자 발진기는 기가헤르츠(GHz, 1초에 109회 진동) 영역에서 동작하지만, 이 기술은 이보다 테라헤르츠(THz, 1초에 1012회 진동) 주파수를 이용하기 때문에 약 1000배 민감한 시간 차 측정이 가능하다.
또한 광섬유 케이블에서 빛이 전파되는 시간이 매우 일정하게 유지되기 때문에 테라헤르츠 주파수를 이용해 높은 분해능으로 측정된 시간차를 광섬유 케이블 내에서의 빛의 전파 시간에 정확하게 맞췄다.
그 결과 국제전기통신연합(ITU)에서 정의한 클럭 신호원의 성능을 나타내는 0.1초 동안의 시간오차인 타이밍 지터(timing jitter)가 3펨토초(333조분의 1초)로 측정됐으며, 이는 환산하면 100만년 동안 1초의 오차를 갖는 성능에 해당한다.
이를 통해 별도의 특수 제작된 고가 소자 없이도 세계적 수준의 클럭 발진기 성능을 얻을 수 있고, 상용화 시 제작비용을 기존 최고 성능 발진기의 10분의 1 이하 수준으로 낮출 것으로 기대된다.
연구팀은 이 기술의 성능과 안정성이 아날로그-디지털 변환기나 고성능 신호 분석기와 같은 ICT 시스템, 레이더, 원격 탐사, 위성항법 등 국방, 우주, 환경 기술 분야에서도 폭넓게 활용될 수 있을 것이라고 밝혔다.
김 교수는 “이 기술은 군용 레이더, 보안 분야와의 연관성 때문에 주요 장비들의 수출이 금지된 경우가 많아 순수 국내 기술로 자체 개발한 것은 그 의의가 크다.”며 “향후 유리기판 위에 시스템을 구현해 칩 스케일의 고성능 클럭으로 발전시킬 계획이다”고 말했다.
KAIST 기계공학과 정광연 박사과정(1저자)의 참여로 이루어진 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 수백조분의 1초 오차의 광섬유 클럭 발진기 개념도
광섬유로 300조분의 1초 오차의 클럭 개발
〈김 정 원 교수〉
우리 대학 기계항공공학부 김정원 교수 연구팀이 광섬유 광학 기술로 수백조분의 1초 오차를 가지는 클럭(clock) 원천기술을 개발했다.
이는 클럭 발진기(oscillator)의 성능을 획기적으로 향상시킬 수 있는 원천 기술로 성과를 인정받아 국제학술지 ‘사이언티픽 리포트(Scientific Reports)’ 11월 4일자 온라인 판에 게재됐다.
클럭 발진기는 일정한 시간 간격의 주기적 신호를 발생시켜 전자시스템이 신호에 맞춰 정확하게 동작하도록 만드는 장치이다. 음악 연주에서 메트로놈과 같은 역할을 한다.
이 클럭 발진기는 오늘날 각종 정보통신 시스템 뿐 아니라 입자가속기나 천체관측장치 같은 거대 과학시설, 초정밀 계측 장비, 레이더, GPS 및 위성항법 시스템 등 전 분야에 걸쳐 핵심적 역할을 하고 있다. 따라서 클럭 발진기에서 발생하는 주기적 신호의 시간 오차를 줄인다면 각종 시스템들의 획기적인 성능 향상과 이전에는 불가능했던 기술 개발도 가능해진다.
기존에는 특수 제작된 공진 회로를 이용한 라디오파 혹은 마이크로파 발진기를 사용하거나 광공진기의 주파수 나눔을 이용한 방식의 기술을 사용했으나, 이 방식은 크기가 클 뿐 아니라 기계적 안정도가 떨어지고 수억 원 이상의 고가였기 때문에 실험실 밖에서의 응용 등에 한계가 있었다.
연구팀은 문제 해결을 위해 신뢰성이 높고 가격경쟁력이 확보된 광통신용 광섬유 부품을 활용한 새로운 방식의 클럭 발진기를 개발했다.
기술의 핵심은 초고속 광섬유 레이저에서 발생하는 넓은 스펙트럼 내의 두 광주파수(optical frequency) 차이를 이용한 것이다. 기존 전자 발진기는 기가헤르츠(GHz, 1초에 109회 진동) 영역에서 동작하지만, 이 기술은 이보다 테라헤르츠(THz, 1초에 1012회 진동) 주파수를 이용하기 때문에 약 1000배 민감한 시간 차 측정이 가능하다.
또한 광섬유 케이블에서 빛이 전파되는 시간이 매우 일정하게 유지되기 때문에 테라헤르츠 주파수를 이용해 높은 분해능으로 측정된 시간차를 광섬유 케이블 내에서의 빛의 전파 시간에 정확하게 맞췄다.
그 결과 국제전기통신연합(ITU)에서 정의한 클럭 신호원의 성능을 나타내는 0.1초 동안의 시간오차인 타이밍 지터(timing jitter)가 3펨토초(333조분의 1초)로 측정됐으며, 이는 환산하면 100만년 동안 1초의 오차를 갖는 성능에 해당한다.
이를 통해 별도의 특수 제작된 고가 소자 없이도 세계적 수준의 클럭 발진기 성능을 얻을 수 있고, 상용화 시 제작비용을 기존 최고 성능 발진기의 10분의 1 이하 수준으로 낮출 것으로 기대된다.
연구팀은 이 기술의 성능과 안정성이 아날로그-디지털 변환기나 고성능 신호 분석기와 같은 ICT 시스템, 레이더, 원격 탐사, 위성항법 등 국방, 우주, 환경 기술 분야에서도 폭넓게 활용될 수 있을 것이라고 밝혔다.
김 교수는 “이 기술은 군용 레이더, 보안 분야와의 연관성 때문에 주요 장비들의 수출이 금지된 경우가 많아 순수 국내 기술로 자체 개발한 것은 그 의의가 크다.”며 “향후 유리기판 위에 시스템을 구현해 칩 스케일의 고성능 클럭으로 발전시킬 계획이다”고 말했다.
KAIST 기계공학과 정광연 박사과정(1저자)의 참여로 이루어진 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 수백조분의 1초 오차의 광섬유 클럭 발진기 개념도
2015.11.12
조회수 13588
-
 기체가 저장물질에 흡착되는 과정 관찰
우리 대학 EEWS 대학원 강정구 교수와 오사무 테라사키 공동 연구팀이 2~5 나노미터(10억분의 1m) 크기의 구멍을 갖는 메조다공성 금속유기골격체(metal organic framework, MOF) 안에 기체가 흡착되는 과정을 관찰하는 데 성공했다.
관찰 과정에서 기체들이 각자의 기공에 일정하지 않은 각기 다른 밀도로 흡착된다는 사실을 발견했다. 이는 기존의 학설과 반대되는 개념으로 금속유기골격체에서 기체가 초격자 구조를 형성한다는 사실을 최초로 발견한 것이다.
이번 연구는 국제 과학 학술지 ‘네이처’ 11월 9일자 온라인 판에 게재됐다.
메조다공성 금속유기골격체는 넓은 비표면적을 갖고 있어 수소나 메탄, 이산화탄소 등의 가스 저장에 용이한 저장물질이다. 효율적인 가스 저장을 위해서는 기체가 저장물질에 어떻게 흡착하는지 이해하는 것이 중요하다.
그러나 일반적인 기체 흡착 측정 장비의 경우에는 흡착 거동을 직접적으로 관찰할 수 없다는 한계가 있었다.
문제 해결을 위해 연구팀은 기존에 존재하는 두 개의 장비를 이용했다. 구조적 정보를 얻을 수 있는 X-선 소각산란(small angle X-ray scattering, SAXS) 측정 장비와 기체흡착 측정 장비를 결합했다.
두 장비가 결합된 실시간 기체 흡착 SAXS 시스템을 개발해 메조다공성 금속유기골격체의 결정에 기체가 흡착하는 과정을 실시간으로 관찰했다.
연구팀은 관찰 과정에서 금속유기골격체의 모든 기공에 기체가 균일하게 흡착되지 않고 각자 다른 밀도로 흡착된다는 사실을 발견했다. 그리고 압력이 증가하면서 급격하게 초격자 구조로 변이된 후 서서히 균일하게 분포하는 것 또한 확인했다.
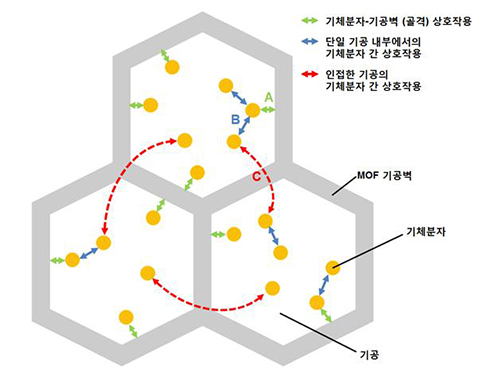
이는 모든 기공에 균일하게 기체가 들어간다는 학설을 뒤집는 발견이다. 이것이 가능했던 이유는 메조다공성 금속유기골격체의 경우 골격이 얇고 기공이 커 다른 구멍의 기체분자끼리도 상호작용하기 때문에 발생하는 현상이다.
따라서 메조다공성 금속유기골격체를 사용한다면 기존 저장물질에 비해 더 적은 용량으로 더 많은 가스를 저장할 수 있는 고효율 저장장치를 개발할 수 있게 된다.
이 기술을 기반으로 새로운 고용량 가스저장 물질의 제작이 가능해짐으로써, 여러 운송수단이나 가스를 사용하는 기계의 성능을 끌어올릴 수 있을 것으로 기대된다.
연구를 주도한 조해성 박사는 “단일 기공 내부의 기체 분자 뿐 아니라 다른 기공의 기체 분자 간 상호작용에 의해 기체의 흡착 메커니즘이 발생함을 새롭게 발견했다”고 말했다.
이번 연구는 미래창조과학부 글로벌프론티어사업, 인공광합성사업, BK21PLUS의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 실시간 기체흡착 SAXS 시스템 모식도
그림2. 메조다공성 MOF 결정에 기체가 흡착되는 과정
그림3. 메조다공성 MOF 결정에서 기체분자의 상호작용 모델
기체가 저장물질에 흡착되는 과정 관찰
우리 대학 EEWS 대학원 강정구 교수와 오사무 테라사키 공동 연구팀이 2~5 나노미터(10억분의 1m) 크기의 구멍을 갖는 메조다공성 금속유기골격체(metal organic framework, MOF) 안에 기체가 흡착되는 과정을 관찰하는 데 성공했다.
관찰 과정에서 기체들이 각자의 기공에 일정하지 않은 각기 다른 밀도로 흡착된다는 사실을 발견했다. 이는 기존의 학설과 반대되는 개념으로 금속유기골격체에서 기체가 초격자 구조를 형성한다는 사실을 최초로 발견한 것이다.
이번 연구는 국제 과학 학술지 ‘네이처’ 11월 9일자 온라인 판에 게재됐다.
메조다공성 금속유기골격체는 넓은 비표면적을 갖고 있어 수소나 메탄, 이산화탄소 등의 가스 저장에 용이한 저장물질이다. 효율적인 가스 저장을 위해서는 기체가 저장물질에 어떻게 흡착하는지 이해하는 것이 중요하다.
그러나 일반적인 기체 흡착 측정 장비의 경우에는 흡착 거동을 직접적으로 관찰할 수 없다는 한계가 있었다.
문제 해결을 위해 연구팀은 기존에 존재하는 두 개의 장비를 이용했다. 구조적 정보를 얻을 수 있는 X-선 소각산란(small angle X-ray scattering, SAXS) 측정 장비와 기체흡착 측정 장비를 결합했다.
두 장비가 결합된 실시간 기체 흡착 SAXS 시스템을 개발해 메조다공성 금속유기골격체의 결정에 기체가 흡착하는 과정을 실시간으로 관찰했다.
연구팀은 관찰 과정에서 금속유기골격체의 모든 기공에 기체가 균일하게 흡착되지 않고 각자 다른 밀도로 흡착된다는 사실을 발견했다. 그리고 압력이 증가하면서 급격하게 초격자 구조로 변이된 후 서서히 균일하게 분포하는 것 또한 확인했다.
이는 모든 기공에 균일하게 기체가 들어간다는 학설을 뒤집는 발견이다. 이것이 가능했던 이유는 메조다공성 금속유기골격체의 경우 골격이 얇고 기공이 커 다른 구멍의 기체분자끼리도 상호작용하기 때문에 발생하는 현상이다.
따라서 메조다공성 금속유기골격체를 사용한다면 기존 저장물질에 비해 더 적은 용량으로 더 많은 가스를 저장할 수 있는 고효율 저장장치를 개발할 수 있게 된다.
이 기술을 기반으로 새로운 고용량 가스저장 물질의 제작이 가능해짐으로써, 여러 운송수단이나 가스를 사용하는 기계의 성능을 끌어올릴 수 있을 것으로 기대된다.
연구를 주도한 조해성 박사는 “단일 기공 내부의 기체 분자 뿐 아니라 다른 기공의 기체 분자 간 상호작용에 의해 기체의 흡착 메커니즘이 발생함을 새롭게 발견했다”고 말했다.
이번 연구는 미래창조과학부 글로벌프론티어사업, 인공광합성사업, BK21PLUS의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 실시간 기체흡착 SAXS 시스템 모식도
그림2. 메조다공성 MOF 결정에 기체가 흡착되는 과정
그림3. 메조다공성 MOF 결정에서 기체분자의 상호작용 모델
2015.11.11
조회수 14987
-
 화합물의 광학 활성 분석 기술 개발
〈 김 현 우 교수〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명 분광분석기(NMR)를 통해 전하를 띠는 화합물의 광학 활성을 간단히 분석할 수 있는 기술을 개발했다.
연구 결과는 화학분야 학술지 ‘미국화학회지(Journal of the American Chemical Society)’ 10월 19일자 온라인 판에 게재됐다.
오른손과 왼손처럼 같은 물질이지만 거울상 대칭이 되는 화합물을 광학 이성질체라고 한다.
지구상의 생명체를 이루는 아미노산과 당은 하나의 광학 이성질체로 이뤄져 있어 새로운 화합물이 생체에 들어갈 때 광학 활성에 따라 서로 다른 생리학적 특징을 나타낸다. 따라서 신약을 개발할 때 광학 활성을 조절하고 분석하는 연구는 필수적이다.
광학 활성의 분석 방법으로 고성능 액체 크로마토그래피(HPLC)가 주로 사용되는데, 고가의 부품을 구비해야 하고 30분에서 1시간 정도의 시간이 소요되는 단점이 있다.
또한 신호의 감도 및 분해 기능이 떨어지고 사용할 수 있는 용매가 무극성에 한정되는 점 때문에 활용에 한계가 있었다.
반면 화합물의 분자 구조 분석에 활용되는 핵자기공명(NMR) 분광분석기는 1~5분 정도의 빠른 분석속도를 갖고 있다. 또한 화학 분야에서 분자의 구조를 확인하기 위한 필수 장비이기 때문에 대부분의 연구실에서 구비된 상태다.
하지만 이 핵자기공명 분광분석기를 통해 광학 활성 화합물의 신호를 분리하는 효과적인 방법은 보고되지 않았다.
연구팀은 기존에 알려지지 않은 음전하를 띠는 금속 화합물과 핵자기공명 분광분석기를 이용해 분석 방법을 개발했다.
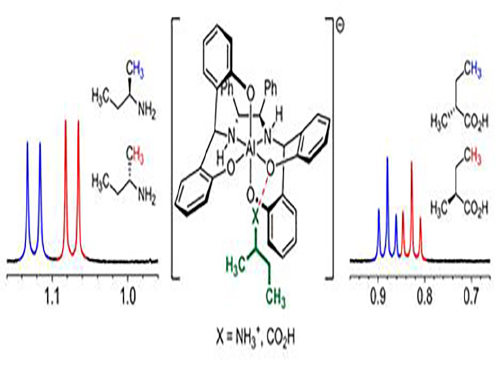
음전하를 띤 금속 화합물이 양전하 및 음전하를 갖는 광학활성 화합물과 이온성 결합을 하면 핵자기공명 분광분석기를 통해 신호가 구별돼 광학 활성을 분석할 수 있는 원리이다.
이 방법을 사용하면 구조적 제약 없이 다양한 화합물을 분석할 수 있고, 비극성 및 극성 용매에 모두 적용 가능하다는 장점을 갖는다.
연구팀은 다양한 신약 및 신약후보 물질들은 전하를 띨 수 있는 작용기를 포함한 경우가 많아 연구팀의 새로운 분석 방법이 신약 개발에 직접적으로 활용 가능할 것으로 기대된다고 밝혔다.
김 교수는 “간단한 화학적 원리를 통해 기존의 틀을 깨는 혁신적 분석방법을 만들었다”며 “이 방법이 신약개발에 많이 활용되길 기대한다”고 말했다.
화학과 서민섭 박사과정(1저자)의 참여로 이루어진 이번 연구는 기초과학연구원(IBS) 나노물질 및 화학반응 연구단과 슈퍼컴퓨팅연구지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 금속 화합물과 이온성 상호작용으로 광학활성을 가진 화합물의 NMR 신호가 분리되는 현상
그림2. 다양한 광학활성 물질이 분리되는 그림
화합물의 광학 활성 분석 기술 개발
〈 김 현 우 교수〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명 분광분석기(NMR)를 통해 전하를 띠는 화합물의 광학 활성을 간단히 분석할 수 있는 기술을 개발했다.
연구 결과는 화학분야 학술지 ‘미국화학회지(Journal of the American Chemical Society)’ 10월 19일자 온라인 판에 게재됐다.
오른손과 왼손처럼 같은 물질이지만 거울상 대칭이 되는 화합물을 광학 이성질체라고 한다.
지구상의 생명체를 이루는 아미노산과 당은 하나의 광학 이성질체로 이뤄져 있어 새로운 화합물이 생체에 들어갈 때 광학 활성에 따라 서로 다른 생리학적 특징을 나타낸다. 따라서 신약을 개발할 때 광학 활성을 조절하고 분석하는 연구는 필수적이다.
광학 활성의 분석 방법으로 고성능 액체 크로마토그래피(HPLC)가 주로 사용되는데, 고가의 부품을 구비해야 하고 30분에서 1시간 정도의 시간이 소요되는 단점이 있다.
또한 신호의 감도 및 분해 기능이 떨어지고 사용할 수 있는 용매가 무극성에 한정되는 점 때문에 활용에 한계가 있었다.
반면 화합물의 분자 구조 분석에 활용되는 핵자기공명(NMR) 분광분석기는 1~5분 정도의 빠른 분석속도를 갖고 있다. 또한 화학 분야에서 분자의 구조를 확인하기 위한 필수 장비이기 때문에 대부분의 연구실에서 구비된 상태다.
하지만 이 핵자기공명 분광분석기를 통해 광학 활성 화합물의 신호를 분리하는 효과적인 방법은 보고되지 않았다.
연구팀은 기존에 알려지지 않은 음전하를 띠는 금속 화합물과 핵자기공명 분광분석기를 이용해 분석 방법을 개발했다.
음전하를 띤 금속 화합물이 양전하 및 음전하를 갖는 광학활성 화합물과 이온성 결합을 하면 핵자기공명 분광분석기를 통해 신호가 구별돼 광학 활성을 분석할 수 있는 원리이다.
이 방법을 사용하면 구조적 제약 없이 다양한 화합물을 분석할 수 있고, 비극성 및 극성 용매에 모두 적용 가능하다는 장점을 갖는다.
연구팀은 다양한 신약 및 신약후보 물질들은 전하를 띨 수 있는 작용기를 포함한 경우가 많아 연구팀의 새로운 분석 방법이 신약 개발에 직접적으로 활용 가능할 것으로 기대된다고 밝혔다.
김 교수는 “간단한 화학적 원리를 통해 기존의 틀을 깨는 혁신적 분석방법을 만들었다”며 “이 방법이 신약개발에 많이 활용되길 기대한다”고 말했다.
화학과 서민섭 박사과정(1저자)의 참여로 이루어진 이번 연구는 기초과학연구원(IBS) 나노물질 및 화학반응 연구단과 슈퍼컴퓨팅연구지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 금속 화합물과 이온성 상호작용으로 광학활성을 가진 화합물의 NMR 신호가 분리되는 현상
그림2. 다양한 광학활성 물질이 분리되는 그림
2015.11.10
조회수 17680
-
 고효율의 하이브리드 자동차 구동 시스템 개발
〈윤 용 산 교수〉
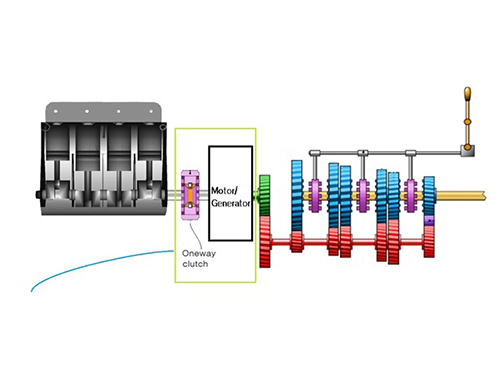
우리 대학 기계공학과 윤용산 교수 연구팀이 클러치 페달 없이 수동 변속이 가능한 독자적 구동시스템의 시작품(Prototype) 제작에 성공했다.
이 기술로 기존 하이브리드 자동차보다 높은 효율의 자동차 개발이 가능할 것으로 보인다. 연구팀의 하이브리드 자동차는 구조가 간단해 기존 자동차에 약간의 변형을 주는 것으로도 구현이 가능하며, 제작비용이 저렴하고 운전이 용이하다는 장점을 갖는다.
이 구동시스템은 ‘대화형 수동변속기를 갖는 하이브리드 차량 및 이의 제어 방법’으로 작년 5월 국제특허(PCT)로 등록됐고, 지난 5월 경기도 고양에서 열린 제 28회 국제 전기자동차 심포지엄 및 전시회에 발표됐다.
하이브리드 자동차는 내연기관 엔진과 변속기에 모터와 발전기를 결합시켜 공해와 연료 소모를 최소화하는 차량이다. 미국에서 발표하는 에너지 아웃룩(Energy Outlook)에 의하면 25년 후에도 하이브리드 자동차가 친환경 자동차 시장을 주도할 것으로 예상하고 있다.
그러나 일본의 자동차 기업이 하이브리드 자동차 관련 특허를 대량으로 선점해 기술 개발에 어려움을 겪고 있는 현실이다.
또한 한때 개발된 컴퓨터에 의한 반자동 수동변속기나 일본 회사의 수동변속기에 모터를 단순 부착한 제품은 비용이나 편의 측면에서 한계가 있었다.
문제 해결을 위해 연구팀은 비용이 제일 저렴한 수동변속기에 모터 발전기를 부착해 독창적인 방식의 비용절감 효과가 큰 하이브리드 자동차 시스템을 구현했다.
연구팀은 수동변속기의 클러치판을 없애고 그 기능을 모터발전기로 대신해 저속에서는 모터발전기로만 운행하게 만들었다.
이를 통해 기존 수동변속기 차량의 문제점인 엔진 꺼짐이나 번거로운 클러치 조작에서 벗어날 수 있다. 또한 변속 시간, 중량이 줄고 구동시스템의 내구성이 향상된다.
윤 교수는 “기존 방식과 달리 모터발전기가 클러치판을 대신해 엔진을 조절하기 때문에 기어 변경이 부드럽게 이뤄질 수 있다”며 “저속에서는 모터발전기에 의해서만 구동되므로 수동변속기의 문제점을 상당부분 해결할 수 있다”고 말했다.
기계공학과 손희운 석사과정 학생의 주도로 진행된 이번 연구는 한국연구재단의 이공분야 기초연구사업, 일반연구자 지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 클러치를 제거하고 일방향 클러치와 모터발전기를 첨가해 반자동의 실용적인 하이브리드 구동시스템을 구현한 모습
고효율의 하이브리드 자동차 구동 시스템 개발
〈윤 용 산 교수〉
우리 대학 기계공학과 윤용산 교수 연구팀이 클러치 페달 없이 수동 변속이 가능한 독자적 구동시스템의 시작품(Prototype) 제작에 성공했다.
이 기술로 기존 하이브리드 자동차보다 높은 효율의 자동차 개발이 가능할 것으로 보인다. 연구팀의 하이브리드 자동차는 구조가 간단해 기존 자동차에 약간의 변형을 주는 것으로도 구현이 가능하며, 제작비용이 저렴하고 운전이 용이하다는 장점을 갖는다.
이 구동시스템은 ‘대화형 수동변속기를 갖는 하이브리드 차량 및 이의 제어 방법’으로 작년 5월 국제특허(PCT)로 등록됐고, 지난 5월 경기도 고양에서 열린 제 28회 국제 전기자동차 심포지엄 및 전시회에 발표됐다.
하이브리드 자동차는 내연기관 엔진과 변속기에 모터와 발전기를 결합시켜 공해와 연료 소모를 최소화하는 차량이다. 미국에서 발표하는 에너지 아웃룩(Energy Outlook)에 의하면 25년 후에도 하이브리드 자동차가 친환경 자동차 시장을 주도할 것으로 예상하고 있다.
그러나 일본의 자동차 기업이 하이브리드 자동차 관련 특허를 대량으로 선점해 기술 개발에 어려움을 겪고 있는 현실이다.
또한 한때 개발된 컴퓨터에 의한 반자동 수동변속기나 일본 회사의 수동변속기에 모터를 단순 부착한 제품은 비용이나 편의 측면에서 한계가 있었다.
문제 해결을 위해 연구팀은 비용이 제일 저렴한 수동변속기에 모터 발전기를 부착해 독창적인 방식의 비용절감 효과가 큰 하이브리드 자동차 시스템을 구현했다.
연구팀은 수동변속기의 클러치판을 없애고 그 기능을 모터발전기로 대신해 저속에서는 모터발전기로만 운행하게 만들었다.
이를 통해 기존 수동변속기 차량의 문제점인 엔진 꺼짐이나 번거로운 클러치 조작에서 벗어날 수 있다. 또한 변속 시간, 중량이 줄고 구동시스템의 내구성이 향상된다.
윤 교수는 “기존 방식과 달리 모터발전기가 클러치판을 대신해 엔진을 조절하기 때문에 기어 변경이 부드럽게 이뤄질 수 있다”며 “저속에서는 모터발전기에 의해서만 구동되므로 수동변속기의 문제점을 상당부분 해결할 수 있다”고 말했다.
기계공학과 손희운 석사과정 학생의 주도로 진행된 이번 연구는 한국연구재단의 이공분야 기초연구사업, 일반연구자 지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 클러치를 제거하고 일방향 클러치와 모터발전기를 첨가해 반자동의 실용적인 하이브리드 구동시스템을 구현한 모습
2015.11.04
조회수 12113
-
 대장균의 생물막 형성 제어 기술 개발
〈이 영 훈 교수〉
우리 대학 화학과 이영훈 교수 연구팀이 작은 RNA(small RNA : sRNA)의 발현을 조절해 대장균의 생물막 형성을 제어할 수 있는 기술을 개발했다.
연구 결과는 네이처 자매지인 ‘사이언티픽 리포트(Scientific Reports)’ 10월 15일자에 게재됐다.
세균들은 외부의 여러 환경으로부터 스스로를 보호하기 위해 다량체로 이뤄진 세포성분을 분비한다. 이로 인해 고체 표면이나 살아있는 생물 조직에서 생물막(biofilm)이라는 3차원 구조물이 형성된다.
이 생물막은 제거가 어려울 뿐 아니라 세균의 생체 내 증식, 치석, 의료기기 오염, 수도관, 정수기 등에 분포해 각종 산업시설에서 광범위한 문제를 일으키고 있다.
특히 생물막을 형성하고 있는 세균들은 항생제에 매우 높은 내성을 가질 수 있어 슈퍼박테리아의 항생제 내성의 주요 원인이기도 하다.
생물막 형성에 크게 관여하는 세균 내의 sRNA는 표적 메신저 RNA(mRNA) 또는 단백질과 상호작용해 세포대사를 조절하는 핵심 요소로 기능한다. 학자들은 생물막 형성의 원리를 규명하기 위해 이 sRNA를 연구해 왔다.
현재 대장균에서는 100여 종의 sRNA가 보고됐다. 연구팀은 이 중 99종을 분석해 각각의 대장균 sRNA를 발현할 수 있는 라이브러리를 구축했다. 이후 이를 통해 환경적 스트레스 대응과 밀접한 관련성을 가져 생물막 형성에 핵심이 되는 sRNA를 탐색했다.
그 결과로 연구팀은 생물막 형성에 관여하는 sRNA를 새롭게 발견했고, 생물막 형성을 위한 생리적 변화(세포운동성, I형 핌브리아 형성, 컬리핌브리아 형성)를 일으키는 sRNA들을 분석하는 데 성공했다.
이 분석 방식은 기존의 유전체적 분석을 통한 sRNA 작용 원리 규명 연구에 비해 이 교수 연구팀은 특정 sRNA의 기능을 직접 분석할 수 있어 신속하고 효율적으로 작용 원리를 규명할 수 있다는 장점을 갖는다.
이번 연구를 통해 생물막 형성과정에 관여하는 신호 전달체계를 이해하는 후속 연구 뿐 아니라, sRNA를 진단 마커나 약물 타겟으로 삼아 세균의 병원성 제어에 활용할 수 있을 것으로 기대된다.
이 교수는 “세균의 생물막 형성과 분해를 원하는 방향으로 제어할 수 있게 됐다”며 “향후 99종의 sRNA 각각에 대한 돌연변이 균주도 확보해 함께 활용할 예정이다”고 말했다.
화학과 박근우, 이정민 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 글로벌프론티어사업(지능형 바이오시스템 설계 및 합성 연구), 기초연구실 지원사업, 중견연구자 지원사업(도약연구)을 통해 수행됐다.
□ 그림 설명
그림 1 . 세균 생물막 형성과정의 모식도
그림 2. sRNA의 발현양에 비례하여 생물막 형성의 억제. 생물막 형성이 많을수록 진한 보라색
그림 3. 99종의 대장균 sRNA와 라이브러리 구축에 사용된 pHMB1 플라스미드의 구조
대장균의 생물막 형성 제어 기술 개발
〈이 영 훈 교수〉
우리 대학 화학과 이영훈 교수 연구팀이 작은 RNA(small RNA : sRNA)의 발현을 조절해 대장균의 생물막 형성을 제어할 수 있는 기술을 개발했다.
연구 결과는 네이처 자매지인 ‘사이언티픽 리포트(Scientific Reports)’ 10월 15일자에 게재됐다.
세균들은 외부의 여러 환경으로부터 스스로를 보호하기 위해 다량체로 이뤄진 세포성분을 분비한다. 이로 인해 고체 표면이나 살아있는 생물 조직에서 생물막(biofilm)이라는 3차원 구조물이 형성된다.
이 생물막은 제거가 어려울 뿐 아니라 세균의 생체 내 증식, 치석, 의료기기 오염, 수도관, 정수기 등에 분포해 각종 산업시설에서 광범위한 문제를 일으키고 있다.
특히 생물막을 형성하고 있는 세균들은 항생제에 매우 높은 내성을 가질 수 있어 슈퍼박테리아의 항생제 내성의 주요 원인이기도 하다.
생물막 형성에 크게 관여하는 세균 내의 sRNA는 표적 메신저 RNA(mRNA) 또는 단백질과 상호작용해 세포대사를 조절하는 핵심 요소로 기능한다. 학자들은 생물막 형성의 원리를 규명하기 위해 이 sRNA를 연구해 왔다.
현재 대장균에서는 100여 종의 sRNA가 보고됐다. 연구팀은 이 중 99종을 분석해 각각의 대장균 sRNA를 발현할 수 있는 라이브러리를 구축했다. 이후 이를 통해 환경적 스트레스 대응과 밀접한 관련성을 가져 생물막 형성에 핵심이 되는 sRNA를 탐색했다.
그 결과로 연구팀은 생물막 형성에 관여하는 sRNA를 새롭게 발견했고, 생물막 형성을 위한 생리적 변화(세포운동성, I형 핌브리아 형성, 컬리핌브리아 형성)를 일으키는 sRNA들을 분석하는 데 성공했다.
이 분석 방식은 기존의 유전체적 분석을 통한 sRNA 작용 원리 규명 연구에 비해 이 교수 연구팀은 특정 sRNA의 기능을 직접 분석할 수 있어 신속하고 효율적으로 작용 원리를 규명할 수 있다는 장점을 갖는다.
이번 연구를 통해 생물막 형성과정에 관여하는 신호 전달체계를 이해하는 후속 연구 뿐 아니라, sRNA를 진단 마커나 약물 타겟으로 삼아 세균의 병원성 제어에 활용할 수 있을 것으로 기대된다.
이 교수는 “세균의 생물막 형성과 분해를 원하는 방향으로 제어할 수 있게 됐다”며 “향후 99종의 sRNA 각각에 대한 돌연변이 균주도 확보해 함께 활용할 예정이다”고 말했다.
화학과 박근우, 이정민 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 글로벌프론티어사업(지능형 바이오시스템 설계 및 합성 연구), 기초연구실 지원사업, 중견연구자 지원사업(도약연구)을 통해 수행됐다.
□ 그림 설명
그림 1 . 세균 생물막 형성과정의 모식도
그림 2. sRNA의 발현양에 비례하여 생물막 형성의 억제. 생물막 형성이 많을수록 진한 보라색
그림 3. 99종의 대장균 sRNA와 라이브러리 구축에 사용된 pHMB1 플라스미드의 구조
2015.10.28
조회수 16413
-
 복합 처방된 약물의 부작용 예측 기술 개발
〈이 도 헌 교수〉
우리 대학 바이오및뇌공학과 이도헌 교수(유전자동의보감사업단장, 제 1저자 박경현 연구원) 연구팀이 복합 처방된 약물들의 인체 내 간섭현상을 컴퓨터 가상인체로 분석해 부작용을 예측할 수 있는 기술을 개발했다.
이번 연구결과는 미국 공공과학도서관 학술지 플러스 원(PLOS ONE) 10월 15일자에 게재됐다.
의료 현장에서는 여러 약물을 함께 처방받아 복약하는 경우가 많다. 이러한 복합처방은 모든 가능성을 미리 시험할 수 없기 때문에 널리 알려진 대표적 위험사례를 제외하면 완벽한 사전시험이 불가능하다.
기존에는 부작용 사례를 의약품 적정사용평가(DUR)에 등재시켜 의료현장에서 활용하는 사후 추적만이 최선의 방법이었다. 따라서 복합처방으로 인한 의료 사고를 막기 어려웠고 부작용 예측에도 한계가 있었다.
문제 해결을 위해 연구팀은 발생 가능한 상황을 사전에 컴퓨터 가상인체로 예측함으로써 위험을 미리 파악할 수 있는 기술을 개발했다.
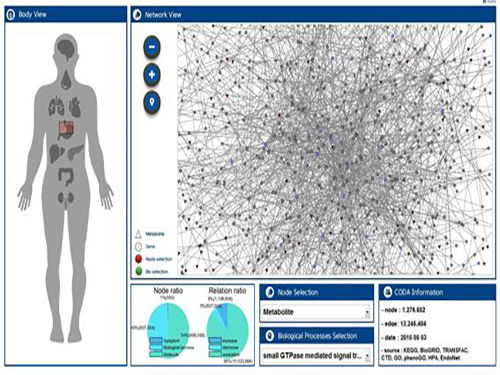
연구팀은 컴퓨터 가상인체에서 랜덤워크 알고리즘을 이용해 약물 표적의 생체 내 분자 신호전파를 시뮬레이션 했다. 약물이 투여됨으로써 신체에 영향을 끼치는 정도를 측정한 것인데, 이를 통해 두 개의 약물이 서로 어느 정도의 영향을 주는지 정량화에 성공했다.
따라서 만약 두 약물 간 간섭이 심해 서로 많은 영향을 준다면 부작용이 발생할 가능성이 높기 때문에 신중한 처방을 해야한다는 결론을 얻을 수 있다.
기존 예측 기술들이 단백질 상호작용 네트워크에서 약물 표적사이의 근거리 간섭만을 고려했다면 이 교수 연구팀은 약물 표적의 생체 내 분자 신호전파 시뮬레이션을 통해 원거리 간섭까지 고려해 정확도를 높였다.
연구팀은 이 기술이 다수의 표적을 갖는 복합 천연물의 신호 전파도 분석해 약물과 천연물 사이의 상호작용 예측에도 활용될 것이라고 예상했다.
이 교수는 “이번 기술은 자체 개발한 대규모 컴퓨터 가상인체 시스템을 통해 진행됐다”며 “약물 복합처방의 부작용을 예측할 수 있는 새로운 방법을 제시했다는 의의를 갖는다”고 말했다.
□ 그림 설명
그림 1. 연구팀이 개발한 컴퓨터 가상인체 시스템
그림 2 . 처방된 복합 약물 사이의 신호전파 간섭 예시
복합 처방된 약물의 부작용 예측 기술 개발
〈이 도 헌 교수〉
우리 대학 바이오및뇌공학과 이도헌 교수(유전자동의보감사업단장, 제 1저자 박경현 연구원) 연구팀이 복합 처방된 약물들의 인체 내 간섭현상을 컴퓨터 가상인체로 분석해 부작용을 예측할 수 있는 기술을 개발했다.
이번 연구결과는 미국 공공과학도서관 학술지 플러스 원(PLOS ONE) 10월 15일자에 게재됐다.
의료 현장에서는 여러 약물을 함께 처방받아 복약하는 경우가 많다. 이러한 복합처방은 모든 가능성을 미리 시험할 수 없기 때문에 널리 알려진 대표적 위험사례를 제외하면 완벽한 사전시험이 불가능하다.
기존에는 부작용 사례를 의약품 적정사용평가(DUR)에 등재시켜 의료현장에서 활용하는 사후 추적만이 최선의 방법이었다. 따라서 복합처방으로 인한 의료 사고를 막기 어려웠고 부작용 예측에도 한계가 있었다.
문제 해결을 위해 연구팀은 발생 가능한 상황을 사전에 컴퓨터 가상인체로 예측함으로써 위험을 미리 파악할 수 있는 기술을 개발했다.
연구팀은 컴퓨터 가상인체에서 랜덤워크 알고리즘을 이용해 약물 표적의 생체 내 분자 신호전파를 시뮬레이션 했다. 약물이 투여됨으로써 신체에 영향을 끼치는 정도를 측정한 것인데, 이를 통해 두 개의 약물이 서로 어느 정도의 영향을 주는지 정량화에 성공했다.
따라서 만약 두 약물 간 간섭이 심해 서로 많은 영향을 준다면 부작용이 발생할 가능성이 높기 때문에 신중한 처방을 해야한다는 결론을 얻을 수 있다.
기존 예측 기술들이 단백질 상호작용 네트워크에서 약물 표적사이의 근거리 간섭만을 고려했다면 이 교수 연구팀은 약물 표적의 생체 내 분자 신호전파 시뮬레이션을 통해 원거리 간섭까지 고려해 정확도를 높였다.
연구팀은 이 기술이 다수의 표적을 갖는 복합 천연물의 신호 전파도 분석해 약물과 천연물 사이의 상호작용 예측에도 활용될 것이라고 예상했다.
이 교수는 “이번 기술은 자체 개발한 대규모 컴퓨터 가상인체 시스템을 통해 진행됐다”며 “약물 복합처방의 부작용을 예측할 수 있는 새로운 방법을 제시했다는 의의를 갖는다”고 말했다.
□ 그림 설명
그림 1. 연구팀이 개발한 컴퓨터 가상인체 시스템
그림 2 . 처방된 복합 약물 사이의 신호전파 간섭 예시
2015.10.22
조회수 12166
-
 소장 내 지방 흡수과정의 비밀 밝혀
김 필 한 교수
우리 대학 나노과학기술대학원 김필한 교수와 의과학대학원 고규영 교수 공동 연구팀이 소장에서 지방이 흡수되는 과정의 고해상도 촬영에 성공했다.
이번 연구는 나노과학기술대학원 최기백 박사과정 학생, 의과학대학원 장전엽 박사, 박인태 박사과정 학생이 1저자로 참여했다.
이를 통해 소장의 융모로 흡수된 지방의 전달 통로인 암죽관의 수축현상을 최초로 발견했다.
이번 연구결과는 의생명과학 분야 국제 학술지인 ‘임상연구(The Journal of Clinical Investigation, Impact Factor 13.261)’ 10월 5일자 온라인판에 게재됐다. 또한 11월에는 이달의 주목할 만한 연구로 ‘JCI This month’에도 소개될 예정이다. (논문명 : Intravital imaging of intestinal lacteals unveils lipid drainage through contractility)
소장은 영양분을 흡수하는 기관이다. 소장의 관찰을 위해 많은 학자들이 노력했지만 소장은 항상 쉬지 않고 움직이기 때문에 고해상도 촬영에 한계가 있었다.
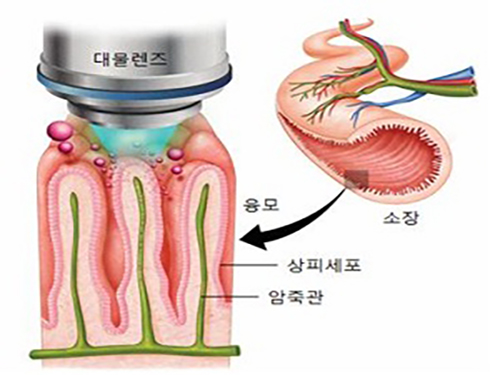
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 소장 의 상태를 보존하고 내벽을 고정할 수 있는 영상 챔버를 이용해 동물 모델의 소장 내벽에서 지방산이 흡수되는 과정을 촬영했다.
이 과정에서 지방의 흡수 통로인 암죽관이 일정 주기로 수축 및 이완하는 현상을 발견했다. 또한 암죽관의 수축 정도가 소장에서의 지방산 흡수 속도에 영향을 미치는 것을 발견했다.
연구팀은 이 암죽관의 움직임이 융모 내부에 다량 존재하는 민무늬근세포에 의해 발생하고, 이는 체내에 분포된 자율신경계를 통해 조절됨을 밝혔다.
이번 연구를 통해 개발된 최첨단 고해상도 생체영상기술로 소장 내 다양한 물질 흡수 과정의 실시간 모니터링이 가능해질 것으로 예상된다.
또한 이 기술은 신약개발 과정에서 지용성 약물이 소장 내 암죽관으로 흡수되게 해 간 독성을 최소화하는 새로운 약물전달 방법 확립에 기여할 것으로 기대된다.
김 교수는 “우리가 섭취하는 다량의 지용성 영양소가 체내로 흡수되는 과정에서 자율신경계로 조절되는 융모 내부의 암죽관 제어 메커니즘이 존재함을 새롭게 밝혀냈다”고 말했다.
이번 연구는 미래창조과학부의 글로벌프론티어사업 및 신기술융합형 성장동력사업의 지원을 받아 수행됐다.
그림 설명
그림1. 소장 내벽에 존재하는 융모에서 지방산이 흡수되는 과정을 광학현미경으로 영상화하는 과정 모식도
그림2. 소장 융모에서 지방산(적색)이 암죽관(녹색)을 통해 흡수되는 과정
그림3. 암죽관(녹색)의 반복적인 이완과 수축 운동. 0초, 2.7초에 이완. 1.6초, 4초에 암죽관의 수축
소장 내 지방 흡수과정의 비밀 밝혀
김 필 한 교수
우리 대학 나노과학기술대학원 김필한 교수와 의과학대학원 고규영 교수 공동 연구팀이 소장에서 지방이 흡수되는 과정의 고해상도 촬영에 성공했다.
이번 연구는 나노과학기술대학원 최기백 박사과정 학생, 의과학대학원 장전엽 박사, 박인태 박사과정 학생이 1저자로 참여했다.
이를 통해 소장의 융모로 흡수된 지방의 전달 통로인 암죽관의 수축현상을 최초로 발견했다.
이번 연구결과는 의생명과학 분야 국제 학술지인 ‘임상연구(The Journal of Clinical Investigation, Impact Factor 13.261)’ 10월 5일자 온라인판에 게재됐다. 또한 11월에는 이달의 주목할 만한 연구로 ‘JCI This month’에도 소개될 예정이다. (논문명 : Intravital imaging of intestinal lacteals unveils lipid drainage through contractility)
소장은 영양분을 흡수하는 기관이다. 소장의 관찰을 위해 많은 학자들이 노력했지만 소장은 항상 쉬지 않고 움직이기 때문에 고해상도 촬영에 한계가 있었다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 소장 의 상태를 보존하고 내벽을 고정할 수 있는 영상 챔버를 이용해 동물 모델의 소장 내벽에서 지방산이 흡수되는 과정을 촬영했다.
이 과정에서 지방의 흡수 통로인 암죽관이 일정 주기로 수축 및 이완하는 현상을 발견했다. 또한 암죽관의 수축 정도가 소장에서의 지방산 흡수 속도에 영향을 미치는 것을 발견했다.
연구팀은 이 암죽관의 움직임이 융모 내부에 다량 존재하는 민무늬근세포에 의해 발생하고, 이는 체내에 분포된 자율신경계를 통해 조절됨을 밝혔다.
이번 연구를 통해 개발된 최첨단 고해상도 생체영상기술로 소장 내 다양한 물질 흡수 과정의 실시간 모니터링이 가능해질 것으로 예상된다.
또한 이 기술은 신약개발 과정에서 지용성 약물이 소장 내 암죽관으로 흡수되게 해 간 독성을 최소화하는 새로운 약물전달 방법 확립에 기여할 것으로 기대된다.
김 교수는 “우리가 섭취하는 다량의 지용성 영양소가 체내로 흡수되는 과정에서 자율신경계로 조절되는 융모 내부의 암죽관 제어 메커니즘이 존재함을 새롭게 밝혀냈다”고 말했다.
이번 연구는 미래창조과학부의 글로벌프론티어사업 및 신기술융합형 성장동력사업의 지원을 받아 수행됐다.
그림 설명
그림1. 소장 내벽에 존재하는 융모에서 지방산이 흡수되는 과정을 광학현미경으로 영상화하는 과정 모식도
그림2. 소장 융모에서 지방산(적색)이 암죽관(녹색)을 통해 흡수되는 과정
그림3. 암죽관(녹색)의 반복적인 이완과 수축 운동. 0초, 2.7초에 이완. 1.6초, 4초에 암죽관의 수축
2015.10.14
조회수 20687
-
 산란된 빛을 다시 집약시키는 시간 역행 거울 개발
우리 대학 물리학과 박용근 교수 연구팀이 빛을 거꾸로 반사시켜 시간이 역행하는 것처럼 보이는 시간 역행 거울을 개발했다.
연구 성과는 물리학분야 학술지인 ‘피지컬 리뷰 레터스(Physical Review Letters)’ 10월 6일자 온라인 판에 게재됐다.
빛의 시간 역행성은 녹화된 비디오를 되감기하듯 빛의 진행을 되돌릴 수 있는 개념을 뜻한다. 이는 마치 쏟은 물을 주워 담는 것과 같이 흩뿌려진 빛을 다시 집약시켜 산란 전의 영상을 복구하는 것과 같은 원리이다.
빛의 시간 역행 실현을 위해선 특별한 거울이 필요했다. 이론상으로만 제안되었던 이 시간 역행 거울(위상 공액 거울)은 빛이 거울에 부딪혔을 때 부딪쳐 온 방향으로 빛이 반사돼 원래 상태로 돌아가는 특성을 갖는다.
많은 학자들이 비선형 레이저 광학 지식을 이용해 시간 역행 거울을 구현하려 노력했다. 하지만 이 특수한 현상의 실현을 위해선 일반적인 거울과 다르게 추가적인 입사 레이저광이 필요하고 주변 환경에 극도로 민감하다는 한계가 있었다.
연구팀은 문제 해결을 위해 기존 복잡한 시도와 반대로 일반 거울에서의 반사를 재해석해 활용했다.
연구팀은 파면제어기라 불리는 수많은 미세 거울로 이루어진 장치를 활용했다. 파면제어기는 입사하는 빛의 모양에 맞춰 거울의 표면을 변경시켜 평행 상태로 만드는 원리인데, 이를 통해 복잡한 물리현상의 도입 없이도 빛의 시간 역행 거울을 구현하는데 성공했다.
또한 연구팀은 구현된 시간 역행 거울을 활용해 모의 생체조직 샘플, 생 닭가슴살 등에 의해 심하게 산란된 빛을 집약시켜 산란 전의 모양으로 재현했다.
연구팀에 의해 구현된 시간 역행 거울은 그 구현방법이 쉽고 주변환경의 영향을 받지 않아 빠른 시일 내에 실제 응용에 접목할 수 있을 것으로 예상된다.
논문의 1저자인 이겨레 박사과정은 “이 기술을 활용하면 기존 생체조직에서 심한 산란으로 인해 불가능했던 생체조직 내부의 빛 집약이 가능하다” 며 “향후 무절개 암 수술 등 미래기술의 기반기술이 될 수 있다”고 말했다.
또한 박 교수는 “이번 기술은 빛 뿐 아니라 소리, 전자파, 라디오 등 일반적인 파동에서 성립하는 개념이다”며 “향후 레이저 및 광통신 기술을 포함한 물리학, 광학, 의학 등 다양한 분야에 응용될 것으로 기대된다”고 말했다.
□ 그림 설명
그림 1. 생체조직,닭가슴살,광섬유를 산란체로 활용한 뒤 시간역행 거울로 원래 이미지를 구현한 사진
그림 2. 일반거울과 시간역행거울의 원리
산란된 빛을 다시 집약시키는 시간 역행 거울 개발
우리 대학 물리학과 박용근 교수 연구팀이 빛을 거꾸로 반사시켜 시간이 역행하는 것처럼 보이는 시간 역행 거울을 개발했다.
연구 성과는 물리학분야 학술지인 ‘피지컬 리뷰 레터스(Physical Review Letters)’ 10월 6일자 온라인 판에 게재됐다.
빛의 시간 역행성은 녹화된 비디오를 되감기하듯 빛의 진행을 되돌릴 수 있는 개념을 뜻한다. 이는 마치 쏟은 물을 주워 담는 것과 같이 흩뿌려진 빛을 다시 집약시켜 산란 전의 영상을 복구하는 것과 같은 원리이다.
빛의 시간 역행 실현을 위해선 특별한 거울이 필요했다. 이론상으로만 제안되었던 이 시간 역행 거울(위상 공액 거울)은 빛이 거울에 부딪혔을 때 부딪쳐 온 방향으로 빛이 반사돼 원래 상태로 돌아가는 특성을 갖는다.
많은 학자들이 비선형 레이저 광학 지식을 이용해 시간 역행 거울을 구현하려 노력했다. 하지만 이 특수한 현상의 실현을 위해선 일반적인 거울과 다르게 추가적인 입사 레이저광이 필요하고 주변 환경에 극도로 민감하다는 한계가 있었다.
연구팀은 문제 해결을 위해 기존 복잡한 시도와 반대로 일반 거울에서의 반사를 재해석해 활용했다.
연구팀은 파면제어기라 불리는 수많은 미세 거울로 이루어진 장치를 활용했다. 파면제어기는 입사하는 빛의 모양에 맞춰 거울의 표면을 변경시켜 평행 상태로 만드는 원리인데, 이를 통해 복잡한 물리현상의 도입 없이도 빛의 시간 역행 거울을 구현하는데 성공했다.
또한 연구팀은 구현된 시간 역행 거울을 활용해 모의 생체조직 샘플, 생 닭가슴살 등에 의해 심하게 산란된 빛을 집약시켜 산란 전의 모양으로 재현했다.
연구팀에 의해 구현된 시간 역행 거울은 그 구현방법이 쉽고 주변환경의 영향을 받지 않아 빠른 시일 내에 실제 응용에 접목할 수 있을 것으로 예상된다.
논문의 1저자인 이겨레 박사과정은 “이 기술을 활용하면 기존 생체조직에서 심한 산란으로 인해 불가능했던 생체조직 내부의 빛 집약이 가능하다” 며 “향후 무절개 암 수술 등 미래기술의 기반기술이 될 수 있다”고 말했다.
또한 박 교수는 “이번 기술은 빛 뿐 아니라 소리, 전자파, 라디오 등 일반적인 파동에서 성립하는 개념이다”며 “향후 레이저 및 광통신 기술을 포함한 물리학, 광학, 의학 등 다양한 분야에 응용될 것으로 기대된다”고 말했다.
□ 그림 설명
그림 1. 생체조직,닭가슴살,광섬유를 산란체로 활용한 뒤 시간역행 거울로 원래 이미지를 구현한 사진
그림 2. 일반거울과 시간역행거울의 원리
2015.10.07
조회수 13656
-
 빛을 이용한 실리카 구조체 가공 기술 개발
우리 대학 생명화학공학과 김희탁 교수, 박정기 교수 공동 연구팀이 단순한 빛 조사만으로 실리카(유리)와 같은 단단한 세라믹 구조체의 모양을 정교하게 제어할 수 있는 기술을 개발했다.
이번 연구 성과는 재료과학분야의 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 9월 21일자 온라인판에 게재됐다.
실리카 구조체는 유기물 구조체에 비해 고온, 고압 및 바이오 물질과의 안정성이 좋고 내화학성, 투명성 등이 높아 미세 유체칩 내부 채널, 태양전지 기판 등에 폭넓게 이용되고 있다.
그러나 실리카 특유의 높은 경도 때문에 실리카 구조체의 모양과 크기를 변화시키기 어려웠다. 특히 나노 스케일 구조 가공은 매우 어려운 것으로 여겨졌다.
연구팀은 문제 해결을 위해 아조 분자(질소 원자 두 개가 이중 결합된 아조기 양 끝에 벤젠링이 결합된 형태의 분자)를 이용했다. 아조 분자는 빛을 받았을 때 빛의 방향과 나란히 배열돼 편광 방향과 동일한 방향으로 움직이는 특성을 갖는다. 이를 응용하면 아조 분자와 결합된 실리카 전구체 분자가 빛의 방향에 따라 움직이는 특성을 갖게 된다.
연구팀은 이 아조 분자와 결합된 실리카 전구체를 용액-마이크로 임프린팅 기법의 잉크로 사용해 도장처럼 찍혀 나오듯 정해진 패턴의 형태로 제작했다.
이후 제작된 물질을 빛으로 가공한 뒤 열처리 하면 아조 분자가 포함된 유기물이 열분해돼 사라지게 된다. 결과적으로 무기물 전구체들만 남아 반응해 유리 구조체가 완성되는 것이다.
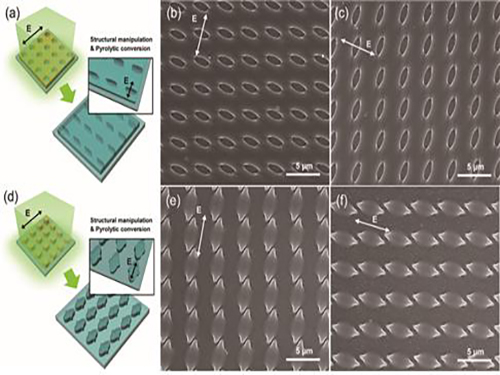
이 방법을 통해 30나노미터 이하 크기의 나노 구조를 갖는 대 면적 실리카 구조체를 제작했다. 또한 원형의 홀에 빛을 조사해 타원형의 홀 및 기둥 구조를 구현했다.
연구팀은 개발된 기술이 초소수성 기판, 미세유체칩 내의 미세채널 등 물리적 및 화학적 내구성이 요구되는 소자에 광범위하게 응용될 수 있을 것이라고 밝혔다.
김 교수는 “기존에 없었던 새로운 방식의 실리카 구조체 가공 방법을 개발했다”며 “세라믹을 나노 영역에서 다양한 형태로 구조 가공이 가능한 최초의 방식이다”고 말했다.
강홍석 박사 후 연구원이 1저자로 참여한 이번 연구는 한국연구재단의 일반연구자사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 빛 조사 및 열처리를 통해 원형형태의 구조체로부터 타원형태의 실리카 구조체 제작
그림 2. 광학 사진 이미지. 전자현미경 사진을 통해 실리카 전구제 구조 변형 및 실리카 구조체 제작 확인
그림 3. 빛을 이용해 실리카 전구체 구조 가공 및 열처리를 통한 실리카 구조체 제작과정
빛을 이용한 실리카 구조체 가공 기술 개발
우리 대학 생명화학공학과 김희탁 교수, 박정기 교수 공동 연구팀이 단순한 빛 조사만으로 실리카(유리)와 같은 단단한 세라믹 구조체의 모양을 정교하게 제어할 수 있는 기술을 개발했다.
이번 연구 성과는 재료과학분야의 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 9월 21일자 온라인판에 게재됐다.
실리카 구조체는 유기물 구조체에 비해 고온, 고압 및 바이오 물질과의 안정성이 좋고 내화학성, 투명성 등이 높아 미세 유체칩 내부 채널, 태양전지 기판 등에 폭넓게 이용되고 있다.
그러나 실리카 특유의 높은 경도 때문에 실리카 구조체의 모양과 크기를 변화시키기 어려웠다. 특히 나노 스케일 구조 가공은 매우 어려운 것으로 여겨졌다.
연구팀은 문제 해결을 위해 아조 분자(질소 원자 두 개가 이중 결합된 아조기 양 끝에 벤젠링이 결합된 형태의 분자)를 이용했다. 아조 분자는 빛을 받았을 때 빛의 방향과 나란히 배열돼 편광 방향과 동일한 방향으로 움직이는 특성을 갖는다. 이를 응용하면 아조 분자와 결합된 실리카 전구체 분자가 빛의 방향에 따라 움직이는 특성을 갖게 된다.
연구팀은 이 아조 분자와 결합된 실리카 전구체를 용액-마이크로 임프린팅 기법의 잉크로 사용해 도장처럼 찍혀 나오듯 정해진 패턴의 형태로 제작했다.
이후 제작된 물질을 빛으로 가공한 뒤 열처리 하면 아조 분자가 포함된 유기물이 열분해돼 사라지게 된다. 결과적으로 무기물 전구체들만 남아 반응해 유리 구조체가 완성되는 것이다.
이 방법을 통해 30나노미터 이하 크기의 나노 구조를 갖는 대 면적 실리카 구조체를 제작했다. 또한 원형의 홀에 빛을 조사해 타원형의 홀 및 기둥 구조를 구현했다.
연구팀은 개발된 기술이 초소수성 기판, 미세유체칩 내의 미세채널 등 물리적 및 화학적 내구성이 요구되는 소자에 광범위하게 응용될 수 있을 것이라고 밝혔다.
김 교수는 “기존에 없었던 새로운 방식의 실리카 구조체 가공 방법을 개발했다”며 “세라믹을 나노 영역에서 다양한 형태로 구조 가공이 가능한 최초의 방식이다”고 말했다.
강홍석 박사 후 연구원이 1저자로 참여한 이번 연구는 한국연구재단의 일반연구자사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 빛 조사 및 열처리를 통해 원형형태의 구조체로부터 타원형태의 실리카 구조체 제작
그림 2. 광학 사진 이미지. 전자현미경 사진을 통해 실리카 전구제 구조 변형 및 실리카 구조체 제작 확인
그림 3. 빛을 이용해 실리카 전구체 구조 가공 및 열처리를 통한 실리카 구조체 제작과정
2015.10.06
조회수 13859
-
 수학 통해 생체시계 유지 원리 60여년 만에 밝혀
김 재 경 교수
우리 대학 수리과학과 김재경 교수가 미분방정식을 이용한 수학적 모델링을 통해 온도 변화에도 생체시계의 속도를 유지하는 원리를 발견했다.
이번 연구는 저명 학술지 셀(Cell) 자매지 몰라큘러 셀(Molecular Cell) 10월 1일자에 게재됐다.
우리 뇌에 위치한 생체시계는 밤 9시 경이 되면 멜라토닌 분비가 시작되게 하고 아침 7시 경에 멈추게 한다. 그로 인해 우리는 매일 일정한 시간에 잠을 자고 기상할 수 있다.
생체시계는 온도가 변화해도 빨라지거나 느려지지 않고 일정한 속도가 유지된다. 따라서 우리의 체온이 변화해도 규칙적인 삶을 살 수 있고, 이는 환경에 따라 체온이 변하는 변온 동물에게도 적용된다.
이러한 생체시계의 성질은 1954년에 발견됐지만 그 원리는 밝혀지지 않아 지난 60여 년간 생체시계 분야의 가장 큰 미스테리로 남아 있었다.
김 교수는 수학 모델링을 통해 이 원리를 밝혀냈고 모델링 결과는 듀크-싱가폴 국립 의과대학 데이빗 벌쉽(David Virshup) 교수 연구팀의 실험을 통해 검증돼 60년의 난제가 풀렸다.
생체시계에는 Period2라는 핵심 단백질이 존재한다. 이 단백질은 12시간 동안 증가하고 나머지 12시간 동안 분해되는 리듬을 평생 반복한다.
김 교수는 이 Period2 분해가 두 가지 방법으로 발생하는 것을 밝혔다. 하나는 매우 빠른 속도로 분해가 일어나는 것이고 나머지 하나는 매우 느린 속도로 분해가 이뤄지는 것이다. 그리고 두 가지 방법의 비율을 조절하는 것이 Period2에 존재하는 인산화 스위치(Phosphoryltion switch)이다.
인산화 스위치의 역할은 온도가 올라갔을 때 느리게 분해되는 Period2의 양을 늘림으로써 전체적인 분해 속도가 천천히 이뤄지게 만든다. 반대로 온도가 내려갔을 때는 빠르게 분해되는 비율을 늘려 생체시계의 속도를 조절하는 것이다.
결국 생체시계 속도 유지의 핵심은 인산화 스위치이고, 다른 생화학 반응이 빨라져도 생체시계의 속도 유지를 가능하게 만드는 요소인 것이다.
이번 연구에서 밝혀진 인산화 스위치는 생체시계의 속도를 조절할 수 있는 핵심 요소가 될 전망이다. 이 인산화 스위치를 조절할 수 있는 약을 개발한다면 잦은 해외 출장으로 인한 시차, 주야 교대 근무 등에 의한 생체 시계 고장 예방 등에 기여할 수 있을 것으로 기대된다.
김 교수는 “이번 성과를 통해 우리나라에선 아직은 부족한 생물학과 수학의 교류가 활발해지길 기대한다”며 “수학이 생물학의 난제들을 해결하는데 기여할 수 있음을 알리고 싶다”고 말했다.
이번 연구는 듀크-국립 싱가폴 의과 대학 데이빗 벌쉽 (David Virshup) 교수 연구팀, 미국 미시간 대학 (University of Michigan, Ann Arbor) 데니 폴저 (Daniel Forger) 교수와의 공동연구로 진행됐다.
□ 그림 설명
그림 1 . 이번 연구에서 밝혀진 인산화 스위치와 그 과정에서 사용된 수학 방정식의 일부
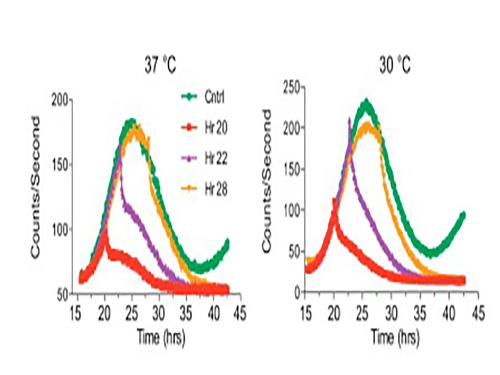
그림 2. Period2 단백질이 인산화 스위치에 의해 낮은 온도(30도) 에서 분해되는 속도가 더 빨라진다는 것을 보여주는 실험
수학 통해 생체시계 유지 원리 60여년 만에 밝혀
김 재 경 교수
우리 대학 수리과학과 김재경 교수가 미분방정식을 이용한 수학적 모델링을 통해 온도 변화에도 생체시계의 속도를 유지하는 원리를 발견했다.
이번 연구는 저명 학술지 셀(Cell) 자매지 몰라큘러 셀(Molecular Cell) 10월 1일자에 게재됐다.
우리 뇌에 위치한 생체시계는 밤 9시 경이 되면 멜라토닌 분비가 시작되게 하고 아침 7시 경에 멈추게 한다. 그로 인해 우리는 매일 일정한 시간에 잠을 자고 기상할 수 있다.
생체시계는 온도가 변화해도 빨라지거나 느려지지 않고 일정한 속도가 유지된다. 따라서 우리의 체온이 변화해도 규칙적인 삶을 살 수 있고, 이는 환경에 따라 체온이 변하는 변온 동물에게도 적용된다.
이러한 생체시계의 성질은 1954년에 발견됐지만 그 원리는 밝혀지지 않아 지난 60여 년간 생체시계 분야의 가장 큰 미스테리로 남아 있었다.
김 교수는 수학 모델링을 통해 이 원리를 밝혀냈고 모델링 결과는 듀크-싱가폴 국립 의과대학 데이빗 벌쉽(David Virshup) 교수 연구팀의 실험을 통해 검증돼 60년의 난제가 풀렸다.
생체시계에는 Period2라는 핵심 단백질이 존재한다. 이 단백질은 12시간 동안 증가하고 나머지 12시간 동안 분해되는 리듬을 평생 반복한다.
김 교수는 이 Period2 분해가 두 가지 방법으로 발생하는 것을 밝혔다. 하나는 매우 빠른 속도로 분해가 일어나는 것이고 나머지 하나는 매우 느린 속도로 분해가 이뤄지는 것이다. 그리고 두 가지 방법의 비율을 조절하는 것이 Period2에 존재하는 인산화 스위치(Phosphoryltion switch)이다.
인산화 스위치의 역할은 온도가 올라갔을 때 느리게 분해되는 Period2의 양을 늘림으로써 전체적인 분해 속도가 천천히 이뤄지게 만든다. 반대로 온도가 내려갔을 때는 빠르게 분해되는 비율을 늘려 생체시계의 속도를 조절하는 것이다.
결국 생체시계 속도 유지의 핵심은 인산화 스위치이고, 다른 생화학 반응이 빨라져도 생체시계의 속도 유지를 가능하게 만드는 요소인 것이다.
이번 연구에서 밝혀진 인산화 스위치는 생체시계의 속도를 조절할 수 있는 핵심 요소가 될 전망이다. 이 인산화 스위치를 조절할 수 있는 약을 개발한다면 잦은 해외 출장으로 인한 시차, 주야 교대 근무 등에 의한 생체 시계 고장 예방 등에 기여할 수 있을 것으로 기대된다.
김 교수는 “이번 성과를 통해 우리나라에선 아직은 부족한 생물학과 수학의 교류가 활발해지길 기대한다”며 “수학이 생물학의 난제들을 해결하는데 기여할 수 있음을 알리고 싶다”고 말했다.
이번 연구는 듀크-국립 싱가폴 의과 대학 데이빗 벌쉽 (David Virshup) 교수 연구팀, 미국 미시간 대학 (University of Michigan, Ann Arbor) 데니 폴저 (Daniel Forger) 교수와의 공동연구로 진행됐다.
□ 그림 설명
그림 1 . 이번 연구에서 밝혀진 인산화 스위치와 그 과정에서 사용된 수학 방정식의 일부
그림 2. Period2 단백질이 인산화 스위치에 의해 낮은 온도(30도) 에서 분해되는 속도가 더 빨라진다는 것을 보여주는 실험
2015.10.05
조회수 18953
-
 바이오부탄올 핵심생산효소 구조 및 특성 규명
이 상 엽 특훈교수
우리 대학 생명화학공학과 이상엽 교수 연구팀이 경북대학교 김경진 교수 연구팀과의 공동연구를 통해 친환경 차세대 에너지인 바이오부탄올의 핵심 생산 효소인 싸이올레이즈(Thiolase)의 구조 및 특성을 규명했다.
연구 결과는 네이처 커뮤니케이션즈(Nature Communications) 9월 22일자 온라인 판에 게재됐다.
바이오부탄올은 바이오연료로 이미 사용되고 있는 바이오에탄올을 능가할 수 있는 친환경 차세대 수송용 바이오연료로 각광받고 있다.
바이오부탄올의 에너지 밀도는 리터당 29.2MJ(메가줄)로 바이오에탄올(19.6MJ)보다 48% 이상 높고 휘발유(32MJ)와 큰 차이가 없다. 또한 폐목재, 볏짚, 잉여 사탕수수, 해조류 등 비식용 바이오매스에서 추출하기 때문에 식량파동 등에서도 자유롭다.
바이오부탄올의 가장 큰 장점은 휘발유와 비교했을 때 공기연료비, 기화열, 옥탄가 등 연료 성능이 비슷해 현재 자동차 등에 사용되고 있는 가솔린 엔진을 그대로 사용할 수 있다는 점이다.
바이오부탄올은 클로스트리듐이라는 미생물로부터 생산이 가능하지만 클로스트리듐의 주요 효소의 구조 및 기작 등에 대한 연구는 체계적으로 이뤄지지 못했다.
이 교수 연구팀은 이 미생물의 성능 향상을 위해 바이오부탄올 생합성에 필요한 주요 효소 중 하나인 싸이올레이즈의 3차원 입체구조를 포항방사광가속기를 이용해 규명했다.
이를 통해 일반적인 미생물의 효소에서는 발견되지 않고 클로스트리듐 내의 싸이올레이즈에서만 관찰되는 산화-환원 스위치 구조를 발견했다.
또한 가상세포모델 등을 활용한 시스템대사공학 기법을 활용해 이 싸이올레이즈가 실제 미생물 내에서 산화-환원의 스위치로 작동한다는 것을 증명했다.
연구팀은 밝혀낸 싸이올레이즈 구조의 원천기술을 활용해 활성이 향상된 돌연변이 효소를 설계했다. 그리고 이를 이용해 바이오부탄올 생산 미생물의 대사회로를 조작해 바이오부탄올 생합성이 향상되는 결과를 얻었다.
이상엽 교수는 “바이오부탄올 생합성 대사회로에서 가장 중요한 효소의 구조와 작용 기작을 세계 최초로 밝혔다”며 “싸이올레이즈 관련 원천기술을 활용해 바이오부탄올을 더욱 경제적으로 생산할 수 있는 대사회로 구축에 응용하겠다”고 말했다.
김상우, 장유신, 하성철 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단의 기후변화대응기술개발사업 및 글로벌프런티어 차세대바이오매스사업단 지원을 받아 수행됐다.
□ 그림 설명
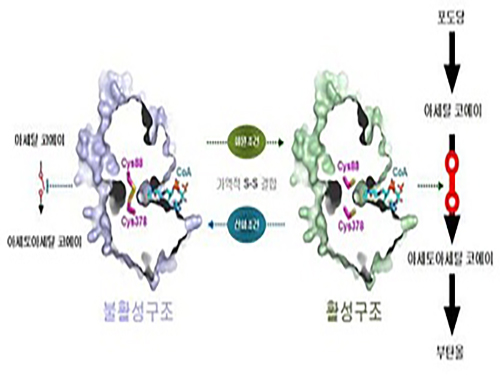
그림 1. 바이오부탄올 생산 효소(thiolase)의 구조 및 산화-환원 스위치 작용기작
그림 2. 바이오부탄올 생산을 위한 포도당 대사회로에서 바이오부탄올 생산 효소(thiolase)의 산화-환원 스위치 작용기작
바이오부탄올 핵심생산효소 구조 및 특성 규명
이 상 엽 특훈교수
우리 대학 생명화학공학과 이상엽 교수 연구팀이 경북대학교 김경진 교수 연구팀과의 공동연구를 통해 친환경 차세대 에너지인 바이오부탄올의 핵심 생산 효소인 싸이올레이즈(Thiolase)의 구조 및 특성을 규명했다.
연구 결과는 네이처 커뮤니케이션즈(Nature Communications) 9월 22일자 온라인 판에 게재됐다.
바이오부탄올은 바이오연료로 이미 사용되고 있는 바이오에탄올을 능가할 수 있는 친환경 차세대 수송용 바이오연료로 각광받고 있다.
바이오부탄올의 에너지 밀도는 리터당 29.2MJ(메가줄)로 바이오에탄올(19.6MJ)보다 48% 이상 높고 휘발유(32MJ)와 큰 차이가 없다. 또한 폐목재, 볏짚, 잉여 사탕수수, 해조류 등 비식용 바이오매스에서 추출하기 때문에 식량파동 등에서도 자유롭다.
바이오부탄올의 가장 큰 장점은 휘발유와 비교했을 때 공기연료비, 기화열, 옥탄가 등 연료 성능이 비슷해 현재 자동차 등에 사용되고 있는 가솔린 엔진을 그대로 사용할 수 있다는 점이다.
바이오부탄올은 클로스트리듐이라는 미생물로부터 생산이 가능하지만 클로스트리듐의 주요 효소의 구조 및 기작 등에 대한 연구는 체계적으로 이뤄지지 못했다.
이 교수 연구팀은 이 미생물의 성능 향상을 위해 바이오부탄올 생합성에 필요한 주요 효소 중 하나인 싸이올레이즈의 3차원 입체구조를 포항방사광가속기를 이용해 규명했다.
이를 통해 일반적인 미생물의 효소에서는 발견되지 않고 클로스트리듐 내의 싸이올레이즈에서만 관찰되는 산화-환원 스위치 구조를 발견했다.
또한 가상세포모델 등을 활용한 시스템대사공학 기법을 활용해 이 싸이올레이즈가 실제 미생물 내에서 산화-환원의 스위치로 작동한다는 것을 증명했다.
연구팀은 밝혀낸 싸이올레이즈 구조의 원천기술을 활용해 활성이 향상된 돌연변이 효소를 설계했다. 그리고 이를 이용해 바이오부탄올 생산 미생물의 대사회로를 조작해 바이오부탄올 생합성이 향상되는 결과를 얻었다.
이상엽 교수는 “바이오부탄올 생합성 대사회로에서 가장 중요한 효소의 구조와 작용 기작을 세계 최초로 밝혔다”며 “싸이올레이즈 관련 원천기술을 활용해 바이오부탄올을 더욱 경제적으로 생산할 수 있는 대사회로 구축에 응용하겠다”고 말했다.
김상우, 장유신, 하성철 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단의 기후변화대응기술개발사업 및 글로벌프런티어 차세대바이오매스사업단 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 바이오부탄올 생산 효소(thiolase)의 구조 및 산화-환원 스위치 작용기작
그림 2. 바이오부탄올 생산을 위한 포도당 대사회로에서 바이오부탄올 생산 효소(thiolase)의 산화-환원 스위치 작용기작
2015.09.22
조회수 18792
 5단 수직 적층 반도체 트랜지스터 개발
우리 대학 전기 및 전자공학부 이병현 연구원(지도교수 최양규)과 나노종합기술원(원장 이재영) 강민호 박사가 실리콘 기반의 5단 수직 적층 반도체 트랜지스터를 개발했다.
그리고 반도체 트랜지스터를 이용한 비휘발성 메모리 개발에 성공했다.
이번 연구는 나노 분야 학술지 ‘나노 레터스(Nano letters)’ 11월 6일자 온라인판에 게재됐다.
반도체 트랜지스터 분야는 모든 전자기기의 핵심 구성요소로 국내 산업과 경제 발전에 큰 영향을 끼쳤다.
세계적 추세에 따라 치열한 소형화를 통해 생산성과 성능의 향상을 거듭했으나 최근 10나노미터 시대에 접어들며 제작 공정의 한계 및 누설전류로 인한 전력소모 문제가 커지고 있다.
학계 및 산업계는 문제 해결을 위해 전면-게이트 실리콘 나노선 구조를 개발했다. 이는 누설전류 제어에 가장 효과적인 구조로 저전력 트랜지스터 개발에 이용됐다. 그러나 이 역시 소형화에 따른 나노선 면적 감소로 성능 저하의 한계가 있었다.
연구팀은 전면-게이트 실리콘 나노선을 수직으로 5단으로 쌓아 문제를 해결했다. 이 5단 적층 실리콘 나노선 채널을 보유한 반도체 트랜지스터는 단일 나노선 기반의 트랜지스터보다 5배의 향상된 성능을 보였다.
또한 수직 적층 나노선 구조는 말 그대로 위로 쌓기 때문에 단일 구조와 달리 면적이 증가되지 않아 집적도 향상에도 기여할 수 있다.
나노선 수직 적층은 개발된 ‘일괄 플라즈마 건식 식각 공정’ 방식을 통해 이뤄졌다. 이 공정은 고분자 중합체를 이용해 패턴이 형성될 영역에 미리 보호막을 친 뒤 등방성 건식 식각을 통해 나노선 구조를 형성하는 기술이다. 수직 적층 나노선 구조는 이 기술의 연속 작용을 통해 확보한 결과물이다.
이 기술은 지속적 소형화로 인해 기술적 한계에 부딪힌 반도체 트랜지스터 분야에 새로운 돌파구를 제시할 것으로 기대된다.
관련 연구가 이전부터 진행됐지만 더 간단한 공정기술을 이용해 가장 많은 나노선 채널의 적층에 성공했기 때문에 비용절감 및 제작 시간 단축, 반도체 트랜지스터의 성능 향상으로 인한 상용화 등에 크게 기여할 것으로 예상된다.
연구팀은 건식 식각 공정 기술이 기존 방법보다 간단하고 안정적으로 수직 적층 실리콘나노선 구조 제작을 가능하게 함으로써 고성능 트랜지스터 개발에 응용 가능할 것이라고 밝혔다.
이병현 연구원과 강민호 박사는 “이번 기술 개발은 미래창조 국가 나노기술 인프라 기관 나노종합기술원의 훌륭한 반도체 연구 기반과 김진수 부장 포함 관련 연구진들의 우수한 공정 능력이 뒷받침돼 가능했다”고 소감을 말했다.
이번 연구는 글로벌프론티어사업 스마트IT융합시스템 연구단의 지원을 받아 수행됐다.
연구를 주도한 이병현 연구원은 우리 대학 최양규 교수 지도하에 박사과정을 수행 중이며, 삼성전자 메모리 사업부의 책임 연구원으로 재직 중이다.
□ 그림 설명
그림1. 일괄 플라즈마 건식 식각 공정 과정의 모식도.
그림2. 서로 다른 방향에서 단면을 관찰한 주사 전자 현미경 사진 및 투과 전자 현미경 사진
2015.11.24 조회수 16500
5단 수직 적층 반도체 트랜지스터 개발
우리 대학 전기 및 전자공학부 이병현 연구원(지도교수 최양규)과 나노종합기술원(원장 이재영) 강민호 박사가 실리콘 기반의 5단 수직 적층 반도체 트랜지스터를 개발했다.
그리고 반도체 트랜지스터를 이용한 비휘발성 메모리 개발에 성공했다.
이번 연구는 나노 분야 학술지 ‘나노 레터스(Nano letters)’ 11월 6일자 온라인판에 게재됐다.
반도체 트랜지스터 분야는 모든 전자기기의 핵심 구성요소로 국내 산업과 경제 발전에 큰 영향을 끼쳤다.
세계적 추세에 따라 치열한 소형화를 통해 생산성과 성능의 향상을 거듭했으나 최근 10나노미터 시대에 접어들며 제작 공정의 한계 및 누설전류로 인한 전력소모 문제가 커지고 있다.
학계 및 산업계는 문제 해결을 위해 전면-게이트 실리콘 나노선 구조를 개발했다. 이는 누설전류 제어에 가장 효과적인 구조로 저전력 트랜지스터 개발에 이용됐다. 그러나 이 역시 소형화에 따른 나노선 면적 감소로 성능 저하의 한계가 있었다.
연구팀은 전면-게이트 실리콘 나노선을 수직으로 5단으로 쌓아 문제를 해결했다. 이 5단 적층 실리콘 나노선 채널을 보유한 반도체 트랜지스터는 단일 나노선 기반의 트랜지스터보다 5배의 향상된 성능을 보였다.
또한 수직 적층 나노선 구조는 말 그대로 위로 쌓기 때문에 단일 구조와 달리 면적이 증가되지 않아 집적도 향상에도 기여할 수 있다.
나노선 수직 적층은 개발된 ‘일괄 플라즈마 건식 식각 공정’ 방식을 통해 이뤄졌다. 이 공정은 고분자 중합체를 이용해 패턴이 형성될 영역에 미리 보호막을 친 뒤 등방성 건식 식각을 통해 나노선 구조를 형성하는 기술이다. 수직 적층 나노선 구조는 이 기술의 연속 작용을 통해 확보한 결과물이다.
이 기술은 지속적 소형화로 인해 기술적 한계에 부딪힌 반도체 트랜지스터 분야에 새로운 돌파구를 제시할 것으로 기대된다.
관련 연구가 이전부터 진행됐지만 더 간단한 공정기술을 이용해 가장 많은 나노선 채널의 적층에 성공했기 때문에 비용절감 및 제작 시간 단축, 반도체 트랜지스터의 성능 향상으로 인한 상용화 등에 크게 기여할 것으로 예상된다.
연구팀은 건식 식각 공정 기술이 기존 방법보다 간단하고 안정적으로 수직 적층 실리콘나노선 구조 제작을 가능하게 함으로써 고성능 트랜지스터 개발에 응용 가능할 것이라고 밝혔다.
이병현 연구원과 강민호 박사는 “이번 기술 개발은 미래창조 국가 나노기술 인프라 기관 나노종합기술원의 훌륭한 반도체 연구 기반과 김진수 부장 포함 관련 연구진들의 우수한 공정 능력이 뒷받침돼 가능했다”고 소감을 말했다.
이번 연구는 글로벌프론티어사업 스마트IT융합시스템 연구단의 지원을 받아 수행됐다.
연구를 주도한 이병현 연구원은 우리 대학 최양규 교수 지도하에 박사과정을 수행 중이며, 삼성전자 메모리 사업부의 책임 연구원으로 재직 중이다.
□ 그림 설명
그림1. 일괄 플라즈마 건식 식각 공정 과정의 모식도.
그림2. 서로 다른 방향에서 단면을 관찰한 주사 전자 현미경 사진 및 투과 전자 현미경 사진
2015.11.24 조회수 16500 광섬유로 300조분의 1초 오차의 클럭 개발
〈김 정 원 교수〉
우리 대학 기계항공공학부 김정원 교수 연구팀이 광섬유 광학 기술로 수백조분의 1초 오차를 가지는 클럭(clock) 원천기술을 개발했다.
이는 클럭 발진기(oscillator)의 성능을 획기적으로 향상시킬 수 있는 원천 기술로 성과를 인정받아 국제학술지 ‘사이언티픽 리포트(Scientific Reports)’ 11월 4일자 온라인 판에 게재됐다.
클럭 발진기는 일정한 시간 간격의 주기적 신호를 발생시켜 전자시스템이 신호에 맞춰 정확하게 동작하도록 만드는 장치이다. 음악 연주에서 메트로놈과 같은 역할을 한다.
이 클럭 발진기는 오늘날 각종 정보통신 시스템 뿐 아니라 입자가속기나 천체관측장치 같은 거대 과학시설, 초정밀 계측 장비, 레이더, GPS 및 위성항법 시스템 등 전 분야에 걸쳐 핵심적 역할을 하고 있다. 따라서 클럭 발진기에서 발생하는 주기적 신호의 시간 오차를 줄인다면 각종 시스템들의 획기적인 성능 향상과 이전에는 불가능했던 기술 개발도 가능해진다.
기존에는 특수 제작된 공진 회로를 이용한 라디오파 혹은 마이크로파 발진기를 사용하거나 광공진기의 주파수 나눔을 이용한 방식의 기술을 사용했으나, 이 방식은 크기가 클 뿐 아니라 기계적 안정도가 떨어지고 수억 원 이상의 고가였기 때문에 실험실 밖에서의 응용 등에 한계가 있었다.
연구팀은 문제 해결을 위해 신뢰성이 높고 가격경쟁력이 확보된 광통신용 광섬유 부품을 활용한 새로운 방식의 클럭 발진기를 개발했다.
기술의 핵심은 초고속 광섬유 레이저에서 발생하는 넓은 스펙트럼 내의 두 광주파수(optical frequency) 차이를 이용한 것이다. 기존 전자 발진기는 기가헤르츠(GHz, 1초에 109회 진동) 영역에서 동작하지만, 이 기술은 이보다 테라헤르츠(THz, 1초에 1012회 진동) 주파수를 이용하기 때문에 약 1000배 민감한 시간 차 측정이 가능하다.
또한 광섬유 케이블에서 빛이 전파되는 시간이 매우 일정하게 유지되기 때문에 테라헤르츠 주파수를 이용해 높은 분해능으로 측정된 시간차를 광섬유 케이블 내에서의 빛의 전파 시간에 정확하게 맞췄다.
그 결과 국제전기통신연합(ITU)에서 정의한 클럭 신호원의 성능을 나타내는 0.1초 동안의 시간오차인 타이밍 지터(timing jitter)가 3펨토초(333조분의 1초)로 측정됐으며, 이는 환산하면 100만년 동안 1초의 오차를 갖는 성능에 해당한다.
이를 통해 별도의 특수 제작된 고가 소자 없이도 세계적 수준의 클럭 발진기 성능을 얻을 수 있고, 상용화 시 제작비용을 기존 최고 성능 발진기의 10분의 1 이하 수준으로 낮출 것으로 기대된다.
연구팀은 이 기술의 성능과 안정성이 아날로그-디지털 변환기나 고성능 신호 분석기와 같은 ICT 시스템, 레이더, 원격 탐사, 위성항법 등 국방, 우주, 환경 기술 분야에서도 폭넓게 활용될 수 있을 것이라고 밝혔다.
김 교수는 “이 기술은 군용 레이더, 보안 분야와의 연관성 때문에 주요 장비들의 수출이 금지된 경우가 많아 순수 국내 기술로 자체 개발한 것은 그 의의가 크다.”며 “향후 유리기판 위에 시스템을 구현해 칩 스케일의 고성능 클럭으로 발전시킬 계획이다”고 말했다.
KAIST 기계공학과 정광연 박사과정(1저자)의 참여로 이루어진 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 수백조분의 1초 오차의 광섬유 클럭 발진기 개념도
2015.11.12 조회수 13588
광섬유로 300조분의 1초 오차의 클럭 개발
〈김 정 원 교수〉
우리 대학 기계항공공학부 김정원 교수 연구팀이 광섬유 광학 기술로 수백조분의 1초 오차를 가지는 클럭(clock) 원천기술을 개발했다.
이는 클럭 발진기(oscillator)의 성능을 획기적으로 향상시킬 수 있는 원천 기술로 성과를 인정받아 국제학술지 ‘사이언티픽 리포트(Scientific Reports)’ 11월 4일자 온라인 판에 게재됐다.
클럭 발진기는 일정한 시간 간격의 주기적 신호를 발생시켜 전자시스템이 신호에 맞춰 정확하게 동작하도록 만드는 장치이다. 음악 연주에서 메트로놈과 같은 역할을 한다.
이 클럭 발진기는 오늘날 각종 정보통신 시스템 뿐 아니라 입자가속기나 천체관측장치 같은 거대 과학시설, 초정밀 계측 장비, 레이더, GPS 및 위성항법 시스템 등 전 분야에 걸쳐 핵심적 역할을 하고 있다. 따라서 클럭 발진기에서 발생하는 주기적 신호의 시간 오차를 줄인다면 각종 시스템들의 획기적인 성능 향상과 이전에는 불가능했던 기술 개발도 가능해진다.
기존에는 특수 제작된 공진 회로를 이용한 라디오파 혹은 마이크로파 발진기를 사용하거나 광공진기의 주파수 나눔을 이용한 방식의 기술을 사용했으나, 이 방식은 크기가 클 뿐 아니라 기계적 안정도가 떨어지고 수억 원 이상의 고가였기 때문에 실험실 밖에서의 응용 등에 한계가 있었다.
연구팀은 문제 해결을 위해 신뢰성이 높고 가격경쟁력이 확보된 광통신용 광섬유 부품을 활용한 새로운 방식의 클럭 발진기를 개발했다.
기술의 핵심은 초고속 광섬유 레이저에서 발생하는 넓은 스펙트럼 내의 두 광주파수(optical frequency) 차이를 이용한 것이다. 기존 전자 발진기는 기가헤르츠(GHz, 1초에 109회 진동) 영역에서 동작하지만, 이 기술은 이보다 테라헤르츠(THz, 1초에 1012회 진동) 주파수를 이용하기 때문에 약 1000배 민감한 시간 차 측정이 가능하다.
또한 광섬유 케이블에서 빛이 전파되는 시간이 매우 일정하게 유지되기 때문에 테라헤르츠 주파수를 이용해 높은 분해능으로 측정된 시간차를 광섬유 케이블 내에서의 빛의 전파 시간에 정확하게 맞췄다.
그 결과 국제전기통신연합(ITU)에서 정의한 클럭 신호원의 성능을 나타내는 0.1초 동안의 시간오차인 타이밍 지터(timing jitter)가 3펨토초(333조분의 1초)로 측정됐으며, 이는 환산하면 100만년 동안 1초의 오차를 갖는 성능에 해당한다.
이를 통해 별도의 특수 제작된 고가 소자 없이도 세계적 수준의 클럭 발진기 성능을 얻을 수 있고, 상용화 시 제작비용을 기존 최고 성능 발진기의 10분의 1 이하 수준으로 낮출 것으로 기대된다.
연구팀은 이 기술의 성능과 안정성이 아날로그-디지털 변환기나 고성능 신호 분석기와 같은 ICT 시스템, 레이더, 원격 탐사, 위성항법 등 국방, 우주, 환경 기술 분야에서도 폭넓게 활용될 수 있을 것이라고 밝혔다.
김 교수는 “이 기술은 군용 레이더, 보안 분야와의 연관성 때문에 주요 장비들의 수출이 금지된 경우가 많아 순수 국내 기술로 자체 개발한 것은 그 의의가 크다.”며 “향후 유리기판 위에 시스템을 구현해 칩 스케일의 고성능 클럭으로 발전시킬 계획이다”고 말했다.
KAIST 기계공학과 정광연 박사과정(1저자)의 참여로 이루어진 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 수백조분의 1초 오차의 광섬유 클럭 발진기 개념도
2015.11.12 조회수 13588 기체가 저장물질에 흡착되는 과정 관찰
우리 대학 EEWS 대학원 강정구 교수와 오사무 테라사키 공동 연구팀이 2~5 나노미터(10억분의 1m) 크기의 구멍을 갖는 메조다공성 금속유기골격체(metal organic framework, MOF) 안에 기체가 흡착되는 과정을 관찰하는 데 성공했다.
관찰 과정에서 기체들이 각자의 기공에 일정하지 않은 각기 다른 밀도로 흡착된다는 사실을 발견했다. 이는 기존의 학설과 반대되는 개념으로 금속유기골격체에서 기체가 초격자 구조를 형성한다는 사실을 최초로 발견한 것이다.
이번 연구는 국제 과학 학술지 ‘네이처’ 11월 9일자 온라인 판에 게재됐다.
메조다공성 금속유기골격체는 넓은 비표면적을 갖고 있어 수소나 메탄, 이산화탄소 등의 가스 저장에 용이한 저장물질이다. 효율적인 가스 저장을 위해서는 기체가 저장물질에 어떻게 흡착하는지 이해하는 것이 중요하다.
그러나 일반적인 기체 흡착 측정 장비의 경우에는 흡착 거동을 직접적으로 관찰할 수 없다는 한계가 있었다.
문제 해결을 위해 연구팀은 기존에 존재하는 두 개의 장비를 이용했다. 구조적 정보를 얻을 수 있는 X-선 소각산란(small angle X-ray scattering, SAXS) 측정 장비와 기체흡착 측정 장비를 결합했다.
두 장비가 결합된 실시간 기체 흡착 SAXS 시스템을 개발해 메조다공성 금속유기골격체의 결정에 기체가 흡착하는 과정을 실시간으로 관찰했다.
연구팀은 관찰 과정에서 금속유기골격체의 모든 기공에 기체가 균일하게 흡착되지 않고 각자 다른 밀도로 흡착된다는 사실을 발견했다. 그리고 압력이 증가하면서 급격하게 초격자 구조로 변이된 후 서서히 균일하게 분포하는 것 또한 확인했다.
이는 모든 기공에 균일하게 기체가 들어간다는 학설을 뒤집는 발견이다. 이것이 가능했던 이유는 메조다공성 금속유기골격체의 경우 골격이 얇고 기공이 커 다른 구멍의 기체분자끼리도 상호작용하기 때문에 발생하는 현상이다.
따라서 메조다공성 금속유기골격체를 사용한다면 기존 저장물질에 비해 더 적은 용량으로 더 많은 가스를 저장할 수 있는 고효율 저장장치를 개발할 수 있게 된다.
이 기술을 기반으로 새로운 고용량 가스저장 물질의 제작이 가능해짐으로써, 여러 운송수단이나 가스를 사용하는 기계의 성능을 끌어올릴 수 있을 것으로 기대된다.
연구를 주도한 조해성 박사는 “단일 기공 내부의 기체 분자 뿐 아니라 다른 기공의 기체 분자 간 상호작용에 의해 기체의 흡착 메커니즘이 발생함을 새롭게 발견했다”고 말했다.
이번 연구는 미래창조과학부 글로벌프론티어사업, 인공광합성사업, BK21PLUS의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 실시간 기체흡착 SAXS 시스템 모식도
그림2. 메조다공성 MOF 결정에 기체가 흡착되는 과정
그림3. 메조다공성 MOF 결정에서 기체분자의 상호작용 모델
2015.11.11 조회수 14987
기체가 저장물질에 흡착되는 과정 관찰
우리 대학 EEWS 대학원 강정구 교수와 오사무 테라사키 공동 연구팀이 2~5 나노미터(10억분의 1m) 크기의 구멍을 갖는 메조다공성 금속유기골격체(metal organic framework, MOF) 안에 기체가 흡착되는 과정을 관찰하는 데 성공했다.
관찰 과정에서 기체들이 각자의 기공에 일정하지 않은 각기 다른 밀도로 흡착된다는 사실을 발견했다. 이는 기존의 학설과 반대되는 개념으로 금속유기골격체에서 기체가 초격자 구조를 형성한다는 사실을 최초로 발견한 것이다.
이번 연구는 국제 과학 학술지 ‘네이처’ 11월 9일자 온라인 판에 게재됐다.
메조다공성 금속유기골격체는 넓은 비표면적을 갖고 있어 수소나 메탄, 이산화탄소 등의 가스 저장에 용이한 저장물질이다. 효율적인 가스 저장을 위해서는 기체가 저장물질에 어떻게 흡착하는지 이해하는 것이 중요하다.
그러나 일반적인 기체 흡착 측정 장비의 경우에는 흡착 거동을 직접적으로 관찰할 수 없다는 한계가 있었다.
문제 해결을 위해 연구팀은 기존에 존재하는 두 개의 장비를 이용했다. 구조적 정보를 얻을 수 있는 X-선 소각산란(small angle X-ray scattering, SAXS) 측정 장비와 기체흡착 측정 장비를 결합했다.
두 장비가 결합된 실시간 기체 흡착 SAXS 시스템을 개발해 메조다공성 금속유기골격체의 결정에 기체가 흡착하는 과정을 실시간으로 관찰했다.
연구팀은 관찰 과정에서 금속유기골격체의 모든 기공에 기체가 균일하게 흡착되지 않고 각자 다른 밀도로 흡착된다는 사실을 발견했다. 그리고 압력이 증가하면서 급격하게 초격자 구조로 변이된 후 서서히 균일하게 분포하는 것 또한 확인했다.
이는 모든 기공에 균일하게 기체가 들어간다는 학설을 뒤집는 발견이다. 이것이 가능했던 이유는 메조다공성 금속유기골격체의 경우 골격이 얇고 기공이 커 다른 구멍의 기체분자끼리도 상호작용하기 때문에 발생하는 현상이다.
따라서 메조다공성 금속유기골격체를 사용한다면 기존 저장물질에 비해 더 적은 용량으로 더 많은 가스를 저장할 수 있는 고효율 저장장치를 개발할 수 있게 된다.
이 기술을 기반으로 새로운 고용량 가스저장 물질의 제작이 가능해짐으로써, 여러 운송수단이나 가스를 사용하는 기계의 성능을 끌어올릴 수 있을 것으로 기대된다.
연구를 주도한 조해성 박사는 “단일 기공 내부의 기체 분자 뿐 아니라 다른 기공의 기체 분자 간 상호작용에 의해 기체의 흡착 메커니즘이 발생함을 새롭게 발견했다”고 말했다.
이번 연구는 미래창조과학부 글로벌프론티어사업, 인공광합성사업, BK21PLUS의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 실시간 기체흡착 SAXS 시스템 모식도
그림2. 메조다공성 MOF 결정에 기체가 흡착되는 과정
그림3. 메조다공성 MOF 결정에서 기체분자의 상호작용 모델
2015.11.11 조회수 14987 화합물의 광학 활성 분석 기술 개발
〈 김 현 우 교수〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명 분광분석기(NMR)를 통해 전하를 띠는 화합물의 광학 활성을 간단히 분석할 수 있는 기술을 개발했다.
연구 결과는 화학분야 학술지 ‘미국화학회지(Journal of the American Chemical Society)’ 10월 19일자 온라인 판에 게재됐다.
오른손과 왼손처럼 같은 물질이지만 거울상 대칭이 되는 화합물을 광학 이성질체라고 한다.
지구상의 생명체를 이루는 아미노산과 당은 하나의 광학 이성질체로 이뤄져 있어 새로운 화합물이 생체에 들어갈 때 광학 활성에 따라 서로 다른 생리학적 특징을 나타낸다. 따라서 신약을 개발할 때 광학 활성을 조절하고 분석하는 연구는 필수적이다.
광학 활성의 분석 방법으로 고성능 액체 크로마토그래피(HPLC)가 주로 사용되는데, 고가의 부품을 구비해야 하고 30분에서 1시간 정도의 시간이 소요되는 단점이 있다.
또한 신호의 감도 및 분해 기능이 떨어지고 사용할 수 있는 용매가 무극성에 한정되는 점 때문에 활용에 한계가 있었다.
반면 화합물의 분자 구조 분석에 활용되는 핵자기공명(NMR) 분광분석기는 1~5분 정도의 빠른 분석속도를 갖고 있다. 또한 화학 분야에서 분자의 구조를 확인하기 위한 필수 장비이기 때문에 대부분의 연구실에서 구비된 상태다.
하지만 이 핵자기공명 분광분석기를 통해 광학 활성 화합물의 신호를 분리하는 효과적인 방법은 보고되지 않았다.
연구팀은 기존에 알려지지 않은 음전하를 띠는 금속 화합물과 핵자기공명 분광분석기를 이용해 분석 방법을 개발했다.
음전하를 띤 금속 화합물이 양전하 및 음전하를 갖는 광학활성 화합물과 이온성 결합을 하면 핵자기공명 분광분석기를 통해 신호가 구별돼 광학 활성을 분석할 수 있는 원리이다.
이 방법을 사용하면 구조적 제약 없이 다양한 화합물을 분석할 수 있고, 비극성 및 극성 용매에 모두 적용 가능하다는 장점을 갖는다.
연구팀은 다양한 신약 및 신약후보 물질들은 전하를 띨 수 있는 작용기를 포함한 경우가 많아 연구팀의 새로운 분석 방법이 신약 개발에 직접적으로 활용 가능할 것으로 기대된다고 밝혔다.
김 교수는 “간단한 화학적 원리를 통해 기존의 틀을 깨는 혁신적 분석방법을 만들었다”며 “이 방법이 신약개발에 많이 활용되길 기대한다”고 말했다.
화학과 서민섭 박사과정(1저자)의 참여로 이루어진 이번 연구는 기초과학연구원(IBS) 나노물질 및 화학반응 연구단과 슈퍼컴퓨팅연구지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 금속 화합물과 이온성 상호작용으로 광학활성을 가진 화합물의 NMR 신호가 분리되는 현상
그림2. 다양한 광학활성 물질이 분리되는 그림
2015.11.10 조회수 17680
화합물의 광학 활성 분석 기술 개발
〈 김 현 우 교수〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명 분광분석기(NMR)를 통해 전하를 띠는 화합물의 광학 활성을 간단히 분석할 수 있는 기술을 개발했다.
연구 결과는 화학분야 학술지 ‘미국화학회지(Journal of the American Chemical Society)’ 10월 19일자 온라인 판에 게재됐다.
오른손과 왼손처럼 같은 물질이지만 거울상 대칭이 되는 화합물을 광학 이성질체라고 한다.
지구상의 생명체를 이루는 아미노산과 당은 하나의 광학 이성질체로 이뤄져 있어 새로운 화합물이 생체에 들어갈 때 광학 활성에 따라 서로 다른 생리학적 특징을 나타낸다. 따라서 신약을 개발할 때 광학 활성을 조절하고 분석하는 연구는 필수적이다.
광학 활성의 분석 방법으로 고성능 액체 크로마토그래피(HPLC)가 주로 사용되는데, 고가의 부품을 구비해야 하고 30분에서 1시간 정도의 시간이 소요되는 단점이 있다.
또한 신호의 감도 및 분해 기능이 떨어지고 사용할 수 있는 용매가 무극성에 한정되는 점 때문에 활용에 한계가 있었다.
반면 화합물의 분자 구조 분석에 활용되는 핵자기공명(NMR) 분광분석기는 1~5분 정도의 빠른 분석속도를 갖고 있다. 또한 화학 분야에서 분자의 구조를 확인하기 위한 필수 장비이기 때문에 대부분의 연구실에서 구비된 상태다.
하지만 이 핵자기공명 분광분석기를 통해 광학 활성 화합물의 신호를 분리하는 효과적인 방법은 보고되지 않았다.
연구팀은 기존에 알려지지 않은 음전하를 띠는 금속 화합물과 핵자기공명 분광분석기를 이용해 분석 방법을 개발했다.
음전하를 띤 금속 화합물이 양전하 및 음전하를 갖는 광학활성 화합물과 이온성 결합을 하면 핵자기공명 분광분석기를 통해 신호가 구별돼 광학 활성을 분석할 수 있는 원리이다.
이 방법을 사용하면 구조적 제약 없이 다양한 화합물을 분석할 수 있고, 비극성 및 극성 용매에 모두 적용 가능하다는 장점을 갖는다.
연구팀은 다양한 신약 및 신약후보 물질들은 전하를 띨 수 있는 작용기를 포함한 경우가 많아 연구팀의 새로운 분석 방법이 신약 개발에 직접적으로 활용 가능할 것으로 기대된다고 밝혔다.
김 교수는 “간단한 화학적 원리를 통해 기존의 틀을 깨는 혁신적 분석방법을 만들었다”며 “이 방법이 신약개발에 많이 활용되길 기대한다”고 말했다.
화학과 서민섭 박사과정(1저자)의 참여로 이루어진 이번 연구는 기초과학연구원(IBS) 나노물질 및 화학반응 연구단과 슈퍼컴퓨팅연구지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 금속 화합물과 이온성 상호작용으로 광학활성을 가진 화합물의 NMR 신호가 분리되는 현상
그림2. 다양한 광학활성 물질이 분리되는 그림
2015.11.10 조회수 17680 고효율의 하이브리드 자동차 구동 시스템 개발
〈윤 용 산 교수〉
우리 대학 기계공학과 윤용산 교수 연구팀이 클러치 페달 없이 수동 변속이 가능한 독자적 구동시스템의 시작품(Prototype) 제작에 성공했다.
이 기술로 기존 하이브리드 자동차보다 높은 효율의 자동차 개발이 가능할 것으로 보인다. 연구팀의 하이브리드 자동차는 구조가 간단해 기존 자동차에 약간의 변형을 주는 것으로도 구현이 가능하며, 제작비용이 저렴하고 운전이 용이하다는 장점을 갖는다.
이 구동시스템은 ‘대화형 수동변속기를 갖는 하이브리드 차량 및 이의 제어 방법’으로 작년 5월 국제특허(PCT)로 등록됐고, 지난 5월 경기도 고양에서 열린 제 28회 국제 전기자동차 심포지엄 및 전시회에 발표됐다.
하이브리드 자동차는 내연기관 엔진과 변속기에 모터와 발전기를 결합시켜 공해와 연료 소모를 최소화하는 차량이다. 미국에서 발표하는 에너지 아웃룩(Energy Outlook)에 의하면 25년 후에도 하이브리드 자동차가 친환경 자동차 시장을 주도할 것으로 예상하고 있다.
그러나 일본의 자동차 기업이 하이브리드 자동차 관련 특허를 대량으로 선점해 기술 개발에 어려움을 겪고 있는 현실이다.
또한 한때 개발된 컴퓨터에 의한 반자동 수동변속기나 일본 회사의 수동변속기에 모터를 단순 부착한 제품은 비용이나 편의 측면에서 한계가 있었다.
문제 해결을 위해 연구팀은 비용이 제일 저렴한 수동변속기에 모터 발전기를 부착해 독창적인 방식의 비용절감 효과가 큰 하이브리드 자동차 시스템을 구현했다.
연구팀은 수동변속기의 클러치판을 없애고 그 기능을 모터발전기로 대신해 저속에서는 모터발전기로만 운행하게 만들었다.
이를 통해 기존 수동변속기 차량의 문제점인 엔진 꺼짐이나 번거로운 클러치 조작에서 벗어날 수 있다. 또한 변속 시간, 중량이 줄고 구동시스템의 내구성이 향상된다.
윤 교수는 “기존 방식과 달리 모터발전기가 클러치판을 대신해 엔진을 조절하기 때문에 기어 변경이 부드럽게 이뤄질 수 있다”며 “저속에서는 모터발전기에 의해서만 구동되므로 수동변속기의 문제점을 상당부분 해결할 수 있다”고 말했다.
기계공학과 손희운 석사과정 학생의 주도로 진행된 이번 연구는 한국연구재단의 이공분야 기초연구사업, 일반연구자 지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 클러치를 제거하고 일방향 클러치와 모터발전기를 첨가해 반자동의 실용적인 하이브리드 구동시스템을 구현한 모습
2015.11.04 조회수 12113
고효율의 하이브리드 자동차 구동 시스템 개발
〈윤 용 산 교수〉
우리 대학 기계공학과 윤용산 교수 연구팀이 클러치 페달 없이 수동 변속이 가능한 독자적 구동시스템의 시작품(Prototype) 제작에 성공했다.
이 기술로 기존 하이브리드 자동차보다 높은 효율의 자동차 개발이 가능할 것으로 보인다. 연구팀의 하이브리드 자동차는 구조가 간단해 기존 자동차에 약간의 변형을 주는 것으로도 구현이 가능하며, 제작비용이 저렴하고 운전이 용이하다는 장점을 갖는다.
이 구동시스템은 ‘대화형 수동변속기를 갖는 하이브리드 차량 및 이의 제어 방법’으로 작년 5월 국제특허(PCT)로 등록됐고, 지난 5월 경기도 고양에서 열린 제 28회 국제 전기자동차 심포지엄 및 전시회에 발표됐다.
하이브리드 자동차는 내연기관 엔진과 변속기에 모터와 발전기를 결합시켜 공해와 연료 소모를 최소화하는 차량이다. 미국에서 발표하는 에너지 아웃룩(Energy Outlook)에 의하면 25년 후에도 하이브리드 자동차가 친환경 자동차 시장을 주도할 것으로 예상하고 있다.
그러나 일본의 자동차 기업이 하이브리드 자동차 관련 특허를 대량으로 선점해 기술 개발에 어려움을 겪고 있는 현실이다.
또한 한때 개발된 컴퓨터에 의한 반자동 수동변속기나 일본 회사의 수동변속기에 모터를 단순 부착한 제품은 비용이나 편의 측면에서 한계가 있었다.
문제 해결을 위해 연구팀은 비용이 제일 저렴한 수동변속기에 모터 발전기를 부착해 독창적인 방식의 비용절감 효과가 큰 하이브리드 자동차 시스템을 구현했다.
연구팀은 수동변속기의 클러치판을 없애고 그 기능을 모터발전기로 대신해 저속에서는 모터발전기로만 운행하게 만들었다.
이를 통해 기존 수동변속기 차량의 문제점인 엔진 꺼짐이나 번거로운 클러치 조작에서 벗어날 수 있다. 또한 변속 시간, 중량이 줄고 구동시스템의 내구성이 향상된다.
윤 교수는 “기존 방식과 달리 모터발전기가 클러치판을 대신해 엔진을 조절하기 때문에 기어 변경이 부드럽게 이뤄질 수 있다”며 “저속에서는 모터발전기에 의해서만 구동되므로 수동변속기의 문제점을 상당부분 해결할 수 있다”고 말했다.
기계공학과 손희운 석사과정 학생의 주도로 진행된 이번 연구는 한국연구재단의 이공분야 기초연구사업, 일반연구자 지원사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 클러치를 제거하고 일방향 클러치와 모터발전기를 첨가해 반자동의 실용적인 하이브리드 구동시스템을 구현한 모습
2015.11.04 조회수 12113 대장균의 생물막 형성 제어 기술 개발
〈이 영 훈 교수〉
우리 대학 화학과 이영훈 교수 연구팀이 작은 RNA(small RNA : sRNA)의 발현을 조절해 대장균의 생물막 형성을 제어할 수 있는 기술을 개발했다.
연구 결과는 네이처 자매지인 ‘사이언티픽 리포트(Scientific Reports)’ 10월 15일자에 게재됐다.
세균들은 외부의 여러 환경으로부터 스스로를 보호하기 위해 다량체로 이뤄진 세포성분을 분비한다. 이로 인해 고체 표면이나 살아있는 생물 조직에서 생물막(biofilm)이라는 3차원 구조물이 형성된다.
이 생물막은 제거가 어려울 뿐 아니라 세균의 생체 내 증식, 치석, 의료기기 오염, 수도관, 정수기 등에 분포해 각종 산업시설에서 광범위한 문제를 일으키고 있다.
특히 생물막을 형성하고 있는 세균들은 항생제에 매우 높은 내성을 가질 수 있어 슈퍼박테리아의 항생제 내성의 주요 원인이기도 하다.
생물막 형성에 크게 관여하는 세균 내의 sRNA는 표적 메신저 RNA(mRNA) 또는 단백질과 상호작용해 세포대사를 조절하는 핵심 요소로 기능한다. 학자들은 생물막 형성의 원리를 규명하기 위해 이 sRNA를 연구해 왔다.
현재 대장균에서는 100여 종의 sRNA가 보고됐다. 연구팀은 이 중 99종을 분석해 각각의 대장균 sRNA를 발현할 수 있는 라이브러리를 구축했다. 이후 이를 통해 환경적 스트레스 대응과 밀접한 관련성을 가져 생물막 형성에 핵심이 되는 sRNA를 탐색했다.
그 결과로 연구팀은 생물막 형성에 관여하는 sRNA를 새롭게 발견했고, 생물막 형성을 위한 생리적 변화(세포운동성, I형 핌브리아 형성, 컬리핌브리아 형성)를 일으키는 sRNA들을 분석하는 데 성공했다.
이 분석 방식은 기존의 유전체적 분석을 통한 sRNA 작용 원리 규명 연구에 비해 이 교수 연구팀은 특정 sRNA의 기능을 직접 분석할 수 있어 신속하고 효율적으로 작용 원리를 규명할 수 있다는 장점을 갖는다.
이번 연구를 통해 생물막 형성과정에 관여하는 신호 전달체계를 이해하는 후속 연구 뿐 아니라, sRNA를 진단 마커나 약물 타겟으로 삼아 세균의 병원성 제어에 활용할 수 있을 것으로 기대된다.
이 교수는 “세균의 생물막 형성과 분해를 원하는 방향으로 제어할 수 있게 됐다”며 “향후 99종의 sRNA 각각에 대한 돌연변이 균주도 확보해 함께 활용할 예정이다”고 말했다.
화학과 박근우, 이정민 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 글로벌프론티어사업(지능형 바이오시스템 설계 및 합성 연구), 기초연구실 지원사업, 중견연구자 지원사업(도약연구)을 통해 수행됐다.
□ 그림 설명
그림 1 . 세균 생물막 형성과정의 모식도
그림 2. sRNA의 발현양에 비례하여 생물막 형성의 억제. 생물막 형성이 많을수록 진한 보라색
그림 3. 99종의 대장균 sRNA와 라이브러리 구축에 사용된 pHMB1 플라스미드의 구조
2015.10.28 조회수 16413
대장균의 생물막 형성 제어 기술 개발
〈이 영 훈 교수〉
우리 대학 화학과 이영훈 교수 연구팀이 작은 RNA(small RNA : sRNA)의 발현을 조절해 대장균의 생물막 형성을 제어할 수 있는 기술을 개발했다.
연구 결과는 네이처 자매지인 ‘사이언티픽 리포트(Scientific Reports)’ 10월 15일자에 게재됐다.
세균들은 외부의 여러 환경으로부터 스스로를 보호하기 위해 다량체로 이뤄진 세포성분을 분비한다. 이로 인해 고체 표면이나 살아있는 생물 조직에서 생물막(biofilm)이라는 3차원 구조물이 형성된다.
이 생물막은 제거가 어려울 뿐 아니라 세균의 생체 내 증식, 치석, 의료기기 오염, 수도관, 정수기 등에 분포해 각종 산업시설에서 광범위한 문제를 일으키고 있다.
특히 생물막을 형성하고 있는 세균들은 항생제에 매우 높은 내성을 가질 수 있어 슈퍼박테리아의 항생제 내성의 주요 원인이기도 하다.
생물막 형성에 크게 관여하는 세균 내의 sRNA는 표적 메신저 RNA(mRNA) 또는 단백질과 상호작용해 세포대사를 조절하는 핵심 요소로 기능한다. 학자들은 생물막 형성의 원리를 규명하기 위해 이 sRNA를 연구해 왔다.
현재 대장균에서는 100여 종의 sRNA가 보고됐다. 연구팀은 이 중 99종을 분석해 각각의 대장균 sRNA를 발현할 수 있는 라이브러리를 구축했다. 이후 이를 통해 환경적 스트레스 대응과 밀접한 관련성을 가져 생물막 형성에 핵심이 되는 sRNA를 탐색했다.
그 결과로 연구팀은 생물막 형성에 관여하는 sRNA를 새롭게 발견했고, 생물막 형성을 위한 생리적 변화(세포운동성, I형 핌브리아 형성, 컬리핌브리아 형성)를 일으키는 sRNA들을 분석하는 데 성공했다.
이 분석 방식은 기존의 유전체적 분석을 통한 sRNA 작용 원리 규명 연구에 비해 이 교수 연구팀은 특정 sRNA의 기능을 직접 분석할 수 있어 신속하고 효율적으로 작용 원리를 규명할 수 있다는 장점을 갖는다.
이번 연구를 통해 생물막 형성과정에 관여하는 신호 전달체계를 이해하는 후속 연구 뿐 아니라, sRNA를 진단 마커나 약물 타겟으로 삼아 세균의 병원성 제어에 활용할 수 있을 것으로 기대된다.
이 교수는 “세균의 생물막 형성과 분해를 원하는 방향으로 제어할 수 있게 됐다”며 “향후 99종의 sRNA 각각에 대한 돌연변이 균주도 확보해 함께 활용할 예정이다”고 말했다.
화학과 박근우, 이정민 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 글로벌프론티어사업(지능형 바이오시스템 설계 및 합성 연구), 기초연구실 지원사업, 중견연구자 지원사업(도약연구)을 통해 수행됐다.
□ 그림 설명
그림 1 . 세균 생물막 형성과정의 모식도
그림 2. sRNA의 발현양에 비례하여 생물막 형성의 억제. 생물막 형성이 많을수록 진한 보라색
그림 3. 99종의 대장균 sRNA와 라이브러리 구축에 사용된 pHMB1 플라스미드의 구조
2015.10.28 조회수 16413 복합 처방된 약물의 부작용 예측 기술 개발
〈이 도 헌 교수〉
우리 대학 바이오및뇌공학과 이도헌 교수(유전자동의보감사업단장, 제 1저자 박경현 연구원) 연구팀이 복합 처방된 약물들의 인체 내 간섭현상을 컴퓨터 가상인체로 분석해 부작용을 예측할 수 있는 기술을 개발했다.
이번 연구결과는 미국 공공과학도서관 학술지 플러스 원(PLOS ONE) 10월 15일자에 게재됐다.
의료 현장에서는 여러 약물을 함께 처방받아 복약하는 경우가 많다. 이러한 복합처방은 모든 가능성을 미리 시험할 수 없기 때문에 널리 알려진 대표적 위험사례를 제외하면 완벽한 사전시험이 불가능하다.
기존에는 부작용 사례를 의약품 적정사용평가(DUR)에 등재시켜 의료현장에서 활용하는 사후 추적만이 최선의 방법이었다. 따라서 복합처방으로 인한 의료 사고를 막기 어려웠고 부작용 예측에도 한계가 있었다.
문제 해결을 위해 연구팀은 발생 가능한 상황을 사전에 컴퓨터 가상인체로 예측함으로써 위험을 미리 파악할 수 있는 기술을 개발했다.
연구팀은 컴퓨터 가상인체에서 랜덤워크 알고리즘을 이용해 약물 표적의 생체 내 분자 신호전파를 시뮬레이션 했다. 약물이 투여됨으로써 신체에 영향을 끼치는 정도를 측정한 것인데, 이를 통해 두 개의 약물이 서로 어느 정도의 영향을 주는지 정량화에 성공했다.
따라서 만약 두 약물 간 간섭이 심해 서로 많은 영향을 준다면 부작용이 발생할 가능성이 높기 때문에 신중한 처방을 해야한다는 결론을 얻을 수 있다.
기존 예측 기술들이 단백질 상호작용 네트워크에서 약물 표적사이의 근거리 간섭만을 고려했다면 이 교수 연구팀은 약물 표적의 생체 내 분자 신호전파 시뮬레이션을 통해 원거리 간섭까지 고려해 정확도를 높였다.
연구팀은 이 기술이 다수의 표적을 갖는 복합 천연물의 신호 전파도 분석해 약물과 천연물 사이의 상호작용 예측에도 활용될 것이라고 예상했다.
이 교수는 “이번 기술은 자체 개발한 대규모 컴퓨터 가상인체 시스템을 통해 진행됐다”며 “약물 복합처방의 부작용을 예측할 수 있는 새로운 방법을 제시했다는 의의를 갖는다”고 말했다.
□ 그림 설명
그림 1. 연구팀이 개발한 컴퓨터 가상인체 시스템
그림 2 . 처방된 복합 약물 사이의 신호전파 간섭 예시
2015.10.22 조회수 12166
복합 처방된 약물의 부작용 예측 기술 개발
〈이 도 헌 교수〉
우리 대학 바이오및뇌공학과 이도헌 교수(유전자동의보감사업단장, 제 1저자 박경현 연구원) 연구팀이 복합 처방된 약물들의 인체 내 간섭현상을 컴퓨터 가상인체로 분석해 부작용을 예측할 수 있는 기술을 개발했다.
이번 연구결과는 미국 공공과학도서관 학술지 플러스 원(PLOS ONE) 10월 15일자에 게재됐다.
의료 현장에서는 여러 약물을 함께 처방받아 복약하는 경우가 많다. 이러한 복합처방은 모든 가능성을 미리 시험할 수 없기 때문에 널리 알려진 대표적 위험사례를 제외하면 완벽한 사전시험이 불가능하다.
기존에는 부작용 사례를 의약품 적정사용평가(DUR)에 등재시켜 의료현장에서 활용하는 사후 추적만이 최선의 방법이었다. 따라서 복합처방으로 인한 의료 사고를 막기 어려웠고 부작용 예측에도 한계가 있었다.
문제 해결을 위해 연구팀은 발생 가능한 상황을 사전에 컴퓨터 가상인체로 예측함으로써 위험을 미리 파악할 수 있는 기술을 개발했다.
연구팀은 컴퓨터 가상인체에서 랜덤워크 알고리즘을 이용해 약물 표적의 생체 내 분자 신호전파를 시뮬레이션 했다. 약물이 투여됨으로써 신체에 영향을 끼치는 정도를 측정한 것인데, 이를 통해 두 개의 약물이 서로 어느 정도의 영향을 주는지 정량화에 성공했다.
따라서 만약 두 약물 간 간섭이 심해 서로 많은 영향을 준다면 부작용이 발생할 가능성이 높기 때문에 신중한 처방을 해야한다는 결론을 얻을 수 있다.
기존 예측 기술들이 단백질 상호작용 네트워크에서 약물 표적사이의 근거리 간섭만을 고려했다면 이 교수 연구팀은 약물 표적의 생체 내 분자 신호전파 시뮬레이션을 통해 원거리 간섭까지 고려해 정확도를 높였다.
연구팀은 이 기술이 다수의 표적을 갖는 복합 천연물의 신호 전파도 분석해 약물과 천연물 사이의 상호작용 예측에도 활용될 것이라고 예상했다.
이 교수는 “이번 기술은 자체 개발한 대규모 컴퓨터 가상인체 시스템을 통해 진행됐다”며 “약물 복합처방의 부작용을 예측할 수 있는 새로운 방법을 제시했다는 의의를 갖는다”고 말했다.
□ 그림 설명
그림 1. 연구팀이 개발한 컴퓨터 가상인체 시스템
그림 2 . 처방된 복합 약물 사이의 신호전파 간섭 예시
2015.10.22 조회수 12166 소장 내 지방 흡수과정의 비밀 밝혀
김 필 한 교수
우리 대학 나노과학기술대학원 김필한 교수와 의과학대학원 고규영 교수 공동 연구팀이 소장에서 지방이 흡수되는 과정의 고해상도 촬영에 성공했다.
이번 연구는 나노과학기술대학원 최기백 박사과정 학생, 의과학대학원 장전엽 박사, 박인태 박사과정 학생이 1저자로 참여했다.
이를 통해 소장의 융모로 흡수된 지방의 전달 통로인 암죽관의 수축현상을 최초로 발견했다.
이번 연구결과는 의생명과학 분야 국제 학술지인 ‘임상연구(The Journal of Clinical Investigation, Impact Factor 13.261)’ 10월 5일자 온라인판에 게재됐다. 또한 11월에는 이달의 주목할 만한 연구로 ‘JCI This month’에도 소개될 예정이다. (논문명 : Intravital imaging of intestinal lacteals unveils lipid drainage through contractility)
소장은 영양분을 흡수하는 기관이다. 소장의 관찰을 위해 많은 학자들이 노력했지만 소장은 항상 쉬지 않고 움직이기 때문에 고해상도 촬영에 한계가 있었다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 소장 의 상태를 보존하고 내벽을 고정할 수 있는 영상 챔버를 이용해 동물 모델의 소장 내벽에서 지방산이 흡수되는 과정을 촬영했다.
이 과정에서 지방의 흡수 통로인 암죽관이 일정 주기로 수축 및 이완하는 현상을 발견했다. 또한 암죽관의 수축 정도가 소장에서의 지방산 흡수 속도에 영향을 미치는 것을 발견했다.
연구팀은 이 암죽관의 움직임이 융모 내부에 다량 존재하는 민무늬근세포에 의해 발생하고, 이는 체내에 분포된 자율신경계를 통해 조절됨을 밝혔다.
이번 연구를 통해 개발된 최첨단 고해상도 생체영상기술로 소장 내 다양한 물질 흡수 과정의 실시간 모니터링이 가능해질 것으로 예상된다.
또한 이 기술은 신약개발 과정에서 지용성 약물이 소장 내 암죽관으로 흡수되게 해 간 독성을 최소화하는 새로운 약물전달 방법 확립에 기여할 것으로 기대된다.
김 교수는 “우리가 섭취하는 다량의 지용성 영양소가 체내로 흡수되는 과정에서 자율신경계로 조절되는 융모 내부의 암죽관 제어 메커니즘이 존재함을 새롭게 밝혀냈다”고 말했다.
이번 연구는 미래창조과학부의 글로벌프론티어사업 및 신기술융합형 성장동력사업의 지원을 받아 수행됐다.
그림 설명
그림1. 소장 내벽에 존재하는 융모에서 지방산이 흡수되는 과정을 광학현미경으로 영상화하는 과정 모식도
그림2. 소장 융모에서 지방산(적색)이 암죽관(녹색)을 통해 흡수되는 과정
그림3. 암죽관(녹색)의 반복적인 이완과 수축 운동. 0초, 2.7초에 이완. 1.6초, 4초에 암죽관의 수축
2015.10.14 조회수 20687
소장 내 지방 흡수과정의 비밀 밝혀
김 필 한 교수
우리 대학 나노과학기술대학원 김필한 교수와 의과학대학원 고규영 교수 공동 연구팀이 소장에서 지방이 흡수되는 과정의 고해상도 촬영에 성공했다.
이번 연구는 나노과학기술대학원 최기백 박사과정 학생, 의과학대학원 장전엽 박사, 박인태 박사과정 학생이 1저자로 참여했다.
이를 통해 소장의 융모로 흡수된 지방의 전달 통로인 암죽관의 수축현상을 최초로 발견했다.
이번 연구결과는 의생명과학 분야 국제 학술지인 ‘임상연구(The Journal of Clinical Investigation, Impact Factor 13.261)’ 10월 5일자 온라인판에 게재됐다. 또한 11월에는 이달의 주목할 만한 연구로 ‘JCI This month’에도 소개될 예정이다. (논문명 : Intravital imaging of intestinal lacteals unveils lipid drainage through contractility)
소장은 영양분을 흡수하는 기관이다. 소장의 관찰을 위해 많은 학자들이 노력했지만 소장은 항상 쉬지 않고 움직이기 때문에 고해상도 촬영에 한계가 있었다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 소장 의 상태를 보존하고 내벽을 고정할 수 있는 영상 챔버를 이용해 동물 모델의 소장 내벽에서 지방산이 흡수되는 과정을 촬영했다.
이 과정에서 지방의 흡수 통로인 암죽관이 일정 주기로 수축 및 이완하는 현상을 발견했다. 또한 암죽관의 수축 정도가 소장에서의 지방산 흡수 속도에 영향을 미치는 것을 발견했다.
연구팀은 이 암죽관의 움직임이 융모 내부에 다량 존재하는 민무늬근세포에 의해 발생하고, 이는 체내에 분포된 자율신경계를 통해 조절됨을 밝혔다.
이번 연구를 통해 개발된 최첨단 고해상도 생체영상기술로 소장 내 다양한 물질 흡수 과정의 실시간 모니터링이 가능해질 것으로 예상된다.
또한 이 기술은 신약개발 과정에서 지용성 약물이 소장 내 암죽관으로 흡수되게 해 간 독성을 최소화하는 새로운 약물전달 방법 확립에 기여할 것으로 기대된다.
김 교수는 “우리가 섭취하는 다량의 지용성 영양소가 체내로 흡수되는 과정에서 자율신경계로 조절되는 융모 내부의 암죽관 제어 메커니즘이 존재함을 새롭게 밝혀냈다”고 말했다.
이번 연구는 미래창조과학부의 글로벌프론티어사업 및 신기술융합형 성장동력사업의 지원을 받아 수행됐다.
그림 설명
그림1. 소장 내벽에 존재하는 융모에서 지방산이 흡수되는 과정을 광학현미경으로 영상화하는 과정 모식도
그림2. 소장 융모에서 지방산(적색)이 암죽관(녹색)을 통해 흡수되는 과정
그림3. 암죽관(녹색)의 반복적인 이완과 수축 운동. 0초, 2.7초에 이완. 1.6초, 4초에 암죽관의 수축
2015.10.14 조회수 20687 산란된 빛을 다시 집약시키는 시간 역행 거울 개발
우리 대학 물리학과 박용근 교수 연구팀이 빛을 거꾸로 반사시켜 시간이 역행하는 것처럼 보이는 시간 역행 거울을 개발했다.
연구 성과는 물리학분야 학술지인 ‘피지컬 리뷰 레터스(Physical Review Letters)’ 10월 6일자 온라인 판에 게재됐다.
빛의 시간 역행성은 녹화된 비디오를 되감기하듯 빛의 진행을 되돌릴 수 있는 개념을 뜻한다. 이는 마치 쏟은 물을 주워 담는 것과 같이 흩뿌려진 빛을 다시 집약시켜 산란 전의 영상을 복구하는 것과 같은 원리이다.
빛의 시간 역행 실현을 위해선 특별한 거울이 필요했다. 이론상으로만 제안되었던 이 시간 역행 거울(위상 공액 거울)은 빛이 거울에 부딪혔을 때 부딪쳐 온 방향으로 빛이 반사돼 원래 상태로 돌아가는 특성을 갖는다.
많은 학자들이 비선형 레이저 광학 지식을 이용해 시간 역행 거울을 구현하려 노력했다. 하지만 이 특수한 현상의 실현을 위해선 일반적인 거울과 다르게 추가적인 입사 레이저광이 필요하고 주변 환경에 극도로 민감하다는 한계가 있었다.
연구팀은 문제 해결을 위해 기존 복잡한 시도와 반대로 일반 거울에서의 반사를 재해석해 활용했다.
연구팀은 파면제어기라 불리는 수많은 미세 거울로 이루어진 장치를 활용했다. 파면제어기는 입사하는 빛의 모양에 맞춰 거울의 표면을 변경시켜 평행 상태로 만드는 원리인데, 이를 통해 복잡한 물리현상의 도입 없이도 빛의 시간 역행 거울을 구현하는데 성공했다.
또한 연구팀은 구현된 시간 역행 거울을 활용해 모의 생체조직 샘플, 생 닭가슴살 등에 의해 심하게 산란된 빛을 집약시켜 산란 전의 모양으로 재현했다.
연구팀에 의해 구현된 시간 역행 거울은 그 구현방법이 쉽고 주변환경의 영향을 받지 않아 빠른 시일 내에 실제 응용에 접목할 수 있을 것으로 예상된다.
논문의 1저자인 이겨레 박사과정은 “이 기술을 활용하면 기존 생체조직에서 심한 산란으로 인해 불가능했던 생체조직 내부의 빛 집약이 가능하다” 며 “향후 무절개 암 수술 등 미래기술의 기반기술이 될 수 있다”고 말했다.
또한 박 교수는 “이번 기술은 빛 뿐 아니라 소리, 전자파, 라디오 등 일반적인 파동에서 성립하는 개념이다”며 “향후 레이저 및 광통신 기술을 포함한 물리학, 광학, 의학 등 다양한 분야에 응용될 것으로 기대된다”고 말했다.
□ 그림 설명
그림 1. 생체조직,닭가슴살,광섬유를 산란체로 활용한 뒤 시간역행 거울로 원래 이미지를 구현한 사진
그림 2. 일반거울과 시간역행거울의 원리
2015.10.07 조회수 13656
산란된 빛을 다시 집약시키는 시간 역행 거울 개발
우리 대학 물리학과 박용근 교수 연구팀이 빛을 거꾸로 반사시켜 시간이 역행하는 것처럼 보이는 시간 역행 거울을 개발했다.
연구 성과는 물리학분야 학술지인 ‘피지컬 리뷰 레터스(Physical Review Letters)’ 10월 6일자 온라인 판에 게재됐다.
빛의 시간 역행성은 녹화된 비디오를 되감기하듯 빛의 진행을 되돌릴 수 있는 개념을 뜻한다. 이는 마치 쏟은 물을 주워 담는 것과 같이 흩뿌려진 빛을 다시 집약시켜 산란 전의 영상을 복구하는 것과 같은 원리이다.
빛의 시간 역행 실현을 위해선 특별한 거울이 필요했다. 이론상으로만 제안되었던 이 시간 역행 거울(위상 공액 거울)은 빛이 거울에 부딪혔을 때 부딪쳐 온 방향으로 빛이 반사돼 원래 상태로 돌아가는 특성을 갖는다.
많은 학자들이 비선형 레이저 광학 지식을 이용해 시간 역행 거울을 구현하려 노력했다. 하지만 이 특수한 현상의 실현을 위해선 일반적인 거울과 다르게 추가적인 입사 레이저광이 필요하고 주변 환경에 극도로 민감하다는 한계가 있었다.
연구팀은 문제 해결을 위해 기존 복잡한 시도와 반대로 일반 거울에서의 반사를 재해석해 활용했다.
연구팀은 파면제어기라 불리는 수많은 미세 거울로 이루어진 장치를 활용했다. 파면제어기는 입사하는 빛의 모양에 맞춰 거울의 표면을 변경시켜 평행 상태로 만드는 원리인데, 이를 통해 복잡한 물리현상의 도입 없이도 빛의 시간 역행 거울을 구현하는데 성공했다.
또한 연구팀은 구현된 시간 역행 거울을 활용해 모의 생체조직 샘플, 생 닭가슴살 등에 의해 심하게 산란된 빛을 집약시켜 산란 전의 모양으로 재현했다.
연구팀에 의해 구현된 시간 역행 거울은 그 구현방법이 쉽고 주변환경의 영향을 받지 않아 빠른 시일 내에 실제 응용에 접목할 수 있을 것으로 예상된다.
논문의 1저자인 이겨레 박사과정은 “이 기술을 활용하면 기존 생체조직에서 심한 산란으로 인해 불가능했던 생체조직 내부의 빛 집약이 가능하다” 며 “향후 무절개 암 수술 등 미래기술의 기반기술이 될 수 있다”고 말했다.
또한 박 교수는 “이번 기술은 빛 뿐 아니라 소리, 전자파, 라디오 등 일반적인 파동에서 성립하는 개념이다”며 “향후 레이저 및 광통신 기술을 포함한 물리학, 광학, 의학 등 다양한 분야에 응용될 것으로 기대된다”고 말했다.
□ 그림 설명
그림 1. 생체조직,닭가슴살,광섬유를 산란체로 활용한 뒤 시간역행 거울로 원래 이미지를 구현한 사진
그림 2. 일반거울과 시간역행거울의 원리
2015.10.07 조회수 13656 빛을 이용한 실리카 구조체 가공 기술 개발
우리 대학 생명화학공학과 김희탁 교수, 박정기 교수 공동 연구팀이 단순한 빛 조사만으로 실리카(유리)와 같은 단단한 세라믹 구조체의 모양을 정교하게 제어할 수 있는 기술을 개발했다.
이번 연구 성과는 재료과학분야의 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 9월 21일자 온라인판에 게재됐다.
실리카 구조체는 유기물 구조체에 비해 고온, 고압 및 바이오 물질과의 안정성이 좋고 내화학성, 투명성 등이 높아 미세 유체칩 내부 채널, 태양전지 기판 등에 폭넓게 이용되고 있다.
그러나 실리카 특유의 높은 경도 때문에 실리카 구조체의 모양과 크기를 변화시키기 어려웠다. 특히 나노 스케일 구조 가공은 매우 어려운 것으로 여겨졌다.
연구팀은 문제 해결을 위해 아조 분자(질소 원자 두 개가 이중 결합된 아조기 양 끝에 벤젠링이 결합된 형태의 분자)를 이용했다. 아조 분자는 빛을 받았을 때 빛의 방향과 나란히 배열돼 편광 방향과 동일한 방향으로 움직이는 특성을 갖는다. 이를 응용하면 아조 분자와 결합된 실리카 전구체 분자가 빛의 방향에 따라 움직이는 특성을 갖게 된다.
연구팀은 이 아조 분자와 결합된 실리카 전구체를 용액-마이크로 임프린팅 기법의 잉크로 사용해 도장처럼 찍혀 나오듯 정해진 패턴의 형태로 제작했다.
이후 제작된 물질을 빛으로 가공한 뒤 열처리 하면 아조 분자가 포함된 유기물이 열분해돼 사라지게 된다. 결과적으로 무기물 전구체들만 남아 반응해 유리 구조체가 완성되는 것이다.
이 방법을 통해 30나노미터 이하 크기의 나노 구조를 갖는 대 면적 실리카 구조체를 제작했다. 또한 원형의 홀에 빛을 조사해 타원형의 홀 및 기둥 구조를 구현했다.
연구팀은 개발된 기술이 초소수성 기판, 미세유체칩 내의 미세채널 등 물리적 및 화학적 내구성이 요구되는 소자에 광범위하게 응용될 수 있을 것이라고 밝혔다.
김 교수는 “기존에 없었던 새로운 방식의 실리카 구조체 가공 방법을 개발했다”며 “세라믹을 나노 영역에서 다양한 형태로 구조 가공이 가능한 최초의 방식이다”고 말했다.
강홍석 박사 후 연구원이 1저자로 참여한 이번 연구는 한국연구재단의 일반연구자사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 빛 조사 및 열처리를 통해 원형형태의 구조체로부터 타원형태의 실리카 구조체 제작
그림 2. 광학 사진 이미지. 전자현미경 사진을 통해 실리카 전구제 구조 변형 및 실리카 구조체 제작 확인
그림 3. 빛을 이용해 실리카 전구체 구조 가공 및 열처리를 통한 실리카 구조체 제작과정
2015.10.06 조회수 13859
빛을 이용한 실리카 구조체 가공 기술 개발
우리 대학 생명화학공학과 김희탁 교수, 박정기 교수 공동 연구팀이 단순한 빛 조사만으로 실리카(유리)와 같은 단단한 세라믹 구조체의 모양을 정교하게 제어할 수 있는 기술을 개발했다.
이번 연구 성과는 재료과학분야의 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 9월 21일자 온라인판에 게재됐다.
실리카 구조체는 유기물 구조체에 비해 고온, 고압 및 바이오 물질과의 안정성이 좋고 내화학성, 투명성 등이 높아 미세 유체칩 내부 채널, 태양전지 기판 등에 폭넓게 이용되고 있다.
그러나 실리카 특유의 높은 경도 때문에 실리카 구조체의 모양과 크기를 변화시키기 어려웠다. 특히 나노 스케일 구조 가공은 매우 어려운 것으로 여겨졌다.
연구팀은 문제 해결을 위해 아조 분자(질소 원자 두 개가 이중 결합된 아조기 양 끝에 벤젠링이 결합된 형태의 분자)를 이용했다. 아조 분자는 빛을 받았을 때 빛의 방향과 나란히 배열돼 편광 방향과 동일한 방향으로 움직이는 특성을 갖는다. 이를 응용하면 아조 분자와 결합된 실리카 전구체 분자가 빛의 방향에 따라 움직이는 특성을 갖게 된다.
연구팀은 이 아조 분자와 결합된 실리카 전구체를 용액-마이크로 임프린팅 기법의 잉크로 사용해 도장처럼 찍혀 나오듯 정해진 패턴의 형태로 제작했다.
이후 제작된 물질을 빛으로 가공한 뒤 열처리 하면 아조 분자가 포함된 유기물이 열분해돼 사라지게 된다. 결과적으로 무기물 전구체들만 남아 반응해 유리 구조체가 완성되는 것이다.
이 방법을 통해 30나노미터 이하 크기의 나노 구조를 갖는 대 면적 실리카 구조체를 제작했다. 또한 원형의 홀에 빛을 조사해 타원형의 홀 및 기둥 구조를 구현했다.
연구팀은 개발된 기술이 초소수성 기판, 미세유체칩 내의 미세채널 등 물리적 및 화학적 내구성이 요구되는 소자에 광범위하게 응용될 수 있을 것이라고 밝혔다.
김 교수는 “기존에 없었던 새로운 방식의 실리카 구조체 가공 방법을 개발했다”며 “세라믹을 나노 영역에서 다양한 형태로 구조 가공이 가능한 최초의 방식이다”고 말했다.
강홍석 박사 후 연구원이 1저자로 참여한 이번 연구는 한국연구재단의 일반연구자사업의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 빛 조사 및 열처리를 통해 원형형태의 구조체로부터 타원형태의 실리카 구조체 제작
그림 2. 광학 사진 이미지. 전자현미경 사진을 통해 실리카 전구제 구조 변형 및 실리카 구조체 제작 확인
그림 3. 빛을 이용해 실리카 전구체 구조 가공 및 열처리를 통한 실리카 구조체 제작과정
2015.10.06 조회수 13859 수학 통해 생체시계 유지 원리 60여년 만에 밝혀
김 재 경 교수
우리 대학 수리과학과 김재경 교수가 미분방정식을 이용한 수학적 모델링을 통해 온도 변화에도 생체시계의 속도를 유지하는 원리를 발견했다.
이번 연구는 저명 학술지 셀(Cell) 자매지 몰라큘러 셀(Molecular Cell) 10월 1일자에 게재됐다.
우리 뇌에 위치한 생체시계는 밤 9시 경이 되면 멜라토닌 분비가 시작되게 하고 아침 7시 경에 멈추게 한다. 그로 인해 우리는 매일 일정한 시간에 잠을 자고 기상할 수 있다.
생체시계는 온도가 변화해도 빨라지거나 느려지지 않고 일정한 속도가 유지된다. 따라서 우리의 체온이 변화해도 규칙적인 삶을 살 수 있고, 이는 환경에 따라 체온이 변하는 변온 동물에게도 적용된다.
이러한 생체시계의 성질은 1954년에 발견됐지만 그 원리는 밝혀지지 않아 지난 60여 년간 생체시계 분야의 가장 큰 미스테리로 남아 있었다.
김 교수는 수학 모델링을 통해 이 원리를 밝혀냈고 모델링 결과는 듀크-싱가폴 국립 의과대학 데이빗 벌쉽(David Virshup) 교수 연구팀의 실험을 통해 검증돼 60년의 난제가 풀렸다.
생체시계에는 Period2라는 핵심 단백질이 존재한다. 이 단백질은 12시간 동안 증가하고 나머지 12시간 동안 분해되는 리듬을 평생 반복한다.
김 교수는 이 Period2 분해가 두 가지 방법으로 발생하는 것을 밝혔다. 하나는 매우 빠른 속도로 분해가 일어나는 것이고 나머지 하나는 매우 느린 속도로 분해가 이뤄지는 것이다. 그리고 두 가지 방법의 비율을 조절하는 것이 Period2에 존재하는 인산화 스위치(Phosphoryltion switch)이다.
인산화 스위치의 역할은 온도가 올라갔을 때 느리게 분해되는 Period2의 양을 늘림으로써 전체적인 분해 속도가 천천히 이뤄지게 만든다. 반대로 온도가 내려갔을 때는 빠르게 분해되는 비율을 늘려 생체시계의 속도를 조절하는 것이다.
결국 생체시계 속도 유지의 핵심은 인산화 스위치이고, 다른 생화학 반응이 빨라져도 생체시계의 속도 유지를 가능하게 만드는 요소인 것이다.
이번 연구에서 밝혀진 인산화 스위치는 생체시계의 속도를 조절할 수 있는 핵심 요소가 될 전망이다. 이 인산화 스위치를 조절할 수 있는 약을 개발한다면 잦은 해외 출장으로 인한 시차, 주야 교대 근무 등에 의한 생체 시계 고장 예방 등에 기여할 수 있을 것으로 기대된다.
김 교수는 “이번 성과를 통해 우리나라에선 아직은 부족한 생물학과 수학의 교류가 활발해지길 기대한다”며 “수학이 생물학의 난제들을 해결하는데 기여할 수 있음을 알리고 싶다”고 말했다.
이번 연구는 듀크-국립 싱가폴 의과 대학 데이빗 벌쉽 (David Virshup) 교수 연구팀, 미국 미시간 대학 (University of Michigan, Ann Arbor) 데니 폴저 (Daniel Forger) 교수와의 공동연구로 진행됐다.
□ 그림 설명
그림 1 . 이번 연구에서 밝혀진 인산화 스위치와 그 과정에서 사용된 수학 방정식의 일부
그림 2. Period2 단백질이 인산화 스위치에 의해 낮은 온도(30도) 에서 분해되는 속도가 더 빨라진다는 것을 보여주는 실험
2015.10.05 조회수 18953
수학 통해 생체시계 유지 원리 60여년 만에 밝혀
김 재 경 교수
우리 대학 수리과학과 김재경 교수가 미분방정식을 이용한 수학적 모델링을 통해 온도 변화에도 생체시계의 속도를 유지하는 원리를 발견했다.
이번 연구는 저명 학술지 셀(Cell) 자매지 몰라큘러 셀(Molecular Cell) 10월 1일자에 게재됐다.
우리 뇌에 위치한 생체시계는 밤 9시 경이 되면 멜라토닌 분비가 시작되게 하고 아침 7시 경에 멈추게 한다. 그로 인해 우리는 매일 일정한 시간에 잠을 자고 기상할 수 있다.
생체시계는 온도가 변화해도 빨라지거나 느려지지 않고 일정한 속도가 유지된다. 따라서 우리의 체온이 변화해도 규칙적인 삶을 살 수 있고, 이는 환경에 따라 체온이 변하는 변온 동물에게도 적용된다.
이러한 생체시계의 성질은 1954년에 발견됐지만 그 원리는 밝혀지지 않아 지난 60여 년간 생체시계 분야의 가장 큰 미스테리로 남아 있었다.
김 교수는 수학 모델링을 통해 이 원리를 밝혀냈고 모델링 결과는 듀크-싱가폴 국립 의과대학 데이빗 벌쉽(David Virshup) 교수 연구팀의 실험을 통해 검증돼 60년의 난제가 풀렸다.
생체시계에는 Period2라는 핵심 단백질이 존재한다. 이 단백질은 12시간 동안 증가하고 나머지 12시간 동안 분해되는 리듬을 평생 반복한다.
김 교수는 이 Period2 분해가 두 가지 방법으로 발생하는 것을 밝혔다. 하나는 매우 빠른 속도로 분해가 일어나는 것이고 나머지 하나는 매우 느린 속도로 분해가 이뤄지는 것이다. 그리고 두 가지 방법의 비율을 조절하는 것이 Period2에 존재하는 인산화 스위치(Phosphoryltion switch)이다.
인산화 스위치의 역할은 온도가 올라갔을 때 느리게 분해되는 Period2의 양을 늘림으로써 전체적인 분해 속도가 천천히 이뤄지게 만든다. 반대로 온도가 내려갔을 때는 빠르게 분해되는 비율을 늘려 생체시계의 속도를 조절하는 것이다.
결국 생체시계 속도 유지의 핵심은 인산화 스위치이고, 다른 생화학 반응이 빨라져도 생체시계의 속도 유지를 가능하게 만드는 요소인 것이다.
이번 연구에서 밝혀진 인산화 스위치는 생체시계의 속도를 조절할 수 있는 핵심 요소가 될 전망이다. 이 인산화 스위치를 조절할 수 있는 약을 개발한다면 잦은 해외 출장으로 인한 시차, 주야 교대 근무 등에 의한 생체 시계 고장 예방 등에 기여할 수 있을 것으로 기대된다.
김 교수는 “이번 성과를 통해 우리나라에선 아직은 부족한 생물학과 수학의 교류가 활발해지길 기대한다”며 “수학이 생물학의 난제들을 해결하는데 기여할 수 있음을 알리고 싶다”고 말했다.
이번 연구는 듀크-국립 싱가폴 의과 대학 데이빗 벌쉽 (David Virshup) 교수 연구팀, 미국 미시간 대학 (University of Michigan, Ann Arbor) 데니 폴저 (Daniel Forger) 교수와의 공동연구로 진행됐다.
□ 그림 설명
그림 1 . 이번 연구에서 밝혀진 인산화 스위치와 그 과정에서 사용된 수학 방정식의 일부
그림 2. Period2 단백질이 인산화 스위치에 의해 낮은 온도(30도) 에서 분해되는 속도가 더 빨라진다는 것을 보여주는 실험
2015.10.05 조회수 18953 바이오부탄올 핵심생산효소 구조 및 특성 규명
이 상 엽 특훈교수
우리 대학 생명화학공학과 이상엽 교수 연구팀이 경북대학교 김경진 교수 연구팀과의 공동연구를 통해 친환경 차세대 에너지인 바이오부탄올의 핵심 생산 효소인 싸이올레이즈(Thiolase)의 구조 및 특성을 규명했다.
연구 결과는 네이처 커뮤니케이션즈(Nature Communications) 9월 22일자 온라인 판에 게재됐다.
바이오부탄올은 바이오연료로 이미 사용되고 있는 바이오에탄올을 능가할 수 있는 친환경 차세대 수송용 바이오연료로 각광받고 있다.
바이오부탄올의 에너지 밀도는 리터당 29.2MJ(메가줄)로 바이오에탄올(19.6MJ)보다 48% 이상 높고 휘발유(32MJ)와 큰 차이가 없다. 또한 폐목재, 볏짚, 잉여 사탕수수, 해조류 등 비식용 바이오매스에서 추출하기 때문에 식량파동 등에서도 자유롭다.
바이오부탄올의 가장 큰 장점은 휘발유와 비교했을 때 공기연료비, 기화열, 옥탄가 등 연료 성능이 비슷해 현재 자동차 등에 사용되고 있는 가솔린 엔진을 그대로 사용할 수 있다는 점이다.
바이오부탄올은 클로스트리듐이라는 미생물로부터 생산이 가능하지만 클로스트리듐의 주요 효소의 구조 및 기작 등에 대한 연구는 체계적으로 이뤄지지 못했다.
이 교수 연구팀은 이 미생물의 성능 향상을 위해 바이오부탄올 생합성에 필요한 주요 효소 중 하나인 싸이올레이즈의 3차원 입체구조를 포항방사광가속기를 이용해 규명했다.
이를 통해 일반적인 미생물의 효소에서는 발견되지 않고 클로스트리듐 내의 싸이올레이즈에서만 관찰되는 산화-환원 스위치 구조를 발견했다.
또한 가상세포모델 등을 활용한 시스템대사공학 기법을 활용해 이 싸이올레이즈가 실제 미생물 내에서 산화-환원의 스위치로 작동한다는 것을 증명했다.
연구팀은 밝혀낸 싸이올레이즈 구조의 원천기술을 활용해 활성이 향상된 돌연변이 효소를 설계했다. 그리고 이를 이용해 바이오부탄올 생산 미생물의 대사회로를 조작해 바이오부탄올 생합성이 향상되는 결과를 얻었다.
이상엽 교수는 “바이오부탄올 생합성 대사회로에서 가장 중요한 효소의 구조와 작용 기작을 세계 최초로 밝혔다”며 “싸이올레이즈 관련 원천기술을 활용해 바이오부탄올을 더욱 경제적으로 생산할 수 있는 대사회로 구축에 응용하겠다”고 말했다.
김상우, 장유신, 하성철 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단의 기후변화대응기술개발사업 및 글로벌프런티어 차세대바이오매스사업단 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 바이오부탄올 생산 효소(thiolase)의 구조 및 산화-환원 스위치 작용기작
그림 2. 바이오부탄올 생산을 위한 포도당 대사회로에서 바이오부탄올 생산 효소(thiolase)의 산화-환원 스위치 작용기작
2015.09.22 조회수 18792
바이오부탄올 핵심생산효소 구조 및 특성 규명
이 상 엽 특훈교수
우리 대학 생명화학공학과 이상엽 교수 연구팀이 경북대학교 김경진 교수 연구팀과의 공동연구를 통해 친환경 차세대 에너지인 바이오부탄올의 핵심 생산 효소인 싸이올레이즈(Thiolase)의 구조 및 특성을 규명했다.
연구 결과는 네이처 커뮤니케이션즈(Nature Communications) 9월 22일자 온라인 판에 게재됐다.
바이오부탄올은 바이오연료로 이미 사용되고 있는 바이오에탄올을 능가할 수 있는 친환경 차세대 수송용 바이오연료로 각광받고 있다.
바이오부탄올의 에너지 밀도는 리터당 29.2MJ(메가줄)로 바이오에탄올(19.6MJ)보다 48% 이상 높고 휘발유(32MJ)와 큰 차이가 없다. 또한 폐목재, 볏짚, 잉여 사탕수수, 해조류 등 비식용 바이오매스에서 추출하기 때문에 식량파동 등에서도 자유롭다.
바이오부탄올의 가장 큰 장점은 휘발유와 비교했을 때 공기연료비, 기화열, 옥탄가 등 연료 성능이 비슷해 현재 자동차 등에 사용되고 있는 가솔린 엔진을 그대로 사용할 수 있다는 점이다.
바이오부탄올은 클로스트리듐이라는 미생물로부터 생산이 가능하지만 클로스트리듐의 주요 효소의 구조 및 기작 등에 대한 연구는 체계적으로 이뤄지지 못했다.
이 교수 연구팀은 이 미생물의 성능 향상을 위해 바이오부탄올 생합성에 필요한 주요 효소 중 하나인 싸이올레이즈의 3차원 입체구조를 포항방사광가속기를 이용해 규명했다.
이를 통해 일반적인 미생물의 효소에서는 발견되지 않고 클로스트리듐 내의 싸이올레이즈에서만 관찰되는 산화-환원 스위치 구조를 발견했다.
또한 가상세포모델 등을 활용한 시스템대사공학 기법을 활용해 이 싸이올레이즈가 실제 미생물 내에서 산화-환원의 스위치로 작동한다는 것을 증명했다.
연구팀은 밝혀낸 싸이올레이즈 구조의 원천기술을 활용해 활성이 향상된 돌연변이 효소를 설계했다. 그리고 이를 이용해 바이오부탄올 생산 미생물의 대사회로를 조작해 바이오부탄올 생합성이 향상되는 결과를 얻었다.
이상엽 교수는 “바이오부탄올 생합성 대사회로에서 가장 중요한 효소의 구조와 작용 기작을 세계 최초로 밝혔다”며 “싸이올레이즈 관련 원천기술을 활용해 바이오부탄올을 더욱 경제적으로 생산할 수 있는 대사회로 구축에 응용하겠다”고 말했다.
김상우, 장유신, 하성철 박사가 공동 1저자로 참여한 이번 연구는 미래창조과학부와 한국연구재단의 기후변화대응기술개발사업 및 글로벌프런티어 차세대바이오매스사업단 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 바이오부탄올 생산 효소(thiolase)의 구조 및 산화-환원 스위치 작용기작
그림 2. 바이오부탄올 생산을 위한 포도당 대사회로에서 바이오부탄올 생산 효소(thiolase)의 산화-환원 스위치 작용기작
2015.09.22 조회수 18792