%ED%99%94%ED%95%99%EA%B3%B5%ED%95%99%EA%B3%BC
-
 양승만 교수, 인조오팔로부터 초소형 분광분석기 제조
- Advanced Materials 3월 5일자 표지 논문으로 소개 돼 - 초정밀 극미량 물질 인식센서로 활용
오팔은 크기가 수백 나노미터(머리카락 굵기의 약 100 분의 1정도)의 유리구슬이 차곡차곡 쌓여 있는 것으로서, 그것이 아름다운 색을 띄는 것은 오팔이 선택적으로 반사하는 파장영역대의 빛만을 우리가 볼 수 있기 때문이다. 이렇게 오팔보석이 발산하는 아름다운 색깔은 색소에 의한 것이 아니라 이 물질을 이루는 구조가 규칙적인 나노구조로 되어 있기 때문이며 이러한 구조를 광결정이라 한다. 이러한 구조의 광결정은 특정한 파장 영역대의 빛만을 완전히 선택적으로 반사시키는 기능을 보유하게 된다.
생명화학공학과 양승만 교수팀 (광자유체집적소자 창의연구단)은 파장이 서로 다른 빛들을 반사하는 오팔 광결정을 미세소자에 연속적으로 도입하여 무지개 같은 띠 모양으로 제작할 수 있는 기술을 확보했으며 이를 이용해 극미량의 물질을 정밀하게 분석할 수 있는 칩 크기 수준의 미세분광기를 최근 제조했다.
사람마다 고유한 지문을 갖듯이 물질을 이루는 분자도 고유한 지문을 갖는데 이는 분자마다 특정 파장의 빛만을 선택적으로 흡수하거나 방출하는 독특한 스펙트럼을 갖기 때문이다.
따라서, 물질을 구성하는 분자를 광학적으로 인식하기 위해서는 분광분석기 (spectrometer)라는 기기가 필요하며 이는 물질이 갖고 있는 다양한 광정보 처리를 위해 광자소자 및 분석소자를 구성하는데 꼭 필요한 요소 중 하나이다.
그러나 기존의 분광기는 파장에 따른 빛의 공간적 분할을 위한 격자(grating) 및 빛의 진행에 필요한 공간을 요구하므로 고가의 큰 장치로만 제작이 가능하였다.
최근에 많은 주목을 받고 있는 생명공학의 산업적 이용이나 신약개발을 위해서는 부피가 나노리터(10-9L)~펨토리터(10-15L) 정도의 극미량의 샘플을 처리해야 하므로 분석실험실을 반도체 칩과 같이 초소형화한 소위 ‘칩위의 실험실: Lab on a Chip’이 필연적으로 요구된다.
이를 구현하기 위해서는 칩 내부에 분광분석기와 같은 분석소자를 설계해 도입해야 하나 기존의 기술로는 현실적으로 불가능 했다.
이번 연구 결과는 초소형 분석소자의 실용성을 구현하는데 크게 기여한 점을 인정받아 국제적 저명학술지인 어드밴스드 머티리얼스(Advanced Materials) 3월호 표지논문(cover paper)으로 게재됐다. 또한, 나노기술 분야의 세계적 포털사이트인 Nanowerk (http://www.nanowerk.com/)는 이번 연구결과를 ‘광결정으로 미세 분광기를 만들다(Photonic crystals allow the fabrication of miniaturized spectrometers)’라는 제목의 스포트라이트(Spotlight)로 소개하기도 했다.
칩규모의 초소형 물질감지소자는 세계적인 연구그룹들이 활발히 개발 중이다. 이번 연구의 결과는 초소형 분광분석기 구조를 자기조립법으로 만든 최초의 사례로서 이 분야의 국제경쟁에서 우위를 확보하는데 필요한 핵심요소이다.
그림1. 반사색이 연속적으로 변하는 광결정 분광기의 저배율 및 고배율 사진 (분광기가 손톱크기로 초소형화 되었음을 확인할 수 있다)
기본 원리는 아래 그림과 같이 다른 반사스펙트럼을 갖는 콜로이드 광결정을 패턴화하면 미지의 빛이 입사할 경우 반사하는 빛의 세기만을 통해 입사한 미지의 빛의 스펙트럼을 알아낼 수 있다는 것이다.
이러한 아름다운 반사색을 보이는 광결정은 오팔보석, 공작새 깃털, 나비날개, 딱정벌레 등 자연계에 많이 존재하는데 양 교수 연구팀에서는 이를 규칙적으로 패턴화하여 전체 가시광 영역에서 배열한 것이다. 이러한 광결정을 이용하면 공간에 따른 빛의 세기분포를 파장에 따른 빛의 세기분포 즉 스펙트럼으로 물질을 이루는 분자를 재분석해낼 수 있다. 이는 기존의 분광기와는 달리 긴 진행거리를 요구하지 않기 때문에 소형화가 가능하고 신호의 검출은 미세검출기 배열을 통해 가능할 것으로 예상된다.
그림2. 가시광 영역에서 반사스펙트럼을 갖는 콜로이드 광결정 (내부의 나노구조는 나비날개와 공작새 깃털 구조의 광결정와 유사하다)
<용어설명>○ 콜로이드 : 물질의 분산상태를 나타내는 것인데, 보통의 분자나 이온보다 크고 지름이 1nm~100nm 정도의 미립자가 기체 또는 액체 중에 분산된 것은 콜로이드 상태라고 부른다. 예를 들어, 생물체를 구성하는 물질 대부분이 콜로이드 상태로 존재한다.
2010.03.16 조회수 26740
양승만 교수, 인조오팔로부터 초소형 분광분석기 제조
- Advanced Materials 3월 5일자 표지 논문으로 소개 돼 - 초정밀 극미량 물질 인식센서로 활용
오팔은 크기가 수백 나노미터(머리카락 굵기의 약 100 분의 1정도)의 유리구슬이 차곡차곡 쌓여 있는 것으로서, 그것이 아름다운 색을 띄는 것은 오팔이 선택적으로 반사하는 파장영역대의 빛만을 우리가 볼 수 있기 때문이다. 이렇게 오팔보석이 발산하는 아름다운 색깔은 색소에 의한 것이 아니라 이 물질을 이루는 구조가 규칙적인 나노구조로 되어 있기 때문이며 이러한 구조를 광결정이라 한다. 이러한 구조의 광결정은 특정한 파장 영역대의 빛만을 완전히 선택적으로 반사시키는 기능을 보유하게 된다.
생명화학공학과 양승만 교수팀 (광자유체집적소자 창의연구단)은 파장이 서로 다른 빛들을 반사하는 오팔 광결정을 미세소자에 연속적으로 도입하여 무지개 같은 띠 모양으로 제작할 수 있는 기술을 확보했으며 이를 이용해 극미량의 물질을 정밀하게 분석할 수 있는 칩 크기 수준의 미세분광기를 최근 제조했다.
사람마다 고유한 지문을 갖듯이 물질을 이루는 분자도 고유한 지문을 갖는데 이는 분자마다 특정 파장의 빛만을 선택적으로 흡수하거나 방출하는 독특한 스펙트럼을 갖기 때문이다.
따라서, 물질을 구성하는 분자를 광학적으로 인식하기 위해서는 분광분석기 (spectrometer)라는 기기가 필요하며 이는 물질이 갖고 있는 다양한 광정보 처리를 위해 광자소자 및 분석소자를 구성하는데 꼭 필요한 요소 중 하나이다.
그러나 기존의 분광기는 파장에 따른 빛의 공간적 분할을 위한 격자(grating) 및 빛의 진행에 필요한 공간을 요구하므로 고가의 큰 장치로만 제작이 가능하였다.
최근에 많은 주목을 받고 있는 생명공학의 산업적 이용이나 신약개발을 위해서는 부피가 나노리터(10-9L)~펨토리터(10-15L) 정도의 극미량의 샘플을 처리해야 하므로 분석실험실을 반도체 칩과 같이 초소형화한 소위 ‘칩위의 실험실: Lab on a Chip’이 필연적으로 요구된다.
이를 구현하기 위해서는 칩 내부에 분광분석기와 같은 분석소자를 설계해 도입해야 하나 기존의 기술로는 현실적으로 불가능 했다.
이번 연구 결과는 초소형 분석소자의 실용성을 구현하는데 크게 기여한 점을 인정받아 국제적 저명학술지인 어드밴스드 머티리얼스(Advanced Materials) 3월호 표지논문(cover paper)으로 게재됐다. 또한, 나노기술 분야의 세계적 포털사이트인 Nanowerk (http://www.nanowerk.com/)는 이번 연구결과를 ‘광결정으로 미세 분광기를 만들다(Photonic crystals allow the fabrication of miniaturized spectrometers)’라는 제목의 스포트라이트(Spotlight)로 소개하기도 했다.
칩규모의 초소형 물질감지소자는 세계적인 연구그룹들이 활발히 개발 중이다. 이번 연구의 결과는 초소형 분광분석기 구조를 자기조립법으로 만든 최초의 사례로서 이 분야의 국제경쟁에서 우위를 확보하는데 필요한 핵심요소이다.
그림1. 반사색이 연속적으로 변하는 광결정 분광기의 저배율 및 고배율 사진 (분광기가 손톱크기로 초소형화 되었음을 확인할 수 있다)
기본 원리는 아래 그림과 같이 다른 반사스펙트럼을 갖는 콜로이드 광결정을 패턴화하면 미지의 빛이 입사할 경우 반사하는 빛의 세기만을 통해 입사한 미지의 빛의 스펙트럼을 알아낼 수 있다는 것이다.
이러한 아름다운 반사색을 보이는 광결정은 오팔보석, 공작새 깃털, 나비날개, 딱정벌레 등 자연계에 많이 존재하는데 양 교수 연구팀에서는 이를 규칙적으로 패턴화하여 전체 가시광 영역에서 배열한 것이다. 이러한 광결정을 이용하면 공간에 따른 빛의 세기분포를 파장에 따른 빛의 세기분포 즉 스펙트럼으로 물질을 이루는 분자를 재분석해낼 수 있다. 이는 기존의 분광기와는 달리 긴 진행거리를 요구하지 않기 때문에 소형화가 가능하고 신호의 검출은 미세검출기 배열을 통해 가능할 것으로 예상된다.
그림2. 가시광 영역에서 반사스펙트럼을 갖는 콜로이드 광결정 (내부의 나노구조는 나비날개와 공작새 깃털 구조의 광결정와 유사하다)
<용어설명>○ 콜로이드 : 물질의 분산상태를 나타내는 것인데, 보통의 분자나 이온보다 크고 지름이 1nm~100nm 정도의 미립자가 기체 또는 액체 중에 분산된 것은 콜로이드 상태라고 부른다. 예를 들어, 생물체를 구성하는 물질 대부분이 콜로이드 상태로 존재한다.
2010.03.16 조회수 26740 -
 가상세포를 이용한 병원균의 약물표적 예측기술 개발
- 가상세포 시스템 활용한 새로운 항생제 개발에 큰 파급효과 기대
- 분자 바이오시스템(Molecular BioSystems)지 표지 논문으로 게재
생명화학공학과 이상엽(李相燁, 46세, LG화학 석좌교수, 생명과학기술대학 학장)특훈교수팀이 항생제에 내성을 가지는 병원성 미생물의 가상세포를 구축하고 이를 이용해 병원균의 성장을 효과적으로 억제할 수 있는 약물 표적을 예측하는 기술을 최근 개발했다.
김현욱(생명화학공학과 박사과정)연구원의 학위 논문연구로 수행한 이번 연구 결과는 유럽 화학 관련 학술단체 RSC(The Royal Society of Chemistry)에서 발간하는 분자 바이오시스템(Molecular BioSystems)지의 2월호 표지 논문으로 게재됐다.
예전에는 병원성 세균들을 항생제로 쉽게 치유할 수 있었지만 이제는 항생제의 오남용으로 인해서 병원균들은 항생제에 대한 내성을 가지게 됐으며, 따라서 한 번 감염이 되면 치유가 이전보다 쉽지 않다.
그 대표적인 병원균이 바로 아시네토박터 바우마니(Acinetobacter baumannaii)다. 본래 흙이나 물에서 쉽게 발견되는 이 미생물은 항생제에 내성을 갖지 않아 치료가 쉽고 건강한 사람은 잘 감염되지 않는 균이었다. 그러나 지난 10년 동안에 항생제에 내성을 갖는 슈퍼박테리아로 변했으며, 이라크 전쟁에 참전한 다수의 미군과 프랑스군도 이 균에 감염되면서 상처가 낫질 않아 많은 희생을 야기했다.
李 교수 연구팀은 아시네토박터 바우마니의 게놈과 전체적인 대사특성을 알아보기 위해 각종 데이터베이스에 산재해 있는 생물정보와 문헌정보를 컴퓨터에 입력, 분석, 디자인하여 가상세포를 구축하고, 다양한 네트워크 분석기법, 필수 대사반응 및 대사산물 분석 등 융합 방법론을 이용해 이 병원균의 성장을 효과적으로 차단할 수 있는 약물표적을 예측했다. 인간에게는 영향을 미치지 않으면서 병원균에게만 작용하는 최종 약물표적들이다.
필수 대사반응은 생명체가 대사활동을 정상적으로 하기 위하여 반드시 필요한 효소반응을 말하며, 필수 대사산물이란 생명체가 생존하기 위해 대사에 반드시 필요로 하는 화학물질로서 이들을 제거할 경우 이와 반응을 하는 효소들을 모두 억제되는 효과가 있다.
이 약물표적은 가상세포를 구성하고 있는 대사 유전자, 효소 반응, 신진대사들의 기능을 짧은 시간 안에 빠짐없이 체계적으로 검토해 예측함으로써 그 신뢰성을 높였다.
이번 연구 결과는 최근 많은 관심을 받고 있는 시스템 생물학 연구기법을 이용하여, 처음으로 필수 대사물질의 체계적인 발굴을 통해 효과적인 약물표적을 찾고, 나아가 새로운 항생제 개발의 가능성을 열었다는 점에서 높이 평가받고 있다. 또한 병원균에 의한 감염 현상과 신약개발에 큰 공헌을 할 것으로 기대를 모으고 있다.
李 교수는 “현재 수많은 생물의 게놈 정보가 쏟아지고 있지만 이것을 실질적으로 유용한 정보로 전환하는 데에는 아직도 많은 어려움이 있다. 아시네토박토 바우마니의 게놈 정보로부터 의학적으로 실용성이 있는 정보를 재생산했다는 점에서 의의가 있다”며 “특히 이 병원균의 가상세포 개발은 특정 환경에서 필수 유전자나 효소 반응에 대한 대량의 새로운 생물정보를 제공할 수 있는 계기를 마련했다.”고 말했다.
李 교수팀은 교육과학기술부 시스템 생물학 연구개발사업의 지원으로 이번 연구를 수행했으며, 다양한 병원성 균주의 가상세포 개발 및 항생제 약물표적 예측 방법을 특허 출원했다.
▣ 용어설명 ○ 약물표적 : 차단 시 병원성 미생물의 성장을 효과적으로 억제할 수 있는 단백질 효소 및 그와 관련된 화학물질
▣ (자료1) 가상세포.
(자료2) 가상세포로부터 필수대사산물을 예측한 후에, 병원균을 가장 효과적으로 죽일 수 있으면서 동시에 인간에게는 영향을 미치지 않는 약물표적만을 추리는 과정
2010.02.18 조회수 19303
가상세포를 이용한 병원균의 약물표적 예측기술 개발
- 가상세포 시스템 활용한 새로운 항생제 개발에 큰 파급효과 기대
- 분자 바이오시스템(Molecular BioSystems)지 표지 논문으로 게재
생명화학공학과 이상엽(李相燁, 46세, LG화학 석좌교수, 생명과학기술대학 학장)특훈교수팀이 항생제에 내성을 가지는 병원성 미생물의 가상세포를 구축하고 이를 이용해 병원균의 성장을 효과적으로 억제할 수 있는 약물 표적을 예측하는 기술을 최근 개발했다.
김현욱(생명화학공학과 박사과정)연구원의 학위 논문연구로 수행한 이번 연구 결과는 유럽 화학 관련 학술단체 RSC(The Royal Society of Chemistry)에서 발간하는 분자 바이오시스템(Molecular BioSystems)지의 2월호 표지 논문으로 게재됐다.
예전에는 병원성 세균들을 항생제로 쉽게 치유할 수 있었지만 이제는 항생제의 오남용으로 인해서 병원균들은 항생제에 대한 내성을 가지게 됐으며, 따라서 한 번 감염이 되면 치유가 이전보다 쉽지 않다.
그 대표적인 병원균이 바로 아시네토박터 바우마니(Acinetobacter baumannaii)다. 본래 흙이나 물에서 쉽게 발견되는 이 미생물은 항생제에 내성을 갖지 않아 치료가 쉽고 건강한 사람은 잘 감염되지 않는 균이었다. 그러나 지난 10년 동안에 항생제에 내성을 갖는 슈퍼박테리아로 변했으며, 이라크 전쟁에 참전한 다수의 미군과 프랑스군도 이 균에 감염되면서 상처가 낫질 않아 많은 희생을 야기했다.
李 교수 연구팀은 아시네토박터 바우마니의 게놈과 전체적인 대사특성을 알아보기 위해 각종 데이터베이스에 산재해 있는 생물정보와 문헌정보를 컴퓨터에 입력, 분석, 디자인하여 가상세포를 구축하고, 다양한 네트워크 분석기법, 필수 대사반응 및 대사산물 분석 등 융합 방법론을 이용해 이 병원균의 성장을 효과적으로 차단할 수 있는 약물표적을 예측했다. 인간에게는 영향을 미치지 않으면서 병원균에게만 작용하는 최종 약물표적들이다.
필수 대사반응은 생명체가 대사활동을 정상적으로 하기 위하여 반드시 필요한 효소반응을 말하며, 필수 대사산물이란 생명체가 생존하기 위해 대사에 반드시 필요로 하는 화학물질로서 이들을 제거할 경우 이와 반응을 하는 효소들을 모두 억제되는 효과가 있다.
이 약물표적은 가상세포를 구성하고 있는 대사 유전자, 효소 반응, 신진대사들의 기능을 짧은 시간 안에 빠짐없이 체계적으로 검토해 예측함으로써 그 신뢰성을 높였다.
이번 연구 결과는 최근 많은 관심을 받고 있는 시스템 생물학 연구기법을 이용하여, 처음으로 필수 대사물질의 체계적인 발굴을 통해 효과적인 약물표적을 찾고, 나아가 새로운 항생제 개발의 가능성을 열었다는 점에서 높이 평가받고 있다. 또한 병원균에 의한 감염 현상과 신약개발에 큰 공헌을 할 것으로 기대를 모으고 있다.
李 교수는 “현재 수많은 생물의 게놈 정보가 쏟아지고 있지만 이것을 실질적으로 유용한 정보로 전환하는 데에는 아직도 많은 어려움이 있다. 아시네토박토 바우마니의 게놈 정보로부터 의학적으로 실용성이 있는 정보를 재생산했다는 점에서 의의가 있다”며 “특히 이 병원균의 가상세포 개발은 특정 환경에서 필수 유전자나 효소 반응에 대한 대량의 새로운 생물정보를 제공할 수 있는 계기를 마련했다.”고 말했다.
李 교수팀은 교육과학기술부 시스템 생물학 연구개발사업의 지원으로 이번 연구를 수행했으며, 다양한 병원성 균주의 가상세포 개발 및 항생제 약물표적 예측 방법을 특허 출원했다.
▣ 용어설명 ○ 약물표적 : 차단 시 병원성 미생물의 성장을 효과적으로 억제할 수 있는 단백질 효소 및 그와 관련된 화학물질
▣ (자료1) 가상세포.
(자료2) 가상세포로부터 필수대사산물을 예측한 후에, 병원균을 가장 효과적으로 죽일 수 있으면서 동시에 인간에게는 영향을 미치지 않는 약물표적만을 추리는 과정
2010.02.18 조회수 19303 -
 홍원희교수팀, 다양한 나노구조유도 기술개발
생명화학공학과 홍원희교수팀, 이온성액체를 이용한 다양한 나노구조 유도 기술 개발
-무기산화물, 탄소나노튜브, 그래펜, 유무기 하이브리드 등 다양한 재료의 나노구조를 유도--상용 산화철보다 10배 이상의 흡착 및 광촉매 효율 높여-
공과대학 생명화학공학과 홍원희 교수팀(62)은 이온성액체를 이용한 자기조립기술을 이용해 탄소나노튜브, 그래펜, 무기산화물, 유무기 복합체에 이르기까지 다양한 재료의 나노구조를 유도할 수 있는 기술을 최근 개발했다.
이 연구결과는 ‘광촉매 응용을 위한 이온성액체를 이용한 무기산화물 하이브리드의 에너지 전달(Energy Transfer in Ionic-Liquid-Functionalized Inorganic Nanorods for Highly Efficient Photocatalytic Applications)’이라는 제목으로 나노분야의 저명 학술지인 스몰(Small)지에 지난 11월 게재됐다.
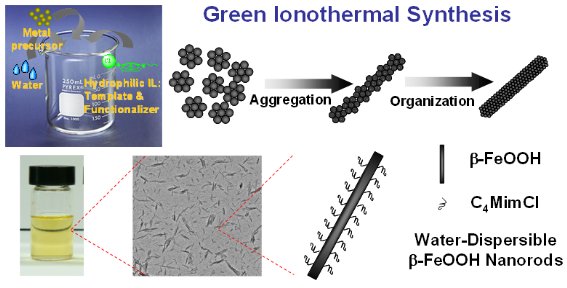
이 기술은 이온성 액체의 구조 유도와 용매 기능을 이용한 무기산화물 하이브리드 나노재료를 제조할 수 있는 ‘청정 한 반응기 이온열 합성법(Green One-Pot Ionothermal Synthesis)’이다. 대기압하의 열린반응기내에서 제조된 무기산화물 나노재료는 쉽게 물이나 다양한 유기 용매에서 분산된다.
홍교수팀은 이 합성법을 산화철 계열의 무기산화물 나노재료에까지 적용해 0차원에서 1차원에 이르기까지 구조를 제어했고, 계면에서의 에너지 전이현상을 통해 상용 산화철보다 10배 이상의 흡착 및 광촉매 효율을 높였다.
이 기술을 바탕으로 제조된 나노재료는 유기물 산화 및 분해기능이 뛰어나 태양광만으로 폐수처리가 가능하다. 이로써 페수처리 과정에서 에너지 소비와 이산화탄소의 배출량을 줄일 수 있고, 광촉매가 가지는 우수한 항균 및 탈취기능은 건축재료 분야에 응용될 것으로 기대된다. 또한, 태양광을 이용한 물의 광분해로 수소 에너지원 생산도 가능하다.
홍교수는 “이번 연구는 이온성 액체의 청정용매로써의 기능을 이용해 나노기술이 가지는 인간과 환경에 대한 악영향을 감소시키고, 동시에 디자인된 나노재료에 새로운 기능을 부여해 기존 기술의 한계를 극복할 수 있는 새로운 대안을 마련했다”는데 의미가 있다고 말했다.
현재 홍교수팀은 친환경 합성법으로 제조된 무기산화물, 탄소나노튜브, 그래펜, 유.무기 하이브리등의 나노재료를 환경 및 에너지 분야에 적용하는 연구를 진행하고 있다.
※ 보충자료나노 스케일에서의 재료나 현상을 연구하고 구조나 구성 요소를 제어해서 새로운 소재‧소자‧시스템을 개발하는 나노 기술 역시, 환경 유해성이나 인체 독성에 대한 연구 결과가 발표되면서 친환경 기술에 대한 관심이 급증하고 있다.
이온성 액체는 소금과 같이 양이온과 음이온의 이온결합으로 이루어진 이온성 염 화합물로써 상온에서부터 넓은 온도에 걸쳐 액체로 존재할 수 있는 ‘청정용매(Green Solvent)’라고 불리면서 각광을 받고 있다. 특히, 이론적으로 1018가지 정도의 조합에 의해서 비휘발성, 비가연성, 열적 안정성, 높은 이온전도도, 전기화학적 안정성, 높은 끓는점 등의 물리화학적 특성을 쉽게 변화시킬 수 있어서 다기능성(multifunctional) ‘디자이너용매(Designer Solvent)’로 사용가능하다.
세계적으로 아직 초기단계이긴 하지만, 미국 국방관련 연구소 (US Air Force, US Naval Research Laboratory) 및 국가 연구소 (Argonne 연구소, Oak Ridge 연구소, Brookhaven 연구소), 독일의 Max Planck 연구소, 스위스 EPFL의 Gratzel 그룹, 일본의 도쿄대, G24i & BASF 등이 최근 이온성 액체를 이용한 나노기술 응용 분야에 주목하면서 집중 투자와 연구를 진행하고 있는 반면, 국내에서는 아직 시작 단계에 불과할 정도로 뒤쳐져 있다.
홍 교수 팀의 연구결과는 기존 산업뿐만 아니라, 전 세계적으로 주목 받고 있는 ‘녹색 성장기술’과 21세기를 선도할 ‘첨단 나노기술’을 융합한 ‘청정 나노기술(Green Nanotechnolgy)’의 원천기술로써 활용될 수 있으며 이 분야의 국제경쟁에서 우위를 확보할 수 있을 것으로 전망된다.
현재까지 이온성액체는 유기합성, 전기화학, 화학공학, 생물공학 및 분리공정 등을 포함하는 여러 분야에서 유기 용매를 대체하기 위한 ‘지속가능기술(sustainable technology)’로써 향후 산업 전 분야에 걸쳐서 엄청난 파급효과가 있을 것으로 기대되고 있다.
※ 용어설명 ○ 열린반응기 : 고압,저압의 용기가 아닌 대기압하의 일반용기 즉, 비이커 등.
<그림1> 대표적인 이미다졸륨계 이온성액체의 분자 구조
<그림2> Green One-Pot Ionothermal Synthesis에 의한 물에 분산되는 산화철 나노 막대기의 합성 과정 모식도.
2009.12.14 조회수 31211
홍원희교수팀, 다양한 나노구조유도 기술개발
생명화학공학과 홍원희교수팀, 이온성액체를 이용한 다양한 나노구조 유도 기술 개발
-무기산화물, 탄소나노튜브, 그래펜, 유무기 하이브리드 등 다양한 재료의 나노구조를 유도--상용 산화철보다 10배 이상의 흡착 및 광촉매 효율 높여-
공과대학 생명화학공학과 홍원희 교수팀(62)은 이온성액체를 이용한 자기조립기술을 이용해 탄소나노튜브, 그래펜, 무기산화물, 유무기 복합체에 이르기까지 다양한 재료의 나노구조를 유도할 수 있는 기술을 최근 개발했다.
이 연구결과는 ‘광촉매 응용을 위한 이온성액체를 이용한 무기산화물 하이브리드의 에너지 전달(Energy Transfer in Ionic-Liquid-Functionalized Inorganic Nanorods for Highly Efficient Photocatalytic Applications)’이라는 제목으로 나노분야의 저명 학술지인 스몰(Small)지에 지난 11월 게재됐다.
이 기술은 이온성 액체의 구조 유도와 용매 기능을 이용한 무기산화물 하이브리드 나노재료를 제조할 수 있는 ‘청정 한 반응기 이온열 합성법(Green One-Pot Ionothermal Synthesis)’이다. 대기압하의 열린반응기내에서 제조된 무기산화물 나노재료는 쉽게 물이나 다양한 유기 용매에서 분산된다.
홍교수팀은 이 합성법을 산화철 계열의 무기산화물 나노재료에까지 적용해 0차원에서 1차원에 이르기까지 구조를 제어했고, 계면에서의 에너지 전이현상을 통해 상용 산화철보다 10배 이상의 흡착 및 광촉매 효율을 높였다.
이 기술을 바탕으로 제조된 나노재료는 유기물 산화 및 분해기능이 뛰어나 태양광만으로 폐수처리가 가능하다. 이로써 페수처리 과정에서 에너지 소비와 이산화탄소의 배출량을 줄일 수 있고, 광촉매가 가지는 우수한 항균 및 탈취기능은 건축재료 분야에 응용될 것으로 기대된다. 또한, 태양광을 이용한 물의 광분해로 수소 에너지원 생산도 가능하다.
홍교수는 “이번 연구는 이온성 액체의 청정용매로써의 기능을 이용해 나노기술이 가지는 인간과 환경에 대한 악영향을 감소시키고, 동시에 디자인된 나노재료에 새로운 기능을 부여해 기존 기술의 한계를 극복할 수 있는 새로운 대안을 마련했다”는데 의미가 있다고 말했다.
현재 홍교수팀은 친환경 합성법으로 제조된 무기산화물, 탄소나노튜브, 그래펜, 유.무기 하이브리등의 나노재료를 환경 및 에너지 분야에 적용하는 연구를 진행하고 있다.
※ 보충자료나노 스케일에서의 재료나 현상을 연구하고 구조나 구성 요소를 제어해서 새로운 소재‧소자‧시스템을 개발하는 나노 기술 역시, 환경 유해성이나 인체 독성에 대한 연구 결과가 발표되면서 친환경 기술에 대한 관심이 급증하고 있다.
이온성 액체는 소금과 같이 양이온과 음이온의 이온결합으로 이루어진 이온성 염 화합물로써 상온에서부터 넓은 온도에 걸쳐 액체로 존재할 수 있는 ‘청정용매(Green Solvent)’라고 불리면서 각광을 받고 있다. 특히, 이론적으로 1018가지 정도의 조합에 의해서 비휘발성, 비가연성, 열적 안정성, 높은 이온전도도, 전기화학적 안정성, 높은 끓는점 등의 물리화학적 특성을 쉽게 변화시킬 수 있어서 다기능성(multifunctional) ‘디자이너용매(Designer Solvent)’로 사용가능하다.
세계적으로 아직 초기단계이긴 하지만, 미국 국방관련 연구소 (US Air Force, US Naval Research Laboratory) 및 국가 연구소 (Argonne 연구소, Oak Ridge 연구소, Brookhaven 연구소), 독일의 Max Planck 연구소, 스위스 EPFL의 Gratzel 그룹, 일본의 도쿄대, G24i & BASF 등이 최근 이온성 액체를 이용한 나노기술 응용 분야에 주목하면서 집중 투자와 연구를 진행하고 있는 반면, 국내에서는 아직 시작 단계에 불과할 정도로 뒤쳐져 있다.
홍 교수 팀의 연구결과는 기존 산업뿐만 아니라, 전 세계적으로 주목 받고 있는 ‘녹색 성장기술’과 21세기를 선도할 ‘첨단 나노기술’을 융합한 ‘청정 나노기술(Green Nanotechnolgy)’의 원천기술로써 활용될 수 있으며 이 분야의 국제경쟁에서 우위를 확보할 수 있을 것으로 전망된다.
현재까지 이온성액체는 유기합성, 전기화학, 화학공학, 생물공학 및 분리공정 등을 포함하는 여러 분야에서 유기 용매를 대체하기 위한 ‘지속가능기술(sustainable technology)’로써 향후 산업 전 분야에 걸쳐서 엄청난 파급효과가 있을 것으로 기대되고 있다.
※ 용어설명 ○ 열린반응기 : 고압,저압의 용기가 아닌 대기압하의 일반용기 즉, 비이커 등.
<그림1> 대표적인 이미다졸륨계 이온성액체의 분자 구조
<그림2> Green One-Pot Ionothermal Synthesis에 의한 물에 분산되는 산화철 나노 막대기의 합성 과정 모식도.
2009.12.14 조회수 31211 -
 대사공학적으로 개량된 박테리아로 범용 플라스틱 생산기술 개발
- 이상엽 교수팀과 LG 화학 연구팀 공동개발
- 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지 게재예정
생명화학공학과 이상엽(李相燁, 45세, LG화학 석좌교수, 생명과학기술대학 학장) 특훈교수팀과 LG화학 기술연구원(원장 유진녕) 박시재, 양택호박사팀이 4년여 간의 공동연구를 통해 박테리아를 이용하여 재생 가능한 바이오매스로부터 플라스틱을 생산하는 기술을 최근 개발했다.
교육과학기술부 시스템생물학 연구개발 사업과 LG화학 석좌교수 연구비로 지원된 이번 연구에서는 시스템 대사공학과 효소공학 기법을 접목, 자연적으로는 생성되지 않는 플라스틱(unnatural polymer)의 일종으로 최근 각광을 받고 있는 폴리유산(Polylactic acid, PLA)을 효율적으로 생산할 수 있는 대장균을 개발한 것이다.
이번 연구 결과는 바이오공학 분야 최고 전통의 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지에 게재 승인됐으며 스포트라이트 논문(Spotlight paper)으로 선정돼 2010년 1월호에 두 편의 연속 논문으로 게재될 예정이다.
두 논문의 제목은 ‘개량된 프로피오네이트 코엔자임 에이 트랜스퍼레이즈와 폴리하이드록시알카노에이트 중합효소를 이용한 폴리유산과 그의 공중합체의 생합성(Biosynthesis of Polylactic acid and its Copolymers Using Evolved Propionate CoA Transferase and PHA Synthase)’과 ‘폴리유산과 그의 공중합체의 생산을 위한 대장균의 대사공학(Metabolic Engineering of Escherichia coli for the Production of Polylactic Acid and its Copolymers)’이다. 19건의 특허가 전 세계 출원 중이다.
기존의 복잡한 2단계 공정을 통해 생산되던 폴리유산을 재생가능한 원료로부터 미생물의 직접 발효에 의해 생산이 가능하도록 한 혁신적인 본 연구 전략은 앞으로 석유 유래 플라스틱을 대체할 수 있는 다양한 비자연 고분자(unnatural polymer)들의 생산에 활용될 획기적인 기술로 평가되고 있다.
폴리유산 (Polylactic acid, PLA)은 많은 바이오매스 유래 고분자들 중에서도 생분해성, 생체적합성, 구조적 안정성, 그리고 낮은 독성과 같은 뛰어난 물성으로 인해 석유 유래 플라스틱의 대체물로서 대두되고 있다.
그러나, 폴리유산은 현재 두 단계 공정으로 합성된다. 우선, 미생물 발효를 통해 유산(락트산, Lactic acid)을 생산, 정제한 후 여러 가지 시약, 용매 및 촉매가 첨가되는 복잡한 공정의 화학적 중합반응에 의해 폴리유산이 합성된다.
또한, 폴리유산의 물성을 다양하게 개선하기 위해 폴리하이드록시알카노에이트 (Polyhydroxyalkanoate, PHA)와 같은 다른 고분자들과의 공중합이나 혼합반응 등의 연구가 이루어지고 있다.
이러한 노력에도 불구하고, 공중합 반응에 사용되는 락톤계 모노머들의 가용성과 비용을 고려했을 때, 기존의 화학적 합성 방법은 효과적이지 않다. 이에, 미생물 유래 고분자인 폴리하이드록시알카노에이트의 생합성 시스템을 기반으로, 폴리유산과 그의 공중합체들의 생합성이 가능할 수 있는 대사경로를 효소공학을 통해 구축했다.
그러나, 외래 대사경로의 도입 및 조작만으로는 폴리유산 단일 중합체와 유산의 함량이 높은 공중합체의 생산이 효율적이지 않아, 시스템 수준으로 세포 내 대사흐름을 증가시킬 필요성을 인지했다. 이에, 대장균 균주의 인실리코 게놈 수준의 시뮬레이션을 이용한 대사흐름분석 기법을 활용하여 고분자 생산을 위한 주요 전구체의 대사 흐름을 논리적으로 강화시킴으로써, 세포성장과 함께 목적 고분자의 효율적 생산이 가능하도록 했다.
따라서, 효소공학을 통한 고분자 합성 경로의 직접적 조작 및 강화 뿐 아니라, 시스템 대사공학을 통한 논리적 접근으로 조작된 대사흐름을 바탕으로 다양한 폴리유산 플라스틱을 보다 효율적으로 생산할 수 있었다.
이는 시스템 대사공학과 효소공학을 접목시킨 고기술 전략으로 비자연 고분자를 효율적으로 생산한 최초의 성공적인 예로서, 재생가능한 자원으로부터 폴리유산뿐 아니라 석유유래 플라스틱을 대체할 수 있는 다른 비자연 고분자들의 일단계 생산을 위한 기반 기술을 마련해줌으로써, 플라스틱 생산 공정에 있어 새로운 전략을 제시했다.
李 교수는 “자연계에 없는 고분자를 미생물로 생산하는 것이 과연 될까? 라는 의문을 갖고 시작했다. 우리 KAIST 연구실의 정유경박사와 LG화학 기술연구원 연구팀원 10여명이 4년간의 끈질긴 노력 끝에 성공했다”며, “이번 연구는 대장균의 가상세포 시뮬레이션을 통해 세포 내 대사흐름을 목적한 고분자 생산에 유리하도록 논리적으로 조작하고, 고분자 생합성 경로를 구성하는 외래 효소들을 새롭게 만들어 도입함으로써, 강화된 대사흐름을 이용해 보다 효율적으로 목적 고분자를 생산할 수 있는 균주를 개발하는데 성공한 세계 첫 번째 케이스다. 특히, 유산이 단량체로 함유된 공중합체의 경우에는 세계최초로 만든 것이 되어 물질특허들로 출원중이다”라고 밝혔다.
한편, 이 혁신적인 연구 성과는 22일 미국 CNN 홈페이지의 Top기사 등 해외언론의 주요기사로 소개됐다. 주요내용은 한국의 KAIST 이상엽 교수팀과 LG화학 연구팀이 전 세계적으로 석유고갈, 지구온난화 및 환경오염 문제로 재생가능한 자원을 이용한 바이오매스 기반 기술의 개발이 시급한 현 시대의 흐름에 부응하면서, 재생가능한 자원으로부터 효율적으로 바이오공학을 통한 플라스틱 (Bioengineered plastics) 폴리유산의 생산이 가능한 대장균 균주를 개발했다는 내용이다.
2009.11.24 조회수 26729
대사공학적으로 개량된 박테리아로 범용 플라스틱 생산기술 개발
- 이상엽 교수팀과 LG 화학 연구팀 공동개발
- 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지 게재예정
생명화학공학과 이상엽(李相燁, 45세, LG화학 석좌교수, 생명과학기술대학 학장) 특훈교수팀과 LG화학 기술연구원(원장 유진녕) 박시재, 양택호박사팀이 4년여 간의 공동연구를 통해 박테리아를 이용하여 재생 가능한 바이오매스로부터 플라스틱을 생산하는 기술을 최근 개발했다.
교육과학기술부 시스템생물학 연구개발 사업과 LG화학 석좌교수 연구비로 지원된 이번 연구에서는 시스템 대사공학과 효소공학 기법을 접목, 자연적으로는 생성되지 않는 플라스틱(unnatural polymer)의 일종으로 최근 각광을 받고 있는 폴리유산(Polylactic acid, PLA)을 효율적으로 생산할 수 있는 대장균을 개발한 것이다.
이번 연구 결과는 바이오공학 분야 최고 전통의 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지에 게재 승인됐으며 스포트라이트 논문(Spotlight paper)으로 선정돼 2010년 1월호에 두 편의 연속 논문으로 게재될 예정이다.
두 논문의 제목은 ‘개량된 프로피오네이트 코엔자임 에이 트랜스퍼레이즈와 폴리하이드록시알카노에이트 중합효소를 이용한 폴리유산과 그의 공중합체의 생합성(Biosynthesis of Polylactic acid and its Copolymers Using Evolved Propionate CoA Transferase and PHA Synthase)’과 ‘폴리유산과 그의 공중합체의 생산을 위한 대장균의 대사공학(Metabolic Engineering of Escherichia coli for the Production of Polylactic Acid and its Copolymers)’이다. 19건의 특허가 전 세계 출원 중이다.
기존의 복잡한 2단계 공정을 통해 생산되던 폴리유산을 재생가능한 원료로부터 미생물의 직접 발효에 의해 생산이 가능하도록 한 혁신적인 본 연구 전략은 앞으로 석유 유래 플라스틱을 대체할 수 있는 다양한 비자연 고분자(unnatural polymer)들의 생산에 활용될 획기적인 기술로 평가되고 있다.
폴리유산 (Polylactic acid, PLA)은 많은 바이오매스 유래 고분자들 중에서도 생분해성, 생체적합성, 구조적 안정성, 그리고 낮은 독성과 같은 뛰어난 물성으로 인해 석유 유래 플라스틱의 대체물로서 대두되고 있다.
그러나, 폴리유산은 현재 두 단계 공정으로 합성된다. 우선, 미생물 발효를 통해 유산(락트산, Lactic acid)을 생산, 정제한 후 여러 가지 시약, 용매 및 촉매가 첨가되는 복잡한 공정의 화학적 중합반응에 의해 폴리유산이 합성된다.
또한, 폴리유산의 물성을 다양하게 개선하기 위해 폴리하이드록시알카노에이트 (Polyhydroxyalkanoate, PHA)와 같은 다른 고분자들과의 공중합이나 혼합반응 등의 연구가 이루어지고 있다.
이러한 노력에도 불구하고, 공중합 반응에 사용되는 락톤계 모노머들의 가용성과 비용을 고려했을 때, 기존의 화학적 합성 방법은 효과적이지 않다. 이에, 미생물 유래 고분자인 폴리하이드록시알카노에이트의 생합성 시스템을 기반으로, 폴리유산과 그의 공중합체들의 생합성이 가능할 수 있는 대사경로를 효소공학을 통해 구축했다.
그러나, 외래 대사경로의 도입 및 조작만으로는 폴리유산 단일 중합체와 유산의 함량이 높은 공중합체의 생산이 효율적이지 않아, 시스템 수준으로 세포 내 대사흐름을 증가시킬 필요성을 인지했다. 이에, 대장균 균주의 인실리코 게놈 수준의 시뮬레이션을 이용한 대사흐름분석 기법을 활용하여 고분자 생산을 위한 주요 전구체의 대사 흐름을 논리적으로 강화시킴으로써, 세포성장과 함께 목적 고분자의 효율적 생산이 가능하도록 했다.
따라서, 효소공학을 통한 고분자 합성 경로의 직접적 조작 및 강화 뿐 아니라, 시스템 대사공학을 통한 논리적 접근으로 조작된 대사흐름을 바탕으로 다양한 폴리유산 플라스틱을 보다 효율적으로 생산할 수 있었다.
이는 시스템 대사공학과 효소공학을 접목시킨 고기술 전략으로 비자연 고분자를 효율적으로 생산한 최초의 성공적인 예로서, 재생가능한 자원으로부터 폴리유산뿐 아니라 석유유래 플라스틱을 대체할 수 있는 다른 비자연 고분자들의 일단계 생산을 위한 기반 기술을 마련해줌으로써, 플라스틱 생산 공정에 있어 새로운 전략을 제시했다.
李 교수는 “자연계에 없는 고분자를 미생물로 생산하는 것이 과연 될까? 라는 의문을 갖고 시작했다. 우리 KAIST 연구실의 정유경박사와 LG화학 기술연구원 연구팀원 10여명이 4년간의 끈질긴 노력 끝에 성공했다”며, “이번 연구는 대장균의 가상세포 시뮬레이션을 통해 세포 내 대사흐름을 목적한 고분자 생산에 유리하도록 논리적으로 조작하고, 고분자 생합성 경로를 구성하는 외래 효소들을 새롭게 만들어 도입함으로써, 강화된 대사흐름을 이용해 보다 효율적으로 목적 고분자를 생산할 수 있는 균주를 개발하는데 성공한 세계 첫 번째 케이스다. 특히, 유산이 단량체로 함유된 공중합체의 경우에는 세계최초로 만든 것이 되어 물질특허들로 출원중이다”라고 밝혔다.
한편, 이 혁신적인 연구 성과는 22일 미국 CNN 홈페이지의 Top기사 등 해외언론의 주요기사로 소개됐다. 주요내용은 한국의 KAIST 이상엽 교수팀과 LG화학 연구팀이 전 세계적으로 석유고갈, 지구온난화 및 환경오염 문제로 재생가능한 자원을 이용한 바이오매스 기반 기술의 개발이 시급한 현 시대의 흐름에 부응하면서, 재생가능한 자원으로부터 효율적으로 바이오공학을 통한 플라스틱 (Bioengineered plastics) 폴리유산의 생산이 가능한 대장균 균주를 개발했다는 내용이다.
2009.11.24 조회수 26729 -
 양승만 교수, 액체 방울을 이용한 초소형 인조곤충눈 구조 제조
- 초정밀 극미량 물질 인식센서로 활용 - 네이처 포토닉스에서‘미세패턴기술-광자돔’이라는 제목의 하이라이트로 소개
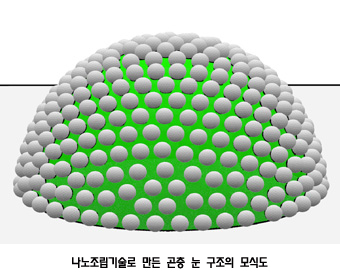
곤충 및 갑각류 등의 눈은 포유류의 눈과는 달리 수백~수만개의 홑눈(또는 낱눈)이 모여 생긴 겹눈 구조를 갖고 있다. 각각의 홑눈은 투명한 볼록렌즈로서 빛을 모아 명암, 색깔(파장)과 같은 빛 정보를 뇌에 전해 주며 뇌에서 전달된 정보를 재조합하여 사물을 감지한다. 각 홑눈은 육방밀집구조로 서로 빈틈없이 배열되어 돔 형태의 겹눈 표면을 메우고 있다. (파리와 잠자리의 눈 사진참조)
생명화학공학과 양승만 교수의 광자유체집적소자 창의연구단은 다양한 기능을 갖는 나노입자를 제조하고 이들 입자들이 스스로 조립되는 자기조립 원리를 규명하는 연구를 수행하여 실제 곤충눈의 수백분의 일 크기의 초소형 인조겹눈구조를 실용적으로 제조할 수 있는 방법을 최근 개발했다.
이 연구결과는 최근 국제적 저명학술지인 어드밴스드 머티리얼스(Advanced Materials) 誌 10월호 표지논문(cover paper)으로 게재 됐으며 인조곤충눈 구조의 실용성을 구현하는데 크게 기여한다고 인정받아 특별히 주목해야할 논문(Advances in Advance)으로 선정됐다.
특히, 네이처 포토닉스(Nature Photonics)지는 10월호에서 양 교수팀 연구의 중요성과 응용성에 주목하여 이 연구결과를 "미세패턴기술-광자돔(Micropatterning–Photonic domes)"이라는 제목으로 "뉴스와 논평(News & Views)"란에 하이라이트로 선정하여 비중있게 게재했다.
지난 20여 년 동안 곤충눈, 오팔, 나비날개 등 빛정보를 처리할 수 있는 자연계에 존재하는 구조를 인공적으로 제조하기 위한 연구가 많은 과학자들에 의하여 시도되어 왔으나, 실용적인 구조를 얻는 데에는 한계가 있었다. 양 교수팀은 2006년부터 교육과학기술부의 ‘창의적연구진흥사업’으로부터 지원을 받아 초소형 인조곤충눈 구조를 실용적으로 제조할 수 있는 기술을 확보하기 위한 연구를 수행해 왔다.
Nature Photonics지 10월호가 하이라이트로 선정하여 주목한 양 교수팀의 이번연구에서는 실제 곤충눈 크기의 수백분의 일 정도로 초소형이며 균일한 크기와 모양을 갖는 인조곤충눈 구조를, 크기가 수십 마이크로미터인 균일한 기름방울을 이용하여 성공적으로 제조하여 규칙적으로 배열하였다. 특히 주목할 것은 제조공정이 손쉽고 빠른 나노구슬의 자기조립 원리를 이용한 점이다.
우선 크기가 수백 나노미터인 균일한 유리구슬(낱눈렌즈)을 물속에 분산시킨 후, 크기가 수십 마이크로미터인 균일한 기름방울을 주입하고 물-기름-유리구슬 사이의 표면화학적 힘의 균형을 유지시키면 유리구슬이 물과 기름방울 사이의 경계면으로 이동한다. 그 후 물-유리-기름방울의 혼합물을 기판 위에 뿌리면 기름방울이 반구의 돔 모양으로 변형되고 유리구슬렌즈는 저절로 기름방울 표면 위에 촘촘히 육방밀집구조로 배열하게 된다 (전자현미경사진 참조). 이 때 자외선을 기름방울에 쪼여서 고형화시킴으로써 종래에 수십 시간이 소요되는 인조곤충눈 조립공정을 불과 수분 만에 제조할 수 있다.
수 천개의 미세렌즈가 장착된 돔 구조의 초소형 인조곤충눈은 인간의 눈에 비해 시야각이 넓고 빛을 모으는 능력도 매우 높다. 따라서, 환경의 미세한 변화를 감지할 수 있는 능력을 보유하므로 신약개발을 비롯하여 극미량의 물질을 인식할 수 있는 초고감도 감지소자를 요구하는 다양한 분야에 응용될 수 있다.
특히 최근에 신약개발 등 바이오 산업의 실용화에 사용되고 있는 극미량의 시료를 처리할 수 있는 반도체칩 규모의 실험실인 랩언어칩(Lab on a Chip)에 초소형 인조곤충눈을 도입할 경우 높은 정밀도를 갖는 물질 감지소자로 활용될 수 있다.
이러한 인조곤충눈 구조는 세계적인 연구그룹들이 활발히 개발 중이며 최근에 수 밀리미터 크기의 실제 곤충눈 크기의 인조곤충눈은 보고된 바 있다. 그러나, 본 연구의 결과는 초소형 인공곤충눈 구조를 자기조립법으로 만든 최초의 사례로서 이 분야의 국제경쟁에서 우위를 확보하는데 필요한 핵심요소다.
2009.10.06 조회수 30024
양승만 교수, 액체 방울을 이용한 초소형 인조곤충눈 구조 제조
- 초정밀 극미량 물질 인식센서로 활용 - 네이처 포토닉스에서‘미세패턴기술-광자돔’이라는 제목의 하이라이트로 소개
곤충 및 갑각류 등의 눈은 포유류의 눈과는 달리 수백~수만개의 홑눈(또는 낱눈)이 모여 생긴 겹눈 구조를 갖고 있다. 각각의 홑눈은 투명한 볼록렌즈로서 빛을 모아 명암, 색깔(파장)과 같은 빛 정보를 뇌에 전해 주며 뇌에서 전달된 정보를 재조합하여 사물을 감지한다. 각 홑눈은 육방밀집구조로 서로 빈틈없이 배열되어 돔 형태의 겹눈 표면을 메우고 있다. (파리와 잠자리의 눈 사진참조)
생명화학공학과 양승만 교수의 광자유체집적소자 창의연구단은 다양한 기능을 갖는 나노입자를 제조하고 이들 입자들이 스스로 조립되는 자기조립 원리를 규명하는 연구를 수행하여 실제 곤충눈의 수백분의 일 크기의 초소형 인조겹눈구조를 실용적으로 제조할 수 있는 방법을 최근 개발했다.
이 연구결과는 최근 국제적 저명학술지인 어드밴스드 머티리얼스(Advanced Materials) 誌 10월호 표지논문(cover paper)으로 게재 됐으며 인조곤충눈 구조의 실용성을 구현하는데 크게 기여한다고 인정받아 특별히 주목해야할 논문(Advances in Advance)으로 선정됐다.
특히, 네이처 포토닉스(Nature Photonics)지는 10월호에서 양 교수팀 연구의 중요성과 응용성에 주목하여 이 연구결과를 "미세패턴기술-광자돔(Micropatterning–Photonic domes)"이라는 제목으로 "뉴스와 논평(News & Views)"란에 하이라이트로 선정하여 비중있게 게재했다.
지난 20여 년 동안 곤충눈, 오팔, 나비날개 등 빛정보를 처리할 수 있는 자연계에 존재하는 구조를 인공적으로 제조하기 위한 연구가 많은 과학자들에 의하여 시도되어 왔으나, 실용적인 구조를 얻는 데에는 한계가 있었다. 양 교수팀은 2006년부터 교육과학기술부의 ‘창의적연구진흥사업’으로부터 지원을 받아 초소형 인조곤충눈 구조를 실용적으로 제조할 수 있는 기술을 확보하기 위한 연구를 수행해 왔다.
Nature Photonics지 10월호가 하이라이트로 선정하여 주목한 양 교수팀의 이번연구에서는 실제 곤충눈 크기의 수백분의 일 정도로 초소형이며 균일한 크기와 모양을 갖는 인조곤충눈 구조를, 크기가 수십 마이크로미터인 균일한 기름방울을 이용하여 성공적으로 제조하여 규칙적으로 배열하였다. 특히 주목할 것은 제조공정이 손쉽고 빠른 나노구슬의 자기조립 원리를 이용한 점이다.
우선 크기가 수백 나노미터인 균일한 유리구슬(낱눈렌즈)을 물속에 분산시킨 후, 크기가 수십 마이크로미터인 균일한 기름방울을 주입하고 물-기름-유리구슬 사이의 표면화학적 힘의 균형을 유지시키면 유리구슬이 물과 기름방울 사이의 경계면으로 이동한다. 그 후 물-유리-기름방울의 혼합물을 기판 위에 뿌리면 기름방울이 반구의 돔 모양으로 변형되고 유리구슬렌즈는 저절로 기름방울 표면 위에 촘촘히 육방밀집구조로 배열하게 된다 (전자현미경사진 참조). 이 때 자외선을 기름방울에 쪼여서 고형화시킴으로써 종래에 수십 시간이 소요되는 인조곤충눈 조립공정을 불과 수분 만에 제조할 수 있다.
수 천개의 미세렌즈가 장착된 돔 구조의 초소형 인조곤충눈은 인간의 눈에 비해 시야각이 넓고 빛을 모으는 능력도 매우 높다. 따라서, 환경의 미세한 변화를 감지할 수 있는 능력을 보유하므로 신약개발을 비롯하여 극미량의 물질을 인식할 수 있는 초고감도 감지소자를 요구하는 다양한 분야에 응용될 수 있다.
특히 최근에 신약개발 등 바이오 산업의 실용화에 사용되고 있는 극미량의 시료를 처리할 수 있는 반도체칩 규모의 실험실인 랩언어칩(Lab on a Chip)에 초소형 인조곤충눈을 도입할 경우 높은 정밀도를 갖는 물질 감지소자로 활용될 수 있다.
이러한 인조곤충눈 구조는 세계적인 연구그룹들이 활발히 개발 중이며 최근에 수 밀리미터 크기의 실제 곤충눈 크기의 인조곤충눈은 보고된 바 있다. 그러나, 본 연구의 결과는 초소형 인공곤충눈 구조를 자기조립법으로 만든 최초의 사례로서 이 분야의 국제경쟁에서 우위를 확보하는데 필요한 핵심요소다.
2009.10.06 조회수 30024 -
 유룡 교수, 나노판상 제올라이트 촉매 물질 합성 성공
화학과 유룡(54)교수가 특수한 계면활성제 분자와 실리카를 조립하는 새로운 방법으로 세계 최초로 2나노미터(nm) 극미세 두께의 나노판상형 제올라이트 촉매 물질을 합성하는데 성공했다.
이 연구결과는 세계 최고 권위의 과학저널인 ‘네이처(Nature)지’ 10일자에 게재됐으며, 이 논문은 세계 과학계에서 저자의 위상과 연구결과의 과학적 중요성을 인정받아 네이처 인터뷰 기사로 소개되는 영예를 얻었다.
이번에 합성된 제올라이트는 2nm두께의 판상으로, 제올라이트 물질에 대해 이론적으로 예상할 수 있는 최소 두께다. 또한 이렇게 얇은 두께임에도 불구하고, 이 물질은 섭씨 700도의 고온에서도 높은 안정성을 나타냈다.
연구를 주도한 유교수는 “이처럼 극미세 두께의 제올라이트 물질은 분자가 얇은 층을 뚫고 쉽게 확산할 수 있기 때문에 석유화학공정에서 중질유 성분처럼 부피가 큰 분자를 반응시키는 촉매로 사용될 수 있다. 특히 이 제올라이트 촉매는 메탄올을 가솔린으로 전환시키는 화학공정에서 기존의 제올라이트 촉매에 비해 수명이 5배 이상 길어, 촉매 교체 주기를 연장시킬 수 있기 때문에 경제효과가 매우 높다.”라고 연구의의를 설명했다.
이번 연구결과는 앞으로 대체에너지 자원개발과 녹색성장에 적합한 친환경 고성능 촉매 개발연구에 직접적으로 활용될 수 있을 것으로 기대된다.
유교수팀이 독창적으로 설계한 계면활성제 분자는 머리 부분에 제올라이트 마이크로 기공(micropore)유도체를 포함하여 제올라이트 골격의 형성을 유도하고, 꼬리 부분에 긴 알킬(alkyl) 그룹이 연결되어 제올라이트의 마이크로 기공보다 더 큰 메조 기공(mesopore)을 규칙적으로 배열할 수 있도록 했다.
이러한 독창적인 물질 설계는 제올라이트 합성 메커니즘에 대한 과학적 지식을 넓히는 획기적인 연구 결과로서, 향후 다양한 구조의 다른 물질을 합성하는 새로운 분야를 개척한 선구적인 성과라고 평가할 수 있다.
유교수는 2000, 2001년에 국내 최초로 2년 연속 ‘Nature’지에 메조다공성 실리카와 메조다공성 탄소에 대한 논문을 게재했고, 2003년과 2006년에 ‘Nature Materials"지에 고분자-탄소 복합물질과 메조다공성 제올라이트에 관한 논문을 게재한 후, 이번에 세 번째로 ’Nature"지에 책임저자(교신저자)로 논문을 게재하는 쾌거를 올렸다. 이것은 국내 과학자도 세계 과학을 선도하는 그룹의 반열에 올랐다는 것을 의미하며, 우리나라 과학의 우수성을 전 세계에 알리는 기회가 됐다.
이 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 ‘국가과학자지원사업’의 지원을 받아 이뤄졌다. 또한 교육과학기술부와 한국연구재단이 추진하는 ‘세계수준의 연구중심대학(WCU, World Class University)육성사업’과 나노기술육성사업(나노팹사업)에 따른 결실이다. 이번 연구에서 유 교수팀은 KAIST 부설 나노팹센터와 테라사키교수 연구팀의 협조로, 전자현미경을 통해 물질의 세부구조를 분석하였다. 특히 나노팹의 높은 기술력은 연구시간을 최대로 단축시켜 단시간에 훌륭한 연구 성과를 도출할 수 있도록 했다.
2007년 국가과학자로 임명된 유교수의 주도 하에, KAIST 최민기 박사, 나경수연구원(화학과 박사과정), 김정남연구원(화학과 박사과정)이 연구를 수행하고, 분해능이 높은 현미경 사진으로 구조를 확인하기 위해 스웨덴 스톡홀름대학교의 오사무 테라사키 교수와 야수히로 사카모토 박사가 추가로 참여했다. 테라사키 교수는 현재 스웨덴 스톡홀름대학교 석좌교수로, WCU사업의 지원을 받아 올해부터 KAIST EEWS(Energy, Environment, Water and Sustainability)학과에 겸임교수로 재직하고 있다.
이번 연구결과는 세계 수준의 연구중심대학과 세계적인 나노과학기술 육성을 위한 정부의 지원으로, 우리나라 과학기술의 수준을 한 단계 발전시킨 결과로서, 국내 기술력과 해외 우수 연구자들의 연구능력과 기술력을 통합한 국제공동연구의 모범사례로 평가된다.
2009.09.10 조회수 28418
유룡 교수, 나노판상 제올라이트 촉매 물질 합성 성공
화학과 유룡(54)교수가 특수한 계면활성제 분자와 실리카를 조립하는 새로운 방법으로 세계 최초로 2나노미터(nm) 극미세 두께의 나노판상형 제올라이트 촉매 물질을 합성하는데 성공했다.
이 연구결과는 세계 최고 권위의 과학저널인 ‘네이처(Nature)지’ 10일자에 게재됐으며, 이 논문은 세계 과학계에서 저자의 위상과 연구결과의 과학적 중요성을 인정받아 네이처 인터뷰 기사로 소개되는 영예를 얻었다.
이번에 합성된 제올라이트는 2nm두께의 판상으로, 제올라이트 물질에 대해 이론적으로 예상할 수 있는 최소 두께다. 또한 이렇게 얇은 두께임에도 불구하고, 이 물질은 섭씨 700도의 고온에서도 높은 안정성을 나타냈다.
연구를 주도한 유교수는 “이처럼 극미세 두께의 제올라이트 물질은 분자가 얇은 층을 뚫고 쉽게 확산할 수 있기 때문에 석유화학공정에서 중질유 성분처럼 부피가 큰 분자를 반응시키는 촉매로 사용될 수 있다. 특히 이 제올라이트 촉매는 메탄올을 가솔린으로 전환시키는 화학공정에서 기존의 제올라이트 촉매에 비해 수명이 5배 이상 길어, 촉매 교체 주기를 연장시킬 수 있기 때문에 경제효과가 매우 높다.”라고 연구의의를 설명했다.
이번 연구결과는 앞으로 대체에너지 자원개발과 녹색성장에 적합한 친환경 고성능 촉매 개발연구에 직접적으로 활용될 수 있을 것으로 기대된다.
유교수팀이 독창적으로 설계한 계면활성제 분자는 머리 부분에 제올라이트 마이크로 기공(micropore)유도체를 포함하여 제올라이트 골격의 형성을 유도하고, 꼬리 부분에 긴 알킬(alkyl) 그룹이 연결되어 제올라이트의 마이크로 기공보다 더 큰 메조 기공(mesopore)을 규칙적으로 배열할 수 있도록 했다.
이러한 독창적인 물질 설계는 제올라이트 합성 메커니즘에 대한 과학적 지식을 넓히는 획기적인 연구 결과로서, 향후 다양한 구조의 다른 물질을 합성하는 새로운 분야를 개척한 선구적인 성과라고 평가할 수 있다.
유교수는 2000, 2001년에 국내 최초로 2년 연속 ‘Nature’지에 메조다공성 실리카와 메조다공성 탄소에 대한 논문을 게재했고, 2003년과 2006년에 ‘Nature Materials"지에 고분자-탄소 복합물질과 메조다공성 제올라이트에 관한 논문을 게재한 후, 이번에 세 번째로 ’Nature"지에 책임저자(교신저자)로 논문을 게재하는 쾌거를 올렸다. 이것은 국내 과학자도 세계 과학을 선도하는 그룹의 반열에 올랐다는 것을 의미하며, 우리나라 과학의 우수성을 전 세계에 알리는 기회가 됐다.
이 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 ‘국가과학자지원사업’의 지원을 받아 이뤄졌다. 또한 교육과학기술부와 한국연구재단이 추진하는 ‘세계수준의 연구중심대학(WCU, World Class University)육성사업’과 나노기술육성사업(나노팹사업)에 따른 결실이다. 이번 연구에서 유 교수팀은 KAIST 부설 나노팹센터와 테라사키교수 연구팀의 협조로, 전자현미경을 통해 물질의 세부구조를 분석하였다. 특히 나노팹의 높은 기술력은 연구시간을 최대로 단축시켜 단시간에 훌륭한 연구 성과를 도출할 수 있도록 했다.
2007년 국가과학자로 임명된 유교수의 주도 하에, KAIST 최민기 박사, 나경수연구원(화학과 박사과정), 김정남연구원(화학과 박사과정)이 연구를 수행하고, 분해능이 높은 현미경 사진으로 구조를 확인하기 위해 스웨덴 스톡홀름대학교의 오사무 테라사키 교수와 야수히로 사카모토 박사가 추가로 참여했다. 테라사키 교수는 현재 스웨덴 스톡홀름대학교 석좌교수로, WCU사업의 지원을 받아 올해부터 KAIST EEWS(Energy, Environment, Water and Sustainability)학과에 겸임교수로 재직하고 있다.
이번 연구결과는 세계 수준의 연구중심대학과 세계적인 나노과학기술 육성을 위한 정부의 지원으로, 우리나라 과학기술의 수준을 한 단계 발전시킨 결과로서, 국내 기술력과 해외 우수 연구자들의 연구능력과 기술력을 통합한 국제공동연구의 모범사례로 평가된다.
2009.09.10 조회수 28418 -
 이상엽 특훈교수팀, 대사공학기술로 바이오매스로부터 나일론 원료를 생산하는 녹색기술 개발
- 화석원료 기반의 화학산업에서 바이오 기반 녹색 화학산업으로 -
우리대학 생명화학공학과 이상엽 특훈교수(45, 생명과학기술대학 학장, 바이오융합연구소 공동소장, LG화학 석좌교수)팀이 대사공학 기술을 이용하여 대장균으로부터 나일론의 원료가 되는 다이아민(diamine)을 효율적으로 생산하는 시스템을 최근 개발했다.
이 연구결과는 미국 와일리-블랙웰(Wiley-Blackwell)사가 발간하는 가장 오랜 전통의 공학계열 생명공학 학술지인 바이오테크놀로지 바이오엔지니어링지(Biotechnology and Bioengineering) 27일자 온라인 판으로 소개됐다.
현재, 의약을 제외하고도 1,800조원 시장 규모의 화학 물질들은 주로 화석원료에 기반한 석유화학 공정으로 생산돼 왔다. 이 연구결과는 세계에서 처음으로 나일론 등의 원료로 쓰이는 1,4-다이아미노부탄 (1,4-diaminobutane), 일명 푸트레신 (putrescine)을 석유화학공정이 아닌 포도당이나 설탕과 같은 바이오매스 유래 원료로부터 대사공학으로 개량된 대장균을 이용하여 생산하는 기술을 제공하고 있다.
와일리(Wiley)사는 이 연구결과를 향후 석유화학 산업을 환경 친화적인 바이오기반 화학산업으로 바꾸는데 핵심이 되는 대사공학의 적용 예를 잘 보인 것으로 높이 평가하여 지난 27일 보도자료를 통해 언론에 소개하기도 했다.
李 교수는 “본 연구는 교육과학기술부의 시스템생물학 연구개발 사업의 결실 중에 하나로서, 다이아민을 바이오 기반 환경 친화적인 공정으로 생산할 수 있다는 것을 보여준 좋을 예라고 생각한다. 본 기술에 이용된 시스템대사공학 기법은 다른 화학물질의 바이오 기반 생산도 효율적으로 가능하게 할 것이다. 현재 특허 출원된 본 기술 관련하여 박사학위 주제로 잘 수행한 취안지강(Qian Zhi Gang) 박사와 시아샤시아(Xia Xiao Xia) 박사와 함께 다른 다이아민 생산 공정도 개발 중이다”고 밝혔다.
바이오테크놀로지 바이오엔지니어링지의 50주년 기념해를 맞이하여 투고한 본 논문은 학술지의 표지논문, 스포트라이트 논문, 그리고 편집장 우수 논문으로 동시에 선정되기도 했다.
KAIST 관계자는 “이 교수팀은 세계적인 대사공학 연구 전문그륩으로서 이 기술을 이용한 산업바이오텍 기술 개발에서 탁월한 연구 결과들을 내 놓고 있다. 우리나라에서 주도하고 있는 녹색성장의 핵심 전략으로 바이오 기반 화학산업을 발전시키는데 크게 기여할 수 있을 것으로 생각한다.”고 했다.
李 교수는 내년 6월 제주도에서 개최되는 세계 대사공학 학술회의의 의장으로 최근 추대됐으며, 지난 달 미국 듀퐁사, 델라웨어주립대학교, 마이크로소프트사, 스탠포드대학교, 캘리포니아 버클리 주립대학교, 시스템생물학연구소 등에서 시스템대사공학을 통한 산업바이오텍을 주제로 초청강연을 하는 등 대사공학 연구를 선도하고 있다.
2009.08.31 조회수 22502
이상엽 특훈교수팀, 대사공학기술로 바이오매스로부터 나일론 원료를 생산하는 녹색기술 개발
- 화석원료 기반의 화학산업에서 바이오 기반 녹색 화학산업으로 -
우리대학 생명화학공학과 이상엽 특훈교수(45, 생명과학기술대학 학장, 바이오융합연구소 공동소장, LG화학 석좌교수)팀이 대사공학 기술을 이용하여 대장균으로부터 나일론의 원료가 되는 다이아민(diamine)을 효율적으로 생산하는 시스템을 최근 개발했다.
이 연구결과는 미국 와일리-블랙웰(Wiley-Blackwell)사가 발간하는 가장 오랜 전통의 공학계열 생명공학 학술지인 바이오테크놀로지 바이오엔지니어링지(Biotechnology and Bioengineering) 27일자 온라인 판으로 소개됐다.
현재, 의약을 제외하고도 1,800조원 시장 규모의 화학 물질들은 주로 화석원료에 기반한 석유화학 공정으로 생산돼 왔다. 이 연구결과는 세계에서 처음으로 나일론 등의 원료로 쓰이는 1,4-다이아미노부탄 (1,4-diaminobutane), 일명 푸트레신 (putrescine)을 석유화학공정이 아닌 포도당이나 설탕과 같은 바이오매스 유래 원료로부터 대사공학으로 개량된 대장균을 이용하여 생산하는 기술을 제공하고 있다.
와일리(Wiley)사는 이 연구결과를 향후 석유화학 산업을 환경 친화적인 바이오기반 화학산업으로 바꾸는데 핵심이 되는 대사공학의 적용 예를 잘 보인 것으로 높이 평가하여 지난 27일 보도자료를 통해 언론에 소개하기도 했다.
李 교수는 “본 연구는 교육과학기술부의 시스템생물학 연구개발 사업의 결실 중에 하나로서, 다이아민을 바이오 기반 환경 친화적인 공정으로 생산할 수 있다는 것을 보여준 좋을 예라고 생각한다. 본 기술에 이용된 시스템대사공학 기법은 다른 화학물질의 바이오 기반 생산도 효율적으로 가능하게 할 것이다. 현재 특허 출원된 본 기술 관련하여 박사학위 주제로 잘 수행한 취안지강(Qian Zhi Gang) 박사와 시아샤시아(Xia Xiao Xia) 박사와 함께 다른 다이아민 생산 공정도 개발 중이다”고 밝혔다.
바이오테크놀로지 바이오엔지니어링지의 50주년 기념해를 맞이하여 투고한 본 논문은 학술지의 표지논문, 스포트라이트 논문, 그리고 편집장 우수 논문으로 동시에 선정되기도 했다.
KAIST 관계자는 “이 교수팀은 세계적인 대사공학 연구 전문그륩으로서 이 기술을 이용한 산업바이오텍 기술 개발에서 탁월한 연구 결과들을 내 놓고 있다. 우리나라에서 주도하고 있는 녹색성장의 핵심 전략으로 바이오 기반 화학산업을 발전시키는데 크게 기여할 수 있을 것으로 생각한다.”고 했다.
李 교수는 내년 6월 제주도에서 개최되는 세계 대사공학 학술회의의 의장으로 최근 추대됐으며, 지난 달 미국 듀퐁사, 델라웨어주립대학교, 마이크로소프트사, 스탠포드대학교, 캘리포니아 버클리 주립대학교, 시스템생물학연구소 등에서 시스템대사공학을 통한 산업바이오텍을 주제로 초청강연을 하는 등 대사공학 연구를 선도하고 있다.
2009.08.31 조회수 22502 -
 생명화학공학과 양승만교수 광자유체 신기술개발
생명화학공학과 양승만(梁承萬, 58세, 교육과학기술부 지정 광자유체집적소자 창의연구단 단장) 교수 연구팀이 다양한 기능을 갖는 나노입자를 제조하고 이들 입자들이 스스로 조립되는 ‘자기조립원리’를 규명하는 연구를 수행하여, 방대한 량의 정보를 처리할 수 있는 프로토타입(prototype)의 광․바이오 기능성 광자결정(photonic crystal)구조체를 개발했다.
자연계에 존재하는 대표적인 광자결정은 오팔보석, 나비의 날개, 공작새의 깃털 등이 있다. 이들 광자결정 물질들이 발산하는 아름다운 색깔은 색소에 의한 것이 아니라 이 물질들을 이루는 구조 자체가 규칙적인 나노구조로 되어 있기 때문이다. 즉, 광자결정은 굴절률이 다른 물질들이 규칙적으로 쌓여 조립된 3차원 구조체로 특정한 영역의 파장에 해당하는 빛만 완전히 반사시킨다. 이 성질을 이용하면 반도체가 전자의 흐름을 제어하듯 빛의 흐름을 제어할 수 있다. 이러한 광자결정의 특수한 기능 때문에 나노레이저, 다중파장의 광 정보를 처리할 수 있는 슈퍼프리즘(superprism), 빛을 원하는 위치로 가이드 할 수 있는 광도파로(waveguide) 등 차세대 광통신 소자와 현재의 컴퓨터 속도를 획기적으로 높일 수 있는 수십 테라급 초고속 정보처리능력을 갖춘 광자컴퓨터의 개발 등에 필요한 소재로 주목 받아왔다. 광자결정은 광자(빛)가 정보를 처리하는 미래에 오늘날의 반도체와 같은 역할을 할 것이므로 ‘빛의 반도체’라 불린다. 지난 20여 년 동안 자연 상태에 존재하는 광자결정의 나노구조를 인공적으로 제조하기 위한 연구가 많은 과학자들에 의하여 시도되어 왔지만 실용적인 구조를 얻는 데에는 한계가 있었다. 梁 교수팀은 2006년부터 교육과학기술부와 한국과학재단의 ‘창의적연구진흥사업’으로부터 지원을 받아 광자결정소재의 실용성을 확보하기 위한 연구를 수행하여 최근 해외 저명학술지로부터 크게 주목 받는 일련의 연구 성과를 거뒀다.
첫 번째 연구 성과로 굴절률 조절이 가능한 미세입자 대량 생산기술을 개발했다. 지금까지 구현된 3차원 광자결정은 결정을 이루는 물질의 굴절률이 1.5-2.0 정도로 낮고, 굴절률을 다양하게 조절할 수 있는 입자를 제조할 수 없어서 광자결정의 실용성에 한계가 있었다. 최근 梁 교수 연구팀은 굴절률을 1.4-2.8까지 마음대로 조절할 수 있는 입자를 대량으로 제조할 수 있는 실용적 방법을 개발했다. 제조된 고 굴절률 입자는 나노레이저, 광 공명기, 마이크로렌즈, 디스플레이 등 각종 광학소자와 광촉매 등으로 활용될 수 있다. 이 연구결과는 최근 어드밴스드 머티리얼스 인터넷판(6. 19)과 제 17호(2008. 9)의 표지논문으로 게재 예정이다. 특히, 이 논문은 저명 학술지인 네이처 포토닉스(Nature Photonics)誌 8월호(8. 1)에 리서치 하이라이트(Research Highlights)로 선정되어 연구의 중요성과 응용성에 대하여 특별기사로 조명했다.
그림 1. 초고굴절률 타이타니아 입자의 전자 현미경 사진
두 번째 연구 성과로 광자유체 기술을 이용한 광결정구 연속생산 기술을 개발했다. 균일한 크기와 모양을 갖는 광자결정구를 빛을 매개로 반응시킴으로써 종래에 수십 시간이 소요되는 공정을 불과 수십 초 만에 연속적으로 제조할 수 있는 기술을 확보했다. 이들 광자결정구는 차세대 반사형디스플레이 색소나, 나노바코드, 생물감지소자 등으로 활용될 수 있다. 특히 주목할 것은 몇 개의 다른 색을 반사하는 야누스 광자결정구슬을 제조하였는데 이들은 전자종이와 같은 접거나 말 수 있는 차세대 디스플레이 소자에 활용될 수 도 있다. 이러한 광자결정 표시소재는 세계굴지의 화학회사인 독일 머크(Merck)社 등에서도 개발 중이며 이번 연구 결과는 이 분야의 국제경쟁에서 우위를 확보하는데 필요한 핵심요소이다. 주요 연구결과는 국제적저명학술지인 미국화학회지(JACS)와 어드밴스드 머티리얼스(Advanced Materials)誌에 6편의 논문을 최근 4개월(5~8월) 동안 연속 게재하여 광자결정의 실용성을 구현하는데 크게 기여했다고 인정받았다. 특히, 이들 논문들은 해당 학술지 편집인(Editor)과 심사위원들에 의하여 가장 앞선 연구결과로서 주목해야 할 논문(Advances in Advance)으로 선정됐으며, 9호(5. 5) 표지논문에 게재됐다.
그림 2. 3원광 광자결정구와 다색상 야누스 광자결정구의 현미경사진과 휘어지는 기판 위에 픽셀화된 3원광 광자결정.
세 번째 연구 성과로 광자유체 기술을 이용한 광결정 나노레이저를 개발했다. 현재까지 개발된 나노레이저는 발생하는 고열로 인하여 발진하는 레이저의 파장을 변화시키기 어려운 단점이 있었다. 梁 교수 연구팀은 KAIST 물리학과의 이용희 교수 연구팀과 공동으로 연속가변파장 나노레이저를 최초로 개발했다. 레이저를 발진하는 광자결정과 매우 미세한 유량을 도입할 수 있는 미세유체소자를 결합한 후 물과 같은 액체를 흘려줌으로써 온도를 낮추어 연속파 레이저 발진을 가능케 하였다. 또한 굴절률이 다른 액체를 흘려주어 광밴드갭을 조절함으로써 레이저의 파장을 조절 할 수 있었다. 가변파장 나노레이저는 신약개발 등 생명공학에서 요구되는 극미량의 시료로부터 방대한 량의 바이오정보를 광학적으로 신속하게 처리하는데 필요한 광원으로 사용될 수 있다. 이 연구 결과는 광물리 분야의 저명학술지인 옵틱스 익스프레스(Optics Express)에 게재(4. 9) 됐으며 이 논문의 독창성과 실용성은 영국왕립화학회(Royal Society of Chemistry)에서 발간하는 저명학술지 랩온어칩(Lab on a Chip) 8월호(8. 1)에 해설과 함께 “리서치 하이라이트”로 소개됐다.
그림 3. 나노레이저 발진모드
2008.08.19 조회수 26747
생명화학공학과 양승만교수 광자유체 신기술개발
생명화학공학과 양승만(梁承萬, 58세, 교육과학기술부 지정 광자유체집적소자 창의연구단 단장) 교수 연구팀이 다양한 기능을 갖는 나노입자를 제조하고 이들 입자들이 스스로 조립되는 ‘자기조립원리’를 규명하는 연구를 수행하여, 방대한 량의 정보를 처리할 수 있는 프로토타입(prototype)의 광․바이오 기능성 광자결정(photonic crystal)구조체를 개발했다.
자연계에 존재하는 대표적인 광자결정은 오팔보석, 나비의 날개, 공작새의 깃털 등이 있다. 이들 광자결정 물질들이 발산하는 아름다운 색깔은 색소에 의한 것이 아니라 이 물질들을 이루는 구조 자체가 규칙적인 나노구조로 되어 있기 때문이다. 즉, 광자결정은 굴절률이 다른 물질들이 규칙적으로 쌓여 조립된 3차원 구조체로 특정한 영역의 파장에 해당하는 빛만 완전히 반사시킨다. 이 성질을 이용하면 반도체가 전자의 흐름을 제어하듯 빛의 흐름을 제어할 수 있다. 이러한 광자결정의 특수한 기능 때문에 나노레이저, 다중파장의 광 정보를 처리할 수 있는 슈퍼프리즘(superprism), 빛을 원하는 위치로 가이드 할 수 있는 광도파로(waveguide) 등 차세대 광통신 소자와 현재의 컴퓨터 속도를 획기적으로 높일 수 있는 수십 테라급 초고속 정보처리능력을 갖춘 광자컴퓨터의 개발 등에 필요한 소재로 주목 받아왔다. 광자결정은 광자(빛)가 정보를 처리하는 미래에 오늘날의 반도체와 같은 역할을 할 것이므로 ‘빛의 반도체’라 불린다. 지난 20여 년 동안 자연 상태에 존재하는 광자결정의 나노구조를 인공적으로 제조하기 위한 연구가 많은 과학자들에 의하여 시도되어 왔지만 실용적인 구조를 얻는 데에는 한계가 있었다. 梁 교수팀은 2006년부터 교육과학기술부와 한국과학재단의 ‘창의적연구진흥사업’으로부터 지원을 받아 광자결정소재의 실용성을 확보하기 위한 연구를 수행하여 최근 해외 저명학술지로부터 크게 주목 받는 일련의 연구 성과를 거뒀다.
첫 번째 연구 성과로 굴절률 조절이 가능한 미세입자 대량 생산기술을 개발했다. 지금까지 구현된 3차원 광자결정은 결정을 이루는 물질의 굴절률이 1.5-2.0 정도로 낮고, 굴절률을 다양하게 조절할 수 있는 입자를 제조할 수 없어서 광자결정의 실용성에 한계가 있었다. 최근 梁 교수 연구팀은 굴절률을 1.4-2.8까지 마음대로 조절할 수 있는 입자를 대량으로 제조할 수 있는 실용적 방법을 개발했다. 제조된 고 굴절률 입자는 나노레이저, 광 공명기, 마이크로렌즈, 디스플레이 등 각종 광학소자와 광촉매 등으로 활용될 수 있다. 이 연구결과는 최근 어드밴스드 머티리얼스 인터넷판(6. 19)과 제 17호(2008. 9)의 표지논문으로 게재 예정이다. 특히, 이 논문은 저명 학술지인 네이처 포토닉스(Nature Photonics)誌 8월호(8. 1)에 리서치 하이라이트(Research Highlights)로 선정되어 연구의 중요성과 응용성에 대하여 특별기사로 조명했다.
그림 1. 초고굴절률 타이타니아 입자의 전자 현미경 사진
두 번째 연구 성과로 광자유체 기술을 이용한 광결정구 연속생산 기술을 개발했다. 균일한 크기와 모양을 갖는 광자결정구를 빛을 매개로 반응시킴으로써 종래에 수십 시간이 소요되는 공정을 불과 수십 초 만에 연속적으로 제조할 수 있는 기술을 확보했다. 이들 광자결정구는 차세대 반사형디스플레이 색소나, 나노바코드, 생물감지소자 등으로 활용될 수 있다. 특히 주목할 것은 몇 개의 다른 색을 반사하는 야누스 광자결정구슬을 제조하였는데 이들은 전자종이와 같은 접거나 말 수 있는 차세대 디스플레이 소자에 활용될 수 도 있다. 이러한 광자결정 표시소재는 세계굴지의 화학회사인 독일 머크(Merck)社 등에서도 개발 중이며 이번 연구 결과는 이 분야의 국제경쟁에서 우위를 확보하는데 필요한 핵심요소이다. 주요 연구결과는 국제적저명학술지인 미국화학회지(JACS)와 어드밴스드 머티리얼스(Advanced Materials)誌에 6편의 논문을 최근 4개월(5~8월) 동안 연속 게재하여 광자결정의 실용성을 구현하는데 크게 기여했다고 인정받았다. 특히, 이들 논문들은 해당 학술지 편집인(Editor)과 심사위원들에 의하여 가장 앞선 연구결과로서 주목해야 할 논문(Advances in Advance)으로 선정됐으며, 9호(5. 5) 표지논문에 게재됐다.
그림 2. 3원광 광자결정구와 다색상 야누스 광자결정구의 현미경사진과 휘어지는 기판 위에 픽셀화된 3원광 광자결정.
세 번째 연구 성과로 광자유체 기술을 이용한 광결정 나노레이저를 개발했다. 현재까지 개발된 나노레이저는 발생하는 고열로 인하여 발진하는 레이저의 파장을 변화시키기 어려운 단점이 있었다. 梁 교수 연구팀은 KAIST 물리학과의 이용희 교수 연구팀과 공동으로 연속가변파장 나노레이저를 최초로 개발했다. 레이저를 발진하는 광자결정과 매우 미세한 유량을 도입할 수 있는 미세유체소자를 결합한 후 물과 같은 액체를 흘려줌으로써 온도를 낮추어 연속파 레이저 발진을 가능케 하였다. 또한 굴절률이 다른 액체를 흘려주어 광밴드갭을 조절함으로써 레이저의 파장을 조절 할 수 있었다. 가변파장 나노레이저는 신약개발 등 생명공학에서 요구되는 극미량의 시료로부터 방대한 량의 바이오정보를 광학적으로 신속하게 처리하는데 필요한 광원으로 사용될 수 있다. 이 연구 결과는 광물리 분야의 저명학술지인 옵틱스 익스프레스(Optics Express)에 게재(4. 9) 됐으며 이 논문의 독창성과 실용성은 영국왕립화학회(Royal Society of Chemistry)에서 발간하는 저명학술지 랩온어칩(Lab on a Chip) 8월호(8. 1)에 해설과 함께 “리서치 하이라이트”로 소개됐다.
그림 3. 나노레이저 발진모드
2008.08.19 조회수 26747 -
 이상엽교수팀, 시스템생물학 기반 산업용 미생물 개발 전략 제시
-생명공학분야 권위 리뷰지 “생명공학의 동향 (Trends in Biotechnology, Cell Press)” 표지 논문 게재
우리학교 생명화학공학과 및 바이오융합연구소 이상엽(李相燁, 44세, LG화학 석좌교수) 특훈교수와 바이오융합연구소 박진환(朴軫煥, 38세) 박사 연구팀이 다가오는 산업바이오텍 시대에 경쟁력을 갖추기 위한 시스템 생물학 기반의 미생물 대사공학 전략을 개발했다. 이 연구 결과는 셀(Cell)誌가 발행하는 생명공학 분야 최고 권위 리뷰지인 생명공학의 동향(Trends in Biotechnology) 8월호 표지 논문에 게재됐다. 교육과학기술부 게놈 정보 활용 통합 생물공정 개발 사업의 일환으로 수행한 이번 연구는 산업용 미생물을 개발함에 있어 유전체 및 기능 유전체 정보와 가상세포 시뮬레이션을 통합 적용하고, 발효 및 분리정제 공정까지 고려한 대사공학 방법을 제시함으로서 다가오는 바이오 기반 산업 시대에 경쟁력을 갖는 균주 개발 전략을 체계적으로 제시한 것으로 평가됐다.
유가가 고공행진을 계속하고 지구온난화 등 환경문제가 심각하게 대두되는 지금 세계 각국은 바이오매스를 이용하여 화학, 물질, 에너지 등을 생산하는 바이오기반 산업 시스템 구축에 박차를 가하고 있다. 미생물을 이용한 산업바이오텍 공정이 경쟁력을 갖추기 위해서는 자연계에서 분리된 미생물의 낮은 성능을 대폭 향상시키기 위하여 대사공학으로 미생물을 개량하여야 한다. 기존의 산업바이오텍에 사용되는 미생물 균주 제조 방법과 공정개발은 무작위 돌연변이화 및 균주의 일부분만 직관적으로 조작하는 방법에 의해 수행되었다. 하지만 이들은 원하지 않은 부분에도 돌연변이를 일으켜, 균주 전체의 대사 상태를 한눈에 볼 수 없으며, 향후 환경이 바뀌었을 때 추가 개발이 용이하지 않다는 단점이 있었다. 李 교수 연구팀은 시스템 생물학의 원리에 입각하여 크게 3 단계로 나누어 체계적으로 미생물을 개발하는 새로운 전략을 제시하였다. 1단계에서는 미생물의 조절 기작 등 연구를 통해 알게 된 사실에 기반하여 게놈상의 필요한 부위만을 조작, 초기 생산균주를 제작한다. 2단계에서는 시스템 수준의 분석을 통하여 확보한 오믹스 데이터와 가상세포의 시뮬레이션 결과를 융합, 세포내의 대사흐름 최적화를 통해 목적 산물을 최고 수율로 생산할 수 있는 균주를 제작한다. 마지막 3단계에서는 실제 생산 공정 개발 단계에서 생길 수 있는 문제점들을 시스템 생물학 기법에 입각하여 해결함으로써 우수 산업용 균주의 제조를 완료한다. 이 전략은 시스템 생물학 원리를 이용하여 균주 전체의 생리 대사 현상을 한눈에 파악하면서 균주의 대사공학적 개량이 가능하다는 점에서 기존의 방법과는 차별된 한 차원 높은 수준의 균주개발 전략이라고 할 수 있다.
이번 논문의 첫 번째 저자인 朴 박사는 "최근 연구팀에서 수행 중인 시스템 생물학 기법을 이용한 실제 균주 제작 과정의 경험과 결과를 토대로 전략을 확립 제시하였기 때문에 실제 생명공학 산업계에 종사하는 연구자들에게 실질적인 도움이 될 것으로 생각한다“고 말했다. 李 교수팀은 실제로 이 전략을 이용하여 최근 용도가 다양한 숙신산을 고효율로 생산하는 미생물과 고수율의 아미노산 (발린, 쓰레오닌) 생산균주, 바이오부탄올 생산균주 등을 개발한 바 있다.
<용어설명>
1) 가상세포: 세포내에서 일어나는 모든 효소 반응을 컴퓨터에서 재구성하여 실제 세포처럼 반응 시켜 결과를 예측하는 시스템을 말한다.
2) 대사공학: 세포의 대사 및 조절 회로를 체계적으로 조작하여 원하는 생산물을 고효율로 생산할 수 있도록 만드는 기술을 말한다.
3) 오믹스 (omics): 세포 또는 개체 내에서 발현되는 단백체(proteome), 전사체(transcriptome), 대사체(metabolome), 흐름체(fluxome) 등 생명현상과 관련된 중요한 물질에 대한 대량의 정보를 획득하여 이를 생물정보학 기법으로 분석하여 전체적인 생명현상을 밝히려는 학문이다4) 시스템 생물학 (systems biology): 각종 오믹스(transcriptome, proteome, fluxome, metabolome) 데이터를 융합하고 전산 생물학 기법으로 해석하여 세포의 생리 상태를 다차원에서 규명함으로써 세포와 생명체 전체를 이해하고자 하는 학문이며, 이 플랫폼을 기반으로 유용한 미생물의 개발이 가능하다.
2008.07.24 조회수 25593
이상엽교수팀, 시스템생물학 기반 산업용 미생물 개발 전략 제시
-생명공학분야 권위 리뷰지 “생명공학의 동향 (Trends in Biotechnology, Cell Press)” 표지 논문 게재
우리학교 생명화학공학과 및 바이오융합연구소 이상엽(李相燁, 44세, LG화학 석좌교수) 특훈교수와 바이오융합연구소 박진환(朴軫煥, 38세) 박사 연구팀이 다가오는 산업바이오텍 시대에 경쟁력을 갖추기 위한 시스템 생물학 기반의 미생물 대사공학 전략을 개발했다. 이 연구 결과는 셀(Cell)誌가 발행하는 생명공학 분야 최고 권위 리뷰지인 생명공학의 동향(Trends in Biotechnology) 8월호 표지 논문에 게재됐다. 교육과학기술부 게놈 정보 활용 통합 생물공정 개발 사업의 일환으로 수행한 이번 연구는 산업용 미생물을 개발함에 있어 유전체 및 기능 유전체 정보와 가상세포 시뮬레이션을 통합 적용하고, 발효 및 분리정제 공정까지 고려한 대사공학 방법을 제시함으로서 다가오는 바이오 기반 산업 시대에 경쟁력을 갖는 균주 개발 전략을 체계적으로 제시한 것으로 평가됐다.
유가가 고공행진을 계속하고 지구온난화 등 환경문제가 심각하게 대두되는 지금 세계 각국은 바이오매스를 이용하여 화학, 물질, 에너지 등을 생산하는 바이오기반 산업 시스템 구축에 박차를 가하고 있다. 미생물을 이용한 산업바이오텍 공정이 경쟁력을 갖추기 위해서는 자연계에서 분리된 미생물의 낮은 성능을 대폭 향상시키기 위하여 대사공학으로 미생물을 개량하여야 한다. 기존의 산업바이오텍에 사용되는 미생물 균주 제조 방법과 공정개발은 무작위 돌연변이화 및 균주의 일부분만 직관적으로 조작하는 방법에 의해 수행되었다. 하지만 이들은 원하지 않은 부분에도 돌연변이를 일으켜, 균주 전체의 대사 상태를 한눈에 볼 수 없으며, 향후 환경이 바뀌었을 때 추가 개발이 용이하지 않다는 단점이 있었다. 李 교수 연구팀은 시스템 생물학의 원리에 입각하여 크게 3 단계로 나누어 체계적으로 미생물을 개발하는 새로운 전략을 제시하였다. 1단계에서는 미생물의 조절 기작 등 연구를 통해 알게 된 사실에 기반하여 게놈상의 필요한 부위만을 조작, 초기 생산균주를 제작한다. 2단계에서는 시스템 수준의 분석을 통하여 확보한 오믹스 데이터와 가상세포의 시뮬레이션 결과를 융합, 세포내의 대사흐름 최적화를 통해 목적 산물을 최고 수율로 생산할 수 있는 균주를 제작한다. 마지막 3단계에서는 실제 생산 공정 개발 단계에서 생길 수 있는 문제점들을 시스템 생물학 기법에 입각하여 해결함으로써 우수 산업용 균주의 제조를 완료한다. 이 전략은 시스템 생물학 원리를 이용하여 균주 전체의 생리 대사 현상을 한눈에 파악하면서 균주의 대사공학적 개량이 가능하다는 점에서 기존의 방법과는 차별된 한 차원 높은 수준의 균주개발 전략이라고 할 수 있다.
이번 논문의 첫 번째 저자인 朴 박사는 "최근 연구팀에서 수행 중인 시스템 생물학 기법을 이용한 실제 균주 제작 과정의 경험과 결과를 토대로 전략을 확립 제시하였기 때문에 실제 생명공학 산업계에 종사하는 연구자들에게 실질적인 도움이 될 것으로 생각한다“고 말했다. 李 교수팀은 실제로 이 전략을 이용하여 최근 용도가 다양한 숙신산을 고효율로 생산하는 미생물과 고수율의 아미노산 (발린, 쓰레오닌) 생산균주, 바이오부탄올 생산균주 등을 개발한 바 있다.
<용어설명>
1) 가상세포: 세포내에서 일어나는 모든 효소 반응을 컴퓨터에서 재구성하여 실제 세포처럼 반응 시켜 결과를 예측하는 시스템을 말한다.
2) 대사공학: 세포의 대사 및 조절 회로를 체계적으로 조작하여 원하는 생산물을 고효율로 생산할 수 있도록 만드는 기술을 말한다.
3) 오믹스 (omics): 세포 또는 개체 내에서 발현되는 단백체(proteome), 전사체(transcriptome), 대사체(metabolome), 흐름체(fluxome) 등 생명현상과 관련된 중요한 물질에 대한 대량의 정보를 획득하여 이를 생물정보학 기법으로 분석하여 전체적인 생명현상을 밝히려는 학문이다4) 시스템 생물학 (systems biology): 각종 오믹스(transcriptome, proteome, fluxome, metabolome) 데이터를 융합하고 전산 생물학 기법으로 해석하여 세포의 생리 상태를 다차원에서 규명함으로써 세포와 생명체 전체를 이해하고자 하는 학문이며, 이 플랫폼을 기반으로 유용한 미생물의 개발이 가능하다.
2008.07.24 조회수 25593 -
 KAIST-GS칼텍스 공동, 바이오부탄올 생산균주개발
- 대사공학적으로 개량된 균주 개발로 효율적 생산가능
- 바이오부탄올은 에너지량이 높고 수송편의 등 장점 많아 차세새 연로로 각광
우리학교와 GS칼텍스(대표 허동수회장)가 공동연구를 통해 차세대 바이오연료로 각광받고 있는 ‘바이오부탄올’을 생산하는 새로운 균주를 개발하는데 성공했다.
이상엽(李相燁, 44세) KAIST 생명화학공학과 및 바이오융합연구소 특훈교수(생명과학기술대학장)와 GS칼텍스 공동연구팀은 폐목재, 볏짚, 잉여 사탕수수 등 비식용 바이오매스를 이용, 많은 양의 ‘바이오부탄올’을 선택적으로 생산 가능케 하는 대사공학적으로 개량된 균주개발에 성공했으며, 특허를 출원했다고 밝혔다.
이번 KAIST와 GS칼텍스가 공동으로 개발, 특허 출원한 기술은 바이오매스 발효과정에 사용되는 균주를 대사공학적으로 개량, 아세톤의 생산을 억제하고 부탄올과 에탄올만 6:1의 비율로 생산되도록 한 것으로, 아세톤을 부탄올로부터 분리할 필요가 없어 공정비용을 절감할 수 있는 장점을 가지고 있다. 클로스트리디움 박테리아를 사용하여 부탄올을 생산하는 전통적인 발효방식에서는 발효시 대사특성으로 인해 부탄올과 아세톤, 그리고 에탄올을 6:3:1의 비율로 생산되는데, 이 때 생산되는 아세톤은 연료로는 사용이 곤란하다는 단점이 있다.
‘바이오부탄올’은 탄소가 4개로 구성된 알코올로서 1리터당 에너지량이 7,323kcal로 현재 널리 사용되고 있는 바이오에탄올의 에너지량 5,592kcal보다 단위 부피당 에너지량이 30% 이상 높으며, 가솔린의 7,656kcal와도 큰 차이가 없다.
또한, 바이오에탄올은 철도나 바지선, 트럭 등으로 운송하여야 하나, ‘바이오부탄올’은 흡수성이 적어 상(相)이 분리되는 문제나 부식성의 문제가 없어 기존의 연료수송 파이프라인을 통해 수송할 수 있다는 장점 때문에 차세대 바이오연료로 각광받고 있으며, 전 세계적으로 많은 연구기관과 기업들의 개발 노력이 치열하게 전개되고 있다.
‘바이오부탄올’은 1900년대 초부터 미생물 발효를 이용하여 생산되기 시작했으나, 1950년대 석유화학산업이 급속히 발달함에 따라 사양길로 접어들었으며, 당밀 등 원료가격이 싼 남아프리카공화국 등지에서만 1980년대까지 발효 생산되다가 중단된 바 있다.
하지만, 최근 고유가시대가 고착화되면서 석유를 일정부분 대체할 수 있는 연료로 다시 부각되고 있다.
이상엽 교수팀과 GS칼텍스는 현재 바이오부탄올 연속 생산공정 등의 조업 최적화 연구를 수행 중이며, 부탄올에 대한 내성 향상 및 생산성을 한층 높이는 균주 개발 연구를 계속하고 있다.
GS칼텍스 중앙기술연구소 정광섭 소장은 “전 세계적으로 바이오부탄올 생산을 위한 개발 경쟁이 치열한 가운데 산학 공동연구를 통해 개량된 고성능 균주를 확보함으로써 차세대 바이오연료 개발에 유리한 고지를 차지할 수 있게 되었다.”고 이번 연구개발의 의미를 밝혔다.
<용어 설명>
- 바이오매스(Biomass)
바이오매스(biomass)는 에너지 전용의 작물과 나무, 농산품과 사료작물, 농작 폐기물과 찌꺼기, 임산 폐기물과 부스러기, 수초, 동물의 배설물, 도시 쓰레기, 그리고 여타의 폐기물에서 추출된 재생가능한 유기 물질 로 현재 에너지원으로 쓰이고 있는 목재, 식물, 농·임산 부산물, 도시 쓰레기와 산업 폐기물 내의 유기 성분 등을 일컫는다.
- 선택성(Selectivity)
촉매나 미생물의 성능을 나타낼 수 있는 인자로써 전체 생성물(Total Product) 중에 우리가 원하는 생성물(Target Product)의 비율로 계산함.
- 대사공학(Metabolic Engineering)
유전자 재조합기술과 관련 분자생물학 및 화학공학적 기술을 이용하여 미생물에 새로운 대사회로를 도입하거나 기존의 대사회로를 제거 증폭 변경시켜 세포나 균주의 대사특성을 우리가 원하는 방향으로 바꾸는 일 련의 기술을 뜻함.
- 균주
우리가 원하는 물질을 생산해 내는 미생물을 포괄적으로 뜻함.
- 에너지량
단위 질량의 연료를 연소하였을 때 발생하는 에너지
- 상(相): Phase
물리학·화학 용어로, 어떤 물질이 물리적·화학적으로 같은 성질을 나타 낼 때를 표현하는 것. 상은 기체상, 액체상, 고체상이 존재하고, 하나의 상으로 이루어지는 균일계와 2개 이상의 상으로 이루어지는 불균일계로 나뉜다.
2008.06.03 조회수 21759
KAIST-GS칼텍스 공동, 바이오부탄올 생산균주개발
- 대사공학적으로 개량된 균주 개발로 효율적 생산가능
- 바이오부탄올은 에너지량이 높고 수송편의 등 장점 많아 차세새 연로로 각광
우리학교와 GS칼텍스(대표 허동수회장)가 공동연구를 통해 차세대 바이오연료로 각광받고 있는 ‘바이오부탄올’을 생산하는 새로운 균주를 개발하는데 성공했다.
이상엽(李相燁, 44세) KAIST 생명화학공학과 및 바이오융합연구소 특훈교수(생명과학기술대학장)와 GS칼텍스 공동연구팀은 폐목재, 볏짚, 잉여 사탕수수 등 비식용 바이오매스를 이용, 많은 양의 ‘바이오부탄올’을 선택적으로 생산 가능케 하는 대사공학적으로 개량된 균주개발에 성공했으며, 특허를 출원했다고 밝혔다.
이번 KAIST와 GS칼텍스가 공동으로 개발, 특허 출원한 기술은 바이오매스 발효과정에 사용되는 균주를 대사공학적으로 개량, 아세톤의 생산을 억제하고 부탄올과 에탄올만 6:1의 비율로 생산되도록 한 것으로, 아세톤을 부탄올로부터 분리할 필요가 없어 공정비용을 절감할 수 있는 장점을 가지고 있다. 클로스트리디움 박테리아를 사용하여 부탄올을 생산하는 전통적인 발효방식에서는 발효시 대사특성으로 인해 부탄올과 아세톤, 그리고 에탄올을 6:3:1의 비율로 생산되는데, 이 때 생산되는 아세톤은 연료로는 사용이 곤란하다는 단점이 있다.
‘바이오부탄올’은 탄소가 4개로 구성된 알코올로서 1리터당 에너지량이 7,323kcal로 현재 널리 사용되고 있는 바이오에탄올의 에너지량 5,592kcal보다 단위 부피당 에너지량이 30% 이상 높으며, 가솔린의 7,656kcal와도 큰 차이가 없다.
또한, 바이오에탄올은 철도나 바지선, 트럭 등으로 운송하여야 하나, ‘바이오부탄올’은 흡수성이 적어 상(相)이 분리되는 문제나 부식성의 문제가 없어 기존의 연료수송 파이프라인을 통해 수송할 수 있다는 장점 때문에 차세대 바이오연료로 각광받고 있으며, 전 세계적으로 많은 연구기관과 기업들의 개발 노력이 치열하게 전개되고 있다.
‘바이오부탄올’은 1900년대 초부터 미생물 발효를 이용하여 생산되기 시작했으나, 1950년대 석유화학산업이 급속히 발달함에 따라 사양길로 접어들었으며, 당밀 등 원료가격이 싼 남아프리카공화국 등지에서만 1980년대까지 발효 생산되다가 중단된 바 있다.
하지만, 최근 고유가시대가 고착화되면서 석유를 일정부분 대체할 수 있는 연료로 다시 부각되고 있다.
이상엽 교수팀과 GS칼텍스는 현재 바이오부탄올 연속 생산공정 등의 조업 최적화 연구를 수행 중이며, 부탄올에 대한 내성 향상 및 생산성을 한층 높이는 균주 개발 연구를 계속하고 있다.
GS칼텍스 중앙기술연구소 정광섭 소장은 “전 세계적으로 바이오부탄올 생산을 위한 개발 경쟁이 치열한 가운데 산학 공동연구를 통해 개량된 고성능 균주를 확보함으로써 차세대 바이오연료 개발에 유리한 고지를 차지할 수 있게 되었다.”고 이번 연구개발의 의미를 밝혔다.
<용어 설명>
- 바이오매스(Biomass)
바이오매스(biomass)는 에너지 전용의 작물과 나무, 농산품과 사료작물, 농작 폐기물과 찌꺼기, 임산 폐기물과 부스러기, 수초, 동물의 배설물, 도시 쓰레기, 그리고 여타의 폐기물에서 추출된 재생가능한 유기 물질 로 현재 에너지원으로 쓰이고 있는 목재, 식물, 농·임산 부산물, 도시 쓰레기와 산업 폐기물 내의 유기 성분 등을 일컫는다.
- 선택성(Selectivity)
촉매나 미생물의 성능을 나타낼 수 있는 인자로써 전체 생성물(Total Product) 중에 우리가 원하는 생성물(Target Product)의 비율로 계산함.
- 대사공학(Metabolic Engineering)
유전자 재조합기술과 관련 분자생물학 및 화학공학적 기술을 이용하여 미생물에 새로운 대사회로를 도입하거나 기존의 대사회로를 제거 증폭 변경시켜 세포나 균주의 대사특성을 우리가 원하는 방향으로 바꾸는 일 련의 기술을 뜻함.
- 균주
우리가 원하는 물질을 생산해 내는 미생물을 포괄적으로 뜻함.
- 에너지량
단위 질량의 연료를 연소하였을 때 발생하는 에너지
- 상(相): Phase
물리학·화학 용어로, 어떤 물질이 물리적·화학적으로 같은 성질을 나타 낼 때를 표현하는 것. 상은 기체상, 액체상, 고체상이 존재하고, 하나의 상으로 이루어지는 균일계와 2개 이상의 상으로 이루어지는 불균일계로 나뉜다.
2008.06.03 조회수 21759 -
 생명화공 정희태교수, 세계최초 액정 초미세 나노패턴소자 개발
- 15일자 네이처 머티리얼스誌 온라인판 게재- 나노-바이오 전자소자 산업분야에서 시장 선점 기대우리 학교 생명화학공학과 정희태(鄭喜台, 42) 교수 연구팀이 액정 디스플레이 (LCD)의 핵심소재로 잘 알려져 있는 액정물질을 이용, 나노기술의 핵심인 차세대 초미세 나노패턴소자를 세계최초로 개발했다. 관련 연구논문은 15일자 네이처 머티리얼스(Nature Materials)誌 온라인판에 게재된다. 나노패턴 제작은 차세대 초고밀도 반도체 메모리기술과 바이오칩 등 나노기술의 핵심분야다. 특히, 鄭 교수팀의 액정을 이용한 패턴구현은 기존의 패턴 방식에 비해 대면적을 구현할 수 있을 뿐만 아니라 바이오 특성을 가지는 나노물질도 액정 패턴 내에 배열할 수 있다는 것이 큰 장점이다.
LCD를 구동하는 물질인 네마틱 액정과 달리 鄭 교수가 사용한 스메틱 액정은 LCD 응답특성이 매우 우수함에도 불구하고 자연적으로 존재하는 결함구조 때문에 LCD 구동물질로 사용하지 못하고 있다. 이러한 스메틱 액정은 기판의 표면특성에 따라서 무질서한 형태의 회오리 형 결함구조를 가진다. 이번 연구에서는 마이크로미터 수준의 직선이 새겨진 표면 처리된 실리콘 기판을 사용함으로써 무질서한 회오리 형태의 액정 결함구조를 규칙적으로 제어하였다(첨부 자료그림 참조). 특히 이 공정은 기존의 나노패턴에 적용하는 방식과 비교하여 제작시간을 수십 배 이상 줄일 수 있으며, 결함구조 내에 다른 형태의 기능성 물질도 규칙적으로 배열 할 수 있음을 확인하였다. 이는 다양한 형태의 패턴이 필요한 실제 반도체와 단백질 칩 등의 바이오 소자에 적용할 수 있는 가능성을 제시하고 있다 (자료그림 중 삽입사진 참조).
이번 연구결과로 LCD의 세계적 강국인 우리나라가 액정을 이용한 나노분야에서도 세계 최고의 원천기술을 갖게 되었다. 향후 액정을 이용한 새로운 응용의 신기원을 열게 되었으며, 나노-바이오 전자소자 산업분야에서 시장 선점 및 막대한 부가가치 창출 등을 통해 국가경쟁력 강화에 크게 기여할 것으로 기대된다. 연성재료(Soft Materials)를 이용하여 나노패턴을 제조하는 기술은 전 세계적으로 나노-바이오 분야에서 큰 이슈가 되는 연구로써, 연구의 핵심은 바이오 및 광전자소자 응용을 위하여 대면적에서 결함이 없는 소재의 개발에 있다. 이번 鄭 교수팀이 적용한 액정은 결함구조를 가지는 대표적인 물질로서 지금까지 학계에서는 대면적 나노패턴이 불가능하다고 인식돼 왔다.
鄭 교수는 “이번 연구결과는 연성소재를 이용한 나노패턴소자 제작방식의 기존 개념을 완전히 뒤엎는 것이다. 결함을 없애야만 한다는 기존의 생각에서 탈피하여 결함을 규칙적으로 구현하면 패턴에 이용할 수 있다는 발상의 전환으로 대면적 나노패턴을 개발했다는데 의미가 있으며, 향후 나노분야 전반에 걸쳐 영향이 클 것” 이라고 밝혔다.
이번 연구결과는 鄭 교수(교신저자)의 주도 하에 KAIST 물리학과 김만원 교수팀과 미국 캔트 주립대학의 액정센터 올래그 라브랜토비치(Oleg Lavrentovich)교수가 함께 일궈낸 성과다. 鄭 교수는 나노물질분야에서 사이언스, PNAS, Advanced Materials에 최정상급 논문을 다수 발표하는 등 나노물질 분야에서 차세대 주자로서 두각을 나타내고 있는 젊은 과학자다.
<해설>
액정: 유동성이 있으면서 고체적인 특성을 나타낸다. 전기적 특성이 매우 뛰어나 LCD 구동을 위한 핵심 물질로 사용된다. 네마틱, 스메틱, 콜레스테릭 등 다양한 종류의 액정이 존재한다. 현재 LCD에 사용하는 액정은 네마틱 액정이며 콜레스테릭 액정은 반사거울과 초정밀 온도계에 사용된다. 鄭 교수팀이 사용한 액정은 스메틱 액정으로서 네마틱 액정보다 자연계와 합성물질에서 더욱 많이 존재하고, 산업체와 학계에서 오랜기간 동안 연구해 왔음에도 불구하고 결함구조 등의 문제점으로 인하여 산업에 적용하지 못하고 있는 물질이다.
<첨부. 수 밀리미터 크기의 대면적 액정물질 나노패턴 현미경 사진>우측상단 삽입사진은 액정나노패턴내에 형광나노입자를 규칙적으로 포집한 리소그라피 제작사진
2007.10.15 조회수 27420
생명화공 정희태교수, 세계최초 액정 초미세 나노패턴소자 개발
- 15일자 네이처 머티리얼스誌 온라인판 게재- 나노-바이오 전자소자 산업분야에서 시장 선점 기대우리 학교 생명화학공학과 정희태(鄭喜台, 42) 교수 연구팀이 액정 디스플레이 (LCD)의 핵심소재로 잘 알려져 있는 액정물질을 이용, 나노기술의 핵심인 차세대 초미세 나노패턴소자를 세계최초로 개발했다. 관련 연구논문은 15일자 네이처 머티리얼스(Nature Materials)誌 온라인판에 게재된다. 나노패턴 제작은 차세대 초고밀도 반도체 메모리기술과 바이오칩 등 나노기술의 핵심분야다. 특히, 鄭 교수팀의 액정을 이용한 패턴구현은 기존의 패턴 방식에 비해 대면적을 구현할 수 있을 뿐만 아니라 바이오 특성을 가지는 나노물질도 액정 패턴 내에 배열할 수 있다는 것이 큰 장점이다.
LCD를 구동하는 물질인 네마틱 액정과 달리 鄭 교수가 사용한 스메틱 액정은 LCD 응답특성이 매우 우수함에도 불구하고 자연적으로 존재하는 결함구조 때문에 LCD 구동물질로 사용하지 못하고 있다. 이러한 스메틱 액정은 기판의 표면특성에 따라서 무질서한 형태의 회오리 형 결함구조를 가진다. 이번 연구에서는 마이크로미터 수준의 직선이 새겨진 표면 처리된 실리콘 기판을 사용함으로써 무질서한 회오리 형태의 액정 결함구조를 규칙적으로 제어하였다(첨부 자료그림 참조). 특히 이 공정은 기존의 나노패턴에 적용하는 방식과 비교하여 제작시간을 수십 배 이상 줄일 수 있으며, 결함구조 내에 다른 형태의 기능성 물질도 규칙적으로 배열 할 수 있음을 확인하였다. 이는 다양한 형태의 패턴이 필요한 실제 반도체와 단백질 칩 등의 바이오 소자에 적용할 수 있는 가능성을 제시하고 있다 (자료그림 중 삽입사진 참조).
이번 연구결과로 LCD의 세계적 강국인 우리나라가 액정을 이용한 나노분야에서도 세계 최고의 원천기술을 갖게 되었다. 향후 액정을 이용한 새로운 응용의 신기원을 열게 되었으며, 나노-바이오 전자소자 산업분야에서 시장 선점 및 막대한 부가가치 창출 등을 통해 국가경쟁력 강화에 크게 기여할 것으로 기대된다. 연성재료(Soft Materials)를 이용하여 나노패턴을 제조하는 기술은 전 세계적으로 나노-바이오 분야에서 큰 이슈가 되는 연구로써, 연구의 핵심은 바이오 및 광전자소자 응용을 위하여 대면적에서 결함이 없는 소재의 개발에 있다. 이번 鄭 교수팀이 적용한 액정은 결함구조를 가지는 대표적인 물질로서 지금까지 학계에서는 대면적 나노패턴이 불가능하다고 인식돼 왔다.
鄭 교수는 “이번 연구결과는 연성소재를 이용한 나노패턴소자 제작방식의 기존 개념을 완전히 뒤엎는 것이다. 결함을 없애야만 한다는 기존의 생각에서 탈피하여 결함을 규칙적으로 구현하면 패턴에 이용할 수 있다는 발상의 전환으로 대면적 나노패턴을 개발했다는데 의미가 있으며, 향후 나노분야 전반에 걸쳐 영향이 클 것” 이라고 밝혔다.
이번 연구결과는 鄭 교수(교신저자)의 주도 하에 KAIST 물리학과 김만원 교수팀과 미국 캔트 주립대학의 액정센터 올래그 라브랜토비치(Oleg Lavrentovich)교수가 함께 일궈낸 성과다. 鄭 교수는 나노물질분야에서 사이언스, PNAS, Advanced Materials에 최정상급 논문을 다수 발표하는 등 나노물질 분야에서 차세대 주자로서 두각을 나타내고 있는 젊은 과학자다.
<해설>
액정: 유동성이 있으면서 고체적인 특성을 나타낸다. 전기적 특성이 매우 뛰어나 LCD 구동을 위한 핵심 물질로 사용된다. 네마틱, 스메틱, 콜레스테릭 등 다양한 종류의 액정이 존재한다. 현재 LCD에 사용하는 액정은 네마틱 액정이며 콜레스테릭 액정은 반사거울과 초정밀 온도계에 사용된다. 鄭 교수팀이 사용한 액정은 스메틱 액정으로서 네마틱 액정보다 자연계와 합성물질에서 더욱 많이 존재하고, 산업체와 학계에서 오랜기간 동안 연구해 왔음에도 불구하고 결함구조 등의 문제점으로 인하여 산업에 적용하지 못하고 있는 물질이다.
<첨부. 수 밀리미터 크기의 대면적 액정물질 나노패턴 현미경 사진>우측상단 삽입사진은 액정나노패턴내에 형광나노입자를 규칙적으로 포집한 리소그라피 제작사진
2007.10.15 조회수 27420 -
 시스템 생명공학 활용, 최고 수율의 아미노산 생산 균주 개발
- 세계 아미노산 시장, 화이트 바이오텍 제품 생산에 파급 효과 큰 원천 기술
- KAIST 이상엽 교수팀 개발, 미국 국립과학원회보 온라인판 게재KAIST(총장 서남표) 생명화학공학과 이상엽(李相燁, 43세, 특훈교수/LG화학 석좌교수) 교수팀은 시스템 생명공학 기법을 이용, 세계 최고 수율(收率)의 발린(L-valine) 생산 균주 개발에 성공했다. 이 연구 결과는 4월 넷째주(23일-27일사이) 미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the USA)에 게재된다.
李 교수팀은 필수 아미노산의 하나인 발린(L-valine)을 타켓 물질로 선정, 미생물 가상세포 시스템과 시뮬레이션 기법을 활용하여 최고 수율의 아미노산 생산 균주를 개발했다.
대장균 게놈에서 필요한 부위만을 선택적으로 조작하여 초기 생산 균주를 제작하고, DNA 칩을 이용한 전사체(transcriptome) 분석을 통해 새롭게 조작할 1차 타겟 유전자들을 발굴했다. 대장균 가상 세포인 MBEL979를 이용, 유전자 결실(缺失) 실험을 컴퓨터상에서 대량으로 수행한 뒤 2차 엔지니어링 타겟들을 발굴했다. 이 실험 결과를 실제 균주 개발에 적용, 세포내 대사흐름 최적화를 달성하여 최종적으로 100 그램의 포도당으로부터 37.8 그램의 발린을 추출할 수 있는 세계 최고 수율의 발린 생산균주 제작에 성공했다.
이상엽 교수는 “시스템 생명공학 기법이 체계적인 시스템 수준에서 균주개발에 성공적으로 이용됨에 따라, 기타 아미노산을 비롯하여 모든 생물공학산업 발전에 크게 기여할 것으로 기대된다. 초기에는 IT와 BT를 융합함에 있어 어려움이 많았으나 이를 슬기롭게 극복한 연구팀원들이 자랑스럽다.”고 말했다. 연구 관련 생산균주와 그 제조 방법은 국제특허(PCT)를 출원했다.
2007.04.24 조회수 24207
시스템 생명공학 활용, 최고 수율의 아미노산 생산 균주 개발
- 세계 아미노산 시장, 화이트 바이오텍 제품 생산에 파급 효과 큰 원천 기술
- KAIST 이상엽 교수팀 개발, 미국 국립과학원회보 온라인판 게재KAIST(총장 서남표) 생명화학공학과 이상엽(李相燁, 43세, 특훈교수/LG화학 석좌교수) 교수팀은 시스템 생명공학 기법을 이용, 세계 최고 수율(收率)의 발린(L-valine) 생산 균주 개발에 성공했다. 이 연구 결과는 4월 넷째주(23일-27일사이) 미국 국립과학원회보(PNAS, Proceedings of the National Academy of Sciences of the USA)에 게재된다.
李 교수팀은 필수 아미노산의 하나인 발린(L-valine)을 타켓 물질로 선정, 미생물 가상세포 시스템과 시뮬레이션 기법을 활용하여 최고 수율의 아미노산 생산 균주를 개발했다.
대장균 게놈에서 필요한 부위만을 선택적으로 조작하여 초기 생산 균주를 제작하고, DNA 칩을 이용한 전사체(transcriptome) 분석을 통해 새롭게 조작할 1차 타겟 유전자들을 발굴했다. 대장균 가상 세포인 MBEL979를 이용, 유전자 결실(缺失) 실험을 컴퓨터상에서 대량으로 수행한 뒤 2차 엔지니어링 타겟들을 발굴했다. 이 실험 결과를 실제 균주 개발에 적용, 세포내 대사흐름 최적화를 달성하여 최종적으로 100 그램의 포도당으로부터 37.8 그램의 발린을 추출할 수 있는 세계 최고 수율의 발린 생산균주 제작에 성공했다.
이상엽 교수는 “시스템 생명공학 기법이 체계적인 시스템 수준에서 균주개발에 성공적으로 이용됨에 따라, 기타 아미노산을 비롯하여 모든 생물공학산업 발전에 크게 기여할 것으로 기대된다. 초기에는 IT와 BT를 융합함에 있어 어려움이 많았으나 이를 슬기롭게 극복한 연구팀원들이 자랑스럽다.”고 말했다. 연구 관련 생산균주와 그 제조 방법은 국제특허(PCT)를 출원했다.
2007.04.24 조회수 24207