-
 인공지능 기반 대장암 3차원 게놈 지도 최초 해독
세계 최초로 예전에 비해 최대 규모로 한국인 대장암 환자 3차원 게놈 지도를 작성하여 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 서울대학교 암연구소 김태유 교수 연구팀과의 공동연구를 통해 인공지능 기반 알고리즘을 활용, 한국인 대장암 환자의 3차원 게놈 지도를 최초로 제시했으며 이를 토대로 암 세포 특이적인 유전자 조절 기전을 통해 특정 종양유전자들이 과발현되는 현상을 규명했다고 24일 밝혔다.
1차원적 게놈 서열 분석에 기반한 현재의 암 유전체 연구는 종양유전자들의 과발현 기작을 설명하는데 한계가 있었다. 하지만 3차원 공간상에 게놈이 어떻게 배열되는지를 분석하는 3차원 게놈 (3D genome) 구조 연구는 이러한 한계를 극복 가능케 하고 있다. 본 연구에서는 정상 세포에서는 존재하지 않는 암 세포 특이적 염색질 고리(chromatin loop) 구조가 유전자 발현 촉진 인자인 인핸서와 종양유전자 사이의 상호작용을 형성하여 과발현을 유도하는 인핸서 납치(enhancer-hijacking) 현상에 초점을 두어 연구하였다.
우리 대학 생명과학과 김규광 박사과정이 주도한 이번 연구는 게놈간의 공간상 상호작용을 측정할 수 있는 대용량 염색체 구조 포착 Hi-C (High-throughput Chromosome Conformation Capture) 실험 기법을 활용하여 대장암 3차원 게놈 지도를 작성하고 대장암 특이적 3차원 게놈 변화를 환자 개개인별로 분석할 수 있는 인공지능 기반 알고리즘을 개발했다. 그 결과 공동연구팀은 광범위한 규모의 3차원 게놈 구조 변화와 이로 인한 다양한 종양유전자의 활성화를 확인했다.
연구팀은 이번 연구를 통해 암 특이적 3차원 게놈 구조의 변화로 인한 종양유전자 활성 기작을 명확히 제시하였으며 이로 인한 환자 예후와 약물 반응 등 임상적인 특성과의 연관성까지 제시해 맞춤 치료 원천기술 확보에 기여했다.
지금까지 암 세포주에 대한 3차원 게놈 구조 연구는 일부 보고 되었으나, 대규모 환자 암조직에 대한 연구는 조직 내 세포 이질성, 종양 순도, 암세포 이질성 등의 문제로 인한 정밀 암 특이적 3차원 게놈 구조 분석의 한계로 수행되지 못하였다.
반면에 이번 연구에서 연구팀은 AI 기반 알고리즘으로 환자 개인 종양 조직으로부터 얻어진 복잡한 신호를 해석할 수 있었으며 그 결과 최대 규모인 환자 40명의 종양 조직과 인접한 정상 대장 조직을 사용해 3차원 게놈 지도를 작성할 수 있었다. 또한 DNA 서열정보를 보여주는 전장유전체 지도의 경우 다양한 인종에 대해 생산되고 있고 한국인의 전장유전체 지도 또한 개발되었으나 한국인 3차원 게놈 지도, 특히 종양 조직에 대한 3차원 게놈 지도는 이번 연구에서 최초로 제시됐다.
이번 연구 결과는 국제 학술지, `셀 리포츠(Cell Reports, IF=9.995)'에 7월 13일 자로 출판됐다. (논문명: Spatial and clonality-resolved 3D cancer genome alterations reveal enhancer-hijacking as a potential prognostic marker for colorectal cancer)
서울대학교병원 혈액종양내과 김태유 교수는 “이러한 결과는 개별 암 환자들마다 서로 다르게 나타나는 종양 이질성을 이해하는 데 매우 중요한 요소가 될 수 있으며, 이를 이용한 환자 맞춤형 치료 연구의 시발점이 될 것이다”라고 말했다. 생명과학과 정인경 교수는 “기존의 점돌연변이나 유전체 변이만으로는 설명이 어려운 암 유전체를 3차원 게놈 구조 관점에서 재해독하고 신규 암 타겟을 발굴할 수 있는 수 있는 새로운 접근법을 제시했다”라고 밝혔다.
한편 이번 연구는 과학기술정보통신부와 서경배과학재단의 지원을 받아 수행됐다.
인공지능 기반 대장암 3차원 게놈 지도 최초 해독
세계 최초로 예전에 비해 최대 규모로 한국인 대장암 환자 3차원 게놈 지도를 작성하여 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 서울대학교 암연구소 김태유 교수 연구팀과의 공동연구를 통해 인공지능 기반 알고리즘을 활용, 한국인 대장암 환자의 3차원 게놈 지도를 최초로 제시했으며 이를 토대로 암 세포 특이적인 유전자 조절 기전을 통해 특정 종양유전자들이 과발현되는 현상을 규명했다고 24일 밝혔다.
1차원적 게놈 서열 분석에 기반한 현재의 암 유전체 연구는 종양유전자들의 과발현 기작을 설명하는데 한계가 있었다. 하지만 3차원 공간상에 게놈이 어떻게 배열되는지를 분석하는 3차원 게놈 (3D genome) 구조 연구는 이러한 한계를 극복 가능케 하고 있다. 본 연구에서는 정상 세포에서는 존재하지 않는 암 세포 특이적 염색질 고리(chromatin loop) 구조가 유전자 발현 촉진 인자인 인핸서와 종양유전자 사이의 상호작용을 형성하여 과발현을 유도하는 인핸서 납치(enhancer-hijacking) 현상에 초점을 두어 연구하였다.
우리 대학 생명과학과 김규광 박사과정이 주도한 이번 연구는 게놈간의 공간상 상호작용을 측정할 수 있는 대용량 염색체 구조 포착 Hi-C (High-throughput Chromosome Conformation Capture) 실험 기법을 활용하여 대장암 3차원 게놈 지도를 작성하고 대장암 특이적 3차원 게놈 변화를 환자 개개인별로 분석할 수 있는 인공지능 기반 알고리즘을 개발했다. 그 결과 공동연구팀은 광범위한 규모의 3차원 게놈 구조 변화와 이로 인한 다양한 종양유전자의 활성화를 확인했다.
연구팀은 이번 연구를 통해 암 특이적 3차원 게놈 구조의 변화로 인한 종양유전자 활성 기작을 명확히 제시하였으며 이로 인한 환자 예후와 약물 반응 등 임상적인 특성과의 연관성까지 제시해 맞춤 치료 원천기술 확보에 기여했다.
지금까지 암 세포주에 대한 3차원 게놈 구조 연구는 일부 보고 되었으나, 대규모 환자 암조직에 대한 연구는 조직 내 세포 이질성, 종양 순도, 암세포 이질성 등의 문제로 인한 정밀 암 특이적 3차원 게놈 구조 분석의 한계로 수행되지 못하였다.
반면에 이번 연구에서 연구팀은 AI 기반 알고리즘으로 환자 개인 종양 조직으로부터 얻어진 복잡한 신호를 해석할 수 있었으며 그 결과 최대 규모인 환자 40명의 종양 조직과 인접한 정상 대장 조직을 사용해 3차원 게놈 지도를 작성할 수 있었다. 또한 DNA 서열정보를 보여주는 전장유전체 지도의 경우 다양한 인종에 대해 생산되고 있고 한국인의 전장유전체 지도 또한 개발되었으나 한국인 3차원 게놈 지도, 특히 종양 조직에 대한 3차원 게놈 지도는 이번 연구에서 최초로 제시됐다.
이번 연구 결과는 국제 학술지, `셀 리포츠(Cell Reports, IF=9.995)'에 7월 13일 자로 출판됐다. (논문명: Spatial and clonality-resolved 3D cancer genome alterations reveal enhancer-hijacking as a potential prognostic marker for colorectal cancer)
서울대학교병원 혈액종양내과 김태유 교수는 “이러한 결과는 개별 암 환자들마다 서로 다르게 나타나는 종양 이질성을 이해하는 데 매우 중요한 요소가 될 수 있으며, 이를 이용한 환자 맞춤형 치료 연구의 시발점이 될 것이다”라고 말했다. 생명과학과 정인경 교수는 “기존의 점돌연변이나 유전체 변이만으로는 설명이 어려운 암 유전체를 3차원 게놈 구조 관점에서 재해독하고 신규 암 타겟을 발굴할 수 있는 수 있는 새로운 접근법을 제시했다”라고 밝혔다.
한편 이번 연구는 과학기술정보통신부와 서경배과학재단의 지원을 받아 수행됐다.
2023.07.24
조회수 8843
-
 천식 등 만성질환 염증 조절 실마리 풀어
우리 몸에 침입한 병원균이나 암세포를 치료할 수 있는 면역세포인 T세포 중 CD4+ T세포는 적응면역계의 지휘관과 같은 역할을 하며, 이러한 CD4+ T세포의 활성 정도에 따라서 천식과 같은 만성질환의 진행 양상과 예후가 달라지게 된다. T세포의 활성화 증폭을 위해서는 마치 과녁 모양처럼 면역학적 시냅스 형성이 필요하다는 보고들이 있으나 어떠한 메커니즘으로 면역학적 시냅스가 형성이 되는지는 잘 알려져 있지 않았다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 면역학적 시냅스 형성에 섬모 형성 단백질(IFT20)과 엔도솜 형성 단백질(TSG101)의 결합이 중요한 역할을 한다고 26일 밝혔다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사), 강인 박사과정, 생명과학과 김유민 박사과정 등이 주도한 이번 연구에서 연구팀은 단일세포 전사체 분석법을 활용해 활성화된 CD4+ T세포에서 섬모 형성 단백질(IFT20)의 발현이 증가해 있음을 확인했다.
연구팀은 T세포에 국한되어 섬모 형성 단백질(IFT20)이 결핍된 마우스를 제작해 해당 마우스가 정상 마우스보다 천식 증상의 특징이 감소함을 확인했고, 이는 정상 CD4+ T세포와 비교했을 때 섬모 형성 단백질(IFT20) 결핍 CD4+ T세포가 면역학적 시냅스 형성을 감소시켜 T세포 증식, 해당작용 및 세포호흡이 감소하기 때문임을 확인했다.
또한, 연구팀은 섬모 형성 단백질(IFT20)에 결합하는 단백질을 찾기 위해 효모단백질잡종법과 면역침강법을 이용함으로써 섬모 형성 단백질(IFT20)이 엔도솜 형성단백질(TSG101)과 서로 결합한다는 것을 세계 최초로 규명했다.
이를 입증하기 위해 연구팀은 T세포에 국한되어 엔도솜 형성단백질(TSG101)이 결핍된 마우스를 제작해 엔도솜 형성단백질(TSG101)이 결핍된 CD4+ T세포가 정상 CD4+ T세포에 비해 면역학적 시냅스 형성이 감소함을 확인했다. 결과적으로 기존에 알려지지 않았던 면역학적 시냅스 형성에 기여하는 섬모형성 단백질(IFT20)과 엔도솜 형성단백질(TSG101)의 역할을 밝힘으로써 T세포 활성화를 조절할 수 있는 단서를 제공했다는 점에서 큰 의의가 있다.
이번 연구를 주도한 정지웅 박사는 "그동안 잘 알려지지 않은 면역학적 시냅스 형성을 조절하는 단백질을 확인하는 중요한 연구”라고 설명했다. 이흥규 교수는 “면역학적 시냅스 형성의 변화를 통해 천식의 염증 정도가 변화할 수 있음을 확인했고, 향후 면역학적 시냅스를 조절함으로써 천식을 비롯한 다양한 면역 질환 등에서 질환의 염증을 조절하는 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사)가 제1 저자로 참여한 이번 연구는 면역학 분야 국제 학술지 `세포 및 분자 면역학(Cellular & Molecular Immunology, JCR IF = 22.10)'에 4월 7일 字 온라인판에 게재됐다. (논문명: Regulation of c-SMAC formation and AKT-mTOR signaling by the TSG101-IFT20 axis in CD4+ T cells)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업 및 글로벌박사양성사업의 지원을 받아 수행됐다.
천식 등 만성질환 염증 조절 실마리 풀어
우리 몸에 침입한 병원균이나 암세포를 치료할 수 있는 면역세포인 T세포 중 CD4+ T세포는 적응면역계의 지휘관과 같은 역할을 하며, 이러한 CD4+ T세포의 활성 정도에 따라서 천식과 같은 만성질환의 진행 양상과 예후가 달라지게 된다. T세포의 활성화 증폭을 위해서는 마치 과녁 모양처럼 면역학적 시냅스 형성이 필요하다는 보고들이 있으나 어떠한 메커니즘으로 면역학적 시냅스가 형성이 되는지는 잘 알려져 있지 않았다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 면역학적 시냅스 형성에 섬모 형성 단백질(IFT20)과 엔도솜 형성 단백질(TSG101)의 결합이 중요한 역할을 한다고 26일 밝혔다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사), 강인 박사과정, 생명과학과 김유민 박사과정 등이 주도한 이번 연구에서 연구팀은 단일세포 전사체 분석법을 활용해 활성화된 CD4+ T세포에서 섬모 형성 단백질(IFT20)의 발현이 증가해 있음을 확인했다.
연구팀은 T세포에 국한되어 섬모 형성 단백질(IFT20)이 결핍된 마우스를 제작해 해당 마우스가 정상 마우스보다 천식 증상의 특징이 감소함을 확인했고, 이는 정상 CD4+ T세포와 비교했을 때 섬모 형성 단백질(IFT20) 결핍 CD4+ T세포가 면역학적 시냅스 형성을 감소시켜 T세포 증식, 해당작용 및 세포호흡이 감소하기 때문임을 확인했다.
또한, 연구팀은 섬모 형성 단백질(IFT20)에 결합하는 단백질을 찾기 위해 효모단백질잡종법과 면역침강법을 이용함으로써 섬모 형성 단백질(IFT20)이 엔도솜 형성단백질(TSG101)과 서로 결합한다는 것을 세계 최초로 규명했다.
이를 입증하기 위해 연구팀은 T세포에 국한되어 엔도솜 형성단백질(TSG101)이 결핍된 마우스를 제작해 엔도솜 형성단백질(TSG101)이 결핍된 CD4+ T세포가 정상 CD4+ T세포에 비해 면역학적 시냅스 형성이 감소함을 확인했다. 결과적으로 기존에 알려지지 않았던 면역학적 시냅스 형성에 기여하는 섬모형성 단백질(IFT20)과 엔도솜 형성단백질(TSG101)의 역할을 밝힘으로써 T세포 활성화를 조절할 수 있는 단서를 제공했다는 점에서 큰 의의가 있다.
이번 연구를 주도한 정지웅 박사는 "그동안 잘 알려지지 않은 면역학적 시냅스 형성을 조절하는 단백질을 확인하는 중요한 연구”라고 설명했다. 이흥규 교수는 “면역학적 시냅스 형성의 변화를 통해 천식의 염증 정도가 변화할 수 있음을 확인했고, 향후 면역학적 시냅스를 조절함으로써 천식을 비롯한 다양한 면역 질환 등에서 질환의 염증을 조절하는 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사)가 제1 저자로 참여한 이번 연구는 면역학 분야 국제 학술지 `세포 및 분자 면역학(Cellular & Molecular Immunology, JCR IF = 22.10)'에 4월 7일 字 온라인판에 게재됐다. (논문명: Regulation of c-SMAC formation and AKT-mTOR signaling by the TSG101-IFT20 axis in CD4+ T cells)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업 및 글로벌박사양성사업의 지원을 받아 수행됐다.
2023.04.26
조회수 8011
-
 노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
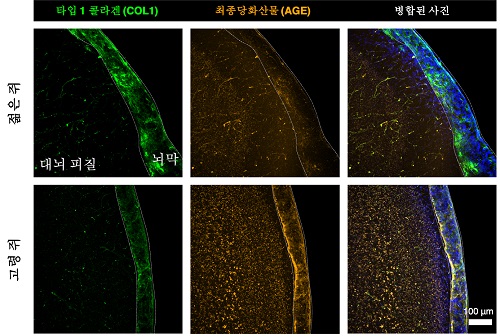
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
2023.03.15
조회수 7726
-
 비만이 성병 헤르페스를 억제하는 메커니즘 규명
우리 연구진이 성병을 일으키는 2형 헤르페스 감염에 대해 비만인 암컷 생쥐가 더 높은 저항성을 갖는다는 사실을 밝혔다. 나쁘기만 할 것 같은 비만이 오히려 도움이 되는 역설적인 현상을 관찰한 것이다.
※ 2형 헤르페스: 헤르페스 바이러스의 일종으로 주로 성병을 일으키는 것으로 알려짐. 여성이 남성보다 더 높은 감염률을 보이는 것으로 알려짐.
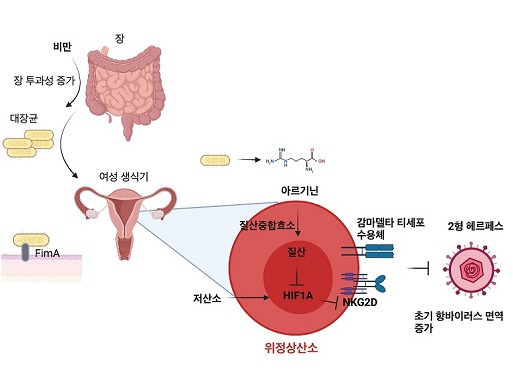
의과학대학원 이흥규 교수 연구팀이 비만이 여성 생식기를 통한 단순 2형 헤르페스 바이러스(herpes simplex virus type 2) 감염에 대해 저항성을 강화하는 현상을 발견했으며, 그 메커니즘을 규명했음을 6일 밝혔다.
비만은 종양 등 각종 질병에 대해 안 좋은 영향을 끼치는 인자로 잘 알려져 있다. 하지만, 여성 생식기를 통한 2형 헤르페스 감염 시 질 내 공생미생물과 감마델타 T세포의 상호작용을 통해 바이러스에 저항성이 생긴다는 사실을 연구팀은 발견했다.
여성의 생식기 내에는 젖산균을 포함한 공생미생물이 서식하고 있다. 비만인 여성은 마른 여성과는 질 내 공생미생물의 조성이 다른 것으로 알려져 있는데, 연구팀은 비만인 암컷 생쥐의 질 내에는 장에서 유래한 것으로 보이는 균들이 섞여 있는 것을 발견했다.
연구팀은 장에서 유래된 것으로 보이는 비만 암컷 생쥐의 질 내에 유입된 균들이 아미노산의 일종인 아르기닌을 활발하게 생산하고 있다는 사실을 발견했고, 아르기닌이 바이러스 초기 감염에 중요한 역할을 한다는 사실을 발견했다.
연구팀은 이어서 아르기닌이 질 내의 감마델타 T 세포의 항바이러스 면역반응을 강화하고, 적응 면역세포가 활성화되는 시기보다 이른 시기에 바이러스 감염과 전파를 이미 억제하고 있음을 발견했다.
연구를 주도한 의과학대학원 이흥규 교수는 "이번 연구는 비만이 특정 감염 질병에는 도움이 될 수도 있다는 사실을 밝혔다는 점에서 의의가 있고, 앞으로 비만인 환자들의 바이러스 감염증 치료에 참고가 될 것이며, 연구 결과를 바탕으로 분자 메커니즘을 응용해 항바이러스제 개발에 박차를 가할 것이다ˮ고 연구의 중요성을 설명했다.
비만이 바이러스를 억제하는 현상을 발견하고 그 메커니즘을 규명한 이번 연구는 한국연구재단의 중견연구지원사업 및 바이오의료기술개발사업의 지원으로 수행됐으며, 의과학대학원 박장현 박사가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제학술지 `셀 리포트(Cell Reports)'에 지난 11월 8일 字 게재됐다.
비만이 성병 헤르페스를 억제하는 메커니즘 규명
우리 연구진이 성병을 일으키는 2형 헤르페스 감염에 대해 비만인 암컷 생쥐가 더 높은 저항성을 갖는다는 사실을 밝혔다. 나쁘기만 할 것 같은 비만이 오히려 도움이 되는 역설적인 현상을 관찰한 것이다.
※ 2형 헤르페스: 헤르페스 바이러스의 일종으로 주로 성병을 일으키는 것으로 알려짐. 여성이 남성보다 더 높은 감염률을 보이는 것으로 알려짐.
의과학대학원 이흥규 교수 연구팀이 비만이 여성 생식기를 통한 단순 2형 헤르페스 바이러스(herpes simplex virus type 2) 감염에 대해 저항성을 강화하는 현상을 발견했으며, 그 메커니즘을 규명했음을 6일 밝혔다.
비만은 종양 등 각종 질병에 대해 안 좋은 영향을 끼치는 인자로 잘 알려져 있다. 하지만, 여성 생식기를 통한 2형 헤르페스 감염 시 질 내 공생미생물과 감마델타 T세포의 상호작용을 통해 바이러스에 저항성이 생긴다는 사실을 연구팀은 발견했다.
여성의 생식기 내에는 젖산균을 포함한 공생미생물이 서식하고 있다. 비만인 여성은 마른 여성과는 질 내 공생미생물의 조성이 다른 것으로 알려져 있는데, 연구팀은 비만인 암컷 생쥐의 질 내에는 장에서 유래한 것으로 보이는 균들이 섞여 있는 것을 발견했다.
연구팀은 장에서 유래된 것으로 보이는 비만 암컷 생쥐의 질 내에 유입된 균들이 아미노산의 일종인 아르기닌을 활발하게 생산하고 있다는 사실을 발견했고, 아르기닌이 바이러스 초기 감염에 중요한 역할을 한다는 사실을 발견했다.
연구팀은 이어서 아르기닌이 질 내의 감마델타 T 세포의 항바이러스 면역반응을 강화하고, 적응 면역세포가 활성화되는 시기보다 이른 시기에 바이러스 감염과 전파를 이미 억제하고 있음을 발견했다.
연구를 주도한 의과학대학원 이흥규 교수는 "이번 연구는 비만이 특정 감염 질병에는 도움이 될 수도 있다는 사실을 밝혔다는 점에서 의의가 있고, 앞으로 비만인 환자들의 바이러스 감염증 치료에 참고가 될 것이며, 연구 결과를 바탕으로 분자 메커니즘을 응용해 항바이러스제 개발에 박차를 가할 것이다ˮ고 연구의 중요성을 설명했다.
비만이 바이러스를 억제하는 현상을 발견하고 그 메커니즘을 규명한 이번 연구는 한국연구재단의 중견연구지원사업 및 바이오의료기술개발사업의 지원으로 수행됐으며, 의과학대학원 박장현 박사가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제학술지 `셀 리포트(Cell Reports)'에 지난 11월 8일 字 게재됐다.
2022.12.06
조회수 9386
-
 장 조직의 항상성과 염증성 장염 회복의 핵심 효소 발견
우리 대학 생명과학과 김세윤, 양한슬 교수 공동연구팀이 `장 상피조직의 발생과 염증성 장염 회복과정의 핵심 효소발굴'에 성공했다고 6일 밝혔다.
생명과학과 박승은 박사, 이동은 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `세포 및 분자 소화기학 및 간장학 (Cellular and Molecular Gastroenterology & Hepatology)'에 지난 8월 19일 字 온라인 게재됐다.
※ 논문명 : Gut Epithelial Inositol Polyphosphate Multikinase Alleviates Experimental Colitis via Governing Tuft Cell Homeostasis
※ 저자 정보 : 박승은 (한국과학기술원, 공동 제1 저자), 이동은 (한국과학기술원, 공동 제1 저자), 정재웅 (연세대학교 의과대학, 제2 저자), 이수형 (반더빌트 의과대학, 공동 저자), 박승주 (한국과학기술원, 공동 저자), 류재승 (한국과학기술원, 공동 저자), 오세규 (카이노젠, 공동 저자), 양한슬 (한국과학기술원, 공동 교신저자), 황성순 (연세대학교 의과대학, 공동 교신저자), 김세윤 (한국과학기술원, 공동 교신저자), 포함 총 10명
염증성 장 질환은 1980년대 중반까지만 해도 국내 발병률은 매우 낮은 질환이었으나 건강보험심사평가원 자료에 따르면 2011년 말 만성 염증성 장 질환인 크론병 환자가 1만3천여 명, 궤양성 대장염 환자가 2만9천여 명으로 집계됐으며 이후로도 환자 수가 빠르게 증가하고 있다.
궤양성 대장염과 크론병과 같은 염증성 장 질환(Inflammatory bowel disease)은 복통, 설사뿐 아니라 전신 무력감, 체중 감소, 장 천공 등의 합병증을 유발해 환자의 삶의 질을 크게 낮추는 심각한 질환이다.
이러한 염증성 장 질환은 아직 발병 메커니즘이 명확하게 규명되지 않았으며 서구화된 식습관과 함께 유전적 이상이나 면역학적 장애 또는 스트레스와 같은 환경적인 요인이 복합적으로 관여하는 것으로 여겨진다.
최근 염증성 장 질환의 환자군 일부에서 이노시톨 대사(체내 합성 또는 음식을 통하여 공급되는 이노시톨 영양소를 이노시톨 인산 물질들로 전환하는 세포 내 생화학적 반응)의 핵심 효소인 이노시톨 폴리인산 카이네이즈(Inositol polyphosphate multikinase, 이하 IPMK) 유전자에서 단일염기변이(single nucleotide polymorphism, SNP) 등이 보고됐다. IPMK 효소는 포유류의 이노시톨 대사에서 매우 중추적인 역할을 하는 단백질로서 세포의 성장과 대사뿐 아니라 면역 반응 및 중추 신경계 기억 조절 등의 다각적인 생물학적 기능을 수행하는 것으로 알려졌으나 소화기계에서의 생물학적 기능은 밝혀진 바가 전혀 없다.
이에 우리 대학 생명과학과 및 줄기세포 연구센터 김세윤 교수, 양한슬 교수 연구팀은 연세대학교 의과대학 황성순 교수 연구팀과의 공동연구를 통해 장 상피세포에서의 IPMK 효소의 역할규명연구를 다각적으로 수행했다.
연구팀은 먼저 장 상피세포에서 IPMK 유전자가 결손된 생쥐 연구모델을 제작했고 이를 분석한 결과에 따르면 정상적인 환경에서는 뚜렷한 장 조직의 구조와 기능에 있어 문제가 발생하지 않았다. 그러나 덱스트란 황산나트륨(DSS)을 투여해 대장염을 유발할 경우, IPMK 유전자가 결손된 생쥐로부터 대장염 회복반응이 현저하게 둔화됨을 관찰했고 이로부터 IPMK 효소가 손상된 대장 조직이 회복되는데 필수적인 인자임을 규명했다.
특히 연구팀은 IPMK 효소가 제거된 장 조직에서는 솔세포(tuft cell)의 발생과 기능에 심각한 장애가 발생함을 관찰했다. 솔세포란 소장과 대장뿐 아니라 흉선, 췌장 등에 존재하는 세포로서 표면에 미세 융모구조를 보이는 독특한 세포다. 장 조직의 전체 세포 중 불과 2~3% 이하로 존재하는 솔세포는 외부로부터의 기생충 감염에 대응하는 면역기능을 수행한다. 또한 솔세포로부터 합성돼 분비되는 아세틸콜린 신경전달물질은 장내 줄기세포 및 신경세포를 자극해 장 조직의 항상성 유지와 손상 복구에 중요한 기능을 담당하는 것으로 알려져 있다. 이러한 중요성에도 불구하고 솔세포의 발생과 기능을 조절하는 분자 타깃에 대한 이해는 극히 부족한 것으로 알려져 있다.
공동연구팀은 첨단 단일세포 RNA 유전자 배열 순서 분석기술(single cell RNA sequencing)을 통해 IPMK 효소가 제거된 장 상피조직에서 아세틸콜린 분비를 담당하는 솔세포군의 발생이 특이적으로 감소함을 규명했다. 또한 이러한 분석과정에서 생쥐의 대장에 존재하는 솔세포는 크게 면역기능을 담당하는 세포군, 아세틸콜린 분비 솔세포군 외에 유전자 발현 능력이 감소한 새로운 솔세포군이 있다는 사실을 발견해 학계에 최초 보고했다.
연구팀 관계자는 "발굴한 IPMK 효소에 기반한 아세틸콜린 분비성 솔세포의 발생 및 기능조절은 향후 장 상피조직의 항상성 유지의 학문적 이해와 더불어 염증성 장 질환의 진단 및 치료기술 개발 등에 적극적으로 활용될 것ˮ이라며 연구의 의의를 설명했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 서경배과학재단, KAIST 줄기세포 연구센터 지원사업, KAIST 그랜드챌린지 30 (KC30) 사업 및 포스코청암펠로십의 지원을 받아 수행됐다.
장 조직의 항상성과 염증성 장염 회복의 핵심 효소 발견
우리 대학 생명과학과 김세윤, 양한슬 교수 공동연구팀이 `장 상피조직의 발생과 염증성 장염 회복과정의 핵심 효소발굴'에 성공했다고 6일 밝혔다.
생명과학과 박승은 박사, 이동은 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `세포 및 분자 소화기학 및 간장학 (Cellular and Molecular Gastroenterology & Hepatology)'에 지난 8월 19일 字 온라인 게재됐다.
※ 논문명 : Gut Epithelial Inositol Polyphosphate Multikinase Alleviates Experimental Colitis via Governing Tuft Cell Homeostasis
※ 저자 정보 : 박승은 (한국과학기술원, 공동 제1 저자), 이동은 (한국과학기술원, 공동 제1 저자), 정재웅 (연세대학교 의과대학, 제2 저자), 이수형 (반더빌트 의과대학, 공동 저자), 박승주 (한국과학기술원, 공동 저자), 류재승 (한국과학기술원, 공동 저자), 오세규 (카이노젠, 공동 저자), 양한슬 (한국과학기술원, 공동 교신저자), 황성순 (연세대학교 의과대학, 공동 교신저자), 김세윤 (한국과학기술원, 공동 교신저자), 포함 총 10명
염증성 장 질환은 1980년대 중반까지만 해도 국내 발병률은 매우 낮은 질환이었으나 건강보험심사평가원 자료에 따르면 2011년 말 만성 염증성 장 질환인 크론병 환자가 1만3천여 명, 궤양성 대장염 환자가 2만9천여 명으로 집계됐으며 이후로도 환자 수가 빠르게 증가하고 있다.
궤양성 대장염과 크론병과 같은 염증성 장 질환(Inflammatory bowel disease)은 복통, 설사뿐 아니라 전신 무력감, 체중 감소, 장 천공 등의 합병증을 유발해 환자의 삶의 질을 크게 낮추는 심각한 질환이다.
이러한 염증성 장 질환은 아직 발병 메커니즘이 명확하게 규명되지 않았으며 서구화된 식습관과 함께 유전적 이상이나 면역학적 장애 또는 스트레스와 같은 환경적인 요인이 복합적으로 관여하는 것으로 여겨진다.
최근 염증성 장 질환의 환자군 일부에서 이노시톨 대사(체내 합성 또는 음식을 통하여 공급되는 이노시톨 영양소를 이노시톨 인산 물질들로 전환하는 세포 내 생화학적 반응)의 핵심 효소인 이노시톨 폴리인산 카이네이즈(Inositol polyphosphate multikinase, 이하 IPMK) 유전자에서 단일염기변이(single nucleotide polymorphism, SNP) 등이 보고됐다. IPMK 효소는 포유류의 이노시톨 대사에서 매우 중추적인 역할을 하는 단백질로서 세포의 성장과 대사뿐 아니라 면역 반응 및 중추 신경계 기억 조절 등의 다각적인 생물학적 기능을 수행하는 것으로 알려졌으나 소화기계에서의 생물학적 기능은 밝혀진 바가 전혀 없다.
이에 우리 대학 생명과학과 및 줄기세포 연구센터 김세윤 교수, 양한슬 교수 연구팀은 연세대학교 의과대학 황성순 교수 연구팀과의 공동연구를 통해 장 상피세포에서의 IPMK 효소의 역할규명연구를 다각적으로 수행했다.
연구팀은 먼저 장 상피세포에서 IPMK 유전자가 결손된 생쥐 연구모델을 제작했고 이를 분석한 결과에 따르면 정상적인 환경에서는 뚜렷한 장 조직의 구조와 기능에 있어 문제가 발생하지 않았다. 그러나 덱스트란 황산나트륨(DSS)을 투여해 대장염을 유발할 경우, IPMK 유전자가 결손된 생쥐로부터 대장염 회복반응이 현저하게 둔화됨을 관찰했고 이로부터 IPMK 효소가 손상된 대장 조직이 회복되는데 필수적인 인자임을 규명했다.
특히 연구팀은 IPMK 효소가 제거된 장 조직에서는 솔세포(tuft cell)의 발생과 기능에 심각한 장애가 발생함을 관찰했다. 솔세포란 소장과 대장뿐 아니라 흉선, 췌장 등에 존재하는 세포로서 표면에 미세 융모구조를 보이는 독특한 세포다. 장 조직의 전체 세포 중 불과 2~3% 이하로 존재하는 솔세포는 외부로부터의 기생충 감염에 대응하는 면역기능을 수행한다. 또한 솔세포로부터 합성돼 분비되는 아세틸콜린 신경전달물질은 장내 줄기세포 및 신경세포를 자극해 장 조직의 항상성 유지와 손상 복구에 중요한 기능을 담당하는 것으로 알려져 있다. 이러한 중요성에도 불구하고 솔세포의 발생과 기능을 조절하는 분자 타깃에 대한 이해는 극히 부족한 것으로 알려져 있다.
공동연구팀은 첨단 단일세포 RNA 유전자 배열 순서 분석기술(single cell RNA sequencing)을 통해 IPMK 효소가 제거된 장 상피조직에서 아세틸콜린 분비를 담당하는 솔세포군의 발생이 특이적으로 감소함을 규명했다. 또한 이러한 분석과정에서 생쥐의 대장에 존재하는 솔세포는 크게 면역기능을 담당하는 세포군, 아세틸콜린 분비 솔세포군 외에 유전자 발현 능력이 감소한 새로운 솔세포군이 있다는 사실을 발견해 학계에 최초 보고했다.
연구팀 관계자는 "발굴한 IPMK 효소에 기반한 아세틸콜린 분비성 솔세포의 발생 및 기능조절은 향후 장 상피조직의 항상성 유지의 학문적 이해와 더불어 염증성 장 질환의 진단 및 치료기술 개발 등에 적극적으로 활용될 것ˮ이라며 연구의 의의를 설명했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 서경배과학재단, KAIST 줄기세포 연구센터 지원사업, KAIST 그랜드챌린지 30 (KC30) 사업 및 포스코청암펠로십의 지원을 받아 수행됐다.
2022.10.06
조회수 10781
-
 유방암 환자의 면역 항암치료 원리 발견해 효과적인 치료 전략 제시
우리 대학 의과학대학원 신의철 교수 연구팀이 연세대학교 의과대학 김승일 교수, 가톨릭대 의과대학 박우찬 교수 연구팀과 공동 연구를 통해 유방암 환자의 면역 항암치료 핵심 원리를 발견했다고 14일 밝혔다.
이번 연구를 통해, 최근 유행하는 면역 항암치료에 좋은 반응을 보일 것으로 예상되는 유방암 환자들을 선별해 효과적인 암 치료 전략을 제시할 것으로 기대된다.
연세대학교 의과대학 외과학 교실 이용준 강사, 김지예 임상 조교수가 공동 제1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 `사이언스 면역학(Science Immunology)' 8월 26일 字 온라인판에 게재됐다. (논문명 : CD39+ tissue-resident memory CD8+ T cells with a clonal overlap across compartments mediate anti-tumor immunity in breast cancer)
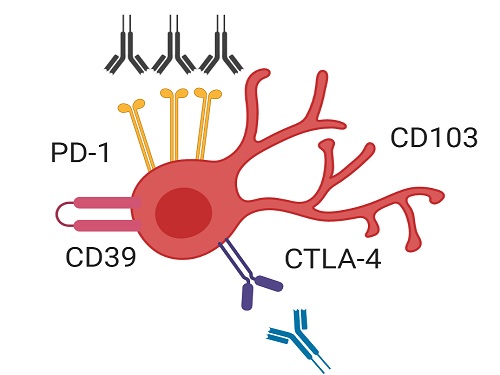
암 환자는 암세포에 대항해 이를 제거하는 역할을 하는 세포독성 T세포의 기능이 현저히 약해져 암세포에 대한 효과적인 면역반응을 나타내지 못한다. 이러한 세포독성 T세포 약화의 주된 이유는 PD-1이라는 세포독성 T세포의 기능을 저하하는 억제 수용체가 종양 조직 내 세포독성 T세포에 과다하게 발현되기 때문으로 알려져 있다.
최근 유행하고 있는 면역항암제의 기본원리는 바로 이 PD-1 억제 수용체의 기능을 차단해 약화돼 있던 세포독성 T세포의 기능을 회복시키는 것이다. 이러한 면역항암제는 유방암 환자에게서 기존의 치료를 대체할 수 있는 표준치료로 자리 잡아 가고 있지만, 투여받은 유방암 환자 중 일부에서만 치료 효과가 나타나며 이에 대한 이유를 알지 못하고 있다. 따라서, 많은 연구자가 유방암에서 면역 항암치료의 기전을 이해하고 치료에 효과를 보이는 환자를 선별하고자 하는 연구를 활발히 수행하고 있다.
이번 연구에서 공동 연구팀은 종양 조직에 존재하는 세포독성 T세포 중에서도 CD39 단백질과 조직 상주 마커 단백질을 동시에 발현하는 조직 상주 기억 T세포(CD39+ tissue-resident memory CD8+ T cell)가 유방암 환자에서 효과적인 항암 면역반응을 매개하는 핵심 면역세포임을 새롭게 밝혔다.
종양 조직에 존재하는 세포독성 T세포 중에는 항암 면역반응에 영향을 주지 않는 방관자(bystander) 세포들이 존재한다는 사실은 이미 잘 알려져 있었다. 이렇게 항암 면역반응과는 상관없는 방관자 세포들도 종양 조직에 있기 때문에 암 환자의 항암 면역반응을 정확히 측정하고 분석하는 데 어려움이 있었다. 연구팀은 CD39 단백질과 조직 상주 마커 단백질의 발현을 측정해 항암 면역반응과 관련이 있는 세포독성 T세포들만 분리해 개별 환자의 항암 면역반응을 정확히 측정할 수 있음을 새롭게 밝혔다.
그리고 유방암 환자에서 CD39를 발현하는 조직 상주 기억 세포독성 T세포는 특징적으로 삼중음성유방암(triple-negative breast cancer) 환자에게서 증가해 있었고, CD39를 발현하는 조직 상주 기억 세포독성 T세포가 증가해 있는 유방암 환자들은 수술 이후에도 재발이 적게 나타나는 등 좋은 예후를 보였다.
이번 연구에서 연구팀은 유방암 환자에서 면역항암제 치료 효율을 높이는 전략을 제시했다. 구체적으로, CD39를 발현하는 조직 상주 기억 세포독성 T세포들이 PD-1을 차단하는 면역항암제 처리에 반응해 그 기능이 효과적으로 회복됐다. 그리고 CTLA-4라는 다른 억제 수용체까지 함께 차단하자 세포독성 T세포의 기능 회복은 더욱 크게 나타났다. 따라서 이러한 면역항암제의 병용요법을 CD39 발현 조직 상주 기억 세포독성 T세포가 증가해 있는 환자들에게 선별적으로 사용한다면 치료 효과를 극대화할 수 있을 것으로 기대할 수 있다.
이번 연구는 연세대학교 및 가톨릭대 의과대학 외과 연구팀과 KAIST 의과학대학원이 유방암 환자의 항암 면역반응 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로서 중개 연구(translational research)의 주요 성과로 평가받는다.
신의철 교수는 "이번 연구는 항암 면역반응의 메커니즘과 측정에 대해 상세히 연구함으로써 유방암에서 새로운 임상 치료 전략을 제시하게 된 중요한 연구ˮ라며 "향후 암 환자의 생존율을 보다 높일 수 있도록 항암 면역반응 연구 및 면역 항암치료의 *적응증에 관한 연구를 계속하겠다ˮ라고 말했다.
☞ 적응증(indication): 어떠한 약제나 수술 따위에 의하여 치료 효과가 기대되는 병이나 증상
유방암 환자의 면역 항암치료 원리 발견해 효과적인 치료 전략 제시
우리 대학 의과학대학원 신의철 교수 연구팀이 연세대학교 의과대학 김승일 교수, 가톨릭대 의과대학 박우찬 교수 연구팀과 공동 연구를 통해 유방암 환자의 면역 항암치료 핵심 원리를 발견했다고 14일 밝혔다.
이번 연구를 통해, 최근 유행하는 면역 항암치료에 좋은 반응을 보일 것으로 예상되는 유방암 환자들을 선별해 효과적인 암 치료 전략을 제시할 것으로 기대된다.
연세대학교 의과대학 외과학 교실 이용준 강사, 김지예 임상 조교수가 공동 제1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 `사이언스 면역학(Science Immunology)' 8월 26일 字 온라인판에 게재됐다. (논문명 : CD39+ tissue-resident memory CD8+ T cells with a clonal overlap across compartments mediate anti-tumor immunity in breast cancer)
암 환자는 암세포에 대항해 이를 제거하는 역할을 하는 세포독성 T세포의 기능이 현저히 약해져 암세포에 대한 효과적인 면역반응을 나타내지 못한다. 이러한 세포독성 T세포 약화의 주된 이유는 PD-1이라는 세포독성 T세포의 기능을 저하하는 억제 수용체가 종양 조직 내 세포독성 T세포에 과다하게 발현되기 때문으로 알려져 있다.
최근 유행하고 있는 면역항암제의 기본원리는 바로 이 PD-1 억제 수용체의 기능을 차단해 약화돼 있던 세포독성 T세포의 기능을 회복시키는 것이다. 이러한 면역항암제는 유방암 환자에게서 기존의 치료를 대체할 수 있는 표준치료로 자리 잡아 가고 있지만, 투여받은 유방암 환자 중 일부에서만 치료 효과가 나타나며 이에 대한 이유를 알지 못하고 있다. 따라서, 많은 연구자가 유방암에서 면역 항암치료의 기전을 이해하고 치료에 효과를 보이는 환자를 선별하고자 하는 연구를 활발히 수행하고 있다.
이번 연구에서 공동 연구팀은 종양 조직에 존재하는 세포독성 T세포 중에서도 CD39 단백질과 조직 상주 마커 단백질을 동시에 발현하는 조직 상주 기억 T세포(CD39+ tissue-resident memory CD8+ T cell)가 유방암 환자에서 효과적인 항암 면역반응을 매개하는 핵심 면역세포임을 새롭게 밝혔다.
종양 조직에 존재하는 세포독성 T세포 중에는 항암 면역반응에 영향을 주지 않는 방관자(bystander) 세포들이 존재한다는 사실은 이미 잘 알려져 있었다. 이렇게 항암 면역반응과는 상관없는 방관자 세포들도 종양 조직에 있기 때문에 암 환자의 항암 면역반응을 정확히 측정하고 분석하는 데 어려움이 있었다. 연구팀은 CD39 단백질과 조직 상주 마커 단백질의 발현을 측정해 항암 면역반응과 관련이 있는 세포독성 T세포들만 분리해 개별 환자의 항암 면역반응을 정확히 측정할 수 있음을 새롭게 밝혔다.
그리고 유방암 환자에서 CD39를 발현하는 조직 상주 기억 세포독성 T세포는 특징적으로 삼중음성유방암(triple-negative breast cancer) 환자에게서 증가해 있었고, CD39를 발현하는 조직 상주 기억 세포독성 T세포가 증가해 있는 유방암 환자들은 수술 이후에도 재발이 적게 나타나는 등 좋은 예후를 보였다.
이번 연구에서 연구팀은 유방암 환자에서 면역항암제 치료 효율을 높이는 전략을 제시했다. 구체적으로, CD39를 발현하는 조직 상주 기억 세포독성 T세포들이 PD-1을 차단하는 면역항암제 처리에 반응해 그 기능이 효과적으로 회복됐다. 그리고 CTLA-4라는 다른 억제 수용체까지 함께 차단하자 세포독성 T세포의 기능 회복은 더욱 크게 나타났다. 따라서 이러한 면역항암제의 병용요법을 CD39 발현 조직 상주 기억 세포독성 T세포가 증가해 있는 환자들에게 선별적으로 사용한다면 치료 효과를 극대화할 수 있을 것으로 기대할 수 있다.
이번 연구는 연세대학교 및 가톨릭대 의과대학 외과 연구팀과 KAIST 의과학대학원이 유방암 환자의 항암 면역반응 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로서 중개 연구(translational research)의 주요 성과로 평가받는다.
신의철 교수는 "이번 연구는 항암 면역반응의 메커니즘과 측정에 대해 상세히 연구함으로써 유방암에서 새로운 임상 치료 전략을 제시하게 된 중요한 연구ˮ라며 "향후 암 환자의 생존율을 보다 높일 수 있도록 항암 면역반응 연구 및 면역 항암치료의 *적응증에 관한 연구를 계속하겠다ˮ라고 말했다.
☞ 적응증(indication): 어떠한 약제나 수술 따위에 의하여 치료 효과가 기대되는 병이나 증상
2022.09.14
조회수 9782
-
 RNA 활용해 퇴행성 관절염 획기적 조기진단 가능성 열어
우리 대학 생명화학공학과 김유식 교수와 분당서울대병원 류마티스내과 이윤종 교수 공동 연구팀이 골관절염(Osteoarthritis)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
골관절염은 뼈의 관절면을 감싸고 있는 관절 연골이 마모돼 연골 밑의 뼈가 노출되고, 관절 주변 활액막에 염증이 생겨서 통증과 변형이 발생하는 질환이다. 흔히 퇴행성 관절염이라고도 불리며, 관절 질환 중에서 가장 많이 발생하는 질환이다.
연구팀은 골관절염의 발병 과정 중 손상된 연골에서 염증을 일으켜 세포사멸을 촉진하는 물질이 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)라는 것을 밝혔다.
이번 연구는 골관절염에서 발견되는 다양한 증상들의 원인을 mt-dsRNA라는 개념을 통해 하나로 통합함으로써 골관절염 진단 및 치료에 획기적인 방안을 제시할 것으로 기대된다.
생명화학공학과 박사과정에 재학 중인 김수진 학생과 이건용 학생이 공동 제1 저자로 참여한 이번 연구는 국제학술지 `셀 리포트(Cell Reports)' 지난 8월 9일 字에 게재됐다. (논문명 : Mitochondrial double-stranded RNAs govern the stress response in chondrocytes to promote osteoarthritis development)
골관절염은 우리나라 70세 이상의 여성 인구에서 약 50%의 유병률을 보이는 매우 흔한 질환이다. 골관절염은 일반적으로 노화와 함께 진행되기 때문에 초기에 이들을 구분하는 데 한계가 있다. 골관절염의 진행을 늦추기 위해 증상의 심각성에 따라 약물을 활용한 보존적 치료 혹은 수술을 비롯한 다양한 시도를 활발히 하고 있지만, 기존 접근방법으로 골관절염이 완치될 것이라는 기대를 하기는 어려운 상황이다. 연구팀은 질병의 발병 및 진행 메커니즘을 분석함으로써 골관절염의 조기진단과 완치에 한 걸음 다가갈 수 있는 완전히 새로운 표적 물질을 찾고자 했다.
이중나선 RNA(dsRNA)는 비정상적인 면역반응을 유발해 세포사멸 및 염증반응을 촉진한다고 알려져 있다. dsRNA의 과발현은 다양한 퇴행성 질환과 밀접한 관련이 있어 dsRNA의 조절은 건강한 세포를 유지하기 위해 필수적이다. 세포에서 dsRNA를 생성하는 대표적인 기관은 세포에 에너지를 제공한다고 알려진 미토콘드리아다. 미토콘드리아는 자체 생산하는 dsRNA를 세포질로부터 분리해 dsRNA의 노출과 이에 따른 면역반응을 막는다. 하지만 자극 혹은 세포 스트레스에 의해 mt-dsRNA가 세포질에 노출되면 RNA가 면역반응 단백질에 의해 인지돼 비정상적인 면역반응을 일으킬 수 있다.
연구팀은 골관절염에서 미토콘드리아의 손상과 원인을 알 수 없는 면역반응 단백질의 활성화가 관찰된다는 점에 착안해 mt-dsRNA가 골관절염 발병에서 중요한 기능을 할 것이라는 가설을 세웠다.
연구팀은 연골세포에서 구축한 골관절염 모사 환경에서 mt-dsRNA가 미토콘드리아 외부로 노출돼 선천성 면역반응 단백질에 의해 인지됨에 따라 면역반응을 일으킨다는 것을 확인했다. 또한 골관절염 환자들의 무릎 활막액 및 연골 조직과 골관절염 생쥐 모델의 연골에서도 mt-dsRNA가 유의미하게 증가해 있는 것을 확인했다.
특히, 다른 관절 질환인 류마티스 관절염과 통풍 환자들의 활막액과 비교했을 때 골관절염 환자들의 활막액에서 더 많은 양의 mt-dsRNA가 검출됐다. 또한 초기 골관절염을 앓고 있는 환자들의 연골에서 mt-dsRNA가 많이 증가했다. 따라서 연구팀은 골관절염을 특이적으로 조기진단 할 수 있는 바이오마커로서 mt-dsRNA의 가능성을 제시했다.
더 나아가 연구팀은 골관절염의 전도유망한 치료법 중 하나인 자가포식(Autophagy)의 치료 메커니즘에서 mt-dsRNA의 역할을 규명했다. 연구팀은 자가포식이 세포질에서 mt-dsRNA를 제거함으로써 골관절염의 증상을 완화할 수 있다는 사실을 밝힘으로써 골관절염 치료를 위한 신개념의 표적 물질로서 mt-dsRNA을 제시했다.
생명화학공학과 김유식 교수는 "이번 연구는 세포 수준의 골관절염 모사 환경에서 mt-dsRNA의 기능 규명을 넘어서 실제 골관절염 생쥐 모델의 연골 및 환자의 인체유래물에서 mt-dsRNA의 특이적인 발현 증가를 검증했다ˮ면서 "골관절염처럼 미토콘드리아 손상이 관찰되는 알츠하이머를 비롯한 퇴행성 질환의 발병 메커니즘 분석에 mt-dsRNA를 활용한다면 효과적인 치료전략을 마련하는데 유용할 것ˮ이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 박사과정생 연구장려금 지원사업의 지원을 받아 수행했다.
RNA 활용해 퇴행성 관절염 획기적 조기진단 가능성 열어
우리 대학 생명화학공학과 김유식 교수와 분당서울대병원 류마티스내과 이윤종 교수 공동 연구팀이 골관절염(Osteoarthritis)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
골관절염은 뼈의 관절면을 감싸고 있는 관절 연골이 마모돼 연골 밑의 뼈가 노출되고, 관절 주변 활액막에 염증이 생겨서 통증과 변형이 발생하는 질환이다. 흔히 퇴행성 관절염이라고도 불리며, 관절 질환 중에서 가장 많이 발생하는 질환이다.
연구팀은 골관절염의 발병 과정 중 손상된 연골에서 염증을 일으켜 세포사멸을 촉진하는 물질이 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)라는 것을 밝혔다.
이번 연구는 골관절염에서 발견되는 다양한 증상들의 원인을 mt-dsRNA라는 개념을 통해 하나로 통합함으로써 골관절염 진단 및 치료에 획기적인 방안을 제시할 것으로 기대된다.
생명화학공학과 박사과정에 재학 중인 김수진 학생과 이건용 학생이 공동 제1 저자로 참여한 이번 연구는 국제학술지 `셀 리포트(Cell Reports)' 지난 8월 9일 字에 게재됐다. (논문명 : Mitochondrial double-stranded RNAs govern the stress response in chondrocytes to promote osteoarthritis development)
골관절염은 우리나라 70세 이상의 여성 인구에서 약 50%의 유병률을 보이는 매우 흔한 질환이다. 골관절염은 일반적으로 노화와 함께 진행되기 때문에 초기에 이들을 구분하는 데 한계가 있다. 골관절염의 진행을 늦추기 위해 증상의 심각성에 따라 약물을 활용한 보존적 치료 혹은 수술을 비롯한 다양한 시도를 활발히 하고 있지만, 기존 접근방법으로 골관절염이 완치될 것이라는 기대를 하기는 어려운 상황이다. 연구팀은 질병의 발병 및 진행 메커니즘을 분석함으로써 골관절염의 조기진단과 완치에 한 걸음 다가갈 수 있는 완전히 새로운 표적 물질을 찾고자 했다.
이중나선 RNA(dsRNA)는 비정상적인 면역반응을 유발해 세포사멸 및 염증반응을 촉진한다고 알려져 있다. dsRNA의 과발현은 다양한 퇴행성 질환과 밀접한 관련이 있어 dsRNA의 조절은 건강한 세포를 유지하기 위해 필수적이다. 세포에서 dsRNA를 생성하는 대표적인 기관은 세포에 에너지를 제공한다고 알려진 미토콘드리아다. 미토콘드리아는 자체 생산하는 dsRNA를 세포질로부터 분리해 dsRNA의 노출과 이에 따른 면역반응을 막는다. 하지만 자극 혹은 세포 스트레스에 의해 mt-dsRNA가 세포질에 노출되면 RNA가 면역반응 단백질에 의해 인지돼 비정상적인 면역반응을 일으킬 수 있다.
연구팀은 골관절염에서 미토콘드리아의 손상과 원인을 알 수 없는 면역반응 단백질의 활성화가 관찰된다는 점에 착안해 mt-dsRNA가 골관절염 발병에서 중요한 기능을 할 것이라는 가설을 세웠다.
연구팀은 연골세포에서 구축한 골관절염 모사 환경에서 mt-dsRNA가 미토콘드리아 외부로 노출돼 선천성 면역반응 단백질에 의해 인지됨에 따라 면역반응을 일으킨다는 것을 확인했다. 또한 골관절염 환자들의 무릎 활막액 및 연골 조직과 골관절염 생쥐 모델의 연골에서도 mt-dsRNA가 유의미하게 증가해 있는 것을 확인했다.
특히, 다른 관절 질환인 류마티스 관절염과 통풍 환자들의 활막액과 비교했을 때 골관절염 환자들의 활막액에서 더 많은 양의 mt-dsRNA가 검출됐다. 또한 초기 골관절염을 앓고 있는 환자들의 연골에서 mt-dsRNA가 많이 증가했다. 따라서 연구팀은 골관절염을 특이적으로 조기진단 할 수 있는 바이오마커로서 mt-dsRNA의 가능성을 제시했다.
더 나아가 연구팀은 골관절염의 전도유망한 치료법 중 하나인 자가포식(Autophagy)의 치료 메커니즘에서 mt-dsRNA의 역할을 규명했다. 연구팀은 자가포식이 세포질에서 mt-dsRNA를 제거함으로써 골관절염의 증상을 완화할 수 있다는 사실을 밝힘으로써 골관절염 치료를 위한 신개념의 표적 물질로서 mt-dsRNA을 제시했다.
생명화학공학과 김유식 교수는 "이번 연구는 세포 수준의 골관절염 모사 환경에서 mt-dsRNA의 기능 규명을 넘어서 실제 골관절염 생쥐 모델의 연골 및 환자의 인체유래물에서 mt-dsRNA의 특이적인 발현 증가를 검증했다ˮ면서 "골관절염처럼 미토콘드리아 손상이 관찰되는 알츠하이머를 비롯한 퇴행성 질환의 발병 메커니즘 분석에 mt-dsRNA를 활용한다면 효과적인 치료전략을 마련하는데 유용할 것ˮ이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 박사과정생 연구장려금 지원사업의 지원을 받아 수행했다.
2022.08.31
조회수 8772
-
 인공지능 기반 약물 가상 스크리닝 기술로 신규 항암 치료제 발굴 성공
우리 대학 생명과학과 김세윤 교수 연구팀이 `약물 가상 스크리닝 기술을 이용한 신규 항암 치료제 개발'에 성공했다고 12일 밝혔다.
이번 연구 결과는 국제 학술지인 `세포 사멸과 질병(Cell Death & Disease)'에 지난 7월 12일 字 온라인 게재됐다.
※ 논문명 : Lomitapide, a cholesterol-lowering drug, is an anticancer agent that induces autophagic cell death via inhibiting mTOR
※ 저자 정보 : 이보아 (한국과학기술원, 공동 제1 저자), 박승주 (한국과학기술원, 공동 제1 저자), 이슬기 (한국과학기술원, 제2 저자), 오병철 (가천대학교 의과대학, 공동 저자), 정원석 (한국과학기술원, 공동 저자), 손종우 (한국과학기술원, 공동 저자), 김세윤 (한국과학기술원, 교신저자), 포함 총 10명
`엠토르(mTOR)'라고 알려진 신호전달 단백질은 많은 암세포에서 활성이 비정상적으로 높아져 있으며 또한 암뿐만 아니라 당뇨, 염증 및 노화와 같은 다양한 질병에서 핵심적인 역할을 한다. 특히 암을 유발하는 다양한 신호전달 경로가 엠토르 단백질을 통해 매개되기 때문에 많은 제약사에서 항암 치료제 개발의 목적으로 엠토르 저해제 개발에 많은 투자를 하고 있다.
자가포식(autophagy, 오토파지)으로 알려진 생명 현상은 세포 내 엠토르 단백질에 의해 활성 조절이 정교하게 매개되는 것으로 잘 알려져 있다. 자가포식이란 `세포가 자기 살을 먹는다'는 의미로, 영양분이 과도하게 부족하거나 세포 내외적 스트레스 조건에 처한 경우, 세포가 스스로 내부 구성물질들을 파괴해 활용함으로써 세포 내 항상성을 유지하는 일종의 방어기전이다.
이러한 자가포식 활성의 조절은 양날의 칼과 같이 작용하는 것으로 알려져 있으며, 이는 암, 당뇨와 같은 질환의 발생 및 치료에 이용 가능하다고 주목받고 있다. 암세포에 과도하게 활성화돼있는 엠토르 단백질의 활성을 저해하면 자가포식을 과도하게 증가시킬 수 있으며 이를 통해 암세포의 세포 사멸이 유도될 수 있다는 사실이 알려져 있으며 이를 바탕으로 자가포식 강화에 기반한 항암제 약물의 개발전략이 제시되고 있다.
이에 김세윤 교수 연구팀은 단백질의 3차원적 구조를 활용해 화합물과 표적 단백질 사이의 물리적 상호작용을 모델링하는 유효 결합 판별 기술에 기반한 약물 재창출 전략으로 엠토르 억제성 항암제 개발 연구를 수행했다.
약물 재창출은 이미 안전성이 검증된 FDA 승인 약물 또는 임상 진행 중인 약물군을 대상으로 새로운 적응증을 찾는 신약 개발 방식이다. 이 전략은 전통적으로 10년 이상 소요되는 신약 개발의 막대한 시간과 투자를 혁신적으로 단축할 수 있는 미래 시대 신약 개발전략이다.
연구팀은 FDA 승인 약물 또는 임상 시험 중인 약물에 기반한 데이터베이스를 통해 3,391종의 약물 라이브러리를 활용했다. 라이브러리의 모든 약물을 실험적으로 검증하기에는 연구비용과 시간이 많이 소요되므로, 3차 구조 모델링을 통한 유효 결합 판별 기술을 적용해 엠토르 활성 저해능력을 보이는 약물만 신속하게 스크리닝했다.
연구팀은 엠토르 단백질의 활성을 담당하는 효소 활성부위의 3차 구조 분석과 인공지능 기반 유효 결합 판별 기술을 도입해 후보 물질 발굴의 정확도와 예측도를 높이는 데 성공했다. 그리고 3차 구조를 타깃으로 약물 결합 분석 모듈을 도입해 가상 스크리닝의 정확도와 예측도를 높이는 데 성공했다. 이번 연구를 통해 개발된 기술의 가장 큰 특징은 타깃 단백질과 약물 간의 3차 구조 정보를 이용해 많은 양의 후보 성분들을 빠르고 정확하게 분석하고 결합 여부를 예측할 수 있는 것이다.
우리 대학 생명과학과 이보아 박사, 박승주 박사는 현재 가족성 고콜레스테롤혈증(familial hypercholesterolemia) 치료제로서 임상에서 판매, 활용되고 있는 로미타피드(lomitapide) 약물의 엠토르 활성 억제 가능성을 예측했다. 연구팀은 생화학적 및 세포 생물학적 분석을 통해 로미타피드에 의한 엠토르 효소활성의 억제효능을 검증하는 데 성공했다. 대장암, 피부암 등의 암세포에 로미타피드를 처리할 경우, 암세포의 엠토르 활성이 효과적으로 억제되고 이후 과도한 자가포식이 유도됨으로써 암세포 사멸효과가 발생함을 다각적으로 확인해 로미타피드의 항암 효능을 확립했다.
또한 대장암 환자로부터 유래한 암 오가노이드(organoid)에 로미타피드를 처리할 경우, 기존의 화학 항암 치료제 대비 우수한 암세포 사멸 능력을 보였다. 나아가 최근 차세대 고형암 치료용 항암 전략으로 주목받고 있는 면역관문억제제(immune checkpoint inhibitor)와 로미티피드를 병행할 경우, 면역관문억제제의 단독 처리 대비 비약적으로 개선된 시너지 항암효과를 나타냄을 동물모델 연구를 통해 검증하는 데 성공했다.
연구팀이 발굴한 로미타피드의 항암 효능 성과는 향후 엠토르 억제 및 자가포식 기반 항암제 개발 및 임상적 활용에 적극 활용될 것으로 기대된다.
이러한 연구성과는 벤처창업으로 연계돼 이보아 박사, 박승주 박사, 이슬기 박사는 인공지능 기반 신약개발 전문기업 `에아스텍'을 공동창업했으며 중소벤처기업부 팁스(TIPS) 창업지원 프로그램에 선정되는 등 활발한 연구개발을 수행하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 창의도전연구사업 및 KAIX 포스트닥펠로사업의 지원을 받아 수행됐다.
인공지능 기반 약물 가상 스크리닝 기술로 신규 항암 치료제 발굴 성공
우리 대학 생명과학과 김세윤 교수 연구팀이 `약물 가상 스크리닝 기술을 이용한 신규 항암 치료제 개발'에 성공했다고 12일 밝혔다.
이번 연구 결과는 국제 학술지인 `세포 사멸과 질병(Cell Death & Disease)'에 지난 7월 12일 字 온라인 게재됐다.
※ 논문명 : Lomitapide, a cholesterol-lowering drug, is an anticancer agent that induces autophagic cell death via inhibiting mTOR
※ 저자 정보 : 이보아 (한국과학기술원, 공동 제1 저자), 박승주 (한국과학기술원, 공동 제1 저자), 이슬기 (한국과학기술원, 제2 저자), 오병철 (가천대학교 의과대학, 공동 저자), 정원석 (한국과학기술원, 공동 저자), 손종우 (한국과학기술원, 공동 저자), 김세윤 (한국과학기술원, 교신저자), 포함 총 10명
`엠토르(mTOR)'라고 알려진 신호전달 단백질은 많은 암세포에서 활성이 비정상적으로 높아져 있으며 또한 암뿐만 아니라 당뇨, 염증 및 노화와 같은 다양한 질병에서 핵심적인 역할을 한다. 특히 암을 유발하는 다양한 신호전달 경로가 엠토르 단백질을 통해 매개되기 때문에 많은 제약사에서 항암 치료제 개발의 목적으로 엠토르 저해제 개발에 많은 투자를 하고 있다.
자가포식(autophagy, 오토파지)으로 알려진 생명 현상은 세포 내 엠토르 단백질에 의해 활성 조절이 정교하게 매개되는 것으로 잘 알려져 있다. 자가포식이란 `세포가 자기 살을 먹는다'는 의미로, 영양분이 과도하게 부족하거나 세포 내외적 스트레스 조건에 처한 경우, 세포가 스스로 내부 구성물질들을 파괴해 활용함으로써 세포 내 항상성을 유지하는 일종의 방어기전이다.
이러한 자가포식 활성의 조절은 양날의 칼과 같이 작용하는 것으로 알려져 있으며, 이는 암, 당뇨와 같은 질환의 발생 및 치료에 이용 가능하다고 주목받고 있다. 암세포에 과도하게 활성화돼있는 엠토르 단백질의 활성을 저해하면 자가포식을 과도하게 증가시킬 수 있으며 이를 통해 암세포의 세포 사멸이 유도될 수 있다는 사실이 알려져 있으며 이를 바탕으로 자가포식 강화에 기반한 항암제 약물의 개발전략이 제시되고 있다.
이에 김세윤 교수 연구팀은 단백질의 3차원적 구조를 활용해 화합물과 표적 단백질 사이의 물리적 상호작용을 모델링하는 유효 결합 판별 기술에 기반한 약물 재창출 전략으로 엠토르 억제성 항암제 개발 연구를 수행했다.
약물 재창출은 이미 안전성이 검증된 FDA 승인 약물 또는 임상 진행 중인 약물군을 대상으로 새로운 적응증을 찾는 신약 개발 방식이다. 이 전략은 전통적으로 10년 이상 소요되는 신약 개발의 막대한 시간과 투자를 혁신적으로 단축할 수 있는 미래 시대 신약 개발전략이다.
연구팀은 FDA 승인 약물 또는 임상 시험 중인 약물에 기반한 데이터베이스를 통해 3,391종의 약물 라이브러리를 활용했다. 라이브러리의 모든 약물을 실험적으로 검증하기에는 연구비용과 시간이 많이 소요되므로, 3차 구조 모델링을 통한 유효 결합 판별 기술을 적용해 엠토르 활성 저해능력을 보이는 약물만 신속하게 스크리닝했다.
연구팀은 엠토르 단백질의 활성을 담당하는 효소 활성부위의 3차 구조 분석과 인공지능 기반 유효 결합 판별 기술을 도입해 후보 물질 발굴의 정확도와 예측도를 높이는 데 성공했다. 그리고 3차 구조를 타깃으로 약물 결합 분석 모듈을 도입해 가상 스크리닝의 정확도와 예측도를 높이는 데 성공했다. 이번 연구를 통해 개발된 기술의 가장 큰 특징은 타깃 단백질과 약물 간의 3차 구조 정보를 이용해 많은 양의 후보 성분들을 빠르고 정확하게 분석하고 결합 여부를 예측할 수 있는 것이다.
우리 대학 생명과학과 이보아 박사, 박승주 박사는 현재 가족성 고콜레스테롤혈증(familial hypercholesterolemia) 치료제로서 임상에서 판매, 활용되고 있는 로미타피드(lomitapide) 약물의 엠토르 활성 억제 가능성을 예측했다. 연구팀은 생화학적 및 세포 생물학적 분석을 통해 로미타피드에 의한 엠토르 효소활성의 억제효능을 검증하는 데 성공했다. 대장암, 피부암 등의 암세포에 로미타피드를 처리할 경우, 암세포의 엠토르 활성이 효과적으로 억제되고 이후 과도한 자가포식이 유도됨으로써 암세포 사멸효과가 발생함을 다각적으로 확인해 로미타피드의 항암 효능을 확립했다.
또한 대장암 환자로부터 유래한 암 오가노이드(organoid)에 로미타피드를 처리할 경우, 기존의 화학 항암 치료제 대비 우수한 암세포 사멸 능력을 보였다. 나아가 최근 차세대 고형암 치료용 항암 전략으로 주목받고 있는 면역관문억제제(immune checkpoint inhibitor)와 로미티피드를 병행할 경우, 면역관문억제제의 단독 처리 대비 비약적으로 개선된 시너지 항암효과를 나타냄을 동물모델 연구를 통해 검증하는 데 성공했다.
연구팀이 발굴한 로미타피드의 항암 효능 성과는 향후 엠토르 억제 및 자가포식 기반 항암제 개발 및 임상적 활용에 적극 활용될 것으로 기대된다.
이러한 연구성과는 벤처창업으로 연계돼 이보아 박사, 박승주 박사, 이슬기 박사는 인공지능 기반 신약개발 전문기업 `에아스텍'을 공동창업했으며 중소벤처기업부 팁스(TIPS) 창업지원 프로그램에 선정되는 등 활발한 연구개발을 수행하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 창의도전연구사업 및 KAIX 포스트닥펠로사업의 지원을 받아 수행됐다.
2022.08.12
조회수 11712
-
 인공지능의 오랜 난제를 뇌 기반 인공지능으로 풀다
우리 대학 바이오및뇌공학과 이상완 교수(신경과학 인공지능 융합연구센터장) 연구팀이 뇌 기반 인공지능 기술을 이용해 인공지능의 난제 중 하나인 과적합-과소적합 상충 문제를 해결하는 원리를 풀어내는 데 성공했다고 5일 밝혔다.
이상완 교수와 김동재 박사(現 뉴욕대학교 박사후 연구원)가 주도하고 우리 대학 정재승 교수가 참여한 이번 연구는 `강화학습 중 편향-분산 상충 문제에 대한 전두엽의 해법'이라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 지난해 12월 28일 字 온라인판에 게재됐다. (논문명: Prefrontal solution to the bias-variance tradeoff during reinforcement learning)
최근 인공지능 모델들은 다양한 실제 문제들에 대해 최적의 해법을 제시하지만, 상황 변화에 유동적으로 대응하는 부분에 있어서는 여전히 어려움을 겪고 있다. 기계학습에서는 이를 과소적합-과적합의 위험성 (underfitting-overfitting risk) 또는 편향-분산 상충 문제(bias-variance tradeoff)라 하며 오랫동안 연구됐지만, 실제 세계와 같이 상충 조건이 계속 변하는 상황에서의 명확한 해법은 아직 제안된 바가 없다.
반면 인간은 현재 주어진 문제에 집중하면서도(과소적합 문제 해결), 당면 문제에 과하게 집착하지 않고(과적합 문제 해결) 변하는 상황에 맞게 유동적으로 대처한다. 연구팀은 뇌 데이터, 확률과정 추론 모형, 강화학습 알고리즘을 이용해 인간의 뇌가 이 문제를 어떻게 해결하는지에 대한 이론적 틀을 마련하고 이로부터 유동적인 메타 강화학습 모델을 도출해냈다.
놀랍게도 인간의 뇌는 중뇌 도파민 회로와 전두엽에서 처리되는 `예측 오차'의 하한선(prediction error lower bound)이라는 단 한 가지 정보를 이용해 이 문제를 해결한다. 우리의 전두엽, 특히 복외측전전두피질은 현재 내가 사용하고 있는 문제 해결 방식으로 주어진 문제를 얼마나 잘 풀 수 있을지에 대한 기대치의 한계를 추정하고(예: `이렇게 풀면 90점까지는 받을 수 있어'), 변화하는 상황에 맞춰 최적인 문제 해결전략을 유동적으로 선택하는 과정 (예: `이렇게 풀면 기껏해야 70점이니 다르게 풀어보자')을 통해 과소적합-과적합의 위험을 최소화하게 된다.
이상완 교수 연구팀은 2014년 해당 전두엽 영역이 환경의 불확실성을 바탕으로 강화학습전략을 유동적으로 조절하는 데 관여한다는 사실을 처음 발견했고(`뉴런(Neuron)' 학술지에 발표), 2015년에는 인과관계 추론 과정에도 관여한다는 사실을 발견했다(`PLOS Biology' 학술지에 발표). 이어 2019년에는 해당 뇌 영역이 문제의 복잡도까지 고려할 수 있다는 사실을 발견했다(`네이처 커뮤니케이션즈(Nature Communications)' 학술지에 발표).
이러한 일련의 연구 결과들은 자신의 학습 및 추론 능력을 스스로 평가하는 인간의 메타 인지 능력을 보여주는 증거로, 이 능력을 바탕으로 인공지능이 풀기 어려워하는 현실 세계의 다양한 상충적 상황들을 풀어낼 수 있다는 `전두엽 메타 학습 이론'을 정립한 바 있다(`사이언스 로보틱스(Science Robotics)' 학술지에 발표). 이번 연구는 이 이론에 기반해 인공지능의 오랜 난제 중 하나인 과소적합-과적합 상충 문제를 실제로 풀어낸 최초의 사례로 평가된다.
연구를 통해 개발된 메타 강화학습 모델을 이용하면 간단한 게임을 통해 인간의 유동적 문제 해결 능력을 간접적으로 측정할 수 있다. 더 나아가 스마트 교육이나 중독과 관련된 인지 행동치료에 적용할 경우 상황 변화에 유동적으로 대처하는 인간의 문제 해결 능력 자체를 향상할 수 있을 것으로 기대된다. 차세대 인공지능, 스마트 교육, 인지 행동치료 등 다양한 분야에 파급력이 큰 원천 기술로 최근 국내 및 해외 특허 출원이 완료된 상태다.
연구를 주도한 제1 저자 김동재 박사는 "인간 지능의 특장점에 대한 이해가 얼마나 중요한지 보여주는 연구 중 하나ˮ라고 말했다. 연구 책임자인 이상완 교수는 "인공지능이 우리보다 잘 푸는 문제가 많지만, 반대로 인공지능으로 풀기 어려운 문제들이 우리에게는 정말 쉽게 느껴지는 경우들이 많다. 인간의 다양한 고위 수준 능력을 인공지능 이론 관점에서 형식화하는 연구를 통해 인간 지능의 비밀을 하나씩 풀어나갈 수 있을 것으로 기대된다ˮ라며 "이러한 뇌 기반 인공지능 연구는 인간의 지능을 공학적으로 탐구하는 과정으로 볼 수 있으며, 인간과 인공지능이 서로 도우며 함께 성장해 나갈 수 있는 명확한 기준점을 마련할 수 있을 것ˮ이라고 말했다. 이상완 교수는 뇌 기반 인공지능 연구의 독창성과 도전성을 인정받아 구글 교수 연구상과 IBM 학술상을 받은 바 있다.
연구팀은 과학기술정보통신부의 재원으로 정보통신기획평가원의 지원을 받아 설립한 KAIST 신경과학-인공지능 융합연구센터에서 기반 기술을 활용해 인간 지능을 모사한 차세대 인공지능 모델을 개발하고, 아울러 딥마인드, IBM 인공지능 연구소, MIT, 옥스퍼드 대학 등 국제 공동연구 협약 기관과 공동연구를 통해 기술의 파급력을 높여나갈 계획이라고 말했다.
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 및 한국연구재단의 지원을 받아 수행됐다.
인공지능의 오랜 난제를 뇌 기반 인공지능으로 풀다
우리 대학 바이오및뇌공학과 이상완 교수(신경과학 인공지능 융합연구센터장) 연구팀이 뇌 기반 인공지능 기술을 이용해 인공지능의 난제 중 하나인 과적합-과소적합 상충 문제를 해결하는 원리를 풀어내는 데 성공했다고 5일 밝혔다.
이상완 교수와 김동재 박사(現 뉴욕대학교 박사후 연구원)가 주도하고 우리 대학 정재승 교수가 참여한 이번 연구는 `강화학습 중 편향-분산 상충 문제에 대한 전두엽의 해법'이라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 지난해 12월 28일 字 온라인판에 게재됐다. (논문명: Prefrontal solution to the bias-variance tradeoff during reinforcement learning)
최근 인공지능 모델들은 다양한 실제 문제들에 대해 최적의 해법을 제시하지만, 상황 변화에 유동적으로 대응하는 부분에 있어서는 여전히 어려움을 겪고 있다. 기계학습에서는 이를 과소적합-과적합의 위험성 (underfitting-overfitting risk) 또는 편향-분산 상충 문제(bias-variance tradeoff)라 하며 오랫동안 연구됐지만, 실제 세계와 같이 상충 조건이 계속 변하는 상황에서의 명확한 해법은 아직 제안된 바가 없다.
반면 인간은 현재 주어진 문제에 집중하면서도(과소적합 문제 해결), 당면 문제에 과하게 집착하지 않고(과적합 문제 해결) 변하는 상황에 맞게 유동적으로 대처한다. 연구팀은 뇌 데이터, 확률과정 추론 모형, 강화학습 알고리즘을 이용해 인간의 뇌가 이 문제를 어떻게 해결하는지에 대한 이론적 틀을 마련하고 이로부터 유동적인 메타 강화학습 모델을 도출해냈다.
놀랍게도 인간의 뇌는 중뇌 도파민 회로와 전두엽에서 처리되는 `예측 오차'의 하한선(prediction error lower bound)이라는 단 한 가지 정보를 이용해 이 문제를 해결한다. 우리의 전두엽, 특히 복외측전전두피질은 현재 내가 사용하고 있는 문제 해결 방식으로 주어진 문제를 얼마나 잘 풀 수 있을지에 대한 기대치의 한계를 추정하고(예: `이렇게 풀면 90점까지는 받을 수 있어'), 변화하는 상황에 맞춰 최적인 문제 해결전략을 유동적으로 선택하는 과정 (예: `이렇게 풀면 기껏해야 70점이니 다르게 풀어보자')을 통해 과소적합-과적합의 위험을 최소화하게 된다.
이상완 교수 연구팀은 2014년 해당 전두엽 영역이 환경의 불확실성을 바탕으로 강화학습전략을 유동적으로 조절하는 데 관여한다는 사실을 처음 발견했고(`뉴런(Neuron)' 학술지에 발표), 2015년에는 인과관계 추론 과정에도 관여한다는 사실을 발견했다(`PLOS Biology' 학술지에 발표). 이어 2019년에는 해당 뇌 영역이 문제의 복잡도까지 고려할 수 있다는 사실을 발견했다(`네이처 커뮤니케이션즈(Nature Communications)' 학술지에 발표).
이러한 일련의 연구 결과들은 자신의 학습 및 추론 능력을 스스로 평가하는 인간의 메타 인지 능력을 보여주는 증거로, 이 능력을 바탕으로 인공지능이 풀기 어려워하는 현실 세계의 다양한 상충적 상황들을 풀어낼 수 있다는 `전두엽 메타 학습 이론'을 정립한 바 있다(`사이언스 로보틱스(Science Robotics)' 학술지에 발표). 이번 연구는 이 이론에 기반해 인공지능의 오랜 난제 중 하나인 과소적합-과적합 상충 문제를 실제로 풀어낸 최초의 사례로 평가된다.
연구를 통해 개발된 메타 강화학습 모델을 이용하면 간단한 게임을 통해 인간의 유동적 문제 해결 능력을 간접적으로 측정할 수 있다. 더 나아가 스마트 교육이나 중독과 관련된 인지 행동치료에 적용할 경우 상황 변화에 유동적으로 대처하는 인간의 문제 해결 능력 자체를 향상할 수 있을 것으로 기대된다. 차세대 인공지능, 스마트 교육, 인지 행동치료 등 다양한 분야에 파급력이 큰 원천 기술로 최근 국내 및 해외 특허 출원이 완료된 상태다.
연구를 주도한 제1 저자 김동재 박사는 "인간 지능의 특장점에 대한 이해가 얼마나 중요한지 보여주는 연구 중 하나ˮ라고 말했다. 연구 책임자인 이상완 교수는 "인공지능이 우리보다 잘 푸는 문제가 많지만, 반대로 인공지능으로 풀기 어려운 문제들이 우리에게는 정말 쉽게 느껴지는 경우들이 많다. 인간의 다양한 고위 수준 능력을 인공지능 이론 관점에서 형식화하는 연구를 통해 인간 지능의 비밀을 하나씩 풀어나갈 수 있을 것으로 기대된다ˮ라며 "이러한 뇌 기반 인공지능 연구는 인간의 지능을 공학적으로 탐구하는 과정으로 볼 수 있으며, 인간과 인공지능이 서로 도우며 함께 성장해 나갈 수 있는 명확한 기준점을 마련할 수 있을 것ˮ이라고 말했다. 이상완 교수는 뇌 기반 인공지능 연구의 독창성과 도전성을 인정받아 구글 교수 연구상과 IBM 학술상을 받은 바 있다.
연구팀은 과학기술정보통신부의 재원으로 정보통신기획평가원의 지원을 받아 설립한 KAIST 신경과학-인공지능 융합연구센터에서 기반 기술을 활용해 인간 지능을 모사한 차세대 인공지능 모델을 개발하고, 아울러 딥마인드, IBM 인공지능 연구소, MIT, 옥스퍼드 대학 등 국제 공동연구 협약 기관과 공동연구를 통해 기술의 파급력을 높여나갈 계획이라고 말했다.
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 및 한국연구재단의 지원을 받아 수행됐다.
2022.01.05
조회수 12160
-
 형광 염색 없이 분자 정보를 보는 AI 현미경 개발
우리 대학 물리학과 박용근 석좌교수 연구팀이 형광 염색 없이 세포의 분자 정보를 볼 수 있는 인공지능 현미경 기술을 개발했다고 20일 밝혔다.
광학 현미경은 수백 년 전부터 현재에 이르기까지 생물학 및 의학에서 가장 중요하게 쓰이는 기술 중 하나로, 이미지 형성 원리에 따라 여러 형태로 발전해왔다. 최근 수십 년간 분자생물학이 눈부시게 발전하면서 세포 내의 특정 구조를 형광(fluorescence) 으로 표지하는 것이 가능해졌고, 이처럼 높은 생화학적 특이성(biochemical specificity) 덕분에 형광 현미경은 현재 가장 폭넓게 쓰이는 광학 현미경 기술이 됐다.
그러나 형광 현미경은 형광 표지 자체가 세포를 변형하는 것이기 때문에 세포에 부담을 주게 되고, 밝기와 세포독성, 안정성 문제 때문에 초고속 또는 장기간 측정이 힘들며, 제한된 색깔로 인해 다양한 구조를 동시에 보는 것이 어려운 근본적인 한계가 있다.
이와는 대조적으로, 각 물질과 빛의 상호작용을 결정하는 근본적인 특성인 굴절률(refractive index)을 이용해 아무런 염색을 하지 않아도 되는 현미경 기술 또한 꾸준히 발전해왔다. 굴절률로부터 파생되는 빛의 흡수, 위상차 등을 이용한 전통적인 현미경은 물론, 최근에는 굴절률 자체를 3차원 상에서 정량적으로 측정하는 다양한 홀로그래픽 현미경(holographic microscopy) 기술이 박용근 교수 연구팀에서 개발돼 상용화된 바 있다. 이러한 비표지(label-free) 현미경 기술은 형광 현미경과 비교해 여러 가지 장점을 갖고 있지만, 굴절률과 세포 내 구조들의 관계가 명확하지 않아 분자 특이성이 떨어진다는 단점이 있었다.
박용근 교수 연구팀에서는 2012년 초부터 조영주 졸업생(제1 저자, 물리학과·수리과학과 학사 11학번·KAIST 총장 장학생, 現 스탠퍼드대학교 응용물리학과 박사과정) 주도로 홀로그래픽 현미경 분야에 인공지능을 도입해 특이성 문제를 해결하려는 일련의 연구가 시작됐다.
우선 형태적으로는 비슷하나 생화학적인 구성에 차이가 있는 시료(여러 종의 박테리아, 다양한 분류의 백혈구 등)의 굴절률 영상은 사람 눈에는 비슷하게 보이는데, 흥미롭게도 인공지능은 이를 높은 정확도로 분류할 수 있음을 보였다(2013-2014년 KAIST 학부연구프로그램(URP) 이후, 2015년 Optics Express, 2017년 Science Advances, 2020년 ACS Nano 등 게재). 이러한 결과는 매우 다양한 생체 시료에서 일관되게 관찰됐고, 따라서 연구팀은 생화학적 특이성이 높은 정보가 굴절률의 공간 분포에 숨겨져 있다는 가설을 세웠다.
세포생물학 분야 최고 권위지인 `네이처 셀 바이올로지(Nature Cell Biology, IF 28.82)'에 12월 7일 발표된 이번 연구(논문명: Label-free multiplexed microtomography of endogenous subcellular dynamics using generalizable deep learning)에서, 연구팀은 홀로그래픽 현미경 영상으로부터 형광 현미경 영상을 직접 예측할 수 있음을 보임으로써 이 가설을 증명했다. 인공지능이 찾아낸 굴절률 공간 분포와 세포 내 주요 구조 간의 정량적인 관계를 이용해 굴절률의 공간 분포 해독이 가능해졌고, 놀랍게도 이러한 관계는 세포 종류와 관계없이 보존돼 있음을 확인했다.
이 과정에서 만들어진 `인공지능 현미경'은 홀로그래픽 현미경과 형광 현미경의 장점만을 갖는다. 즉, 형광 표지 없이 형광 현미경의 특이적인 영상을 얻을 수 있다. 따라서 자연 상태 그대로의 세포에서 동시에 수많은 종류의 구조를 3차원으로 볼 수 있으며, 밀리초(ms) 수준의 초고속 측정과 수십 일 수준의 장기간 측정이 가능해졌다. 더욱이 기존 데이터에 포함되지 않은 새로운 종류의 세포에도 즉시 적용이 가능하기에, 다양한 생물학 및 의학 연구에 응용이 가능할 것으로 기대된다.
이번 연구는 조영주 박사과정과 박용근 교수가 지난 10여 년간 발전시켜온 광학 및 인공지능 기술력 이외에도, 다학제적 접근과 KAIST 기술을 바탕으로 한 창업 덕분에 가능했다. 생명과학과 허원도 교수(공동 교신저자)와 박외선 박사(공동 제1 저자)가 오랜 기간 발전시켜온 분자생물학 및 형광 현미경 기술 덕분에 인공지능 학습에 필요한 데이터를 얻을 수 있었으며, 조영주 박사과정이 허원도 교수 연구팀에서 2015년 1년간 연구했던 경험 덕분에 구체적인 아이디어가 나오게 됐다.
또한 박용근 교수 연구팀 홀로그래픽 현미경 기술로 창업한 ㈜토모큐브를 통해 현미경 및 데이터 형식이 규격화돼 대규모 인공지능 학습이 용이했고, 이를 바탕으로 ㈜토모큐브 조형주 연구원(공동 제1 저자) 및 민현석 연구원(공동 교신저자) 등 인공지능 전문 인력이 합류하면서 최신 인공지능 기법들의 빠른 도입이 가능했다.
한편 이번 연구는 한국연구재단의 창의연구사업, 과학기술정보통신부의 정보통신방송 기술개발사업 (홀로그램핵심기술), 일자리진흥원의 연구장비개발 및 고도화지원사업, 한국보건산업진흥원의 보건의료기술 연구개발사업의 지원을 받아 수행됐다.
형광 염색 없이 분자 정보를 보는 AI 현미경 개발
우리 대학 물리학과 박용근 석좌교수 연구팀이 형광 염색 없이 세포의 분자 정보를 볼 수 있는 인공지능 현미경 기술을 개발했다고 20일 밝혔다.
광학 현미경은 수백 년 전부터 현재에 이르기까지 생물학 및 의학에서 가장 중요하게 쓰이는 기술 중 하나로, 이미지 형성 원리에 따라 여러 형태로 발전해왔다. 최근 수십 년간 분자생물학이 눈부시게 발전하면서 세포 내의 특정 구조를 형광(fluorescence) 으로 표지하는 것이 가능해졌고, 이처럼 높은 생화학적 특이성(biochemical specificity) 덕분에 형광 현미경은 현재 가장 폭넓게 쓰이는 광학 현미경 기술이 됐다.
그러나 형광 현미경은 형광 표지 자체가 세포를 변형하는 것이기 때문에 세포에 부담을 주게 되고, 밝기와 세포독성, 안정성 문제 때문에 초고속 또는 장기간 측정이 힘들며, 제한된 색깔로 인해 다양한 구조를 동시에 보는 것이 어려운 근본적인 한계가 있다.
이와는 대조적으로, 각 물질과 빛의 상호작용을 결정하는 근본적인 특성인 굴절률(refractive index)을 이용해 아무런 염색을 하지 않아도 되는 현미경 기술 또한 꾸준히 발전해왔다. 굴절률로부터 파생되는 빛의 흡수, 위상차 등을 이용한 전통적인 현미경은 물론, 최근에는 굴절률 자체를 3차원 상에서 정량적으로 측정하는 다양한 홀로그래픽 현미경(holographic microscopy) 기술이 박용근 교수 연구팀에서 개발돼 상용화된 바 있다. 이러한 비표지(label-free) 현미경 기술은 형광 현미경과 비교해 여러 가지 장점을 갖고 있지만, 굴절률과 세포 내 구조들의 관계가 명확하지 않아 분자 특이성이 떨어진다는 단점이 있었다.
박용근 교수 연구팀에서는 2012년 초부터 조영주 졸업생(제1 저자, 물리학과·수리과학과 학사 11학번·KAIST 총장 장학생, 現 스탠퍼드대학교 응용물리학과 박사과정) 주도로 홀로그래픽 현미경 분야에 인공지능을 도입해 특이성 문제를 해결하려는 일련의 연구가 시작됐다.
우선 형태적으로는 비슷하나 생화학적인 구성에 차이가 있는 시료(여러 종의 박테리아, 다양한 분류의 백혈구 등)의 굴절률 영상은 사람 눈에는 비슷하게 보이는데, 흥미롭게도 인공지능은 이를 높은 정확도로 분류할 수 있음을 보였다(2013-2014년 KAIST 학부연구프로그램(URP) 이후, 2015년 Optics Express, 2017년 Science Advances, 2020년 ACS Nano 등 게재). 이러한 결과는 매우 다양한 생체 시료에서 일관되게 관찰됐고, 따라서 연구팀은 생화학적 특이성이 높은 정보가 굴절률의 공간 분포에 숨겨져 있다는 가설을 세웠다.
세포생물학 분야 최고 권위지인 `네이처 셀 바이올로지(Nature Cell Biology, IF 28.82)'에 12월 7일 발표된 이번 연구(논문명: Label-free multiplexed microtomography of endogenous subcellular dynamics using generalizable deep learning)에서, 연구팀은 홀로그래픽 현미경 영상으로부터 형광 현미경 영상을 직접 예측할 수 있음을 보임으로써 이 가설을 증명했다. 인공지능이 찾아낸 굴절률 공간 분포와 세포 내 주요 구조 간의 정량적인 관계를 이용해 굴절률의 공간 분포 해독이 가능해졌고, 놀랍게도 이러한 관계는 세포 종류와 관계없이 보존돼 있음을 확인했다.
이 과정에서 만들어진 `인공지능 현미경'은 홀로그래픽 현미경과 형광 현미경의 장점만을 갖는다. 즉, 형광 표지 없이 형광 현미경의 특이적인 영상을 얻을 수 있다. 따라서 자연 상태 그대로의 세포에서 동시에 수많은 종류의 구조를 3차원으로 볼 수 있으며, 밀리초(ms) 수준의 초고속 측정과 수십 일 수준의 장기간 측정이 가능해졌다. 더욱이 기존 데이터에 포함되지 않은 새로운 종류의 세포에도 즉시 적용이 가능하기에, 다양한 생물학 및 의학 연구에 응용이 가능할 것으로 기대된다.
이번 연구는 조영주 박사과정과 박용근 교수가 지난 10여 년간 발전시켜온 광학 및 인공지능 기술력 이외에도, 다학제적 접근과 KAIST 기술을 바탕으로 한 창업 덕분에 가능했다. 생명과학과 허원도 교수(공동 교신저자)와 박외선 박사(공동 제1 저자)가 오랜 기간 발전시켜온 분자생물학 및 형광 현미경 기술 덕분에 인공지능 학습에 필요한 데이터를 얻을 수 있었으며, 조영주 박사과정이 허원도 교수 연구팀에서 2015년 1년간 연구했던 경험 덕분에 구체적인 아이디어가 나오게 됐다.
또한 박용근 교수 연구팀 홀로그래픽 현미경 기술로 창업한 ㈜토모큐브를 통해 현미경 및 데이터 형식이 규격화돼 대규모 인공지능 학습이 용이했고, 이를 바탕으로 ㈜토모큐브 조형주 연구원(공동 제1 저자) 및 민현석 연구원(공동 교신저자) 등 인공지능 전문 인력이 합류하면서 최신 인공지능 기법들의 빠른 도입이 가능했다.
한편 이번 연구는 한국연구재단의 창의연구사업, 과학기술정보통신부의 정보통신방송 기술개발사업 (홀로그램핵심기술), 일자리진흥원의 연구장비개발 및 고도화지원사업, 한국보건산업진흥원의 보건의료기술 연구개발사업의 지원을 받아 수행됐다.
2021.12.20
조회수 11521
-
 코로나19 환자에서 나타나는 자연살해 세포 변화 규명
우리 대학 의과학대학원 신의철 교수 연구팀이 충남대학교병원 감염내과 김연숙, 천신혜 교수팀과의 공동연구를 통해 코로나19 환자들에서 자연살해 세포의 항바이러스 기능이 약화돼 있고, 이러한 기능 변화는 경증 코로나19 환자에서는 일주일 내로 사라지지만 중증 환자에서는 오래 지속됨을 규명했다고 10일 밝혔다. 이로써, 항바이러스 선천면역 반응의 한 축을 담당하는 자연살해 세포의 기능 이상을 중증 코로나19 환자에서 처음으로 규명하게 됐다.
우리 몸은 바이러스에 감염되면 이에 대항하여 일차적으로 선천면역 반응이 나타나며, 항바이러스 선천면역 반응을 담당하는 주된 세포가 바로 자연살해 세포다. 이러한 자연살해 세포의 대부분을 차지하는 것이 바이러스에 감염된 세포를 직접 죽이는 세포독성 자연살해 세포인데, 코로나19 환자에서 이러한 세포독성 자연살해 세포의 수나 기능이 감소돼 있다는 보고는 있었지만, 자연살해 세포의 구체적인 변화나 기능감소 기전에 대해서는 규명된 바가 없었다.
이번 연구에서 KAIST-충남대병원 공동연구팀은 한국인 코로나19 환자들을 대상으로 진단 초기부터 회복 시까지 추적 연구를 수행해 코로나19 바이러스 감염증에서 질병의 진행 과정에 따라 자연살해 세포에 일어나는 변화를 최초로 규명했고, 중증 환자와 경증 환자에서 자연살해 세포의 특성 및 기능의 차이점에 대해 밝혔다. 특히 이번 연구에서는 최첨단 면역학 연구기법과 유전자 발현 분석을 동시에 활용해 코로나19 환자에서 자연살해 세포들에 나타나는 변화를 다각도에서 분석하고 규명했다.
공동연구팀은 정상인이나 독감 환자와는 달리 코로나19 환자에게서만 특징적으로 나타나는 비정형 자연살해 세포를 발견했고, 이러한 비정형 자연살해 세포가 일반적인 자연살해 세포보다 세포독성 기능이 감소해있음을 밝혔다.
연구팀은 이러한 비정형 자연살해 세포들이 질병의 중증도와 관계없이 코로나19 바이러스에 감염된 환자들에서 공통적으로 질병 초기에 빠르게 증가하며, 이로 인해 코로나19 환자의 선천면역 반응이 약화되어 있음을 밝혔다. 그리고 코로나19 환자들의 질병 진행 과정에서 자연살해 세포 특성을 추적 관찰한 결과, 중증 코로나19 환자에서 이러한 비정형 자연살해 세포들의 증가 상태가 더 장기간 지속되며 이는 선천면역 반응의 손상과 연관됨을 밝혔다.
이번 연구는 세계 처음으로 코로나19 환자에서 비정형 자연살해 세포의 증가를 발견해 코로나19 환자에서 나타나는 선천면역 반응 손상의 기전을 보고한 연구로 세계 면역학계의 주목을 받고 있다.
과학기술원 공동연구과제의 지원을 받아 수행한 이번 연구 결과는 국제 저명 학술지인 `알레르기 및 임상면역학 저널(The Journal of Allergy and Clinical Immunolgy)'에 게재됐다. 특히 이번 논문은 저널 편집자로부터 주목을 받아야 할 주요 연구성과로 선정돼 하이라이트 논문으로 저널에 소개될 예정이다. (논문명: Abnormality in the NK cell population is prolonged in severe COVID-19 patients)
이번 연구의 제1 저자인 우리 대학 임가람 박사 연구원(現 연세의대 소화기내과 임상강사)은 "코로나19 바이러스 감염증에서 특징적으로 비정형 자연살해 세포들이 증가해 있음을 발견했다ˮ며 "다른 호흡기 바이러스 감염에서는 보이지 않는 이러한 자연살해 세포 변화는 코로나19 바이러스 감염증의 임상적 특징을 이해하고, 중증 환자에서 선제적인 치료를 조기에 시작하는 임상적 근거가 될 것이다ˮ고 설명했다.
충남대병원 김연숙 교수는 "이번 연구는 코로나19 환자의 질병 과정의 초기부터 회복기까지 자연살해 세포의 변화 및 특성을 세계에서 최초로 분석해 규명한 연구 결과로서 코로나19 환자에서 나타나는 선천면역 반응의 손상 기전을 최초로 밝혔다는 점에서 의미가 있는 연구ˮ라고 말했다.
코로나19 환자에서 나타나는 자연살해 세포 변화 규명
우리 대학 의과학대학원 신의철 교수 연구팀이 충남대학교병원 감염내과 김연숙, 천신혜 교수팀과의 공동연구를 통해 코로나19 환자들에서 자연살해 세포의 항바이러스 기능이 약화돼 있고, 이러한 기능 변화는 경증 코로나19 환자에서는 일주일 내로 사라지지만 중증 환자에서는 오래 지속됨을 규명했다고 10일 밝혔다. 이로써, 항바이러스 선천면역 반응의 한 축을 담당하는 자연살해 세포의 기능 이상을 중증 코로나19 환자에서 처음으로 규명하게 됐다.
우리 몸은 바이러스에 감염되면 이에 대항하여 일차적으로 선천면역 반응이 나타나며, 항바이러스 선천면역 반응을 담당하는 주된 세포가 바로 자연살해 세포다. 이러한 자연살해 세포의 대부분을 차지하는 것이 바이러스에 감염된 세포를 직접 죽이는 세포독성 자연살해 세포인데, 코로나19 환자에서 이러한 세포독성 자연살해 세포의 수나 기능이 감소돼 있다는 보고는 있었지만, 자연살해 세포의 구체적인 변화나 기능감소 기전에 대해서는 규명된 바가 없었다.
이번 연구에서 KAIST-충남대병원 공동연구팀은 한국인 코로나19 환자들을 대상으로 진단 초기부터 회복 시까지 추적 연구를 수행해 코로나19 바이러스 감염증에서 질병의 진행 과정에 따라 자연살해 세포에 일어나는 변화를 최초로 규명했고, 중증 환자와 경증 환자에서 자연살해 세포의 특성 및 기능의 차이점에 대해 밝혔다. 특히 이번 연구에서는 최첨단 면역학 연구기법과 유전자 발현 분석을 동시에 활용해 코로나19 환자에서 자연살해 세포들에 나타나는 변화를 다각도에서 분석하고 규명했다.
공동연구팀은 정상인이나 독감 환자와는 달리 코로나19 환자에게서만 특징적으로 나타나는 비정형 자연살해 세포를 발견했고, 이러한 비정형 자연살해 세포가 일반적인 자연살해 세포보다 세포독성 기능이 감소해있음을 밝혔다.
연구팀은 이러한 비정형 자연살해 세포들이 질병의 중증도와 관계없이 코로나19 바이러스에 감염된 환자들에서 공통적으로 질병 초기에 빠르게 증가하며, 이로 인해 코로나19 환자의 선천면역 반응이 약화되어 있음을 밝혔다. 그리고 코로나19 환자들의 질병 진행 과정에서 자연살해 세포 특성을 추적 관찰한 결과, 중증 코로나19 환자에서 이러한 비정형 자연살해 세포들의 증가 상태가 더 장기간 지속되며 이는 선천면역 반응의 손상과 연관됨을 밝혔다.
이번 연구는 세계 처음으로 코로나19 환자에서 비정형 자연살해 세포의 증가를 발견해 코로나19 환자에서 나타나는 선천면역 반응 손상의 기전을 보고한 연구로 세계 면역학계의 주목을 받고 있다.
과학기술원 공동연구과제의 지원을 받아 수행한 이번 연구 결과는 국제 저명 학술지인 `알레르기 및 임상면역학 저널(The Journal of Allergy and Clinical Immunolgy)'에 게재됐다. 특히 이번 논문은 저널 편집자로부터 주목을 받아야 할 주요 연구성과로 선정돼 하이라이트 논문으로 저널에 소개될 예정이다. (논문명: Abnormality in the NK cell population is prolonged in severe COVID-19 patients)
이번 연구의 제1 저자인 우리 대학 임가람 박사 연구원(現 연세의대 소화기내과 임상강사)은 "코로나19 바이러스 감염증에서 특징적으로 비정형 자연살해 세포들이 증가해 있음을 발견했다ˮ며 "다른 호흡기 바이러스 감염에서는 보이지 않는 이러한 자연살해 세포 변화는 코로나19 바이러스 감염증의 임상적 특징을 이해하고, 중증 환자에서 선제적인 치료를 조기에 시작하는 임상적 근거가 될 것이다ˮ고 설명했다.
충남대병원 김연숙 교수는 "이번 연구는 코로나19 환자의 질병 과정의 초기부터 회복기까지 자연살해 세포의 변화 및 특성을 세계에서 최초로 분석해 규명한 연구 결과로서 코로나19 환자에서 나타나는 선천면역 반응의 손상 기전을 최초로 밝혔다는 점에서 의미가 있는 연구ˮ라고 말했다.
2021.08.11
조회수 10991
-
 효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2021.01.06
조회수 56551
 인공지능 기반 대장암 3차원 게놈 지도 최초 해독
세계 최초로 예전에 비해 최대 규모로 한국인 대장암 환자 3차원 게놈 지도를 작성하여 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 서울대학교 암연구소 김태유 교수 연구팀과의 공동연구를 통해 인공지능 기반 알고리즘을 활용, 한국인 대장암 환자의 3차원 게놈 지도를 최초로 제시했으며 이를 토대로 암 세포 특이적인 유전자 조절 기전을 통해 특정 종양유전자들이 과발현되는 현상을 규명했다고 24일 밝혔다.
1차원적 게놈 서열 분석에 기반한 현재의 암 유전체 연구는 종양유전자들의 과발현 기작을 설명하는데 한계가 있었다. 하지만 3차원 공간상에 게놈이 어떻게 배열되는지를 분석하는 3차원 게놈 (3D genome) 구조 연구는 이러한 한계를 극복 가능케 하고 있다. 본 연구에서는 정상 세포에서는 존재하지 않는 암 세포 특이적 염색질 고리(chromatin loop) 구조가 유전자 발현 촉진 인자인 인핸서와 종양유전자 사이의 상호작용을 형성하여 과발현을 유도하는 인핸서 납치(enhancer-hijacking) 현상에 초점을 두어 연구하였다.
우리 대학 생명과학과 김규광 박사과정이 주도한 이번 연구는 게놈간의 공간상 상호작용을 측정할 수 있는 대용량 염색체 구조 포착 Hi-C (High-throughput Chromosome Conformation Capture) 실험 기법을 활용하여 대장암 3차원 게놈 지도를 작성하고 대장암 특이적 3차원 게놈 변화를 환자 개개인별로 분석할 수 있는 인공지능 기반 알고리즘을 개발했다. 그 결과 공동연구팀은 광범위한 규모의 3차원 게놈 구조 변화와 이로 인한 다양한 종양유전자의 활성화를 확인했다.
연구팀은 이번 연구를 통해 암 특이적 3차원 게놈 구조의 변화로 인한 종양유전자 활성 기작을 명확히 제시하였으며 이로 인한 환자 예후와 약물 반응 등 임상적인 특성과의 연관성까지 제시해 맞춤 치료 원천기술 확보에 기여했다.
지금까지 암 세포주에 대한 3차원 게놈 구조 연구는 일부 보고 되었으나, 대규모 환자 암조직에 대한 연구는 조직 내 세포 이질성, 종양 순도, 암세포 이질성 등의 문제로 인한 정밀 암 특이적 3차원 게놈 구조 분석의 한계로 수행되지 못하였다.
반면에 이번 연구에서 연구팀은 AI 기반 알고리즘으로 환자 개인 종양 조직으로부터 얻어진 복잡한 신호를 해석할 수 있었으며 그 결과 최대 규모인 환자 40명의 종양 조직과 인접한 정상 대장 조직을 사용해 3차원 게놈 지도를 작성할 수 있었다. 또한 DNA 서열정보를 보여주는 전장유전체 지도의 경우 다양한 인종에 대해 생산되고 있고 한국인의 전장유전체 지도 또한 개발되었으나 한국인 3차원 게놈 지도, 특히 종양 조직에 대한 3차원 게놈 지도는 이번 연구에서 최초로 제시됐다.
이번 연구 결과는 국제 학술지, `셀 리포츠(Cell Reports, IF=9.995)'에 7월 13일 자로 출판됐다. (논문명: Spatial and clonality-resolved 3D cancer genome alterations reveal enhancer-hijacking as a potential prognostic marker for colorectal cancer)
서울대학교병원 혈액종양내과 김태유 교수는 “이러한 결과는 개별 암 환자들마다 서로 다르게 나타나는 종양 이질성을 이해하는 데 매우 중요한 요소가 될 수 있으며, 이를 이용한 환자 맞춤형 치료 연구의 시발점이 될 것이다”라고 말했다. 생명과학과 정인경 교수는 “기존의 점돌연변이나 유전체 변이만으로는 설명이 어려운 암 유전체를 3차원 게놈 구조 관점에서 재해독하고 신규 암 타겟을 발굴할 수 있는 수 있는 새로운 접근법을 제시했다”라고 밝혔다.
한편 이번 연구는 과학기술정보통신부와 서경배과학재단의 지원을 받아 수행됐다.
2023.07.24 조회수 8843
인공지능 기반 대장암 3차원 게놈 지도 최초 해독
세계 최초로 예전에 비해 최대 규모로 한국인 대장암 환자 3차원 게놈 지도를 작성하여 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 서울대학교 암연구소 김태유 교수 연구팀과의 공동연구를 통해 인공지능 기반 알고리즘을 활용, 한국인 대장암 환자의 3차원 게놈 지도를 최초로 제시했으며 이를 토대로 암 세포 특이적인 유전자 조절 기전을 통해 특정 종양유전자들이 과발현되는 현상을 규명했다고 24일 밝혔다.
1차원적 게놈 서열 분석에 기반한 현재의 암 유전체 연구는 종양유전자들의 과발현 기작을 설명하는데 한계가 있었다. 하지만 3차원 공간상에 게놈이 어떻게 배열되는지를 분석하는 3차원 게놈 (3D genome) 구조 연구는 이러한 한계를 극복 가능케 하고 있다. 본 연구에서는 정상 세포에서는 존재하지 않는 암 세포 특이적 염색질 고리(chromatin loop) 구조가 유전자 발현 촉진 인자인 인핸서와 종양유전자 사이의 상호작용을 형성하여 과발현을 유도하는 인핸서 납치(enhancer-hijacking) 현상에 초점을 두어 연구하였다.
우리 대학 생명과학과 김규광 박사과정이 주도한 이번 연구는 게놈간의 공간상 상호작용을 측정할 수 있는 대용량 염색체 구조 포착 Hi-C (High-throughput Chromosome Conformation Capture) 실험 기법을 활용하여 대장암 3차원 게놈 지도를 작성하고 대장암 특이적 3차원 게놈 변화를 환자 개개인별로 분석할 수 있는 인공지능 기반 알고리즘을 개발했다. 그 결과 공동연구팀은 광범위한 규모의 3차원 게놈 구조 변화와 이로 인한 다양한 종양유전자의 활성화를 확인했다.
연구팀은 이번 연구를 통해 암 특이적 3차원 게놈 구조의 변화로 인한 종양유전자 활성 기작을 명확히 제시하였으며 이로 인한 환자 예후와 약물 반응 등 임상적인 특성과의 연관성까지 제시해 맞춤 치료 원천기술 확보에 기여했다.
지금까지 암 세포주에 대한 3차원 게놈 구조 연구는 일부 보고 되었으나, 대규모 환자 암조직에 대한 연구는 조직 내 세포 이질성, 종양 순도, 암세포 이질성 등의 문제로 인한 정밀 암 특이적 3차원 게놈 구조 분석의 한계로 수행되지 못하였다.
반면에 이번 연구에서 연구팀은 AI 기반 알고리즘으로 환자 개인 종양 조직으로부터 얻어진 복잡한 신호를 해석할 수 있었으며 그 결과 최대 규모인 환자 40명의 종양 조직과 인접한 정상 대장 조직을 사용해 3차원 게놈 지도를 작성할 수 있었다. 또한 DNA 서열정보를 보여주는 전장유전체 지도의 경우 다양한 인종에 대해 생산되고 있고 한국인의 전장유전체 지도 또한 개발되었으나 한국인 3차원 게놈 지도, 특히 종양 조직에 대한 3차원 게놈 지도는 이번 연구에서 최초로 제시됐다.
이번 연구 결과는 국제 학술지, `셀 리포츠(Cell Reports, IF=9.995)'에 7월 13일 자로 출판됐다. (논문명: Spatial and clonality-resolved 3D cancer genome alterations reveal enhancer-hijacking as a potential prognostic marker for colorectal cancer)
서울대학교병원 혈액종양내과 김태유 교수는 “이러한 결과는 개별 암 환자들마다 서로 다르게 나타나는 종양 이질성을 이해하는 데 매우 중요한 요소가 될 수 있으며, 이를 이용한 환자 맞춤형 치료 연구의 시발점이 될 것이다”라고 말했다. 생명과학과 정인경 교수는 “기존의 점돌연변이나 유전체 변이만으로는 설명이 어려운 암 유전체를 3차원 게놈 구조 관점에서 재해독하고 신규 암 타겟을 발굴할 수 있는 수 있는 새로운 접근법을 제시했다”라고 밝혔다.
한편 이번 연구는 과학기술정보통신부와 서경배과학재단의 지원을 받아 수행됐다.
2023.07.24 조회수 8843 천식 등 만성질환 염증 조절 실마리 풀어
우리 몸에 침입한 병원균이나 암세포를 치료할 수 있는 면역세포인 T세포 중 CD4+ T세포는 적응면역계의 지휘관과 같은 역할을 하며, 이러한 CD4+ T세포의 활성 정도에 따라서 천식과 같은 만성질환의 진행 양상과 예후가 달라지게 된다. T세포의 활성화 증폭을 위해서는 마치 과녁 모양처럼 면역학적 시냅스 형성이 필요하다는 보고들이 있으나 어떠한 메커니즘으로 면역학적 시냅스가 형성이 되는지는 잘 알려져 있지 않았다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 면역학적 시냅스 형성에 섬모 형성 단백질(IFT20)과 엔도솜 형성 단백질(TSG101)의 결합이 중요한 역할을 한다고 26일 밝혔다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사), 강인 박사과정, 생명과학과 김유민 박사과정 등이 주도한 이번 연구에서 연구팀은 단일세포 전사체 분석법을 활용해 활성화된 CD4+ T세포에서 섬모 형성 단백질(IFT20)의 발현이 증가해 있음을 확인했다.
연구팀은 T세포에 국한되어 섬모 형성 단백질(IFT20)이 결핍된 마우스를 제작해 해당 마우스가 정상 마우스보다 천식 증상의 특징이 감소함을 확인했고, 이는 정상 CD4+ T세포와 비교했을 때 섬모 형성 단백질(IFT20) 결핍 CD4+ T세포가 면역학적 시냅스 형성을 감소시켜 T세포 증식, 해당작용 및 세포호흡이 감소하기 때문임을 확인했다.
또한, 연구팀은 섬모 형성 단백질(IFT20)에 결합하는 단백질을 찾기 위해 효모단백질잡종법과 면역침강법을 이용함으로써 섬모 형성 단백질(IFT20)이 엔도솜 형성단백질(TSG101)과 서로 결합한다는 것을 세계 최초로 규명했다.
이를 입증하기 위해 연구팀은 T세포에 국한되어 엔도솜 형성단백질(TSG101)이 결핍된 마우스를 제작해 엔도솜 형성단백질(TSG101)이 결핍된 CD4+ T세포가 정상 CD4+ T세포에 비해 면역학적 시냅스 형성이 감소함을 확인했다. 결과적으로 기존에 알려지지 않았던 면역학적 시냅스 형성에 기여하는 섬모형성 단백질(IFT20)과 엔도솜 형성단백질(TSG101)의 역할을 밝힘으로써 T세포 활성화를 조절할 수 있는 단서를 제공했다는 점에서 큰 의의가 있다.
이번 연구를 주도한 정지웅 박사는 "그동안 잘 알려지지 않은 면역학적 시냅스 형성을 조절하는 단백질을 확인하는 중요한 연구”라고 설명했다. 이흥규 교수는 “면역학적 시냅스 형성의 변화를 통해 천식의 염증 정도가 변화할 수 있음을 확인했고, 향후 면역학적 시냅스를 조절함으로써 천식을 비롯한 다양한 면역 질환 등에서 질환의 염증을 조절하는 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사)가 제1 저자로 참여한 이번 연구는 면역학 분야 국제 학술지 `세포 및 분자 면역학(Cellular & Molecular Immunology, JCR IF = 22.10)'에 4월 7일 字 온라인판에 게재됐다. (논문명: Regulation of c-SMAC formation and AKT-mTOR signaling by the TSG101-IFT20 axis in CD4+ T cells)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업 및 글로벌박사양성사업의 지원을 받아 수행됐다.
2023.04.26 조회수 8011
천식 등 만성질환 염증 조절 실마리 풀어
우리 몸에 침입한 병원균이나 암세포를 치료할 수 있는 면역세포인 T세포 중 CD4+ T세포는 적응면역계의 지휘관과 같은 역할을 하며, 이러한 CD4+ T세포의 활성 정도에 따라서 천식과 같은 만성질환의 진행 양상과 예후가 달라지게 된다. T세포의 활성화 증폭을 위해서는 마치 과녁 모양처럼 면역학적 시냅스 형성이 필요하다는 보고들이 있으나 어떠한 메커니즘으로 면역학적 시냅스가 형성이 되는지는 잘 알려져 있지 않았다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 면역학적 시냅스 형성에 섬모 형성 단백질(IFT20)과 엔도솜 형성 단백질(TSG101)의 결합이 중요한 역할을 한다고 26일 밝혔다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사), 강인 박사과정, 생명과학과 김유민 박사과정 등이 주도한 이번 연구에서 연구팀은 단일세포 전사체 분석법을 활용해 활성화된 CD4+ T세포에서 섬모 형성 단백질(IFT20)의 발현이 증가해 있음을 확인했다.
연구팀은 T세포에 국한되어 섬모 형성 단백질(IFT20)이 결핍된 마우스를 제작해 해당 마우스가 정상 마우스보다 천식 증상의 특징이 감소함을 확인했고, 이는 정상 CD4+ T세포와 비교했을 때 섬모 형성 단백질(IFT20) 결핍 CD4+ T세포가 면역학적 시냅스 형성을 감소시켜 T세포 증식, 해당작용 및 세포호흡이 감소하기 때문임을 확인했다.
또한, 연구팀은 섬모 형성 단백질(IFT20)에 결합하는 단백질을 찾기 위해 효모단백질잡종법과 면역침강법을 이용함으로써 섬모 형성 단백질(IFT20)이 엔도솜 형성단백질(TSG101)과 서로 결합한다는 것을 세계 최초로 규명했다.
이를 입증하기 위해 연구팀은 T세포에 국한되어 엔도솜 형성단백질(TSG101)이 결핍된 마우스를 제작해 엔도솜 형성단백질(TSG101)이 결핍된 CD4+ T세포가 정상 CD4+ T세포에 비해 면역학적 시냅스 형성이 감소함을 확인했다. 결과적으로 기존에 알려지지 않았던 면역학적 시냅스 형성에 기여하는 섬모형성 단백질(IFT20)과 엔도솜 형성단백질(TSG101)의 역할을 밝힘으로써 T세포 활성화를 조절할 수 있는 단서를 제공했다는 점에서 큰 의의가 있다.
이번 연구를 주도한 정지웅 박사는 "그동안 잘 알려지지 않은 면역학적 시냅스 형성을 조절하는 단백질을 확인하는 중요한 연구”라고 설명했다. 이흥규 교수는 “면역학적 시냅스 형성의 변화를 통해 천식의 염증 정도가 변화할 수 있음을 확인했고, 향후 면역학적 시냅스를 조절함으로써 천식을 비롯한 다양한 면역 질환 등에서 질환의 염증을 조절하는 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 정지웅 박사(현, 서울대병원 알레르기내과 임상강사)가 제1 저자로 참여한 이번 연구는 면역학 분야 국제 학술지 `세포 및 분자 면역학(Cellular & Molecular Immunology, JCR IF = 22.10)'에 4월 7일 字 온라인판에 게재됐다. (논문명: Regulation of c-SMAC formation and AKT-mTOR signaling by the TSG101-IFT20 axis in CD4+ T cells)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업 및 글로벌박사양성사업의 지원을 받아 수행됐다.
2023.04.26 조회수 8011 노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
2023.03.15 조회수 7726
노화된 뇌막 속 쌓인 당이 장애 유발 최초 규명
평균연령 증가로 인해 심각한 뇌 질환을 동반하지 않은 일반적인 노화로 인한 뇌의 변화에 관한 연구 역시 필요한 추세다. 노화 연구와 관련하여 노화가 진행될수록 몸속에 ‘당’이 축적되고 이렇게 축적된 당은 노화-연관 염증, 혈관질환 등 다양한 질환의 원인 물질이 된다. 결국‘남아도는 당 분자’는 몸속 다양한 단백질에 붙어 단백질의 기능을 방해한다.
우리 대학 바이오및뇌공학과 김필남 교수, 정용 교수 공동연구팀이 뇌를 감싸고 있는 뇌막(혹은 뇌수막; brain meninges)이 노화에 따른 `당' 축적이 되면서 뇌 피질을 감싸고 있는 ‘최전선 방어벽'으로의 기능에 장애가 일어남을 확인했다고 15일 밝혔다.
김 교수 연구팀은 고령자의 뇌막에서 당 분자의 과도한 축적을 확인하고, 생쥐 모델에서도 나이에 따른 당의 축적이 이뤄짐을 확인하였다. 뇌막은 뇌를 감싸고 있는 얇은 막으로 뇌척수액과 피질의 경계에 존재하며 뇌를 보호하는 중요한 기능을 하고 있다. 이번 연구에서는 이러한 뇌막이 노화로 인해 생기는 기능이상이 뇌 속 ‘남아도는’ 당에 의해서 유도됨을 밝혔다. 특히, 노화에 의해서 뇌막이 얇아지고 끈적해지면서 뇌척수액과 뇌피질과의 물질교환이 감소하는 것에 대한 원리 규명에 새로운 패러다임을 제공하게 되었다.
이번 연구는 KAIST 바이오및뇌공학과 김효민 박사과정 학생과 김신흔 박사가 공동 제1 저자로 참여해 국제 학술지 `노화하는 세포(Aging Cell)'에 지난 2월 28일 자 온라인판으로 게재됐다. (논문명: Glycation mediated tissue level remodeling of brain meningeal membrane by aging)
뇌척수액과 직접 맞닿아 있는 뇌막은 주로 콜라겐 (collagen)이라는 세포외기질 (Extracellular Matrix, ECM) 단백질로 구성되어 있으며 이 단백질을 생산하는 세포인 섬유아세포 (fibroblast) 로 이루어져 있다. 당이 흡착된 콜라겐 단백질과 부착된 세포는 콜라겐의 생산기능이 떨어지는 반면, 콜라겐의 분해 효소의 발현이 높아지면서 뇌막은 지속적으로 얇아지고 붕괴된다.
지속적인 당 섭취로 인해서 초과된 당 분자가 뇌에 쌓이면서 신경세포의 변성과 뇌 질환 간의 연구는 지속적으로 진행되어 왔다. 하지만 뇌를 감싸고 있는 뇌막 자체에 초점을 두어 당 축적으로 인한 뇌막 변성 및 기능 장애를 확인한 것은 이번 연구에서 최초로 제시되었으며, 이는 뇌 질환 연구에서의 새로운 치료접근을 제시할 것을 기대할 수 있다.
제1 저자인 김효민 연구원은 “인간의 뇌에서 시작해서 생체모사 뇌막 모델과 동물모델을 활용한 융합적 접근으로 노화로 인한 뇌 장벽 변화에 대해 규명한 흥미로운 연구ˮ 라고 연구 결과를 소개했다.
김필남 교수 연구팀은 이러한 뇌막을 비롯한 인체 전반적으로 쌓이는 당을 제거하기 위한 연구개발을 진행하고 있다. 인체에서 단백질과 당이 만나서 형성되는 찌꺼기인 최종당화산물(Advanced glycation end product)는 대식세포에 의해서 일부 제거된다. 하지만, 콜라겐과 같은 세포외기질 단백질과 결합한 당화산물은 자연적으로는 제거되기 어렵다. 본 연구진은 KAIST-세라젬 연구센터를 통해서 ‘몸 속 당 찌꺼기’ 제거를 위한 헬스케어 의료기기를 개발하고 있다.
이번 연구는 한국연구재단 집단연구지원을 받아 수행됐다.
2023.03.15 조회수 7726 비만이 성병 헤르페스를 억제하는 메커니즘 규명
우리 연구진이 성병을 일으키는 2형 헤르페스 감염에 대해 비만인 암컷 생쥐가 더 높은 저항성을 갖는다는 사실을 밝혔다. 나쁘기만 할 것 같은 비만이 오히려 도움이 되는 역설적인 현상을 관찰한 것이다.
※ 2형 헤르페스: 헤르페스 바이러스의 일종으로 주로 성병을 일으키는 것으로 알려짐. 여성이 남성보다 더 높은 감염률을 보이는 것으로 알려짐.
의과학대학원 이흥규 교수 연구팀이 비만이 여성 생식기를 통한 단순 2형 헤르페스 바이러스(herpes simplex virus type 2) 감염에 대해 저항성을 강화하는 현상을 발견했으며, 그 메커니즘을 규명했음을 6일 밝혔다.
비만은 종양 등 각종 질병에 대해 안 좋은 영향을 끼치는 인자로 잘 알려져 있다. 하지만, 여성 생식기를 통한 2형 헤르페스 감염 시 질 내 공생미생물과 감마델타 T세포의 상호작용을 통해 바이러스에 저항성이 생긴다는 사실을 연구팀은 발견했다.
여성의 생식기 내에는 젖산균을 포함한 공생미생물이 서식하고 있다. 비만인 여성은 마른 여성과는 질 내 공생미생물의 조성이 다른 것으로 알려져 있는데, 연구팀은 비만인 암컷 생쥐의 질 내에는 장에서 유래한 것으로 보이는 균들이 섞여 있는 것을 발견했다.
연구팀은 장에서 유래된 것으로 보이는 비만 암컷 생쥐의 질 내에 유입된 균들이 아미노산의 일종인 아르기닌을 활발하게 생산하고 있다는 사실을 발견했고, 아르기닌이 바이러스 초기 감염에 중요한 역할을 한다는 사실을 발견했다.
연구팀은 이어서 아르기닌이 질 내의 감마델타 T 세포의 항바이러스 면역반응을 강화하고, 적응 면역세포가 활성화되는 시기보다 이른 시기에 바이러스 감염과 전파를 이미 억제하고 있음을 발견했다.
연구를 주도한 의과학대학원 이흥규 교수는 "이번 연구는 비만이 특정 감염 질병에는 도움이 될 수도 있다는 사실을 밝혔다는 점에서 의의가 있고, 앞으로 비만인 환자들의 바이러스 감염증 치료에 참고가 될 것이며, 연구 결과를 바탕으로 분자 메커니즘을 응용해 항바이러스제 개발에 박차를 가할 것이다ˮ고 연구의 중요성을 설명했다.
비만이 바이러스를 억제하는 현상을 발견하고 그 메커니즘을 규명한 이번 연구는 한국연구재단의 중견연구지원사업 및 바이오의료기술개발사업의 지원으로 수행됐으며, 의과학대학원 박장현 박사가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제학술지 `셀 리포트(Cell Reports)'에 지난 11월 8일 字 게재됐다.
2022.12.06 조회수 9386
비만이 성병 헤르페스를 억제하는 메커니즘 규명
우리 연구진이 성병을 일으키는 2형 헤르페스 감염에 대해 비만인 암컷 생쥐가 더 높은 저항성을 갖는다는 사실을 밝혔다. 나쁘기만 할 것 같은 비만이 오히려 도움이 되는 역설적인 현상을 관찰한 것이다.
※ 2형 헤르페스: 헤르페스 바이러스의 일종으로 주로 성병을 일으키는 것으로 알려짐. 여성이 남성보다 더 높은 감염률을 보이는 것으로 알려짐.
의과학대학원 이흥규 교수 연구팀이 비만이 여성 생식기를 통한 단순 2형 헤르페스 바이러스(herpes simplex virus type 2) 감염에 대해 저항성을 강화하는 현상을 발견했으며, 그 메커니즘을 규명했음을 6일 밝혔다.
비만은 종양 등 각종 질병에 대해 안 좋은 영향을 끼치는 인자로 잘 알려져 있다. 하지만, 여성 생식기를 통한 2형 헤르페스 감염 시 질 내 공생미생물과 감마델타 T세포의 상호작용을 통해 바이러스에 저항성이 생긴다는 사실을 연구팀은 발견했다.
여성의 생식기 내에는 젖산균을 포함한 공생미생물이 서식하고 있다. 비만인 여성은 마른 여성과는 질 내 공생미생물의 조성이 다른 것으로 알려져 있는데, 연구팀은 비만인 암컷 생쥐의 질 내에는 장에서 유래한 것으로 보이는 균들이 섞여 있는 것을 발견했다.
연구팀은 장에서 유래된 것으로 보이는 비만 암컷 생쥐의 질 내에 유입된 균들이 아미노산의 일종인 아르기닌을 활발하게 생산하고 있다는 사실을 발견했고, 아르기닌이 바이러스 초기 감염에 중요한 역할을 한다는 사실을 발견했다.
연구팀은 이어서 아르기닌이 질 내의 감마델타 T 세포의 항바이러스 면역반응을 강화하고, 적응 면역세포가 활성화되는 시기보다 이른 시기에 바이러스 감염과 전파를 이미 억제하고 있음을 발견했다.
연구를 주도한 의과학대학원 이흥규 교수는 "이번 연구는 비만이 특정 감염 질병에는 도움이 될 수도 있다는 사실을 밝혔다는 점에서 의의가 있고, 앞으로 비만인 환자들의 바이러스 감염증 치료에 참고가 될 것이며, 연구 결과를 바탕으로 분자 메커니즘을 응용해 항바이러스제 개발에 박차를 가할 것이다ˮ고 연구의 중요성을 설명했다.
비만이 바이러스를 억제하는 현상을 발견하고 그 메커니즘을 규명한 이번 연구는 한국연구재단의 중견연구지원사업 및 바이오의료기술개발사업의 지원으로 수행됐으며, 의과학대학원 박장현 박사가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제학술지 `셀 리포트(Cell Reports)'에 지난 11월 8일 字 게재됐다.
2022.12.06 조회수 9386 장 조직의 항상성과 염증성 장염 회복의 핵심 효소 발견
우리 대학 생명과학과 김세윤, 양한슬 교수 공동연구팀이 `장 상피조직의 발생과 염증성 장염 회복과정의 핵심 효소발굴'에 성공했다고 6일 밝혔다.
생명과학과 박승은 박사, 이동은 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `세포 및 분자 소화기학 및 간장학 (Cellular and Molecular Gastroenterology & Hepatology)'에 지난 8월 19일 字 온라인 게재됐다.
※ 논문명 : Gut Epithelial Inositol Polyphosphate Multikinase Alleviates Experimental Colitis via Governing Tuft Cell Homeostasis
※ 저자 정보 : 박승은 (한국과학기술원, 공동 제1 저자), 이동은 (한국과학기술원, 공동 제1 저자), 정재웅 (연세대학교 의과대학, 제2 저자), 이수형 (반더빌트 의과대학, 공동 저자), 박승주 (한국과학기술원, 공동 저자), 류재승 (한국과학기술원, 공동 저자), 오세규 (카이노젠, 공동 저자), 양한슬 (한국과학기술원, 공동 교신저자), 황성순 (연세대학교 의과대학, 공동 교신저자), 김세윤 (한국과학기술원, 공동 교신저자), 포함 총 10명
염증성 장 질환은 1980년대 중반까지만 해도 국내 발병률은 매우 낮은 질환이었으나 건강보험심사평가원 자료에 따르면 2011년 말 만성 염증성 장 질환인 크론병 환자가 1만3천여 명, 궤양성 대장염 환자가 2만9천여 명으로 집계됐으며 이후로도 환자 수가 빠르게 증가하고 있다.
궤양성 대장염과 크론병과 같은 염증성 장 질환(Inflammatory bowel disease)은 복통, 설사뿐 아니라 전신 무력감, 체중 감소, 장 천공 등의 합병증을 유발해 환자의 삶의 질을 크게 낮추는 심각한 질환이다.
이러한 염증성 장 질환은 아직 발병 메커니즘이 명확하게 규명되지 않았으며 서구화된 식습관과 함께 유전적 이상이나 면역학적 장애 또는 스트레스와 같은 환경적인 요인이 복합적으로 관여하는 것으로 여겨진다.
최근 염증성 장 질환의 환자군 일부에서 이노시톨 대사(체내 합성 또는 음식을 통하여 공급되는 이노시톨 영양소를 이노시톨 인산 물질들로 전환하는 세포 내 생화학적 반응)의 핵심 효소인 이노시톨 폴리인산 카이네이즈(Inositol polyphosphate multikinase, 이하 IPMK) 유전자에서 단일염기변이(single nucleotide polymorphism, SNP) 등이 보고됐다. IPMK 효소는 포유류의 이노시톨 대사에서 매우 중추적인 역할을 하는 단백질로서 세포의 성장과 대사뿐 아니라 면역 반응 및 중추 신경계 기억 조절 등의 다각적인 생물학적 기능을 수행하는 것으로 알려졌으나 소화기계에서의 생물학적 기능은 밝혀진 바가 전혀 없다.
이에 우리 대학 생명과학과 및 줄기세포 연구센터 김세윤 교수, 양한슬 교수 연구팀은 연세대학교 의과대학 황성순 교수 연구팀과의 공동연구를 통해 장 상피세포에서의 IPMK 효소의 역할규명연구를 다각적으로 수행했다.
연구팀은 먼저 장 상피세포에서 IPMK 유전자가 결손된 생쥐 연구모델을 제작했고 이를 분석한 결과에 따르면 정상적인 환경에서는 뚜렷한 장 조직의 구조와 기능에 있어 문제가 발생하지 않았다. 그러나 덱스트란 황산나트륨(DSS)을 투여해 대장염을 유발할 경우, IPMK 유전자가 결손된 생쥐로부터 대장염 회복반응이 현저하게 둔화됨을 관찰했고 이로부터 IPMK 효소가 손상된 대장 조직이 회복되는데 필수적인 인자임을 규명했다.
특히 연구팀은 IPMK 효소가 제거된 장 조직에서는 솔세포(tuft cell)의 발생과 기능에 심각한 장애가 발생함을 관찰했다. 솔세포란 소장과 대장뿐 아니라 흉선, 췌장 등에 존재하는 세포로서 표면에 미세 융모구조를 보이는 독특한 세포다. 장 조직의 전체 세포 중 불과 2~3% 이하로 존재하는 솔세포는 외부로부터의 기생충 감염에 대응하는 면역기능을 수행한다. 또한 솔세포로부터 합성돼 분비되는 아세틸콜린 신경전달물질은 장내 줄기세포 및 신경세포를 자극해 장 조직의 항상성 유지와 손상 복구에 중요한 기능을 담당하는 것으로 알려져 있다. 이러한 중요성에도 불구하고 솔세포의 발생과 기능을 조절하는 분자 타깃에 대한 이해는 극히 부족한 것으로 알려져 있다.
공동연구팀은 첨단 단일세포 RNA 유전자 배열 순서 분석기술(single cell RNA sequencing)을 통해 IPMK 효소가 제거된 장 상피조직에서 아세틸콜린 분비를 담당하는 솔세포군의 발생이 특이적으로 감소함을 규명했다. 또한 이러한 분석과정에서 생쥐의 대장에 존재하는 솔세포는 크게 면역기능을 담당하는 세포군, 아세틸콜린 분비 솔세포군 외에 유전자 발현 능력이 감소한 새로운 솔세포군이 있다는 사실을 발견해 학계에 최초 보고했다.
연구팀 관계자는 "발굴한 IPMK 효소에 기반한 아세틸콜린 분비성 솔세포의 발생 및 기능조절은 향후 장 상피조직의 항상성 유지의 학문적 이해와 더불어 염증성 장 질환의 진단 및 치료기술 개발 등에 적극적으로 활용될 것ˮ이라며 연구의 의의를 설명했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 서경배과학재단, KAIST 줄기세포 연구센터 지원사업, KAIST 그랜드챌린지 30 (KC30) 사업 및 포스코청암펠로십의 지원을 받아 수행됐다.
2022.10.06 조회수 10781
장 조직의 항상성과 염증성 장염 회복의 핵심 효소 발견
우리 대학 생명과학과 김세윤, 양한슬 교수 공동연구팀이 `장 상피조직의 발생과 염증성 장염 회복과정의 핵심 효소발굴'에 성공했다고 6일 밝혔다.
생명과학과 박승은 박사, 이동은 박사과정 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `세포 및 분자 소화기학 및 간장학 (Cellular and Molecular Gastroenterology & Hepatology)'에 지난 8월 19일 字 온라인 게재됐다.
※ 논문명 : Gut Epithelial Inositol Polyphosphate Multikinase Alleviates Experimental Colitis via Governing Tuft Cell Homeostasis
※ 저자 정보 : 박승은 (한국과학기술원, 공동 제1 저자), 이동은 (한국과학기술원, 공동 제1 저자), 정재웅 (연세대학교 의과대학, 제2 저자), 이수형 (반더빌트 의과대학, 공동 저자), 박승주 (한국과학기술원, 공동 저자), 류재승 (한국과학기술원, 공동 저자), 오세규 (카이노젠, 공동 저자), 양한슬 (한국과학기술원, 공동 교신저자), 황성순 (연세대학교 의과대학, 공동 교신저자), 김세윤 (한국과학기술원, 공동 교신저자), 포함 총 10명
염증성 장 질환은 1980년대 중반까지만 해도 국내 발병률은 매우 낮은 질환이었으나 건강보험심사평가원 자료에 따르면 2011년 말 만성 염증성 장 질환인 크론병 환자가 1만3천여 명, 궤양성 대장염 환자가 2만9천여 명으로 집계됐으며 이후로도 환자 수가 빠르게 증가하고 있다.
궤양성 대장염과 크론병과 같은 염증성 장 질환(Inflammatory bowel disease)은 복통, 설사뿐 아니라 전신 무력감, 체중 감소, 장 천공 등의 합병증을 유발해 환자의 삶의 질을 크게 낮추는 심각한 질환이다.
이러한 염증성 장 질환은 아직 발병 메커니즘이 명확하게 규명되지 않았으며 서구화된 식습관과 함께 유전적 이상이나 면역학적 장애 또는 스트레스와 같은 환경적인 요인이 복합적으로 관여하는 것으로 여겨진다.
최근 염증성 장 질환의 환자군 일부에서 이노시톨 대사(체내 합성 또는 음식을 통하여 공급되는 이노시톨 영양소를 이노시톨 인산 물질들로 전환하는 세포 내 생화학적 반응)의 핵심 효소인 이노시톨 폴리인산 카이네이즈(Inositol polyphosphate multikinase, 이하 IPMK) 유전자에서 단일염기변이(single nucleotide polymorphism, SNP) 등이 보고됐다. IPMK 효소는 포유류의 이노시톨 대사에서 매우 중추적인 역할을 하는 단백질로서 세포의 성장과 대사뿐 아니라 면역 반응 및 중추 신경계 기억 조절 등의 다각적인 생물학적 기능을 수행하는 것으로 알려졌으나 소화기계에서의 생물학적 기능은 밝혀진 바가 전혀 없다.
이에 우리 대학 생명과학과 및 줄기세포 연구센터 김세윤 교수, 양한슬 교수 연구팀은 연세대학교 의과대학 황성순 교수 연구팀과의 공동연구를 통해 장 상피세포에서의 IPMK 효소의 역할규명연구를 다각적으로 수행했다.
연구팀은 먼저 장 상피세포에서 IPMK 유전자가 결손된 생쥐 연구모델을 제작했고 이를 분석한 결과에 따르면 정상적인 환경에서는 뚜렷한 장 조직의 구조와 기능에 있어 문제가 발생하지 않았다. 그러나 덱스트란 황산나트륨(DSS)을 투여해 대장염을 유발할 경우, IPMK 유전자가 결손된 생쥐로부터 대장염 회복반응이 현저하게 둔화됨을 관찰했고 이로부터 IPMK 효소가 손상된 대장 조직이 회복되는데 필수적인 인자임을 규명했다.
특히 연구팀은 IPMK 효소가 제거된 장 조직에서는 솔세포(tuft cell)의 발생과 기능에 심각한 장애가 발생함을 관찰했다. 솔세포란 소장과 대장뿐 아니라 흉선, 췌장 등에 존재하는 세포로서 표면에 미세 융모구조를 보이는 독특한 세포다. 장 조직의 전체 세포 중 불과 2~3% 이하로 존재하는 솔세포는 외부로부터의 기생충 감염에 대응하는 면역기능을 수행한다. 또한 솔세포로부터 합성돼 분비되는 아세틸콜린 신경전달물질은 장내 줄기세포 및 신경세포를 자극해 장 조직의 항상성 유지와 손상 복구에 중요한 기능을 담당하는 것으로 알려져 있다. 이러한 중요성에도 불구하고 솔세포의 발생과 기능을 조절하는 분자 타깃에 대한 이해는 극히 부족한 것으로 알려져 있다.
공동연구팀은 첨단 단일세포 RNA 유전자 배열 순서 분석기술(single cell RNA sequencing)을 통해 IPMK 효소가 제거된 장 상피조직에서 아세틸콜린 분비를 담당하는 솔세포군의 발생이 특이적으로 감소함을 규명했다. 또한 이러한 분석과정에서 생쥐의 대장에 존재하는 솔세포는 크게 면역기능을 담당하는 세포군, 아세틸콜린 분비 솔세포군 외에 유전자 발현 능력이 감소한 새로운 솔세포군이 있다는 사실을 발견해 학계에 최초 보고했다.
연구팀 관계자는 "발굴한 IPMK 효소에 기반한 아세틸콜린 분비성 솔세포의 발생 및 기능조절은 향후 장 상피조직의 항상성 유지의 학문적 이해와 더불어 염증성 장 질환의 진단 및 치료기술 개발 등에 적극적으로 활용될 것ˮ이라며 연구의 의의를 설명했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 서경배과학재단, KAIST 줄기세포 연구센터 지원사업, KAIST 그랜드챌린지 30 (KC30) 사업 및 포스코청암펠로십의 지원을 받아 수행됐다.
2022.10.06 조회수 10781 유방암 환자의 면역 항암치료 원리 발견해 효과적인 치료 전략 제시
우리 대학 의과학대학원 신의철 교수 연구팀이 연세대학교 의과대학 김승일 교수, 가톨릭대 의과대학 박우찬 교수 연구팀과 공동 연구를 통해 유방암 환자의 면역 항암치료 핵심 원리를 발견했다고 14일 밝혔다.
이번 연구를 통해, 최근 유행하는 면역 항암치료에 좋은 반응을 보일 것으로 예상되는 유방암 환자들을 선별해 효과적인 암 치료 전략을 제시할 것으로 기대된다.
연세대학교 의과대학 외과학 교실 이용준 강사, 김지예 임상 조교수가 공동 제1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 `사이언스 면역학(Science Immunology)' 8월 26일 字 온라인판에 게재됐다. (논문명 : CD39+ tissue-resident memory CD8+ T cells with a clonal overlap across compartments mediate anti-tumor immunity in breast cancer)
암 환자는 암세포에 대항해 이를 제거하는 역할을 하는 세포독성 T세포의 기능이 현저히 약해져 암세포에 대한 효과적인 면역반응을 나타내지 못한다. 이러한 세포독성 T세포 약화의 주된 이유는 PD-1이라는 세포독성 T세포의 기능을 저하하는 억제 수용체가 종양 조직 내 세포독성 T세포에 과다하게 발현되기 때문으로 알려져 있다.
최근 유행하고 있는 면역항암제의 기본원리는 바로 이 PD-1 억제 수용체의 기능을 차단해 약화돼 있던 세포독성 T세포의 기능을 회복시키는 것이다. 이러한 면역항암제는 유방암 환자에게서 기존의 치료를 대체할 수 있는 표준치료로 자리 잡아 가고 있지만, 투여받은 유방암 환자 중 일부에서만 치료 효과가 나타나며 이에 대한 이유를 알지 못하고 있다. 따라서, 많은 연구자가 유방암에서 면역 항암치료의 기전을 이해하고 치료에 효과를 보이는 환자를 선별하고자 하는 연구를 활발히 수행하고 있다.
이번 연구에서 공동 연구팀은 종양 조직에 존재하는 세포독성 T세포 중에서도 CD39 단백질과 조직 상주 마커 단백질을 동시에 발현하는 조직 상주 기억 T세포(CD39+ tissue-resident memory CD8+ T cell)가 유방암 환자에서 효과적인 항암 면역반응을 매개하는 핵심 면역세포임을 새롭게 밝혔다.
종양 조직에 존재하는 세포독성 T세포 중에는 항암 면역반응에 영향을 주지 않는 방관자(bystander) 세포들이 존재한다는 사실은 이미 잘 알려져 있었다. 이렇게 항암 면역반응과는 상관없는 방관자 세포들도 종양 조직에 있기 때문에 암 환자의 항암 면역반응을 정확히 측정하고 분석하는 데 어려움이 있었다. 연구팀은 CD39 단백질과 조직 상주 마커 단백질의 발현을 측정해 항암 면역반응과 관련이 있는 세포독성 T세포들만 분리해 개별 환자의 항암 면역반응을 정확히 측정할 수 있음을 새롭게 밝혔다.
그리고 유방암 환자에서 CD39를 발현하는 조직 상주 기억 세포독성 T세포는 특징적으로 삼중음성유방암(triple-negative breast cancer) 환자에게서 증가해 있었고, CD39를 발현하는 조직 상주 기억 세포독성 T세포가 증가해 있는 유방암 환자들은 수술 이후에도 재발이 적게 나타나는 등 좋은 예후를 보였다.
이번 연구에서 연구팀은 유방암 환자에서 면역항암제 치료 효율을 높이는 전략을 제시했다. 구체적으로, CD39를 발현하는 조직 상주 기억 세포독성 T세포들이 PD-1을 차단하는 면역항암제 처리에 반응해 그 기능이 효과적으로 회복됐다. 그리고 CTLA-4라는 다른 억제 수용체까지 함께 차단하자 세포독성 T세포의 기능 회복은 더욱 크게 나타났다. 따라서 이러한 면역항암제의 병용요법을 CD39 발현 조직 상주 기억 세포독성 T세포가 증가해 있는 환자들에게 선별적으로 사용한다면 치료 효과를 극대화할 수 있을 것으로 기대할 수 있다.
이번 연구는 연세대학교 및 가톨릭대 의과대학 외과 연구팀과 KAIST 의과학대학원이 유방암 환자의 항암 면역반응 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로서 중개 연구(translational research)의 주요 성과로 평가받는다.
신의철 교수는 "이번 연구는 항암 면역반응의 메커니즘과 측정에 대해 상세히 연구함으로써 유방암에서 새로운 임상 치료 전략을 제시하게 된 중요한 연구ˮ라며 "향후 암 환자의 생존율을 보다 높일 수 있도록 항암 면역반응 연구 및 면역 항암치료의 *적응증에 관한 연구를 계속하겠다ˮ라고 말했다.
☞ 적응증(indication): 어떠한 약제나 수술 따위에 의하여 치료 효과가 기대되는 병이나 증상
2022.09.14 조회수 9782
유방암 환자의 면역 항암치료 원리 발견해 효과적인 치료 전략 제시
우리 대학 의과학대학원 신의철 교수 연구팀이 연세대학교 의과대학 김승일 교수, 가톨릭대 의과대학 박우찬 교수 연구팀과 공동 연구를 통해 유방암 환자의 면역 항암치료 핵심 원리를 발견했다고 14일 밝혔다.
이번 연구를 통해, 최근 유행하는 면역 항암치료에 좋은 반응을 보일 것으로 예상되는 유방암 환자들을 선별해 효과적인 암 치료 전략을 제시할 것으로 기대된다.
연세대학교 의과대학 외과학 교실 이용준 강사, 김지예 임상 조교수가 공동 제1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 `사이언스 면역학(Science Immunology)' 8월 26일 字 온라인판에 게재됐다. (논문명 : CD39+ tissue-resident memory CD8+ T cells with a clonal overlap across compartments mediate anti-tumor immunity in breast cancer)
암 환자는 암세포에 대항해 이를 제거하는 역할을 하는 세포독성 T세포의 기능이 현저히 약해져 암세포에 대한 효과적인 면역반응을 나타내지 못한다. 이러한 세포독성 T세포 약화의 주된 이유는 PD-1이라는 세포독성 T세포의 기능을 저하하는 억제 수용체가 종양 조직 내 세포독성 T세포에 과다하게 발현되기 때문으로 알려져 있다.
최근 유행하고 있는 면역항암제의 기본원리는 바로 이 PD-1 억제 수용체의 기능을 차단해 약화돼 있던 세포독성 T세포의 기능을 회복시키는 것이다. 이러한 면역항암제는 유방암 환자에게서 기존의 치료를 대체할 수 있는 표준치료로 자리 잡아 가고 있지만, 투여받은 유방암 환자 중 일부에서만 치료 효과가 나타나며 이에 대한 이유를 알지 못하고 있다. 따라서, 많은 연구자가 유방암에서 면역 항암치료의 기전을 이해하고 치료에 효과를 보이는 환자를 선별하고자 하는 연구를 활발히 수행하고 있다.
이번 연구에서 공동 연구팀은 종양 조직에 존재하는 세포독성 T세포 중에서도 CD39 단백질과 조직 상주 마커 단백질을 동시에 발현하는 조직 상주 기억 T세포(CD39+ tissue-resident memory CD8+ T cell)가 유방암 환자에서 효과적인 항암 면역반응을 매개하는 핵심 면역세포임을 새롭게 밝혔다.
종양 조직에 존재하는 세포독성 T세포 중에는 항암 면역반응에 영향을 주지 않는 방관자(bystander) 세포들이 존재한다는 사실은 이미 잘 알려져 있었다. 이렇게 항암 면역반응과는 상관없는 방관자 세포들도 종양 조직에 있기 때문에 암 환자의 항암 면역반응을 정확히 측정하고 분석하는 데 어려움이 있었다. 연구팀은 CD39 단백질과 조직 상주 마커 단백질의 발현을 측정해 항암 면역반응과 관련이 있는 세포독성 T세포들만 분리해 개별 환자의 항암 면역반응을 정확히 측정할 수 있음을 새롭게 밝혔다.
그리고 유방암 환자에서 CD39를 발현하는 조직 상주 기억 세포독성 T세포는 특징적으로 삼중음성유방암(triple-negative breast cancer) 환자에게서 증가해 있었고, CD39를 발현하는 조직 상주 기억 세포독성 T세포가 증가해 있는 유방암 환자들은 수술 이후에도 재발이 적게 나타나는 등 좋은 예후를 보였다.
이번 연구에서 연구팀은 유방암 환자에서 면역항암제 치료 효율을 높이는 전략을 제시했다. 구체적으로, CD39를 발현하는 조직 상주 기억 세포독성 T세포들이 PD-1을 차단하는 면역항암제 처리에 반응해 그 기능이 효과적으로 회복됐다. 그리고 CTLA-4라는 다른 억제 수용체까지 함께 차단하자 세포독성 T세포의 기능 회복은 더욱 크게 나타났다. 따라서 이러한 면역항암제의 병용요법을 CD39 발현 조직 상주 기억 세포독성 T세포가 증가해 있는 환자들에게 선별적으로 사용한다면 치료 효과를 극대화할 수 있을 것으로 기대할 수 있다.
이번 연구는 연세대학교 및 가톨릭대 의과대학 외과 연구팀과 KAIST 의과학대학원이 유방암 환자의 항암 면역반응 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로서 중개 연구(translational research)의 주요 성과로 평가받는다.
신의철 교수는 "이번 연구는 항암 면역반응의 메커니즘과 측정에 대해 상세히 연구함으로써 유방암에서 새로운 임상 치료 전략을 제시하게 된 중요한 연구ˮ라며 "향후 암 환자의 생존율을 보다 높일 수 있도록 항암 면역반응 연구 및 면역 항암치료의 *적응증에 관한 연구를 계속하겠다ˮ라고 말했다.
☞ 적응증(indication): 어떠한 약제나 수술 따위에 의하여 치료 효과가 기대되는 병이나 증상
2022.09.14 조회수 9782 RNA 활용해 퇴행성 관절염 획기적 조기진단 가능성 열어
우리 대학 생명화학공학과 김유식 교수와 분당서울대병원 류마티스내과 이윤종 교수 공동 연구팀이 골관절염(Osteoarthritis)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
골관절염은 뼈의 관절면을 감싸고 있는 관절 연골이 마모돼 연골 밑의 뼈가 노출되고, 관절 주변 활액막에 염증이 생겨서 통증과 변형이 발생하는 질환이다. 흔히 퇴행성 관절염이라고도 불리며, 관절 질환 중에서 가장 많이 발생하는 질환이다.
연구팀은 골관절염의 발병 과정 중 손상된 연골에서 염증을 일으켜 세포사멸을 촉진하는 물질이 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)라는 것을 밝혔다.
이번 연구는 골관절염에서 발견되는 다양한 증상들의 원인을 mt-dsRNA라는 개념을 통해 하나로 통합함으로써 골관절염 진단 및 치료에 획기적인 방안을 제시할 것으로 기대된다.
생명화학공학과 박사과정에 재학 중인 김수진 학생과 이건용 학생이 공동 제1 저자로 참여한 이번 연구는 국제학술지 `셀 리포트(Cell Reports)' 지난 8월 9일 字에 게재됐다. (논문명 : Mitochondrial double-stranded RNAs govern the stress response in chondrocytes to promote osteoarthritis development)
골관절염은 우리나라 70세 이상의 여성 인구에서 약 50%의 유병률을 보이는 매우 흔한 질환이다. 골관절염은 일반적으로 노화와 함께 진행되기 때문에 초기에 이들을 구분하는 데 한계가 있다. 골관절염의 진행을 늦추기 위해 증상의 심각성에 따라 약물을 활용한 보존적 치료 혹은 수술을 비롯한 다양한 시도를 활발히 하고 있지만, 기존 접근방법으로 골관절염이 완치될 것이라는 기대를 하기는 어려운 상황이다. 연구팀은 질병의 발병 및 진행 메커니즘을 분석함으로써 골관절염의 조기진단과 완치에 한 걸음 다가갈 수 있는 완전히 새로운 표적 물질을 찾고자 했다.
이중나선 RNA(dsRNA)는 비정상적인 면역반응을 유발해 세포사멸 및 염증반응을 촉진한다고 알려져 있다. dsRNA의 과발현은 다양한 퇴행성 질환과 밀접한 관련이 있어 dsRNA의 조절은 건강한 세포를 유지하기 위해 필수적이다. 세포에서 dsRNA를 생성하는 대표적인 기관은 세포에 에너지를 제공한다고 알려진 미토콘드리아다. 미토콘드리아는 자체 생산하는 dsRNA를 세포질로부터 분리해 dsRNA의 노출과 이에 따른 면역반응을 막는다. 하지만 자극 혹은 세포 스트레스에 의해 mt-dsRNA가 세포질에 노출되면 RNA가 면역반응 단백질에 의해 인지돼 비정상적인 면역반응을 일으킬 수 있다.
연구팀은 골관절염에서 미토콘드리아의 손상과 원인을 알 수 없는 면역반응 단백질의 활성화가 관찰된다는 점에 착안해 mt-dsRNA가 골관절염 발병에서 중요한 기능을 할 것이라는 가설을 세웠다.
연구팀은 연골세포에서 구축한 골관절염 모사 환경에서 mt-dsRNA가 미토콘드리아 외부로 노출돼 선천성 면역반응 단백질에 의해 인지됨에 따라 면역반응을 일으킨다는 것을 확인했다. 또한 골관절염 환자들의 무릎 활막액 및 연골 조직과 골관절염 생쥐 모델의 연골에서도 mt-dsRNA가 유의미하게 증가해 있는 것을 확인했다.
특히, 다른 관절 질환인 류마티스 관절염과 통풍 환자들의 활막액과 비교했을 때 골관절염 환자들의 활막액에서 더 많은 양의 mt-dsRNA가 검출됐다. 또한 초기 골관절염을 앓고 있는 환자들의 연골에서 mt-dsRNA가 많이 증가했다. 따라서 연구팀은 골관절염을 특이적으로 조기진단 할 수 있는 바이오마커로서 mt-dsRNA의 가능성을 제시했다.
더 나아가 연구팀은 골관절염의 전도유망한 치료법 중 하나인 자가포식(Autophagy)의 치료 메커니즘에서 mt-dsRNA의 역할을 규명했다. 연구팀은 자가포식이 세포질에서 mt-dsRNA를 제거함으로써 골관절염의 증상을 완화할 수 있다는 사실을 밝힘으로써 골관절염 치료를 위한 신개념의 표적 물질로서 mt-dsRNA을 제시했다.
생명화학공학과 김유식 교수는 "이번 연구는 세포 수준의 골관절염 모사 환경에서 mt-dsRNA의 기능 규명을 넘어서 실제 골관절염 생쥐 모델의 연골 및 환자의 인체유래물에서 mt-dsRNA의 특이적인 발현 증가를 검증했다ˮ면서 "골관절염처럼 미토콘드리아 손상이 관찰되는 알츠하이머를 비롯한 퇴행성 질환의 발병 메커니즘 분석에 mt-dsRNA를 활용한다면 효과적인 치료전략을 마련하는데 유용할 것ˮ이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 박사과정생 연구장려금 지원사업의 지원을 받아 수행했다.
2022.08.31 조회수 8772
RNA 활용해 퇴행성 관절염 획기적 조기진단 가능성 열어
우리 대학 생명화학공학과 김유식 교수와 분당서울대병원 류마티스내과 이윤종 교수 공동 연구팀이 골관절염(Osteoarthritis)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
골관절염은 뼈의 관절면을 감싸고 있는 관절 연골이 마모돼 연골 밑의 뼈가 노출되고, 관절 주변 활액막에 염증이 생겨서 통증과 변형이 발생하는 질환이다. 흔히 퇴행성 관절염이라고도 불리며, 관절 질환 중에서 가장 많이 발생하는 질환이다.
연구팀은 골관절염의 발병 과정 중 손상된 연골에서 염증을 일으켜 세포사멸을 촉진하는 물질이 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)라는 것을 밝혔다.
이번 연구는 골관절염에서 발견되는 다양한 증상들의 원인을 mt-dsRNA라는 개념을 통해 하나로 통합함으로써 골관절염 진단 및 치료에 획기적인 방안을 제시할 것으로 기대된다.
생명화학공학과 박사과정에 재학 중인 김수진 학생과 이건용 학생이 공동 제1 저자로 참여한 이번 연구는 국제학술지 `셀 리포트(Cell Reports)' 지난 8월 9일 字에 게재됐다. (논문명 : Mitochondrial double-stranded RNAs govern the stress response in chondrocytes to promote osteoarthritis development)
골관절염은 우리나라 70세 이상의 여성 인구에서 약 50%의 유병률을 보이는 매우 흔한 질환이다. 골관절염은 일반적으로 노화와 함께 진행되기 때문에 초기에 이들을 구분하는 데 한계가 있다. 골관절염의 진행을 늦추기 위해 증상의 심각성에 따라 약물을 활용한 보존적 치료 혹은 수술을 비롯한 다양한 시도를 활발히 하고 있지만, 기존 접근방법으로 골관절염이 완치될 것이라는 기대를 하기는 어려운 상황이다. 연구팀은 질병의 발병 및 진행 메커니즘을 분석함으로써 골관절염의 조기진단과 완치에 한 걸음 다가갈 수 있는 완전히 새로운 표적 물질을 찾고자 했다.
이중나선 RNA(dsRNA)는 비정상적인 면역반응을 유발해 세포사멸 및 염증반응을 촉진한다고 알려져 있다. dsRNA의 과발현은 다양한 퇴행성 질환과 밀접한 관련이 있어 dsRNA의 조절은 건강한 세포를 유지하기 위해 필수적이다. 세포에서 dsRNA를 생성하는 대표적인 기관은 세포에 에너지를 제공한다고 알려진 미토콘드리아다. 미토콘드리아는 자체 생산하는 dsRNA를 세포질로부터 분리해 dsRNA의 노출과 이에 따른 면역반응을 막는다. 하지만 자극 혹은 세포 스트레스에 의해 mt-dsRNA가 세포질에 노출되면 RNA가 면역반응 단백질에 의해 인지돼 비정상적인 면역반응을 일으킬 수 있다.
연구팀은 골관절염에서 미토콘드리아의 손상과 원인을 알 수 없는 면역반응 단백질의 활성화가 관찰된다는 점에 착안해 mt-dsRNA가 골관절염 발병에서 중요한 기능을 할 것이라는 가설을 세웠다.
연구팀은 연골세포에서 구축한 골관절염 모사 환경에서 mt-dsRNA가 미토콘드리아 외부로 노출돼 선천성 면역반응 단백질에 의해 인지됨에 따라 면역반응을 일으킨다는 것을 확인했다. 또한 골관절염 환자들의 무릎 활막액 및 연골 조직과 골관절염 생쥐 모델의 연골에서도 mt-dsRNA가 유의미하게 증가해 있는 것을 확인했다.
특히, 다른 관절 질환인 류마티스 관절염과 통풍 환자들의 활막액과 비교했을 때 골관절염 환자들의 활막액에서 더 많은 양의 mt-dsRNA가 검출됐다. 또한 초기 골관절염을 앓고 있는 환자들의 연골에서 mt-dsRNA가 많이 증가했다. 따라서 연구팀은 골관절염을 특이적으로 조기진단 할 수 있는 바이오마커로서 mt-dsRNA의 가능성을 제시했다.
더 나아가 연구팀은 골관절염의 전도유망한 치료법 중 하나인 자가포식(Autophagy)의 치료 메커니즘에서 mt-dsRNA의 역할을 규명했다. 연구팀은 자가포식이 세포질에서 mt-dsRNA를 제거함으로써 골관절염의 증상을 완화할 수 있다는 사실을 밝힘으로써 골관절염 치료를 위한 신개념의 표적 물질로서 mt-dsRNA을 제시했다.
생명화학공학과 김유식 교수는 "이번 연구는 세포 수준의 골관절염 모사 환경에서 mt-dsRNA의 기능 규명을 넘어서 실제 골관절염 생쥐 모델의 연골 및 환자의 인체유래물에서 mt-dsRNA의 특이적인 발현 증가를 검증했다ˮ면서 "골관절염처럼 미토콘드리아 손상이 관찰되는 알츠하이머를 비롯한 퇴행성 질환의 발병 메커니즘 분석에 mt-dsRNA를 활용한다면 효과적인 치료전략을 마련하는데 유용할 것ˮ이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 박사과정생 연구장려금 지원사업의 지원을 받아 수행했다.
2022.08.31 조회수 8772 인공지능 기반 약물 가상 스크리닝 기술로 신규 항암 치료제 발굴 성공
우리 대학 생명과학과 김세윤 교수 연구팀이 `약물 가상 스크리닝 기술을 이용한 신규 항암 치료제 개발'에 성공했다고 12일 밝혔다.
이번 연구 결과는 국제 학술지인 `세포 사멸과 질병(Cell Death & Disease)'에 지난 7월 12일 字 온라인 게재됐다.
※ 논문명 : Lomitapide, a cholesterol-lowering drug, is an anticancer agent that induces autophagic cell death via inhibiting mTOR
※ 저자 정보 : 이보아 (한국과학기술원, 공동 제1 저자), 박승주 (한국과학기술원, 공동 제1 저자), 이슬기 (한국과학기술원, 제2 저자), 오병철 (가천대학교 의과대학, 공동 저자), 정원석 (한국과학기술원, 공동 저자), 손종우 (한국과학기술원, 공동 저자), 김세윤 (한국과학기술원, 교신저자), 포함 총 10명
`엠토르(mTOR)'라고 알려진 신호전달 단백질은 많은 암세포에서 활성이 비정상적으로 높아져 있으며 또한 암뿐만 아니라 당뇨, 염증 및 노화와 같은 다양한 질병에서 핵심적인 역할을 한다. 특히 암을 유발하는 다양한 신호전달 경로가 엠토르 단백질을 통해 매개되기 때문에 많은 제약사에서 항암 치료제 개발의 목적으로 엠토르 저해제 개발에 많은 투자를 하고 있다.
자가포식(autophagy, 오토파지)으로 알려진 생명 현상은 세포 내 엠토르 단백질에 의해 활성 조절이 정교하게 매개되는 것으로 잘 알려져 있다. 자가포식이란 `세포가 자기 살을 먹는다'는 의미로, 영양분이 과도하게 부족하거나 세포 내외적 스트레스 조건에 처한 경우, 세포가 스스로 내부 구성물질들을 파괴해 활용함으로써 세포 내 항상성을 유지하는 일종의 방어기전이다.
이러한 자가포식 활성의 조절은 양날의 칼과 같이 작용하는 것으로 알려져 있으며, 이는 암, 당뇨와 같은 질환의 발생 및 치료에 이용 가능하다고 주목받고 있다. 암세포에 과도하게 활성화돼있는 엠토르 단백질의 활성을 저해하면 자가포식을 과도하게 증가시킬 수 있으며 이를 통해 암세포의 세포 사멸이 유도될 수 있다는 사실이 알려져 있으며 이를 바탕으로 자가포식 강화에 기반한 항암제 약물의 개발전략이 제시되고 있다.
이에 김세윤 교수 연구팀은 단백질의 3차원적 구조를 활용해 화합물과 표적 단백질 사이의 물리적 상호작용을 모델링하는 유효 결합 판별 기술에 기반한 약물 재창출 전략으로 엠토르 억제성 항암제 개발 연구를 수행했다.
약물 재창출은 이미 안전성이 검증된 FDA 승인 약물 또는 임상 진행 중인 약물군을 대상으로 새로운 적응증을 찾는 신약 개발 방식이다. 이 전략은 전통적으로 10년 이상 소요되는 신약 개발의 막대한 시간과 투자를 혁신적으로 단축할 수 있는 미래 시대 신약 개발전략이다.
연구팀은 FDA 승인 약물 또는 임상 시험 중인 약물에 기반한 데이터베이스를 통해 3,391종의 약물 라이브러리를 활용했다. 라이브러리의 모든 약물을 실험적으로 검증하기에는 연구비용과 시간이 많이 소요되므로, 3차 구조 모델링을 통한 유효 결합 판별 기술을 적용해 엠토르 활성 저해능력을 보이는 약물만 신속하게 스크리닝했다.
연구팀은 엠토르 단백질의 활성을 담당하는 효소 활성부위의 3차 구조 분석과 인공지능 기반 유효 결합 판별 기술을 도입해 후보 물질 발굴의 정확도와 예측도를 높이는 데 성공했다. 그리고 3차 구조를 타깃으로 약물 결합 분석 모듈을 도입해 가상 스크리닝의 정확도와 예측도를 높이는 데 성공했다. 이번 연구를 통해 개발된 기술의 가장 큰 특징은 타깃 단백질과 약물 간의 3차 구조 정보를 이용해 많은 양의 후보 성분들을 빠르고 정확하게 분석하고 결합 여부를 예측할 수 있는 것이다.
우리 대학 생명과학과 이보아 박사, 박승주 박사는 현재 가족성 고콜레스테롤혈증(familial hypercholesterolemia) 치료제로서 임상에서 판매, 활용되고 있는 로미타피드(lomitapide) 약물의 엠토르 활성 억제 가능성을 예측했다. 연구팀은 생화학적 및 세포 생물학적 분석을 통해 로미타피드에 의한 엠토르 효소활성의 억제효능을 검증하는 데 성공했다. 대장암, 피부암 등의 암세포에 로미타피드를 처리할 경우, 암세포의 엠토르 활성이 효과적으로 억제되고 이후 과도한 자가포식이 유도됨으로써 암세포 사멸효과가 발생함을 다각적으로 확인해 로미타피드의 항암 효능을 확립했다.
또한 대장암 환자로부터 유래한 암 오가노이드(organoid)에 로미타피드를 처리할 경우, 기존의 화학 항암 치료제 대비 우수한 암세포 사멸 능력을 보였다. 나아가 최근 차세대 고형암 치료용 항암 전략으로 주목받고 있는 면역관문억제제(immune checkpoint inhibitor)와 로미티피드를 병행할 경우, 면역관문억제제의 단독 처리 대비 비약적으로 개선된 시너지 항암효과를 나타냄을 동물모델 연구를 통해 검증하는 데 성공했다.
연구팀이 발굴한 로미타피드의 항암 효능 성과는 향후 엠토르 억제 및 자가포식 기반 항암제 개발 및 임상적 활용에 적극 활용될 것으로 기대된다.
이러한 연구성과는 벤처창업으로 연계돼 이보아 박사, 박승주 박사, 이슬기 박사는 인공지능 기반 신약개발 전문기업 `에아스텍'을 공동창업했으며 중소벤처기업부 팁스(TIPS) 창업지원 프로그램에 선정되는 등 활발한 연구개발을 수행하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 창의도전연구사업 및 KAIX 포스트닥펠로사업의 지원을 받아 수행됐다.
2022.08.12 조회수 11712
인공지능 기반 약물 가상 스크리닝 기술로 신규 항암 치료제 발굴 성공
우리 대학 생명과학과 김세윤 교수 연구팀이 `약물 가상 스크리닝 기술을 이용한 신규 항암 치료제 개발'에 성공했다고 12일 밝혔다.
이번 연구 결과는 국제 학술지인 `세포 사멸과 질병(Cell Death & Disease)'에 지난 7월 12일 字 온라인 게재됐다.
※ 논문명 : Lomitapide, a cholesterol-lowering drug, is an anticancer agent that induces autophagic cell death via inhibiting mTOR
※ 저자 정보 : 이보아 (한국과학기술원, 공동 제1 저자), 박승주 (한국과학기술원, 공동 제1 저자), 이슬기 (한국과학기술원, 제2 저자), 오병철 (가천대학교 의과대학, 공동 저자), 정원석 (한국과학기술원, 공동 저자), 손종우 (한국과학기술원, 공동 저자), 김세윤 (한국과학기술원, 교신저자), 포함 총 10명
`엠토르(mTOR)'라고 알려진 신호전달 단백질은 많은 암세포에서 활성이 비정상적으로 높아져 있으며 또한 암뿐만 아니라 당뇨, 염증 및 노화와 같은 다양한 질병에서 핵심적인 역할을 한다. 특히 암을 유발하는 다양한 신호전달 경로가 엠토르 단백질을 통해 매개되기 때문에 많은 제약사에서 항암 치료제 개발의 목적으로 엠토르 저해제 개발에 많은 투자를 하고 있다.
자가포식(autophagy, 오토파지)으로 알려진 생명 현상은 세포 내 엠토르 단백질에 의해 활성 조절이 정교하게 매개되는 것으로 잘 알려져 있다. 자가포식이란 `세포가 자기 살을 먹는다'는 의미로, 영양분이 과도하게 부족하거나 세포 내외적 스트레스 조건에 처한 경우, 세포가 스스로 내부 구성물질들을 파괴해 활용함으로써 세포 내 항상성을 유지하는 일종의 방어기전이다.
이러한 자가포식 활성의 조절은 양날의 칼과 같이 작용하는 것으로 알려져 있으며, 이는 암, 당뇨와 같은 질환의 발생 및 치료에 이용 가능하다고 주목받고 있다. 암세포에 과도하게 활성화돼있는 엠토르 단백질의 활성을 저해하면 자가포식을 과도하게 증가시킬 수 있으며 이를 통해 암세포의 세포 사멸이 유도될 수 있다는 사실이 알려져 있으며 이를 바탕으로 자가포식 강화에 기반한 항암제 약물의 개발전략이 제시되고 있다.
이에 김세윤 교수 연구팀은 단백질의 3차원적 구조를 활용해 화합물과 표적 단백질 사이의 물리적 상호작용을 모델링하는 유효 결합 판별 기술에 기반한 약물 재창출 전략으로 엠토르 억제성 항암제 개발 연구를 수행했다.
약물 재창출은 이미 안전성이 검증된 FDA 승인 약물 또는 임상 진행 중인 약물군을 대상으로 새로운 적응증을 찾는 신약 개발 방식이다. 이 전략은 전통적으로 10년 이상 소요되는 신약 개발의 막대한 시간과 투자를 혁신적으로 단축할 수 있는 미래 시대 신약 개발전략이다.
연구팀은 FDA 승인 약물 또는 임상 시험 중인 약물에 기반한 데이터베이스를 통해 3,391종의 약물 라이브러리를 활용했다. 라이브러리의 모든 약물을 실험적으로 검증하기에는 연구비용과 시간이 많이 소요되므로, 3차 구조 모델링을 통한 유효 결합 판별 기술을 적용해 엠토르 활성 저해능력을 보이는 약물만 신속하게 스크리닝했다.
연구팀은 엠토르 단백질의 활성을 담당하는 효소 활성부위의 3차 구조 분석과 인공지능 기반 유효 결합 판별 기술을 도입해 후보 물질 발굴의 정확도와 예측도를 높이는 데 성공했다. 그리고 3차 구조를 타깃으로 약물 결합 분석 모듈을 도입해 가상 스크리닝의 정확도와 예측도를 높이는 데 성공했다. 이번 연구를 통해 개발된 기술의 가장 큰 특징은 타깃 단백질과 약물 간의 3차 구조 정보를 이용해 많은 양의 후보 성분들을 빠르고 정확하게 분석하고 결합 여부를 예측할 수 있는 것이다.
우리 대학 생명과학과 이보아 박사, 박승주 박사는 현재 가족성 고콜레스테롤혈증(familial hypercholesterolemia) 치료제로서 임상에서 판매, 활용되고 있는 로미타피드(lomitapide) 약물의 엠토르 활성 억제 가능성을 예측했다. 연구팀은 생화학적 및 세포 생물학적 분석을 통해 로미타피드에 의한 엠토르 효소활성의 억제효능을 검증하는 데 성공했다. 대장암, 피부암 등의 암세포에 로미타피드를 처리할 경우, 암세포의 엠토르 활성이 효과적으로 억제되고 이후 과도한 자가포식이 유도됨으로써 암세포 사멸효과가 발생함을 다각적으로 확인해 로미타피드의 항암 효능을 확립했다.
또한 대장암 환자로부터 유래한 암 오가노이드(organoid)에 로미타피드를 처리할 경우, 기존의 화학 항암 치료제 대비 우수한 암세포 사멸 능력을 보였다. 나아가 최근 차세대 고형암 치료용 항암 전략으로 주목받고 있는 면역관문억제제(immune checkpoint inhibitor)와 로미티피드를 병행할 경우, 면역관문억제제의 단독 처리 대비 비약적으로 개선된 시너지 항암효과를 나타냄을 동물모델 연구를 통해 검증하는 데 성공했다.
연구팀이 발굴한 로미타피드의 항암 효능 성과는 향후 엠토르 억제 및 자가포식 기반 항암제 개발 및 임상적 활용에 적극 활용될 것으로 기대된다.
이러한 연구성과는 벤처창업으로 연계돼 이보아 박사, 박승주 박사, 이슬기 박사는 인공지능 기반 신약개발 전문기업 `에아스텍'을 공동창업했으며 중소벤처기업부 팁스(TIPS) 창업지원 프로그램에 선정되는 등 활발한 연구개발을 수행하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 선도연구센터, 창의도전연구사업 및 KAIX 포스트닥펠로사업의 지원을 받아 수행됐다.
2022.08.12 조회수 11712 인공지능의 오랜 난제를 뇌 기반 인공지능으로 풀다
우리 대학 바이오및뇌공학과 이상완 교수(신경과학 인공지능 융합연구센터장) 연구팀이 뇌 기반 인공지능 기술을 이용해 인공지능의 난제 중 하나인 과적합-과소적합 상충 문제를 해결하는 원리를 풀어내는 데 성공했다고 5일 밝혔다.
이상완 교수와 김동재 박사(現 뉴욕대학교 박사후 연구원)가 주도하고 우리 대학 정재승 교수가 참여한 이번 연구는 `강화학습 중 편향-분산 상충 문제에 대한 전두엽의 해법'이라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 지난해 12월 28일 字 온라인판에 게재됐다. (논문명: Prefrontal solution to the bias-variance tradeoff during reinforcement learning)
최근 인공지능 모델들은 다양한 실제 문제들에 대해 최적의 해법을 제시하지만, 상황 변화에 유동적으로 대응하는 부분에 있어서는 여전히 어려움을 겪고 있다. 기계학습에서는 이를 과소적합-과적합의 위험성 (underfitting-overfitting risk) 또는 편향-분산 상충 문제(bias-variance tradeoff)라 하며 오랫동안 연구됐지만, 실제 세계와 같이 상충 조건이 계속 변하는 상황에서의 명확한 해법은 아직 제안된 바가 없다.
반면 인간은 현재 주어진 문제에 집중하면서도(과소적합 문제 해결), 당면 문제에 과하게 집착하지 않고(과적합 문제 해결) 변하는 상황에 맞게 유동적으로 대처한다. 연구팀은 뇌 데이터, 확률과정 추론 모형, 강화학습 알고리즘을 이용해 인간의 뇌가 이 문제를 어떻게 해결하는지에 대한 이론적 틀을 마련하고 이로부터 유동적인 메타 강화학습 모델을 도출해냈다.
놀랍게도 인간의 뇌는 중뇌 도파민 회로와 전두엽에서 처리되는 `예측 오차'의 하한선(prediction error lower bound)이라는 단 한 가지 정보를 이용해 이 문제를 해결한다. 우리의 전두엽, 특히 복외측전전두피질은 현재 내가 사용하고 있는 문제 해결 방식으로 주어진 문제를 얼마나 잘 풀 수 있을지에 대한 기대치의 한계를 추정하고(예: `이렇게 풀면 90점까지는 받을 수 있어'), 변화하는 상황에 맞춰 최적인 문제 해결전략을 유동적으로 선택하는 과정 (예: `이렇게 풀면 기껏해야 70점이니 다르게 풀어보자')을 통해 과소적합-과적합의 위험을 최소화하게 된다.
이상완 교수 연구팀은 2014년 해당 전두엽 영역이 환경의 불확실성을 바탕으로 강화학습전략을 유동적으로 조절하는 데 관여한다는 사실을 처음 발견했고(`뉴런(Neuron)' 학술지에 발표), 2015년에는 인과관계 추론 과정에도 관여한다는 사실을 발견했다(`PLOS Biology' 학술지에 발표). 이어 2019년에는 해당 뇌 영역이 문제의 복잡도까지 고려할 수 있다는 사실을 발견했다(`네이처 커뮤니케이션즈(Nature Communications)' 학술지에 발표).
이러한 일련의 연구 결과들은 자신의 학습 및 추론 능력을 스스로 평가하는 인간의 메타 인지 능력을 보여주는 증거로, 이 능력을 바탕으로 인공지능이 풀기 어려워하는 현실 세계의 다양한 상충적 상황들을 풀어낼 수 있다는 `전두엽 메타 학습 이론'을 정립한 바 있다(`사이언스 로보틱스(Science Robotics)' 학술지에 발표). 이번 연구는 이 이론에 기반해 인공지능의 오랜 난제 중 하나인 과소적합-과적합 상충 문제를 실제로 풀어낸 최초의 사례로 평가된다.
연구를 통해 개발된 메타 강화학습 모델을 이용하면 간단한 게임을 통해 인간의 유동적 문제 해결 능력을 간접적으로 측정할 수 있다. 더 나아가 스마트 교육이나 중독과 관련된 인지 행동치료에 적용할 경우 상황 변화에 유동적으로 대처하는 인간의 문제 해결 능력 자체를 향상할 수 있을 것으로 기대된다. 차세대 인공지능, 스마트 교육, 인지 행동치료 등 다양한 분야에 파급력이 큰 원천 기술로 최근 국내 및 해외 특허 출원이 완료된 상태다.
연구를 주도한 제1 저자 김동재 박사는 "인간 지능의 특장점에 대한 이해가 얼마나 중요한지 보여주는 연구 중 하나ˮ라고 말했다. 연구 책임자인 이상완 교수는 "인공지능이 우리보다 잘 푸는 문제가 많지만, 반대로 인공지능으로 풀기 어려운 문제들이 우리에게는 정말 쉽게 느껴지는 경우들이 많다. 인간의 다양한 고위 수준 능력을 인공지능 이론 관점에서 형식화하는 연구를 통해 인간 지능의 비밀을 하나씩 풀어나갈 수 있을 것으로 기대된다ˮ라며 "이러한 뇌 기반 인공지능 연구는 인간의 지능을 공학적으로 탐구하는 과정으로 볼 수 있으며, 인간과 인공지능이 서로 도우며 함께 성장해 나갈 수 있는 명확한 기준점을 마련할 수 있을 것ˮ이라고 말했다. 이상완 교수는 뇌 기반 인공지능 연구의 독창성과 도전성을 인정받아 구글 교수 연구상과 IBM 학술상을 받은 바 있다.
연구팀은 과학기술정보통신부의 재원으로 정보통신기획평가원의 지원을 받아 설립한 KAIST 신경과학-인공지능 융합연구센터에서 기반 기술을 활용해 인간 지능을 모사한 차세대 인공지능 모델을 개발하고, 아울러 딥마인드, IBM 인공지능 연구소, MIT, 옥스퍼드 대학 등 국제 공동연구 협약 기관과 공동연구를 통해 기술의 파급력을 높여나갈 계획이라고 말했다.
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 및 한국연구재단의 지원을 받아 수행됐다.
2022.01.05 조회수 12160
인공지능의 오랜 난제를 뇌 기반 인공지능으로 풀다
우리 대학 바이오및뇌공학과 이상완 교수(신경과학 인공지능 융합연구센터장) 연구팀이 뇌 기반 인공지능 기술을 이용해 인공지능의 난제 중 하나인 과적합-과소적합 상충 문제를 해결하는 원리를 풀어내는 데 성공했다고 5일 밝혔다.
이상완 교수와 김동재 박사(現 뉴욕대학교 박사후 연구원)가 주도하고 우리 대학 정재승 교수가 참여한 이번 연구는 `강화학습 중 편향-분산 상충 문제에 대한 전두엽의 해법'이라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 지난해 12월 28일 字 온라인판에 게재됐다. (논문명: Prefrontal solution to the bias-variance tradeoff during reinforcement learning)
최근 인공지능 모델들은 다양한 실제 문제들에 대해 최적의 해법을 제시하지만, 상황 변화에 유동적으로 대응하는 부분에 있어서는 여전히 어려움을 겪고 있다. 기계학습에서는 이를 과소적합-과적합의 위험성 (underfitting-overfitting risk) 또는 편향-분산 상충 문제(bias-variance tradeoff)라 하며 오랫동안 연구됐지만, 실제 세계와 같이 상충 조건이 계속 변하는 상황에서의 명확한 해법은 아직 제안된 바가 없다.
반면 인간은 현재 주어진 문제에 집중하면서도(과소적합 문제 해결), 당면 문제에 과하게 집착하지 않고(과적합 문제 해결) 변하는 상황에 맞게 유동적으로 대처한다. 연구팀은 뇌 데이터, 확률과정 추론 모형, 강화학습 알고리즘을 이용해 인간의 뇌가 이 문제를 어떻게 해결하는지에 대한 이론적 틀을 마련하고 이로부터 유동적인 메타 강화학습 모델을 도출해냈다.
놀랍게도 인간의 뇌는 중뇌 도파민 회로와 전두엽에서 처리되는 `예측 오차'의 하한선(prediction error lower bound)이라는 단 한 가지 정보를 이용해 이 문제를 해결한다. 우리의 전두엽, 특히 복외측전전두피질은 현재 내가 사용하고 있는 문제 해결 방식으로 주어진 문제를 얼마나 잘 풀 수 있을지에 대한 기대치의 한계를 추정하고(예: `이렇게 풀면 90점까지는 받을 수 있어'), 변화하는 상황에 맞춰 최적인 문제 해결전략을 유동적으로 선택하는 과정 (예: `이렇게 풀면 기껏해야 70점이니 다르게 풀어보자')을 통해 과소적합-과적합의 위험을 최소화하게 된다.
이상완 교수 연구팀은 2014년 해당 전두엽 영역이 환경의 불확실성을 바탕으로 강화학습전략을 유동적으로 조절하는 데 관여한다는 사실을 처음 발견했고(`뉴런(Neuron)' 학술지에 발표), 2015년에는 인과관계 추론 과정에도 관여한다는 사실을 발견했다(`PLOS Biology' 학술지에 발표). 이어 2019년에는 해당 뇌 영역이 문제의 복잡도까지 고려할 수 있다는 사실을 발견했다(`네이처 커뮤니케이션즈(Nature Communications)' 학술지에 발표).
이러한 일련의 연구 결과들은 자신의 학습 및 추론 능력을 스스로 평가하는 인간의 메타 인지 능력을 보여주는 증거로, 이 능력을 바탕으로 인공지능이 풀기 어려워하는 현실 세계의 다양한 상충적 상황들을 풀어낼 수 있다는 `전두엽 메타 학습 이론'을 정립한 바 있다(`사이언스 로보틱스(Science Robotics)' 학술지에 발표). 이번 연구는 이 이론에 기반해 인공지능의 오랜 난제 중 하나인 과소적합-과적합 상충 문제를 실제로 풀어낸 최초의 사례로 평가된다.
연구를 통해 개발된 메타 강화학습 모델을 이용하면 간단한 게임을 통해 인간의 유동적 문제 해결 능력을 간접적으로 측정할 수 있다. 더 나아가 스마트 교육이나 중독과 관련된 인지 행동치료에 적용할 경우 상황 변화에 유동적으로 대처하는 인간의 문제 해결 능력 자체를 향상할 수 있을 것으로 기대된다. 차세대 인공지능, 스마트 교육, 인지 행동치료 등 다양한 분야에 파급력이 큰 원천 기술로 최근 국내 및 해외 특허 출원이 완료된 상태다.
연구를 주도한 제1 저자 김동재 박사는 "인간 지능의 특장점에 대한 이해가 얼마나 중요한지 보여주는 연구 중 하나ˮ라고 말했다. 연구 책임자인 이상완 교수는 "인공지능이 우리보다 잘 푸는 문제가 많지만, 반대로 인공지능으로 풀기 어려운 문제들이 우리에게는 정말 쉽게 느껴지는 경우들이 많다. 인간의 다양한 고위 수준 능력을 인공지능 이론 관점에서 형식화하는 연구를 통해 인간 지능의 비밀을 하나씩 풀어나갈 수 있을 것으로 기대된다ˮ라며 "이러한 뇌 기반 인공지능 연구는 인간의 지능을 공학적으로 탐구하는 과정으로 볼 수 있으며, 인간과 인공지능이 서로 도우며 함께 성장해 나갈 수 있는 명확한 기준점을 마련할 수 있을 것ˮ이라고 말했다. 이상완 교수는 뇌 기반 인공지능 연구의 독창성과 도전성을 인정받아 구글 교수 연구상과 IBM 학술상을 받은 바 있다.
연구팀은 과학기술정보통신부의 재원으로 정보통신기획평가원의 지원을 받아 설립한 KAIST 신경과학-인공지능 융합연구센터에서 기반 기술을 활용해 인간 지능을 모사한 차세대 인공지능 모델을 개발하고, 아울러 딥마인드, IBM 인공지능 연구소, MIT, 옥스퍼드 대학 등 국제 공동연구 협약 기관과 공동연구를 통해 기술의 파급력을 높여나갈 계획이라고 말했다.
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 및 한국연구재단의 지원을 받아 수행됐다.
2022.01.05 조회수 12160 형광 염색 없이 분자 정보를 보는 AI 현미경 개발
우리 대학 물리학과 박용근 석좌교수 연구팀이 형광 염색 없이 세포의 분자 정보를 볼 수 있는 인공지능 현미경 기술을 개발했다고 20일 밝혔다.
광학 현미경은 수백 년 전부터 현재에 이르기까지 생물학 및 의학에서 가장 중요하게 쓰이는 기술 중 하나로, 이미지 형성 원리에 따라 여러 형태로 발전해왔다. 최근 수십 년간 분자생물학이 눈부시게 발전하면서 세포 내의 특정 구조를 형광(fluorescence) 으로 표지하는 것이 가능해졌고, 이처럼 높은 생화학적 특이성(biochemical specificity) 덕분에 형광 현미경은 현재 가장 폭넓게 쓰이는 광학 현미경 기술이 됐다.
그러나 형광 현미경은 형광 표지 자체가 세포를 변형하는 것이기 때문에 세포에 부담을 주게 되고, 밝기와 세포독성, 안정성 문제 때문에 초고속 또는 장기간 측정이 힘들며, 제한된 색깔로 인해 다양한 구조를 동시에 보는 것이 어려운 근본적인 한계가 있다.
이와는 대조적으로, 각 물질과 빛의 상호작용을 결정하는 근본적인 특성인 굴절률(refractive index)을 이용해 아무런 염색을 하지 않아도 되는 현미경 기술 또한 꾸준히 발전해왔다. 굴절률로부터 파생되는 빛의 흡수, 위상차 등을 이용한 전통적인 현미경은 물론, 최근에는 굴절률 자체를 3차원 상에서 정량적으로 측정하는 다양한 홀로그래픽 현미경(holographic microscopy) 기술이 박용근 교수 연구팀에서 개발돼 상용화된 바 있다. 이러한 비표지(label-free) 현미경 기술은 형광 현미경과 비교해 여러 가지 장점을 갖고 있지만, 굴절률과 세포 내 구조들의 관계가 명확하지 않아 분자 특이성이 떨어진다는 단점이 있었다.
박용근 교수 연구팀에서는 2012년 초부터 조영주 졸업생(제1 저자, 물리학과·수리과학과 학사 11학번·KAIST 총장 장학생, 現 스탠퍼드대학교 응용물리학과 박사과정) 주도로 홀로그래픽 현미경 분야에 인공지능을 도입해 특이성 문제를 해결하려는 일련의 연구가 시작됐다.
우선 형태적으로는 비슷하나 생화학적인 구성에 차이가 있는 시료(여러 종의 박테리아, 다양한 분류의 백혈구 등)의 굴절률 영상은 사람 눈에는 비슷하게 보이는데, 흥미롭게도 인공지능은 이를 높은 정확도로 분류할 수 있음을 보였다(2013-2014년 KAIST 학부연구프로그램(URP) 이후, 2015년 Optics Express, 2017년 Science Advances, 2020년 ACS Nano 등 게재). 이러한 결과는 매우 다양한 생체 시료에서 일관되게 관찰됐고, 따라서 연구팀은 생화학적 특이성이 높은 정보가 굴절률의 공간 분포에 숨겨져 있다는 가설을 세웠다.
세포생물학 분야 최고 권위지인 `네이처 셀 바이올로지(Nature Cell Biology, IF 28.82)'에 12월 7일 발표된 이번 연구(논문명: Label-free multiplexed microtomography of endogenous subcellular dynamics using generalizable deep learning)에서, 연구팀은 홀로그래픽 현미경 영상으로부터 형광 현미경 영상을 직접 예측할 수 있음을 보임으로써 이 가설을 증명했다. 인공지능이 찾아낸 굴절률 공간 분포와 세포 내 주요 구조 간의 정량적인 관계를 이용해 굴절률의 공간 분포 해독이 가능해졌고, 놀랍게도 이러한 관계는 세포 종류와 관계없이 보존돼 있음을 확인했다.
이 과정에서 만들어진 `인공지능 현미경'은 홀로그래픽 현미경과 형광 현미경의 장점만을 갖는다. 즉, 형광 표지 없이 형광 현미경의 특이적인 영상을 얻을 수 있다. 따라서 자연 상태 그대로의 세포에서 동시에 수많은 종류의 구조를 3차원으로 볼 수 있으며, 밀리초(ms) 수준의 초고속 측정과 수십 일 수준의 장기간 측정이 가능해졌다. 더욱이 기존 데이터에 포함되지 않은 새로운 종류의 세포에도 즉시 적용이 가능하기에, 다양한 생물학 및 의학 연구에 응용이 가능할 것으로 기대된다.
이번 연구는 조영주 박사과정과 박용근 교수가 지난 10여 년간 발전시켜온 광학 및 인공지능 기술력 이외에도, 다학제적 접근과 KAIST 기술을 바탕으로 한 창업 덕분에 가능했다. 생명과학과 허원도 교수(공동 교신저자)와 박외선 박사(공동 제1 저자)가 오랜 기간 발전시켜온 분자생물학 및 형광 현미경 기술 덕분에 인공지능 학습에 필요한 데이터를 얻을 수 있었으며, 조영주 박사과정이 허원도 교수 연구팀에서 2015년 1년간 연구했던 경험 덕분에 구체적인 아이디어가 나오게 됐다.
또한 박용근 교수 연구팀 홀로그래픽 현미경 기술로 창업한 ㈜토모큐브를 통해 현미경 및 데이터 형식이 규격화돼 대규모 인공지능 학습이 용이했고, 이를 바탕으로 ㈜토모큐브 조형주 연구원(공동 제1 저자) 및 민현석 연구원(공동 교신저자) 등 인공지능 전문 인력이 합류하면서 최신 인공지능 기법들의 빠른 도입이 가능했다.
한편 이번 연구는 한국연구재단의 창의연구사업, 과학기술정보통신부의 정보통신방송 기술개발사업 (홀로그램핵심기술), 일자리진흥원의 연구장비개발 및 고도화지원사업, 한국보건산업진흥원의 보건의료기술 연구개발사업의 지원을 받아 수행됐다.
2021.12.20 조회수 11521
형광 염색 없이 분자 정보를 보는 AI 현미경 개발
우리 대학 물리학과 박용근 석좌교수 연구팀이 형광 염색 없이 세포의 분자 정보를 볼 수 있는 인공지능 현미경 기술을 개발했다고 20일 밝혔다.
광학 현미경은 수백 년 전부터 현재에 이르기까지 생물학 및 의학에서 가장 중요하게 쓰이는 기술 중 하나로, 이미지 형성 원리에 따라 여러 형태로 발전해왔다. 최근 수십 년간 분자생물학이 눈부시게 발전하면서 세포 내의 특정 구조를 형광(fluorescence) 으로 표지하는 것이 가능해졌고, 이처럼 높은 생화학적 특이성(biochemical specificity) 덕분에 형광 현미경은 현재 가장 폭넓게 쓰이는 광학 현미경 기술이 됐다.
그러나 형광 현미경은 형광 표지 자체가 세포를 변형하는 것이기 때문에 세포에 부담을 주게 되고, 밝기와 세포독성, 안정성 문제 때문에 초고속 또는 장기간 측정이 힘들며, 제한된 색깔로 인해 다양한 구조를 동시에 보는 것이 어려운 근본적인 한계가 있다.
이와는 대조적으로, 각 물질과 빛의 상호작용을 결정하는 근본적인 특성인 굴절률(refractive index)을 이용해 아무런 염색을 하지 않아도 되는 현미경 기술 또한 꾸준히 발전해왔다. 굴절률로부터 파생되는 빛의 흡수, 위상차 등을 이용한 전통적인 현미경은 물론, 최근에는 굴절률 자체를 3차원 상에서 정량적으로 측정하는 다양한 홀로그래픽 현미경(holographic microscopy) 기술이 박용근 교수 연구팀에서 개발돼 상용화된 바 있다. 이러한 비표지(label-free) 현미경 기술은 형광 현미경과 비교해 여러 가지 장점을 갖고 있지만, 굴절률과 세포 내 구조들의 관계가 명확하지 않아 분자 특이성이 떨어진다는 단점이 있었다.
박용근 교수 연구팀에서는 2012년 초부터 조영주 졸업생(제1 저자, 물리학과·수리과학과 학사 11학번·KAIST 총장 장학생, 現 스탠퍼드대학교 응용물리학과 박사과정) 주도로 홀로그래픽 현미경 분야에 인공지능을 도입해 특이성 문제를 해결하려는 일련의 연구가 시작됐다.
우선 형태적으로는 비슷하나 생화학적인 구성에 차이가 있는 시료(여러 종의 박테리아, 다양한 분류의 백혈구 등)의 굴절률 영상은 사람 눈에는 비슷하게 보이는데, 흥미롭게도 인공지능은 이를 높은 정확도로 분류할 수 있음을 보였다(2013-2014년 KAIST 학부연구프로그램(URP) 이후, 2015년 Optics Express, 2017년 Science Advances, 2020년 ACS Nano 등 게재). 이러한 결과는 매우 다양한 생체 시료에서 일관되게 관찰됐고, 따라서 연구팀은 생화학적 특이성이 높은 정보가 굴절률의 공간 분포에 숨겨져 있다는 가설을 세웠다.
세포생물학 분야 최고 권위지인 `네이처 셀 바이올로지(Nature Cell Biology, IF 28.82)'에 12월 7일 발표된 이번 연구(논문명: Label-free multiplexed microtomography of endogenous subcellular dynamics using generalizable deep learning)에서, 연구팀은 홀로그래픽 현미경 영상으로부터 형광 현미경 영상을 직접 예측할 수 있음을 보임으로써 이 가설을 증명했다. 인공지능이 찾아낸 굴절률 공간 분포와 세포 내 주요 구조 간의 정량적인 관계를 이용해 굴절률의 공간 분포 해독이 가능해졌고, 놀랍게도 이러한 관계는 세포 종류와 관계없이 보존돼 있음을 확인했다.
이 과정에서 만들어진 `인공지능 현미경'은 홀로그래픽 현미경과 형광 현미경의 장점만을 갖는다. 즉, 형광 표지 없이 형광 현미경의 특이적인 영상을 얻을 수 있다. 따라서 자연 상태 그대로의 세포에서 동시에 수많은 종류의 구조를 3차원으로 볼 수 있으며, 밀리초(ms) 수준의 초고속 측정과 수십 일 수준의 장기간 측정이 가능해졌다. 더욱이 기존 데이터에 포함되지 않은 새로운 종류의 세포에도 즉시 적용이 가능하기에, 다양한 생물학 및 의학 연구에 응용이 가능할 것으로 기대된다.
이번 연구는 조영주 박사과정과 박용근 교수가 지난 10여 년간 발전시켜온 광학 및 인공지능 기술력 이외에도, 다학제적 접근과 KAIST 기술을 바탕으로 한 창업 덕분에 가능했다. 생명과학과 허원도 교수(공동 교신저자)와 박외선 박사(공동 제1 저자)가 오랜 기간 발전시켜온 분자생물학 및 형광 현미경 기술 덕분에 인공지능 학습에 필요한 데이터를 얻을 수 있었으며, 조영주 박사과정이 허원도 교수 연구팀에서 2015년 1년간 연구했던 경험 덕분에 구체적인 아이디어가 나오게 됐다.
또한 박용근 교수 연구팀 홀로그래픽 현미경 기술로 창업한 ㈜토모큐브를 통해 현미경 및 데이터 형식이 규격화돼 대규모 인공지능 학습이 용이했고, 이를 바탕으로 ㈜토모큐브 조형주 연구원(공동 제1 저자) 및 민현석 연구원(공동 교신저자) 등 인공지능 전문 인력이 합류하면서 최신 인공지능 기법들의 빠른 도입이 가능했다.
한편 이번 연구는 한국연구재단의 창의연구사업, 과학기술정보통신부의 정보통신방송 기술개발사업 (홀로그램핵심기술), 일자리진흥원의 연구장비개발 및 고도화지원사업, 한국보건산업진흥원의 보건의료기술 연구개발사업의 지원을 받아 수행됐다.
2021.12.20 조회수 11521 코로나19 환자에서 나타나는 자연살해 세포 변화 규명
우리 대학 의과학대학원 신의철 교수 연구팀이 충남대학교병원 감염내과 김연숙, 천신혜 교수팀과의 공동연구를 통해 코로나19 환자들에서 자연살해 세포의 항바이러스 기능이 약화돼 있고, 이러한 기능 변화는 경증 코로나19 환자에서는 일주일 내로 사라지지만 중증 환자에서는 오래 지속됨을 규명했다고 10일 밝혔다. 이로써, 항바이러스 선천면역 반응의 한 축을 담당하는 자연살해 세포의 기능 이상을 중증 코로나19 환자에서 처음으로 규명하게 됐다.
우리 몸은 바이러스에 감염되면 이에 대항하여 일차적으로 선천면역 반응이 나타나며, 항바이러스 선천면역 반응을 담당하는 주된 세포가 바로 자연살해 세포다. 이러한 자연살해 세포의 대부분을 차지하는 것이 바이러스에 감염된 세포를 직접 죽이는 세포독성 자연살해 세포인데, 코로나19 환자에서 이러한 세포독성 자연살해 세포의 수나 기능이 감소돼 있다는 보고는 있었지만, 자연살해 세포의 구체적인 변화나 기능감소 기전에 대해서는 규명된 바가 없었다.
이번 연구에서 KAIST-충남대병원 공동연구팀은 한국인 코로나19 환자들을 대상으로 진단 초기부터 회복 시까지 추적 연구를 수행해 코로나19 바이러스 감염증에서 질병의 진행 과정에 따라 자연살해 세포에 일어나는 변화를 최초로 규명했고, 중증 환자와 경증 환자에서 자연살해 세포의 특성 및 기능의 차이점에 대해 밝혔다. 특히 이번 연구에서는 최첨단 면역학 연구기법과 유전자 발현 분석을 동시에 활용해 코로나19 환자에서 자연살해 세포들에 나타나는 변화를 다각도에서 분석하고 규명했다.
공동연구팀은 정상인이나 독감 환자와는 달리 코로나19 환자에게서만 특징적으로 나타나는 비정형 자연살해 세포를 발견했고, 이러한 비정형 자연살해 세포가 일반적인 자연살해 세포보다 세포독성 기능이 감소해있음을 밝혔다.
연구팀은 이러한 비정형 자연살해 세포들이 질병의 중증도와 관계없이 코로나19 바이러스에 감염된 환자들에서 공통적으로 질병 초기에 빠르게 증가하며, 이로 인해 코로나19 환자의 선천면역 반응이 약화되어 있음을 밝혔다. 그리고 코로나19 환자들의 질병 진행 과정에서 자연살해 세포 특성을 추적 관찰한 결과, 중증 코로나19 환자에서 이러한 비정형 자연살해 세포들의 증가 상태가 더 장기간 지속되며 이는 선천면역 반응의 손상과 연관됨을 밝혔다.
이번 연구는 세계 처음으로 코로나19 환자에서 비정형 자연살해 세포의 증가를 발견해 코로나19 환자에서 나타나는 선천면역 반응 손상의 기전을 보고한 연구로 세계 면역학계의 주목을 받고 있다.
과학기술원 공동연구과제의 지원을 받아 수행한 이번 연구 결과는 국제 저명 학술지인 `알레르기 및 임상면역학 저널(The Journal of Allergy and Clinical Immunolgy)'에 게재됐다. 특히 이번 논문은 저널 편집자로부터 주목을 받아야 할 주요 연구성과로 선정돼 하이라이트 논문으로 저널에 소개될 예정이다. (논문명: Abnormality in the NK cell population is prolonged in severe COVID-19 patients)
이번 연구의 제1 저자인 우리 대학 임가람 박사 연구원(現 연세의대 소화기내과 임상강사)은 "코로나19 바이러스 감염증에서 특징적으로 비정형 자연살해 세포들이 증가해 있음을 발견했다ˮ며 "다른 호흡기 바이러스 감염에서는 보이지 않는 이러한 자연살해 세포 변화는 코로나19 바이러스 감염증의 임상적 특징을 이해하고, 중증 환자에서 선제적인 치료를 조기에 시작하는 임상적 근거가 될 것이다ˮ고 설명했다.
충남대병원 김연숙 교수는 "이번 연구는 코로나19 환자의 질병 과정의 초기부터 회복기까지 자연살해 세포의 변화 및 특성을 세계에서 최초로 분석해 규명한 연구 결과로서 코로나19 환자에서 나타나는 선천면역 반응의 손상 기전을 최초로 밝혔다는 점에서 의미가 있는 연구ˮ라고 말했다.
2021.08.11 조회수 10991
코로나19 환자에서 나타나는 자연살해 세포 변화 규명
우리 대학 의과학대학원 신의철 교수 연구팀이 충남대학교병원 감염내과 김연숙, 천신혜 교수팀과의 공동연구를 통해 코로나19 환자들에서 자연살해 세포의 항바이러스 기능이 약화돼 있고, 이러한 기능 변화는 경증 코로나19 환자에서는 일주일 내로 사라지지만 중증 환자에서는 오래 지속됨을 규명했다고 10일 밝혔다. 이로써, 항바이러스 선천면역 반응의 한 축을 담당하는 자연살해 세포의 기능 이상을 중증 코로나19 환자에서 처음으로 규명하게 됐다.
우리 몸은 바이러스에 감염되면 이에 대항하여 일차적으로 선천면역 반응이 나타나며, 항바이러스 선천면역 반응을 담당하는 주된 세포가 바로 자연살해 세포다. 이러한 자연살해 세포의 대부분을 차지하는 것이 바이러스에 감염된 세포를 직접 죽이는 세포독성 자연살해 세포인데, 코로나19 환자에서 이러한 세포독성 자연살해 세포의 수나 기능이 감소돼 있다는 보고는 있었지만, 자연살해 세포의 구체적인 변화나 기능감소 기전에 대해서는 규명된 바가 없었다.
이번 연구에서 KAIST-충남대병원 공동연구팀은 한국인 코로나19 환자들을 대상으로 진단 초기부터 회복 시까지 추적 연구를 수행해 코로나19 바이러스 감염증에서 질병의 진행 과정에 따라 자연살해 세포에 일어나는 변화를 최초로 규명했고, 중증 환자와 경증 환자에서 자연살해 세포의 특성 및 기능의 차이점에 대해 밝혔다. 특히 이번 연구에서는 최첨단 면역학 연구기법과 유전자 발현 분석을 동시에 활용해 코로나19 환자에서 자연살해 세포들에 나타나는 변화를 다각도에서 분석하고 규명했다.
공동연구팀은 정상인이나 독감 환자와는 달리 코로나19 환자에게서만 특징적으로 나타나는 비정형 자연살해 세포를 발견했고, 이러한 비정형 자연살해 세포가 일반적인 자연살해 세포보다 세포독성 기능이 감소해있음을 밝혔다.
연구팀은 이러한 비정형 자연살해 세포들이 질병의 중증도와 관계없이 코로나19 바이러스에 감염된 환자들에서 공통적으로 질병 초기에 빠르게 증가하며, 이로 인해 코로나19 환자의 선천면역 반응이 약화되어 있음을 밝혔다. 그리고 코로나19 환자들의 질병 진행 과정에서 자연살해 세포 특성을 추적 관찰한 결과, 중증 코로나19 환자에서 이러한 비정형 자연살해 세포들의 증가 상태가 더 장기간 지속되며 이는 선천면역 반응의 손상과 연관됨을 밝혔다.
이번 연구는 세계 처음으로 코로나19 환자에서 비정형 자연살해 세포의 증가를 발견해 코로나19 환자에서 나타나는 선천면역 반응 손상의 기전을 보고한 연구로 세계 면역학계의 주목을 받고 있다.
과학기술원 공동연구과제의 지원을 받아 수행한 이번 연구 결과는 국제 저명 학술지인 `알레르기 및 임상면역학 저널(The Journal of Allergy and Clinical Immunolgy)'에 게재됐다. 특히 이번 논문은 저널 편집자로부터 주목을 받아야 할 주요 연구성과로 선정돼 하이라이트 논문으로 저널에 소개될 예정이다. (논문명: Abnormality in the NK cell population is prolonged in severe COVID-19 patients)
이번 연구의 제1 저자인 우리 대학 임가람 박사 연구원(現 연세의대 소화기내과 임상강사)은 "코로나19 바이러스 감염증에서 특징적으로 비정형 자연살해 세포들이 증가해 있음을 발견했다ˮ며 "다른 호흡기 바이러스 감염에서는 보이지 않는 이러한 자연살해 세포 변화는 코로나19 바이러스 감염증의 임상적 특징을 이해하고, 중증 환자에서 선제적인 치료를 조기에 시작하는 임상적 근거가 될 것이다ˮ고 설명했다.
충남대병원 김연숙 교수는 "이번 연구는 코로나19 환자의 질병 과정의 초기부터 회복기까지 자연살해 세포의 변화 및 특성을 세계에서 최초로 분석해 규명한 연구 결과로서 코로나19 환자에서 나타나는 선천면역 반응의 손상 기전을 최초로 밝혔다는 점에서 의미가 있는 연구ˮ라고 말했다.
2021.08.11 조회수 10991 효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2021.01.06 조회수 56551
효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2021.01.06 조회수 56551