%EC%83%9D%EB%AA%85%EA%B3%BC%ED%95%99%EA%B8%B0%EC%88%A0%EB%8C%80%ED%95%99
-
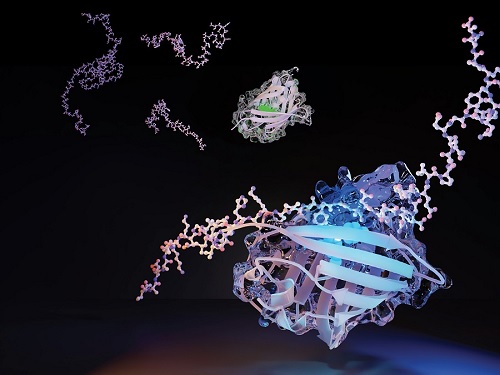 알츠하이머 조기 진단하는 센서단백질 디자인하다
고정된 3차원 구조가 없는 상태로 존재하는 비정형 단백질((Intrinsically disordered protein)은 알츠하이머, 파킨슨병과 같은 신경계 질환부터 암, 심혈관계 질환, 대사질환을 유발하는 것으로 알려져 있다. 따라서, 이들을 신속하게 검출하고 분석할 수 있다면 조기 진단을 통해 질병의 진행을 막고 환자의 예후를 개선할 수 있을 뿐 아니라, 병리기전을 밝히고 나아가 치료제를 개발하는 데 큰 도움이 될 수 있다.
우리 대학 생명과학과 김학성 교수 연구팀이 이러한 비정형 단백질을 간단하게 검출할 수 있는 센서 단백질을 디자인하는 데에 성공했다고 8일 밝혔다.
단백질은 특정한 3차원 구조를 가지며 생체 내 다양한 기능을 수행하는 데 실제 인간 단백질 중 44%는 상황에 따라 구조가 변화는 비정형 단백질로 고정된 구조를 갖는 일반 단백질보다 더욱 다양한 기능을 수행한다. 그러나, 비정형 단백질은 고정된 구조가 없어서 이들 단백질의 분석과 기능 연구가 매우 어려웠다.
연구팀은 비정형 단백질이 단백질 2차 구조인 베타 스트랜드(β-strand)를 형성하는 특정 아미노산 서열을 갖고 있다는 점에 착안하여 이러한 특정 서열과 상보적으로 결합할 경우에만 신호를 방출하는 새로운 형태의 센서 단백질 디자인 방법을 정립하였다.
연구팀은 자연계에 존재하는 녹색 형광 단백질(Green Fluorescent Protein, GFP)의 베타 스트랜드 하나를 제거한 후, 비정형 단백질의 특정 서열이 결합하면 형광 단백질 발색단(chromophore)의 파장 스펙트럼이 변화하는 센서 단백질을 컴퓨터 및 방향적 진화 방법을 이용하여 성공적으로 개발하였다. (그림 1)
연구팀은 대표적 비정형 단백질의 하나로 알츠하이머를 유발하는 세포 내 베타-아밀로이드(β-amyloid)를 검출할 수 있는 센서 단백질을 개발하여 실시간으로 세포막과의 상호작용을 추적하고 영상화할 수 있었다. 기존에는 비정형 단백질을 분석하기 위해 복잡한 여러 단계의 전처리 과정이 필요하였고 이로 인해 비정형 단백질 자체가 크게 변형되어 실제 비정형 단백질의 분석과 기능 연구에 많은 제약이 있었다. 그러나, 이번에 개발된 센서 단백질은 단순히 비정형 단백질과 섞어줌으로써 매우 간편하고 빠르게 비정형 단백질을 검출할 수 있어서 향후 비정형 단백질 분석 및 관련 질병 연구에 크게 기여할 것으로 기대된다.
생명과학과 유태근 박사가 제1 저자로 참여하고 이진수 박사 (허원도 교수 연구실)와 윤정민 박사(송지준 교수 연구실)가 공동으로 진행한 이번 연구는 국제 학술지 '잭스 골드 (JACS Au)'에 지난 10월 26일 자 3권 11호에 출판됐으며, 표지 논문으로 선정됐다. (그림 2) (논문명 : Engineering of a Fluorescent Protein for a Sensing of an Intrinsically Disordered Protein through Transition in the Chromophore State)
제1 저자인 유태근 박사는 “고정된 구조가 없는 비정형 단백질은 일반적 단백질에 비해 센서 단백질의 디자인과 개발이 매우 어려운 표적이었다”라며 “이번 연구가 비정형 단백질의 분석과 관련 병리기전의 연구에 새로운 방법과 전략을 제시할 수 있을 것이다”라고 말했다.
한편 이번 연구는 한국연구재단 기초연구사업과 중견연구자지원사업의 지원을 받아 수행됐다.
2023.12.08 조회수 6490
알츠하이머 조기 진단하는 센서단백질 디자인하다
고정된 3차원 구조가 없는 상태로 존재하는 비정형 단백질((Intrinsically disordered protein)은 알츠하이머, 파킨슨병과 같은 신경계 질환부터 암, 심혈관계 질환, 대사질환을 유발하는 것으로 알려져 있다. 따라서, 이들을 신속하게 검출하고 분석할 수 있다면 조기 진단을 통해 질병의 진행을 막고 환자의 예후를 개선할 수 있을 뿐 아니라, 병리기전을 밝히고 나아가 치료제를 개발하는 데 큰 도움이 될 수 있다.
우리 대학 생명과학과 김학성 교수 연구팀이 이러한 비정형 단백질을 간단하게 검출할 수 있는 센서 단백질을 디자인하는 데에 성공했다고 8일 밝혔다.
단백질은 특정한 3차원 구조를 가지며 생체 내 다양한 기능을 수행하는 데 실제 인간 단백질 중 44%는 상황에 따라 구조가 변화는 비정형 단백질로 고정된 구조를 갖는 일반 단백질보다 더욱 다양한 기능을 수행한다. 그러나, 비정형 단백질은 고정된 구조가 없어서 이들 단백질의 분석과 기능 연구가 매우 어려웠다.
연구팀은 비정형 단백질이 단백질 2차 구조인 베타 스트랜드(β-strand)를 형성하는 특정 아미노산 서열을 갖고 있다는 점에 착안하여 이러한 특정 서열과 상보적으로 결합할 경우에만 신호를 방출하는 새로운 형태의 센서 단백질 디자인 방법을 정립하였다.
연구팀은 자연계에 존재하는 녹색 형광 단백질(Green Fluorescent Protein, GFP)의 베타 스트랜드 하나를 제거한 후, 비정형 단백질의 특정 서열이 결합하면 형광 단백질 발색단(chromophore)의 파장 스펙트럼이 변화하는 센서 단백질을 컴퓨터 및 방향적 진화 방법을 이용하여 성공적으로 개발하였다. (그림 1)
연구팀은 대표적 비정형 단백질의 하나로 알츠하이머를 유발하는 세포 내 베타-아밀로이드(β-amyloid)를 검출할 수 있는 센서 단백질을 개발하여 실시간으로 세포막과의 상호작용을 추적하고 영상화할 수 있었다. 기존에는 비정형 단백질을 분석하기 위해 복잡한 여러 단계의 전처리 과정이 필요하였고 이로 인해 비정형 단백질 자체가 크게 변형되어 실제 비정형 단백질의 분석과 기능 연구에 많은 제약이 있었다. 그러나, 이번에 개발된 센서 단백질은 단순히 비정형 단백질과 섞어줌으로써 매우 간편하고 빠르게 비정형 단백질을 검출할 수 있어서 향후 비정형 단백질 분석 및 관련 질병 연구에 크게 기여할 것으로 기대된다.
생명과학과 유태근 박사가 제1 저자로 참여하고 이진수 박사 (허원도 교수 연구실)와 윤정민 박사(송지준 교수 연구실)가 공동으로 진행한 이번 연구는 국제 학술지 '잭스 골드 (JACS Au)'에 지난 10월 26일 자 3권 11호에 출판됐으며, 표지 논문으로 선정됐다. (그림 2) (논문명 : Engineering of a Fluorescent Protein for a Sensing of an Intrinsically Disordered Protein through Transition in the Chromophore State)
제1 저자인 유태근 박사는 “고정된 구조가 없는 비정형 단백질은 일반적 단백질에 비해 센서 단백질의 디자인과 개발이 매우 어려운 표적이었다”라며 “이번 연구가 비정형 단백질의 분석과 관련 병리기전의 연구에 새로운 방법과 전략을 제시할 수 있을 것이다”라고 말했다.
한편 이번 연구는 한국연구재단 기초연구사업과 중견연구자지원사업의 지원을 받아 수행됐다.
2023.12.08 조회수 6490 -
 DNA 인식 선천면역인자의 방호패치 발견
우리 대학 생명과학과 강석조 교수 연구팀이 선천면역반응을 매개하는 중요 단백질인 STING의 활성을 조절하는 새로운 기전으로, 미토콘드리아 막 단백질이자 E3 유비퀴틴 리가아제인 MARCH5가 STING을 유비퀴틴시켜서 활성산소에 의해 STING이 비활성형 다량체로 응집되는 것을 억제함을 규명했다고 4일 밝혔다.
STING(Stimulator of interferon genes)은 선천면역 신호경로의 필수적인 어댑터 단백질로서 외부로부터 들어온 세균 및 바이러스로부터 유래한 세포질 내 DNA를 감지하는 cGAS(cyclic GMP-AMP synthase)가 생성한 cGAMP(2'3'-cyclic GMP-AMP)에 결합하여 활성화되면 TBK1(TANK-binding kinase 1)과 IRF3(Interferon regulatory factor 3)를 활성화하여 제1형 인터페론을 유도한다. 이를 통해서 염증반응과 다양한 면역세포를 활성화하여 병원균으로부터 우리 몸을 방어하는 면역반응을 일으킨다. STING은 또한 자가 염증성 질환, 암, 노화 및 퇴행성 뇌질환을 포함한 다양한 염증질환의 주요 매개체로 작용한다.
STING의 활성은 다양한 방법으로 조절되는 데, 세포내 이동, 번역 후 변형(post-translational modification, PTM), 고차원 구조체인 다량체 (polymer)의 형성 등이 알려져 있다. STING은 세포내 소기관인 소포체(endoplasmic reticulum)에 위치하고 활성 후 골지체로 이동하여 하위 신호전달을 매개한다. 인산화(phosphorylation), 유비퀴틴화(ubiquitination), 팔미토일화(palmitoylation), 산화(oxidation) 등의 다양한 번역 후 변형을 받으며, 활성화된 STING은 이량체(dimer)를 거쳐 활성형 다량체를 형성하여 신호전달을 매개한다. 하지만, 이들 조절 기전의 다이나믹스와 상호작용에 대해서는 알려진 바가 적다. 특히, 염증과 같은 조건에서 다량 생성되는 활성산소에 의해 STING이 비활성형 다량체를 형성하는 데 이를 억제하는 번역 후 변형 및 그 조절 기전에 대해서는 전혀 알려지지 않았다.
강 교수 연구팀은 이전 연구에서 STING이 위치한 소포체와 인접한 미토콘드리아의 다이나믹스를 조절하는 인자가 STING 활성에 영향을 미친다는 것을 밝혔다. 이에 대한 후속연구를 수행하던 중, 미토콘드리아 막 단백질이자 E3 유비퀴틴 리가아제로 알려진 MARCH5(Membrane associated RING-CH-type finger 5)가 결손된 마우스 배아 섬유아세포에서 STING 매개 제1형 인터페론 형성이 감소하며 STING 활성경로의 하위단계인 TBK1, IRF3의 활성 또한 저해되어있음을 통해 MARCH5가 STING의 활성에 양성 조절자로서 역할을 한다는 사실을 밝혔다. 나아가 강 교수팀은 MARCH5가 결손된 세포주에서 활성산소(reactive oxygen species, ROS)가 정상 세포주에 비해 높다는 것과 높은 활성산소는 STING이 정상 세포주에 보이는 STING의 활성형 다량체가 아닌 비활성형 다량체로의 형성을 촉진한다는 사실을 확인하였다.
기전적으로 MARCH5 단백질이 STING과 결합하며 STING의 Lysine 19 잔기를 선택적으로 타겟하여 Lysine-63형으로 유비퀴틴화하는 것을 확인하였다. STING은 높은 활성산소 조건에서 Cysteine 205 잔기에 산화가 일어나는데, MARCH5에 의한 STING 유비퀴틴화는 과도한 활성산소 조건에서 산화된 STING이 비활성 STING 다량체를 형성하는 것을 억제하여 정상적인 STING활성을 갖도록 돕는다는 사실을 규명하였다.
강석조 교수는 “본 연구는 미토콘드리아 막 단백질이 산화된 STING의 다량체 형성을 조절하는 원리를 최초로 제공한 연구이면서 STING이라는 단백질을 통하여, 다양한 번역 후 변형간의 상호 작용과 고차원 구조적 변화, 그리고 이에 기여하는 세포내 소기관의 교류를 동시에 밝혀 보다 넓은 학문분야에 활용되는 지식을 제공했다는 데 의의가 크다”고 언급하면서, “본 연구를 통해 얻은 새로운 지식은 STING이 매개하는 다양한 염증성 질환에 대한 보다 깊은 이해와 치료제 개발 연구에 가치 있게 활용될 것으로 기대한다”고 전했다.
이번 연구는 유럽 분자생물학의 권위있는 국제 학술지 `엠보 리포트 저널 (EMBO (European Molecular Biology Organization) Reports)’에 11월 2일 字 온라인판에 게재됐다 (논문명: MARCH5 promotes STING pathway activation by suppressing polymer formation of oxidized STING). KAIST 생명과학과 손경표 박사과정, 정석환 박사과정, 엄은총 박사과정이 공동 제1 저자로 연구를 주도하였고, 권도형 박사(現 부스트이뮨)가 함께 참여하였다.
이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2023.12.04 조회수 6080
DNA 인식 선천면역인자의 방호패치 발견
우리 대학 생명과학과 강석조 교수 연구팀이 선천면역반응을 매개하는 중요 단백질인 STING의 활성을 조절하는 새로운 기전으로, 미토콘드리아 막 단백질이자 E3 유비퀴틴 리가아제인 MARCH5가 STING을 유비퀴틴시켜서 활성산소에 의해 STING이 비활성형 다량체로 응집되는 것을 억제함을 규명했다고 4일 밝혔다.
STING(Stimulator of interferon genes)은 선천면역 신호경로의 필수적인 어댑터 단백질로서 외부로부터 들어온 세균 및 바이러스로부터 유래한 세포질 내 DNA를 감지하는 cGAS(cyclic GMP-AMP synthase)가 생성한 cGAMP(2'3'-cyclic GMP-AMP)에 결합하여 활성화되면 TBK1(TANK-binding kinase 1)과 IRF3(Interferon regulatory factor 3)를 활성화하여 제1형 인터페론을 유도한다. 이를 통해서 염증반응과 다양한 면역세포를 활성화하여 병원균으로부터 우리 몸을 방어하는 면역반응을 일으킨다. STING은 또한 자가 염증성 질환, 암, 노화 및 퇴행성 뇌질환을 포함한 다양한 염증질환의 주요 매개체로 작용한다.
STING의 활성은 다양한 방법으로 조절되는 데, 세포내 이동, 번역 후 변형(post-translational modification, PTM), 고차원 구조체인 다량체 (polymer)의 형성 등이 알려져 있다. STING은 세포내 소기관인 소포체(endoplasmic reticulum)에 위치하고 활성 후 골지체로 이동하여 하위 신호전달을 매개한다. 인산화(phosphorylation), 유비퀴틴화(ubiquitination), 팔미토일화(palmitoylation), 산화(oxidation) 등의 다양한 번역 후 변형을 받으며, 활성화된 STING은 이량체(dimer)를 거쳐 활성형 다량체를 형성하여 신호전달을 매개한다. 하지만, 이들 조절 기전의 다이나믹스와 상호작용에 대해서는 알려진 바가 적다. 특히, 염증과 같은 조건에서 다량 생성되는 활성산소에 의해 STING이 비활성형 다량체를 형성하는 데 이를 억제하는 번역 후 변형 및 그 조절 기전에 대해서는 전혀 알려지지 않았다.
강 교수 연구팀은 이전 연구에서 STING이 위치한 소포체와 인접한 미토콘드리아의 다이나믹스를 조절하는 인자가 STING 활성에 영향을 미친다는 것을 밝혔다. 이에 대한 후속연구를 수행하던 중, 미토콘드리아 막 단백질이자 E3 유비퀴틴 리가아제로 알려진 MARCH5(Membrane associated RING-CH-type finger 5)가 결손된 마우스 배아 섬유아세포에서 STING 매개 제1형 인터페론 형성이 감소하며 STING 활성경로의 하위단계인 TBK1, IRF3의 활성 또한 저해되어있음을 통해 MARCH5가 STING의 활성에 양성 조절자로서 역할을 한다는 사실을 밝혔다. 나아가 강 교수팀은 MARCH5가 결손된 세포주에서 활성산소(reactive oxygen species, ROS)가 정상 세포주에 비해 높다는 것과 높은 활성산소는 STING이 정상 세포주에 보이는 STING의 활성형 다량체가 아닌 비활성형 다량체로의 형성을 촉진한다는 사실을 확인하였다.
기전적으로 MARCH5 단백질이 STING과 결합하며 STING의 Lysine 19 잔기를 선택적으로 타겟하여 Lysine-63형으로 유비퀴틴화하는 것을 확인하였다. STING은 높은 활성산소 조건에서 Cysteine 205 잔기에 산화가 일어나는데, MARCH5에 의한 STING 유비퀴틴화는 과도한 활성산소 조건에서 산화된 STING이 비활성 STING 다량체를 형성하는 것을 억제하여 정상적인 STING활성을 갖도록 돕는다는 사실을 규명하였다.
강석조 교수는 “본 연구는 미토콘드리아 막 단백질이 산화된 STING의 다량체 형성을 조절하는 원리를 최초로 제공한 연구이면서 STING이라는 단백질을 통하여, 다양한 번역 후 변형간의 상호 작용과 고차원 구조적 변화, 그리고 이에 기여하는 세포내 소기관의 교류를 동시에 밝혀 보다 넓은 학문분야에 활용되는 지식을 제공했다는 데 의의가 크다”고 언급하면서, “본 연구를 통해 얻은 새로운 지식은 STING이 매개하는 다양한 염증성 질환에 대한 보다 깊은 이해와 치료제 개발 연구에 가치 있게 활용될 것으로 기대한다”고 전했다.
이번 연구는 유럽 분자생물학의 권위있는 국제 학술지 `엠보 리포트 저널 (EMBO (European Molecular Biology Organization) Reports)’에 11월 2일 字 온라인판에 게재됐다 (논문명: MARCH5 promotes STING pathway activation by suppressing polymer formation of oxidized STING). KAIST 생명과학과 손경표 박사과정, 정석환 박사과정, 엄은총 박사과정이 공동 제1 저자로 연구를 주도하였고, 권도형 박사(現 부스트이뮨)가 함께 참여하였다.
이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2023.12.04 조회수 6080 -
 이행 호염구, 알레르기 매개 세포에 대한 새로운 이해
우리 대학 생명과학과 강석조 교수 연구팀이 알레르기를 매개하는 중요한 면역세포인 호염구의 새로운 전구세포를 발견하고, 호염구 말단 분화단계에서 그 고유 기능을 획득하는 데 중요한 전사인자를 규명했다고 7일 밝혔다.
호염구(basophil)는 체내에 극소수로 존재하는 백혈구지만, 알레르기와 같이 제2형 면역 반응으로 매개되는 질환의 주된 작용 세포다. 호염구의 혈액 내 증감을 통해서 알레르기 반응 정도를 판별할 수 있고, 질환의 면역 반응의 중증도에도 영향을 미친다. 호염구는 인체 내로 유입된 알레르기 유발 물질에 특이적인 Immunoglobulin E (IgE)에 대한 수용체를 통해 활성화되면 탈과립(degranulation)과 면역조절 물질인 사이토카인(cytokine)을 비롯해 다양한 염증 유도 물질들을 분비한다. 이를 통하여 호염구는 알레르기 반응을 매개하고 다른 면역세포들의 침윤을 도와 염증 반응을 심화시킨다. 하지만, 이러한 호염구의 초기 분화 과정 연구에 비해 그 고유 기능을 획득하는 말단 분화 과정과 이를 조절하는 인자에 대해서는 알려진 바가 없었다.
강 교수 연구팀은 마우스 골수 내에서 호염구 전구세포(basophil progenitor, BaP)가 세포분열이 없는 최종 분화단계의 성숙한 호염구(mature basophil)로 분화하는 과정 중간에 위치한, 세포분열 능력을 보유한 새로운 전구세포를 발견하였으며 그 특성을 다양한 실험으로 규명하고 ‘이행 호염구(transitional basophil, tBaso)’로 명명하였다. 이행 호염구의 발견을 통하여 강 교수팀은 호염구의 분화과정에서 변화하는 유전자 발현을 더욱 세밀하게 분석할 수 있었으며 세포분열 및 주기 조절과 호염구의 고유한 기능의 조절에 관계하는 유전자의 발현은 분화단계에 따라 다르게 조절됨을 확인하였다.
이어, 호염구의 분화단계에 따라 발현이 변화하는 전사인자 NFIL3를 확인하였고, NFIL3 단백질이 호염구의 말단 분화단계에서 IgE 수용체 활성화에 따라 유도된 호염구의 기능적 특징을 부여하는 중요 인자임을 규명하여 보고하였다. 또한, 호염구 특이적으로 NFIL3가 결손된 마우스를 이용하여, 호염구 내 NFIL3 단백질이 아토피성 피부 질환의 염증 반응을 조절함을 밝혔다.
연구팀은 이행 호염구가 성숙 호염구에 비해 사이토카인 생성 능력이 뛰어남을 추가로 확인하였으며, 사이토카인 자극의 종류에 따라 다른 종류의 제2형 면역반응 사이토카인을 생성함을 밝혔다. 이러한 차별적 사이토카인 생성 능력은 호염구에서는 최초로 발견된 것으로, 추후 호염구 매개 질환에서 그 작용기전을 설명하는 데 중요한 지식을 제공할 것으로 기대한다.
강석조 교수는 “호염구의 말단 분화과정의 중요 전구세포를 발견하고 호염구의 기능적 전문성을 획득하는 다이나믹한 과정을 밝힌 연구”라고 언급하면서, “본 연구를 통해 얻은 새로운 지식은 호염구가 매개하는 알레르기 질환에 대한 이해와 치료제 개발에 활용될 것으로 기대한다”고 전했다.
이번 연구는 면역학 및 알레르기 분야의 세계 최고 국제 학술지 ‘알레르기 및 임상면역학 저널 (The Journal of Allergy and Clinical Immunology)’에 10월 1일 字 온라인판에 게재됐다 (논문명: The transcription factor NFIL3/E4BP4 regulates the developmental stage-specific acquisition of basophil function). KAIST 생명과학과 강석조 교수 연구팀 박지연 박사, 조유리 박사(現 LG화학)가 공동 제1 저자로 연구를 주도하였고, 바이오및뇌공학과 양동찬 박사, 생명과학과 양한슬, 이대엽 교수팀, RIKEN Masato Kubo 교수 연구팀이 함께 참여하였다.
한편 이번 연구는 한국연구재단의 선도연구센터사업의 지원을 받아 수행됐다.
2023.11.07 조회수 5513
이행 호염구, 알레르기 매개 세포에 대한 새로운 이해
우리 대학 생명과학과 강석조 교수 연구팀이 알레르기를 매개하는 중요한 면역세포인 호염구의 새로운 전구세포를 발견하고, 호염구 말단 분화단계에서 그 고유 기능을 획득하는 데 중요한 전사인자를 규명했다고 7일 밝혔다.
호염구(basophil)는 체내에 극소수로 존재하는 백혈구지만, 알레르기와 같이 제2형 면역 반응으로 매개되는 질환의 주된 작용 세포다. 호염구의 혈액 내 증감을 통해서 알레르기 반응 정도를 판별할 수 있고, 질환의 면역 반응의 중증도에도 영향을 미친다. 호염구는 인체 내로 유입된 알레르기 유발 물질에 특이적인 Immunoglobulin E (IgE)에 대한 수용체를 통해 활성화되면 탈과립(degranulation)과 면역조절 물질인 사이토카인(cytokine)을 비롯해 다양한 염증 유도 물질들을 분비한다. 이를 통하여 호염구는 알레르기 반응을 매개하고 다른 면역세포들의 침윤을 도와 염증 반응을 심화시킨다. 하지만, 이러한 호염구의 초기 분화 과정 연구에 비해 그 고유 기능을 획득하는 말단 분화 과정과 이를 조절하는 인자에 대해서는 알려진 바가 없었다.
강 교수 연구팀은 마우스 골수 내에서 호염구 전구세포(basophil progenitor, BaP)가 세포분열이 없는 최종 분화단계의 성숙한 호염구(mature basophil)로 분화하는 과정 중간에 위치한, 세포분열 능력을 보유한 새로운 전구세포를 발견하였으며 그 특성을 다양한 실험으로 규명하고 ‘이행 호염구(transitional basophil, tBaso)’로 명명하였다. 이행 호염구의 발견을 통하여 강 교수팀은 호염구의 분화과정에서 변화하는 유전자 발현을 더욱 세밀하게 분석할 수 있었으며 세포분열 및 주기 조절과 호염구의 고유한 기능의 조절에 관계하는 유전자의 발현은 분화단계에 따라 다르게 조절됨을 확인하였다.
이어, 호염구의 분화단계에 따라 발현이 변화하는 전사인자 NFIL3를 확인하였고, NFIL3 단백질이 호염구의 말단 분화단계에서 IgE 수용체 활성화에 따라 유도된 호염구의 기능적 특징을 부여하는 중요 인자임을 규명하여 보고하였다. 또한, 호염구 특이적으로 NFIL3가 결손된 마우스를 이용하여, 호염구 내 NFIL3 단백질이 아토피성 피부 질환의 염증 반응을 조절함을 밝혔다.
연구팀은 이행 호염구가 성숙 호염구에 비해 사이토카인 생성 능력이 뛰어남을 추가로 확인하였으며, 사이토카인 자극의 종류에 따라 다른 종류의 제2형 면역반응 사이토카인을 생성함을 밝혔다. 이러한 차별적 사이토카인 생성 능력은 호염구에서는 최초로 발견된 것으로, 추후 호염구 매개 질환에서 그 작용기전을 설명하는 데 중요한 지식을 제공할 것으로 기대한다.
강석조 교수는 “호염구의 말단 분화과정의 중요 전구세포를 발견하고 호염구의 기능적 전문성을 획득하는 다이나믹한 과정을 밝힌 연구”라고 언급하면서, “본 연구를 통해 얻은 새로운 지식은 호염구가 매개하는 알레르기 질환에 대한 이해와 치료제 개발에 활용될 것으로 기대한다”고 전했다.
이번 연구는 면역학 및 알레르기 분야의 세계 최고 국제 학술지 ‘알레르기 및 임상면역학 저널 (The Journal of Allergy and Clinical Immunology)’에 10월 1일 字 온라인판에 게재됐다 (논문명: The transcription factor NFIL3/E4BP4 regulates the developmental stage-specific acquisition of basophil function). KAIST 생명과학과 강석조 교수 연구팀 박지연 박사, 조유리 박사(現 LG화학)가 공동 제1 저자로 연구를 주도하였고, 바이오및뇌공학과 양동찬 박사, 생명과학과 양한슬, 이대엽 교수팀, RIKEN Masato Kubo 교수 연구팀이 함께 참여하였다.
한편 이번 연구는 한국연구재단의 선도연구센터사업의 지원을 받아 수행됐다.
2023.11.07 조회수 5513 -
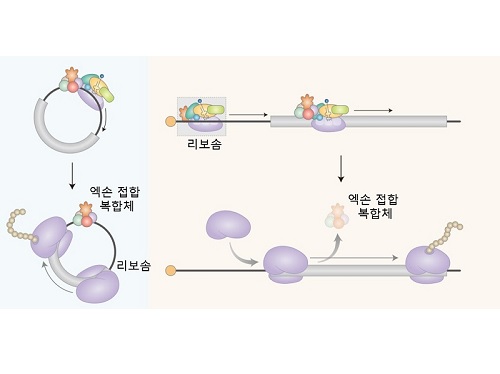 저용량 고효율 RNA백신 개발 가능해지다
현재 널리 사용되고 있는 코로나바이러스 mRNA 백신은 선형 형태의 mRNA를 가지고 있어 세포내에서 매우 불안정한 특징이 있다. 반면 원형 형태의 RNA(circular RNA)는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
우리 대학 생명과학과 김윤기 교수 연구팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA)의 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
분자생물학에서 ‘중심원리(central dogma)’라고 알려진 DNA로부터 시작해 RNA, 단백질로 이어지는 유전정보의 흐름은 다양한 생물학적 기능을 나타내는 중요 원리다. 이때 최종 생산 산물인 단백질은 번역 과정에 의해 생성되며 이와 관련한 메커니즘 연구는 예로부터 활발히 진행돼오고 있었다.
특히 최근에는 mRNA 백신과 관련해 RNA의 안정성과 합성 효율을 극대화할 수 있는 기법에 관해 관심이 쏠리고 있다. 선형 mRNA는 세포내에서 매우 불안정하기 때문에, 항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명하였다. 세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (Exon junction complex; EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명하였다.
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다. 특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍(주) 벤처회사의 공동대표를 맡고 있다.
생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 `핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다. (논문명 : An interaction between eIF4A3 and eIF3g drives the internal initiation of translation).
한편 이번 연구는 한국 연구재단의 지원을 받아 수행됐다.
2023.10.24 조회수 7212
저용량 고효율 RNA백신 개발 가능해지다
현재 널리 사용되고 있는 코로나바이러스 mRNA 백신은 선형 형태의 mRNA를 가지고 있어 세포내에서 매우 불안정한 특징이 있다. 반면 원형 형태의 RNA(circular RNA)는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
우리 대학 생명과학과 김윤기 교수 연구팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA)의 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
분자생물학에서 ‘중심원리(central dogma)’라고 알려진 DNA로부터 시작해 RNA, 단백질로 이어지는 유전정보의 흐름은 다양한 생물학적 기능을 나타내는 중요 원리다. 이때 최종 생산 산물인 단백질은 번역 과정에 의해 생성되며 이와 관련한 메커니즘 연구는 예로부터 활발히 진행돼오고 있었다.
특히 최근에는 mRNA 백신과 관련해 RNA의 안정성과 합성 효율을 극대화할 수 있는 기법에 관해 관심이 쏠리고 있다. 선형 mRNA는 세포내에서 매우 불안정하기 때문에, 항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명하였다. 세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (Exon junction complex; EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명하였다.
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다. 특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍(주) 벤처회사의 공동대표를 맡고 있다.
생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 `핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다. (논문명 : An interaction between eIF4A3 and eIF3g drives the internal initiation of translation).
한편 이번 연구는 한국 연구재단의 지원을 받아 수행됐다.
2023.10.24 조회수 7212 -
 뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
2023.10.16 조회수 7042
뇌종양 면역치료를 고 포도당 음료로?
뇌에서 발생하는 가장 흔한 악성 뇌종양인 교모세포종은 현재 수술, 항암화학요법, 그리고 방사선치료로 대표되는 암치료요법을 모두 동원해도 평균 생존 기간이 평균 15개월 정도밖에 되지 않는 치료가 매우 힘든 암종이다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 교모세포종 실험 쥐 모델에서 고 포도당 음료 보충을 통해 뇌종양의 성장이 억제되는 현상을 관측했고 이에 더해 이러한 억제 효과가 장내 미생물의 특정 균주 변화를 통해 암세포 증식을 억제하는 항종양 면역반응을 증진한 작용원리를 규명했다고 16일 밝혔다.
장내 미생물은 우리 몸과 긴밀한 관련이 있으며, 악성종양에 대한 항종양 면역반응을 조절하는 데 중요한 역할을 하는 것으로 최근 연구에서 알려졌다. 하지만 대다수의 연구가 항종양 면역반응이 활성화된 흑색종과 같은 암종에서 연구가 이뤄졌으며, 뇌종양에 미치는 영향에 대해서는 거의 알려진 바가 없었다.
이번 연구에서 연구팀은 고 포도당 음료와 특정 균주의 복합처리가 뇌종양 내 면역세포 중 T 세포, 특히 CD4+ T 세포의 아형에서 세포독성 기능이 증대되는 것을 단일 세포 전사체 분석을 통해 확인했고, 더 나아가 암미세환경에서 탈진한 T 세포를 재활성화하는 면역관문억제제인 항 PD-1 항체와 복합처리시 탈진된 T세포 표면에 있는 단백질(PD-1)과 결합하여 T 세포 재활성을 유도하여 항암면역 치료의 효과를 더 증진함을 확인했다.
이러한 연구 결과는 기존 면역관문억제제의 효과가 미미했던 교모세포종에서 장내 미생물, 장내 미생물 유래 대사체, 또는 균주 유래 물질의 복합처리를 통해 항종양 면역기능을 향상하는 방식의 뇌종양 치료가 가능하다는 것을 보여주는 결과로, 추후 교모세포종에 항 PD-1 항체와 같은 면역관문억제제 치료를 적용하는데 응용될 수 있을 것으로 기대된다.
이번 연구를 주도한 KAIST 의과학대학원 김재호 박사는 "그동안 잘 알려지지 않은 장내 미생물 분석을 통해 뇌종양 성장을 억제할 수 있는 균주를 확보했으며 이러한 균주에 의한 항 뇌종양 면역조절 기전을 규명한 중요한 연구”라고 설명했다. 이흥규 교수는 “면역관문 치료제에 의한 뇌종양 치료 임상 시험 실패를 극복할 수 있는 대안으로 면역관문 치료제와 뇌종양 억제 유용 균주의 복합 치료를 통해 뇌종양 치료의 가능성을 보여준 동물실험 결과로 향후 장내 미생물을 이용한 항암 치료제 개발의 실마리를 제공할 것으로 기대한다ˮ 라고 연구 결과를 소개했다.
의과학대학원 김재호 박사(現, 미국 LA 소재 시티오브호프 암센터 방사선종양학과 박사후연구원)가 제1 저자로 참여한 이번 연구는 생명과학 분야 국제 학술지 `셀 리포트 (Cell Reports)'에 10월 6일 字 온라인판에 게재됐다. (논문명: Supplementation with a high-glucose drink stimulates anti-tumor immune responses to glioblastoma via gut microbiota modulation)
한편 이번 연구는 한국연구재단 바이오의료기술개발사업의 지원을 받아 수행됐다.
2023.10.16 조회수 7042 -
 비정상 단백질 처리에 관여하는 새로운 인자 발견
우리 대학 생명과학과 김윤기 교수, 조원기 교수 공동연구팀이 비정상 단백질을 처리하기 위해 형성되는 응집체의 형성 경로를 촉진하는 새로운 인자를 규명했다고 밝혔다.
김윤기 교수, 조원기 교수 공동연구팀은 비정상 단백질 처리경로에서 YTHDF2 단백질이 UPF1을 통해 기존에 알려진 CTIF, eEF1A1, 디낵틴1(Dynactin1) 복합체와 상호작용하며, 비정상 단백질을 비정상 단백질 집합소인 애그리좀(aggresome)으로 수송하는 경로를 조절한다고 밝혔다. 비정상 단백질 처리경로에 관여하는 새로운 인자를 규명하고, 단백질 품질검증에서 중요한 역할을 한다는 사실을 밝힘으로써 비정상 단백질에 의해 야기 되는 퇴행성 신경질환의 치료제 개발에 기여할 것으로 기대된다.
생명과학과 황현정 박사, 박태림 박사과정, 김형인 박사과정이 공동 제1 저자로 참여한 이번 연구는 10월 6일 국제 학술지 `네이처 커뮤니케이션즈(Nature communications)'에 게재됐다.
인간의 몸에서는 다양한 생명 활동을 위해 끊임없이 새로운 단백질이 생성되고 사라진다. 단백질 형성과정에서 정상적인 단백질뿐만 아니라 비정상적인 단백질이 형성되기도 한다. 새롭게 형성되는 단백질의 품질검증은 정상적인 생명 활동에 매우 중요하다. 비정상적인 단백질의 축적은 다양한 질환을 일으킬 수 있다.
비정상 단백질 처리경로는 CTIF, eEF1A1, 디낵틴1 복합체와 UPF1이 관여하며 비정상 단백질을 애그리좀으로 수송한다. 이와 같은 비정상 단백질 응집체는 특히 치매, 파킨슨병 등 퇴행성 신경질환 환자의 뇌에서 많이 발견된다.
mRNA에는 전사 후 변형 과정을 통한 다양한 mRNA 변형이 일어난다. mRNA 변형은 mRNA 품질검증, 단백질 번역 등 다양한 mRNA 대사에 중요하다. 그 중 m6A(N6-메틸아데노신)는 mRNA 내부에 가장 많이 존재하는 mRNA 변형으로 알려져 있다.
m6A는 다양한 인식 단백질에 의해 인식되며, 어떤 단백질에 의해 인식되는가에 따라 다양한 mRNA 대사에 영향을 준다. 그 중 YTHDF2 단백질은 m6A 인식 단백질로써 UPF1과 상호작용하며 RNA 분해경로를 조절한다.
연구팀은 YTHDF2 단백질이 기존 연구에서 밝혀진 mRNA 분해경로뿐만 아니라 비정상 단백질 처리경로를 조절한다는 사실을 밝혔다.
연구 결과, YTHDF2 단백질은 m6A RNA와 독립적으로 비정상 단백질 처리경로에서 애그리좀 형성을 조절했다. 면역 침강반응에서 YTHDF2 단백질은 UPF1과의 상호작용을 통해 CTIF, eEF1A1, 디낵틴1으로 이루어진 복합체에 합류하여 복합체와 모터 단백질 디네인(Dynein) 사이의 상호작용을 조절했다.
복합체와 YTHDF2 단백질이 상호작용하지 못하는 경우 애그리좀이 잘 형성되지 않았으며, 그로 인한 세포 사멸이 촉진됐다. 이는 YTHDF2 단백질이 비정상 단백질 처리경로의 핵심 단백질임을 나타낸다.
또한, 연구팀은 단일입자추적(Single-particle imaging) 기법, 초고해상도 이미징(Super-resolution imaging) 기법을 사용하여 YTHDF2 단백질이 없는 경우 비정상 단백질의 수송 속도가 느려지며, 애그리좀이 비정상적인 형태로 형성된다는 것을 입증했다.
비정상 단백질 처리경로에 관여하는 새로운 인자를 규명하고 기존에 알려져 있던 인자들과의 관계를 밝힘으로써 비정상 단백질에 의해 야기 되는 퇴행성 신경질환의 치료제 개발에 기여할 것으로 기대된다.
한편 이번 연구는 한국연구재단과 서경배과학재단의 지원을 받아 수행됐다.
2023.10.12 조회수 7307
비정상 단백질 처리에 관여하는 새로운 인자 발견
우리 대학 생명과학과 김윤기 교수, 조원기 교수 공동연구팀이 비정상 단백질을 처리하기 위해 형성되는 응집체의 형성 경로를 촉진하는 새로운 인자를 규명했다고 밝혔다.
김윤기 교수, 조원기 교수 공동연구팀은 비정상 단백질 처리경로에서 YTHDF2 단백질이 UPF1을 통해 기존에 알려진 CTIF, eEF1A1, 디낵틴1(Dynactin1) 복합체와 상호작용하며, 비정상 단백질을 비정상 단백질 집합소인 애그리좀(aggresome)으로 수송하는 경로를 조절한다고 밝혔다. 비정상 단백질 처리경로에 관여하는 새로운 인자를 규명하고, 단백질 품질검증에서 중요한 역할을 한다는 사실을 밝힘으로써 비정상 단백질에 의해 야기 되는 퇴행성 신경질환의 치료제 개발에 기여할 것으로 기대된다.
생명과학과 황현정 박사, 박태림 박사과정, 김형인 박사과정이 공동 제1 저자로 참여한 이번 연구는 10월 6일 국제 학술지 `네이처 커뮤니케이션즈(Nature communications)'에 게재됐다.
인간의 몸에서는 다양한 생명 활동을 위해 끊임없이 새로운 단백질이 생성되고 사라진다. 단백질 형성과정에서 정상적인 단백질뿐만 아니라 비정상적인 단백질이 형성되기도 한다. 새롭게 형성되는 단백질의 품질검증은 정상적인 생명 활동에 매우 중요하다. 비정상적인 단백질의 축적은 다양한 질환을 일으킬 수 있다.
비정상 단백질 처리경로는 CTIF, eEF1A1, 디낵틴1 복합체와 UPF1이 관여하며 비정상 단백질을 애그리좀으로 수송한다. 이와 같은 비정상 단백질 응집체는 특히 치매, 파킨슨병 등 퇴행성 신경질환 환자의 뇌에서 많이 발견된다.
mRNA에는 전사 후 변형 과정을 통한 다양한 mRNA 변형이 일어난다. mRNA 변형은 mRNA 품질검증, 단백질 번역 등 다양한 mRNA 대사에 중요하다. 그 중 m6A(N6-메틸아데노신)는 mRNA 내부에 가장 많이 존재하는 mRNA 변형으로 알려져 있다.
m6A는 다양한 인식 단백질에 의해 인식되며, 어떤 단백질에 의해 인식되는가에 따라 다양한 mRNA 대사에 영향을 준다. 그 중 YTHDF2 단백질은 m6A 인식 단백질로써 UPF1과 상호작용하며 RNA 분해경로를 조절한다.
연구팀은 YTHDF2 단백질이 기존 연구에서 밝혀진 mRNA 분해경로뿐만 아니라 비정상 단백질 처리경로를 조절한다는 사실을 밝혔다.
연구 결과, YTHDF2 단백질은 m6A RNA와 독립적으로 비정상 단백질 처리경로에서 애그리좀 형성을 조절했다. 면역 침강반응에서 YTHDF2 단백질은 UPF1과의 상호작용을 통해 CTIF, eEF1A1, 디낵틴1으로 이루어진 복합체에 합류하여 복합체와 모터 단백질 디네인(Dynein) 사이의 상호작용을 조절했다.
복합체와 YTHDF2 단백질이 상호작용하지 못하는 경우 애그리좀이 잘 형성되지 않았으며, 그로 인한 세포 사멸이 촉진됐다. 이는 YTHDF2 단백질이 비정상 단백질 처리경로의 핵심 단백질임을 나타낸다.
또한, 연구팀은 단일입자추적(Single-particle imaging) 기법, 초고해상도 이미징(Super-resolution imaging) 기법을 사용하여 YTHDF2 단백질이 없는 경우 비정상 단백질의 수송 속도가 느려지며, 애그리좀이 비정상적인 형태로 형성된다는 것을 입증했다.
비정상 단백질 처리경로에 관여하는 새로운 인자를 규명하고 기존에 알려져 있던 인자들과의 관계를 밝힘으로써 비정상 단백질에 의해 야기 되는 퇴행성 신경질환의 치료제 개발에 기여할 것으로 기대된다.
한편 이번 연구는 한국연구재단과 서경배과학재단의 지원을 받아 수행됐다.
2023.10.12 조회수 7307 -
 팬데믹을 예견할 의사공학자 양성을 꿈꾸며
최근 25년간 노벨 생리의학상 수상자의 37%, 글로벌 상위 10개 제약회사 대표 과학책임자의 70%가 의사과학자다. 코로나를 겪으며 한국에서도 임상 현장과 최신 연구를 연결하는 가교 역할을 하는 의사과학자 양성이 더욱 절실해졌다. 우리 정부도 바이오·디지털헬스 글로벌 중심국가로의 도약을 위해 의사과학자 육성사업을 국정과제로 추진하고 있으며, 과학적 소양을 바탕으로 임상의 과제를 해결하는 의사과학자가 의료계와 바이오산업의 화두로 떠오르고 있다.
우리 대학은 글로벌 바이오헬스사업을 선두할 MD-데이터 공학자, AI 전문가 등의 의사공학자 양성을 위해 그간 추진해온 의과학대학원의 성공적인 운영을 12일 밝혔다. 이와 함께 그간의 성과를 바탕으로 바이오의료 분야에 특화된 과학자 및 공학자 양성을 위해 과학기술의학전문대학원을 설립할 계획이라고 밝혔다.
우리 대학은 2004년 의과학대학원을 설립하여 의사들이 첨단과학 연구역량을 습득할 수 있는 혁신적인 교육환경을 마련하고 현재까지 184명의 의사과학자를 양성하여 산·학·연·병 생태계에 새로운 활력을 불어넣는데 성공하였다. 국내 이공계대학 최초로 의사를 대상으로 선도 연구자 양성을 위한 의사과학자 양성과정(박사학위)을 시행하여 지난 30여년 간 우리나라 의사과학자 양성의 절반 이상을 담당했다.
KAIST 의과학대학원에서는 의학, 생명과학, 자연과학, 공학 등 다양한 학문적 배경을 지닌 28명의 교수진이 연간 총액 330억 원이 넘는 규모의 다학제 융합연구와 교육을 수행하고 있다. 이러한 연구 환경은 우수한 실적으로 이어져, 연간 100편 이상의 SCI급 논문이 의과학대학원에서 발표된다. 논문의 질도 세계 최고 수준이다. 발표 논문의 FWCI(논문영향력지수)의 평균도 3.59에 달한다. 참고로 세계 상위 20개 대학의 FWCI 평균값은 2.06이다.
의과학대학원의 연구가 질적으로 높은 수준을 유지하는 데는 설립 이후 KAIST의 연구풍토로 자리잡은 ‘문제해결형’ 접근법이 큰 역할을 했다. 해결할 과제와 목표를 명확하게 정의하고, 현재 보유한 자원을 고려하여 해결 전략을 수립하는 공학적 방법론이다. 대표적인 사례가 코로나19 팬데믹 기간 중 의과학대학원 신의철 교수가 수행한 연구다. 신 교수 연구팀은 코로나19 대응 방안을 모색하는 과정에서 바이러스에 대한 인체 면역반응의 특성을 규명하여 코로나19 환자의 치료 전략을 마련하는 데 기여했다.
KAIST 특유의 공학적인 방법론 덕분에 의과학대학원은 임상 현장에서 해답을 찾기 어려운 문제를 해결하는 데 탁월한 역량을 보인다. 김진국 교수는 데이터 과학을 기반으로 진단 프로세스를 설계하여 유전체 분석으로 희귀질환을 조기에 찾아내 환자맞춤형 치료제를 개발하는 방법을 제시했다. 김 교수의 성과는 난치병 치료에 중대한 돌파구를 마련하여 세계적으로 주목받았다. 의과학대학원 박종은 교수 연구팀은 인공지능을 활용한 빅데이터 분석을 바탕으로 신개념 암 치료에 활용할 수 있는 ‘스마트 면역세포’를 개발하는 데 성공했다. 박 교수 연구팀의 출발점 역시 데이터과학과 인공지능이었다. 연구팀은 KAIST 내 협력 연구를 통해 수백만 개의 세포에 대한 유전자 발현 데이터베이스를 구축하고, 종양세포와 정상세포 간 유전자 발현 양상 차이를 찾아내는 딥러닝 알고리즘을 개발했다.
의과학대학원의 질병문제 해결에 집중한 혁신적인 연구는 의과학대학원 교수와 졸업생의 딥테크 기반의 바이오 벤처 창업으로 이어지고 있다. 대표적인 사례로 의과학대학원 주영석 교수와 이정석 교수는 지놈인사이트를 공동으로 창업하였다. 지놈인사이트는 세계 최초로 전장유전체분석(WGS·Whole Genome Sequencing) 기반 암 정밀진단 플랫폼을 만들고, 샌디에이고로 본사를 이전하여 적극적인 해외 진출에 나서고 있다. 최근에는 WGS 기반 암 정밀진단 서비스 ‘캔서비전(CancerVision)’을 미국에서 출시하였다. 이외에도 김필한 교수(아이빔테크놀로지(주), CEO), 이정호 교수(소바젠(주), CTO) 등 약 10명의 교원이 6개 기업을 창업했으며, 의과학대학원을 졸업한 의사과학자들도 온코크로스 등 다양한 창업 사례를 내고 있다. 온코크로스는 인공지능을 기반으로 한 의약개발 솔루션 기업이다.
의과학대학원의 우수한 연구 성과는 의과학대학원 교수와 학생에 대한 높은 평가로 이어지고 있다. 의과학대학원의 고규영 교수(특훈교수)는 2023년 대한민국 최고 과학기술인상을 수상하였고, 신의철 교수와 함께 기초과학연구원(IBS) 연구단장으로 활동중이다. 의과학대학원 교수 세 명이 한국연구재단의 개인기초 리더과제에 선정되었고, 네 명이 서경배과학재단의 신진연구자 지원 프로그램에 선정되었다. 그리고 졸업생들은 지난 수년간 분쉬의학상과 아산의학상의 젊은의학자부문, 연강학술상등 젊은과학자에게 수여하는 상의 다수를 수상하였다.
의과학대학원은 KAIST가 보유한 탄탄한 글로벌 네트워크를 바탕으로 국제적인 교류에도 본격적으로 나섰다. 지난 4월에는 미국 보스턴에서 세계적인 연구중심 병원인 하버드의대 매사추세츠 종합병원(MGH) 및 바이오테크놀로지 기업 모더나(Moderna)와 MOU를 체결했다. 이를 바탕으로 향후 보스턴에 소재한 바이오의료 분야 기관들과 의과학자 양성을 위한 공동연구, 인적교류 등 국제 협력을 이어나갈 계획이다.
우리 대학 의과학대학원이 적지 않은 성과를 낳았지만 여전히 우리나라의 의사과학자는 부족하다. 현재 우리나라의 의사과학자는 전체 의사의 1% 미만으로 미국 등 선진국과 비교하면 턱없이 적다. 게다가 임상을 위한 기초 이론을 연구하는 의사과학자를 넘어, 진단이나 치료의 효율적인 프로세스와 방법론을 개발하는 의사공학자의 역할에 대한 인식이 커지고 있지만 의사공학자의 양성은 거의 전무하다. 바이오헬스 산업생태계를 구축하려면 두 부류의 인재가 모두 필요하다. 특히 AI와 빅데이터를 이용한 연구와 진단 및 치료제 개발이 일반화될 것이 자명함을 고려하면 의학에 대한 공학적인 접근이 가능한 의사공학자의 양성을 더욱 시급하다.
이미 산업계에서도 지각변동이 일어나고 있다. 바이오의료는 더 이상 제약회사나 대형병원의 전담분야가 아니다. ‘디지털 의료’라는 현재의 바이오의료 패러다임 전환을 이끄는 주축은 다름아닌 애플, 구글, IBM 아마존, NVIDIA와 같은 이른바 ‘빅테크’다. 국내에서도 삼성 등 IT 분야의 대기업들이 이러한 흐름에 동참하여 바이오의료 분야에 적극적으로 진출하려 한다. 그러나 우리나라에서는 과학과 공학을 기반으로 바이오의료의 문제를 해결하려는 의사과학자와 의사공학자가 부족해서 세계적인 흐름을 따라잡기 쉽지 않다.
이에 우리 대학은 메디컬 산업의 대전환에 대비하고자 새로운 도전을 준비하고 있다. 그간 축적해 온 의사과학자 양성 시스템과 노하우를 기반으로 ‘과학기술의학전문대학원(과기의전원)’의 설립을 추진하고 있다. 과기의전원은 의학교육 단계부터 과학 및 공학적 소양을 갖춘 의사공학자를 양성하고 이후 박사과정을 통해 MD-데이터공학자·AI전문가·전자공학자·신약개발자 등으로 양성하는 것을 목표로 하고 있다.
우리 대학이 과기의전원을 신설하려는 이유는 현재의 의과학대학원만으로 미래의 바이오의료 환경에 완벽하게 대응하기는 어렵기 때문이다. 의과학대학원은 기존의 의과대학을 졸업한 의사를 대상으로 운영되는 프로그램으로 생명과학분야의 연구에는 탁월한 성과를 냈지만, 공학분야에서는 아직 성과가 미약하다. 이는 의과학대학원 연구자의 학술적 배경이 의학이다 보니 지금처럼 전공자도 따라잡기 벅찰 만큼 빠르게 발전하는 공학적 자원을 자유자재로 활용하기는 어렵고, 최신 기술적 성과를 신속하게 의료 분야에 접목하기는 어렵기 때문이다. 과기의전원은 과학과 공학을 기반으로 의학적 소양을 갖춘 인재를 양성하는 데 목표를 둔다. 의학교육단계부터 시작하는 MD-PhD 융합 과정을 운영하려는 이유가 여기에 있다.
과기의전원은 이처럼 급변하는 기술과 산업 트렌드를 바이오의료와 실시간으로 조화시키는 특화된 인재를 양성함으로써 바이오의료의 최신 연구 성과가 산업계에 조기에 안착하는 데 중요한 역할을 할 것이다. 무엇보다 학부 때부터 공학 기반 의료라는 특화된 교육을 실시한다면 과학/공학박사와 임상의 훈련 과정을 모두 거쳐야 했던 기존의 의사과학자 양성과정에 비해 훨씬 신속하게 바이오의료 산업에 필요한 전문가를 공급할 수 있을 것이다.
한편으로는 우수한 과학기술 인재에게 ‘공학과 의학의 융합’이라는 새로운 진로를 제시하여 의료 분야를 지망하는 우수한 인재들이 자신의 관심사를 좇아 연구자의 길을 선택하는 데 기여할 것으로 기대된다. 이처럼 기존의 의학이나 공학과 전혀 다른 융합교육을 받은 혁신 인재들이 바이오헬스 산업의 주역으로 성장한다면 우리나라도 연간 2조달러가 넘는 글로벌 바이오 헬스산업 시장의 퍼스트무버(First-mover)에 당당히 이름을 올릴 수 있을 것이다.
2023.09.12 조회수 7573
팬데믹을 예견할 의사공학자 양성을 꿈꾸며
최근 25년간 노벨 생리의학상 수상자의 37%, 글로벌 상위 10개 제약회사 대표 과학책임자의 70%가 의사과학자다. 코로나를 겪으며 한국에서도 임상 현장과 최신 연구를 연결하는 가교 역할을 하는 의사과학자 양성이 더욱 절실해졌다. 우리 정부도 바이오·디지털헬스 글로벌 중심국가로의 도약을 위해 의사과학자 육성사업을 국정과제로 추진하고 있으며, 과학적 소양을 바탕으로 임상의 과제를 해결하는 의사과학자가 의료계와 바이오산업의 화두로 떠오르고 있다.
우리 대학은 글로벌 바이오헬스사업을 선두할 MD-데이터 공학자, AI 전문가 등의 의사공학자 양성을 위해 그간 추진해온 의과학대학원의 성공적인 운영을 12일 밝혔다. 이와 함께 그간의 성과를 바탕으로 바이오의료 분야에 특화된 과학자 및 공학자 양성을 위해 과학기술의학전문대학원을 설립할 계획이라고 밝혔다.
우리 대학은 2004년 의과학대학원을 설립하여 의사들이 첨단과학 연구역량을 습득할 수 있는 혁신적인 교육환경을 마련하고 현재까지 184명의 의사과학자를 양성하여 산·학·연·병 생태계에 새로운 활력을 불어넣는데 성공하였다. 국내 이공계대학 최초로 의사를 대상으로 선도 연구자 양성을 위한 의사과학자 양성과정(박사학위)을 시행하여 지난 30여년 간 우리나라 의사과학자 양성의 절반 이상을 담당했다.
KAIST 의과학대학원에서는 의학, 생명과학, 자연과학, 공학 등 다양한 학문적 배경을 지닌 28명의 교수진이 연간 총액 330억 원이 넘는 규모의 다학제 융합연구와 교육을 수행하고 있다. 이러한 연구 환경은 우수한 실적으로 이어져, 연간 100편 이상의 SCI급 논문이 의과학대학원에서 발표된다. 논문의 질도 세계 최고 수준이다. 발표 논문의 FWCI(논문영향력지수)의 평균도 3.59에 달한다. 참고로 세계 상위 20개 대학의 FWCI 평균값은 2.06이다.
의과학대학원의 연구가 질적으로 높은 수준을 유지하는 데는 설립 이후 KAIST의 연구풍토로 자리잡은 ‘문제해결형’ 접근법이 큰 역할을 했다. 해결할 과제와 목표를 명확하게 정의하고, 현재 보유한 자원을 고려하여 해결 전략을 수립하는 공학적 방법론이다. 대표적인 사례가 코로나19 팬데믹 기간 중 의과학대학원 신의철 교수가 수행한 연구다. 신 교수 연구팀은 코로나19 대응 방안을 모색하는 과정에서 바이러스에 대한 인체 면역반응의 특성을 규명하여 코로나19 환자의 치료 전략을 마련하는 데 기여했다.
KAIST 특유의 공학적인 방법론 덕분에 의과학대학원은 임상 현장에서 해답을 찾기 어려운 문제를 해결하는 데 탁월한 역량을 보인다. 김진국 교수는 데이터 과학을 기반으로 진단 프로세스를 설계하여 유전체 분석으로 희귀질환을 조기에 찾아내 환자맞춤형 치료제를 개발하는 방법을 제시했다. 김 교수의 성과는 난치병 치료에 중대한 돌파구를 마련하여 세계적으로 주목받았다. 의과학대학원 박종은 교수 연구팀은 인공지능을 활용한 빅데이터 분석을 바탕으로 신개념 암 치료에 활용할 수 있는 ‘스마트 면역세포’를 개발하는 데 성공했다. 박 교수 연구팀의 출발점 역시 데이터과학과 인공지능이었다. 연구팀은 KAIST 내 협력 연구를 통해 수백만 개의 세포에 대한 유전자 발현 데이터베이스를 구축하고, 종양세포와 정상세포 간 유전자 발현 양상 차이를 찾아내는 딥러닝 알고리즘을 개발했다.
의과학대학원의 질병문제 해결에 집중한 혁신적인 연구는 의과학대학원 교수와 졸업생의 딥테크 기반의 바이오 벤처 창업으로 이어지고 있다. 대표적인 사례로 의과학대학원 주영석 교수와 이정석 교수는 지놈인사이트를 공동으로 창업하였다. 지놈인사이트는 세계 최초로 전장유전체분석(WGS·Whole Genome Sequencing) 기반 암 정밀진단 플랫폼을 만들고, 샌디에이고로 본사를 이전하여 적극적인 해외 진출에 나서고 있다. 최근에는 WGS 기반 암 정밀진단 서비스 ‘캔서비전(CancerVision)’을 미국에서 출시하였다. 이외에도 김필한 교수(아이빔테크놀로지(주), CEO), 이정호 교수(소바젠(주), CTO) 등 약 10명의 교원이 6개 기업을 창업했으며, 의과학대학원을 졸업한 의사과학자들도 온코크로스 등 다양한 창업 사례를 내고 있다. 온코크로스는 인공지능을 기반으로 한 의약개발 솔루션 기업이다.
의과학대학원의 우수한 연구 성과는 의과학대학원 교수와 학생에 대한 높은 평가로 이어지고 있다. 의과학대학원의 고규영 교수(특훈교수)는 2023년 대한민국 최고 과학기술인상을 수상하였고, 신의철 교수와 함께 기초과학연구원(IBS) 연구단장으로 활동중이다. 의과학대학원 교수 세 명이 한국연구재단의 개인기초 리더과제에 선정되었고, 네 명이 서경배과학재단의 신진연구자 지원 프로그램에 선정되었다. 그리고 졸업생들은 지난 수년간 분쉬의학상과 아산의학상의 젊은의학자부문, 연강학술상등 젊은과학자에게 수여하는 상의 다수를 수상하였다.
의과학대학원은 KAIST가 보유한 탄탄한 글로벌 네트워크를 바탕으로 국제적인 교류에도 본격적으로 나섰다. 지난 4월에는 미국 보스턴에서 세계적인 연구중심 병원인 하버드의대 매사추세츠 종합병원(MGH) 및 바이오테크놀로지 기업 모더나(Moderna)와 MOU를 체결했다. 이를 바탕으로 향후 보스턴에 소재한 바이오의료 분야 기관들과 의과학자 양성을 위한 공동연구, 인적교류 등 국제 협력을 이어나갈 계획이다.
우리 대학 의과학대학원이 적지 않은 성과를 낳았지만 여전히 우리나라의 의사과학자는 부족하다. 현재 우리나라의 의사과학자는 전체 의사의 1% 미만으로 미국 등 선진국과 비교하면 턱없이 적다. 게다가 임상을 위한 기초 이론을 연구하는 의사과학자를 넘어, 진단이나 치료의 효율적인 프로세스와 방법론을 개발하는 의사공학자의 역할에 대한 인식이 커지고 있지만 의사공학자의 양성은 거의 전무하다. 바이오헬스 산업생태계를 구축하려면 두 부류의 인재가 모두 필요하다. 특히 AI와 빅데이터를 이용한 연구와 진단 및 치료제 개발이 일반화될 것이 자명함을 고려하면 의학에 대한 공학적인 접근이 가능한 의사공학자의 양성을 더욱 시급하다.
이미 산업계에서도 지각변동이 일어나고 있다. 바이오의료는 더 이상 제약회사나 대형병원의 전담분야가 아니다. ‘디지털 의료’라는 현재의 바이오의료 패러다임 전환을 이끄는 주축은 다름아닌 애플, 구글, IBM 아마존, NVIDIA와 같은 이른바 ‘빅테크’다. 국내에서도 삼성 등 IT 분야의 대기업들이 이러한 흐름에 동참하여 바이오의료 분야에 적극적으로 진출하려 한다. 그러나 우리나라에서는 과학과 공학을 기반으로 바이오의료의 문제를 해결하려는 의사과학자와 의사공학자가 부족해서 세계적인 흐름을 따라잡기 쉽지 않다.
이에 우리 대학은 메디컬 산업의 대전환에 대비하고자 새로운 도전을 준비하고 있다. 그간 축적해 온 의사과학자 양성 시스템과 노하우를 기반으로 ‘과학기술의학전문대학원(과기의전원)’의 설립을 추진하고 있다. 과기의전원은 의학교육 단계부터 과학 및 공학적 소양을 갖춘 의사공학자를 양성하고 이후 박사과정을 통해 MD-데이터공학자·AI전문가·전자공학자·신약개발자 등으로 양성하는 것을 목표로 하고 있다.
우리 대학이 과기의전원을 신설하려는 이유는 현재의 의과학대학원만으로 미래의 바이오의료 환경에 완벽하게 대응하기는 어렵기 때문이다. 의과학대학원은 기존의 의과대학을 졸업한 의사를 대상으로 운영되는 프로그램으로 생명과학분야의 연구에는 탁월한 성과를 냈지만, 공학분야에서는 아직 성과가 미약하다. 이는 의과학대학원 연구자의 학술적 배경이 의학이다 보니 지금처럼 전공자도 따라잡기 벅찰 만큼 빠르게 발전하는 공학적 자원을 자유자재로 활용하기는 어렵고, 최신 기술적 성과를 신속하게 의료 분야에 접목하기는 어렵기 때문이다. 과기의전원은 과학과 공학을 기반으로 의학적 소양을 갖춘 인재를 양성하는 데 목표를 둔다. 의학교육단계부터 시작하는 MD-PhD 융합 과정을 운영하려는 이유가 여기에 있다.
과기의전원은 이처럼 급변하는 기술과 산업 트렌드를 바이오의료와 실시간으로 조화시키는 특화된 인재를 양성함으로써 바이오의료의 최신 연구 성과가 산업계에 조기에 안착하는 데 중요한 역할을 할 것이다. 무엇보다 학부 때부터 공학 기반 의료라는 특화된 교육을 실시한다면 과학/공학박사와 임상의 훈련 과정을 모두 거쳐야 했던 기존의 의사과학자 양성과정에 비해 훨씬 신속하게 바이오의료 산업에 필요한 전문가를 공급할 수 있을 것이다.
한편으로는 우수한 과학기술 인재에게 ‘공학과 의학의 융합’이라는 새로운 진로를 제시하여 의료 분야를 지망하는 우수한 인재들이 자신의 관심사를 좇아 연구자의 길을 선택하는 데 기여할 것으로 기대된다. 이처럼 기존의 의학이나 공학과 전혀 다른 융합교육을 받은 혁신 인재들이 바이오헬스 산업의 주역으로 성장한다면 우리나라도 연간 2조달러가 넘는 글로벌 바이오 헬스산업 시장의 퍼스트무버(First-mover)에 당당히 이름을 올릴 수 있을 것이다.
2023.09.12 조회수 7573 -
 유전자 가위와 약물로 동시에 암을 잡는 신약 개발
암은 과거부터 인류의 건강을 위협하는 요인이다. 암을 치료하는 방법으로 임상에서 주로 화학 약물 및 항체 치료가 사용되고 있으나, 심각한 부작용 또는 반복 투여가 필요해 어려움이 있다. 따라서, 영구적인 유전자 조절을 일으키는 유전자가위(CRISPR, 이하 크리스퍼) 기반 유전자 교정 기술을 이용하면 문제를 극복할 수 있지만, 생체 내 전달이 어려워 효과적인 전달 방법이 절실히 필요한 실정이다.
우리 대학 생명과학과 정현정 교수, 화학과 박희성 교수 공동연구팀이 유전자가위 기반 항암 신약으로 크리스퍼 단백질 및 화학 약물을 동시에 생체 내에 전달하는 나노복합체를 개발해 기존 항암제보다 월등한 항암 효능을 보였다고 3일 밝혔다.
크리스퍼 기술은 표적 세포에서 정밀하고 영구적으로 유전자 교정을 일으킬 수 있어 기존 유전자 조절 방법에 비해 암의 치료제로서 큰 장점이 있다. 하지만 크리스퍼의 구성 요소인 단백질과 가이드 RNA를 생체 내에 전달했을 때 극히 낮은 조직 투과성 및 세포 유입 효율로 인해 치료 효능이 떨어진다. 이러한 한계점을 극복하기 위해 지질 나노입자, 고분자, 무기나노입자 등에 나노 전달체에 기반한 전달 방법이 개발됐으나, 여전히 효능이 떨어지고 심각한 독성 및 부작용 문제가 나타났다.
이러한 문제점들을 극복하기 위해 연구팀은 크리스퍼 단백질 Cas9에 서로다른 작용기가 간단히 결합되는 클릭 화학 작용기를 내재하기 위해 비천연 아미노산을 도입한 생직교 반응형 Cas9을 개발했다. 생직교 반응은 살아있는 시스템 내에서 본질적인 생화학 과정을 방해하지 않고 일어나는 반응을 말한다. 연구팀은 기존 나노 전달체의 독성 및 한계를 극복하기 위해 극미량의 고분자 물질을 생직교 반응형 Cas9에 결합시킴으로써 생체 내에 안전하게 전달 및 유전자 교정을 일으킬 수 있음을 확인했다. 또, 항암 신약으로써 효능을 극대화하기 위해 기존에 유방암 항암제로 사용되는 올라파리브(olaparib)을 생직교 반응에 의해 Cas9에 결합시킴으로써 병용 치료를 위한 유전자가위 나노복합체인 콤바인 (ComBiNE, Combinatorial and bioorthogonal nano-editing complex)을 개발했다.
연구팀은 개발한 유전자교정 나노복합체를 이용해 유방암 세포 및 동물모델에서 DNA 복구에 관여하는 유전자 교정 및 올라파리브의 작용으로 기존 항암제 및 단독 치료제에 비해 월등한 항암효과가 나타남을 확인했다.
이번 연구는 최초로 크리스퍼 단백질과 화학 항암제를 단일 제형으로 안전하고 효과적인 생체 내 유전자 교정을 일으켜 높은 항암 효능을 보였다는 점에서 큰 의의가 있다. 연구팀은 이번 연구 결과가 향후 다양한 암종에 대해 유전자 및 화학 약물 기반 병용 치료제로서 적용할 수 있는 강력한 플랫폼 기술로 활용될 것을 기대하고 있다.
우리 대학 생명과학과 마셀 야니스 베하(Marcel Janis Beha) 박사와 석박사통합과정 임산해 학생, 화학과 석박사통합과정 김주찬 학생이 제1 저자로 참여한 이번 연구는 국제학술지 `어드밴스드 사이언스(Advanced Science)'에 7월 23일 온라인 게재됐다. (논문명: Bioorthogonal CRISPR/Cas9-Drug Conjugate: A Combinatorial Nanomedicine Platform)
한편 이번 연구는 한국연구재단, 보건복지부 및 삼성미래기술육성사업의 지원을 통해 이뤄졌다.
2023.08.03 조회수 10380
유전자 가위와 약물로 동시에 암을 잡는 신약 개발
암은 과거부터 인류의 건강을 위협하는 요인이다. 암을 치료하는 방법으로 임상에서 주로 화학 약물 및 항체 치료가 사용되고 있으나, 심각한 부작용 또는 반복 투여가 필요해 어려움이 있다. 따라서, 영구적인 유전자 조절을 일으키는 유전자가위(CRISPR, 이하 크리스퍼) 기반 유전자 교정 기술을 이용하면 문제를 극복할 수 있지만, 생체 내 전달이 어려워 효과적인 전달 방법이 절실히 필요한 실정이다.
우리 대학 생명과학과 정현정 교수, 화학과 박희성 교수 공동연구팀이 유전자가위 기반 항암 신약으로 크리스퍼 단백질 및 화학 약물을 동시에 생체 내에 전달하는 나노복합체를 개발해 기존 항암제보다 월등한 항암 효능을 보였다고 3일 밝혔다.
크리스퍼 기술은 표적 세포에서 정밀하고 영구적으로 유전자 교정을 일으킬 수 있어 기존 유전자 조절 방법에 비해 암의 치료제로서 큰 장점이 있다. 하지만 크리스퍼의 구성 요소인 단백질과 가이드 RNA를 생체 내에 전달했을 때 극히 낮은 조직 투과성 및 세포 유입 효율로 인해 치료 효능이 떨어진다. 이러한 한계점을 극복하기 위해 지질 나노입자, 고분자, 무기나노입자 등에 나노 전달체에 기반한 전달 방법이 개발됐으나, 여전히 효능이 떨어지고 심각한 독성 및 부작용 문제가 나타났다.
이러한 문제점들을 극복하기 위해 연구팀은 크리스퍼 단백질 Cas9에 서로다른 작용기가 간단히 결합되는 클릭 화학 작용기를 내재하기 위해 비천연 아미노산을 도입한 생직교 반응형 Cas9을 개발했다. 생직교 반응은 살아있는 시스템 내에서 본질적인 생화학 과정을 방해하지 않고 일어나는 반응을 말한다. 연구팀은 기존 나노 전달체의 독성 및 한계를 극복하기 위해 극미량의 고분자 물질을 생직교 반응형 Cas9에 결합시킴으로써 생체 내에 안전하게 전달 및 유전자 교정을 일으킬 수 있음을 확인했다. 또, 항암 신약으로써 효능을 극대화하기 위해 기존에 유방암 항암제로 사용되는 올라파리브(olaparib)을 생직교 반응에 의해 Cas9에 결합시킴으로써 병용 치료를 위한 유전자가위 나노복합체인 콤바인 (ComBiNE, Combinatorial and bioorthogonal nano-editing complex)을 개발했다.
연구팀은 개발한 유전자교정 나노복합체를 이용해 유방암 세포 및 동물모델에서 DNA 복구에 관여하는 유전자 교정 및 올라파리브의 작용으로 기존 항암제 및 단독 치료제에 비해 월등한 항암효과가 나타남을 확인했다.
이번 연구는 최초로 크리스퍼 단백질과 화학 항암제를 단일 제형으로 안전하고 효과적인 생체 내 유전자 교정을 일으켜 높은 항암 효능을 보였다는 점에서 큰 의의가 있다. 연구팀은 이번 연구 결과가 향후 다양한 암종에 대해 유전자 및 화학 약물 기반 병용 치료제로서 적용할 수 있는 강력한 플랫폼 기술로 활용될 것을 기대하고 있다.
우리 대학 생명과학과 마셀 야니스 베하(Marcel Janis Beha) 박사와 석박사통합과정 임산해 학생, 화학과 석박사통합과정 김주찬 학생이 제1 저자로 참여한 이번 연구는 국제학술지 `어드밴스드 사이언스(Advanced Science)'에 7월 23일 온라인 게재됐다. (논문명: Bioorthogonal CRISPR/Cas9-Drug Conjugate: A Combinatorial Nanomedicine Platform)
한편 이번 연구는 한국연구재단, 보건복지부 및 삼성미래기술육성사업의 지원을 통해 이뤄졌다.
2023.08.03 조회수 10380 -
 탄수화물 나노입자로 염증성 장 질환 치료하다
위장관에 발병하는 만성적인 염증성 장 질환은 아직 뚜렷한 원인이 밝혀지지 않아 비스테로이드성 항염증제들과 주사용 항체 치료제들을 이용한 치료법이 일반적이지만 면역약화 등의 부작용들로 인해 치료에 어려움이 있다.
우리 대학 생명과학과 전상용 교수와 화학과 이희승 교수 공동연구팀이 장 내 당질층을 모사한 탄수화물 나노입자에 생체 내에서 항산화 및 항염증 작용을 하는 빌리루빈을 결합해 ‘항염증 탄수화물 나노입자(Anti-inflammatory Glycocalyx-mimicking nanoparticles)‘ 수십 종을 합성하고 이를 염증성 장 질환 치료에 적용함으로써 탁월한 효능을 보이는 의약을 개발했다고 2일 밝혔다.
세포막은 다양한 형태의 당 사슬 집합체인 당질층(glycocalyx)으로 둘러싸여 있다. 염증성 장 질환이 있는 사람의 장 조직에서는 정상인들과 다른 당질층이 형성되어 있다. 이러한 당질층은 우리 몸이나 음식에 많이 존재하는 탄수화물을 이루는 구성 성분인 여러 가지 당들에 대해 선택적인 결합력을 보인다. 이에 착안해 연구팀은 자연에 존재하는 탄수화물을 구성하는 대표적인 다섯 가지의 당들을 조합해 수 십가지의 인공 탄수화물(glycopolymers) 후보군들을 합성하여 염증성 장 질환 조직에 형성된 당질층에 잘 결합하는 인공 탄수화물 후보군을 선별하고자 하였다. 합성된 수 십가지의 인공 탄수화물에 우리 몸속에서 항산화 및 항염증 작용을 하는 빌리루빈 생리활성 물질을 결합하여 최종적으로 당질층을 표적할 수 있는 ‘항염증 탄수화물 나노입자(anti-inflammatory glyconanoparticles)’후보군들을 구축하였다.
연구팀은 구축된 항염증 탄수화물 나노입자 후보군들을 염증성 장 질환 생쥐모델에서 직접 경구투여를 통해 치료효능이 가장 우수한 탄수화물 나노입자를 선별할 수 있었다. 선별된 항염증 탄수화물 나노입자가 어떻게 치료효능 및 작용기전을 나타냈는지도 조사하였고 치료 효능이 기존에 사용하던 저분자 합성의약보다 더 우수한 효능을 가질 수 있음을 확인했다.
우리 대학 생명과학과 유도현 박사 및 황창희 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 정상급 학술지인 `앙게반테 케미(Angewandte Chemie International Edition, ISSN: 1433-7851 print, 1521-3773 online, Impact Factor: 16.823)' 6월 13일 字 온라인판에 게재됐다.
(https://doi.org/10.1002/anie.202304815 논문명: Anti-inflammatory Glycocalyx-Mimicking Nanoparticles for Colitis Treatment: Construction and In Vivo Evaluation).
전상용 교수는 “본 연구를 통해 당질층 표적형 항염증 탄수화물 나노입자 플랫폼 기술은 염증성 장 질환 외에도 다양한 염증 질환들의 치료에 적용될 수 있을 것으로 기대한다” 라고 말했다.
이 논문은 해당 학술지에서 선정한 특별 언론홍보 대상으로 선정돼 해외 과학 전문 보도 매체인 ‘ScienceDaily’ 와 ‘ChemistryViews’ 등에도 소개된 바 있다.(ScienceDaily: https://www.sciencedaily.com, ChemistryViews: https://www.chemistryviews.org)
한편 이번 연구는 한국연구재단의 리더연구사업(종양/염증 미세환경 표적 및 감응형 정밀 바이오-나노메디신 연구단) 및 선도연구센터사업(멀티스케일 카이랄 구조체 연구센터, CMCA)의 지원을 받아 수행됐다.
2023.08.02 조회수 7519
탄수화물 나노입자로 염증성 장 질환 치료하다
위장관에 발병하는 만성적인 염증성 장 질환은 아직 뚜렷한 원인이 밝혀지지 않아 비스테로이드성 항염증제들과 주사용 항체 치료제들을 이용한 치료법이 일반적이지만 면역약화 등의 부작용들로 인해 치료에 어려움이 있다.
우리 대학 생명과학과 전상용 교수와 화학과 이희승 교수 공동연구팀이 장 내 당질층을 모사한 탄수화물 나노입자에 생체 내에서 항산화 및 항염증 작용을 하는 빌리루빈을 결합해 ‘항염증 탄수화물 나노입자(Anti-inflammatory Glycocalyx-mimicking nanoparticles)‘ 수십 종을 합성하고 이를 염증성 장 질환 치료에 적용함으로써 탁월한 효능을 보이는 의약을 개발했다고 2일 밝혔다.
세포막은 다양한 형태의 당 사슬 집합체인 당질층(glycocalyx)으로 둘러싸여 있다. 염증성 장 질환이 있는 사람의 장 조직에서는 정상인들과 다른 당질층이 형성되어 있다. 이러한 당질층은 우리 몸이나 음식에 많이 존재하는 탄수화물을 이루는 구성 성분인 여러 가지 당들에 대해 선택적인 결합력을 보인다. 이에 착안해 연구팀은 자연에 존재하는 탄수화물을 구성하는 대표적인 다섯 가지의 당들을 조합해 수 십가지의 인공 탄수화물(glycopolymers) 후보군들을 합성하여 염증성 장 질환 조직에 형성된 당질층에 잘 결합하는 인공 탄수화물 후보군을 선별하고자 하였다. 합성된 수 십가지의 인공 탄수화물에 우리 몸속에서 항산화 및 항염증 작용을 하는 빌리루빈 생리활성 물질을 결합하여 최종적으로 당질층을 표적할 수 있는 ‘항염증 탄수화물 나노입자(anti-inflammatory glyconanoparticles)’후보군들을 구축하였다.
연구팀은 구축된 항염증 탄수화물 나노입자 후보군들을 염증성 장 질환 생쥐모델에서 직접 경구투여를 통해 치료효능이 가장 우수한 탄수화물 나노입자를 선별할 수 있었다. 선별된 항염증 탄수화물 나노입자가 어떻게 치료효능 및 작용기전을 나타냈는지도 조사하였고 치료 효능이 기존에 사용하던 저분자 합성의약보다 더 우수한 효능을 가질 수 있음을 확인했다.
우리 대학 생명과학과 유도현 박사 및 황창희 박사가 공동 제1 저자로 참여한 이번 연구는 화학 분야 정상급 학술지인 `앙게반테 케미(Angewandte Chemie International Edition, ISSN: 1433-7851 print, 1521-3773 online, Impact Factor: 16.823)' 6월 13일 字 온라인판에 게재됐다.
(https://doi.org/10.1002/anie.202304815 논문명: Anti-inflammatory Glycocalyx-Mimicking Nanoparticles for Colitis Treatment: Construction and In Vivo Evaluation).
전상용 교수는 “본 연구를 통해 당질층 표적형 항염증 탄수화물 나노입자 플랫폼 기술은 염증성 장 질환 외에도 다양한 염증 질환들의 치료에 적용될 수 있을 것으로 기대한다” 라고 말했다.
이 논문은 해당 학술지에서 선정한 특별 언론홍보 대상으로 선정돼 해외 과학 전문 보도 매체인 ‘ScienceDaily’ 와 ‘ChemistryViews’ 등에도 소개된 바 있다.(ScienceDaily: https://www.sciencedaily.com, ChemistryViews: https://www.chemistryviews.org)
한편 이번 연구는 한국연구재단의 리더연구사업(종양/염증 미세환경 표적 및 감응형 정밀 바이오-나노메디신 연구단) 및 선도연구센터사업(멀티스케일 카이랄 구조체 연구센터, CMCA)의 지원을 받아 수행됐다.
2023.08.02 조회수 7519 -
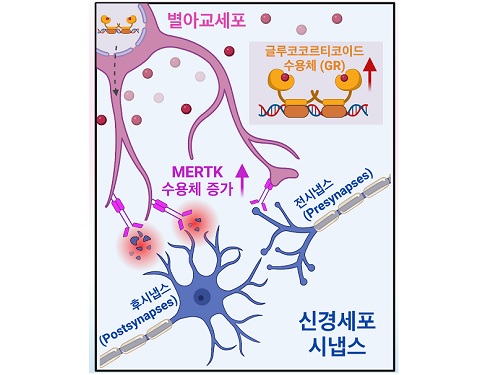 아동 학대로 인한 정신질환 발병 원인 최초 규명
아동기 시 부모에게서 떨어져서 방치되거나 학대를 받을 경우, 극심한 스트레스 현상이 일어난다. 이러한 스트레스 상황을 겪게 되면 성인으로 성장하는 과정 동안 뇌 신경 회로망 및 기능이 크게 변화되어 조현병 및 우울증과 같은 정신질환이 발생될 수 있다. 하지만 현재까지 아동기 스트레스에 따른 정신질환의 원인과 그 제어 방법에 대해서는 정확히 알려진 바가 없다.
우리 대학 생명과학과 정원석 교수 연구팀이 아동 학대 및 방임 등의 아동기 스트레스로 인해 발병되는 정신질환이 별아교세포의 과도한 시냅스 제거에서 기인함을 최초로 규명해 면역 관련 최고 국제 학술지인 ‘이뮤니티(Immunity)’에 발표했다고 1일 밝혔다.
정원석 교수 연구팀은 뇌에서 면역기능을 담당하는 별아교세포가 스트레스 호르몬에 반응하여 과도하게 흥분성 시냅스를 제거하는 현상이, 아동 학대 및 방임에 따른 정신질환 발병의 주요 원인임을 최초로 규명하였다. 과도한 스트레스가 다양한 정신질환의 원인으로 작용할 수 있음이 임상적으로 알려져 있었지만, 그 정확한 발병 기전은 알려지지 않았기 때문에 이번 연구는 스트레스로 인한 정신질환의 예방 및 치료에 크게 응용될 수 있을 것으로 기대된다.
연구팀은 미국식품의약국 (FDA)에서 승인된 임상 약물 스크리닝을 진행해 별아교세포의 외부 물질을 잡아 먹어 제거하는 역할(포식 작용)을 조절하는 새로운 기작을 발굴했다. 그 결과, 연구팀은 스트레스 호르몬이라 불리는 합성 글루코코르티코이드(synthetic glucocorticoid)가 별아교세포의 포식 작용을 비정상적으로 크게 높이는 것을 발견했다. 글루코코르티코이드는 당대사, 항염증 등 생명 유지에 필요한 역할을 하는 한편 스트레스와 같은 외부 자극에 의해 분비돼 신체가 대응할 수 있도록 한다. 하지만 만성 스트레스로 인해 글루코코르티코이드에 과도하게 장기간 노출되면 우울증, 인지장애, 불안 증세와 같은 다양한 정신질환이 발병할 수 있다.
연구팀은 아동기 스트레스로 인한 별아교세포의 기능 변화를 이해하고자 아동기 사회성 결핍(early social deprivation) 생쥐 모델을 활용했고, 그 결과 스트레스 호르몬이 별아교세포의 글루코코르티코이드 수용체 (glucocorticoid receptor; GR)와 결합해 별아교세포의 포식 작용에 중요한 역할을 하는 MERTK(Mer Tyrosine Kinase)라는 수용체의 발현을 크게 증가시킴을 알아냈다. 놀랍게도 별아교세포는 증가된 MERTK를 통해 다양한 대뇌 피질에 존재하는 특정 신경 세포의 흥분성 시냅스만을 선택적으로 잡아 먹어 감소시켰으며, 이로 인한 비정상적인 신경 회로망 형성으로 추후 성인기에 사회성 결핍과 우울증 같은 복합적인 행동 이상이 일어남을 발견했다.
뿐만 아니라 연구팀은 별아교세포와 함께 뇌 면역 기능에 중요한 역할을 담당하는 것으로 알려진 미세아교세포는 아동기 사회성 결핍 쥐 모델에서의 시냅스 제거에는 전혀 참여하고 있지 않음을 관찰했다. 이는 아동기 스트레스 상황에서 미세아교세포가 아닌 별아교세포가 특이적으로 스트레스 호르몬에 반응해 뇌의 환경을 조절하고 있음을 확인한 것이다.
연구팀은 이 같은 발견이 인간에게도 적용될 수 있는지를 알아보기 위해, 인간 만능 유도 줄기세포에서 유래한 뇌 오가노이드를 활용해 스트레스 호르몬에 대한 반응을 확인했다. 중요하게도 연구팀은 인간 뇌 오가노이드에서도 스트레스 호르몬에 의해 별아교세포의 글루코코르티코이드 수용체와 포식 수용체가 모두 활성화됨을 발견했으며, 또한 별아교세포가 흥분성 시냅스를 과도하게 제거함을 확인했다. 이로써 스트레스 반응에 대한 쥐와 인간의 시냅스 조절 메커니즘이 같음을 보임으로써, 연구팀은 이번 발견이 인간의 정신질환 치료에도 응용될 수 있음을 제시했다.
정원석 교수는 “지금까지 아동기 스트레스와 뇌 질환 발병의 메커니즘은 잘 밝혀져 있지 않았지만, 이번 연구를 통해 과도한 별아교세포의 포식 작용이 정신질환 발병에 있어 중요한 원인이 될 수 있음을 최초로 증명했다”고 언급하며 “추후 다양한 뇌 질환의 이해와 치료에 있어서 별아교세포의 면역기능 조절이 근본적인 타겟으로 응용될 수 있을 것”이라고 밝혔다.
우리 대학 생명과학과 변유경, 김규리 박사과정 학생과 김남식 박사후연구원이 공동 제1 저자로 참여한 이번 연구는 셀(Cell) 자매지이자 면역 관련 최고 국제 학술지인 `이뮤니티 (IMMUNITY)' 7월 31일 字 온라인 출판됐다. (논문명 : Stress induces behavioral abnormalities by increasing expression of phagocytic receptor MERTK in astrocytes to promote synapse phagocytosis).
한편 이번 연구는 연구재단 중견 연구, 뇌질환극복연구사업, 뇌기능 규명 조절 기술 개발사업의 지원을 받아 수행됐다.
2023.08.01 조회수 7578
아동 학대로 인한 정신질환 발병 원인 최초 규명
아동기 시 부모에게서 떨어져서 방치되거나 학대를 받을 경우, 극심한 스트레스 현상이 일어난다. 이러한 스트레스 상황을 겪게 되면 성인으로 성장하는 과정 동안 뇌 신경 회로망 및 기능이 크게 변화되어 조현병 및 우울증과 같은 정신질환이 발생될 수 있다. 하지만 현재까지 아동기 스트레스에 따른 정신질환의 원인과 그 제어 방법에 대해서는 정확히 알려진 바가 없다.
우리 대학 생명과학과 정원석 교수 연구팀이 아동 학대 및 방임 등의 아동기 스트레스로 인해 발병되는 정신질환이 별아교세포의 과도한 시냅스 제거에서 기인함을 최초로 규명해 면역 관련 최고 국제 학술지인 ‘이뮤니티(Immunity)’에 발표했다고 1일 밝혔다.
정원석 교수 연구팀은 뇌에서 면역기능을 담당하는 별아교세포가 스트레스 호르몬에 반응하여 과도하게 흥분성 시냅스를 제거하는 현상이, 아동 학대 및 방임에 따른 정신질환 발병의 주요 원인임을 최초로 규명하였다. 과도한 스트레스가 다양한 정신질환의 원인으로 작용할 수 있음이 임상적으로 알려져 있었지만, 그 정확한 발병 기전은 알려지지 않았기 때문에 이번 연구는 스트레스로 인한 정신질환의 예방 및 치료에 크게 응용될 수 있을 것으로 기대된다.
연구팀은 미국식품의약국 (FDA)에서 승인된 임상 약물 스크리닝을 진행해 별아교세포의 외부 물질을 잡아 먹어 제거하는 역할(포식 작용)을 조절하는 새로운 기작을 발굴했다. 그 결과, 연구팀은 스트레스 호르몬이라 불리는 합성 글루코코르티코이드(synthetic glucocorticoid)가 별아교세포의 포식 작용을 비정상적으로 크게 높이는 것을 발견했다. 글루코코르티코이드는 당대사, 항염증 등 생명 유지에 필요한 역할을 하는 한편 스트레스와 같은 외부 자극에 의해 분비돼 신체가 대응할 수 있도록 한다. 하지만 만성 스트레스로 인해 글루코코르티코이드에 과도하게 장기간 노출되면 우울증, 인지장애, 불안 증세와 같은 다양한 정신질환이 발병할 수 있다.
연구팀은 아동기 스트레스로 인한 별아교세포의 기능 변화를 이해하고자 아동기 사회성 결핍(early social deprivation) 생쥐 모델을 활용했고, 그 결과 스트레스 호르몬이 별아교세포의 글루코코르티코이드 수용체 (glucocorticoid receptor; GR)와 결합해 별아교세포의 포식 작용에 중요한 역할을 하는 MERTK(Mer Tyrosine Kinase)라는 수용체의 발현을 크게 증가시킴을 알아냈다. 놀랍게도 별아교세포는 증가된 MERTK를 통해 다양한 대뇌 피질에 존재하는 특정 신경 세포의 흥분성 시냅스만을 선택적으로 잡아 먹어 감소시켰으며, 이로 인한 비정상적인 신경 회로망 형성으로 추후 성인기에 사회성 결핍과 우울증 같은 복합적인 행동 이상이 일어남을 발견했다.
뿐만 아니라 연구팀은 별아교세포와 함께 뇌 면역 기능에 중요한 역할을 담당하는 것으로 알려진 미세아교세포는 아동기 사회성 결핍 쥐 모델에서의 시냅스 제거에는 전혀 참여하고 있지 않음을 관찰했다. 이는 아동기 스트레스 상황에서 미세아교세포가 아닌 별아교세포가 특이적으로 스트레스 호르몬에 반응해 뇌의 환경을 조절하고 있음을 확인한 것이다.
연구팀은 이 같은 발견이 인간에게도 적용될 수 있는지를 알아보기 위해, 인간 만능 유도 줄기세포에서 유래한 뇌 오가노이드를 활용해 스트레스 호르몬에 대한 반응을 확인했다. 중요하게도 연구팀은 인간 뇌 오가노이드에서도 스트레스 호르몬에 의해 별아교세포의 글루코코르티코이드 수용체와 포식 수용체가 모두 활성화됨을 발견했으며, 또한 별아교세포가 흥분성 시냅스를 과도하게 제거함을 확인했다. 이로써 스트레스 반응에 대한 쥐와 인간의 시냅스 조절 메커니즘이 같음을 보임으로써, 연구팀은 이번 발견이 인간의 정신질환 치료에도 응용될 수 있음을 제시했다.
정원석 교수는 “지금까지 아동기 스트레스와 뇌 질환 발병의 메커니즘은 잘 밝혀져 있지 않았지만, 이번 연구를 통해 과도한 별아교세포의 포식 작용이 정신질환 발병에 있어 중요한 원인이 될 수 있음을 최초로 증명했다”고 언급하며 “추후 다양한 뇌 질환의 이해와 치료에 있어서 별아교세포의 면역기능 조절이 근본적인 타겟으로 응용될 수 있을 것”이라고 밝혔다.
우리 대학 생명과학과 변유경, 김규리 박사과정 학생과 김남식 박사후연구원이 공동 제1 저자로 참여한 이번 연구는 셀(Cell) 자매지이자 면역 관련 최고 국제 학술지인 `이뮤니티 (IMMUNITY)' 7월 31일 字 온라인 출판됐다. (논문명 : Stress induces behavioral abnormalities by increasing expression of phagocytic receptor MERTK in astrocytes to promote synapse phagocytosis).
한편 이번 연구는 연구재단 중견 연구, 뇌질환극복연구사업, 뇌기능 규명 조절 기술 개발사업의 지원을 받아 수행됐다.
2023.08.01 조회수 7578 -
 갈색 지방 열 생성 조절 인자 규명
우리 대학 의과학대학원 서재명 교수가 한국생명공학연구원(원장 김장성, 이하 생명연) 대사제어연구센터 배광희 박사, 김원곤 박사 연구팀과 공동연구를 통해 갈색지방의 신규 대사 조절 인자를 규명했다고 밝혔다.
갈색지방은 백색지방과는 달리 열 생성을 통해 에너지를 소모하며 갈색지방의 활성은 나이나 신체 대사적 상태 특히, 비만과 반비례 관계를 가지고 있다. 이러한 특성으로 갈색지방은 비만과 대사 질환 제어의 새로운 치료제 표적으로 간주되고 있다. 세포 내 에너지를 생성하는 미토콘드리아 기질에 위치한 짝풀림 단백질(UCP1)이 갈색지방의 열 생성 과정에서 핵심적인 역할을 하는 것으로 알려져 있으나, 다른 열 생성 인자들에 관해서는 많이 알려지지 않았다.
공동 연구팀은 갈색지방의 RNA 전사체와 단백질체 정보를 이용한 다중오믹스 분석을 통해 LETMD1이라는 단백질이 갈색지방조직의 분화 및 발달 단계에서 선택적으로 발현되고 있음을 발견했다. 나아가 LETMD1 단백질이 기존 보고와는 달리 미토콘드리아 기질에 위치하고 있음을 새롭게 확인했다.
LETMD1 유전자 결핍 마우스를 제작하여 추위에 노출 시킨 결과, UCP1 단백질의 발현이 억제되어 있어 체온과 호흡을 유지시키지 못한다는 결과를 관찰했으며, 기전 연구를 통해 LETMD1 단백질이 호흡복합체의 발현과 기능에 영향을 준다는 사실을 밝혔다.
공동 제1 저자인 김광은 박사는 "갈색지방은 섭취한 에너지를 열로 전환할 수 있기 때문에, LETMD1 단백질을 통해 비만 등 대사성 질환의 예방 및 중재기술 개발에 활용될 수 있을 것ˮ이라고 말했다.
우리 대학 의과학대학원 김광은 박사 (현 서울대학교 화학부 박사후연구원)와 생명연 박안나 박사 (현 미시간대 의대 박사후연구원)가 공동 제 1 저자로 참여한 이번 연구는 국제 학술지 `네이쳐 커뮤니케이션즈(Nature Communications)' 6월 23일자 온라인판에 출판되었다. (논문명 : Mitochondrial matrix protein LETMD1 maintains thermogenic capacity of brown adipose tissue in male mice).
이번 연구는 과기정통부 중견연구자 지원사업, 산업자원부 알키미스트사업, 국가신약개발사업, 생명연 주요사업, KAIST 국제공동연구지원사업의 지원으로 수행되었다.
2023.07.31 조회수 7406
갈색 지방 열 생성 조절 인자 규명
우리 대학 의과학대학원 서재명 교수가 한국생명공학연구원(원장 김장성, 이하 생명연) 대사제어연구센터 배광희 박사, 김원곤 박사 연구팀과 공동연구를 통해 갈색지방의 신규 대사 조절 인자를 규명했다고 밝혔다.
갈색지방은 백색지방과는 달리 열 생성을 통해 에너지를 소모하며 갈색지방의 활성은 나이나 신체 대사적 상태 특히, 비만과 반비례 관계를 가지고 있다. 이러한 특성으로 갈색지방은 비만과 대사 질환 제어의 새로운 치료제 표적으로 간주되고 있다. 세포 내 에너지를 생성하는 미토콘드리아 기질에 위치한 짝풀림 단백질(UCP1)이 갈색지방의 열 생성 과정에서 핵심적인 역할을 하는 것으로 알려져 있으나, 다른 열 생성 인자들에 관해서는 많이 알려지지 않았다.
공동 연구팀은 갈색지방의 RNA 전사체와 단백질체 정보를 이용한 다중오믹스 분석을 통해 LETMD1이라는 단백질이 갈색지방조직의 분화 및 발달 단계에서 선택적으로 발현되고 있음을 발견했다. 나아가 LETMD1 단백질이 기존 보고와는 달리 미토콘드리아 기질에 위치하고 있음을 새롭게 확인했다.
LETMD1 유전자 결핍 마우스를 제작하여 추위에 노출 시킨 결과, UCP1 단백질의 발현이 억제되어 있어 체온과 호흡을 유지시키지 못한다는 결과를 관찰했으며, 기전 연구를 통해 LETMD1 단백질이 호흡복합체의 발현과 기능에 영향을 준다는 사실을 밝혔다.
공동 제1 저자인 김광은 박사는 "갈색지방은 섭취한 에너지를 열로 전환할 수 있기 때문에, LETMD1 단백질을 통해 비만 등 대사성 질환의 예방 및 중재기술 개발에 활용될 수 있을 것ˮ이라고 말했다.
우리 대학 의과학대학원 김광은 박사 (현 서울대학교 화학부 박사후연구원)와 생명연 박안나 박사 (현 미시간대 의대 박사후연구원)가 공동 제 1 저자로 참여한 이번 연구는 국제 학술지 `네이쳐 커뮤니케이션즈(Nature Communications)' 6월 23일자 온라인판에 출판되었다. (논문명 : Mitochondrial matrix protein LETMD1 maintains thermogenic capacity of brown adipose tissue in male mice).
이번 연구는 과기정통부 중견연구자 지원사업, 산업자원부 알키미스트사업, 국가신약개발사업, 생명연 주요사업, KAIST 국제공동연구지원사업의 지원으로 수행되었다.
2023.07.31 조회수 7406 -
 인공지능 기반 대장암 3차원 게놈 지도 최초 해독
세계 최초로 예전에 비해 최대 규모로 한국인 대장암 환자 3차원 게놈 지도를 작성하여 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 서울대학교 암연구소 김태유 교수 연구팀과의 공동연구를 통해 인공지능 기반 알고리즘을 활용, 한국인 대장암 환자의 3차원 게놈 지도를 최초로 제시했으며 이를 토대로 암 세포 특이적인 유전자 조절 기전을 통해 특정 종양유전자들이 과발현되는 현상을 규명했다고 24일 밝혔다.
1차원적 게놈 서열 분석에 기반한 현재의 암 유전체 연구는 종양유전자들의 과발현 기작을 설명하는데 한계가 있었다. 하지만 3차원 공간상에 게놈이 어떻게 배열되는지를 분석하는 3차원 게놈 (3D genome) 구조 연구는 이러한 한계를 극복 가능케 하고 있다. 본 연구에서는 정상 세포에서는 존재하지 않는 암 세포 특이적 염색질 고리(chromatin loop) 구조가 유전자 발현 촉진 인자인 인핸서와 종양유전자 사이의 상호작용을 형성하여 과발현을 유도하는 인핸서 납치(enhancer-hijacking) 현상에 초점을 두어 연구하였다.
우리 대학 생명과학과 김규광 박사과정이 주도한 이번 연구는 게놈간의 공간상 상호작용을 측정할 수 있는 대용량 염색체 구조 포착 Hi-C (High-throughput Chromosome Conformation Capture) 실험 기법을 활용하여 대장암 3차원 게놈 지도를 작성하고 대장암 특이적 3차원 게놈 변화를 환자 개개인별로 분석할 수 있는 인공지능 기반 알고리즘을 개발했다. 그 결과 공동연구팀은 광범위한 규모의 3차원 게놈 구조 변화와 이로 인한 다양한 종양유전자의 활성화를 확인했다.
연구팀은 이번 연구를 통해 암 특이적 3차원 게놈 구조의 변화로 인한 종양유전자 활성 기작을 명확히 제시하였으며 이로 인한 환자 예후와 약물 반응 등 임상적인 특성과의 연관성까지 제시해 맞춤 치료 원천기술 확보에 기여했다.
지금까지 암 세포주에 대한 3차원 게놈 구조 연구는 일부 보고 되었으나, 대규모 환자 암조직에 대한 연구는 조직 내 세포 이질성, 종양 순도, 암세포 이질성 등의 문제로 인한 정밀 암 특이적 3차원 게놈 구조 분석의 한계로 수행되지 못하였다.
반면에 이번 연구에서 연구팀은 AI 기반 알고리즘으로 환자 개인 종양 조직으로부터 얻어진 복잡한 신호를 해석할 수 있었으며 그 결과 최대 규모인 환자 40명의 종양 조직과 인접한 정상 대장 조직을 사용해 3차원 게놈 지도를 작성할 수 있었다. 또한 DNA 서열정보를 보여주는 전장유전체 지도의 경우 다양한 인종에 대해 생산되고 있고 한국인의 전장유전체 지도 또한 개발되었으나 한국인 3차원 게놈 지도, 특히 종양 조직에 대한 3차원 게놈 지도는 이번 연구에서 최초로 제시됐다.
이번 연구 결과는 국제 학술지, `셀 리포츠(Cell Reports, IF=9.995)'에 7월 13일 자로 출판됐다. (논문명: Spatial and clonality-resolved 3D cancer genome alterations reveal enhancer-hijacking as a potential prognostic marker for colorectal cancer)
서울대학교병원 혈액종양내과 김태유 교수는 “이러한 결과는 개별 암 환자들마다 서로 다르게 나타나는 종양 이질성을 이해하는 데 매우 중요한 요소가 될 수 있으며, 이를 이용한 환자 맞춤형 치료 연구의 시발점이 될 것이다”라고 말했다. 생명과학과 정인경 교수는 “기존의 점돌연변이나 유전체 변이만으로는 설명이 어려운 암 유전체를 3차원 게놈 구조 관점에서 재해독하고 신규 암 타겟을 발굴할 수 있는 수 있는 새로운 접근법을 제시했다”라고 밝혔다.
한편 이번 연구는 과학기술정보통신부와 서경배과학재단의 지원을 받아 수행됐다.
2023.07.24 조회수 8448
인공지능 기반 대장암 3차원 게놈 지도 최초 해독
세계 최초로 예전에 비해 최대 규모로 한국인 대장암 환자 3차원 게놈 지도를 작성하여 화제다.
우리 대학 생명과학과 정인경 교수 연구팀이 서울대학교 암연구소 김태유 교수 연구팀과의 공동연구를 통해 인공지능 기반 알고리즘을 활용, 한국인 대장암 환자의 3차원 게놈 지도를 최초로 제시했으며 이를 토대로 암 세포 특이적인 유전자 조절 기전을 통해 특정 종양유전자들이 과발현되는 현상을 규명했다고 24일 밝혔다.
1차원적 게놈 서열 분석에 기반한 현재의 암 유전체 연구는 종양유전자들의 과발현 기작을 설명하는데 한계가 있었다. 하지만 3차원 공간상에 게놈이 어떻게 배열되는지를 분석하는 3차원 게놈 (3D genome) 구조 연구는 이러한 한계를 극복 가능케 하고 있다. 본 연구에서는 정상 세포에서는 존재하지 않는 암 세포 특이적 염색질 고리(chromatin loop) 구조가 유전자 발현 촉진 인자인 인핸서와 종양유전자 사이의 상호작용을 형성하여 과발현을 유도하는 인핸서 납치(enhancer-hijacking) 현상에 초점을 두어 연구하였다.
우리 대학 생명과학과 김규광 박사과정이 주도한 이번 연구는 게놈간의 공간상 상호작용을 측정할 수 있는 대용량 염색체 구조 포착 Hi-C (High-throughput Chromosome Conformation Capture) 실험 기법을 활용하여 대장암 3차원 게놈 지도를 작성하고 대장암 특이적 3차원 게놈 변화를 환자 개개인별로 분석할 수 있는 인공지능 기반 알고리즘을 개발했다. 그 결과 공동연구팀은 광범위한 규모의 3차원 게놈 구조 변화와 이로 인한 다양한 종양유전자의 활성화를 확인했다.
연구팀은 이번 연구를 통해 암 특이적 3차원 게놈 구조의 변화로 인한 종양유전자 활성 기작을 명확히 제시하였으며 이로 인한 환자 예후와 약물 반응 등 임상적인 특성과의 연관성까지 제시해 맞춤 치료 원천기술 확보에 기여했다.
지금까지 암 세포주에 대한 3차원 게놈 구조 연구는 일부 보고 되었으나, 대규모 환자 암조직에 대한 연구는 조직 내 세포 이질성, 종양 순도, 암세포 이질성 등의 문제로 인한 정밀 암 특이적 3차원 게놈 구조 분석의 한계로 수행되지 못하였다.
반면에 이번 연구에서 연구팀은 AI 기반 알고리즘으로 환자 개인 종양 조직으로부터 얻어진 복잡한 신호를 해석할 수 있었으며 그 결과 최대 규모인 환자 40명의 종양 조직과 인접한 정상 대장 조직을 사용해 3차원 게놈 지도를 작성할 수 있었다. 또한 DNA 서열정보를 보여주는 전장유전체 지도의 경우 다양한 인종에 대해 생산되고 있고 한국인의 전장유전체 지도 또한 개발되었으나 한국인 3차원 게놈 지도, 특히 종양 조직에 대한 3차원 게놈 지도는 이번 연구에서 최초로 제시됐다.
이번 연구 결과는 국제 학술지, `셀 리포츠(Cell Reports, IF=9.995)'에 7월 13일 자로 출판됐다. (논문명: Spatial and clonality-resolved 3D cancer genome alterations reveal enhancer-hijacking as a potential prognostic marker for colorectal cancer)
서울대학교병원 혈액종양내과 김태유 교수는 “이러한 결과는 개별 암 환자들마다 서로 다르게 나타나는 종양 이질성을 이해하는 데 매우 중요한 요소가 될 수 있으며, 이를 이용한 환자 맞춤형 치료 연구의 시발점이 될 것이다”라고 말했다. 생명과학과 정인경 교수는 “기존의 점돌연변이나 유전체 변이만으로는 설명이 어려운 암 유전체를 3차원 게놈 구조 관점에서 재해독하고 신규 암 타겟을 발굴할 수 있는 수 있는 새로운 접근법을 제시했다”라고 밝혔다.
한편 이번 연구는 과학기술정보통신부와 서경배과학재단의 지원을 받아 수행됐다.
2023.07.24 조회수 8448