%EC%A4%91%EA%B2%AC%EC%97%B0%EA%B5%AC%EC%9E%90
-
 신용카드 두께 플렉서블 리튬이온 배터리 개발
최장욱 교수
우리 대학 EEWS 대학원 최장욱(40) 교수와 한국표준과학연구원 송재용(44) 박사 공동 연구팀은 신용카드보다 얇고 무선 충전이 가능한 플렉서블 리튬이온 배터리를 개발했다고 밝혔다.
연구 성과는 나노과학분야 학술지 ‘나노 레터스(Nano Letters)’ 3월 6일자 온라인 판에 게재됐다.
이번 연구는 모바일 전자기기, 전기 자동차 등 폭넓은 분야의 전원으로 사용되는 리튬이온 배터리가 플렉서블 전자기기에도 적합한 전원으로 개발됐다는 의의를 갖는다.
기존 리튬이온 배터리는 양극, 분리막, 음극을 샌드위치처럼 층층이 쌓는 적층방식이기 때문에 두께를 줄이기 어려웠다. 또한 층 사이에 발생하는 마찰로 인해 구부리기 어렵고, 전극 필름이 벗겨져 성능 유지에 한계가 있었다.
연구팀은 적층이라는 고정관념에서 벗어나 분리막을 없애고 양극과 음극을 평면으로 동일선상에 배열한 뒤, 양극 간 격벽을 둬 리튬이온 배터리에서 발생할 수 있는 합선, 전압강하 등의 현상을 없애는 데 주력했다.
이후 5천 번 이상의 연속 굽힘 실험을 통해 배터리 성능 유지와 더불어 더 유연한 새로운 개념의 전극 구조가 가능함을 확인했다.
플렉서블 배터리는 통합형 스마트 카드, 미용 및 의료용 패치, 영화 ‘아이언 맨’처럼 목소리와 몸짓으로 컴퓨터에 명령할 수 있는 피부 부착형 센서 등에 적용될 수 있다.
더 나아가 연구팀은 이 배터리에 전자기 유도 및 태양전지를 적용해 무선 충전 기술도 함께 개발하는 데 성공했다.
현재는 이 동일 평면상 배터리 기술을 프린팅 기술과 접목해 대량 생산 공정을 개발 중이며, 궁극적으로 반도체, 배터리 등의 전자제품을 3D 프린터로 생산할 수 있는 새 패러다임을 목표로 하고 있다.
최장욱 교수는 “현재 개발된 기술은 피부 부착형 의료용 패치의 전원 역할을 해 패치 기능의 다양화에 기여할 것”이라고 말했다.
이번 연구는 한국연구재단의 중견연구자사업과 국가과학기술연구회 융합실용화 연구사업의 지원을 받아 수행됐다.
□ 사진설명
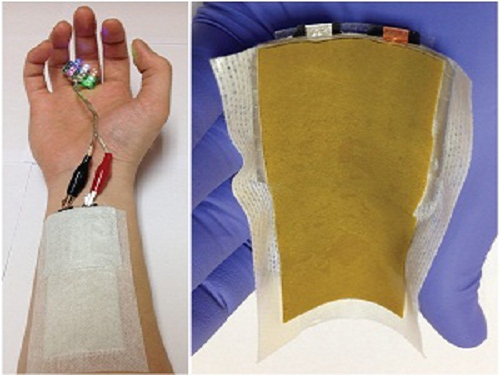
사진 1. 약물 전달 패치와 일체화된 플렉서블 이차전지
사진 2. 플렉서블 배터리 구성도
사진 3. 플렉서블 배터리를 이용해 제작한 스마트카드
2015.03.17 조회수 17144
신용카드 두께 플렉서블 리튬이온 배터리 개발
최장욱 교수
우리 대학 EEWS 대학원 최장욱(40) 교수와 한국표준과학연구원 송재용(44) 박사 공동 연구팀은 신용카드보다 얇고 무선 충전이 가능한 플렉서블 리튬이온 배터리를 개발했다고 밝혔다.
연구 성과는 나노과학분야 학술지 ‘나노 레터스(Nano Letters)’ 3월 6일자 온라인 판에 게재됐다.
이번 연구는 모바일 전자기기, 전기 자동차 등 폭넓은 분야의 전원으로 사용되는 리튬이온 배터리가 플렉서블 전자기기에도 적합한 전원으로 개발됐다는 의의를 갖는다.
기존 리튬이온 배터리는 양극, 분리막, 음극을 샌드위치처럼 층층이 쌓는 적층방식이기 때문에 두께를 줄이기 어려웠다. 또한 층 사이에 발생하는 마찰로 인해 구부리기 어렵고, 전극 필름이 벗겨져 성능 유지에 한계가 있었다.
연구팀은 적층이라는 고정관념에서 벗어나 분리막을 없애고 양극과 음극을 평면으로 동일선상에 배열한 뒤, 양극 간 격벽을 둬 리튬이온 배터리에서 발생할 수 있는 합선, 전압강하 등의 현상을 없애는 데 주력했다.
이후 5천 번 이상의 연속 굽힘 실험을 통해 배터리 성능 유지와 더불어 더 유연한 새로운 개념의 전극 구조가 가능함을 확인했다.
플렉서블 배터리는 통합형 스마트 카드, 미용 및 의료용 패치, 영화 ‘아이언 맨’처럼 목소리와 몸짓으로 컴퓨터에 명령할 수 있는 피부 부착형 센서 등에 적용될 수 있다.
더 나아가 연구팀은 이 배터리에 전자기 유도 및 태양전지를 적용해 무선 충전 기술도 함께 개발하는 데 성공했다.
현재는 이 동일 평면상 배터리 기술을 프린팅 기술과 접목해 대량 생산 공정을 개발 중이며, 궁극적으로 반도체, 배터리 등의 전자제품을 3D 프린터로 생산할 수 있는 새 패러다임을 목표로 하고 있다.
최장욱 교수는 “현재 개발된 기술은 피부 부착형 의료용 패치의 전원 역할을 해 패치 기능의 다양화에 기여할 것”이라고 말했다.
이번 연구는 한국연구재단의 중견연구자사업과 국가과학기술연구회 융합실용화 연구사업의 지원을 받아 수행됐다.
□ 사진설명
사진 1. 약물 전달 패치와 일체화된 플렉서블 이차전지
사진 2. 플렉서블 배터리 구성도
사진 3. 플렉서블 배터리를 이용해 제작한 스마트카드
2015.03.17 조회수 17144 -
 빛을 이용한 약물효소반응 촉진 플랫폼 개발
우리 대학 신소재공학과 박찬범 교수와 생명화학공학과 정기준 교수 연구팀은 빛으로 약물효소반응을 유도할 수 있는 새로운 반응 플랫폼을 개발했다.
연구결과는 지난 12일, 화학분야의 세계적 학술지인 ‘앙게반테 케미’에 후면 표지논문으로 게재됐다.
이 기술을 활용하면 저가의 염료로 고지혈증 등의 심혈관질환 치료제 및 오메프라졸과 같은 위궤양 치료제 등 고부가가치 의약품 생산이 가능할 것으로 보인다.
시토크롬 P450(cytochrome P450)은 생물체 안에서 약물 및 호르몬 등의 대사 과정에서 중요한 산화반응을 수행하는 효소이다. 사람에게 투여되는 약물의 75% 이상의 대사를 담당하고 있기 때문에 신약개발 과정에서 핵심적인 요소로 알려져 있다.
시토크롬 P450의 활성화를 위해선 환원효소로부터 전자를 받아야 하며 전달물질인 NADPH(생물 세포 내의 조효소)가 필요하다. 하지만 NADPH의 높은 가격 때문에 시토크롬 P450의 활용은 실험실 수준에 머무르고 있었으며, 산업적 활용에도 제 역할을 다하지 못했다.
연구팀은 NADPH 대신 빛에 반응하는 감광제인 에오신 Y를 활용해 대장균 기반의 ‘전세포 광-생촉매’ 방법을 개발했다. 저가의 에오신 Y를 빛에 노출시켜 시토크롬 P450의 효소반응을 촉진하여 고가의 대사물질을 생산한다는 원리다.
박 교수는 “이번 연구를 통해 산업적 활용에 제한이 컸던 시토크롬 P450 효소의 활용이 수월해졌다” 며 “우리의 기술은 시토크롬 P450 효소가 고부가가치 의약 물질을 생산하는데 큰 도움을 줄 것이다”라고 말했다.
박찬범, 정기준 교수(교신저자)의 지도아래 박종현 박사과정 학생, 이상하 박사가 주저자로 참여한 이번 연구는 한국연구재단이 추진하는 중견연구자사업과 글로벌프론티어사업, KAIST HRHRP (High Risk High Return Project)의 지원으로 수행됐다.
□ 그림설명
그림1. 빛으로부터 에오신 와이 (eosin Y, EY)를 통해 시토크롬 P450 효소로 전자를 전달하는 모식도
그림2. 연구결과를 설명하는 1월 12일자 ‘앙게반테 케미’ 후면 논문 표지
2015.01.21 조회수 20251
빛을 이용한 약물효소반응 촉진 플랫폼 개발
우리 대학 신소재공학과 박찬범 교수와 생명화학공학과 정기준 교수 연구팀은 빛으로 약물효소반응을 유도할 수 있는 새로운 반응 플랫폼을 개발했다.
연구결과는 지난 12일, 화학분야의 세계적 학술지인 ‘앙게반테 케미’에 후면 표지논문으로 게재됐다.
이 기술을 활용하면 저가의 염료로 고지혈증 등의 심혈관질환 치료제 및 오메프라졸과 같은 위궤양 치료제 등 고부가가치 의약품 생산이 가능할 것으로 보인다.
시토크롬 P450(cytochrome P450)은 생물체 안에서 약물 및 호르몬 등의 대사 과정에서 중요한 산화반응을 수행하는 효소이다. 사람에게 투여되는 약물의 75% 이상의 대사를 담당하고 있기 때문에 신약개발 과정에서 핵심적인 요소로 알려져 있다.
시토크롬 P450의 활성화를 위해선 환원효소로부터 전자를 받아야 하며 전달물질인 NADPH(생물 세포 내의 조효소)가 필요하다. 하지만 NADPH의 높은 가격 때문에 시토크롬 P450의 활용은 실험실 수준에 머무르고 있었으며, 산업적 활용에도 제 역할을 다하지 못했다.
연구팀은 NADPH 대신 빛에 반응하는 감광제인 에오신 Y를 활용해 대장균 기반의 ‘전세포 광-생촉매’ 방법을 개발했다. 저가의 에오신 Y를 빛에 노출시켜 시토크롬 P450의 효소반응을 촉진하여 고가의 대사물질을 생산한다는 원리다.
박 교수는 “이번 연구를 통해 산업적 활용에 제한이 컸던 시토크롬 P450 효소의 활용이 수월해졌다” 며 “우리의 기술은 시토크롬 P450 효소가 고부가가치 의약 물질을 생산하는데 큰 도움을 줄 것이다”라고 말했다.
박찬범, 정기준 교수(교신저자)의 지도아래 박종현 박사과정 학생, 이상하 박사가 주저자로 참여한 이번 연구는 한국연구재단이 추진하는 중견연구자사업과 글로벌프론티어사업, KAIST HRHRP (High Risk High Return Project)의 지원으로 수행됐다.
□ 그림설명
그림1. 빛으로부터 에오신 와이 (eosin Y, EY)를 통해 시토크롬 P450 효소로 전자를 전달하는 모식도
그림2. 연구결과를 설명하는 1월 12일자 ‘앙게반테 케미’ 후면 논문 표지
2015.01.21 조회수 20251 -
 심장세포의 핵심 신호전달경로 스위치 규명
심장근육세포내 베타수용체 신호전달경로의 자극 세기에 따라 세포의 생존과 사멸이라는 상반된 운명이 어떻게 결정되는지 그 근본원리가 우리 학교 연구진에 의해 규명되었다. 향후 심부전을 비롯한 다양한 심장질환의 치료에 활용될 것으로 기대된다.
우리 학교 바이오및뇌공학과 조광현 석좌교수(교신저자)가 주도하고 신성영 박사(제1저자), 이호성 박사과정학생, 강준혁 박사과정학생이 참여하였으며, 광주과학기술원 생명과학부 김도한 교수팀이 공동으로 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약/전략연구)과 바이오·의료기술개발사업 및 KAIST 미래형 시스템헬스케어사업의 지원으로 수행되었고, 연구결과는 네이처(Nature) 자매지인 네이처 커뮤니케이션스(Nature Communications)지에 12월 17일자로 게재되었다. * (논문명) The switching role of β-adrenergic receptor signalling in cell survival or death decision of cardiomyocytes
베타수용체 신호전달경로는 심장근육세포의 생존을 촉진(베타2수용체 매개)하지만 동시에 심장근육세포의 사멸을 유도하기도 하여 심장독성을 유발(베타1수용체 매개)함으로써 심부전 등 다양한 심장질환을 일으킨다. 지금까지 베타수용체 신호전달경로에 의해 조절되는 심장근육세포의 상반된 운명결정과정(생존 혹은 사멸)에 대한 근본 원리를 밝히고자 하는 많은 시도가 있어왔으나 아직 밝혀지지 않았다. ※ 베타수용체(β-adrenergic receptor): 심장근육세포의 세포막에 존재하는 단백질로서 에피네프린이나 노르에피네프린 등의 신경호르몬에 의해 자극받으면 심장근육세포가 더 강하고 빠르게 수축하도록 촉진하는 신호를 전달한다.
연구팀은 대규모 컴퓨터시뮬레이션 분석과 세포생물학 실험의 융합연구인 시스템생물학 연구를 통하여 ERK* 신호전달경로와 ICER** 신호전달경로가 매개하는 피드포워드회로가 심장근육세포의 생존과 사멸을 결정하는 핵심 분자스위치임을 밝혀냈다.
* ERK(Extracellular signal-regulated kinases): 세포생존에 관여하는 신호전달분자 ** ICER(Inducible cAMP early repressor): 세포사멸에 관여하는 신호전달분자
약한 베타수용체의 자극에 대해서는 ERK 신호전달경로가 활성화되고 이로 인하여 Bcl-2*** 단백질의 발현량이 증가되어 심장근육세포의 생존이 촉진되지만, 강한 베타수용체의 자극에 대해서는 ICER 신호전달경로가 활성화되고 Bcl-2 단백질의 발현량이 감소하게 되어 심장근육세포의 사멸이 유발되는 것이다. *** Bcl-2(B-cell lymphoma 2): 세포생존 촉진에 핵심적인 역할을 하는 신호전달분자
또한 연구팀은 시스템생물학적 접근을 통해 실제 심부전 환자에게 널리 사용되는 약물인 베타차단제(β-blocker)****의 작동원리를 밝혀내었다. 심장근육세포에 베타1차단제를 처리하였을 때 강한 베타수용체 자극에서의 Bcl-2 발현량이 증가하고 이로 인하여 심장근육세포의 생존율이 향상되어 세포보호효과가 일어난다는 것을 발견함으로써, 베타차단제의 근본약리기전을 신호전달경로 수준에서 규명하였다. **** 베타차단제(β-blocker): 베타수용체의 활성화를 저해하는 약물이며, 심부전의 진행을 억제시키는 효과가 있어서 임상에서 가장 널리 처방되는 심부전 치료약물이다.
조광현 교수는 “정보기술(IT)과 생명과학(BT)의 융합연구인 시스템생물학 연구를 통해 지금껏 밝혀지지 않았던 베타수용체 신호전달경로에 의해 조절되는 심장근육세포의 상반된 운명결정과정에 대한 핵심 원리를 성공적으로 규명한 것으로 향후 심장근육세포운명의 제어 및 이를 통한 심부전 등의 다양한 심장질환 치료에 널리 활용될 것으로 기대된다.”고 밝혔다.
조광현 교수 연구팀은 IT와 BT가 융합된 시스템생물학 분야를 세계 최초로 개척해왔으며 특히 인체의 복잡한 질병과 관련된 신호전달네트워크의 모델링과 시뮬레이션 분석, 실험적 증명에 관한 혁신적인 연구를 수행해오고 있다. 지금까지 140여편의 국제저널논문을 게재하였으며, 2014년에는 Cell, Science, Nature 자매지에 연이어 연구성과를 게재하였다.
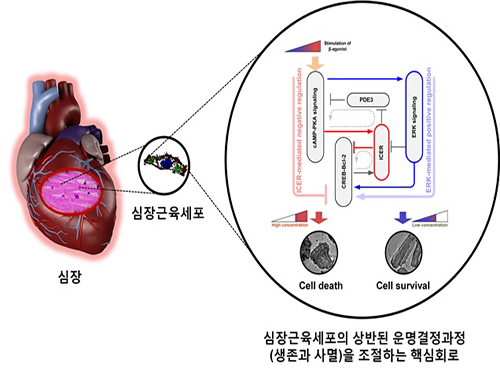
심장근육세포의 상반된 운명결정과정을 조절하는 핵심회로의 규명 및 제어기술 개발: 수학모델링과 대규모 컴퓨터시뮬레이션 분석을 통해 규명된 심장근육세포의 상반된 운명결정과정을 조절하는 핵심회로의 규명. ERK 신호전달경로와 ICER 신호전달경로가 매개하는 피드포워드회로는 심장근육세포의 생존과 사멸을 결정하는 핵심 분자스위치이다. 약한 베타수용체의 자극에 대해서는 ERK 신호전달경로(파란색 화살표)가 활성화되고 이로 인하여 Bcl-2의 발현량이 증가되어 결과적으로 심장근육세포의 생존이 촉진된다. 반면 강한 베타수용체의 자극에 대해서는 ICER 신호전달경로(빨간색 화살표)가 활성화되고, 이로 인해 Bcl-2의 발현량이 감소하게 되어 심장근육세포의 사멸이 유발된다. 이로서 심장근육세포의 사멸을 방지하면서 심장박동의 기능을 유지시킬 수 있는 원천제어기술의 토대가 마련되었다.
2014.12.26 조회수 21280
심장세포의 핵심 신호전달경로 스위치 규명
심장근육세포내 베타수용체 신호전달경로의 자극 세기에 따라 세포의 생존과 사멸이라는 상반된 운명이 어떻게 결정되는지 그 근본원리가 우리 학교 연구진에 의해 규명되었다. 향후 심부전을 비롯한 다양한 심장질환의 치료에 활용될 것으로 기대된다.
우리 학교 바이오및뇌공학과 조광현 석좌교수(교신저자)가 주도하고 신성영 박사(제1저자), 이호성 박사과정학생, 강준혁 박사과정학생이 참여하였으며, 광주과학기술원 생명과학부 김도한 교수팀이 공동으로 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약/전략연구)과 바이오·의료기술개발사업 및 KAIST 미래형 시스템헬스케어사업의 지원으로 수행되었고, 연구결과는 네이처(Nature) 자매지인 네이처 커뮤니케이션스(Nature Communications)지에 12월 17일자로 게재되었다. * (논문명) The switching role of β-adrenergic receptor signalling in cell survival or death decision of cardiomyocytes
베타수용체 신호전달경로는 심장근육세포의 생존을 촉진(베타2수용체 매개)하지만 동시에 심장근육세포의 사멸을 유도하기도 하여 심장독성을 유발(베타1수용체 매개)함으로써 심부전 등 다양한 심장질환을 일으킨다. 지금까지 베타수용체 신호전달경로에 의해 조절되는 심장근육세포의 상반된 운명결정과정(생존 혹은 사멸)에 대한 근본 원리를 밝히고자 하는 많은 시도가 있어왔으나 아직 밝혀지지 않았다. ※ 베타수용체(β-adrenergic receptor): 심장근육세포의 세포막에 존재하는 단백질로서 에피네프린이나 노르에피네프린 등의 신경호르몬에 의해 자극받으면 심장근육세포가 더 강하고 빠르게 수축하도록 촉진하는 신호를 전달한다.
연구팀은 대규모 컴퓨터시뮬레이션 분석과 세포생물학 실험의 융합연구인 시스템생물학 연구를 통하여 ERK* 신호전달경로와 ICER** 신호전달경로가 매개하는 피드포워드회로가 심장근육세포의 생존과 사멸을 결정하는 핵심 분자스위치임을 밝혀냈다.
* ERK(Extracellular signal-regulated kinases): 세포생존에 관여하는 신호전달분자 ** ICER(Inducible cAMP early repressor): 세포사멸에 관여하는 신호전달분자
약한 베타수용체의 자극에 대해서는 ERK 신호전달경로가 활성화되고 이로 인하여 Bcl-2*** 단백질의 발현량이 증가되어 심장근육세포의 생존이 촉진되지만, 강한 베타수용체의 자극에 대해서는 ICER 신호전달경로가 활성화되고 Bcl-2 단백질의 발현량이 감소하게 되어 심장근육세포의 사멸이 유발되는 것이다. *** Bcl-2(B-cell lymphoma 2): 세포생존 촉진에 핵심적인 역할을 하는 신호전달분자
또한 연구팀은 시스템생물학적 접근을 통해 실제 심부전 환자에게 널리 사용되는 약물인 베타차단제(β-blocker)****의 작동원리를 밝혀내었다. 심장근육세포에 베타1차단제를 처리하였을 때 강한 베타수용체 자극에서의 Bcl-2 발현량이 증가하고 이로 인하여 심장근육세포의 생존율이 향상되어 세포보호효과가 일어난다는 것을 발견함으로써, 베타차단제의 근본약리기전을 신호전달경로 수준에서 규명하였다. **** 베타차단제(β-blocker): 베타수용체의 활성화를 저해하는 약물이며, 심부전의 진행을 억제시키는 효과가 있어서 임상에서 가장 널리 처방되는 심부전 치료약물이다.
조광현 교수는 “정보기술(IT)과 생명과학(BT)의 융합연구인 시스템생물학 연구를 통해 지금껏 밝혀지지 않았던 베타수용체 신호전달경로에 의해 조절되는 심장근육세포의 상반된 운명결정과정에 대한 핵심 원리를 성공적으로 규명한 것으로 향후 심장근육세포운명의 제어 및 이를 통한 심부전 등의 다양한 심장질환 치료에 널리 활용될 것으로 기대된다.”고 밝혔다.
조광현 교수 연구팀은 IT와 BT가 융합된 시스템생물학 분야를 세계 최초로 개척해왔으며 특히 인체의 복잡한 질병과 관련된 신호전달네트워크의 모델링과 시뮬레이션 분석, 실험적 증명에 관한 혁신적인 연구를 수행해오고 있다. 지금까지 140여편의 국제저널논문을 게재하였으며, 2014년에는 Cell, Science, Nature 자매지에 연이어 연구성과를 게재하였다.
심장근육세포의 상반된 운명결정과정을 조절하는 핵심회로의 규명 및 제어기술 개발: 수학모델링과 대규모 컴퓨터시뮬레이션 분석을 통해 규명된 심장근육세포의 상반된 운명결정과정을 조절하는 핵심회로의 규명. ERK 신호전달경로와 ICER 신호전달경로가 매개하는 피드포워드회로는 심장근육세포의 생존과 사멸을 결정하는 핵심 분자스위치이다. 약한 베타수용체의 자극에 대해서는 ERK 신호전달경로(파란색 화살표)가 활성화되고 이로 인하여 Bcl-2의 발현량이 증가되어 결과적으로 심장근육세포의 생존이 촉진된다. 반면 강한 베타수용체의 자극에 대해서는 ICER 신호전달경로(빨간색 화살표)가 활성화되고, 이로 인해 Bcl-2의 발현량이 감소하게 되어 심장근육세포의 사멸이 유발된다. 이로서 심장근육세포의 사멸을 방지하면서 심장박동의 기능을 유지시킬 수 있는 원천제어기술의 토대가 마련되었다.
2014.12.26 조회수 21280 -
 다빈치가 르네상스 이후에 태어났다면 모나리자를 어떻게 그렸을까
우리 학교 물리학과 정하웅 교수와 한양대학교 응용물리학과 손승우 교수는 중세부터 사실주의까지 약 1000년에 걸친 서양화 1만 여점의 빅데이터를 복잡계 이론으로 분석해 서양 미술의 변천사를 밝혀냈다. 또 이를 바탕으로 르네상스 시대의 대표 작품인 모나리자를 시대별로 재구성했다.
연구결과는 세계적인 과학저널 네이처(Nature)가 발행하는 ‘사이언티픽 리포트(Scientific Reports)’ 11일자 온라인판에 실렸으며 리서치 하이라이트로 선정되어 네이처 홈페이지 메인 화면에 소개되기도 했다.
최근 빅데이터가 관심을 받으면서 과학자들은 예술·인문학 자료를 전산화해 분석하려는 시도가 많이 있다. 이 같은 자료는 방대하고 복잡해서 다루기가 쉽지 않다. 연구자들은 빅데이터에서 질서를 찾기 위해 복잡계(Complex Systems) 과학 방법론을 이용하며 이를 ‘데이터 과학’이라고 한다.
그동안 회화에 사용된 물감의 구성 성분, 연대측정, 회화의 진위여부를 정량적으로 판별하는 방법 등에 관한 연구결과는 꾸준히 있었다. 하지만 서양 미술사 전반을 아우르는 대규모 분석에는 데이터가 충분하지 않았다.
연구팀은 헝가리 부다페스트 물리학 컴퓨터 네트워킹 연구센터(Computer Networking Centre of the Wigner Research Centre for Physics)에서 운영하는 온라인 갤러리에서 중세부터 19세기까지 디지털 형태의 서양회화 1만여 점을 모은 데이터를 기반으로 서양 미술을 객관적으로 분석할 수 있었다.
연구팀은 물리학에서 사용하는 상관 함수를 온라인 갤러리에서 취합된 서양 미술의 빅데이터에 적용해 분석한 결과 시간이 흐를수록 명암대비 효과가 점점 높아지는 경향이 있다는 사실을 밝혀냈다.
연구팀은 여기서 사용한 상관 함수를 잭슨 폴록의 드립 페인팅에 적용한 결과, 공간적인 명암대비 효과가 거의 없어 무작위로 만든 그림에 상당히 가깝다는 것을 분석해내기도 했다.
이와 함께 이 기간 동안 서양미술은 그림 속 물체의 윤곽선이 모호해지다 낭만주의 시대 무렵 다시 뚜렷해지는 변화가 있었다.
아울러 중세 시대에는 색상을 다양하게 사용하지 않았고 정치 및 종교적인 이유로 특정 염료만을 선호했다. 같은 이유로 당시에는 색을 직접 혼합하지 않고 오직 덧칠로만 다양한 색을 표현했다. 즉, 연구팀은 염료와 채색 방식으로 인한 중세 시대 색상 표현의 한계와 그 이후 변화를 분석해냈다.
정하웅 교수는 “물질세계의 복잡성에 대한 연구는 자연과학에서 오래된 주요 관심사였지만, 예술 및 인문사회분야와 관련한 체계적인 복잡성 연구는 인터넷 대중화 이후의 일”이라며 “이번 연구는 물질세계의 복잡성을 다루던 방법으로 인류의 귀중한 문화유산인 회화에서 숨은 복잡성을 찾아 구체적인 숫자로 제시했다는데 의의가 있다”고 말했다.
손승우 교수는 “학문 사이의 통섭은 이제 융·복합이라는 키워드로 우리 사회에 자리매김하고 있다”며 “학문간 더욱 활발한 대화를 통해 미술 분야를 넘어 예술 및 인문사회 분야에 숨겨진 복잡성을 더욱 폭넓게 이해하는 것이 필요하다”고 설명했다.
미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업의 지원으로 수행한 이번 연구는 KAIST와 한양대 교수진의 지도아래 KAIST 물리학과 김영호(28) 박사과정 학생이 주도했다.
동영상 링크 http://youtu.be/SFo0h1EU2aw
[자료 그림] 중세 회화와 드립 페인팅 비교: a은 중세 회화로 구성한 밝기 표면, b은 잭슨 폴록의 드립 페인팅 작품으로 구성한 밝기 표면이다. 각 픽셀의 밝기를 픽셀 위치의 높이로 두어 표면을 구성하고 각 밝기 표면에서 거리에 따른 평균 밝기차이 상관함수를 구했다. c와 d에서 빨간색 점은 그림에서 거리에 따른 평균 밝기차이 상관함수, 파란색 점은 그림을 무작위로 섞어서 만든 이미지에서 거리에 따른 평균 밝기차이 상관함수이다. 중세 회화와 다르게 잭슨 폴록의 드립 페인팅은 무작위로 섞어서 만든 이미지와 거리에 따른 평균 밝기차이 상관함수가 거의 차이가 없다. © 2014 The Polock-Krasner Foundation/ARS, NY - SACK, Seoul
1. 르네상스 시대의 대표 작품인 모나리자를 시대별 스타일에 맞게 재구성
2. 각 그림으로 표면을 구성하고 명암 대비 기법의 강도를 측정하는 짧은 영상. 선별한 그림을 중심으로 명암 대비 기법의 강도가 시대에 따라 증가하는 경향을 영상에서 확인할 수 있다.
3. 회화에서 밝기 표면을 구성하는 방법
4. 네이처 홈페이지(12월 11일)
2014.12.15 조회수 17263
다빈치가 르네상스 이후에 태어났다면 모나리자를 어떻게 그렸을까
우리 학교 물리학과 정하웅 교수와 한양대학교 응용물리학과 손승우 교수는 중세부터 사실주의까지 약 1000년에 걸친 서양화 1만 여점의 빅데이터를 복잡계 이론으로 분석해 서양 미술의 변천사를 밝혀냈다. 또 이를 바탕으로 르네상스 시대의 대표 작품인 모나리자를 시대별로 재구성했다.
연구결과는 세계적인 과학저널 네이처(Nature)가 발행하는 ‘사이언티픽 리포트(Scientific Reports)’ 11일자 온라인판에 실렸으며 리서치 하이라이트로 선정되어 네이처 홈페이지 메인 화면에 소개되기도 했다.
최근 빅데이터가 관심을 받으면서 과학자들은 예술·인문학 자료를 전산화해 분석하려는 시도가 많이 있다. 이 같은 자료는 방대하고 복잡해서 다루기가 쉽지 않다. 연구자들은 빅데이터에서 질서를 찾기 위해 복잡계(Complex Systems) 과학 방법론을 이용하며 이를 ‘데이터 과학’이라고 한다.
그동안 회화에 사용된 물감의 구성 성분, 연대측정, 회화의 진위여부를 정량적으로 판별하는 방법 등에 관한 연구결과는 꾸준히 있었다. 하지만 서양 미술사 전반을 아우르는 대규모 분석에는 데이터가 충분하지 않았다.
연구팀은 헝가리 부다페스트 물리학 컴퓨터 네트워킹 연구센터(Computer Networking Centre of the Wigner Research Centre for Physics)에서 운영하는 온라인 갤러리에서 중세부터 19세기까지 디지털 형태의 서양회화 1만여 점을 모은 데이터를 기반으로 서양 미술을 객관적으로 분석할 수 있었다.
연구팀은 물리학에서 사용하는 상관 함수를 온라인 갤러리에서 취합된 서양 미술의 빅데이터에 적용해 분석한 결과 시간이 흐를수록 명암대비 효과가 점점 높아지는 경향이 있다는 사실을 밝혀냈다.
연구팀은 여기서 사용한 상관 함수를 잭슨 폴록의 드립 페인팅에 적용한 결과, 공간적인 명암대비 효과가 거의 없어 무작위로 만든 그림에 상당히 가깝다는 것을 분석해내기도 했다.
이와 함께 이 기간 동안 서양미술은 그림 속 물체의 윤곽선이 모호해지다 낭만주의 시대 무렵 다시 뚜렷해지는 변화가 있었다.
아울러 중세 시대에는 색상을 다양하게 사용하지 않았고 정치 및 종교적인 이유로 특정 염료만을 선호했다. 같은 이유로 당시에는 색을 직접 혼합하지 않고 오직 덧칠로만 다양한 색을 표현했다. 즉, 연구팀은 염료와 채색 방식으로 인한 중세 시대 색상 표현의 한계와 그 이후 변화를 분석해냈다.
정하웅 교수는 “물질세계의 복잡성에 대한 연구는 자연과학에서 오래된 주요 관심사였지만, 예술 및 인문사회분야와 관련한 체계적인 복잡성 연구는 인터넷 대중화 이후의 일”이라며 “이번 연구는 물질세계의 복잡성을 다루던 방법으로 인류의 귀중한 문화유산인 회화에서 숨은 복잡성을 찾아 구체적인 숫자로 제시했다는데 의의가 있다”고 말했다.
손승우 교수는 “학문 사이의 통섭은 이제 융·복합이라는 키워드로 우리 사회에 자리매김하고 있다”며 “학문간 더욱 활발한 대화를 통해 미술 분야를 넘어 예술 및 인문사회 분야에 숨겨진 복잡성을 더욱 폭넓게 이해하는 것이 필요하다”고 설명했다.
미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업의 지원으로 수행한 이번 연구는 KAIST와 한양대 교수진의 지도아래 KAIST 물리학과 김영호(28) 박사과정 학생이 주도했다.
동영상 링크 http://youtu.be/SFo0h1EU2aw
[자료 그림] 중세 회화와 드립 페인팅 비교: a은 중세 회화로 구성한 밝기 표면, b은 잭슨 폴록의 드립 페인팅 작품으로 구성한 밝기 표면이다. 각 픽셀의 밝기를 픽셀 위치의 높이로 두어 표면을 구성하고 각 밝기 표면에서 거리에 따른 평균 밝기차이 상관함수를 구했다. c와 d에서 빨간색 점은 그림에서 거리에 따른 평균 밝기차이 상관함수, 파란색 점은 그림을 무작위로 섞어서 만든 이미지에서 거리에 따른 평균 밝기차이 상관함수이다. 중세 회화와 다르게 잭슨 폴록의 드립 페인팅은 무작위로 섞어서 만든 이미지와 거리에 따른 평균 밝기차이 상관함수가 거의 차이가 없다. © 2014 The Polock-Krasner Foundation/ARS, NY - SACK, Seoul
1. 르네상스 시대의 대표 작품인 모나리자를 시대별 스타일에 맞게 재구성
2. 각 그림으로 표면을 구성하고 명암 대비 기법의 강도를 측정하는 짧은 영상. 선별한 그림을 중심으로 명암 대비 기법의 강도가 시대에 따라 증가하는 경향을 영상에서 확인할 수 있다.
3. 회화에서 밝기 표면을 구성하는 방법
4. 네이처 홈페이지(12월 11일)
2014.12.15 조회수 17263 -
 활성산소에 대한 세포반응 원리 규명 - 암과 노화 극복의 실마리 제공
우리 학교 연구진이 활성산소* 농도에 따라 세포의 운명이 어떻게 달라지는지 그 원리를 규명해냈다. 활성산소는 세포의 성장을 돕는 한편 세포손상을 일으켜 노화 등을 촉진하는 것으로 알려져 있었다. 이처럼 세포를 죽게도 하고 살리기도 하는 활성산소의 상반된 역할을 설명할 수 있는 실마리가 찾아진 것이다. * 활성산소(ROS) : 인체 대사활동에 의해 발생되는 산소 부산물로 세포의 성장과 분화를 돕고 염증을 억제하는 유익한 기능을 하는 한편 세포손상을 유발하여 암, 당뇨 등 여러 질병을 일으키고, 노화를 촉진시키는 것으로 알려져 있다.
우리 대학 바이오및뇌공학과 조광현 석좌교수(교신저자)가 주도하고 이호성 박사과정 연구원(제1저자), 황채영 박사(공동 제1저자), 신성영 박사가 참여하였으며, 한국생명공학연구원 권기선 박사(교신저자)가 공동으로 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)과 바이오·의료기술개발사업의 지원으로 수행되었고 연구결과는 사이언스(Science) 자매지인 사이언스 시그널링(Science Signaling)지 6월 3일자에 게재되었다. * 논문명 : MLK3 is part of a feedback mechanism that regulates different cellular responses to reactive oxygen species
연구팀은 활성산소의 농도에 따라 세포의 증식 또는 세포의 사멸이라는 운명을 가르는 분자스위치가 MLK3* 중심의 피드백회로임을 알아냈다. * MLK3 : 루신-지퍼 구조의 인산화효소로 세포 사멸에 관여하는 단백질이다.
적절한 스트레스가 주어지는 환경에서는 세포가 분열하도록 신호를 보내는 반면 과도한 스트레스 상황에서는 오히려 세포분열을 멈추고 세포가 죽도록 유도하는 결정적 단백질회로가 밝혀짐에 따라 향후 활성산소와 관련된 인체질환 연구의 실마리가 될 것으로 기대된다.
연구팀은 활성산소 농도가 낮을 때는 세포증식에 관여하는 ERK* 단백질이 활성화되는 반면 활성산소 농도가 높아지면 세포사멸에 관여하는 JNK** 단백질이 활성화 되는 것을 알아냈다.
* ERK(Extracellular signal-regulated kinases) : 세포의 생존 및 증식에 관여하는 대표적인 신호전달 분자 ** JNK(c-Jun N-terminal kinases) : 세포의 스트레스 반응 및 사멸에 관여하는 대표적인 신호전달 분자
나아가 수학모델링과 컴퓨터시뮬레이션 분석, 그리고 분자세포생물학 실험을 융합한 시스템생물학 연구를 통해 MLK3 중심의 피드백회로가 활성산소에 대한 ERK와 JNK 경로 간의 신호흐름 균형을 조절하여 세포 반응을 결정하는 핵심적인 분자스위치임을 밝혀내었다.
조 교수는 “IT와 BT의 융합연구인 시스템생물학 연구를 통해 수수께끼로 남아있던 활성산소에 대한 상반된 세포반응의 원리를 규명한 것으로 향후 활성산소로 인한 노화나 암을 극복하기 위한 연구에 활용될 것으로 기대된다”고 밝혔다.
연구 개요도. (A, B) 낮은 농도의 활성산소에 대해서는 세포 증식에 관여하는 단백질인 ERK가 높은 활성도를 보이는 반면, 높은 농도의 활성산소에 대해서는 세포 사멸에 관여하는 단백질인 JNK가 높은 활성도를 보인다는 것을 실험을 통해 확인하였다. 이 실험 결과는 ERK와 JNK가 활성산소의 농도에 따른 상반된 세포 반응을 유발할 수 있음을 시사한다. (C) 대규모 컴퓨터 시뮬레이션 분석을 통해 MLK3을 매개하는 양성피드백 회로와 MKPs를 통한 ERK와 JNK 간 상호소통이 활성산소의 농도에 따른 ERK와 JNK의 상반된 활성화를 일으키는 핵심회로임을 밝혀내었다. (D) MLK3을 매개하는 양성피드백회로는 활성산소에 대한 ERK와 JNK 경로 간의 신호흐름 균형을 조절하여 세포 반응을 결정하는 분자스위치 역할을 한다.
2014.06.09 조회수 20881
활성산소에 대한 세포반응 원리 규명 - 암과 노화 극복의 실마리 제공
우리 학교 연구진이 활성산소* 농도에 따라 세포의 운명이 어떻게 달라지는지 그 원리를 규명해냈다. 활성산소는 세포의 성장을 돕는 한편 세포손상을 일으켜 노화 등을 촉진하는 것으로 알려져 있었다. 이처럼 세포를 죽게도 하고 살리기도 하는 활성산소의 상반된 역할을 설명할 수 있는 실마리가 찾아진 것이다. * 활성산소(ROS) : 인체 대사활동에 의해 발생되는 산소 부산물로 세포의 성장과 분화를 돕고 염증을 억제하는 유익한 기능을 하는 한편 세포손상을 유발하여 암, 당뇨 등 여러 질병을 일으키고, 노화를 촉진시키는 것으로 알려져 있다.
우리 대학 바이오및뇌공학과 조광현 석좌교수(교신저자)가 주도하고 이호성 박사과정 연구원(제1저자), 황채영 박사(공동 제1저자), 신성영 박사가 참여하였으며, 한국생명공학연구원 권기선 박사(교신저자)가 공동으로 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)과 바이오·의료기술개발사업의 지원으로 수행되었고 연구결과는 사이언스(Science) 자매지인 사이언스 시그널링(Science Signaling)지 6월 3일자에 게재되었다. * 논문명 : MLK3 is part of a feedback mechanism that regulates different cellular responses to reactive oxygen species
연구팀은 활성산소의 농도에 따라 세포의 증식 또는 세포의 사멸이라는 운명을 가르는 분자스위치가 MLK3* 중심의 피드백회로임을 알아냈다. * MLK3 : 루신-지퍼 구조의 인산화효소로 세포 사멸에 관여하는 단백질이다.
적절한 스트레스가 주어지는 환경에서는 세포가 분열하도록 신호를 보내는 반면 과도한 스트레스 상황에서는 오히려 세포분열을 멈추고 세포가 죽도록 유도하는 결정적 단백질회로가 밝혀짐에 따라 향후 활성산소와 관련된 인체질환 연구의 실마리가 될 것으로 기대된다.
연구팀은 활성산소 농도가 낮을 때는 세포증식에 관여하는 ERK* 단백질이 활성화되는 반면 활성산소 농도가 높아지면 세포사멸에 관여하는 JNK** 단백질이 활성화 되는 것을 알아냈다.
* ERK(Extracellular signal-regulated kinases) : 세포의 생존 및 증식에 관여하는 대표적인 신호전달 분자 ** JNK(c-Jun N-terminal kinases) : 세포의 스트레스 반응 및 사멸에 관여하는 대표적인 신호전달 분자
나아가 수학모델링과 컴퓨터시뮬레이션 분석, 그리고 분자세포생물학 실험을 융합한 시스템생물학 연구를 통해 MLK3 중심의 피드백회로가 활성산소에 대한 ERK와 JNK 경로 간의 신호흐름 균형을 조절하여 세포 반응을 결정하는 핵심적인 분자스위치임을 밝혀내었다.
조 교수는 “IT와 BT의 융합연구인 시스템생물학 연구를 통해 수수께끼로 남아있던 활성산소에 대한 상반된 세포반응의 원리를 규명한 것으로 향후 활성산소로 인한 노화나 암을 극복하기 위한 연구에 활용될 것으로 기대된다”고 밝혔다.
연구 개요도. (A, B) 낮은 농도의 활성산소에 대해서는 세포 증식에 관여하는 단백질인 ERK가 높은 활성도를 보이는 반면, 높은 농도의 활성산소에 대해서는 세포 사멸에 관여하는 단백질인 JNK가 높은 활성도를 보인다는 것을 실험을 통해 확인하였다. 이 실험 결과는 ERK와 JNK가 활성산소의 농도에 따른 상반된 세포 반응을 유발할 수 있음을 시사한다. (C) 대규모 컴퓨터 시뮬레이션 분석을 통해 MLK3을 매개하는 양성피드백 회로와 MKPs를 통한 ERK와 JNK 간 상호소통이 활성산소의 농도에 따른 ERK와 JNK의 상반된 활성화를 일으키는 핵심회로임을 밝혀내었다. (D) MLK3을 매개하는 양성피드백회로는 활성산소에 대한 ERK와 JNK 경로 간의 신호흐름 균형을 조절하여 세포 반응을 결정하는 분자스위치 역할을 한다.
2014.06.09 조회수 20881 -
 대장조직의 숨겨진 암발생 억제 메커니즘 규명
KAIST 연구진이 대장조직에 숨겨진 암발생 억제 메커니즘을 규명해냈다. 대장조직에 내재된 방어 메커니즘이 밝혀짐에 따라 대장암 발병에 대한 이해를 돕는 계기가 될 것으로 기대된다.
우리 학교 바이오및뇌공학과 조광현 석좌교수(교신저자)가 주도하고 송제훈 박사과정 연구원(제1저자)이 참여하였으며, 영국 암연구소 오웬 삼손 박사와 데이비드 휴웰, 레이첼 리지웨이, 아일랜드 연구소 보리스 콜로덴코, 월터 콜치 박사가 참여한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약연구)의 지원으로 수행되었고 연구결과는 셀(Cell) 자매지 셀 리포트(Cell Reports)지 온라인판 3월 28일자에 게재되었다.
* 논문명 : The APC network regulates the removal of mutated cells from colonic crypts
생명체는 손상된 조직을 스스로 복구할 수 있지만 복구를 위한 세포분열 과정에서 암을 일으킬 수 있는 유전자 변이가 생길 수 있다. 이는 빠른 세포분열 속도와 소화과정에서의 독성물질 때문에 유전자 변이 확률이 높은 대장의 장샘*에서 특히 문제가 된다.
* 장샘(crypt) : 대장 표면을 형성하는 약 2000여개의 세포로 구성된 동굴모양의 상피 연구팀은 유전자 변이로 발암 가능성이 높아진 세포를 대장의 장샘에서 빨리 내보내는 방식으로 대장조직이 빠르고 빈번한 조직재생과정에서 암 발생을 억제한다는 것을 알아냈다. 변이된 세포의 장샘 체류시간을 줄여 비정상적 세포분열을 억제하는 방어 메커니즘이 대장에 내재되어 있다는 것이다.
수학모델을 만들고 이에 대한 방대한 컴퓨터 시뮬레이션 분석을 수행한 결과 유전자 변이에 의해 윈트신호전달*이 강화된 변이세포는 정상세포에 비해 접착력이 높아지면서 장샘의 위쪽으로 더욱 빠르게 이동, 장샘을 벗어나 장내로 배출되기 쉬운 것으로 나타났다.
* 윈트 신호전달(Wnt Signaling) : 세포의 증식과 분화에 관여하는 신호전달 경로로 배아발달이나 성체조직의 항상성 관리에 특히 중요하다. 세포 외부에서 윈트 신호가 들어오면 베타 카테닌을 분해시켜 농도를 낮게 유지해 주는 분해복합체가 억제되면서 세포증식을 돕는 표적 유전자들이 발현되어 세포증식이 일어나게 된다.
유전자 변이로 윈트 신호전달회로의 핵심인자인 베타 카테닌이 분해되지 못하면 축적된 베타 카테닌이 세포증식을 활성화시키는 한편세포 접착력을 높이게 되는데, 장샘 조직의 특수한 환경과 비슷한 접착력을 가진 세포들이 모이려는 성질로 인해 결국 변이된 세포를 배출시켜 조직의 항상성을 유지한다는 것이다.
실제 생쥐모델에서도 비정상적인 장샘 조직의 경우 증식이 활발한 세포가 오히려 느리게 이동하는 것으로 나타나 이같은 시뮬레이션 결과를 확인할 수 있었다.
조 교수는 “본 연구는 컴퓨터 시뮬레이션으로 다세포 생명체가 비정상적 세포 변이에도 불구하고 조직의 항상성을 유지하도록 정교하게 설계되어 있음을 규명한 것으로 IT와 BT의 융합연구인 시스템생물학 연구를 통해 복잡한 생명현상의 숨겨진 원리를 파악할 수 있음을 보인 것” 이라고 밝혔다.
이 연구를 통해 대장의 장샘조직이 조직 내 암의 진화를 애초에 억제할 수 있는 메커니즘을 내재하고 있다는 놀라운 사실을 밝힘으로써 대장암 발생에 대한 이해를 한 단계 높이게 되었다. 또한 이번 연구결과는 대장암을 치료하기 위한 신약개발의 개발 방향에 대한 새로운 통찰을 제시하였다
주요그림 1 설명.
연구개요 모식도: 세포의 자가복구는 다세포생명체가 손상된 조직을 재생하기 위한 필수적인 과정이지만동시에 암을 일으킬 수 있는 체세포 변이의 위험성을 수반한다. 그렇다면 어떻게 이런 딜레마가 생체조직 내에서 해결될 수 있는 것인가?
이 문제는 재생속도가 빠르고 다양한 변이인자에 노출이 많은 대장조직에서 특히 중요하다. 연구팀은 대장 장샘의 세포증식과 이동에 관한 수학모델의 대규모 컴퓨터시뮬레이션과 생물학 시험을 결합한 시스템생물학(Systems Biology) 연구를 통해 그 분자적 메커니즘을 최초로 규명하였다. 장샘 조직 상단으로 이동하는 단일세포의 동역학 특성을 분석함으로써 암의 발생을 방지하는 장샘의 숨겨진 메커니즘을 밝힌 것이다. 그림은 실험용 생쥐에서 추출한 대장조직의 현미경 사진 위에 규명한 메커니즘을 그림으로 도식화 한 것이다.
주요그림 2 설명. 컴퓨터시뮬레이션 결과와 동물모델 실험을 통한 검증: (A) 야생형 장샘(첫째 행) 및 에이피시 유전자 변이된 장샘(둘째 행), 베타카테닌 유전자 변이된 장샘(셋째 행)에서, 이질적 세포군집에 의한 세포 재배치의 효과를 조사하는 컴퓨터 시뮬레이션이 수행되었다. 여기서 이질성은 균등하게 취해진 100개의 표본세포(첫째와 둘째 열)에 대해서 가해진 랜덤 노이즈를 노이즈가 없는 기준 분자 프로파일(파랑 파선)에 추가함으로써 모사된다. 표본세포들의 초기위치들은 세포 재배치에 의해서 최종위치로 변경된다. 이러한 세포재배치가 가져오는 윈트신호전달 및 세포접착의 분포(셋째와 네째 열)가 변화되는 양상이 조사되었다. 빨강 점 및 초록 점들은 기준 분자 프로파일에 대한 양과 음의 편차를 각각 가리키고, 빨강 및 초록 화살표들은 빨강과 초록 점들의 이동 방향을 각각 가리킨다. (B,C) 동형 에이피시 유전자 변이와 동형 및 이형 베타카테닌 변이들을 가지도록 유전자 조작된 생체모델(실험용 마우스)을 사용하였다(B,C). APCfl/fl(동형) 및 β-cateninexon3/+(이형), β-cateninexon3/exon3(동형) 유전자변이 실험용 마우스 (B, 첫째 행)의 대장 조직에 대해서, BrDU주입 후 2시간 이후에 BrDU 양성으로 마크된 세포들은 장샘의 증식영역(주로 아랫부분)에 한정된다. BrDU 주입 후 48시간 이후 장샘의 BrDU양성 세포들은 장샘의 윗쪽 방향으로 이동하였음을 가리킨다(B, 둘째 열). 에이피시 유전자 변이의 경우에는 동형 변이를 가진 생체모델이 사용되었다 (C, 둘째 열). 베타카테닌 변이의 경우에는 이형 변이(C, 셋째 열) 및 동형 변이(C, 넷째 열)를 가진 생체모델이 사용되었다. 본 연구팀은 BrDU 주입 후 2시간 및 48시간 후 BrDU가 마크된 세포들을 관측하였다. BrDU가 주입 후 2시간 이전에 DNA내에 포함되어지기 때문에 2시간에서의 BrDU마크는 증식영역의 위치를 가리킨다. BrDU 주입 후 48시간에서 장샘 내 세포의 이동과 증식이 관찰되었다. 본 연구팀은 증식성 세포들의 위치와 개수를 정량화하였고(C, 좌측) BrDU 표식 된 세포군집의 이동을 측정하기 위하여 누적빈도를 계산하였다(C, 우측). (C)의 화살표는 BrDU 표식된 세포군집의 이동거리를 가리킨다. 표본 마우스마다 50개의 ½장샘이 기록되었는데, 여기서 유전자 형마다 적어도 3개의 다른 실험용 마우스가 사용되었다.
2014.04.02 조회수 22248
대장조직의 숨겨진 암발생 억제 메커니즘 규명
KAIST 연구진이 대장조직에 숨겨진 암발생 억제 메커니즘을 규명해냈다. 대장조직에 내재된 방어 메커니즘이 밝혀짐에 따라 대장암 발병에 대한 이해를 돕는 계기가 될 것으로 기대된다.
우리 학교 바이오및뇌공학과 조광현 석좌교수(교신저자)가 주도하고 송제훈 박사과정 연구원(제1저자)이 참여하였으며, 영국 암연구소 오웬 삼손 박사와 데이비드 휴웰, 레이첼 리지웨이, 아일랜드 연구소 보리스 콜로덴코, 월터 콜치 박사가 참여한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약연구)의 지원으로 수행되었고 연구결과는 셀(Cell) 자매지 셀 리포트(Cell Reports)지 온라인판 3월 28일자에 게재되었다.
* 논문명 : The APC network regulates the removal of mutated cells from colonic crypts
생명체는 손상된 조직을 스스로 복구할 수 있지만 복구를 위한 세포분열 과정에서 암을 일으킬 수 있는 유전자 변이가 생길 수 있다. 이는 빠른 세포분열 속도와 소화과정에서의 독성물질 때문에 유전자 변이 확률이 높은 대장의 장샘*에서 특히 문제가 된다.
* 장샘(crypt) : 대장 표면을 형성하는 약 2000여개의 세포로 구성된 동굴모양의 상피 연구팀은 유전자 변이로 발암 가능성이 높아진 세포를 대장의 장샘에서 빨리 내보내는 방식으로 대장조직이 빠르고 빈번한 조직재생과정에서 암 발생을 억제한다는 것을 알아냈다. 변이된 세포의 장샘 체류시간을 줄여 비정상적 세포분열을 억제하는 방어 메커니즘이 대장에 내재되어 있다는 것이다.
수학모델을 만들고 이에 대한 방대한 컴퓨터 시뮬레이션 분석을 수행한 결과 유전자 변이에 의해 윈트신호전달*이 강화된 변이세포는 정상세포에 비해 접착력이 높아지면서 장샘의 위쪽으로 더욱 빠르게 이동, 장샘을 벗어나 장내로 배출되기 쉬운 것으로 나타났다.
* 윈트 신호전달(Wnt Signaling) : 세포의 증식과 분화에 관여하는 신호전달 경로로 배아발달이나 성체조직의 항상성 관리에 특히 중요하다. 세포 외부에서 윈트 신호가 들어오면 베타 카테닌을 분해시켜 농도를 낮게 유지해 주는 분해복합체가 억제되면서 세포증식을 돕는 표적 유전자들이 발현되어 세포증식이 일어나게 된다.
유전자 변이로 윈트 신호전달회로의 핵심인자인 베타 카테닌이 분해되지 못하면 축적된 베타 카테닌이 세포증식을 활성화시키는 한편세포 접착력을 높이게 되는데, 장샘 조직의 특수한 환경과 비슷한 접착력을 가진 세포들이 모이려는 성질로 인해 결국 변이된 세포를 배출시켜 조직의 항상성을 유지한다는 것이다.
실제 생쥐모델에서도 비정상적인 장샘 조직의 경우 증식이 활발한 세포가 오히려 느리게 이동하는 것으로 나타나 이같은 시뮬레이션 결과를 확인할 수 있었다.
조 교수는 “본 연구는 컴퓨터 시뮬레이션으로 다세포 생명체가 비정상적 세포 변이에도 불구하고 조직의 항상성을 유지하도록 정교하게 설계되어 있음을 규명한 것으로 IT와 BT의 융합연구인 시스템생물학 연구를 통해 복잡한 생명현상의 숨겨진 원리를 파악할 수 있음을 보인 것” 이라고 밝혔다.
이 연구를 통해 대장의 장샘조직이 조직 내 암의 진화를 애초에 억제할 수 있는 메커니즘을 내재하고 있다는 놀라운 사실을 밝힘으로써 대장암 발생에 대한 이해를 한 단계 높이게 되었다. 또한 이번 연구결과는 대장암을 치료하기 위한 신약개발의 개발 방향에 대한 새로운 통찰을 제시하였다
주요그림 1 설명.
연구개요 모식도: 세포의 자가복구는 다세포생명체가 손상된 조직을 재생하기 위한 필수적인 과정이지만동시에 암을 일으킬 수 있는 체세포 변이의 위험성을 수반한다. 그렇다면 어떻게 이런 딜레마가 생체조직 내에서 해결될 수 있는 것인가?
이 문제는 재생속도가 빠르고 다양한 변이인자에 노출이 많은 대장조직에서 특히 중요하다. 연구팀은 대장 장샘의 세포증식과 이동에 관한 수학모델의 대규모 컴퓨터시뮬레이션과 생물학 시험을 결합한 시스템생물학(Systems Biology) 연구를 통해 그 분자적 메커니즘을 최초로 규명하였다. 장샘 조직 상단으로 이동하는 단일세포의 동역학 특성을 분석함으로써 암의 발생을 방지하는 장샘의 숨겨진 메커니즘을 밝힌 것이다. 그림은 실험용 생쥐에서 추출한 대장조직의 현미경 사진 위에 규명한 메커니즘을 그림으로 도식화 한 것이다.
주요그림 2 설명. 컴퓨터시뮬레이션 결과와 동물모델 실험을 통한 검증: (A) 야생형 장샘(첫째 행) 및 에이피시 유전자 변이된 장샘(둘째 행), 베타카테닌 유전자 변이된 장샘(셋째 행)에서, 이질적 세포군집에 의한 세포 재배치의 효과를 조사하는 컴퓨터 시뮬레이션이 수행되었다. 여기서 이질성은 균등하게 취해진 100개의 표본세포(첫째와 둘째 열)에 대해서 가해진 랜덤 노이즈를 노이즈가 없는 기준 분자 프로파일(파랑 파선)에 추가함으로써 모사된다. 표본세포들의 초기위치들은 세포 재배치에 의해서 최종위치로 변경된다. 이러한 세포재배치가 가져오는 윈트신호전달 및 세포접착의 분포(셋째와 네째 열)가 변화되는 양상이 조사되었다. 빨강 점 및 초록 점들은 기준 분자 프로파일에 대한 양과 음의 편차를 각각 가리키고, 빨강 및 초록 화살표들은 빨강과 초록 점들의 이동 방향을 각각 가리킨다. (B,C) 동형 에이피시 유전자 변이와 동형 및 이형 베타카테닌 변이들을 가지도록 유전자 조작된 생체모델(실험용 마우스)을 사용하였다(B,C). APCfl/fl(동형) 및 β-cateninexon3/+(이형), β-cateninexon3/exon3(동형) 유전자변이 실험용 마우스 (B, 첫째 행)의 대장 조직에 대해서, BrDU주입 후 2시간 이후에 BrDU 양성으로 마크된 세포들은 장샘의 증식영역(주로 아랫부분)에 한정된다. BrDU 주입 후 48시간 이후 장샘의 BrDU양성 세포들은 장샘의 윗쪽 방향으로 이동하였음을 가리킨다(B, 둘째 열). 에이피시 유전자 변이의 경우에는 동형 변이를 가진 생체모델이 사용되었다 (C, 둘째 열). 베타카테닌 변이의 경우에는 이형 변이(C, 셋째 열) 및 동형 변이(C, 넷째 열)를 가진 생체모델이 사용되었다. 본 연구팀은 BrDU 주입 후 2시간 및 48시간 후 BrDU가 마크된 세포들을 관측하였다. BrDU가 주입 후 2시간 이전에 DNA내에 포함되어지기 때문에 2시간에서의 BrDU마크는 증식영역의 위치를 가리킨다. BrDU 주입 후 48시간에서 장샘 내 세포의 이동과 증식이 관찰되었다. 본 연구팀은 증식성 세포들의 위치와 개수를 정량화하였고(C, 좌측) BrDU 표식 된 세포군집의 이동을 측정하기 위하여 누적빈도를 계산하였다(C, 우측). (C)의 화살표는 BrDU 표식된 세포군집의 이동거리를 가리킨다. 표본 마우스마다 50개의 ½장샘이 기록되었는데, 여기서 유전자 형마다 적어도 3개의 다른 실험용 마우스가 사용되었다.
2014.04.02 조회수 22248 -
 3차원 고해상도 혈관내시경 시스템 개발
우리 학교 기계공학전공 오왕열 교수는 현존하는 기술보다 *이미징 속도가 최대 3.5배 빠른 광학 혈관내시경 시스템을 개발하고 이를 이용해 세계 최초로 3차원 고해상도(혈관 깊이 방향 10㎛급, 혈관 둘레 및 길이 방향 30㎛급) 생체 혈관 내부 이미지 획득에 성공했다. *이미징 : 시각적으로 인식할 수 있는 형으로 정보를 표현하는 것
이번에 국내 최초로 개발된 혈관내시경 시스템은 영상속도는 물론 해상도, 영상품질, 영상획득영역 등도 세계 최고의 성능을 갖고 있다. 또 혈관 벽의 취약여부 파악에 용이한 편광 이미징 등 기능성 이미징도 동시에 수행할 수 있어 심혈관계 질환 진단 및 치료에 새로운 전기를 가져올 것으로 기대된다.
혈관내시경 광단층영상(OCT, Optical Coherence Tomography) 시스템은 심근경색으로 대표되는 심혈관계질환 진단을 위해 가장 높은 해상도를 제공하는 장비로써 임상분야에서 주목을 받고 있다.
그러나 기존 시스템은 영상 촬영속도가 느려 빠르게 이미징을 수행해야하는 혈관 내 상황에서 자세한 파악이 불가능하고 혈관 내부를 띄엄띄엄 분석할 수밖에 없었다. 임상에서 생체 혈관 내부 광학적 영상을 위해서는 내시경을 혈관에 삽입한 다음 투명한 액체를 순간적으로 흘려보내 수초 안에 촬영을 해야 하기 때문이라고 연구팀은 전했다.
연구팀은 초고속·고해상도 광단층영상 시스템과 직경 0.8mm(밀리미터)의 유연한 고속·고해상도 내시경 및 이미징 빛을 혈관 내에서 고속으로 스캔할 수 있는 장치를 개발하고, 이를 활용해 혈관 벽 내부 구조를 영상화하는데 성공했다.
연구팀은 개발한 시스템을 활용해 사람의 관상동맥과 비슷한 크기인 토끼 대동맥 7cm 길이의 혈관을 5.8초 만에 초당 350장의 속도로 단층 촬영에 성공, 3차원 모든 방향으로 10~35㎛(마이크로미터, 100만분의 1미터)의 고해상도 이미지를 얻어냈다.
연구팀은 현재 상용화중인 혈관내시경처럼 200㎛ 간격으로 이미징할 경우에는 7cm 길이의 혈관을 1초 안에 모두 이미징할 수 있었다.
오왕열 교수는 “이번에 개발한 혈관내시경 시스템은 세계 최고의 성능을 갖는 것은 물론 살아있는 동물 혈관 내부 촬영을 통해 사람의 혈관과 비슷한 상황에서 테스트가 됐다는 점에서 크게 의미가 있다”고 연구 의의를 밝혔다.
더불어 “병원과 긴밀한 협력을 통해 올 상반기에 사람의 심장과 비슷한 크기를 가진 동물 심장의 관상동맥 촬영을 준비하고 있다”며 “이를 거쳐 향수 수년 내에 임상에서 환자에 적용할 수 있을 것”이라고 임상적용 및 상용화에 대한 강한 기대감을 내비쳤다.
이번 연구는 한국연구재단의 중견연구자지원사업(도약연구) 및 글로벌프론티어사업의 지원을 통해 수행됐으며, 연구결과는 지난 1월 바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express) 지에 게재됐다.
그림1. 내시경 말단 광학부(좌측상단)
그림2. 내시경 고속 광 스캐닝 유닛(우측상단)
그림3. 고해상도로 이미징된 동물 생체 혈관 내부 영상(혈관 둘레 및 길이방향)
그림4. 고해상도로 이미징된 동물 생체 혈관 내부 영상(혈관 깊이방향)
2014.03.12 조회수 21823
3차원 고해상도 혈관내시경 시스템 개발
우리 학교 기계공학전공 오왕열 교수는 현존하는 기술보다 *이미징 속도가 최대 3.5배 빠른 광학 혈관내시경 시스템을 개발하고 이를 이용해 세계 최초로 3차원 고해상도(혈관 깊이 방향 10㎛급, 혈관 둘레 및 길이 방향 30㎛급) 생체 혈관 내부 이미지 획득에 성공했다. *이미징 : 시각적으로 인식할 수 있는 형으로 정보를 표현하는 것
이번에 국내 최초로 개발된 혈관내시경 시스템은 영상속도는 물론 해상도, 영상품질, 영상획득영역 등도 세계 최고의 성능을 갖고 있다. 또 혈관 벽의 취약여부 파악에 용이한 편광 이미징 등 기능성 이미징도 동시에 수행할 수 있어 심혈관계 질환 진단 및 치료에 새로운 전기를 가져올 것으로 기대된다.
혈관내시경 광단층영상(OCT, Optical Coherence Tomography) 시스템은 심근경색으로 대표되는 심혈관계질환 진단을 위해 가장 높은 해상도를 제공하는 장비로써 임상분야에서 주목을 받고 있다.
그러나 기존 시스템은 영상 촬영속도가 느려 빠르게 이미징을 수행해야하는 혈관 내 상황에서 자세한 파악이 불가능하고 혈관 내부를 띄엄띄엄 분석할 수밖에 없었다. 임상에서 생체 혈관 내부 광학적 영상을 위해서는 내시경을 혈관에 삽입한 다음 투명한 액체를 순간적으로 흘려보내 수초 안에 촬영을 해야 하기 때문이라고 연구팀은 전했다.
연구팀은 초고속·고해상도 광단층영상 시스템과 직경 0.8mm(밀리미터)의 유연한 고속·고해상도 내시경 및 이미징 빛을 혈관 내에서 고속으로 스캔할 수 있는 장치를 개발하고, 이를 활용해 혈관 벽 내부 구조를 영상화하는데 성공했다.
연구팀은 개발한 시스템을 활용해 사람의 관상동맥과 비슷한 크기인 토끼 대동맥 7cm 길이의 혈관을 5.8초 만에 초당 350장의 속도로 단층 촬영에 성공, 3차원 모든 방향으로 10~35㎛(마이크로미터, 100만분의 1미터)의 고해상도 이미지를 얻어냈다.
연구팀은 현재 상용화중인 혈관내시경처럼 200㎛ 간격으로 이미징할 경우에는 7cm 길이의 혈관을 1초 안에 모두 이미징할 수 있었다.
오왕열 교수는 “이번에 개발한 혈관내시경 시스템은 세계 최고의 성능을 갖는 것은 물론 살아있는 동물 혈관 내부 촬영을 통해 사람의 혈관과 비슷한 상황에서 테스트가 됐다는 점에서 크게 의미가 있다”고 연구 의의를 밝혔다.
더불어 “병원과 긴밀한 협력을 통해 올 상반기에 사람의 심장과 비슷한 크기를 가진 동물 심장의 관상동맥 촬영을 준비하고 있다”며 “이를 거쳐 향수 수년 내에 임상에서 환자에 적용할 수 있을 것”이라고 임상적용 및 상용화에 대한 강한 기대감을 내비쳤다.
이번 연구는 한국연구재단의 중견연구자지원사업(도약연구) 및 글로벌프론티어사업의 지원을 통해 수행됐으며, 연구결과는 지난 1월 바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express) 지에 게재됐다.
그림1. 내시경 말단 광학부(좌측상단)
그림2. 내시경 고속 광 스캐닝 유닛(우측상단)
그림3. 고해상도로 이미징된 동물 생체 혈관 내부 영상(혈관 둘레 및 길이방향)
그림4. 고해상도로 이미징된 동물 생체 혈관 내부 영상(혈관 깊이방향)
2014.03.12 조회수 21823 -
 손상된 DNA의 돌연변이 수리과정 규명
- DNA 손상을 복구하는 암 관련 핵심 효소 ATM의 조절 메커니즘 밝혀 -
우리 학교 생명과학과 최광욱 교수와 홍성태 박사 연구팀은 생체정보를 저장하는 DNA가 손상됐을 때 이를 수리하는 핵심효소의 기능에 필수적인 단백질 ‘ATM(Ataxia telangiectasia mutated)’의 작동 메커니즘을 규명했다.
연구결과는 네이처 자매지인 ‘네이처 커뮤니케이션즈(Nature communications)’ 19일자 온라인판에 게재됐다.
인간을 포함해 DNA를 갖고 있는 모든 생명체는 자신의 DNA정보를 지키기 위해 끊임없이 노력하고 있으며 이들이 살아가고 있는 자연환경에는 DNA를 손상시킬 수 있는 수많은 요소들이 존재한다.
예를 들면, 우리가 매일 섭취하는 음식물속에 들어있는 탄화물질이나 건물의 시멘트에서 나오는 라돈과 같은 방사선 물질, 강한 태양빛에 포함된 자외선 등 수많은 발암물질들과 함께 살아가고 있다.
생명체는 발암물질들로부터 DNA정보를 일정하게 유지하기 위해 복잡하고 정교한 DNA 수리작업을 항상 수행하고 있는데 이 과정에서 ‘ATM’이라고 하는 DNA 손상복구 단백질이 핵심적인 역할을 한다. 따라서 ATM이 제대로 작동하지 않으면 암 발병 확률이 높아진다.
지금까지 학계에서는 TCTP(Translationally controlled tumor protein)라는 단백질이 ATM의 기능을 조절하는데 중요할 것이라고 추정해 왔다. 그러나 이에 대한 주된 연구결과가 배양된 세포수준에서 확인했기 때문에 정확히 어떠한 방식으로 TCTP가 ATM의 기능을 조절하는지 알 수 없었다.
연구팀은 TCTP에 결합하는 아미노산 조각의 정보를 활용해 TCTP가 ATM과 결합을 할 수 있고, 다양한 분자생화학적인 방법들을 이용해 TCTP가 ATM의 효소기능을 높여준다는 사실을 밝혀냈다.
이와 함께 분자 유전학의 모델동물로 널리 사용되는 초파리를 이용해 TCTP와 ATM이 방사선에 의해 손상된 DNA를 수리하는데 매우 중요한 역할을 하고 있다는 점도 규명했다.
이를 통해 연구팀은 TCTP가 세포배양 수준은 물론 고등생명체에서도 DNA 정보를 일정하게 유지하는데 중요한 역할을 하며, TCTP가 ATM의 기능을 조절하는 방법에 대한 중요하고 구체적인 단초를 제시했다.
최광욱 교수는 이번 연구에 대해 “초파리 모델동물을 이용한 기초연구가 암 등 질병의 과정을 이해하고 치료방법을 개발하는데 중요한 기여를 할 수 있음을 보여주는 좋은 사례”라고 말했다.
이번 연구는 미래창조과학부(장관 최문기)와 한국연구재단이 추진하는 중견연구자지원사업(도약 연구)과 일반연구자지원(대통령포스닥펠로우십)의 지원을 받아 수행됐다.
□ 보충자료
1. ATM(Ataxia telangiectasia mutated)ATM 유전자의 이상은 Louis-Bar syndrome 이라는 희귀 퇴행성 신경질환을 유발하는 것으로 알려져 있다. 운동기능이상, 눈의 흰자위나 피부에 비정상적으로 나타나는 혈관 확장, 약화된 면역반응, 혈액암 (림프종, 백혈병) 과 같은 질병증상을 추가로 일으킬 수 있다. ATM 유전자는 인산화 효소(kinase)의 기능을 가지고 있으며, ATM 단백질은 DNA의 이중나선이 모두 끊어질 경우, 이를 연결하는데 중요한 역할을 수행한다.
2. TCTP(Translationally controlled tumor protein)1988년 처음으로 발견된 단백질로, 이 유전자의 이름은 종양 세포에서 그 양이 비정상적으로 많아지기 때문에 붙여졌다. 그 기능이 본격적으로 밝혀진 것은 2000 초반부터이며, 세포의 생존과 성장에 중요한 역할을 한다. 최근에서야 DNA 정보를 유지하는데 중요하다는 것이 밝혀졌다.
3. Nature communcations네이처를 출간하는 Nature Publishing Group (NPG)에서 발간하는 온라인 전용 과학저널. 생물학, 물리학, 화학, 공학, 천문학, 고고학 등 다양한 분야의 수준 높은 과학연구 주제를 다루고 있다. 2012년을 기준으로 하는 SCI (Science citation index, 과학분야 인용지수)는 10.015 이다.
4. 초파리1900년대 초반, Charles W. Woodworth, William E. Castle, Thomas H. Morgan등이 멘델유전학을 연구하기 위해 처음으로 사용하기 시작한 모델 동물. 진핵세포에서 일어나는 생명현상을 연구하기 위해 오랫동안 사용되어온 대표적인 모델 동물이다.
□ 그림설명
그림1. TCTP단백질의 양이 줄어들면 방사능에 의해 쉽게 초파리 눈 세포의 형태가 비정상적으로 변형된다. (화살촉). Scale bars = 200mm
그림2. TCTP 단백질의 양이 줄어들면, 방사능에 의해 초파리의 염색체가 쉽게 끊어진다 (화살촉 표시). Scale bars = 10 mm.
그림3. TCTP와 ATM의 유전자발현이 줄어들면 눈의 정상적인 발생에 큰 결함이 생긴다.(왼쪽 : 초파리의 정상적인 눈, 오른쪽 : 성장이 결핍된 눈)
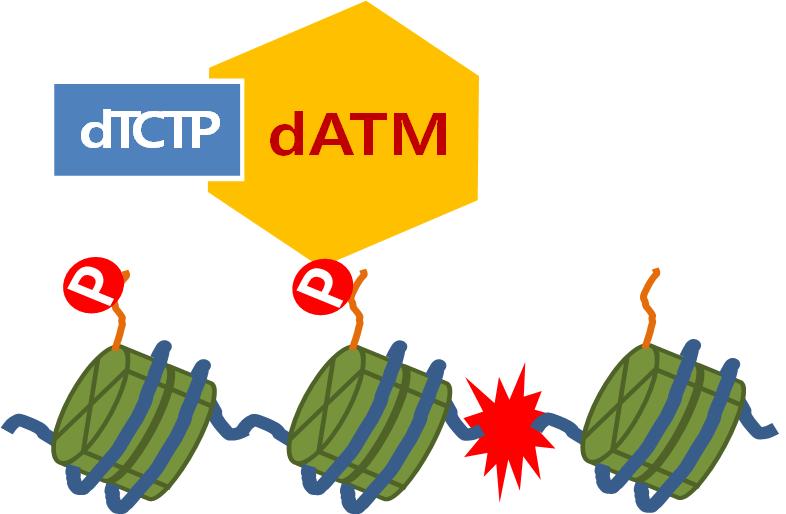
그림4. ATM은 끊어진 DNA의 위치를 표시하며, TCTP는 이 작용이 원활히 일어나도록 돕는다. 세포 핵 안에 들어있는 DNA(파란 선)는 히스톤 단백질(녹색 원통)에 감겨있다. DNA가 끊어지면(붉은 번개표시) 끊어진 자리에 ATM 단백질이 인산기(P)를 부착한다. 다양한 DNA 수리 단백질들은 이 인산기를 DNA에 수리가 필요하다는 신호로 인식하고 모여든다.
2013.12.20 조회수 23949
손상된 DNA의 돌연변이 수리과정 규명
- DNA 손상을 복구하는 암 관련 핵심 효소 ATM의 조절 메커니즘 밝혀 -
우리 학교 생명과학과 최광욱 교수와 홍성태 박사 연구팀은 생체정보를 저장하는 DNA가 손상됐을 때 이를 수리하는 핵심효소의 기능에 필수적인 단백질 ‘ATM(Ataxia telangiectasia mutated)’의 작동 메커니즘을 규명했다.
연구결과는 네이처 자매지인 ‘네이처 커뮤니케이션즈(Nature communications)’ 19일자 온라인판에 게재됐다.
인간을 포함해 DNA를 갖고 있는 모든 생명체는 자신의 DNA정보를 지키기 위해 끊임없이 노력하고 있으며 이들이 살아가고 있는 자연환경에는 DNA를 손상시킬 수 있는 수많은 요소들이 존재한다.
예를 들면, 우리가 매일 섭취하는 음식물속에 들어있는 탄화물질이나 건물의 시멘트에서 나오는 라돈과 같은 방사선 물질, 강한 태양빛에 포함된 자외선 등 수많은 발암물질들과 함께 살아가고 있다.
생명체는 발암물질들로부터 DNA정보를 일정하게 유지하기 위해 복잡하고 정교한 DNA 수리작업을 항상 수행하고 있는데 이 과정에서 ‘ATM’이라고 하는 DNA 손상복구 단백질이 핵심적인 역할을 한다. 따라서 ATM이 제대로 작동하지 않으면 암 발병 확률이 높아진다.
지금까지 학계에서는 TCTP(Translationally controlled tumor protein)라는 단백질이 ATM의 기능을 조절하는데 중요할 것이라고 추정해 왔다. 그러나 이에 대한 주된 연구결과가 배양된 세포수준에서 확인했기 때문에 정확히 어떠한 방식으로 TCTP가 ATM의 기능을 조절하는지 알 수 없었다.
연구팀은 TCTP에 결합하는 아미노산 조각의 정보를 활용해 TCTP가 ATM과 결합을 할 수 있고, 다양한 분자생화학적인 방법들을 이용해 TCTP가 ATM의 효소기능을 높여준다는 사실을 밝혀냈다.
이와 함께 분자 유전학의 모델동물로 널리 사용되는 초파리를 이용해 TCTP와 ATM이 방사선에 의해 손상된 DNA를 수리하는데 매우 중요한 역할을 하고 있다는 점도 규명했다.
이를 통해 연구팀은 TCTP가 세포배양 수준은 물론 고등생명체에서도 DNA 정보를 일정하게 유지하는데 중요한 역할을 하며, TCTP가 ATM의 기능을 조절하는 방법에 대한 중요하고 구체적인 단초를 제시했다.
최광욱 교수는 이번 연구에 대해 “초파리 모델동물을 이용한 기초연구가 암 등 질병의 과정을 이해하고 치료방법을 개발하는데 중요한 기여를 할 수 있음을 보여주는 좋은 사례”라고 말했다.
이번 연구는 미래창조과학부(장관 최문기)와 한국연구재단이 추진하는 중견연구자지원사업(도약 연구)과 일반연구자지원(대통령포스닥펠로우십)의 지원을 받아 수행됐다.
□ 보충자료
1. ATM(Ataxia telangiectasia mutated)ATM 유전자의 이상은 Louis-Bar syndrome 이라는 희귀 퇴행성 신경질환을 유발하는 것으로 알려져 있다. 운동기능이상, 눈의 흰자위나 피부에 비정상적으로 나타나는 혈관 확장, 약화된 면역반응, 혈액암 (림프종, 백혈병) 과 같은 질병증상을 추가로 일으킬 수 있다. ATM 유전자는 인산화 효소(kinase)의 기능을 가지고 있으며, ATM 단백질은 DNA의 이중나선이 모두 끊어질 경우, 이를 연결하는데 중요한 역할을 수행한다.
2. TCTP(Translationally controlled tumor protein)1988년 처음으로 발견된 단백질로, 이 유전자의 이름은 종양 세포에서 그 양이 비정상적으로 많아지기 때문에 붙여졌다. 그 기능이 본격적으로 밝혀진 것은 2000 초반부터이며, 세포의 생존과 성장에 중요한 역할을 한다. 최근에서야 DNA 정보를 유지하는데 중요하다는 것이 밝혀졌다.
3. Nature communcations네이처를 출간하는 Nature Publishing Group (NPG)에서 발간하는 온라인 전용 과학저널. 생물학, 물리학, 화학, 공학, 천문학, 고고학 등 다양한 분야의 수준 높은 과학연구 주제를 다루고 있다. 2012년을 기준으로 하는 SCI (Science citation index, 과학분야 인용지수)는 10.015 이다.
4. 초파리1900년대 초반, Charles W. Woodworth, William E. Castle, Thomas H. Morgan등이 멘델유전학을 연구하기 위해 처음으로 사용하기 시작한 모델 동물. 진핵세포에서 일어나는 생명현상을 연구하기 위해 오랫동안 사용되어온 대표적인 모델 동물이다.
□ 그림설명
그림1. TCTP단백질의 양이 줄어들면 방사능에 의해 쉽게 초파리 눈 세포의 형태가 비정상적으로 변형된다. (화살촉). Scale bars = 200mm
그림2. TCTP 단백질의 양이 줄어들면, 방사능에 의해 초파리의 염색체가 쉽게 끊어진다 (화살촉 표시). Scale bars = 10 mm.
그림3. TCTP와 ATM의 유전자발현이 줄어들면 눈의 정상적인 발생에 큰 결함이 생긴다.(왼쪽 : 초파리의 정상적인 눈, 오른쪽 : 성장이 결핍된 눈)
그림4. ATM은 끊어진 DNA의 위치를 표시하며, TCTP는 이 작용이 원활히 일어나도록 돕는다. 세포 핵 안에 들어있는 DNA(파란 선)는 히스톤 단백질(녹색 원통)에 감겨있다. DNA가 끊어지면(붉은 번개표시) 끊어진 자리에 ATM 단백질이 인산기(P)를 부착한다. 다양한 DNA 수리 단백질들은 이 인산기를 DNA에 수리가 필요하다는 신호로 인식하고 모여든다.
2013.12.20 조회수 23949 -
 건강한 망막혈관 생성을 유도하는 치료방법 개발
- 향후 당뇨망막병증 치료방법으로 적용 기대
우리 학교 연구진이 실명으로 이어질 수 있는 망막혈관 질환치료의 실마리를 찾아냈다. 혈액공급이 잘되지 않는 망막 부위로 건강한 망막혈관이 생성되도록 하여 망막신경을 보호하는 혈관생성단백질을 찾아낸 것. 향후 당뇨망막병증*과 미숙아망막병증**의 치료방법 개선을 위한 연구의 단초가 될 것으로 기대된다.
이번 연구결과는 국내에서 전문적인 기초과학 교육을 받고 있는 안과 전문의 연구원에 의해 이루어진 대표적인 중개연구의 결과여서 더욱 주목받고 있다.
* 미숙아망막병증 : 망막 혈관의 발달이 완성되지 않은 시기에 출생한 미숙아에서 발생하는 망막 혈관질환으로 소아실명의 가장 흔한 원인 질환이다.
* 당뇨망막병증 : 당뇨병의 합병증으로 망막조직으로의 불충분한 혈액공급으로 생기는 망막 혈관질환으로 성인실명의 중요한 원인 질환이다.
우리 학교 의과학대학원 이준엽 연구원이(안과 전문의, 지도교수: 고규영,유욱준) 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)의 지원으로 수행되었고, 연구결과는 사이언스 중개의학(Science Translational Medicine) 표지논문(9월 18일자)으로 소개되었다. 이 학술지는 임상의학과 기초과학을 연계하는 중개의학 분야 권위지로 사이언스지 자매지이다.
(논문명 : Angiopoietin-1 Guides Directional Angiogenesis Through Integrin αvβ5 Signaling for Recovery of Ischemic Retinopathy)
당뇨망막병증의 치료에는 망막조직을 파괴하는 레이저광응고술이나혈관증식과 혈액누출을 억제하는 항체치료제*가 적용되고 있다.
항체치료제는 망막신경을 파괴하지 않는 장점이 있지만 한시적으로 혈관증식을 억제할 뿐, 근본적인 해결이 아니어서 반복적인 치료가 필요하다는 한계가 있었다.
* 항체치료제 : 비정상적인 혈관증식과 혈액누출을 선택적으로 억제하기 위하여 개발된 항체로서, 현재 혈관내피세포성장인자 (VEGF)를 저해하는 아바스틴 (Avastin) 과 루센티스 (Lucentis) 가 대표적인 항체치료제이다.
연구팀은 개체의 발달과정에서 혈관의 생성과 안정화에 필수적이라고 알려진 안지오포이에틴-1* 단백질이 망막혈관의 생성과정에도 중요한 역할을 함을 동물실험을 통해 규명해냈다.
망막출혈에 의한 시력상실의 근본 원인이 되는 망막허혈**을 개선하고 망막신경을 보호하는 단백질을 알아낸 것이다.
망막조직으로 충분한 혈액을 공급해 망막신경의 기능을 보존하는 방식의 근본적인 치료방법 개발의 실마리가 될 것으로 기대된다.
* 망막허혈 : 망막 조직에 충분한 혈액 공급이 되지 않는 상태
* 안지오포이에틴-1(Angiopoietin-1) : 건강한 혈관의 생성을 유도하고 생성된 혈관의 안정화를 유지하는 데 중요한 성장인자.
실제 안지오포이에틴-1을 망막병증 생쥐모델의 안구에 투약한 결과 건강한 망막혈관의 생성이 촉진되어, 망막허혈에 따르는 비정상적인 혈관증식이나 망막출혈, 시력상실이 예방되었다.
이준엽 연구원은 “이번 연구는 안지오포이에틴-1이 망막혈관의 생성과 안정화에 중요한 인자라는 사실을 새롭게 규명함으로써 혈관생성을 억제하는 현재의 치료법에서 건강한 혈관을 생성하고 혈관의 기능을 강화하는 방식의 치료법으로 패러다임이 전환될 것을 기대한다”고 연구 의의를 밝혔다.
그림 1. 망막병증 생쥐모델에서의 안구 내 투여한 Angiopoietin-1의 역할 대조군에 비해 VEGF-Trap 치료군과 Angiopoietin-1 (Ang1) 치료군은 병적인 혈관의 증식을 유의하게 억제함 (아래), 추가적으로 Ang1 치료군은 망막 중심부의 무혈관부위(망막허혈)를 향하여 혈관이 생성되었고, 이러한 현상은 VEGF-Trap 치료군에서는 관찰되지 않음 (위).
그림 2. Angiopoietin-1에 의한 망막허혈과 망막 출혈의 감소 및 혈관의 정상화 (좌) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막허혈부위 면적(화살표)을 유의하게 감소시켰으며, 망막 출혈의 양도 Ang1 치료에 의해 감소함. (우) Ang1 에 의해 새롭게 형성된 혈관은 정상 망막 혈관과 같이 혈관주위세포에 의한 지지를 받는 구조적으로 안정된 혈관임.
그림 3. Angiopoietin-1에 의한 망막 신경 보호 효과 (위) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막 중앙부 와 주변부의 신경세포의 세포자멸사를 유의하게 억제함. (아래) 이러한 Ang1에 의한 망막 신경 보호 효과는 전기 생리학적 검사인 망막전위도 검사를 통해 확인됨.
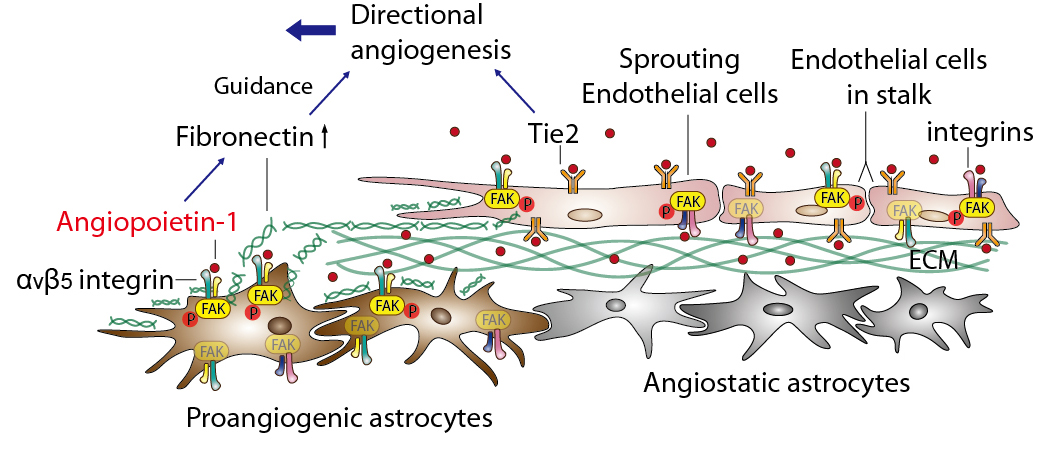
그림 4. Angiopoietin-1 이 망막 혈관 생성을 유도하는 기전 Angiopoietin-1은 망막 혈관의 내피세포 (Endothelial cell) 에 작용하여 혈관의 안정성 유지에 중요한 역할을 할 뿐만 아니라 망막의 별아교세포 (Astrocyte) 의 integrin 수용체를 통하여 fibronectin 이라는 세포외기질의 생성을 증가시켜 망막 조직 내로의 혈관 생성의 경로를 안내하는 역할을 함.
2013.09.22 조회수 22765
건강한 망막혈관 생성을 유도하는 치료방법 개발
- 향후 당뇨망막병증 치료방법으로 적용 기대
우리 학교 연구진이 실명으로 이어질 수 있는 망막혈관 질환치료의 실마리를 찾아냈다. 혈액공급이 잘되지 않는 망막 부위로 건강한 망막혈관이 생성되도록 하여 망막신경을 보호하는 혈관생성단백질을 찾아낸 것. 향후 당뇨망막병증*과 미숙아망막병증**의 치료방법 개선을 위한 연구의 단초가 될 것으로 기대된다.
이번 연구결과는 국내에서 전문적인 기초과학 교육을 받고 있는 안과 전문의 연구원에 의해 이루어진 대표적인 중개연구의 결과여서 더욱 주목받고 있다.
* 미숙아망막병증 : 망막 혈관의 발달이 완성되지 않은 시기에 출생한 미숙아에서 발생하는 망막 혈관질환으로 소아실명의 가장 흔한 원인 질환이다.
* 당뇨망막병증 : 당뇨병의 합병증으로 망막조직으로의 불충분한 혈액공급으로 생기는 망막 혈관질환으로 성인실명의 중요한 원인 질환이다.
우리 학교 의과학대학원 이준엽 연구원이(안과 전문의, 지도교수: 고규영,유욱준) 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)의 지원으로 수행되었고, 연구결과는 사이언스 중개의학(Science Translational Medicine) 표지논문(9월 18일자)으로 소개되었다. 이 학술지는 임상의학과 기초과학을 연계하는 중개의학 분야 권위지로 사이언스지 자매지이다.
(논문명 : Angiopoietin-1 Guides Directional Angiogenesis Through Integrin αvβ5 Signaling for Recovery of Ischemic Retinopathy)
당뇨망막병증의 치료에는 망막조직을 파괴하는 레이저광응고술이나혈관증식과 혈액누출을 억제하는 항체치료제*가 적용되고 있다.
항체치료제는 망막신경을 파괴하지 않는 장점이 있지만 한시적으로 혈관증식을 억제할 뿐, 근본적인 해결이 아니어서 반복적인 치료가 필요하다는 한계가 있었다.
* 항체치료제 : 비정상적인 혈관증식과 혈액누출을 선택적으로 억제하기 위하여 개발된 항체로서, 현재 혈관내피세포성장인자 (VEGF)를 저해하는 아바스틴 (Avastin) 과 루센티스 (Lucentis) 가 대표적인 항체치료제이다.
연구팀은 개체의 발달과정에서 혈관의 생성과 안정화에 필수적이라고 알려진 안지오포이에틴-1* 단백질이 망막혈관의 생성과정에도 중요한 역할을 함을 동물실험을 통해 규명해냈다.
망막출혈에 의한 시력상실의 근본 원인이 되는 망막허혈**을 개선하고 망막신경을 보호하는 단백질을 알아낸 것이다.
망막조직으로 충분한 혈액을 공급해 망막신경의 기능을 보존하는 방식의 근본적인 치료방법 개발의 실마리가 될 것으로 기대된다.
* 망막허혈 : 망막 조직에 충분한 혈액 공급이 되지 않는 상태
* 안지오포이에틴-1(Angiopoietin-1) : 건강한 혈관의 생성을 유도하고 생성된 혈관의 안정화를 유지하는 데 중요한 성장인자.
실제 안지오포이에틴-1을 망막병증 생쥐모델의 안구에 투약한 결과 건강한 망막혈관의 생성이 촉진되어, 망막허혈에 따르는 비정상적인 혈관증식이나 망막출혈, 시력상실이 예방되었다.
이준엽 연구원은 “이번 연구는 안지오포이에틴-1이 망막혈관의 생성과 안정화에 중요한 인자라는 사실을 새롭게 규명함으로써 혈관생성을 억제하는 현재의 치료법에서 건강한 혈관을 생성하고 혈관의 기능을 강화하는 방식의 치료법으로 패러다임이 전환될 것을 기대한다”고 연구 의의를 밝혔다.
그림 1. 망막병증 생쥐모델에서의 안구 내 투여한 Angiopoietin-1의 역할 대조군에 비해 VEGF-Trap 치료군과 Angiopoietin-1 (Ang1) 치료군은 병적인 혈관의 증식을 유의하게 억제함 (아래), 추가적으로 Ang1 치료군은 망막 중심부의 무혈관부위(망막허혈)를 향하여 혈관이 생성되었고, 이러한 현상은 VEGF-Trap 치료군에서는 관찰되지 않음 (위).
그림 2. Angiopoietin-1에 의한 망막허혈과 망막 출혈의 감소 및 혈관의 정상화 (좌) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막허혈부위 면적(화살표)을 유의하게 감소시켰으며, 망막 출혈의 양도 Ang1 치료에 의해 감소함. (우) Ang1 에 의해 새롭게 형성된 혈관은 정상 망막 혈관과 같이 혈관주위세포에 의한 지지를 받는 구조적으로 안정된 혈관임.
그림 3. Angiopoietin-1에 의한 망막 신경 보호 효과 (위) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막 중앙부 와 주변부의 신경세포의 세포자멸사를 유의하게 억제함. (아래) 이러한 Ang1에 의한 망막 신경 보호 효과는 전기 생리학적 검사인 망막전위도 검사를 통해 확인됨.
그림 4. Angiopoietin-1 이 망막 혈관 생성을 유도하는 기전 Angiopoietin-1은 망막 혈관의 내피세포 (Endothelial cell) 에 작용하여 혈관의 안정성 유지에 중요한 역할을 할 뿐만 아니라 망막의 별아교세포 (Astrocyte) 의 integrin 수용체를 통하여 fibronectin 이라는 세포외기질의 생성을 증가시켜 망막 조직 내로의 혈관 생성의 경로를 안내하는 역할을 함.
2013.09.22 조회수 22765 -
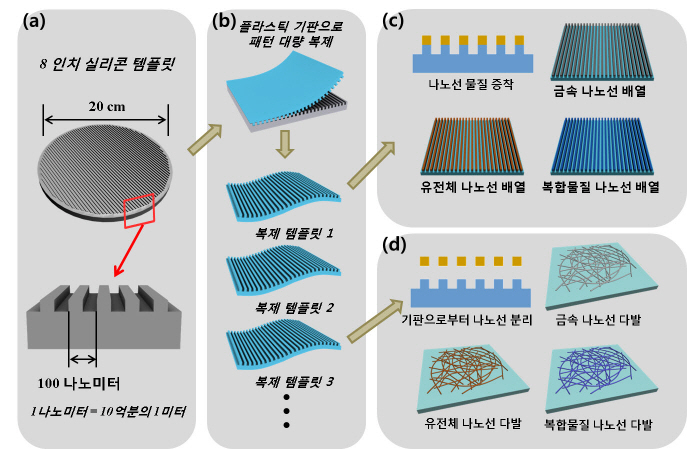 다양한 물질로 만든 나노선 상용화 가능성 열려
- 산·학·연 2년간 공동연구 끝에 나노선 상용화 가능한 기술 개발 -- 폭 50nm, 길이 20cm 나노선 2시간이면 200만 가닥 대량생산 가능해 -
폭이 수십 나노미터 정도로 매우 얇은 나노선의 상용화를 앞당길 혁신적인 기술이 국내 산·학·연 공동연구진에 의해 개발됐다. 향후 나노선을 이용한 반도체, 고성능 센서, 생체소자 등 다양한 분야에 활용될 것으로 전망된다.
우리 학교 전기및전자공학과 윤준보 교수 연구팀은 (주)LG이노텍(대표 이웅범), 나노종합기술원(원장 이재영)과 공동으로 첨단 과학 분야에서 핵심적인 소재로 쓰이고 있는 나노선을 다양한 소재로 필요한 길이만큼 대량 생산할 수 있는 기술을 개발했다.
연구결과는 나노 과학 분야의 권위 있는 학술지인 ‘나노 레터스(Nano Letters)’ 7월 30일자 온라인판에 게재됐다.
나노선은 폭이 최대 100나노미터 정도에 불과한 긴 선 모양의 구조체로 기존에 발견되지 않았던 다양한 열적, 전기적, 기계적 특성을 보이는 다기능성 나노 소재다. 나노 세계에서만 보이는 특성을 활용하기 위해 나노선은 반도체, 에너지, 생체소자, 광학소자 등 다양한 분야에 활용될 수 있는 첨단 소재로 각광 받고 있다.
그러나 수 밀리미터를 성장시키는데 3~4일이 소요될 만큼 합성 속도가 매우 느리고 대량 생산이 어려운 것은 물론 원하는 물질을 자유자재로 나노선으로 제작할 수 있는 기술이 개발되지 않았다.
또 제작된 나노선을 실제로 적용하기 위해서는 가지런히 정렬시켜야 하는데 기존 기술은 정렬을 위해 복잡한 후처리를 해야 하고 정렬 상태도 완벽하지 못해 상용화에 커다란 걸림돌이었다.
연구팀은 이러한 종래의 문제점을 극복하기 위해 기존의 화학적 합성법을 사용하지 않고 반도체공정을 적용했다.
연구팀은 직경 20센티미터의 실리콘 웨이퍼 기판에 광식각 공정을 이용해 목표하는 주기보다 큰 패턴을 형성한 뒤 이 주기를 반복적으로 줄여가는 방법을 이용해 100나노미터 초미세 선격자 패턴을 제작했다.
이 패턴을 기반으로 반도체 제조과정에서 널리 쓰이는 박막증착공정을 활용해 폭 50nm(나노미터), 최대 길이 20cm(센티미터)의 나노선을 완벽한 형태로 대량 제조하는데 성공했다.
개발된 기술은 장시간의 합성 공정을 거칠 필요가 없으며 별도의 후처리를 하지 않아도 완벽하게 정렬된 상태로 만들 수 있어 상용화 가능성이 높은 것으로 학계와 산업계는 평가하고 있다.
윤준보 교수는 이번 연구에 대해 “낮은 생산성, 긴 제조시간, 물질합성의 제약, 나노선 정렬 등과 같은 기존 기술의 문제점을 해결했다는 데 의미가 있다”면서 “그동안 나노선을 산업적으로 널리 활용하지 못했지만 개발된 기술을 활용하면 나노선을 사용한 고성능의 반도체, 광학, 바이오 소자 등의 상용화를 앞당길 수 있을 것”이라고 밝혔다.
KAIST 전기및전자공학과 연정호 박사과정 학생, LG이노텍 이영재 책임연구원 나노종합기술원 유동은 선임연구원이 참여한 이번 연구는 미래창조과학부(장관 최문기)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약연구)의 지원으로 수행됐다.
2013.08.22 조회수 19424
다양한 물질로 만든 나노선 상용화 가능성 열려
- 산·학·연 2년간 공동연구 끝에 나노선 상용화 가능한 기술 개발 -- 폭 50nm, 길이 20cm 나노선 2시간이면 200만 가닥 대량생산 가능해 -
폭이 수십 나노미터 정도로 매우 얇은 나노선의 상용화를 앞당길 혁신적인 기술이 국내 산·학·연 공동연구진에 의해 개발됐다. 향후 나노선을 이용한 반도체, 고성능 센서, 생체소자 등 다양한 분야에 활용될 것으로 전망된다.
우리 학교 전기및전자공학과 윤준보 교수 연구팀은 (주)LG이노텍(대표 이웅범), 나노종합기술원(원장 이재영)과 공동으로 첨단 과학 분야에서 핵심적인 소재로 쓰이고 있는 나노선을 다양한 소재로 필요한 길이만큼 대량 생산할 수 있는 기술을 개발했다.
연구결과는 나노 과학 분야의 권위 있는 학술지인 ‘나노 레터스(Nano Letters)’ 7월 30일자 온라인판에 게재됐다.
나노선은 폭이 최대 100나노미터 정도에 불과한 긴 선 모양의 구조체로 기존에 발견되지 않았던 다양한 열적, 전기적, 기계적 특성을 보이는 다기능성 나노 소재다. 나노 세계에서만 보이는 특성을 활용하기 위해 나노선은 반도체, 에너지, 생체소자, 광학소자 등 다양한 분야에 활용될 수 있는 첨단 소재로 각광 받고 있다.
그러나 수 밀리미터를 성장시키는데 3~4일이 소요될 만큼 합성 속도가 매우 느리고 대량 생산이 어려운 것은 물론 원하는 물질을 자유자재로 나노선으로 제작할 수 있는 기술이 개발되지 않았다.
또 제작된 나노선을 실제로 적용하기 위해서는 가지런히 정렬시켜야 하는데 기존 기술은 정렬을 위해 복잡한 후처리를 해야 하고 정렬 상태도 완벽하지 못해 상용화에 커다란 걸림돌이었다.
연구팀은 이러한 종래의 문제점을 극복하기 위해 기존의 화학적 합성법을 사용하지 않고 반도체공정을 적용했다.
연구팀은 직경 20센티미터의 실리콘 웨이퍼 기판에 광식각 공정을 이용해 목표하는 주기보다 큰 패턴을 형성한 뒤 이 주기를 반복적으로 줄여가는 방법을 이용해 100나노미터 초미세 선격자 패턴을 제작했다.
이 패턴을 기반으로 반도체 제조과정에서 널리 쓰이는 박막증착공정을 활용해 폭 50nm(나노미터), 최대 길이 20cm(센티미터)의 나노선을 완벽한 형태로 대량 제조하는데 성공했다.
개발된 기술은 장시간의 합성 공정을 거칠 필요가 없으며 별도의 후처리를 하지 않아도 완벽하게 정렬된 상태로 만들 수 있어 상용화 가능성이 높은 것으로 학계와 산업계는 평가하고 있다.
윤준보 교수는 이번 연구에 대해 “낮은 생산성, 긴 제조시간, 물질합성의 제약, 나노선 정렬 등과 같은 기존 기술의 문제점을 해결했다는 데 의미가 있다”면서 “그동안 나노선을 산업적으로 널리 활용하지 못했지만 개발된 기술을 활용하면 나노선을 사용한 고성능의 반도체, 광학, 바이오 소자 등의 상용화를 앞당길 수 있을 것”이라고 밝혔다.
KAIST 전기및전자공학과 연정호 박사과정 학생, LG이노텍 이영재 책임연구원 나노종합기술원 유동은 선임연구원이 참여한 이번 연구는 미래창조과학부(장관 최문기)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약연구)의 지원으로 수행됐다.
2013.08.22 조회수 19424 -
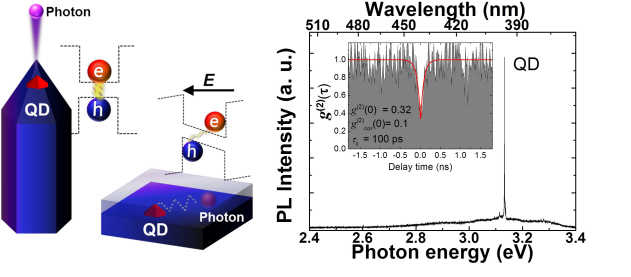 양자점 기반 단파장 초고속 양자 광원 개발
- 나노 오벨리스크 구조 위에 양자점을 형성해 고효율 단광자 광원 개발 -- 단파장 가시광선 대역에서 작동하는 초고속 반도체 양자 광원 연구 -
우리 학교 물리학과 조용훈 교수팀은 오벨리스크 모양의 나노 구조물을 만들고 꼭대기 부분에 높은 신뢰도를 갖는 반도체 단일 양자점을 형성해 초고속 고효율 단광자 방출을 구현하는데 성공했다.
연구결과는 네이처(Nature)가 발행하는 "사이언티픽 리포트(Scientific Reports)" 7월 5일자 온라인판에 게재됐다.
반도체 양자점은 전자를 수 나노미터 크기에 3차원적으로 구속해 불연속적인 에너지 준위를 갖는 원자와 유사한 특성을 나타낸다. 이 성질을 이용하면 차세대 양자정보 통신, 양자 암호의 핵심 구성 요소인 양자광원을 개발할 수 있다.
특히, 반도체 양자점의 경우 높은 구동 온도, 안정성, 빠른 광자 방출, 전류 구동 가능성과 같은 많은 장점을 가지고 있어 차세대 핵심 기술 중 하나로 꼽히고 있다.
그러나 기존의 자발 형성 양자점의 경우, 평면 구조 안에 양자점들이 높은 밀도로 묻혀 있어 단일 양자점 하나의 특성을 파악하기 어렵고 광자 방출 효율이 매우 제한돼 있는 한계가 있다. 또 구성하는 층 사이의 응력으로 인한 내부 전기장 효과 때문에 전자와 정공 사이의 재결합이 어려워 내부 양자 효율이 낮은 문제가 있었다.조 교수 연구팀은 단파장의 빛을 내는 넓은 띠구조를 갖는 질화물 반도체를 이용해 오벨리스크 형태(뾰족한 팁 모양)의 나노 구조를 제작했다. 그 위에 얇은 활성층 구조를 다시 성장해 나노 팁 끝에 단일 양자점을 위치시키는데 성공해 스펙트럼 폭이 매우 작은 에너지 준위에서 발생하는 초고속 단광자 특성을 확인했다.
이 같은 독특한 나노 구조를 활용하면, 패터닝 등의 공정 없이도 단일 양자구조를 얻기가 쉽고, 양자점에서 생성된 빛이 외부로 쉽게 빠져나올 수 있다는 장점이 있다.
이와 함께 연구팀은 박막 형태와는 달리 오벨리스크 형태의 나노구조의 경우 응력을 크게 감소시켜 내부 전기장 효과도 상쇄돼 내부 양자 효율이 크게 증가하는 현상을 밝혔다.
이번에 개발된 양자광원은 발광파장이 기존 장파장 적외선 대역이 아닌 단파장 가시광(400nm) 대역이기 때문에 자유 공간에서의 통신에 사용이 가능하고 광자 검출 효율이 높은 가시광 대역의 검출기를 사용할 수 있다.
조용훈 교수는 “기존의 양자점 성장 방식과는 달리 비교적 쉽게 단일 양자점을 형성하여 제어할 수 있고, 이를 통해 매우 빠른 단일 광자 생성이 가능해 실용적인 양자광원 개발에 기여할 수 있을 것으로 기대된다”며 “오벨리스크 형태 나노구조의 특성 상 손쉽게 분리 및 다른 기판과의 결합이 가능해 단일 칩 양자 광소자 제작에도 활용될 수 있다”고 말했다.
KAIST 물리학과 조용훈 교수 지도아래 김제형(제1저자), 고영호(제2저자) 박사과정 학생이 주도적으로 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업 및 WCU 사업의 지원으로 수행됐다.
그림1. (왼쪽) 프랑스 파리에 위치한 오벨리스크 사진. (오른쪽) 제작된 오벨리스크형 나노 구조의 전자현미경 이미지.
그림2. (왼쪽) 오벨리스크형 나노구조와 기존 평면 박막 구조에 내재된 양자점을 비교한 개념도. (오른쪽) 오벨리스크 나노구조 끝에 형성된 단일 양자점에서 방출되는 좁은 선폭의 스펙트럼과 광원의 양자화 정도와 빠른 단광자 방출 속도를 나타내는 2차 광자 상관 관계 그래프.
2013.07.22 조회수 20207
양자점 기반 단파장 초고속 양자 광원 개발
- 나노 오벨리스크 구조 위에 양자점을 형성해 고효율 단광자 광원 개발 -- 단파장 가시광선 대역에서 작동하는 초고속 반도체 양자 광원 연구 -
우리 학교 물리학과 조용훈 교수팀은 오벨리스크 모양의 나노 구조물을 만들고 꼭대기 부분에 높은 신뢰도를 갖는 반도체 단일 양자점을 형성해 초고속 고효율 단광자 방출을 구현하는데 성공했다.
연구결과는 네이처(Nature)가 발행하는 "사이언티픽 리포트(Scientific Reports)" 7월 5일자 온라인판에 게재됐다.
반도체 양자점은 전자를 수 나노미터 크기에 3차원적으로 구속해 불연속적인 에너지 준위를 갖는 원자와 유사한 특성을 나타낸다. 이 성질을 이용하면 차세대 양자정보 통신, 양자 암호의 핵심 구성 요소인 양자광원을 개발할 수 있다.
특히, 반도체 양자점의 경우 높은 구동 온도, 안정성, 빠른 광자 방출, 전류 구동 가능성과 같은 많은 장점을 가지고 있어 차세대 핵심 기술 중 하나로 꼽히고 있다.
그러나 기존의 자발 형성 양자점의 경우, 평면 구조 안에 양자점들이 높은 밀도로 묻혀 있어 단일 양자점 하나의 특성을 파악하기 어렵고 광자 방출 효율이 매우 제한돼 있는 한계가 있다. 또 구성하는 층 사이의 응력으로 인한 내부 전기장 효과 때문에 전자와 정공 사이의 재결합이 어려워 내부 양자 효율이 낮은 문제가 있었다.조 교수 연구팀은 단파장의 빛을 내는 넓은 띠구조를 갖는 질화물 반도체를 이용해 오벨리스크 형태(뾰족한 팁 모양)의 나노 구조를 제작했다. 그 위에 얇은 활성층 구조를 다시 성장해 나노 팁 끝에 단일 양자점을 위치시키는데 성공해 스펙트럼 폭이 매우 작은 에너지 준위에서 발생하는 초고속 단광자 특성을 확인했다.
이 같은 독특한 나노 구조를 활용하면, 패터닝 등의 공정 없이도 단일 양자구조를 얻기가 쉽고, 양자점에서 생성된 빛이 외부로 쉽게 빠져나올 수 있다는 장점이 있다.
이와 함께 연구팀은 박막 형태와는 달리 오벨리스크 형태의 나노구조의 경우 응력을 크게 감소시켜 내부 전기장 효과도 상쇄돼 내부 양자 효율이 크게 증가하는 현상을 밝혔다.
이번에 개발된 양자광원은 발광파장이 기존 장파장 적외선 대역이 아닌 단파장 가시광(400nm) 대역이기 때문에 자유 공간에서의 통신에 사용이 가능하고 광자 검출 효율이 높은 가시광 대역의 검출기를 사용할 수 있다.
조용훈 교수는 “기존의 양자점 성장 방식과는 달리 비교적 쉽게 단일 양자점을 형성하여 제어할 수 있고, 이를 통해 매우 빠른 단일 광자 생성이 가능해 실용적인 양자광원 개발에 기여할 수 있을 것으로 기대된다”며 “오벨리스크 형태 나노구조의 특성 상 손쉽게 분리 및 다른 기판과의 결합이 가능해 단일 칩 양자 광소자 제작에도 활용될 수 있다”고 말했다.
KAIST 물리학과 조용훈 교수 지도아래 김제형(제1저자), 고영호(제2저자) 박사과정 학생이 주도적으로 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업 및 WCU 사업의 지원으로 수행됐다.
그림1. (왼쪽) 프랑스 파리에 위치한 오벨리스크 사진. (오른쪽) 제작된 오벨리스크형 나노 구조의 전자현미경 이미지.
그림2. (왼쪽) 오벨리스크형 나노구조와 기존 평면 박막 구조에 내재된 양자점을 비교한 개념도. (오른쪽) 오벨리스크 나노구조 끝에 형성된 단일 양자점에서 방출되는 좁은 선폭의 스펙트럼과 광원의 양자화 정도와 빠른 단광자 방출 속도를 나타내는 2차 광자 상관 관계 그래프.
2013.07.22 조회수 20207 -
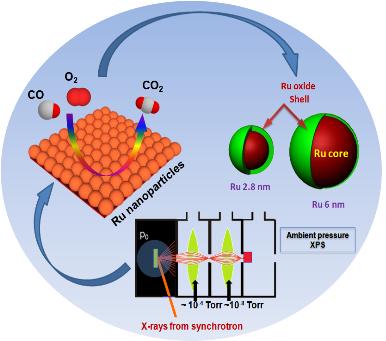 나노촉매의 활성도를 효과적으로 높일 수 있는 원리 규명
박정영 교수
- Nano Letters 발표,“활성도는 높이고 소모는 줄이는 신개념 촉매물질 개발 가능”-
나노촉매*에 산화막을 형성하여 활성도를 자유자재로 제어할 수 있는 기술이 국내 연구진에 의해 개발됨에 따라, 활성도를 극대화하고 소모를 최소화하는 새로운 촉매물질 개발에 가능성이 열렸다.
* 나노촉매(Nanocatalysts) : 표면적이 높은 산화물 지지체에 나노미터(10억분의 1미터) 크기의 금속입자가 분산되어 있는 구조로, 표면에서 기체 반응을 원활하게 하는 재료
우리 학교 EEWS대학원 박정영 교수(42세)가 주도하고 캄란 카디르 박사과정생(Kamran Qadir, 제1저자), 울산과기대 주상훈 교수, 한양대 문봉진 교수 및 UC버클리대 가보 소모자이 교수가 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약연구)과 WCU육성사업 및 지식경제부 둥의 지원으로 수행되었고, 나노분야의 권위 있는 학술지인 ‘Nano Letters’ 온라인 속보(10월 15일)에 게재되었다.(논문명: Intrinsic Relation between Catalytic Activity of CO Oxidation on Ru Nanoparticles and Ru Oxides Uncovered with Ambient Pressure XPS)
우리가 일상생활에서 사용하고 있는 제품의 대부분(80% 이상)은 촉매를 이용해 만들어질 정도로, 촉매는 우리 생활에서 꼭 필요하고 중요한 물질이다.
특히 전 세계 연구자들은 인류가 직면한 중요 이슈인 에너지문제와 환경문제 등을 근본적으로 해결하기 위해 친환경적인 화학공정에 사용될 새로운 나노촉매 물질을 집중적으로 개발하고 있다.
현재 실생활에서 주로 사용되는 촉매는 나노입자와 산화물로 이루어져 있다. 그 중 나노입자는 촉매의 표면적을 최대한 넓혀 촉매의 활성도를 높이는 역할을 한다.
활성도가 높은 촉매를 효과적으로 제조하기 위해서는 나노입자의 표면 산화막이 중요한 요인으로 알려져 왔다. 그러나 이를 과학적으로 입증하기 위해서는 촉매가 반응하는 환경에서 나노입자의 산화상태를 정확히 측정해야 하지만, 그 동안 많은 분석이 진공에서 이루어져와서 이를 정확히 보여주기가 힘들었다. 즉 촉매가 반응하는 환경에서 측정이 이루어지기 위해서는 상압측정이 필요하다. 최근에 개발된 상압 엑스선 광전자 분광법으로 이러한 상압에서 표면의 성분과 산화상태의 연구가 가능하게 되었다.
지금까지 연구자들이 무엇 때문에 정확히 측정하지 못했을까요?
박정영 교수 연구팀은 상압 엑스선 광전자 분광법*으로 나노입자의 산화상태를 촉매환경에서 측정하는데 성공하였다.
* 엑스선 광전자 분광법(X-ray Photoelectron Spectroscopy) : 엑스선을 물질에 쬐었을 때 나오는 광전자의 운동에너지를 조사하여 물질의 성분과 산화상태 등을 연구하는 표면분석법
박 교수팀은 2.8나노미터와 6나노미터 크기의 루테늄 나노입자 2개를 콜로이드 합성법*으로 제작하고, 랭뮤르 블라짓 기법**으로 나노입자 한 층을 표면에 증착시켰다. 연구팀은 나노입자의 산화상태를 온도와 압력을 바꿔가며 측정하였고, 크기가 큰 루테늄 나노입자가 얇은 산화막을 가진다는 결과를 도출하였다.
* 콜로이드 합성법 : 금속염과 안정제가 함께 용해되어 있는 용매에 환원제를 투입 또는 혼합하여 나노입자를 제작하는 방법. 제작 과정의 여러 인자를 바꿈으로써 입자의 크기와 모양, 성분의 제어가 가능하다.
* * 랭뮤르 블라짓(Langmuir-Blodgett) 기법 : 금속나노입자를 단층으로 제작하는 기법. 나노입자가 용액 위에 떠 있을때, 표면압력을 조절하여 나노입자 사이의 평균 간격을 조절할 수 있다.
또한 연구팀은 측정결과를 바탕으로 산화상태가 촉매의 활성도에 미치는 영향을 확인하여, 크기가 큰 루테늄 나노입자의 얇은 산화막이 촉매의 활성도를 높일 수 있고, 산화상태를 바꾸면 활성도도 제어할 수 있다는 사실을 입증하였다.
박정영 교수는 “나노입자의 산화막이 촉매환경에서 만들어지고 촉매활성도에도 직접적인 관계가 있음을 규명한 이번 연구는 활성도가 높은 촉매물질을 만드는데 응용되어 환경오염에 주요한 원인이 될 수 있는 촉매물질의 소모를 획기적으로 줄이는데 기여할 것으로 기대한다”고 연구의의를 밝혔다.
루테늄(Ru) 나노입자의 촉매환경 도중 산화상태조사 : 루테늄 나노입자에서 일어나는 촉매반응 (일산화탄소 산화반응)을 보여줌 (왼쪽). 방사광 가속기에 설치된 상압 엑스선 광전자 분광법을 이용하여 촉매환경에서 루테늄 나노입자의 산화상태가 분석이 됨 (아래). 루테늄 나노입자의 산화막의 두께가 나노입자의 크기에 관계가 되고 이는 촉매의 활성도에 직접적으로 영향을 줌 (오른쪽)
2012.11.08 조회수 23399
나노촉매의 활성도를 효과적으로 높일 수 있는 원리 규명
박정영 교수
- Nano Letters 발표,“활성도는 높이고 소모는 줄이는 신개념 촉매물질 개발 가능”-
나노촉매*에 산화막을 형성하여 활성도를 자유자재로 제어할 수 있는 기술이 국내 연구진에 의해 개발됨에 따라, 활성도를 극대화하고 소모를 최소화하는 새로운 촉매물질 개발에 가능성이 열렸다.
* 나노촉매(Nanocatalysts) : 표면적이 높은 산화물 지지체에 나노미터(10억분의 1미터) 크기의 금속입자가 분산되어 있는 구조로, 표면에서 기체 반응을 원활하게 하는 재료
우리 학교 EEWS대학원 박정영 교수(42세)가 주도하고 캄란 카디르 박사과정생(Kamran Qadir, 제1저자), 울산과기대 주상훈 교수, 한양대 문봉진 교수 및 UC버클리대 가보 소모자이 교수가 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약연구)과 WCU육성사업 및 지식경제부 둥의 지원으로 수행되었고, 나노분야의 권위 있는 학술지인 ‘Nano Letters’ 온라인 속보(10월 15일)에 게재되었다.(논문명: Intrinsic Relation between Catalytic Activity of CO Oxidation on Ru Nanoparticles and Ru Oxides Uncovered with Ambient Pressure XPS)
우리가 일상생활에서 사용하고 있는 제품의 대부분(80% 이상)은 촉매를 이용해 만들어질 정도로, 촉매는 우리 생활에서 꼭 필요하고 중요한 물질이다.
특히 전 세계 연구자들은 인류가 직면한 중요 이슈인 에너지문제와 환경문제 등을 근본적으로 해결하기 위해 친환경적인 화학공정에 사용될 새로운 나노촉매 물질을 집중적으로 개발하고 있다.
현재 실생활에서 주로 사용되는 촉매는 나노입자와 산화물로 이루어져 있다. 그 중 나노입자는 촉매의 표면적을 최대한 넓혀 촉매의 활성도를 높이는 역할을 한다.
활성도가 높은 촉매를 효과적으로 제조하기 위해서는 나노입자의 표면 산화막이 중요한 요인으로 알려져 왔다. 그러나 이를 과학적으로 입증하기 위해서는 촉매가 반응하는 환경에서 나노입자의 산화상태를 정확히 측정해야 하지만, 그 동안 많은 분석이 진공에서 이루어져와서 이를 정확히 보여주기가 힘들었다. 즉 촉매가 반응하는 환경에서 측정이 이루어지기 위해서는 상압측정이 필요하다. 최근에 개발된 상압 엑스선 광전자 분광법으로 이러한 상압에서 표면의 성분과 산화상태의 연구가 가능하게 되었다.
지금까지 연구자들이 무엇 때문에 정확히 측정하지 못했을까요?
박정영 교수 연구팀은 상압 엑스선 광전자 분광법*으로 나노입자의 산화상태를 촉매환경에서 측정하는데 성공하였다.
* 엑스선 광전자 분광법(X-ray Photoelectron Spectroscopy) : 엑스선을 물질에 쬐었을 때 나오는 광전자의 운동에너지를 조사하여 물질의 성분과 산화상태 등을 연구하는 표면분석법
박 교수팀은 2.8나노미터와 6나노미터 크기의 루테늄 나노입자 2개를 콜로이드 합성법*으로 제작하고, 랭뮤르 블라짓 기법**으로 나노입자 한 층을 표면에 증착시켰다. 연구팀은 나노입자의 산화상태를 온도와 압력을 바꿔가며 측정하였고, 크기가 큰 루테늄 나노입자가 얇은 산화막을 가진다는 결과를 도출하였다.
* 콜로이드 합성법 : 금속염과 안정제가 함께 용해되어 있는 용매에 환원제를 투입 또는 혼합하여 나노입자를 제작하는 방법. 제작 과정의 여러 인자를 바꿈으로써 입자의 크기와 모양, 성분의 제어가 가능하다.
* * 랭뮤르 블라짓(Langmuir-Blodgett) 기법 : 금속나노입자를 단층으로 제작하는 기법. 나노입자가 용액 위에 떠 있을때, 표면압력을 조절하여 나노입자 사이의 평균 간격을 조절할 수 있다.
또한 연구팀은 측정결과를 바탕으로 산화상태가 촉매의 활성도에 미치는 영향을 확인하여, 크기가 큰 루테늄 나노입자의 얇은 산화막이 촉매의 활성도를 높일 수 있고, 산화상태를 바꾸면 활성도도 제어할 수 있다는 사실을 입증하였다.
박정영 교수는 “나노입자의 산화막이 촉매환경에서 만들어지고 촉매활성도에도 직접적인 관계가 있음을 규명한 이번 연구는 활성도가 높은 촉매물질을 만드는데 응용되어 환경오염에 주요한 원인이 될 수 있는 촉매물질의 소모를 획기적으로 줄이는데 기여할 것으로 기대한다”고 연구의의를 밝혔다.
루테늄(Ru) 나노입자의 촉매환경 도중 산화상태조사 : 루테늄 나노입자에서 일어나는 촉매반응 (일산화탄소 산화반응)을 보여줌 (왼쪽). 방사광 가속기에 설치된 상압 엑스선 광전자 분광법을 이용하여 촉매환경에서 루테늄 나노입자의 산화상태가 분석이 됨 (아래). 루테늄 나노입자의 산화막의 두께가 나노입자의 크기에 관계가 되고 이는 촉매의 활성도에 직접적으로 영향을 줌 (오른쪽)
2012.11.08 조회수 23399