-
 합성색소 문제를 해결하는 미생물 기반 천연색소 생한을 위한 시스템 대사공학 전략 제시
우리 대학 생명화학공학과 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생을 포함한 이상엽 특훈교수 연구팀이 `미생물 기반의 천연색소 생산을 위한 시스템 대사공학 전략’ 논문을 발표했다고 6일 밝혔다.
생명화학공학과의 신디(Cindy Pricilia Surya Prabowo) 박사과정생, 은현민 박사과정생, 양동수 박사, 담라(Damla) 박사과정생과 농촌진흥청 농업미생물과의 김수진 박사가 함께 참여한 이번 논문은 셀(Cell) 誌가 발행하는 화학 분야 권위 리뷰 저널인 `화학의 동향(Trends in Chemistry)' 7월호 표지논문 및 주 논문 (Featured Article)으로 1일 字 게재됐다.
※ 논문명 : Production of natural colorants by metabolically engineered microorganisms
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), Cindy(한국과학기술원, 공동 제1 저자), 은현민(한국과학기술원, 공동 제1 저자), 양동수(한국과학기술원, 제3 저자), Damla(한국과학기술원, 공동 제4저자), 김수진(농촌진흥청, 제5저자), Raman(농촌진흥청, 제 6저자) 포함 총 7명
천연자원으로부터 비롯되는 천연색소는 식품, 의약품, 화장품, 옷감 염색 등에서 널리 사용될 정도로 인류 역사에서 오랫동안 사용됐지만, 석유화학 산업의 발달과 함께 화학 합성 기반 색소의 수요도 급속도로 늘기 시작했다. 그러나 합성 색소를 지나치게 많이 사용함으로써 환경 오염 초래 및 인류의 건강에 악영향을 미칠 수 있으며, 특히 전체 산업용 폐수 중 약 17~20%의 폐수가 합성 색소를 옷감 염색에 사용하면서 발생하는 폐수로부터 비롯되는 것으로 보고된 바 있다.
환경 오염, 그리고 헬스케어에 대한 인식이 높아짐에 따라 천연색소에 대한 소비자 수요가 점점 증가하고 있지만, 천연자원으로부터 얻을 수 있는 한정된 천연색소의 양, 값비싼 추출 및 정제 공정, 낮은 수율 등의 문제로 인해 대량으로 천연색소를 생산해 시장에 공급하기에는 아직은 한계가 있다. 이러한 문제를 해결하기 위해 천연색소를 친환경적이며 고효율로 생산하기 위한 미생물 세포 공장을 개발하려는 노력이 이뤄지고 있다. 미생물 세포 공장 구축을 위한 핵심 전략인 시스템 대사공학은 기존의 석유화학 산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 우리 대학 생명화학공학과 이상엽 특훈교수가 창시한 연구 분야다.
학생들을 지도한 이상엽 특훈교수는 “학생들이 미생물 기반의 천연색소 생산을 위한 시스템 대사공학 연구를 체계적으로 분석 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있고, 권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 밝혔다. 이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
연구팀은 이번 연구에서 미생물 세포 공장을 개발해 생산된 대표 천연색소들의 생합성 경로를 총망라해, 최신 연구내용과 흐름을 한눈에 파악할 수 있는 대사회로 지도를 정리했다. 이번 논문에서는 천연색소 생산 미생물 세포 공장 개발을 위한 중요한 시스템 대사공학 전략들을 정리했고, 각 단계에서 활용할 수 있는 최신 도구 및 전략을 대사공학이 나아가야 할 방향과 함께 제시했다.
공동 제1 저자인 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생은 "합성 색소로부터 비롯되는 환경 오염 문제와 헬스케어에 대한 소비자들의 인식이 높아짐에 따라 천연색소 산업의 중요성이 더욱 대두되고 있다ˮ라고 말했으며, 공동 저자인 농촌진흥청 농업미생물과 김수진 박사는 "인류가 건강한 삶을 지속적으로 영위하기 위해 천연색소를 대사공학적으로 생산하는 연구가 갈수록 중요해질 것ˮ이라고 말했다.
한편 이번 연구는 농촌진흥청이 지원하는 농업미생물사업단(단장 장판식)의 ‘카로티노이드 생산 미생물 세포 공장 개발’ 과제(과제책임자 국립농업과학원 김수진 박사)의 지원을 받아 수행됐다.
합성색소 문제를 해결하는 미생물 기반 천연색소 생한을 위한 시스템 대사공학 전략 제시
우리 대학 생명화학공학과 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생을 포함한 이상엽 특훈교수 연구팀이 `미생물 기반의 천연색소 생산을 위한 시스템 대사공학 전략’ 논문을 발표했다고 6일 밝혔다.
생명화학공학과의 신디(Cindy Pricilia Surya Prabowo) 박사과정생, 은현민 박사과정생, 양동수 박사, 담라(Damla) 박사과정생과 농촌진흥청 농업미생물과의 김수진 박사가 함께 참여한 이번 논문은 셀(Cell) 誌가 발행하는 화학 분야 권위 리뷰 저널인 `화학의 동향(Trends in Chemistry)' 7월호 표지논문 및 주 논문 (Featured Article)으로 1일 字 게재됐다.
※ 논문명 : Production of natural colorants by metabolically engineered microorganisms
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), Cindy(한국과학기술원, 공동 제1 저자), 은현민(한국과학기술원, 공동 제1 저자), 양동수(한국과학기술원, 제3 저자), Damla(한국과학기술원, 공동 제4저자), 김수진(농촌진흥청, 제5저자), Raman(농촌진흥청, 제 6저자) 포함 총 7명
천연자원으로부터 비롯되는 천연색소는 식품, 의약품, 화장품, 옷감 염색 등에서 널리 사용될 정도로 인류 역사에서 오랫동안 사용됐지만, 석유화학 산업의 발달과 함께 화학 합성 기반 색소의 수요도 급속도로 늘기 시작했다. 그러나 합성 색소를 지나치게 많이 사용함으로써 환경 오염 초래 및 인류의 건강에 악영향을 미칠 수 있으며, 특히 전체 산업용 폐수 중 약 17~20%의 폐수가 합성 색소를 옷감 염색에 사용하면서 발생하는 폐수로부터 비롯되는 것으로 보고된 바 있다.
환경 오염, 그리고 헬스케어에 대한 인식이 높아짐에 따라 천연색소에 대한 소비자 수요가 점점 증가하고 있지만, 천연자원으로부터 얻을 수 있는 한정된 천연색소의 양, 값비싼 추출 및 정제 공정, 낮은 수율 등의 문제로 인해 대량으로 천연색소를 생산해 시장에 공급하기에는 아직은 한계가 있다. 이러한 문제를 해결하기 위해 천연색소를 친환경적이며 고효율로 생산하기 위한 미생물 세포 공장을 개발하려는 노력이 이뤄지고 있다. 미생물 세포 공장 구축을 위한 핵심 전략인 시스템 대사공학은 기존의 석유화학 산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 우리 대학 생명화학공학과 이상엽 특훈교수가 창시한 연구 분야다.
학생들을 지도한 이상엽 특훈교수는 “학생들이 미생물 기반의 천연색소 생산을 위한 시스템 대사공학 연구를 체계적으로 분석 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있고, 권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 밝혔다. 이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
연구팀은 이번 연구에서 미생물 세포 공장을 개발해 생산된 대표 천연색소들의 생합성 경로를 총망라해, 최신 연구내용과 흐름을 한눈에 파악할 수 있는 대사회로 지도를 정리했다. 이번 논문에서는 천연색소 생산 미생물 세포 공장 개발을 위한 중요한 시스템 대사공학 전략들을 정리했고, 각 단계에서 활용할 수 있는 최신 도구 및 전략을 대사공학이 나아가야 할 방향과 함께 제시했다.
공동 제1 저자인 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생은 "합성 색소로부터 비롯되는 환경 오염 문제와 헬스케어에 대한 소비자들의 인식이 높아짐에 따라 천연색소 산업의 중요성이 더욱 대두되고 있다ˮ라고 말했으며, 공동 저자인 농촌진흥청 농업미생물과 김수진 박사는 "인류가 건강한 삶을 지속적으로 영위하기 위해 천연색소를 대사공학적으로 생산하는 연구가 갈수록 중요해질 것ˮ이라고 말했다.
한편 이번 연구는 농촌진흥청이 지원하는 농업미생물사업단(단장 장판식)의 ‘카로티노이드 생산 미생물 세포 공장 개발’ 과제(과제책임자 국립농업과학원 김수진 박사)의 지원을 받아 수행됐다.
2022.07.06
조회수 11262
-
 차세대 에너지 변환기술인 양방향 고체산화물 연료전지용 스마트 전극 개발
우리 대학 기계공학과 이강택 교수 연구팀이 포스텍 한정우 교수, 한국세라믹기술원 신태호 박사팀과의 공동 연구를 통해 양방향 고체산화물 연료전지(SOFC)용 고성능 전극 소재 개발에 성공했다고 21일 밝혔다.
양방향 고체산화물 연료전지는 고온에서 수소와 산소를 자발 반응시켜 고효율로 전력으로 변환(연료전지 모드) 하고, 전기를 가하면 청정 수소(그린 수소)와 같은 친환경 에너지원을 생산(전해전지 모드) 할 수 있는, 탄소중립 사회를 위한 차세대 에너지 변환 기술이다.
이러한 양방향 연료전지의 전기화학적 성능을 높이기 위해서 가역반응에서 전극의 촉매 성능을 획기적으로 높이는 것이 중요하며, 이를 위한 다양한 연구가 진행되고 있다. 그중 다공성 연료극 구조체 표면에 고성능 나노 금속 촉매를 입히는 기존 함침법의 경우 반응점을 늘리기 위해서 반복적인 증착 공정을 수행해야 하고, 고온 장기 구동 시 응집 현상으로 인한 촉매 활성도가 저하되는 한계를 갖고 있다.
연구팀은 이러한 문제점 해결을 위해 연료전지가 작동하는 환경에서, 전극 표면에 금속합금 나노촉매가 자발적으로 형성되는 용출(exsolution) 현상을 활용한 전극을 디자인 했다. 연구팀은 금속합금 나노촉매 형성을 촉진하기 위해 기존 코발타이트계 산화물 구조 내에 팔라듐(Pd)을 미량 첨가해, 양방향 구동 시 가역적으로 고활성을 갖는 전극 개발에 성공했다. 해당 방법으로 설계된 나노 합금 촉매는 페로브스카이트 격자 내부에서부터 전극 표면으로 스스로 용출돼 형성되기 때문에 전극 표면과 응집 현상 없이 강하게 결합하고, 입자의 균일도 또한 우수해 촉매 성능 향상에 큰 이점이 있다.
연구팀은 전해질 지지체 단전지에 개발된 전극을 연료극으로 사용해 성능을 측정한 결과, 연료전지 모드에서 최대출력 2.0W/cm2 (850oC), 전해전지 모드에서 전력밀도 2.23A/cm-2 (1.3V, 850oC)를 구현해, 세계 최고 수준의 양방향 연료전지 성능을 달성했다. 이는 기존 기술 대비 연료전지 모드는 1.6배, 전해전지 모드는 2.4배 향상된 결과다.
기계공학과 김경준 박사, 배경택 박사과정생, 포스텍 임채성 박사과정생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `어플라이드 카탈리시스 비: 인바이러멘탈, Applied Catalysis B: Environmental' (IF:19.503, JCR분야 0.93%) 5월 14일 字 온라인판에 게재됐다. (논문명: Concurrent promotion of phase transition and bimetallic nanocatalyst exsolution in perovskite oxides driven by Pd doping to achieve highly active bifunctional fuel electrodes for reversible solid oxide electrochemical cells)
이강택 교수는 “이번 연구를 통해서 특정 페로브스카이트 전극 물질 내 높은 환원 특성을 가지는 원소의 도핑이 산화물 전극 표면에 이종 금속 나노촉매를 선택적으로 형성하는 방아쇠 역할을 할 수 있으며, 이는 고성능 고 안정성의 양방향 고체산화물 연료전지 상용화를 선도하는 기술이 될 것”이라고 말했다.
한편 이번 연구는 과학기술정보통신부 수소에너지혁신기술개발사업, 중견연구자지원사업 그리고 나노 및 소재 기술개발사업의 지원으로 수행됐다.
차세대 에너지 변환기술인 양방향 고체산화물 연료전지용 스마트 전극 개발
우리 대학 기계공학과 이강택 교수 연구팀이 포스텍 한정우 교수, 한국세라믹기술원 신태호 박사팀과의 공동 연구를 통해 양방향 고체산화물 연료전지(SOFC)용 고성능 전극 소재 개발에 성공했다고 21일 밝혔다.
양방향 고체산화물 연료전지는 고온에서 수소와 산소를 자발 반응시켜 고효율로 전력으로 변환(연료전지 모드) 하고, 전기를 가하면 청정 수소(그린 수소)와 같은 친환경 에너지원을 생산(전해전지 모드) 할 수 있는, 탄소중립 사회를 위한 차세대 에너지 변환 기술이다.
이러한 양방향 연료전지의 전기화학적 성능을 높이기 위해서 가역반응에서 전극의 촉매 성능을 획기적으로 높이는 것이 중요하며, 이를 위한 다양한 연구가 진행되고 있다. 그중 다공성 연료극 구조체 표면에 고성능 나노 금속 촉매를 입히는 기존 함침법의 경우 반응점을 늘리기 위해서 반복적인 증착 공정을 수행해야 하고, 고온 장기 구동 시 응집 현상으로 인한 촉매 활성도가 저하되는 한계를 갖고 있다.
연구팀은 이러한 문제점 해결을 위해 연료전지가 작동하는 환경에서, 전극 표면에 금속합금 나노촉매가 자발적으로 형성되는 용출(exsolution) 현상을 활용한 전극을 디자인 했다. 연구팀은 금속합금 나노촉매 형성을 촉진하기 위해 기존 코발타이트계 산화물 구조 내에 팔라듐(Pd)을 미량 첨가해, 양방향 구동 시 가역적으로 고활성을 갖는 전극 개발에 성공했다. 해당 방법으로 설계된 나노 합금 촉매는 페로브스카이트 격자 내부에서부터 전극 표면으로 스스로 용출돼 형성되기 때문에 전극 표면과 응집 현상 없이 강하게 결합하고, 입자의 균일도 또한 우수해 촉매 성능 향상에 큰 이점이 있다.
연구팀은 전해질 지지체 단전지에 개발된 전극을 연료극으로 사용해 성능을 측정한 결과, 연료전지 모드에서 최대출력 2.0W/cm2 (850oC), 전해전지 모드에서 전력밀도 2.23A/cm-2 (1.3V, 850oC)를 구현해, 세계 최고 수준의 양방향 연료전지 성능을 달성했다. 이는 기존 기술 대비 연료전지 모드는 1.6배, 전해전지 모드는 2.4배 향상된 결과다.
기계공학과 김경준 박사, 배경택 박사과정생, 포스텍 임채성 박사과정생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `어플라이드 카탈리시스 비: 인바이러멘탈, Applied Catalysis B: Environmental' (IF:19.503, JCR분야 0.93%) 5월 14일 字 온라인판에 게재됐다. (논문명: Concurrent promotion of phase transition and bimetallic nanocatalyst exsolution in perovskite oxides driven by Pd doping to achieve highly active bifunctional fuel electrodes for reversible solid oxide electrochemical cells)
이강택 교수는 “이번 연구를 통해서 특정 페로브스카이트 전극 물질 내 높은 환원 특성을 가지는 원소의 도핑이 산화물 전극 표면에 이종 금속 나노촉매를 선택적으로 형성하는 방아쇠 역할을 할 수 있으며, 이는 고성능 고 안정성의 양방향 고체산화물 연료전지 상용화를 선도하는 기술이 될 것”이라고 말했다.
한편 이번 연구는 과학기술정보통신부 수소에너지혁신기술개발사업, 중견연구자지원사업 그리고 나노 및 소재 기술개발사업의 지원으로 수행됐다.
2022.06.21
조회수 9460
-
 디스플레이 소재로 빛 이용해 친환경 암모니아 합성법 제시
우리 대학 생명화학공학과 이도창 교수, 이상엽 특훈교수, 박영신 연구교수 연구팀이 디스플레이 소재인 양자점(퀀텀닷)을 이용해 *질소 고정 박테리아의 암모니아 생산 효율을 대폭 늘렸다고 16일 밝혔다.
☞ 질소 고정(Nitrogen Fixation) : 공기 중 질소 기체 분자(N₂)를 암모니아(NH₃)를 비롯한 질소화합물로 전환하는 과정을 말한다.
이 교수 연구팀은 양자점에 의해 흡수된 빛 에너지가 박테리아의 암모니아 합성 반응에 사용되도록 설계했으며, 그 결과 박테리아의 암모니아 생산량을 큰 폭으로 증가시킬 수 있었다. 이를 위해 연구팀은 양자점을 질소고정 박테리아 안에 더 많이 넣을 수 있는 방법을 제시했다.
생명화학공학과 고성준 박사가 제1저자로 참여한 이번 연구의 결과는 국제 학술지 `미국 화학회지(JACS)'에 표지 논문으로 선정돼 출판됐다. (논문명 : Light-Driven Ammonia Production by Azotobacter vinelandii Cultured in Medium Containing Colloidal Quantum Dots).
질소 고정 박테리아는 질소 고정 효소를 이용해 대기 중 질소를 암모니아로 전환하여 생장에 필요한 단백질을 생산한다. 이러한 질소 고정 반응은 화학적 암모니아 합성법인 하버-보슈 공정에 비해 에너지 소비와 이산화탄소 배출이 현저하게 적다.
하지만, 박테리아는 생장에 필요한 만큼만 암모니아를 생산하도록 진화돼 질소 고정 효소의 반응이 느리기에 이를 산업적으로 활용하기 어렵다. 질소 고정 반응이 느린 이유는 효소의 두 가지 구성요소(전자 전달부, 촉매 반응부)의 비효율적인 상호작용 때문이다. 전자 전달부가 촉매 반응부에 전자를 공급한 후, 반드시 탈착돼야만 촉매 반응부가 새로운 전자를 추가로 공급받아 암모니아를 생성할 수 있다.
연구팀은 문제 해결을 위해 빛을 흡수하는 양자점을 박테리아의 질소 고정 반응에 전자 공급원으로 활용해 나노·바이오 복합 시스템을 구축했다. 양자점은 수 나노미터의 작은 크기를 갖는 반도체 나노입자이며 디스플레이 소재로 많이 알려진 물질이다. 하지만, 양자점이 흡수한 빛 에너지를 표면에 쉽게 전달할 수 있도록 입자의 구조 및 표면을 제어하면 광 감응 및 광 촉매 소재로도 우수한 특성을 보인다. 연구팀은 질소 고정 효소의 전자 전달부 역할을 양자점으로 대체하기 위해 양자점의 코어/쉘 구조를 전자 전달에 유리하게 설계했다. 또한, 양자점이 생물학적 시스템에 결합할 수 있도록 표면 화학 특성을 제어해 수(水)분산 특성을 확보했다.
연구팀은 구조 및 표면이 제어된 양자점을 질소 고정 박테리아의 대사활동이 가장 활발한 성장기에 추가해, 박테리아의 능동적인 양자점 흡수를 유도했다. 이렇게 제작된 양자점-박테리아 복합 시스템에 빛을 조사한 결과, 질소고정 반응 속도가 증가하며 암모니아 생산량이 대폭 증가함을 확인했다. 고성준 박사는 "디스플레이 소재와 미생물의 장점을 합해 빛 에너지를 이용한 새로운 방식의 암모니아 합성법을 제시한 결과ˮ라며 "이번 연구를 활용한 그린 암모니아 생산 플랫폼을 구축한다면, 환경 및 에너지 문제에 적극적으로 대응할 수 있을 것이다ˮ라고 말했다.
한편 이번 연구는 삼성미래기술육성사업의 지원을 받아 수행됐다.
디스플레이 소재로 빛 이용해 친환경 암모니아 합성법 제시
우리 대학 생명화학공학과 이도창 교수, 이상엽 특훈교수, 박영신 연구교수 연구팀이 디스플레이 소재인 양자점(퀀텀닷)을 이용해 *질소 고정 박테리아의 암모니아 생산 효율을 대폭 늘렸다고 16일 밝혔다.
☞ 질소 고정(Nitrogen Fixation) : 공기 중 질소 기체 분자(N₂)를 암모니아(NH₃)를 비롯한 질소화합물로 전환하는 과정을 말한다.
이 교수 연구팀은 양자점에 의해 흡수된 빛 에너지가 박테리아의 암모니아 합성 반응에 사용되도록 설계했으며, 그 결과 박테리아의 암모니아 생산량을 큰 폭으로 증가시킬 수 있었다. 이를 위해 연구팀은 양자점을 질소고정 박테리아 안에 더 많이 넣을 수 있는 방법을 제시했다.
생명화학공학과 고성준 박사가 제1저자로 참여한 이번 연구의 결과는 국제 학술지 `미국 화학회지(JACS)'에 표지 논문으로 선정돼 출판됐다. (논문명 : Light-Driven Ammonia Production by Azotobacter vinelandii Cultured in Medium Containing Colloidal Quantum Dots).
질소 고정 박테리아는 질소 고정 효소를 이용해 대기 중 질소를 암모니아로 전환하여 생장에 필요한 단백질을 생산한다. 이러한 질소 고정 반응은 화학적 암모니아 합성법인 하버-보슈 공정에 비해 에너지 소비와 이산화탄소 배출이 현저하게 적다.
하지만, 박테리아는 생장에 필요한 만큼만 암모니아를 생산하도록 진화돼 질소 고정 효소의 반응이 느리기에 이를 산업적으로 활용하기 어렵다. 질소 고정 반응이 느린 이유는 효소의 두 가지 구성요소(전자 전달부, 촉매 반응부)의 비효율적인 상호작용 때문이다. 전자 전달부가 촉매 반응부에 전자를 공급한 후, 반드시 탈착돼야만 촉매 반응부가 새로운 전자를 추가로 공급받아 암모니아를 생성할 수 있다.
연구팀은 문제 해결을 위해 빛을 흡수하는 양자점을 박테리아의 질소 고정 반응에 전자 공급원으로 활용해 나노·바이오 복합 시스템을 구축했다. 양자점은 수 나노미터의 작은 크기를 갖는 반도체 나노입자이며 디스플레이 소재로 많이 알려진 물질이다. 하지만, 양자점이 흡수한 빛 에너지를 표면에 쉽게 전달할 수 있도록 입자의 구조 및 표면을 제어하면 광 감응 및 광 촉매 소재로도 우수한 특성을 보인다. 연구팀은 질소 고정 효소의 전자 전달부 역할을 양자점으로 대체하기 위해 양자점의 코어/쉘 구조를 전자 전달에 유리하게 설계했다. 또한, 양자점이 생물학적 시스템에 결합할 수 있도록 표면 화학 특성을 제어해 수(水)분산 특성을 확보했다.
연구팀은 구조 및 표면이 제어된 양자점을 질소 고정 박테리아의 대사활동이 가장 활발한 성장기에 추가해, 박테리아의 능동적인 양자점 흡수를 유도했다. 이렇게 제작된 양자점-박테리아 복합 시스템에 빛을 조사한 결과, 질소고정 반응 속도가 증가하며 암모니아 생산량이 대폭 증가함을 확인했다. 고성준 박사는 "디스플레이 소재와 미생물의 장점을 합해 빛 에너지를 이용한 새로운 방식의 암모니아 합성법을 제시한 결과ˮ라며 "이번 연구를 활용한 그린 암모니아 생산 플랫폼을 구축한다면, 환경 및 에너지 문제에 적극적으로 대응할 수 있을 것이다ˮ라고 말했다.
한편 이번 연구는 삼성미래기술육성사업의 지원을 받아 수행됐다.
2022.06.16
조회수 11996
-
 차세대 뉴로모픽 구현을 앞당길 멤리스터 기반 고신뢰성 인공 뉴런(신경세포) 어레이 개발
우리 대학 전기및전자공학부 최신현 교수 연구팀이 뛰어난 안정성과 집적도가 높은 우리 뇌의 뉴런 세포의 동작을 모사하는 *고신뢰성 차세대 저항 변화 소자(멤리스터) 어레이를 개발했다고 7일 밝혔다.
☞ 멤리스터(Memristor): 입력에 따라 소자의 저항 상태가 바뀌는 소자. 입력 전압의 크기와 길이 등에 따라 소자 내부의 저항 값이 바뀌며 정보를 저장하거나 처리한다.
최 교수 연구팀은 기존 멤리스터의 불안정한 특성을 보이는 필라멘트 기반 방식에서 벗어나, 점진적인 산소 농도를 갖는 금속산화물을 이용해 안정적이고 신뢰성 높은 인공 뉴런 어레이를 발표하였다. 기존의 멤리스터 소자는 안정성이 낮고 응용에 사용하기 위한 어레이 형태로 제작하기 힘든 문제점이 있지만, 최 교수 연구팀이 개발한 소자는 뛰어난 안정성을 갖출 뿐만 아니라, 자가 정류 특성과 높은 수율을 갖춰 대용량 어레이 형태로 집적될 수 있다. 따라서 집적도가 높고 안정적인 뉴로모픽 시스템을 구현할 때 활발히 사용될 수 있을 것으로 기대된다.
전기및전자공학부 박시온, 정학천 석박사통합과정, 박종용 석사과정이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션스(Nature Communications)' 6월호에 출판됐다. (논문명 : Experimental demonstration of highly reliable dynamic memristor for artificial neuron and neuromorphic computing)
인간의 뉴런은 들어오는 신호의 크기와 주파수에 따라 스파이크를 내보내거나 내보내지 않는 방식으로 정보를 처리한다. 현대의 컴퓨터가 빅데이터를 처리하는데 많은 에너지를 소모하는 것과 다르게, 사람의 뇌는 매우 적은 에너지만으로도 많은 양의 데이터를 빠르게 처리할 수 있다. 이러한 이유로, 신경의 효율적인 신호전달 시스템을 모사하여 컴퓨팅에 사용하는 `뉴로모픽' 하드웨어 기술이 활발히 연구되고 있다. 멤리스터 소자는 고집적, 고효율로 뉴로모픽 컴퓨팅 시스템을 구현할 수 있는 차세대 소자로 주목받고 있다.
그러나 현존하는 멤리스터로 실용적인 대용량 인공신경망 컴퓨팅(Large-scale Neural Computing) 시스템을 구현하기에는 단위 소자의 신뢰성 및 수율의 문제가 있다. 기존의 멤리스터는 절연체 내부에서 필라멘트가 마치 번개와 같이 무작위적으로 생성되고 사라지며 동작하기 때문에 제어하기가 힘들어 낮은 신뢰성을 보이게 되며, 이로 인해 안정적인 뉴로모픽 시스템을 구현하는 데 한계점으로 지적되어 왔다.
최신현 교수 연구팀은 이러한 무작위적인 필라멘트 문제를 해결하기 위해 필라멘트 기반 저항 변화가 아닌, 산소 이온의 점진적인 이동을 이용해 저항 변화 소자를 구현함으로써 소자의 신뢰성 확보하였다. 또한 단위 소자를 통한 어레이 제작 기술을 확보하여, 400개의 고신뢰성 인공 뉴런 소자를 100% 수율의 크로스바 어레이 형태로 집적하는 데 성공했다.
연구팀은 제작한 고신뢰성 인공 뉴런 어레이 기반 뉴로모픽 시스템을 이용해 항균성 단백질(anti-microbial peptide) 아미노산 서열을 학습하고, 이를 바탕으로 새로운 항균성 단백질을 만들어내는 뉴로모픽 시스템을 구현하였다.
제1 저자인 박시온 석박통합과정 연구원은 "이번에 개발한 고신뢰성 인공 뉴런 소자는 안정적인 특성과 높은 수율을 바탕으로 차세대 멤리스터 기반 뉴로모픽 컴퓨팅 시스템 구현에 기여할 수 있을 것으로 기대되며, 개발된 인공 뉴런 소자를 이용해 촉각 등을 감지하는 로봇의 인공 신경계, 시계열 데이터를 처리하는 축적 컴퓨팅(reservoir computing) 등 다양한 응용을 가능케 하여 미래 전자공학의 기반이 될 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 삼성미래육성사업의 지원을 받아 수행됐다.
차세대 뉴로모픽 구현을 앞당길 멤리스터 기반 고신뢰성 인공 뉴런(신경세포) 어레이 개발
우리 대학 전기및전자공학부 최신현 교수 연구팀이 뛰어난 안정성과 집적도가 높은 우리 뇌의 뉴런 세포의 동작을 모사하는 *고신뢰성 차세대 저항 변화 소자(멤리스터) 어레이를 개발했다고 7일 밝혔다.
☞ 멤리스터(Memristor): 입력에 따라 소자의 저항 상태가 바뀌는 소자. 입력 전압의 크기와 길이 등에 따라 소자 내부의 저항 값이 바뀌며 정보를 저장하거나 처리한다.
최 교수 연구팀은 기존 멤리스터의 불안정한 특성을 보이는 필라멘트 기반 방식에서 벗어나, 점진적인 산소 농도를 갖는 금속산화물을 이용해 안정적이고 신뢰성 높은 인공 뉴런 어레이를 발표하였다. 기존의 멤리스터 소자는 안정성이 낮고 응용에 사용하기 위한 어레이 형태로 제작하기 힘든 문제점이 있지만, 최 교수 연구팀이 개발한 소자는 뛰어난 안정성을 갖출 뿐만 아니라, 자가 정류 특성과 높은 수율을 갖춰 대용량 어레이 형태로 집적될 수 있다. 따라서 집적도가 높고 안정적인 뉴로모픽 시스템을 구현할 때 활발히 사용될 수 있을 것으로 기대된다.
전기및전자공학부 박시온, 정학천 석박사통합과정, 박종용 석사과정이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션스(Nature Communications)' 6월호에 출판됐다. (논문명 : Experimental demonstration of highly reliable dynamic memristor for artificial neuron and neuromorphic computing)
인간의 뉴런은 들어오는 신호의 크기와 주파수에 따라 스파이크를 내보내거나 내보내지 않는 방식으로 정보를 처리한다. 현대의 컴퓨터가 빅데이터를 처리하는데 많은 에너지를 소모하는 것과 다르게, 사람의 뇌는 매우 적은 에너지만으로도 많은 양의 데이터를 빠르게 처리할 수 있다. 이러한 이유로, 신경의 효율적인 신호전달 시스템을 모사하여 컴퓨팅에 사용하는 `뉴로모픽' 하드웨어 기술이 활발히 연구되고 있다. 멤리스터 소자는 고집적, 고효율로 뉴로모픽 컴퓨팅 시스템을 구현할 수 있는 차세대 소자로 주목받고 있다.
그러나 현존하는 멤리스터로 실용적인 대용량 인공신경망 컴퓨팅(Large-scale Neural Computing) 시스템을 구현하기에는 단위 소자의 신뢰성 및 수율의 문제가 있다. 기존의 멤리스터는 절연체 내부에서 필라멘트가 마치 번개와 같이 무작위적으로 생성되고 사라지며 동작하기 때문에 제어하기가 힘들어 낮은 신뢰성을 보이게 되며, 이로 인해 안정적인 뉴로모픽 시스템을 구현하는 데 한계점으로 지적되어 왔다.
최신현 교수 연구팀은 이러한 무작위적인 필라멘트 문제를 해결하기 위해 필라멘트 기반 저항 변화가 아닌, 산소 이온의 점진적인 이동을 이용해 저항 변화 소자를 구현함으로써 소자의 신뢰성 확보하였다. 또한 단위 소자를 통한 어레이 제작 기술을 확보하여, 400개의 고신뢰성 인공 뉴런 소자를 100% 수율의 크로스바 어레이 형태로 집적하는 데 성공했다.
연구팀은 제작한 고신뢰성 인공 뉴런 어레이 기반 뉴로모픽 시스템을 이용해 항균성 단백질(anti-microbial peptide) 아미노산 서열을 학습하고, 이를 바탕으로 새로운 항균성 단백질을 만들어내는 뉴로모픽 시스템을 구현하였다.
제1 저자인 박시온 석박통합과정 연구원은 "이번에 개발한 고신뢰성 인공 뉴런 소자는 안정적인 특성과 높은 수율을 바탕으로 차세대 멤리스터 기반 뉴로모픽 컴퓨팅 시스템 구현에 기여할 수 있을 것으로 기대되며, 개발된 인공 뉴런 소자를 이용해 촉각 등을 감지하는 로봇의 인공 신경계, 시계열 데이터를 처리하는 축적 컴퓨팅(reservoir computing) 등 다양한 응용을 가능케 하여 미래 전자공학의 기반이 될 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 삼성미래육성사업의 지원을 받아 수행됐다.
2022.06.07
조회수 12308
-
 실제 약물로 개발되는 단백질-리간드 상호작용 예측 인공지능 모델 개발
우리 대학 연구진이 물리화학적 아이디어를 인공지능 딥러닝에 접목해 기존의 방법보다 일반화 성능이 높은 단백질-리간드 상호작용 예측 모델을 개발했다. 리간드란 수용체와 같은 큰 생체 분자에 특이적으로 결합하는 물질을 말하며, 생체 내의 중요한 요소이자 의약품의 개발 등에 큰 역할을 한다.
화학과 김우연 교수 연구팀이 교원창업 인공지능 신약 개발 스타트업 HITS 연구진과 함께 물리 기반 삼차원 그래프 심층 신경망을 이용해 일반화 성능을 높인 단백질-리간드 상호작용 예측 모델을 개발했다고 17일 밝혔다.
약물 후보 분자를 발굴하기 위해서 타깃 단백질과 강하게 결합하는 리간드를 찾는 것이 중요하다. 하지만 유효 물질을 찾기 위해 수백만에서 수천만 개의 무작위 리간드 라이브러리를 대상으로 실험 전수 조사를 수행하는 것은 천문학적인 시간과 비용이 필요하다. 이러한 시간과 비용을 절감하기 위해 최근 단백질-리간드 상호작용 예측에 기반한 가상탐색(virtual screening) 기술이 주목받고 있다.
기존의 상호작용 예측 인공지능 모델들은 학습에 사용한 구조에 대해서는 높은 예측 성능을 보여주지만, 새로운 단백질 구조에 대해서는 낮은 성능을 보이는 과적합(over-fitting)이 문제가 됐다. 과적합 문제는 일반적으로 모델의 복잡도에 비해 데이터가 적을 때 발생한다. 이번 연구는 이러한 과적합 문제를 해결함으로써 다양한 단백질에 대해 고른 성능을 보여주는 예측 모델을 개발하는데 주안점을 뒀다.
연구진은 물리화학적 아이디어들을 딥러닝 모델에 적용해 모델의 복잡도를 줄임과 동시에 물리 시뮬레이션을 통해 부족한 데이터를 보강함으로써 과적합 문제를 해결하고자 하였다. 단백질 원자와 리간드 원자 사이의 거리에 따른 반데르발스 힘, 수소 결합력 등을 물리화학적 방정식으로 모델링하고, 매개변수를 딥러닝으로 예측함으로써 물리 법칙을 만족하는 예측을 가능하게 했다.
또한, 학습에 사용한 단백질-리간드 결정 구조가 실험적으로 판명된 가장 안정한 구조임에 착안했다. 부족한 실험 데이터를 보강하기 위해 불안정한 단백질-리간드 구조로 이루어진 수십만 개의 인공 데이터를 생성해 학습에 활용했고, 그 결과 생성된 구조에 비해 실제 구조를 안정하게 예측하도록 모델을 학습할 수 있었다.
연구진은 개발된 모델의 성능을 검증하기 위해 대조군으로 `CASF-2016 벤치마크'를 활용했다. 이 벤치마크는 다양한 단백질-리간드 구조들 사이에서 실험적으로 판명된 결정 구조에 근접한 구조를 찾는 도킹과 상대적으로 결합력이 큰 단백질-리간드 쌍을 찾는 스크리닝 등 실제 약물을 개발하는 과정에 필수적인 과제를 포함하고 있다. 검증 테스트 결과 기존에 보고된 기술에 비해 높은 도킹 및 스크리닝 성공률을 보여줬으며, 특히 스크리닝 성능은 기존에 보고된 최고 성능 대비 약 두 배 높은 수치를 보였다.
연구진이 개발한 물리 기반 딥러닝 방법론의 또 다른 장점은 예측의 결과를 물리적으로 해석 가능하다는 것이다. 이는 딥러닝으로 최적화된 물리화학 식을 통해 최종 상호작용 값을 예측하기 때문이다. 리간드 분자 내 원자별 상호작용 에너지의 기여도를 분석함으로써 어떤 작용기가 단백질-리간드 결합에 있어서 중요한 역할을 했는지 파악할 수 있으며, 이와 같은 정보는 추후 약물 설계를 통해 성능을 높이는 데 직접 활용할 수 있다.
공동 제1 저자로 참여한 화학과 문석현, 정원호, 양수정(현재 MIT 박사과정) 박사과정 학생들은 "데이터가 적은 화학 및 바이오 분야에서 일반화 문제는 항상 중요한 문제로 강조돼왔다ˮ며 "이번 연구에서 사용한 물리 기반 딥러닝 방법론은 단백질-리간드 간 상호작용 예측 뿐 아니라 다양한 물리 문제에 적용될 수 있을 것ˮ이라고 말했다.
한국연구재단의 지원을 받아 수행된 이번 연구는 국제 학술지 `Chemical Science(IF=9.825)' 2022년 4월 13호에 표지 논문 및 `금주의 논문(Pick of the Week)'으로 선정됐다. (논문명 : PIGNet: a physics-informed deep learning model toward generalized drug–target interaction predictions, 논문 링크 : https://doi.org/10.1039/D1SC06946B)
실제 약물로 개발되는 단백질-리간드 상호작용 예측 인공지능 모델 개발
우리 대학 연구진이 물리화학적 아이디어를 인공지능 딥러닝에 접목해 기존의 방법보다 일반화 성능이 높은 단백질-리간드 상호작용 예측 모델을 개발했다. 리간드란 수용체와 같은 큰 생체 분자에 특이적으로 결합하는 물질을 말하며, 생체 내의 중요한 요소이자 의약품의 개발 등에 큰 역할을 한다.
화학과 김우연 교수 연구팀이 교원창업 인공지능 신약 개발 스타트업 HITS 연구진과 함께 물리 기반 삼차원 그래프 심층 신경망을 이용해 일반화 성능을 높인 단백질-리간드 상호작용 예측 모델을 개발했다고 17일 밝혔다.
약물 후보 분자를 발굴하기 위해서 타깃 단백질과 강하게 결합하는 리간드를 찾는 것이 중요하다. 하지만 유효 물질을 찾기 위해 수백만에서 수천만 개의 무작위 리간드 라이브러리를 대상으로 실험 전수 조사를 수행하는 것은 천문학적인 시간과 비용이 필요하다. 이러한 시간과 비용을 절감하기 위해 최근 단백질-리간드 상호작용 예측에 기반한 가상탐색(virtual screening) 기술이 주목받고 있다.
기존의 상호작용 예측 인공지능 모델들은 학습에 사용한 구조에 대해서는 높은 예측 성능을 보여주지만, 새로운 단백질 구조에 대해서는 낮은 성능을 보이는 과적합(over-fitting)이 문제가 됐다. 과적합 문제는 일반적으로 모델의 복잡도에 비해 데이터가 적을 때 발생한다. 이번 연구는 이러한 과적합 문제를 해결함으로써 다양한 단백질에 대해 고른 성능을 보여주는 예측 모델을 개발하는데 주안점을 뒀다.
연구진은 물리화학적 아이디어들을 딥러닝 모델에 적용해 모델의 복잡도를 줄임과 동시에 물리 시뮬레이션을 통해 부족한 데이터를 보강함으로써 과적합 문제를 해결하고자 하였다. 단백질 원자와 리간드 원자 사이의 거리에 따른 반데르발스 힘, 수소 결합력 등을 물리화학적 방정식으로 모델링하고, 매개변수를 딥러닝으로 예측함으로써 물리 법칙을 만족하는 예측을 가능하게 했다.
또한, 학습에 사용한 단백질-리간드 결정 구조가 실험적으로 판명된 가장 안정한 구조임에 착안했다. 부족한 실험 데이터를 보강하기 위해 불안정한 단백질-리간드 구조로 이루어진 수십만 개의 인공 데이터를 생성해 학습에 활용했고, 그 결과 생성된 구조에 비해 실제 구조를 안정하게 예측하도록 모델을 학습할 수 있었다.
연구진은 개발된 모델의 성능을 검증하기 위해 대조군으로 `CASF-2016 벤치마크'를 활용했다. 이 벤치마크는 다양한 단백질-리간드 구조들 사이에서 실험적으로 판명된 결정 구조에 근접한 구조를 찾는 도킹과 상대적으로 결합력이 큰 단백질-리간드 쌍을 찾는 스크리닝 등 실제 약물을 개발하는 과정에 필수적인 과제를 포함하고 있다. 검증 테스트 결과 기존에 보고된 기술에 비해 높은 도킹 및 스크리닝 성공률을 보여줬으며, 특히 스크리닝 성능은 기존에 보고된 최고 성능 대비 약 두 배 높은 수치를 보였다.
연구진이 개발한 물리 기반 딥러닝 방법론의 또 다른 장점은 예측의 결과를 물리적으로 해석 가능하다는 것이다. 이는 딥러닝으로 최적화된 물리화학 식을 통해 최종 상호작용 값을 예측하기 때문이다. 리간드 분자 내 원자별 상호작용 에너지의 기여도를 분석함으로써 어떤 작용기가 단백질-리간드 결합에 있어서 중요한 역할을 했는지 파악할 수 있으며, 이와 같은 정보는 추후 약물 설계를 통해 성능을 높이는 데 직접 활용할 수 있다.
공동 제1 저자로 참여한 화학과 문석현, 정원호, 양수정(현재 MIT 박사과정) 박사과정 학생들은 "데이터가 적은 화학 및 바이오 분야에서 일반화 문제는 항상 중요한 문제로 강조돼왔다ˮ며 "이번 연구에서 사용한 물리 기반 딥러닝 방법론은 단백질-리간드 간 상호작용 예측 뿐 아니라 다양한 물리 문제에 적용될 수 있을 것ˮ이라고 말했다.
한국연구재단의 지원을 받아 수행된 이번 연구는 국제 학술지 `Chemical Science(IF=9.825)' 2022년 4월 13호에 표지 논문 및 `금주의 논문(Pick of the Week)'으로 선정됐다. (논문명 : PIGNet: a physics-informed deep learning model toward generalized drug–target interaction predictions, 논문 링크 : https://doi.org/10.1039/D1SC06946B)
2022.05.17
조회수 15804
-
 무질서로부터 질서를 생성하는 원리 제시
우리 대학 화학과 서명은 교수 연구팀이 물에 녹는 부분과 녹지 않는 부분이 무작위로 섞여 있는 고분자가 물에서 처음 보는 규칙적 구조를 만드는 것을 발견하고, 무질서로부터 질서가 출현할 수 있는 새로운 원리를 제시했다고 11일 밝혔다.
동전을 던져서 앞면과 뒷면이 나올 확률이 똑같다면, 아주 많이 동전을 던졌을 때 앞면이 나온 경우는 전체 중 반에 가까울 것이다. 그렇다고 해서 앞면만 연달아 나올 확률이 없는 것은 아니다. 사실 이 확률은 앞면과 뒷면이 번갈아 가며 나올 확률과 정확히 똑같다. 동전을 여러 번 던질수록 앞뒷면이 나오는 순서의 가짓수는 기하급수적으로 증가하는데(60차례 던지면 1018=100경 가지보다 많은 서열이 생겨난다), 이 서열을 보고 무작위한 과정을 통해 만들어졌는지 판별하기는 생각보다 어렵다. 반대로 온전히 무작위로 난수를 만드는 방법은 전산과학과 보안 등에서 중요한 문제다.
서명은 교수 연구팀은 무작위한 서열 사이의 짝맞추기 문제에 주목했다. 물에 녹는 부분과 녹지 않는 부분을 무작위하게 도입해서 고분자를 만들면 마치 비누에 들어있는 계면활성제나 세포막 이중 층을 이루는 지질처럼 양친매성을 띠어, 물에 넣으면 물에 녹지 않는 지용성 부분끼리 뭉치고 이를 물에 녹는 수용성 부분이 감싸는 형태로 저절로 조립된다. 이때 각 사슬의 서열은 모두 다르므로, 두 사슬이 서로 만나 지용성 부분끼리 뭉칠 때 정확히 들어맞는 짝은 그 수많은 사슬 중 한 쌍밖에 없다.
연구팀은 이 고분자를 고농도로 물에 녹이면 세포막에서 관찰되는 것과 같은 이중 층들이 반복적으로 접히면서 켜켜이 쌓이는 새로운 판상 구조를 만드는 것을 발견했다. 세포는 필요에 따라 세포막을 접어 골지체와 같은 구조를 만들지만, 이중 층 구조 자체를 안정하게 규칙적으로 접을 수 있다는 것은 처음 밝혀지는 것이다. 무작위한 서열에서는 지용성 부분이 몰려 있는 구간이 상당히 큰 확률로 발생하기 때문에, 연구진은 사슬들이 만날 때 필연적으로 짝이 맞지 않는 부분들이 생겨 평평한 판상 구조가 접히는 것으로 이 현상을 설명했다.
연구진은 "흔히 무질서하다고 간주되는 무작위 서열 속에서 어떻게 질서가 태동할 수 있는지 하나의 가능성을 엿볼 수 있었다ˮ며, "무작위성에 대한 이해를 토대로 물리적 복제방지기술(PUF)로 응용함과 아울러 구조적인 특성을 활용하여 인공 근육 등에 쓸 수 있는 나노 연성 구조 소재로 확장할 가능성을 향후 연구하고 싶다ˮ고 소감을 밝혔다.
우리 대학 화학과 신민중 석박사통합과정 학생이 제1 저자로 연구를 주도하고 포항가속기연구소 안형주 박사, 우리 대학 화학과 윤동기 교수 연구팀, GIST 이은지 교수 연구팀이 협업한 이번 연구 결과는 국제학술지 '네이처 커뮤니케이션즈(Nature Communications)'에 5월 4일 字로 온라인 게재됐다. (논문명 : Bilayer-folded Lamellar Mesophase Induced by Random Polymer Sequence)
한편 이번 연구는 한국연구재단(NRF)의 보호연구사업과 선도연구센터지원사업(멀티스케일 카이랄 구조체 연구센터), KAIST의 그랜드 챌린지 30 프로젝트의 지원을 받아 진행됐다.
무질서로부터 질서를 생성하는 원리 제시
우리 대학 화학과 서명은 교수 연구팀이 물에 녹는 부분과 녹지 않는 부분이 무작위로 섞여 있는 고분자가 물에서 처음 보는 규칙적 구조를 만드는 것을 발견하고, 무질서로부터 질서가 출현할 수 있는 새로운 원리를 제시했다고 11일 밝혔다.
동전을 던져서 앞면과 뒷면이 나올 확률이 똑같다면, 아주 많이 동전을 던졌을 때 앞면이 나온 경우는 전체 중 반에 가까울 것이다. 그렇다고 해서 앞면만 연달아 나올 확률이 없는 것은 아니다. 사실 이 확률은 앞면과 뒷면이 번갈아 가며 나올 확률과 정확히 똑같다. 동전을 여러 번 던질수록 앞뒷면이 나오는 순서의 가짓수는 기하급수적으로 증가하는데(60차례 던지면 1018=100경 가지보다 많은 서열이 생겨난다), 이 서열을 보고 무작위한 과정을 통해 만들어졌는지 판별하기는 생각보다 어렵다. 반대로 온전히 무작위로 난수를 만드는 방법은 전산과학과 보안 등에서 중요한 문제다.
서명은 교수 연구팀은 무작위한 서열 사이의 짝맞추기 문제에 주목했다. 물에 녹는 부분과 녹지 않는 부분을 무작위하게 도입해서 고분자를 만들면 마치 비누에 들어있는 계면활성제나 세포막 이중 층을 이루는 지질처럼 양친매성을 띠어, 물에 넣으면 물에 녹지 않는 지용성 부분끼리 뭉치고 이를 물에 녹는 수용성 부분이 감싸는 형태로 저절로 조립된다. 이때 각 사슬의 서열은 모두 다르므로, 두 사슬이 서로 만나 지용성 부분끼리 뭉칠 때 정확히 들어맞는 짝은 그 수많은 사슬 중 한 쌍밖에 없다.
연구팀은 이 고분자를 고농도로 물에 녹이면 세포막에서 관찰되는 것과 같은 이중 층들이 반복적으로 접히면서 켜켜이 쌓이는 새로운 판상 구조를 만드는 것을 발견했다. 세포는 필요에 따라 세포막을 접어 골지체와 같은 구조를 만들지만, 이중 층 구조 자체를 안정하게 규칙적으로 접을 수 있다는 것은 처음 밝혀지는 것이다. 무작위한 서열에서는 지용성 부분이 몰려 있는 구간이 상당히 큰 확률로 발생하기 때문에, 연구진은 사슬들이 만날 때 필연적으로 짝이 맞지 않는 부분들이 생겨 평평한 판상 구조가 접히는 것으로 이 현상을 설명했다.
연구진은 "흔히 무질서하다고 간주되는 무작위 서열 속에서 어떻게 질서가 태동할 수 있는지 하나의 가능성을 엿볼 수 있었다ˮ며, "무작위성에 대한 이해를 토대로 물리적 복제방지기술(PUF)로 응용함과 아울러 구조적인 특성을 활용하여 인공 근육 등에 쓸 수 있는 나노 연성 구조 소재로 확장할 가능성을 향후 연구하고 싶다ˮ고 소감을 밝혔다.
우리 대학 화학과 신민중 석박사통합과정 학생이 제1 저자로 연구를 주도하고 포항가속기연구소 안형주 박사, 우리 대학 화학과 윤동기 교수 연구팀, GIST 이은지 교수 연구팀이 협업한 이번 연구 결과는 국제학술지 '네이처 커뮤니케이션즈(Nature Communications)'에 5월 4일 字로 온라인 게재됐다. (논문명 : Bilayer-folded Lamellar Mesophase Induced by Random Polymer Sequence)
한편 이번 연구는 한국연구재단(NRF)의 보호연구사업과 선도연구센터지원사업(멀티스케일 카이랄 구조체 연구센터), KAIST의 그랜드 챌린지 30 프로젝트의 지원을 받아 진행됐다.
2022.05.11
조회수 10422
-
 ‘컴퓨터의 시간을 멈춘다’, 전원 공급 없이도 모든 정보가 복원, 작동되는 비휘발성 컴퓨터 최초 개발
우리 대학 전기및전자공학부 정명수 교수 연구팀(컴퓨터 아키텍처 및 메모리 시스템 연구실)이 컴퓨터의 시간을 멈추는 하드웨어/소프트웨어 기술, `경량화된 비휘발성 컴퓨팅 시스템(Lightweight Persistence Centric System, 이하 라이트PC)'을 세계 최초로 개발했다고 25일 밝혔다. 연구진의 컴퓨터에서는 시간이 멈춰진 순간의 모든 정보(실행 상태 및 데이터)는 전원 공급 여부와 관계없이 유지되며, 유지되는 모든 정보는 언제든 사용자가 원할 때 바로 복원, 작동될 수 있다.
기존의 컴퓨터는 휘발성 메모리인 D램을 메인 메모리로 사용하기 때문에 전원이 사라지면 메모리가 저장하고 있는 데이터들을 잃어버린다. 이러한 D램보다 적은 전력 소모와 큰 용량을 제공하는 비휘발성 메모리(인텔의 옵테인 메모리)는 영구적으로 데이터를 기억할 수 있는 특징이 있다. 하지만, 복잡한 내부 구조 설계로 인한 느린 성능 때문에 온전히 메인 메모리로 사용되지 못하고, D램과 함께 사용해 비휘발성 메모리에 저장되는 일부 데이터만을 선택적으로 유지하는 형태로 사용된다. 또한 이상적인 환경 아래 비휘발성 메모리의 성능이 향상돼 메인 메모리로 단독 사용하더라도, 갑작스러운 전원 공급차단의 상황에서 컴퓨터의 모든 정보를 유지할 수는 없다. 비휘발성 메모리 내부에 존재하는 휘발성 구성요소와 프로세서 자체가 가지고 있는 레지스터나 캐시 메모리(휘발성) 같은 임시 저장 공간의 데이터는 전원 공급 없이 지속적 보존이 불가능하기 때문이다.
이러한 문제 때문에 기존의 컴퓨터에서 실행 상태와 데이터를 유지하기 위해서는, D램을 포함, 프로세서가 가지고 있는 휘발성 상태의 데이터들을 비휘발성 메모리나 저장장치인 SSD 등으로 옮기는 체크포인팅 기법등이 데이터 센터나 고성능 컴퓨터에서 사용되고 있다. 하지만 체크포인팅 방식은 주기적 데이터 이동에 추가적인 시간과 전력을 소모하며, 정전 후 전원이 인가되면 시스템 전체를 재부팅하는 데이터 복구 과정을 겪어야 하는 치명적인 단점이 존재한다.
우리 대학 정명수 교수 연구팀이 개발한 라이트PC는 이러한 과정 없이 컴퓨터의 모든 프로그램 실행 상태와 데이터들을 전원 없이 비휘발성으로 유지할 수 있는 프로세서와 메모리 컨트롤러, 그리고 운영체제 기술들을 개발해냈다. 이를 위해 연구팀은 기존 메모리나 스토리지 장치 없이 지속성 메모리만을 활용하여 시스템을 구성해, 시스템의 대부분 상태를 비휘발성으로 유지하게 했으며, 전원이 끊긴 직후 전원 공급 장치의 신호에 따라 프로세서의 남아 있는 비지속성 상태들을 비휘발성으로 변환하는 장치를 통해 정전 시에도 컴퓨터의 시간을 멈출 수 있게 만들었다.
이를 위해서 연구팀이 개발한 라이트PC 기술은 프로세서의 하드웨어 데이터 경로상의 휘발성 구성요소를 최소화하고, 복잡한 내부 구조를 최대한 단순화한 뒤, 데이터 처리의 병렬성을 극대화해 사용자가 일반적인 응용실행에서 D램만 사용하는 고성능 시스템과 큰 성능 차이를 느끼지 못하도록 성능을 개선했다. 또한, 컴퓨터의 시간을 멈추는 동안 일관성 유지를 위해 프로그램 실행이 비결정적으로 진행되지 않도록 임의의 상태/데이터의 변경을 막고 다양한 형태의 지속성 기능이 추가된 운영체제를 구축했다. 일관성이 유지되기 때문에 다시 전원이 인가되면 컴퓨터는 부팅 과정 없이 멈춘 시간부터 다시 실행될 수 있다.
연구팀은 라이트PC의 실효성을 검증하기 위해 자체 제작한 시스템 보드에 시제작한 지속성 메모리를 장착해 비휘발성 컴퓨터를 구축하고, 정전 시 컴퓨터의 시간을 멈추게 하는 운영체제 프로토타입을 제작해 비휘발성 컴퓨터 위에서 실행했다. 엔터프라이즈향 응용 프로그램이 실행되는 도중 무작위 시간에 전원을 제거한 뒤, 다시 인가했을 때 전원이 사라지기 직전의 상태로 모든 프로그램 실행과 데이터가 일관성 있게 복구되는 것을 연구팀은 확인했다. 이와 더불어 라이트PC는 기존 컴퓨터 대비 최대 8배 큰 메모리와 4.3배 빠른 응용실행 및 73%의 전력 소모 절감을 보였다.
정명수 교수는 "이번에 개발된 비휘발성 컴퓨터는 대용량 메모리 제공과 동시에 높은 신뢰성 및 서비스의 안전성을 제공할 수 있어 데이터 센터나 고성능 컴퓨팅의 저전력 운영으로 인한 탄소중립에너지 효율화에 극대화를 이룰 수 있을 것으로 예상된다. 또한 관련된 연구 핵심기술은 차량, 핸드폰 모바일, 사물인터넷 장치등의 베터리 사용량을 최소화하고 초연결사회를 이루는 등 다양하게 활용될 수 있을 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 미국 뉴욕시에서 오는 6월에 열릴 컴퓨터 구조 분야 최우수 학술대회인 `이스카(International Symposium on Computer Architecture, ISCA), 2022'에 라이트PC라는 논문명(LightPC: Hardware and Software Co-Desingn for Energy-Efficient Full System Persistence)으로 발표될 예정이다.
해당 연구는 차세대 메모리 개발 및 공급업체 멤레이, 과학기술정보통신부와 한국연구재단이 추진하는 우수신진(중견연계)사업, 그리고 정보통신기획평가원의 연구 지원을 받아 진행됐다. 비휘발성 컴퓨터의 실제 동작 및 자세한 내용은 연구실 웹사이트(http://camelab.org) 및 유튜브(https://youtu.be/mlF7W_RmYRk)에서 확인할 수 있다.
‘컴퓨터의 시간을 멈춘다’, 전원 공급 없이도 모든 정보가 복원, 작동되는 비휘발성 컴퓨터 최초 개발
우리 대학 전기및전자공학부 정명수 교수 연구팀(컴퓨터 아키텍처 및 메모리 시스템 연구실)이 컴퓨터의 시간을 멈추는 하드웨어/소프트웨어 기술, `경량화된 비휘발성 컴퓨팅 시스템(Lightweight Persistence Centric System, 이하 라이트PC)'을 세계 최초로 개발했다고 25일 밝혔다. 연구진의 컴퓨터에서는 시간이 멈춰진 순간의 모든 정보(실행 상태 및 데이터)는 전원 공급 여부와 관계없이 유지되며, 유지되는 모든 정보는 언제든 사용자가 원할 때 바로 복원, 작동될 수 있다.
기존의 컴퓨터는 휘발성 메모리인 D램을 메인 메모리로 사용하기 때문에 전원이 사라지면 메모리가 저장하고 있는 데이터들을 잃어버린다. 이러한 D램보다 적은 전력 소모와 큰 용량을 제공하는 비휘발성 메모리(인텔의 옵테인 메모리)는 영구적으로 데이터를 기억할 수 있는 특징이 있다. 하지만, 복잡한 내부 구조 설계로 인한 느린 성능 때문에 온전히 메인 메모리로 사용되지 못하고, D램과 함께 사용해 비휘발성 메모리에 저장되는 일부 데이터만을 선택적으로 유지하는 형태로 사용된다. 또한 이상적인 환경 아래 비휘발성 메모리의 성능이 향상돼 메인 메모리로 단독 사용하더라도, 갑작스러운 전원 공급차단의 상황에서 컴퓨터의 모든 정보를 유지할 수는 없다. 비휘발성 메모리 내부에 존재하는 휘발성 구성요소와 프로세서 자체가 가지고 있는 레지스터나 캐시 메모리(휘발성) 같은 임시 저장 공간의 데이터는 전원 공급 없이 지속적 보존이 불가능하기 때문이다.
이러한 문제 때문에 기존의 컴퓨터에서 실행 상태와 데이터를 유지하기 위해서는, D램을 포함, 프로세서가 가지고 있는 휘발성 상태의 데이터들을 비휘발성 메모리나 저장장치인 SSD 등으로 옮기는 체크포인팅 기법등이 데이터 센터나 고성능 컴퓨터에서 사용되고 있다. 하지만 체크포인팅 방식은 주기적 데이터 이동에 추가적인 시간과 전력을 소모하며, 정전 후 전원이 인가되면 시스템 전체를 재부팅하는 데이터 복구 과정을 겪어야 하는 치명적인 단점이 존재한다.
우리 대학 정명수 교수 연구팀이 개발한 라이트PC는 이러한 과정 없이 컴퓨터의 모든 프로그램 실행 상태와 데이터들을 전원 없이 비휘발성으로 유지할 수 있는 프로세서와 메모리 컨트롤러, 그리고 운영체제 기술들을 개발해냈다. 이를 위해 연구팀은 기존 메모리나 스토리지 장치 없이 지속성 메모리만을 활용하여 시스템을 구성해, 시스템의 대부분 상태를 비휘발성으로 유지하게 했으며, 전원이 끊긴 직후 전원 공급 장치의 신호에 따라 프로세서의 남아 있는 비지속성 상태들을 비휘발성으로 변환하는 장치를 통해 정전 시에도 컴퓨터의 시간을 멈출 수 있게 만들었다.
이를 위해서 연구팀이 개발한 라이트PC 기술은 프로세서의 하드웨어 데이터 경로상의 휘발성 구성요소를 최소화하고, 복잡한 내부 구조를 최대한 단순화한 뒤, 데이터 처리의 병렬성을 극대화해 사용자가 일반적인 응용실행에서 D램만 사용하는 고성능 시스템과 큰 성능 차이를 느끼지 못하도록 성능을 개선했다. 또한, 컴퓨터의 시간을 멈추는 동안 일관성 유지를 위해 프로그램 실행이 비결정적으로 진행되지 않도록 임의의 상태/데이터의 변경을 막고 다양한 형태의 지속성 기능이 추가된 운영체제를 구축했다. 일관성이 유지되기 때문에 다시 전원이 인가되면 컴퓨터는 부팅 과정 없이 멈춘 시간부터 다시 실행될 수 있다.
연구팀은 라이트PC의 실효성을 검증하기 위해 자체 제작한 시스템 보드에 시제작한 지속성 메모리를 장착해 비휘발성 컴퓨터를 구축하고, 정전 시 컴퓨터의 시간을 멈추게 하는 운영체제 프로토타입을 제작해 비휘발성 컴퓨터 위에서 실행했다. 엔터프라이즈향 응용 프로그램이 실행되는 도중 무작위 시간에 전원을 제거한 뒤, 다시 인가했을 때 전원이 사라지기 직전의 상태로 모든 프로그램 실행과 데이터가 일관성 있게 복구되는 것을 연구팀은 확인했다. 이와 더불어 라이트PC는 기존 컴퓨터 대비 최대 8배 큰 메모리와 4.3배 빠른 응용실행 및 73%의 전력 소모 절감을 보였다.
정명수 교수는 "이번에 개발된 비휘발성 컴퓨터는 대용량 메모리 제공과 동시에 높은 신뢰성 및 서비스의 안전성을 제공할 수 있어 데이터 센터나 고성능 컴퓨팅의 저전력 운영으로 인한 탄소중립에너지 효율화에 극대화를 이룰 수 있을 것으로 예상된다. 또한 관련된 연구 핵심기술은 차량, 핸드폰 모바일, 사물인터넷 장치등의 베터리 사용량을 최소화하고 초연결사회를 이루는 등 다양하게 활용될 수 있을 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 미국 뉴욕시에서 오는 6월에 열릴 컴퓨터 구조 분야 최우수 학술대회인 `이스카(International Symposium on Computer Architecture, ISCA), 2022'에 라이트PC라는 논문명(LightPC: Hardware and Software Co-Desingn for Energy-Efficient Full System Persistence)으로 발표될 예정이다.
해당 연구는 차세대 메모리 개발 및 공급업체 멤레이, 과학기술정보통신부와 한국연구재단이 추진하는 우수신진(중견연계)사업, 그리고 정보통신기획평가원의 연구 지원을 받아 진행됐다. 비휘발성 컴퓨터의 실제 동작 및 자세한 내용은 연구실 웹사이트(http://camelab.org) 및 유튜브(https://youtu.be/mlF7W_RmYRk)에서 확인할 수 있다.
2022.04.25
조회수 10173
-
 합성생물학 기반 차세대 미생물 대사 조절 밸브 개발
국제 공동연구진이 대장균의 모든 전사종결부위*를 해독하고, 이를 바탕으로 미생물의 대사 경로를 수도꼭지처럼 자유자재로 조절하는 합성생물학** 기반 차세대 대사 조절 밸브 기술을 개발했다.
*전사종결부위: DNA가 암호화하는 정보를 RNA로 전사할 때, RNA 합성이 종결되도록 조절하는 DNA 서열
**합성생물학: 생명현상의 복잡성, 다양성으로 인해 발생하는 낮은 재현성, 예측효율 저하 등의 기존 바이오기술의 문제를 해결하기 위해 생명체의 구성요소를 설계, 제작, 조립하는 공학적 접근방식의 바이오 기술
우리 대학 생명과학과 조병관 교수, 한국생명공학연구원 이승구 박사, 바이오융합연구소 조수형 교수, 미국 캘리포니아대학교 샌디에이고(UCSD) 생명공학과(Bioengineering)의 최동희 박사, 버나드 팔슨(Bernhard Palsson) 교수 국제 공동연구팀이 대장균에 존재하는 1,600여 개의 전사종결부위를 대량으로 해독 및 발굴하고, 이를 기반으로 고부가가치 바이오화합물 생산을 위한 미생물 대사 회로 설계를 가능케 하는 합성생물학 기반 기술을 개발했다고 14일 밝혔다.
전사종결부위는 DNA가 암호화하는 유전 정보가 RNA로 전사될 때, 원하는 유전자만이 정확히 전사되도록 조절하는 역할을 한다. 그 중요성에도 불구하고 기존에는 전사 종결에 관한 데이터의 부족으로, 구체적인 조절 기작에 대한 이해가 부족했다. 연구진은 전사종결부위가 다양한 세기를 가져 인접한 유전자들의 발현을 정교하게 조절한다는 사실을 발견하고, 이를 대사회로 조절에 이용했다.
한편 미생물은 다양한 유용 바이오화합물 생산에 이용되고 있는데, 효율적인 생산을 위해서는 대사 회로의 조절이 필수적이다. 그 이유는 단순히 원하는 물질 생산을 위한 유전자만을 과도하게 발현할 경우, 미생물 생장에 필요한 양분과 에너지까지 소모해 생산에 실패하기 때문이다. 공동연구진은 개발한 전사종결부위를 통해 서로 다른 대사 회로의 세기를 수도꼭지처럼 조절해 대사물질 생산을 최적화할 수 있는 '대사 밸브 기술'을 개발했다.
기존에는 전사의 시작이 되는 프로모터, 번역의 시작이 되는 리보솜 결합 부위를 통해 유전자 발현을 조절했는데, 이에는 수많은 인자가 관여하고 있어 실험 간 편차가 크고, 고가의 화학물질을 요구하는 등 한계를 지니고 있었다. 하지만 연구진이 개발한 대사 밸브는 실험 간 편차를 기존 시스템 대비 최대 75% 억제할 수 있는 것으로 나타났고, 대사 밸브를 이용한 생산 최적화를 통해 유용 대사물질인 비타민 B8의 생산을 최대 11배 증대하는 데 성공했다.
또한 개발된 기술은 미생물의 생장 조건(영양분 및 배양 환경)에 거의 영향을 받지 않는 것으로 나타나 실험실 조건에서 출발해 산업 규모로 확장할 시 부수적인 최적화 과정을 최소화할 수 있고, 목적 화합물에 따라 첨가하는 원료와 배양 조건이 변화해도 조절 기작이 유지되는 것으로 나타났다.
이번 연구 결과는 기존에 알려지지 않았던 전사종결부위의 특성을 규명하고, 이를 대사 조절에 이용한 획기적인 시도로 차세대 대사 조절 합성생물학 기반 기술로 기대받고 있다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 C1 가스 리파이너리 프로그램 및 한국 바이오 그랜드챌린지 프로그램의 지원을 받은 KAIST 조병관 교수 연구진과 한국생명공학연구원이 추진하는 KRIBB 연구 혁신 프로그램(Research Initiative Program)의 지원을 받은 이승구 박사(한국생명공학연구원), 기초과학 연구 프로그램(Basic Science Research Program)의 지원을 받은 KAIST 조수형 교수, 노보 노르디스크 재단(Novo Nordisk Foundation)의 연구지원을 받은 버나드 팔슨(Bernhard Palsson) 교수 연구진의 협업을 통해 수행됐으며, 국제적인 학술지인 `핵산 연구(Nucleic Acids Research, 영향력지수 16.971)' 에 3월 31일 게재됐다.
(논문명 : Synthetic 3'-UTR valves for optimal metabolic flux control in Escherichia coli)
합성생물학 기반 차세대 미생물 대사 조절 밸브 개발
국제 공동연구진이 대장균의 모든 전사종결부위*를 해독하고, 이를 바탕으로 미생물의 대사 경로를 수도꼭지처럼 자유자재로 조절하는 합성생물학** 기반 차세대 대사 조절 밸브 기술을 개발했다.
*전사종결부위: DNA가 암호화하는 정보를 RNA로 전사할 때, RNA 합성이 종결되도록 조절하는 DNA 서열
**합성생물학: 생명현상의 복잡성, 다양성으로 인해 발생하는 낮은 재현성, 예측효율 저하 등의 기존 바이오기술의 문제를 해결하기 위해 생명체의 구성요소를 설계, 제작, 조립하는 공학적 접근방식의 바이오 기술
우리 대학 생명과학과 조병관 교수, 한국생명공학연구원 이승구 박사, 바이오융합연구소 조수형 교수, 미국 캘리포니아대학교 샌디에이고(UCSD) 생명공학과(Bioengineering)의 최동희 박사, 버나드 팔슨(Bernhard Palsson) 교수 국제 공동연구팀이 대장균에 존재하는 1,600여 개의 전사종결부위를 대량으로 해독 및 발굴하고, 이를 기반으로 고부가가치 바이오화합물 생산을 위한 미생물 대사 회로 설계를 가능케 하는 합성생물학 기반 기술을 개발했다고 14일 밝혔다.
전사종결부위는 DNA가 암호화하는 유전 정보가 RNA로 전사될 때, 원하는 유전자만이 정확히 전사되도록 조절하는 역할을 한다. 그 중요성에도 불구하고 기존에는 전사 종결에 관한 데이터의 부족으로, 구체적인 조절 기작에 대한 이해가 부족했다. 연구진은 전사종결부위가 다양한 세기를 가져 인접한 유전자들의 발현을 정교하게 조절한다는 사실을 발견하고, 이를 대사회로 조절에 이용했다.
한편 미생물은 다양한 유용 바이오화합물 생산에 이용되고 있는데, 효율적인 생산을 위해서는 대사 회로의 조절이 필수적이다. 그 이유는 단순히 원하는 물질 생산을 위한 유전자만을 과도하게 발현할 경우, 미생물 생장에 필요한 양분과 에너지까지 소모해 생산에 실패하기 때문이다. 공동연구진은 개발한 전사종결부위를 통해 서로 다른 대사 회로의 세기를 수도꼭지처럼 조절해 대사물질 생산을 최적화할 수 있는 '대사 밸브 기술'을 개발했다.
기존에는 전사의 시작이 되는 프로모터, 번역의 시작이 되는 리보솜 결합 부위를 통해 유전자 발현을 조절했는데, 이에는 수많은 인자가 관여하고 있어 실험 간 편차가 크고, 고가의 화학물질을 요구하는 등 한계를 지니고 있었다. 하지만 연구진이 개발한 대사 밸브는 실험 간 편차를 기존 시스템 대비 최대 75% 억제할 수 있는 것으로 나타났고, 대사 밸브를 이용한 생산 최적화를 통해 유용 대사물질인 비타민 B8의 생산을 최대 11배 증대하는 데 성공했다.
또한 개발된 기술은 미생물의 생장 조건(영양분 및 배양 환경)에 거의 영향을 받지 않는 것으로 나타나 실험실 조건에서 출발해 산업 규모로 확장할 시 부수적인 최적화 과정을 최소화할 수 있고, 목적 화합물에 따라 첨가하는 원료와 배양 조건이 변화해도 조절 기작이 유지되는 것으로 나타났다.
이번 연구 결과는 기존에 알려지지 않았던 전사종결부위의 특성을 규명하고, 이를 대사 조절에 이용한 획기적인 시도로 차세대 대사 조절 합성생물학 기반 기술로 기대받고 있다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 C1 가스 리파이너리 프로그램 및 한국 바이오 그랜드챌린지 프로그램의 지원을 받은 KAIST 조병관 교수 연구진과 한국생명공학연구원이 추진하는 KRIBB 연구 혁신 프로그램(Research Initiative Program)의 지원을 받은 이승구 박사(한국생명공학연구원), 기초과학 연구 프로그램(Basic Science Research Program)의 지원을 받은 KAIST 조수형 교수, 노보 노르디스크 재단(Novo Nordisk Foundation)의 연구지원을 받은 버나드 팔슨(Bernhard Palsson) 교수 연구진의 협업을 통해 수행됐으며, 국제적인 학술지인 `핵산 연구(Nucleic Acids Research, 영향력지수 16.971)' 에 3월 31일 게재됐다.
(논문명 : Synthetic 3'-UTR valves for optimal metabolic flux control in Escherichia coli)
2022.04.17
조회수 13258
-
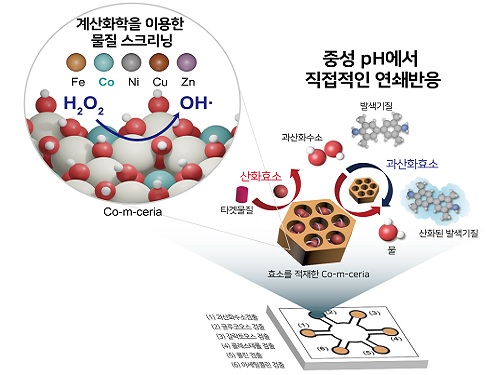 6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2022.03.07
조회수 12901
-
 전하 전달 복합체를 이용한 신개념 디스플레이 소재 개발
우리 대학 신소재공학과 정연식 교수, 전덕영 명예교수, 한국전자통신연구원(ETRI) 권병화 박사 공동 연구팀이 차세대 디스플레이 소자에 적용 가능한 신개념 금속 산화물 복합 나노소재 개발에 성공했다고 19일 밝혔다.
KAIST-ETRI 공동 연구팀은 특정 금속 산화물 나노입자가 다른 산화물 내부에서 나노미터(nm) 크기로 분산될 경우, 접촉면(인터페이스)에서 전하가 교환되면서 전하 전달 복합체(Charge transfer complex)를 형성하는 새로운 현상을 발견했다. 연구팀은 이를 유기발광다이오드(OLED) 등 고부가가치 디스플레이에 적용해 기존 상용 유기 소재 기반의 소자 성능을 뛰어넘는 데 성공했다.
오는 2월에 우리 대학 신소재공학 박사학위 취득 예정인 김무현 연구원이 주도하고 조남명 박사, ETRI 주철웅 선임연구원 등이 참여한 이번 연구는 국제학술지 `네이처 커뮤니케이션스(Nature Communications)' 1월 10일 字 온라인판에 게재됐다. (논문명: Metal Oxide Charge Transfer Complex for Effective Energy Band Tailoring in Multilayer Optoelectronics)
디스플레이 발광 셀 등 다층구조를 가지는 광전자소자에서 금속 산화물은 우수한 전기적 특성 및 안정성 덕분에 전하 수송 및 주입 층으로 널리 활용되고 있다. 하지만, 유기 발광 다이오드(OLED)에서 퀀텀닷 발광다이오드(QLED), 페로브스카이트 발광다이오드(PeLED)로 이어지는 미래 디스플레이 산업에서 이러한 금속 산화물 소재를 더 유용하게 활용하기 위해서는 에너지 레벨 및 전기전도도와 같은 특성들이 더 넓은 범위에서 제어될 수 있어야 한다.
이는 유기 발광 소재, 퀀텀닷, 페로브스카이트 등으로 발광층 소재가 매우 다양해짐에 따라 디스플레이 소자들의 성능을 극대화하기 위해서는 각각의 시스템에 최적화된 전기적 특성을 제공해야 하기 때문이다.
연구팀은 에너지 레벨 차이가 있는 두 금속 산화물 사이에서 일어나는 전하 전달(Charge transfer) 현상에 주목했다. 전하 전달 복합체는 마치 건포도 빵의 형태와 유사한 구조로 되어 있는데, 건포도(나노입자)를 더 넣게 되면 더 많은 당분(전하)이 빵(매트릭스)으로 이동하여 빵 전체가 더 달콤해지는 원리로 비유될 수 있다.
이 새로운 개념을 산화 몰리브덴(MoO3) 나노입자와 산화니켈(NiO)의 조합으로 구현해 두 금속 산화물의 전하 전달 현상을 효과적으로 유도했으며, 광범위한 에너지 레벨 조절 능력 및 최대 2.4배의 전기전도도 향상을 달성했다. 이를 녹색과 청색 OLED에 적용했고 기존의 상용 유기 소재를 적용한 소자보다 32% 더 우수한 외부양자효율을 달성함으로 높은 범용성과 성능을 입증했다.
신소재공학과 정연식 교수는 "이번 기술은 핵심 소재의 성능 제어 방법을 혁신함으로써, 실감형 메타버스 구현에 꼭 필요한 최첨단 디스플레이 구현에 기여할 것ˮ이라고 전망했다.
이번 연구는 과학기술정보통신부 및 한국연구재단이 추진하는 미래소재디스커버리지원사업(단장 최성율), 글로벌프런티어 사업(단장 김광호) 및 나노·소재기술개발사업, 그리고 산업통상자원부에서 추진하는 소재부품장비혁신 Lab기술개발사업의 지원을 받아 수행됐다.
전하 전달 복합체를 이용한 신개념 디스플레이 소재 개발
우리 대학 신소재공학과 정연식 교수, 전덕영 명예교수, 한국전자통신연구원(ETRI) 권병화 박사 공동 연구팀이 차세대 디스플레이 소자에 적용 가능한 신개념 금속 산화물 복합 나노소재 개발에 성공했다고 19일 밝혔다.
KAIST-ETRI 공동 연구팀은 특정 금속 산화물 나노입자가 다른 산화물 내부에서 나노미터(nm) 크기로 분산될 경우, 접촉면(인터페이스)에서 전하가 교환되면서 전하 전달 복합체(Charge transfer complex)를 형성하는 새로운 현상을 발견했다. 연구팀은 이를 유기발광다이오드(OLED) 등 고부가가치 디스플레이에 적용해 기존 상용 유기 소재 기반의 소자 성능을 뛰어넘는 데 성공했다.
오는 2월에 우리 대학 신소재공학 박사학위 취득 예정인 김무현 연구원이 주도하고 조남명 박사, ETRI 주철웅 선임연구원 등이 참여한 이번 연구는 국제학술지 `네이처 커뮤니케이션스(Nature Communications)' 1월 10일 字 온라인판에 게재됐다. (논문명: Metal Oxide Charge Transfer Complex for Effective Energy Band Tailoring in Multilayer Optoelectronics)
디스플레이 발광 셀 등 다층구조를 가지는 광전자소자에서 금속 산화물은 우수한 전기적 특성 및 안정성 덕분에 전하 수송 및 주입 층으로 널리 활용되고 있다. 하지만, 유기 발광 다이오드(OLED)에서 퀀텀닷 발광다이오드(QLED), 페로브스카이트 발광다이오드(PeLED)로 이어지는 미래 디스플레이 산업에서 이러한 금속 산화물 소재를 더 유용하게 활용하기 위해서는 에너지 레벨 및 전기전도도와 같은 특성들이 더 넓은 범위에서 제어될 수 있어야 한다.
이는 유기 발광 소재, 퀀텀닷, 페로브스카이트 등으로 발광층 소재가 매우 다양해짐에 따라 디스플레이 소자들의 성능을 극대화하기 위해서는 각각의 시스템에 최적화된 전기적 특성을 제공해야 하기 때문이다.
연구팀은 에너지 레벨 차이가 있는 두 금속 산화물 사이에서 일어나는 전하 전달(Charge transfer) 현상에 주목했다. 전하 전달 복합체는 마치 건포도 빵의 형태와 유사한 구조로 되어 있는데, 건포도(나노입자)를 더 넣게 되면 더 많은 당분(전하)이 빵(매트릭스)으로 이동하여 빵 전체가 더 달콤해지는 원리로 비유될 수 있다.
이 새로운 개념을 산화 몰리브덴(MoO3) 나노입자와 산화니켈(NiO)의 조합으로 구현해 두 금속 산화물의 전하 전달 현상을 효과적으로 유도했으며, 광범위한 에너지 레벨 조절 능력 및 최대 2.4배의 전기전도도 향상을 달성했다. 이를 녹색과 청색 OLED에 적용했고 기존의 상용 유기 소재를 적용한 소자보다 32% 더 우수한 외부양자효율을 달성함으로 높은 범용성과 성능을 입증했다.
신소재공학과 정연식 교수는 "이번 기술은 핵심 소재의 성능 제어 방법을 혁신함으로써, 실감형 메타버스 구현에 꼭 필요한 최첨단 디스플레이 구현에 기여할 것ˮ이라고 전망했다.
이번 연구는 과학기술정보통신부 및 한국연구재단이 추진하는 미래소재디스커버리지원사업(단장 최성율), 글로벌프런티어 사업(단장 김광호) 및 나노·소재기술개발사업, 그리고 산업통상자원부에서 추진하는 소재부품장비혁신 Lab기술개발사업의 지원을 받아 수행됐다.
2022.01.24
조회수 15125
-
 사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
2021.12.08
조회수 12574
-
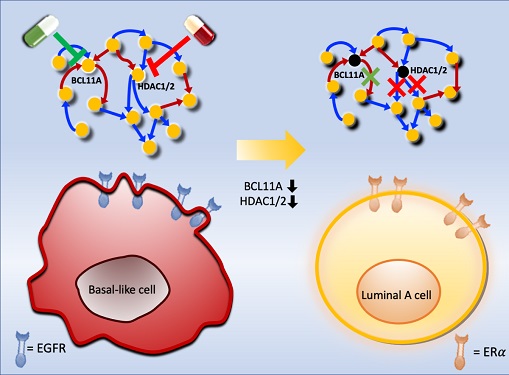 악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30
조회수 12607
 합성색소 문제를 해결하는 미생물 기반 천연색소 생한을 위한 시스템 대사공학 전략 제시
우리 대학 생명화학공학과 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생을 포함한 이상엽 특훈교수 연구팀이 `미생물 기반의 천연색소 생산을 위한 시스템 대사공학 전략’ 논문을 발표했다고 6일 밝혔다.
생명화학공학과의 신디(Cindy Pricilia Surya Prabowo) 박사과정생, 은현민 박사과정생, 양동수 박사, 담라(Damla) 박사과정생과 농촌진흥청 농업미생물과의 김수진 박사가 함께 참여한 이번 논문은 셀(Cell) 誌가 발행하는 화학 분야 권위 리뷰 저널인 `화학의 동향(Trends in Chemistry)' 7월호 표지논문 및 주 논문 (Featured Article)으로 1일 字 게재됐다.
※ 논문명 : Production of natural colorants by metabolically engineered microorganisms
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), Cindy(한국과학기술원, 공동 제1 저자), 은현민(한국과학기술원, 공동 제1 저자), 양동수(한국과학기술원, 제3 저자), Damla(한국과학기술원, 공동 제4저자), 김수진(농촌진흥청, 제5저자), Raman(농촌진흥청, 제 6저자) 포함 총 7명
천연자원으로부터 비롯되는 천연색소는 식품, 의약품, 화장품, 옷감 염색 등에서 널리 사용될 정도로 인류 역사에서 오랫동안 사용됐지만, 석유화학 산업의 발달과 함께 화학 합성 기반 색소의 수요도 급속도로 늘기 시작했다. 그러나 합성 색소를 지나치게 많이 사용함으로써 환경 오염 초래 및 인류의 건강에 악영향을 미칠 수 있으며, 특히 전체 산업용 폐수 중 약 17~20%의 폐수가 합성 색소를 옷감 염색에 사용하면서 발생하는 폐수로부터 비롯되는 것으로 보고된 바 있다.
환경 오염, 그리고 헬스케어에 대한 인식이 높아짐에 따라 천연색소에 대한 소비자 수요가 점점 증가하고 있지만, 천연자원으로부터 얻을 수 있는 한정된 천연색소의 양, 값비싼 추출 및 정제 공정, 낮은 수율 등의 문제로 인해 대량으로 천연색소를 생산해 시장에 공급하기에는 아직은 한계가 있다. 이러한 문제를 해결하기 위해 천연색소를 친환경적이며 고효율로 생산하기 위한 미생물 세포 공장을 개발하려는 노력이 이뤄지고 있다. 미생물 세포 공장 구축을 위한 핵심 전략인 시스템 대사공학은 기존의 석유화학 산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 우리 대학 생명화학공학과 이상엽 특훈교수가 창시한 연구 분야다.
학생들을 지도한 이상엽 특훈교수는 “학생들이 미생물 기반의 천연색소 생산을 위한 시스템 대사공학 연구를 체계적으로 분석 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있고, 권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 밝혔다. 이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
연구팀은 이번 연구에서 미생물 세포 공장을 개발해 생산된 대표 천연색소들의 생합성 경로를 총망라해, 최신 연구내용과 흐름을 한눈에 파악할 수 있는 대사회로 지도를 정리했다. 이번 논문에서는 천연색소 생산 미생물 세포 공장 개발을 위한 중요한 시스템 대사공학 전략들을 정리했고, 각 단계에서 활용할 수 있는 최신 도구 및 전략을 대사공학이 나아가야 할 방향과 함께 제시했다.
공동 제1 저자인 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생은 "합성 색소로부터 비롯되는 환경 오염 문제와 헬스케어에 대한 소비자들의 인식이 높아짐에 따라 천연색소 산업의 중요성이 더욱 대두되고 있다ˮ라고 말했으며, 공동 저자인 농촌진흥청 농업미생물과 김수진 박사는 "인류가 건강한 삶을 지속적으로 영위하기 위해 천연색소를 대사공학적으로 생산하는 연구가 갈수록 중요해질 것ˮ이라고 말했다.
한편 이번 연구는 농촌진흥청이 지원하는 농업미생물사업단(단장 장판식)의 ‘카로티노이드 생산 미생물 세포 공장 개발’ 과제(과제책임자 국립농업과학원 김수진 박사)의 지원을 받아 수행됐다.
2022.07.06 조회수 11262
합성색소 문제를 해결하는 미생물 기반 천연색소 생한을 위한 시스템 대사공학 전략 제시
우리 대학 생명화학공학과 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생을 포함한 이상엽 특훈교수 연구팀이 `미생물 기반의 천연색소 생산을 위한 시스템 대사공학 전략’ 논문을 발표했다고 6일 밝혔다.
생명화학공학과의 신디(Cindy Pricilia Surya Prabowo) 박사과정생, 은현민 박사과정생, 양동수 박사, 담라(Damla) 박사과정생과 농촌진흥청 농업미생물과의 김수진 박사가 함께 참여한 이번 논문은 셀(Cell) 誌가 발행하는 화학 분야 권위 리뷰 저널인 `화학의 동향(Trends in Chemistry)' 7월호 표지논문 및 주 논문 (Featured Article)으로 1일 字 게재됐다.
※ 논문명 : Production of natural colorants by metabolically engineered microorganisms
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), Cindy(한국과학기술원, 공동 제1 저자), 은현민(한국과학기술원, 공동 제1 저자), 양동수(한국과학기술원, 제3 저자), Damla(한국과학기술원, 공동 제4저자), 김수진(농촌진흥청, 제5저자), Raman(농촌진흥청, 제 6저자) 포함 총 7명
천연자원으로부터 비롯되는 천연색소는 식품, 의약품, 화장품, 옷감 염색 등에서 널리 사용될 정도로 인류 역사에서 오랫동안 사용됐지만, 석유화학 산업의 발달과 함께 화학 합성 기반 색소의 수요도 급속도로 늘기 시작했다. 그러나 합성 색소를 지나치게 많이 사용함으로써 환경 오염 초래 및 인류의 건강에 악영향을 미칠 수 있으며, 특히 전체 산업용 폐수 중 약 17~20%의 폐수가 합성 색소를 옷감 염색에 사용하면서 발생하는 폐수로부터 비롯되는 것으로 보고된 바 있다.
환경 오염, 그리고 헬스케어에 대한 인식이 높아짐에 따라 천연색소에 대한 소비자 수요가 점점 증가하고 있지만, 천연자원으로부터 얻을 수 있는 한정된 천연색소의 양, 값비싼 추출 및 정제 공정, 낮은 수율 등의 문제로 인해 대량으로 천연색소를 생산해 시장에 공급하기에는 아직은 한계가 있다. 이러한 문제를 해결하기 위해 천연색소를 친환경적이며 고효율로 생산하기 위한 미생물 세포 공장을 개발하려는 노력이 이뤄지고 있다. 미생물 세포 공장 구축을 위한 핵심 전략인 시스템 대사공학은 기존의 석유화학 산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 우리 대학 생명화학공학과 이상엽 특훈교수가 창시한 연구 분야다.
학생들을 지도한 이상엽 특훈교수는 “학생들이 미생물 기반의 천연색소 생산을 위한 시스템 대사공학 연구를 체계적으로 분석 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있고, 권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 밝혔다. 이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
연구팀은 이번 연구에서 미생물 세포 공장을 개발해 생산된 대표 천연색소들의 생합성 경로를 총망라해, 최신 연구내용과 흐름을 한눈에 파악할 수 있는 대사회로 지도를 정리했다. 이번 논문에서는 천연색소 생산 미생물 세포 공장 개발을 위한 중요한 시스템 대사공학 전략들을 정리했고, 각 단계에서 활용할 수 있는 최신 도구 및 전략을 대사공학이 나아가야 할 방향과 함께 제시했다.
공동 제1 저자인 신디(Cindy Pricilia Surya Prabowo) 박사과정생과 은현민 박사과정생은 "합성 색소로부터 비롯되는 환경 오염 문제와 헬스케어에 대한 소비자들의 인식이 높아짐에 따라 천연색소 산업의 중요성이 더욱 대두되고 있다ˮ라고 말했으며, 공동 저자인 농촌진흥청 농업미생물과 김수진 박사는 "인류가 건강한 삶을 지속적으로 영위하기 위해 천연색소를 대사공학적으로 생산하는 연구가 갈수록 중요해질 것ˮ이라고 말했다.
한편 이번 연구는 농촌진흥청이 지원하는 농업미생물사업단(단장 장판식)의 ‘카로티노이드 생산 미생물 세포 공장 개발’ 과제(과제책임자 국립농업과학원 김수진 박사)의 지원을 받아 수행됐다.
2022.07.06 조회수 11262 차세대 에너지 변환기술인 양방향 고체산화물 연료전지용 스마트 전극 개발
우리 대학 기계공학과 이강택 교수 연구팀이 포스텍 한정우 교수, 한국세라믹기술원 신태호 박사팀과의 공동 연구를 통해 양방향 고체산화물 연료전지(SOFC)용 고성능 전극 소재 개발에 성공했다고 21일 밝혔다.
양방향 고체산화물 연료전지는 고온에서 수소와 산소를 자발 반응시켜 고효율로 전력으로 변환(연료전지 모드) 하고, 전기를 가하면 청정 수소(그린 수소)와 같은 친환경 에너지원을 생산(전해전지 모드) 할 수 있는, 탄소중립 사회를 위한 차세대 에너지 변환 기술이다.
이러한 양방향 연료전지의 전기화학적 성능을 높이기 위해서 가역반응에서 전극의 촉매 성능을 획기적으로 높이는 것이 중요하며, 이를 위한 다양한 연구가 진행되고 있다. 그중 다공성 연료극 구조체 표면에 고성능 나노 금속 촉매를 입히는 기존 함침법의 경우 반응점을 늘리기 위해서 반복적인 증착 공정을 수행해야 하고, 고온 장기 구동 시 응집 현상으로 인한 촉매 활성도가 저하되는 한계를 갖고 있다.
연구팀은 이러한 문제점 해결을 위해 연료전지가 작동하는 환경에서, 전극 표면에 금속합금 나노촉매가 자발적으로 형성되는 용출(exsolution) 현상을 활용한 전극을 디자인 했다. 연구팀은 금속합금 나노촉매 형성을 촉진하기 위해 기존 코발타이트계 산화물 구조 내에 팔라듐(Pd)을 미량 첨가해, 양방향 구동 시 가역적으로 고활성을 갖는 전극 개발에 성공했다. 해당 방법으로 설계된 나노 합금 촉매는 페로브스카이트 격자 내부에서부터 전극 표면으로 스스로 용출돼 형성되기 때문에 전극 표면과 응집 현상 없이 강하게 결합하고, 입자의 균일도 또한 우수해 촉매 성능 향상에 큰 이점이 있다.
연구팀은 전해질 지지체 단전지에 개발된 전극을 연료극으로 사용해 성능을 측정한 결과, 연료전지 모드에서 최대출력 2.0W/cm2 (850oC), 전해전지 모드에서 전력밀도 2.23A/cm-2 (1.3V, 850oC)를 구현해, 세계 최고 수준의 양방향 연료전지 성능을 달성했다. 이는 기존 기술 대비 연료전지 모드는 1.6배, 전해전지 모드는 2.4배 향상된 결과다.
기계공학과 김경준 박사, 배경택 박사과정생, 포스텍 임채성 박사과정생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `어플라이드 카탈리시스 비: 인바이러멘탈, Applied Catalysis B: Environmental' (IF:19.503, JCR분야 0.93%) 5월 14일 字 온라인판에 게재됐다. (논문명: Concurrent promotion of phase transition and bimetallic nanocatalyst exsolution in perovskite oxides driven by Pd doping to achieve highly active bifunctional fuel electrodes for reversible solid oxide electrochemical cells)
이강택 교수는 “이번 연구를 통해서 특정 페로브스카이트 전극 물질 내 높은 환원 특성을 가지는 원소의 도핑이 산화물 전극 표면에 이종 금속 나노촉매를 선택적으로 형성하는 방아쇠 역할을 할 수 있으며, 이는 고성능 고 안정성의 양방향 고체산화물 연료전지 상용화를 선도하는 기술이 될 것”이라고 말했다.
한편 이번 연구는 과학기술정보통신부 수소에너지혁신기술개발사업, 중견연구자지원사업 그리고 나노 및 소재 기술개발사업의 지원으로 수행됐다.
2022.06.21 조회수 9460
차세대 에너지 변환기술인 양방향 고체산화물 연료전지용 스마트 전극 개발
우리 대학 기계공학과 이강택 교수 연구팀이 포스텍 한정우 교수, 한국세라믹기술원 신태호 박사팀과의 공동 연구를 통해 양방향 고체산화물 연료전지(SOFC)용 고성능 전극 소재 개발에 성공했다고 21일 밝혔다.
양방향 고체산화물 연료전지는 고온에서 수소와 산소를 자발 반응시켜 고효율로 전력으로 변환(연료전지 모드) 하고, 전기를 가하면 청정 수소(그린 수소)와 같은 친환경 에너지원을 생산(전해전지 모드) 할 수 있는, 탄소중립 사회를 위한 차세대 에너지 변환 기술이다.
이러한 양방향 연료전지의 전기화학적 성능을 높이기 위해서 가역반응에서 전극의 촉매 성능을 획기적으로 높이는 것이 중요하며, 이를 위한 다양한 연구가 진행되고 있다. 그중 다공성 연료극 구조체 표면에 고성능 나노 금속 촉매를 입히는 기존 함침법의 경우 반응점을 늘리기 위해서 반복적인 증착 공정을 수행해야 하고, 고온 장기 구동 시 응집 현상으로 인한 촉매 활성도가 저하되는 한계를 갖고 있다.
연구팀은 이러한 문제점 해결을 위해 연료전지가 작동하는 환경에서, 전극 표면에 금속합금 나노촉매가 자발적으로 형성되는 용출(exsolution) 현상을 활용한 전극을 디자인 했다. 연구팀은 금속합금 나노촉매 형성을 촉진하기 위해 기존 코발타이트계 산화물 구조 내에 팔라듐(Pd)을 미량 첨가해, 양방향 구동 시 가역적으로 고활성을 갖는 전극 개발에 성공했다. 해당 방법으로 설계된 나노 합금 촉매는 페로브스카이트 격자 내부에서부터 전극 표면으로 스스로 용출돼 형성되기 때문에 전극 표면과 응집 현상 없이 강하게 결합하고, 입자의 균일도 또한 우수해 촉매 성능 향상에 큰 이점이 있다.
연구팀은 전해질 지지체 단전지에 개발된 전극을 연료극으로 사용해 성능을 측정한 결과, 연료전지 모드에서 최대출력 2.0W/cm2 (850oC), 전해전지 모드에서 전력밀도 2.23A/cm-2 (1.3V, 850oC)를 구현해, 세계 최고 수준의 양방향 연료전지 성능을 달성했다. 이는 기존 기술 대비 연료전지 모드는 1.6배, 전해전지 모드는 2.4배 향상된 결과다.
기계공학과 김경준 박사, 배경택 박사과정생, 포스텍 임채성 박사과정생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지인 `어플라이드 카탈리시스 비: 인바이러멘탈, Applied Catalysis B: Environmental' (IF:19.503, JCR분야 0.93%) 5월 14일 字 온라인판에 게재됐다. (논문명: Concurrent promotion of phase transition and bimetallic nanocatalyst exsolution in perovskite oxides driven by Pd doping to achieve highly active bifunctional fuel electrodes for reversible solid oxide electrochemical cells)
이강택 교수는 “이번 연구를 통해서 특정 페로브스카이트 전극 물질 내 높은 환원 특성을 가지는 원소의 도핑이 산화물 전극 표면에 이종 금속 나노촉매를 선택적으로 형성하는 방아쇠 역할을 할 수 있으며, 이는 고성능 고 안정성의 양방향 고체산화물 연료전지 상용화를 선도하는 기술이 될 것”이라고 말했다.
한편 이번 연구는 과학기술정보통신부 수소에너지혁신기술개발사업, 중견연구자지원사업 그리고 나노 및 소재 기술개발사업의 지원으로 수행됐다.
2022.06.21 조회수 9460 디스플레이 소재로 빛 이용해 친환경 암모니아 합성법 제시
우리 대학 생명화학공학과 이도창 교수, 이상엽 특훈교수, 박영신 연구교수 연구팀이 디스플레이 소재인 양자점(퀀텀닷)을 이용해 *질소 고정 박테리아의 암모니아 생산 효율을 대폭 늘렸다고 16일 밝혔다.
☞ 질소 고정(Nitrogen Fixation) : 공기 중 질소 기체 분자(N₂)를 암모니아(NH₃)를 비롯한 질소화합물로 전환하는 과정을 말한다.
이 교수 연구팀은 양자점에 의해 흡수된 빛 에너지가 박테리아의 암모니아 합성 반응에 사용되도록 설계했으며, 그 결과 박테리아의 암모니아 생산량을 큰 폭으로 증가시킬 수 있었다. 이를 위해 연구팀은 양자점을 질소고정 박테리아 안에 더 많이 넣을 수 있는 방법을 제시했다.
생명화학공학과 고성준 박사가 제1저자로 참여한 이번 연구의 결과는 국제 학술지 `미국 화학회지(JACS)'에 표지 논문으로 선정돼 출판됐다. (논문명 : Light-Driven Ammonia Production by Azotobacter vinelandii Cultured in Medium Containing Colloidal Quantum Dots).
질소 고정 박테리아는 질소 고정 효소를 이용해 대기 중 질소를 암모니아로 전환하여 생장에 필요한 단백질을 생산한다. 이러한 질소 고정 반응은 화학적 암모니아 합성법인 하버-보슈 공정에 비해 에너지 소비와 이산화탄소 배출이 현저하게 적다.
하지만, 박테리아는 생장에 필요한 만큼만 암모니아를 생산하도록 진화돼 질소 고정 효소의 반응이 느리기에 이를 산업적으로 활용하기 어렵다. 질소 고정 반응이 느린 이유는 효소의 두 가지 구성요소(전자 전달부, 촉매 반응부)의 비효율적인 상호작용 때문이다. 전자 전달부가 촉매 반응부에 전자를 공급한 후, 반드시 탈착돼야만 촉매 반응부가 새로운 전자를 추가로 공급받아 암모니아를 생성할 수 있다.
연구팀은 문제 해결을 위해 빛을 흡수하는 양자점을 박테리아의 질소 고정 반응에 전자 공급원으로 활용해 나노·바이오 복합 시스템을 구축했다. 양자점은 수 나노미터의 작은 크기를 갖는 반도체 나노입자이며 디스플레이 소재로 많이 알려진 물질이다. 하지만, 양자점이 흡수한 빛 에너지를 표면에 쉽게 전달할 수 있도록 입자의 구조 및 표면을 제어하면 광 감응 및 광 촉매 소재로도 우수한 특성을 보인다. 연구팀은 질소 고정 효소의 전자 전달부 역할을 양자점으로 대체하기 위해 양자점의 코어/쉘 구조를 전자 전달에 유리하게 설계했다. 또한, 양자점이 생물학적 시스템에 결합할 수 있도록 표면 화학 특성을 제어해 수(水)분산 특성을 확보했다.
연구팀은 구조 및 표면이 제어된 양자점을 질소 고정 박테리아의 대사활동이 가장 활발한 성장기에 추가해, 박테리아의 능동적인 양자점 흡수를 유도했다. 이렇게 제작된 양자점-박테리아 복합 시스템에 빛을 조사한 결과, 질소고정 반응 속도가 증가하며 암모니아 생산량이 대폭 증가함을 확인했다. 고성준 박사는 "디스플레이 소재와 미생물의 장점을 합해 빛 에너지를 이용한 새로운 방식의 암모니아 합성법을 제시한 결과ˮ라며 "이번 연구를 활용한 그린 암모니아 생산 플랫폼을 구축한다면, 환경 및 에너지 문제에 적극적으로 대응할 수 있을 것이다ˮ라고 말했다.
한편 이번 연구는 삼성미래기술육성사업의 지원을 받아 수행됐다.
2022.06.16 조회수 11996
디스플레이 소재로 빛 이용해 친환경 암모니아 합성법 제시
우리 대학 생명화학공학과 이도창 교수, 이상엽 특훈교수, 박영신 연구교수 연구팀이 디스플레이 소재인 양자점(퀀텀닷)을 이용해 *질소 고정 박테리아의 암모니아 생산 효율을 대폭 늘렸다고 16일 밝혔다.
☞ 질소 고정(Nitrogen Fixation) : 공기 중 질소 기체 분자(N₂)를 암모니아(NH₃)를 비롯한 질소화합물로 전환하는 과정을 말한다.
이 교수 연구팀은 양자점에 의해 흡수된 빛 에너지가 박테리아의 암모니아 합성 반응에 사용되도록 설계했으며, 그 결과 박테리아의 암모니아 생산량을 큰 폭으로 증가시킬 수 있었다. 이를 위해 연구팀은 양자점을 질소고정 박테리아 안에 더 많이 넣을 수 있는 방법을 제시했다.
생명화학공학과 고성준 박사가 제1저자로 참여한 이번 연구의 결과는 국제 학술지 `미국 화학회지(JACS)'에 표지 논문으로 선정돼 출판됐다. (논문명 : Light-Driven Ammonia Production by Azotobacter vinelandii Cultured in Medium Containing Colloidal Quantum Dots).
질소 고정 박테리아는 질소 고정 효소를 이용해 대기 중 질소를 암모니아로 전환하여 생장에 필요한 단백질을 생산한다. 이러한 질소 고정 반응은 화학적 암모니아 합성법인 하버-보슈 공정에 비해 에너지 소비와 이산화탄소 배출이 현저하게 적다.
하지만, 박테리아는 생장에 필요한 만큼만 암모니아를 생산하도록 진화돼 질소 고정 효소의 반응이 느리기에 이를 산업적으로 활용하기 어렵다. 질소 고정 반응이 느린 이유는 효소의 두 가지 구성요소(전자 전달부, 촉매 반응부)의 비효율적인 상호작용 때문이다. 전자 전달부가 촉매 반응부에 전자를 공급한 후, 반드시 탈착돼야만 촉매 반응부가 새로운 전자를 추가로 공급받아 암모니아를 생성할 수 있다.
연구팀은 문제 해결을 위해 빛을 흡수하는 양자점을 박테리아의 질소 고정 반응에 전자 공급원으로 활용해 나노·바이오 복합 시스템을 구축했다. 양자점은 수 나노미터의 작은 크기를 갖는 반도체 나노입자이며 디스플레이 소재로 많이 알려진 물질이다. 하지만, 양자점이 흡수한 빛 에너지를 표면에 쉽게 전달할 수 있도록 입자의 구조 및 표면을 제어하면 광 감응 및 광 촉매 소재로도 우수한 특성을 보인다. 연구팀은 질소 고정 효소의 전자 전달부 역할을 양자점으로 대체하기 위해 양자점의 코어/쉘 구조를 전자 전달에 유리하게 설계했다. 또한, 양자점이 생물학적 시스템에 결합할 수 있도록 표면 화학 특성을 제어해 수(水)분산 특성을 확보했다.
연구팀은 구조 및 표면이 제어된 양자점을 질소 고정 박테리아의 대사활동이 가장 활발한 성장기에 추가해, 박테리아의 능동적인 양자점 흡수를 유도했다. 이렇게 제작된 양자점-박테리아 복합 시스템에 빛을 조사한 결과, 질소고정 반응 속도가 증가하며 암모니아 생산량이 대폭 증가함을 확인했다. 고성준 박사는 "디스플레이 소재와 미생물의 장점을 합해 빛 에너지를 이용한 새로운 방식의 암모니아 합성법을 제시한 결과ˮ라며 "이번 연구를 활용한 그린 암모니아 생산 플랫폼을 구축한다면, 환경 및 에너지 문제에 적극적으로 대응할 수 있을 것이다ˮ라고 말했다.
한편 이번 연구는 삼성미래기술육성사업의 지원을 받아 수행됐다.
2022.06.16 조회수 11996 차세대 뉴로모픽 구현을 앞당길 멤리스터 기반 고신뢰성 인공 뉴런(신경세포) 어레이 개발
우리 대학 전기및전자공학부 최신현 교수 연구팀이 뛰어난 안정성과 집적도가 높은 우리 뇌의 뉴런 세포의 동작을 모사하는 *고신뢰성 차세대 저항 변화 소자(멤리스터) 어레이를 개발했다고 7일 밝혔다.
☞ 멤리스터(Memristor): 입력에 따라 소자의 저항 상태가 바뀌는 소자. 입력 전압의 크기와 길이 등에 따라 소자 내부의 저항 값이 바뀌며 정보를 저장하거나 처리한다.
최 교수 연구팀은 기존 멤리스터의 불안정한 특성을 보이는 필라멘트 기반 방식에서 벗어나, 점진적인 산소 농도를 갖는 금속산화물을 이용해 안정적이고 신뢰성 높은 인공 뉴런 어레이를 발표하였다. 기존의 멤리스터 소자는 안정성이 낮고 응용에 사용하기 위한 어레이 형태로 제작하기 힘든 문제점이 있지만, 최 교수 연구팀이 개발한 소자는 뛰어난 안정성을 갖출 뿐만 아니라, 자가 정류 특성과 높은 수율을 갖춰 대용량 어레이 형태로 집적될 수 있다. 따라서 집적도가 높고 안정적인 뉴로모픽 시스템을 구현할 때 활발히 사용될 수 있을 것으로 기대된다.
전기및전자공학부 박시온, 정학천 석박사통합과정, 박종용 석사과정이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션스(Nature Communications)' 6월호에 출판됐다. (논문명 : Experimental demonstration of highly reliable dynamic memristor for artificial neuron and neuromorphic computing)
인간의 뉴런은 들어오는 신호의 크기와 주파수에 따라 스파이크를 내보내거나 내보내지 않는 방식으로 정보를 처리한다. 현대의 컴퓨터가 빅데이터를 처리하는데 많은 에너지를 소모하는 것과 다르게, 사람의 뇌는 매우 적은 에너지만으로도 많은 양의 데이터를 빠르게 처리할 수 있다. 이러한 이유로, 신경의 효율적인 신호전달 시스템을 모사하여 컴퓨팅에 사용하는 `뉴로모픽' 하드웨어 기술이 활발히 연구되고 있다. 멤리스터 소자는 고집적, 고효율로 뉴로모픽 컴퓨팅 시스템을 구현할 수 있는 차세대 소자로 주목받고 있다.
그러나 현존하는 멤리스터로 실용적인 대용량 인공신경망 컴퓨팅(Large-scale Neural Computing) 시스템을 구현하기에는 단위 소자의 신뢰성 및 수율의 문제가 있다. 기존의 멤리스터는 절연체 내부에서 필라멘트가 마치 번개와 같이 무작위적으로 생성되고 사라지며 동작하기 때문에 제어하기가 힘들어 낮은 신뢰성을 보이게 되며, 이로 인해 안정적인 뉴로모픽 시스템을 구현하는 데 한계점으로 지적되어 왔다.
최신현 교수 연구팀은 이러한 무작위적인 필라멘트 문제를 해결하기 위해 필라멘트 기반 저항 변화가 아닌, 산소 이온의 점진적인 이동을 이용해 저항 변화 소자를 구현함으로써 소자의 신뢰성 확보하였다. 또한 단위 소자를 통한 어레이 제작 기술을 확보하여, 400개의 고신뢰성 인공 뉴런 소자를 100% 수율의 크로스바 어레이 형태로 집적하는 데 성공했다.
연구팀은 제작한 고신뢰성 인공 뉴런 어레이 기반 뉴로모픽 시스템을 이용해 항균성 단백질(anti-microbial peptide) 아미노산 서열을 학습하고, 이를 바탕으로 새로운 항균성 단백질을 만들어내는 뉴로모픽 시스템을 구현하였다.
제1 저자인 박시온 석박통합과정 연구원은 "이번에 개발한 고신뢰성 인공 뉴런 소자는 안정적인 특성과 높은 수율을 바탕으로 차세대 멤리스터 기반 뉴로모픽 컴퓨팅 시스템 구현에 기여할 수 있을 것으로 기대되며, 개발된 인공 뉴런 소자를 이용해 촉각 등을 감지하는 로봇의 인공 신경계, 시계열 데이터를 처리하는 축적 컴퓨팅(reservoir computing) 등 다양한 응용을 가능케 하여 미래 전자공학의 기반이 될 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 삼성미래육성사업의 지원을 받아 수행됐다.
2022.06.07 조회수 12308
차세대 뉴로모픽 구현을 앞당길 멤리스터 기반 고신뢰성 인공 뉴런(신경세포) 어레이 개발
우리 대학 전기및전자공학부 최신현 교수 연구팀이 뛰어난 안정성과 집적도가 높은 우리 뇌의 뉴런 세포의 동작을 모사하는 *고신뢰성 차세대 저항 변화 소자(멤리스터) 어레이를 개발했다고 7일 밝혔다.
☞ 멤리스터(Memristor): 입력에 따라 소자의 저항 상태가 바뀌는 소자. 입력 전압의 크기와 길이 등에 따라 소자 내부의 저항 값이 바뀌며 정보를 저장하거나 처리한다.
최 교수 연구팀은 기존 멤리스터의 불안정한 특성을 보이는 필라멘트 기반 방식에서 벗어나, 점진적인 산소 농도를 갖는 금속산화물을 이용해 안정적이고 신뢰성 높은 인공 뉴런 어레이를 발표하였다. 기존의 멤리스터 소자는 안정성이 낮고 응용에 사용하기 위한 어레이 형태로 제작하기 힘든 문제점이 있지만, 최 교수 연구팀이 개발한 소자는 뛰어난 안정성을 갖출 뿐만 아니라, 자가 정류 특성과 높은 수율을 갖춰 대용량 어레이 형태로 집적될 수 있다. 따라서 집적도가 높고 안정적인 뉴로모픽 시스템을 구현할 때 활발히 사용될 수 있을 것으로 기대된다.
전기및전자공학부 박시온, 정학천 석박사통합과정, 박종용 석사과정이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 커뮤니케이션스(Nature Communications)' 6월호에 출판됐다. (논문명 : Experimental demonstration of highly reliable dynamic memristor for artificial neuron and neuromorphic computing)
인간의 뉴런은 들어오는 신호의 크기와 주파수에 따라 스파이크를 내보내거나 내보내지 않는 방식으로 정보를 처리한다. 현대의 컴퓨터가 빅데이터를 처리하는데 많은 에너지를 소모하는 것과 다르게, 사람의 뇌는 매우 적은 에너지만으로도 많은 양의 데이터를 빠르게 처리할 수 있다. 이러한 이유로, 신경의 효율적인 신호전달 시스템을 모사하여 컴퓨팅에 사용하는 `뉴로모픽' 하드웨어 기술이 활발히 연구되고 있다. 멤리스터 소자는 고집적, 고효율로 뉴로모픽 컴퓨팅 시스템을 구현할 수 있는 차세대 소자로 주목받고 있다.
그러나 현존하는 멤리스터로 실용적인 대용량 인공신경망 컴퓨팅(Large-scale Neural Computing) 시스템을 구현하기에는 단위 소자의 신뢰성 및 수율의 문제가 있다. 기존의 멤리스터는 절연체 내부에서 필라멘트가 마치 번개와 같이 무작위적으로 생성되고 사라지며 동작하기 때문에 제어하기가 힘들어 낮은 신뢰성을 보이게 되며, 이로 인해 안정적인 뉴로모픽 시스템을 구현하는 데 한계점으로 지적되어 왔다.
최신현 교수 연구팀은 이러한 무작위적인 필라멘트 문제를 해결하기 위해 필라멘트 기반 저항 변화가 아닌, 산소 이온의 점진적인 이동을 이용해 저항 변화 소자를 구현함으로써 소자의 신뢰성 확보하였다. 또한 단위 소자를 통한 어레이 제작 기술을 확보하여, 400개의 고신뢰성 인공 뉴런 소자를 100% 수율의 크로스바 어레이 형태로 집적하는 데 성공했다.
연구팀은 제작한 고신뢰성 인공 뉴런 어레이 기반 뉴로모픽 시스템을 이용해 항균성 단백질(anti-microbial peptide) 아미노산 서열을 학습하고, 이를 바탕으로 새로운 항균성 단백질을 만들어내는 뉴로모픽 시스템을 구현하였다.
제1 저자인 박시온 석박통합과정 연구원은 "이번에 개발한 고신뢰성 인공 뉴런 소자는 안정적인 특성과 높은 수율을 바탕으로 차세대 멤리스터 기반 뉴로모픽 컴퓨팅 시스템 구현에 기여할 수 있을 것으로 기대되며, 개발된 인공 뉴런 소자를 이용해 촉각 등을 감지하는 로봇의 인공 신경계, 시계열 데이터를 처리하는 축적 컴퓨팅(reservoir computing) 등 다양한 응용을 가능케 하여 미래 전자공학의 기반이 될 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 삼성미래육성사업의 지원을 받아 수행됐다.
2022.06.07 조회수 12308 실제 약물로 개발되는 단백질-리간드 상호작용 예측 인공지능 모델 개발
우리 대학 연구진이 물리화학적 아이디어를 인공지능 딥러닝에 접목해 기존의 방법보다 일반화 성능이 높은 단백질-리간드 상호작용 예측 모델을 개발했다. 리간드란 수용체와 같은 큰 생체 분자에 특이적으로 결합하는 물질을 말하며, 생체 내의 중요한 요소이자 의약품의 개발 등에 큰 역할을 한다.
화학과 김우연 교수 연구팀이 교원창업 인공지능 신약 개발 스타트업 HITS 연구진과 함께 물리 기반 삼차원 그래프 심층 신경망을 이용해 일반화 성능을 높인 단백질-리간드 상호작용 예측 모델을 개발했다고 17일 밝혔다.
약물 후보 분자를 발굴하기 위해서 타깃 단백질과 강하게 결합하는 리간드를 찾는 것이 중요하다. 하지만 유효 물질을 찾기 위해 수백만에서 수천만 개의 무작위 리간드 라이브러리를 대상으로 실험 전수 조사를 수행하는 것은 천문학적인 시간과 비용이 필요하다. 이러한 시간과 비용을 절감하기 위해 최근 단백질-리간드 상호작용 예측에 기반한 가상탐색(virtual screening) 기술이 주목받고 있다.
기존의 상호작용 예측 인공지능 모델들은 학습에 사용한 구조에 대해서는 높은 예측 성능을 보여주지만, 새로운 단백질 구조에 대해서는 낮은 성능을 보이는 과적합(over-fitting)이 문제가 됐다. 과적합 문제는 일반적으로 모델의 복잡도에 비해 데이터가 적을 때 발생한다. 이번 연구는 이러한 과적합 문제를 해결함으로써 다양한 단백질에 대해 고른 성능을 보여주는 예측 모델을 개발하는데 주안점을 뒀다.
연구진은 물리화학적 아이디어들을 딥러닝 모델에 적용해 모델의 복잡도를 줄임과 동시에 물리 시뮬레이션을 통해 부족한 데이터를 보강함으로써 과적합 문제를 해결하고자 하였다. 단백질 원자와 리간드 원자 사이의 거리에 따른 반데르발스 힘, 수소 결합력 등을 물리화학적 방정식으로 모델링하고, 매개변수를 딥러닝으로 예측함으로써 물리 법칙을 만족하는 예측을 가능하게 했다.
또한, 학습에 사용한 단백질-리간드 결정 구조가 실험적으로 판명된 가장 안정한 구조임에 착안했다. 부족한 실험 데이터를 보강하기 위해 불안정한 단백질-리간드 구조로 이루어진 수십만 개의 인공 데이터를 생성해 학습에 활용했고, 그 결과 생성된 구조에 비해 실제 구조를 안정하게 예측하도록 모델을 학습할 수 있었다.
연구진은 개발된 모델의 성능을 검증하기 위해 대조군으로 `CASF-2016 벤치마크'를 활용했다. 이 벤치마크는 다양한 단백질-리간드 구조들 사이에서 실험적으로 판명된 결정 구조에 근접한 구조를 찾는 도킹과 상대적으로 결합력이 큰 단백질-리간드 쌍을 찾는 스크리닝 등 실제 약물을 개발하는 과정에 필수적인 과제를 포함하고 있다. 검증 테스트 결과 기존에 보고된 기술에 비해 높은 도킹 및 스크리닝 성공률을 보여줬으며, 특히 스크리닝 성능은 기존에 보고된 최고 성능 대비 약 두 배 높은 수치를 보였다.
연구진이 개발한 물리 기반 딥러닝 방법론의 또 다른 장점은 예측의 결과를 물리적으로 해석 가능하다는 것이다. 이는 딥러닝으로 최적화된 물리화학 식을 통해 최종 상호작용 값을 예측하기 때문이다. 리간드 분자 내 원자별 상호작용 에너지의 기여도를 분석함으로써 어떤 작용기가 단백질-리간드 결합에 있어서 중요한 역할을 했는지 파악할 수 있으며, 이와 같은 정보는 추후 약물 설계를 통해 성능을 높이는 데 직접 활용할 수 있다.
공동 제1 저자로 참여한 화학과 문석현, 정원호, 양수정(현재 MIT 박사과정) 박사과정 학생들은 "데이터가 적은 화학 및 바이오 분야에서 일반화 문제는 항상 중요한 문제로 강조돼왔다ˮ며 "이번 연구에서 사용한 물리 기반 딥러닝 방법론은 단백질-리간드 간 상호작용 예측 뿐 아니라 다양한 물리 문제에 적용될 수 있을 것ˮ이라고 말했다.
한국연구재단의 지원을 받아 수행된 이번 연구는 국제 학술지 `Chemical Science(IF=9.825)' 2022년 4월 13호에 표지 논문 및 `금주의 논문(Pick of the Week)'으로 선정됐다. (논문명 : PIGNet: a physics-informed deep learning model toward generalized drug–target interaction predictions, 논문 링크 : https://doi.org/10.1039/D1SC06946B)
2022.05.17 조회수 15804
실제 약물로 개발되는 단백질-리간드 상호작용 예측 인공지능 모델 개발
우리 대학 연구진이 물리화학적 아이디어를 인공지능 딥러닝에 접목해 기존의 방법보다 일반화 성능이 높은 단백질-리간드 상호작용 예측 모델을 개발했다. 리간드란 수용체와 같은 큰 생체 분자에 특이적으로 결합하는 물질을 말하며, 생체 내의 중요한 요소이자 의약품의 개발 등에 큰 역할을 한다.
화학과 김우연 교수 연구팀이 교원창업 인공지능 신약 개발 스타트업 HITS 연구진과 함께 물리 기반 삼차원 그래프 심층 신경망을 이용해 일반화 성능을 높인 단백질-리간드 상호작용 예측 모델을 개발했다고 17일 밝혔다.
약물 후보 분자를 발굴하기 위해서 타깃 단백질과 강하게 결합하는 리간드를 찾는 것이 중요하다. 하지만 유효 물질을 찾기 위해 수백만에서 수천만 개의 무작위 리간드 라이브러리를 대상으로 실험 전수 조사를 수행하는 것은 천문학적인 시간과 비용이 필요하다. 이러한 시간과 비용을 절감하기 위해 최근 단백질-리간드 상호작용 예측에 기반한 가상탐색(virtual screening) 기술이 주목받고 있다.
기존의 상호작용 예측 인공지능 모델들은 학습에 사용한 구조에 대해서는 높은 예측 성능을 보여주지만, 새로운 단백질 구조에 대해서는 낮은 성능을 보이는 과적합(over-fitting)이 문제가 됐다. 과적합 문제는 일반적으로 모델의 복잡도에 비해 데이터가 적을 때 발생한다. 이번 연구는 이러한 과적합 문제를 해결함으로써 다양한 단백질에 대해 고른 성능을 보여주는 예측 모델을 개발하는데 주안점을 뒀다.
연구진은 물리화학적 아이디어들을 딥러닝 모델에 적용해 모델의 복잡도를 줄임과 동시에 물리 시뮬레이션을 통해 부족한 데이터를 보강함으로써 과적합 문제를 해결하고자 하였다. 단백질 원자와 리간드 원자 사이의 거리에 따른 반데르발스 힘, 수소 결합력 등을 물리화학적 방정식으로 모델링하고, 매개변수를 딥러닝으로 예측함으로써 물리 법칙을 만족하는 예측을 가능하게 했다.
또한, 학습에 사용한 단백질-리간드 결정 구조가 실험적으로 판명된 가장 안정한 구조임에 착안했다. 부족한 실험 데이터를 보강하기 위해 불안정한 단백질-리간드 구조로 이루어진 수십만 개의 인공 데이터를 생성해 학습에 활용했고, 그 결과 생성된 구조에 비해 실제 구조를 안정하게 예측하도록 모델을 학습할 수 있었다.
연구진은 개발된 모델의 성능을 검증하기 위해 대조군으로 `CASF-2016 벤치마크'를 활용했다. 이 벤치마크는 다양한 단백질-리간드 구조들 사이에서 실험적으로 판명된 결정 구조에 근접한 구조를 찾는 도킹과 상대적으로 결합력이 큰 단백질-리간드 쌍을 찾는 스크리닝 등 실제 약물을 개발하는 과정에 필수적인 과제를 포함하고 있다. 검증 테스트 결과 기존에 보고된 기술에 비해 높은 도킹 및 스크리닝 성공률을 보여줬으며, 특히 스크리닝 성능은 기존에 보고된 최고 성능 대비 약 두 배 높은 수치를 보였다.
연구진이 개발한 물리 기반 딥러닝 방법론의 또 다른 장점은 예측의 결과를 물리적으로 해석 가능하다는 것이다. 이는 딥러닝으로 최적화된 물리화학 식을 통해 최종 상호작용 값을 예측하기 때문이다. 리간드 분자 내 원자별 상호작용 에너지의 기여도를 분석함으로써 어떤 작용기가 단백질-리간드 결합에 있어서 중요한 역할을 했는지 파악할 수 있으며, 이와 같은 정보는 추후 약물 설계를 통해 성능을 높이는 데 직접 활용할 수 있다.
공동 제1 저자로 참여한 화학과 문석현, 정원호, 양수정(현재 MIT 박사과정) 박사과정 학생들은 "데이터가 적은 화학 및 바이오 분야에서 일반화 문제는 항상 중요한 문제로 강조돼왔다ˮ며 "이번 연구에서 사용한 물리 기반 딥러닝 방법론은 단백질-리간드 간 상호작용 예측 뿐 아니라 다양한 물리 문제에 적용될 수 있을 것ˮ이라고 말했다.
한국연구재단의 지원을 받아 수행된 이번 연구는 국제 학술지 `Chemical Science(IF=9.825)' 2022년 4월 13호에 표지 논문 및 `금주의 논문(Pick of the Week)'으로 선정됐다. (논문명 : PIGNet: a physics-informed deep learning model toward generalized drug–target interaction predictions, 논문 링크 : https://doi.org/10.1039/D1SC06946B)
2022.05.17 조회수 15804 무질서로부터 질서를 생성하는 원리 제시
우리 대학 화학과 서명은 교수 연구팀이 물에 녹는 부분과 녹지 않는 부분이 무작위로 섞여 있는 고분자가 물에서 처음 보는 규칙적 구조를 만드는 것을 발견하고, 무질서로부터 질서가 출현할 수 있는 새로운 원리를 제시했다고 11일 밝혔다.
동전을 던져서 앞면과 뒷면이 나올 확률이 똑같다면, 아주 많이 동전을 던졌을 때 앞면이 나온 경우는 전체 중 반에 가까울 것이다. 그렇다고 해서 앞면만 연달아 나올 확률이 없는 것은 아니다. 사실 이 확률은 앞면과 뒷면이 번갈아 가며 나올 확률과 정확히 똑같다. 동전을 여러 번 던질수록 앞뒷면이 나오는 순서의 가짓수는 기하급수적으로 증가하는데(60차례 던지면 1018=100경 가지보다 많은 서열이 생겨난다), 이 서열을 보고 무작위한 과정을 통해 만들어졌는지 판별하기는 생각보다 어렵다. 반대로 온전히 무작위로 난수를 만드는 방법은 전산과학과 보안 등에서 중요한 문제다.
서명은 교수 연구팀은 무작위한 서열 사이의 짝맞추기 문제에 주목했다. 물에 녹는 부분과 녹지 않는 부분을 무작위하게 도입해서 고분자를 만들면 마치 비누에 들어있는 계면활성제나 세포막 이중 층을 이루는 지질처럼 양친매성을 띠어, 물에 넣으면 물에 녹지 않는 지용성 부분끼리 뭉치고 이를 물에 녹는 수용성 부분이 감싸는 형태로 저절로 조립된다. 이때 각 사슬의 서열은 모두 다르므로, 두 사슬이 서로 만나 지용성 부분끼리 뭉칠 때 정확히 들어맞는 짝은 그 수많은 사슬 중 한 쌍밖에 없다.
연구팀은 이 고분자를 고농도로 물에 녹이면 세포막에서 관찰되는 것과 같은 이중 층들이 반복적으로 접히면서 켜켜이 쌓이는 새로운 판상 구조를 만드는 것을 발견했다. 세포는 필요에 따라 세포막을 접어 골지체와 같은 구조를 만들지만, 이중 층 구조 자체를 안정하게 규칙적으로 접을 수 있다는 것은 처음 밝혀지는 것이다. 무작위한 서열에서는 지용성 부분이 몰려 있는 구간이 상당히 큰 확률로 발생하기 때문에, 연구진은 사슬들이 만날 때 필연적으로 짝이 맞지 않는 부분들이 생겨 평평한 판상 구조가 접히는 것으로 이 현상을 설명했다.
연구진은 "흔히 무질서하다고 간주되는 무작위 서열 속에서 어떻게 질서가 태동할 수 있는지 하나의 가능성을 엿볼 수 있었다ˮ며, "무작위성에 대한 이해를 토대로 물리적 복제방지기술(PUF)로 응용함과 아울러 구조적인 특성을 활용하여 인공 근육 등에 쓸 수 있는 나노 연성 구조 소재로 확장할 가능성을 향후 연구하고 싶다ˮ고 소감을 밝혔다.
우리 대학 화학과 신민중 석박사통합과정 학생이 제1 저자로 연구를 주도하고 포항가속기연구소 안형주 박사, 우리 대학 화학과 윤동기 교수 연구팀, GIST 이은지 교수 연구팀이 협업한 이번 연구 결과는 국제학술지 '네이처 커뮤니케이션즈(Nature Communications)'에 5월 4일 字로 온라인 게재됐다. (논문명 : Bilayer-folded Lamellar Mesophase Induced by Random Polymer Sequence)
한편 이번 연구는 한국연구재단(NRF)의 보호연구사업과 선도연구센터지원사업(멀티스케일 카이랄 구조체 연구센터), KAIST의 그랜드 챌린지 30 프로젝트의 지원을 받아 진행됐다.
2022.05.11 조회수 10422
무질서로부터 질서를 생성하는 원리 제시
우리 대학 화학과 서명은 교수 연구팀이 물에 녹는 부분과 녹지 않는 부분이 무작위로 섞여 있는 고분자가 물에서 처음 보는 규칙적 구조를 만드는 것을 발견하고, 무질서로부터 질서가 출현할 수 있는 새로운 원리를 제시했다고 11일 밝혔다.
동전을 던져서 앞면과 뒷면이 나올 확률이 똑같다면, 아주 많이 동전을 던졌을 때 앞면이 나온 경우는 전체 중 반에 가까울 것이다. 그렇다고 해서 앞면만 연달아 나올 확률이 없는 것은 아니다. 사실 이 확률은 앞면과 뒷면이 번갈아 가며 나올 확률과 정확히 똑같다. 동전을 여러 번 던질수록 앞뒷면이 나오는 순서의 가짓수는 기하급수적으로 증가하는데(60차례 던지면 1018=100경 가지보다 많은 서열이 생겨난다), 이 서열을 보고 무작위한 과정을 통해 만들어졌는지 판별하기는 생각보다 어렵다. 반대로 온전히 무작위로 난수를 만드는 방법은 전산과학과 보안 등에서 중요한 문제다.
서명은 교수 연구팀은 무작위한 서열 사이의 짝맞추기 문제에 주목했다. 물에 녹는 부분과 녹지 않는 부분을 무작위하게 도입해서 고분자를 만들면 마치 비누에 들어있는 계면활성제나 세포막 이중 층을 이루는 지질처럼 양친매성을 띠어, 물에 넣으면 물에 녹지 않는 지용성 부분끼리 뭉치고 이를 물에 녹는 수용성 부분이 감싸는 형태로 저절로 조립된다. 이때 각 사슬의 서열은 모두 다르므로, 두 사슬이 서로 만나 지용성 부분끼리 뭉칠 때 정확히 들어맞는 짝은 그 수많은 사슬 중 한 쌍밖에 없다.
연구팀은 이 고분자를 고농도로 물에 녹이면 세포막에서 관찰되는 것과 같은 이중 층들이 반복적으로 접히면서 켜켜이 쌓이는 새로운 판상 구조를 만드는 것을 발견했다. 세포는 필요에 따라 세포막을 접어 골지체와 같은 구조를 만들지만, 이중 층 구조 자체를 안정하게 규칙적으로 접을 수 있다는 것은 처음 밝혀지는 것이다. 무작위한 서열에서는 지용성 부분이 몰려 있는 구간이 상당히 큰 확률로 발생하기 때문에, 연구진은 사슬들이 만날 때 필연적으로 짝이 맞지 않는 부분들이 생겨 평평한 판상 구조가 접히는 것으로 이 현상을 설명했다.
연구진은 "흔히 무질서하다고 간주되는 무작위 서열 속에서 어떻게 질서가 태동할 수 있는지 하나의 가능성을 엿볼 수 있었다ˮ며, "무작위성에 대한 이해를 토대로 물리적 복제방지기술(PUF)로 응용함과 아울러 구조적인 특성을 활용하여 인공 근육 등에 쓸 수 있는 나노 연성 구조 소재로 확장할 가능성을 향후 연구하고 싶다ˮ고 소감을 밝혔다.
우리 대학 화학과 신민중 석박사통합과정 학생이 제1 저자로 연구를 주도하고 포항가속기연구소 안형주 박사, 우리 대학 화학과 윤동기 교수 연구팀, GIST 이은지 교수 연구팀이 협업한 이번 연구 결과는 국제학술지 '네이처 커뮤니케이션즈(Nature Communications)'에 5월 4일 字로 온라인 게재됐다. (논문명 : Bilayer-folded Lamellar Mesophase Induced by Random Polymer Sequence)
한편 이번 연구는 한국연구재단(NRF)의 보호연구사업과 선도연구센터지원사업(멀티스케일 카이랄 구조체 연구센터), KAIST의 그랜드 챌린지 30 프로젝트의 지원을 받아 진행됐다.
2022.05.11 조회수 10422 ‘컴퓨터의 시간을 멈춘다’, 전원 공급 없이도 모든 정보가 복원, 작동되는 비휘발성 컴퓨터 최초 개발
우리 대학 전기및전자공학부 정명수 교수 연구팀(컴퓨터 아키텍처 및 메모리 시스템 연구실)이 컴퓨터의 시간을 멈추는 하드웨어/소프트웨어 기술, `경량화된 비휘발성 컴퓨팅 시스템(Lightweight Persistence Centric System, 이하 라이트PC)'을 세계 최초로 개발했다고 25일 밝혔다. 연구진의 컴퓨터에서는 시간이 멈춰진 순간의 모든 정보(실행 상태 및 데이터)는 전원 공급 여부와 관계없이 유지되며, 유지되는 모든 정보는 언제든 사용자가 원할 때 바로 복원, 작동될 수 있다.
기존의 컴퓨터는 휘발성 메모리인 D램을 메인 메모리로 사용하기 때문에 전원이 사라지면 메모리가 저장하고 있는 데이터들을 잃어버린다. 이러한 D램보다 적은 전력 소모와 큰 용량을 제공하는 비휘발성 메모리(인텔의 옵테인 메모리)는 영구적으로 데이터를 기억할 수 있는 특징이 있다. 하지만, 복잡한 내부 구조 설계로 인한 느린 성능 때문에 온전히 메인 메모리로 사용되지 못하고, D램과 함께 사용해 비휘발성 메모리에 저장되는 일부 데이터만을 선택적으로 유지하는 형태로 사용된다. 또한 이상적인 환경 아래 비휘발성 메모리의 성능이 향상돼 메인 메모리로 단독 사용하더라도, 갑작스러운 전원 공급차단의 상황에서 컴퓨터의 모든 정보를 유지할 수는 없다. 비휘발성 메모리 내부에 존재하는 휘발성 구성요소와 프로세서 자체가 가지고 있는 레지스터나 캐시 메모리(휘발성) 같은 임시 저장 공간의 데이터는 전원 공급 없이 지속적 보존이 불가능하기 때문이다.
이러한 문제 때문에 기존의 컴퓨터에서 실행 상태와 데이터를 유지하기 위해서는, D램을 포함, 프로세서가 가지고 있는 휘발성 상태의 데이터들을 비휘발성 메모리나 저장장치인 SSD 등으로 옮기는 체크포인팅 기법등이 데이터 센터나 고성능 컴퓨터에서 사용되고 있다. 하지만 체크포인팅 방식은 주기적 데이터 이동에 추가적인 시간과 전력을 소모하며, 정전 후 전원이 인가되면 시스템 전체를 재부팅하는 데이터 복구 과정을 겪어야 하는 치명적인 단점이 존재한다.
우리 대학 정명수 교수 연구팀이 개발한 라이트PC는 이러한 과정 없이 컴퓨터의 모든 프로그램 실행 상태와 데이터들을 전원 없이 비휘발성으로 유지할 수 있는 프로세서와 메모리 컨트롤러, 그리고 운영체제 기술들을 개발해냈다. 이를 위해 연구팀은 기존 메모리나 스토리지 장치 없이 지속성 메모리만을 활용하여 시스템을 구성해, 시스템의 대부분 상태를 비휘발성으로 유지하게 했으며, 전원이 끊긴 직후 전원 공급 장치의 신호에 따라 프로세서의 남아 있는 비지속성 상태들을 비휘발성으로 변환하는 장치를 통해 정전 시에도 컴퓨터의 시간을 멈출 수 있게 만들었다.
이를 위해서 연구팀이 개발한 라이트PC 기술은 프로세서의 하드웨어 데이터 경로상의 휘발성 구성요소를 최소화하고, 복잡한 내부 구조를 최대한 단순화한 뒤, 데이터 처리의 병렬성을 극대화해 사용자가 일반적인 응용실행에서 D램만 사용하는 고성능 시스템과 큰 성능 차이를 느끼지 못하도록 성능을 개선했다. 또한, 컴퓨터의 시간을 멈추는 동안 일관성 유지를 위해 프로그램 실행이 비결정적으로 진행되지 않도록 임의의 상태/데이터의 변경을 막고 다양한 형태의 지속성 기능이 추가된 운영체제를 구축했다. 일관성이 유지되기 때문에 다시 전원이 인가되면 컴퓨터는 부팅 과정 없이 멈춘 시간부터 다시 실행될 수 있다.
연구팀은 라이트PC의 실효성을 검증하기 위해 자체 제작한 시스템 보드에 시제작한 지속성 메모리를 장착해 비휘발성 컴퓨터를 구축하고, 정전 시 컴퓨터의 시간을 멈추게 하는 운영체제 프로토타입을 제작해 비휘발성 컴퓨터 위에서 실행했다. 엔터프라이즈향 응용 프로그램이 실행되는 도중 무작위 시간에 전원을 제거한 뒤, 다시 인가했을 때 전원이 사라지기 직전의 상태로 모든 프로그램 실행과 데이터가 일관성 있게 복구되는 것을 연구팀은 확인했다. 이와 더불어 라이트PC는 기존 컴퓨터 대비 최대 8배 큰 메모리와 4.3배 빠른 응용실행 및 73%의 전력 소모 절감을 보였다.
정명수 교수는 "이번에 개발된 비휘발성 컴퓨터는 대용량 메모리 제공과 동시에 높은 신뢰성 및 서비스의 안전성을 제공할 수 있어 데이터 센터나 고성능 컴퓨팅의 저전력 운영으로 인한 탄소중립에너지 효율화에 극대화를 이룰 수 있을 것으로 예상된다. 또한 관련된 연구 핵심기술은 차량, 핸드폰 모바일, 사물인터넷 장치등의 베터리 사용량을 최소화하고 초연결사회를 이루는 등 다양하게 활용될 수 있을 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 미국 뉴욕시에서 오는 6월에 열릴 컴퓨터 구조 분야 최우수 학술대회인 `이스카(International Symposium on Computer Architecture, ISCA), 2022'에 라이트PC라는 논문명(LightPC: Hardware and Software Co-Desingn for Energy-Efficient Full System Persistence)으로 발표될 예정이다.
해당 연구는 차세대 메모리 개발 및 공급업체 멤레이, 과학기술정보통신부와 한국연구재단이 추진하는 우수신진(중견연계)사업, 그리고 정보통신기획평가원의 연구 지원을 받아 진행됐다. 비휘발성 컴퓨터의 실제 동작 및 자세한 내용은 연구실 웹사이트(http://camelab.org) 및 유튜브(https://youtu.be/mlF7W_RmYRk)에서 확인할 수 있다.
2022.04.25 조회수 10173
‘컴퓨터의 시간을 멈춘다’, 전원 공급 없이도 모든 정보가 복원, 작동되는 비휘발성 컴퓨터 최초 개발
우리 대학 전기및전자공학부 정명수 교수 연구팀(컴퓨터 아키텍처 및 메모리 시스템 연구실)이 컴퓨터의 시간을 멈추는 하드웨어/소프트웨어 기술, `경량화된 비휘발성 컴퓨팅 시스템(Lightweight Persistence Centric System, 이하 라이트PC)'을 세계 최초로 개발했다고 25일 밝혔다. 연구진의 컴퓨터에서는 시간이 멈춰진 순간의 모든 정보(실행 상태 및 데이터)는 전원 공급 여부와 관계없이 유지되며, 유지되는 모든 정보는 언제든 사용자가 원할 때 바로 복원, 작동될 수 있다.
기존의 컴퓨터는 휘발성 메모리인 D램을 메인 메모리로 사용하기 때문에 전원이 사라지면 메모리가 저장하고 있는 데이터들을 잃어버린다. 이러한 D램보다 적은 전력 소모와 큰 용량을 제공하는 비휘발성 메모리(인텔의 옵테인 메모리)는 영구적으로 데이터를 기억할 수 있는 특징이 있다. 하지만, 복잡한 내부 구조 설계로 인한 느린 성능 때문에 온전히 메인 메모리로 사용되지 못하고, D램과 함께 사용해 비휘발성 메모리에 저장되는 일부 데이터만을 선택적으로 유지하는 형태로 사용된다. 또한 이상적인 환경 아래 비휘발성 메모리의 성능이 향상돼 메인 메모리로 단독 사용하더라도, 갑작스러운 전원 공급차단의 상황에서 컴퓨터의 모든 정보를 유지할 수는 없다. 비휘발성 메모리 내부에 존재하는 휘발성 구성요소와 프로세서 자체가 가지고 있는 레지스터나 캐시 메모리(휘발성) 같은 임시 저장 공간의 데이터는 전원 공급 없이 지속적 보존이 불가능하기 때문이다.
이러한 문제 때문에 기존의 컴퓨터에서 실행 상태와 데이터를 유지하기 위해서는, D램을 포함, 프로세서가 가지고 있는 휘발성 상태의 데이터들을 비휘발성 메모리나 저장장치인 SSD 등으로 옮기는 체크포인팅 기법등이 데이터 센터나 고성능 컴퓨터에서 사용되고 있다. 하지만 체크포인팅 방식은 주기적 데이터 이동에 추가적인 시간과 전력을 소모하며, 정전 후 전원이 인가되면 시스템 전체를 재부팅하는 데이터 복구 과정을 겪어야 하는 치명적인 단점이 존재한다.
우리 대학 정명수 교수 연구팀이 개발한 라이트PC는 이러한 과정 없이 컴퓨터의 모든 프로그램 실행 상태와 데이터들을 전원 없이 비휘발성으로 유지할 수 있는 프로세서와 메모리 컨트롤러, 그리고 운영체제 기술들을 개발해냈다. 이를 위해 연구팀은 기존 메모리나 스토리지 장치 없이 지속성 메모리만을 활용하여 시스템을 구성해, 시스템의 대부분 상태를 비휘발성으로 유지하게 했으며, 전원이 끊긴 직후 전원 공급 장치의 신호에 따라 프로세서의 남아 있는 비지속성 상태들을 비휘발성으로 변환하는 장치를 통해 정전 시에도 컴퓨터의 시간을 멈출 수 있게 만들었다.
이를 위해서 연구팀이 개발한 라이트PC 기술은 프로세서의 하드웨어 데이터 경로상의 휘발성 구성요소를 최소화하고, 복잡한 내부 구조를 최대한 단순화한 뒤, 데이터 처리의 병렬성을 극대화해 사용자가 일반적인 응용실행에서 D램만 사용하는 고성능 시스템과 큰 성능 차이를 느끼지 못하도록 성능을 개선했다. 또한, 컴퓨터의 시간을 멈추는 동안 일관성 유지를 위해 프로그램 실행이 비결정적으로 진행되지 않도록 임의의 상태/데이터의 변경을 막고 다양한 형태의 지속성 기능이 추가된 운영체제를 구축했다. 일관성이 유지되기 때문에 다시 전원이 인가되면 컴퓨터는 부팅 과정 없이 멈춘 시간부터 다시 실행될 수 있다.
연구팀은 라이트PC의 실효성을 검증하기 위해 자체 제작한 시스템 보드에 시제작한 지속성 메모리를 장착해 비휘발성 컴퓨터를 구축하고, 정전 시 컴퓨터의 시간을 멈추게 하는 운영체제 프로토타입을 제작해 비휘발성 컴퓨터 위에서 실행했다. 엔터프라이즈향 응용 프로그램이 실행되는 도중 무작위 시간에 전원을 제거한 뒤, 다시 인가했을 때 전원이 사라지기 직전의 상태로 모든 프로그램 실행과 데이터가 일관성 있게 복구되는 것을 연구팀은 확인했다. 이와 더불어 라이트PC는 기존 컴퓨터 대비 최대 8배 큰 메모리와 4.3배 빠른 응용실행 및 73%의 전력 소모 절감을 보였다.
정명수 교수는 "이번에 개발된 비휘발성 컴퓨터는 대용량 메모리 제공과 동시에 높은 신뢰성 및 서비스의 안전성을 제공할 수 있어 데이터 센터나 고성능 컴퓨팅의 저전력 운영으로 인한 탄소중립에너지 효율화에 극대화를 이룰 수 있을 것으로 예상된다. 또한 관련된 연구 핵심기술은 차량, 핸드폰 모바일, 사물인터넷 장치등의 베터리 사용량을 최소화하고 초연결사회를 이루는 등 다양하게 활용될 수 있을 것으로 기대한다ˮ라고 말했다.
한편 이번 연구는 미국 뉴욕시에서 오는 6월에 열릴 컴퓨터 구조 분야 최우수 학술대회인 `이스카(International Symposium on Computer Architecture, ISCA), 2022'에 라이트PC라는 논문명(LightPC: Hardware and Software Co-Desingn for Energy-Efficient Full System Persistence)으로 발표될 예정이다.
해당 연구는 차세대 메모리 개발 및 공급업체 멤레이, 과학기술정보통신부와 한국연구재단이 추진하는 우수신진(중견연계)사업, 그리고 정보통신기획평가원의 연구 지원을 받아 진행됐다. 비휘발성 컴퓨터의 실제 동작 및 자세한 내용은 연구실 웹사이트(http://camelab.org) 및 유튜브(https://youtu.be/mlF7W_RmYRk)에서 확인할 수 있다.
2022.04.25 조회수 10173 합성생물학 기반 차세대 미생물 대사 조절 밸브 개발
국제 공동연구진이 대장균의 모든 전사종결부위*를 해독하고, 이를 바탕으로 미생물의 대사 경로를 수도꼭지처럼 자유자재로 조절하는 합성생물학** 기반 차세대 대사 조절 밸브 기술을 개발했다.
*전사종결부위: DNA가 암호화하는 정보를 RNA로 전사할 때, RNA 합성이 종결되도록 조절하는 DNA 서열
**합성생물학: 생명현상의 복잡성, 다양성으로 인해 발생하는 낮은 재현성, 예측효율 저하 등의 기존 바이오기술의 문제를 해결하기 위해 생명체의 구성요소를 설계, 제작, 조립하는 공학적 접근방식의 바이오 기술
우리 대학 생명과학과 조병관 교수, 한국생명공학연구원 이승구 박사, 바이오융합연구소 조수형 교수, 미국 캘리포니아대학교 샌디에이고(UCSD) 생명공학과(Bioengineering)의 최동희 박사, 버나드 팔슨(Bernhard Palsson) 교수 국제 공동연구팀이 대장균에 존재하는 1,600여 개의 전사종결부위를 대량으로 해독 및 발굴하고, 이를 기반으로 고부가가치 바이오화합물 생산을 위한 미생물 대사 회로 설계를 가능케 하는 합성생물학 기반 기술을 개발했다고 14일 밝혔다.
전사종결부위는 DNA가 암호화하는 유전 정보가 RNA로 전사될 때, 원하는 유전자만이 정확히 전사되도록 조절하는 역할을 한다. 그 중요성에도 불구하고 기존에는 전사 종결에 관한 데이터의 부족으로, 구체적인 조절 기작에 대한 이해가 부족했다. 연구진은 전사종결부위가 다양한 세기를 가져 인접한 유전자들의 발현을 정교하게 조절한다는 사실을 발견하고, 이를 대사회로 조절에 이용했다.
한편 미생물은 다양한 유용 바이오화합물 생산에 이용되고 있는데, 효율적인 생산을 위해서는 대사 회로의 조절이 필수적이다. 그 이유는 단순히 원하는 물질 생산을 위한 유전자만을 과도하게 발현할 경우, 미생물 생장에 필요한 양분과 에너지까지 소모해 생산에 실패하기 때문이다. 공동연구진은 개발한 전사종결부위를 통해 서로 다른 대사 회로의 세기를 수도꼭지처럼 조절해 대사물질 생산을 최적화할 수 있는 '대사 밸브 기술'을 개발했다.
기존에는 전사의 시작이 되는 프로모터, 번역의 시작이 되는 리보솜 결합 부위를 통해 유전자 발현을 조절했는데, 이에는 수많은 인자가 관여하고 있어 실험 간 편차가 크고, 고가의 화학물질을 요구하는 등 한계를 지니고 있었다. 하지만 연구진이 개발한 대사 밸브는 실험 간 편차를 기존 시스템 대비 최대 75% 억제할 수 있는 것으로 나타났고, 대사 밸브를 이용한 생산 최적화를 통해 유용 대사물질인 비타민 B8의 생산을 최대 11배 증대하는 데 성공했다.
또한 개발된 기술은 미생물의 생장 조건(영양분 및 배양 환경)에 거의 영향을 받지 않는 것으로 나타나 실험실 조건에서 출발해 산업 규모로 확장할 시 부수적인 최적화 과정을 최소화할 수 있고, 목적 화합물에 따라 첨가하는 원료와 배양 조건이 변화해도 조절 기작이 유지되는 것으로 나타났다.
이번 연구 결과는 기존에 알려지지 않았던 전사종결부위의 특성을 규명하고, 이를 대사 조절에 이용한 획기적인 시도로 차세대 대사 조절 합성생물학 기반 기술로 기대받고 있다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 C1 가스 리파이너리 프로그램 및 한국 바이오 그랜드챌린지 프로그램의 지원을 받은 KAIST 조병관 교수 연구진과 한국생명공학연구원이 추진하는 KRIBB 연구 혁신 프로그램(Research Initiative Program)의 지원을 받은 이승구 박사(한국생명공학연구원), 기초과학 연구 프로그램(Basic Science Research Program)의 지원을 받은 KAIST 조수형 교수, 노보 노르디스크 재단(Novo Nordisk Foundation)의 연구지원을 받은 버나드 팔슨(Bernhard Palsson) 교수 연구진의 협업을 통해 수행됐으며, 국제적인 학술지인 `핵산 연구(Nucleic Acids Research, 영향력지수 16.971)' 에 3월 31일 게재됐다.
(논문명 : Synthetic 3'-UTR valves for optimal metabolic flux control in Escherichia coli)
2022.04.17 조회수 13258
합성생물학 기반 차세대 미생물 대사 조절 밸브 개발
국제 공동연구진이 대장균의 모든 전사종결부위*를 해독하고, 이를 바탕으로 미생물의 대사 경로를 수도꼭지처럼 자유자재로 조절하는 합성생물학** 기반 차세대 대사 조절 밸브 기술을 개발했다.
*전사종결부위: DNA가 암호화하는 정보를 RNA로 전사할 때, RNA 합성이 종결되도록 조절하는 DNA 서열
**합성생물학: 생명현상의 복잡성, 다양성으로 인해 발생하는 낮은 재현성, 예측효율 저하 등의 기존 바이오기술의 문제를 해결하기 위해 생명체의 구성요소를 설계, 제작, 조립하는 공학적 접근방식의 바이오 기술
우리 대학 생명과학과 조병관 교수, 한국생명공학연구원 이승구 박사, 바이오융합연구소 조수형 교수, 미국 캘리포니아대학교 샌디에이고(UCSD) 생명공학과(Bioengineering)의 최동희 박사, 버나드 팔슨(Bernhard Palsson) 교수 국제 공동연구팀이 대장균에 존재하는 1,600여 개의 전사종결부위를 대량으로 해독 및 발굴하고, 이를 기반으로 고부가가치 바이오화합물 생산을 위한 미생물 대사 회로 설계를 가능케 하는 합성생물학 기반 기술을 개발했다고 14일 밝혔다.
전사종결부위는 DNA가 암호화하는 유전 정보가 RNA로 전사될 때, 원하는 유전자만이 정확히 전사되도록 조절하는 역할을 한다. 그 중요성에도 불구하고 기존에는 전사 종결에 관한 데이터의 부족으로, 구체적인 조절 기작에 대한 이해가 부족했다. 연구진은 전사종결부위가 다양한 세기를 가져 인접한 유전자들의 발현을 정교하게 조절한다는 사실을 발견하고, 이를 대사회로 조절에 이용했다.
한편 미생물은 다양한 유용 바이오화합물 생산에 이용되고 있는데, 효율적인 생산을 위해서는 대사 회로의 조절이 필수적이다. 그 이유는 단순히 원하는 물질 생산을 위한 유전자만을 과도하게 발현할 경우, 미생물 생장에 필요한 양분과 에너지까지 소모해 생산에 실패하기 때문이다. 공동연구진은 개발한 전사종결부위를 통해 서로 다른 대사 회로의 세기를 수도꼭지처럼 조절해 대사물질 생산을 최적화할 수 있는 '대사 밸브 기술'을 개발했다.
기존에는 전사의 시작이 되는 프로모터, 번역의 시작이 되는 리보솜 결합 부위를 통해 유전자 발현을 조절했는데, 이에는 수많은 인자가 관여하고 있어 실험 간 편차가 크고, 고가의 화학물질을 요구하는 등 한계를 지니고 있었다. 하지만 연구진이 개발한 대사 밸브는 실험 간 편차를 기존 시스템 대비 최대 75% 억제할 수 있는 것으로 나타났고, 대사 밸브를 이용한 생산 최적화를 통해 유용 대사물질인 비타민 B8의 생산을 최대 11배 증대하는 데 성공했다.
또한 개발된 기술은 미생물의 생장 조건(영양분 및 배양 환경)에 거의 영향을 받지 않는 것으로 나타나 실험실 조건에서 출발해 산업 규모로 확장할 시 부수적인 최적화 과정을 최소화할 수 있고, 목적 화합물에 따라 첨가하는 원료와 배양 조건이 변화해도 조절 기작이 유지되는 것으로 나타났다.
이번 연구 결과는 기존에 알려지지 않았던 전사종결부위의 특성을 규명하고, 이를 대사 조절에 이용한 획기적인 시도로 차세대 대사 조절 합성생물학 기반 기술로 기대받고 있다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 C1 가스 리파이너리 프로그램 및 한국 바이오 그랜드챌린지 프로그램의 지원을 받은 KAIST 조병관 교수 연구진과 한국생명공학연구원이 추진하는 KRIBB 연구 혁신 프로그램(Research Initiative Program)의 지원을 받은 이승구 박사(한국생명공학연구원), 기초과학 연구 프로그램(Basic Science Research Program)의 지원을 받은 KAIST 조수형 교수, 노보 노르디스크 재단(Novo Nordisk Foundation)의 연구지원을 받은 버나드 팔슨(Bernhard Palsson) 교수 연구진의 협업을 통해 수행됐으며, 국제적인 학술지인 `핵산 연구(Nucleic Acids Research, 영향력지수 16.971)' 에 3월 31일 게재됐다.
(논문명 : Synthetic 3'-UTR valves for optimal metabolic flux control in Escherichia coli)
2022.04.17 조회수 13258 6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2022.03.07 조회수 12901
6개의 표적 물질을 동시에 검출할 수 있는 질병물질 검출 종이센서 개발
우리 대학 생명화학공학과 이진우 교수 연구팀이 가천대학교 바이오나노학과 김문일 교수팀, POSTECH 화학공학과의 한정우 교수팀과 함께 새로운 무기 소재(*나노자임, Nanozyme)를 합성하는 데 성공하였고, 이를 이용해 종이 기반 질병 물질 검출 센서에 도입, 6개의 표적 물질을 동시에 그리고 민감하게 검출 가능한 종이 센서를 개발했다고 7일 밝혔다.
☞나노자임(Nanozyme): 단백질로 이루어진 효소와 달리 무기물질로 합성된 효소 모방 물질을 말한다. 기존 효소의 단점으로 꼽히는 안정성, 생산성 그리고 가격적 측면에서 매우 뛰어나며, 기존의 효소가 사용되던 질병 진단 시스템에 그대로 활용될 수 있다.
공동연구팀은 기존의 과산화효소 모방 나노자임들과 달리 중성에서 활성을 지니며 큰 기공(구멍)을 가져 산화효소를 적재할 수 있는 코발트가 도핑된 메조 다공성 구조의 산화 세륨을 개발했고, 이를 이용해 질병 진단물질인 글루코오스, 아세틸콜린, 콜레스테롤을 비롯한 6개의 물질을 동시에 검출 가능한 종이 센서를 개발했다.
생명화학공학과 이준상 박사과정생이 가천대학교 바이오나노학과 푸엉 타이 응우옌(Phuong Thy Nguyen) 박사과정생, 포항공과대학교 화학공학과 조아라 박사과정생과 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 펑셔널 머터리얼즈(Advanced Functional Materials)' 2월 19권 2호에 출판됐다. (논문명 : Rational Development of Co-Doped Mesoporous Ceria with High Peroxidase-Mimicking Activity at Neutral pH for Paper-Based Colorimetric Detection of Multiple Biomarkers).
나노자임은 기존의 효소가 사용되던 다양한 질병의 검출에 사용될 수 있을 뿐만 아니라 효소가 사용되기 어려웠던 극한 환경 혹은 다양한 미세환경이 존재하는 체내에서도 그 역할을 수행할 수 있어 목적에 맞는 활성을 지니는 나노자임의 필요성이 더욱 강조되고 있다.
효소는 우리의 몸속의 다양한 화학 반응에 촉매로서 작용을 하고 있었지만, 최근에는 이러한 효소들을 정제해서 다양한 물질들을 검출 및 치료 등 다방면에서의 활용이 가능하다는 것이 보고돼왔다. 특히 과산화효소의 경우 과산화수소의 존재 하에서 투명한 발색 기질을 산화시켜 푸른색을 띠기 때문에 과산화수소를 시각적으로 검출할 수 있으며, 이를 이용해 산화 과정에서 과산화수소를 배출하는 아세틸콜린, 글루코오스를 포함한 다양한 물질들의 산화효소와 함께 사용되면 표적 물질을 시각적으로 검출할 수 있다.
하지만 아세틸콜린, 글루코오스 등을 산화시키는 대부분의 산화 효소는 중성에서 최적 활성을 가지는 것과 달리, 과산화효소 모방 나노자임은 산성에서만 활성을 지니기 때문에 중간에 수소 이온 농도 지수(pH)를 조절하는 버퍼 용액을 변경해야 하거나, 최적 활성이 아닌 지점에서 반응이 일어나 표적 물질의 미세한 검출을 하기 어렵고, 바이오 센서로서의 적용도 어렵다. 이 때문에 중성 상태에서도 과산화효소 활성을 모방하면서 표적 물질의 산화효소를 담을 수 있는 나노자임의 개발이 필수적이다.
공동연구팀은 문제 해결을 위해 밀도범함수이론(Density Functional Theory, DFT)을 도입해 기존에 과산화효소 활성이 있던 산화 세륨 위에 어떠한 원소를 도핑할 경우 중성에도 과산화효소 활성이 유지될지 스크리닝을 진행했고, 코발트 원소가 최적 물질임을 계산을 통해 예측했다.
연구팀은 중성에서의 활성을 유도할 코발트 원소를 도핑하면서 산화효소를 적재할 수 있게 17 나노미터(nm)의 큰 기공을 지니는 메조 다공성 구조의 산화세륨 합성에 성공했다. 메조 다공성 나노물질들이 2~3 나노미터(nm) 기공을 지니는 것과 달리, 연구팀은 열처리 과정에서의 변화를 통해 큰 기공을 지니도록 합성할 수 있었고, 이 기공에 산화효소들을 적재할 수 있다는 것을 확인했다. 또한, 합성된 나노자임은 중성(pH 6)에서 최적 활성을 지녀 pH의 변경 없이 산화효소와 연쇄 반응을 일으킬 수 있었다.
연구팀은 개발한 나노자임에 중요한 질병 진단물질인 글루코오스, 아세틸콜린, 콜린, 갈락토오스, 콜레스테롤의 산화효소를 담아, 과산화수소를 포함한 6개 물질을 동시에 검출이 가능한 종이 센서를 개발했다. 이 종이 센서는 20분 만에 6개 물질을 빠르게 검출할 수 있으며, 기존 하나씩만을 검출할 수 있는 센서들의 검출한계보다 더 좋은 성능을 보였다. 또한 연구팀은 산화효소를 메조 다공성 산화세륨에 적재해 60℃의 고온에서도 안정적이고, 60일이 넘는 시간 동안 안정적으로 작동함을 확인했다.
이 교수는 "나노자임은 분야 자체가 시작된 지 오래되지 않았지만, 기존 효소를 대체해 쓰일 수 있다는 잠재성 때문에 폭발적으로 관심이 증가하고 있다ˮ라며 "앞으로 종이 센서 뿐만 아니라 각종 진단 및 암 치료에 나노자임을 도입해 진단 및 치료 분야에 큰 도약을 이뤄낼 가능성이 있다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.
2022.03.07 조회수 12901 전하 전달 복합체를 이용한 신개념 디스플레이 소재 개발
우리 대학 신소재공학과 정연식 교수, 전덕영 명예교수, 한국전자통신연구원(ETRI) 권병화 박사 공동 연구팀이 차세대 디스플레이 소자에 적용 가능한 신개념 금속 산화물 복합 나노소재 개발에 성공했다고 19일 밝혔다.
KAIST-ETRI 공동 연구팀은 특정 금속 산화물 나노입자가 다른 산화물 내부에서 나노미터(nm) 크기로 분산될 경우, 접촉면(인터페이스)에서 전하가 교환되면서 전하 전달 복합체(Charge transfer complex)를 형성하는 새로운 현상을 발견했다. 연구팀은 이를 유기발광다이오드(OLED) 등 고부가가치 디스플레이에 적용해 기존 상용 유기 소재 기반의 소자 성능을 뛰어넘는 데 성공했다.
오는 2월에 우리 대학 신소재공학 박사학위 취득 예정인 김무현 연구원이 주도하고 조남명 박사, ETRI 주철웅 선임연구원 등이 참여한 이번 연구는 국제학술지 `네이처 커뮤니케이션스(Nature Communications)' 1월 10일 字 온라인판에 게재됐다. (논문명: Metal Oxide Charge Transfer Complex for Effective Energy Band Tailoring in Multilayer Optoelectronics)
디스플레이 발광 셀 등 다층구조를 가지는 광전자소자에서 금속 산화물은 우수한 전기적 특성 및 안정성 덕분에 전하 수송 및 주입 층으로 널리 활용되고 있다. 하지만, 유기 발광 다이오드(OLED)에서 퀀텀닷 발광다이오드(QLED), 페로브스카이트 발광다이오드(PeLED)로 이어지는 미래 디스플레이 산업에서 이러한 금속 산화물 소재를 더 유용하게 활용하기 위해서는 에너지 레벨 및 전기전도도와 같은 특성들이 더 넓은 범위에서 제어될 수 있어야 한다.
이는 유기 발광 소재, 퀀텀닷, 페로브스카이트 등으로 발광층 소재가 매우 다양해짐에 따라 디스플레이 소자들의 성능을 극대화하기 위해서는 각각의 시스템에 최적화된 전기적 특성을 제공해야 하기 때문이다.
연구팀은 에너지 레벨 차이가 있는 두 금속 산화물 사이에서 일어나는 전하 전달(Charge transfer) 현상에 주목했다. 전하 전달 복합체는 마치 건포도 빵의 형태와 유사한 구조로 되어 있는데, 건포도(나노입자)를 더 넣게 되면 더 많은 당분(전하)이 빵(매트릭스)으로 이동하여 빵 전체가 더 달콤해지는 원리로 비유될 수 있다.
이 새로운 개념을 산화 몰리브덴(MoO3) 나노입자와 산화니켈(NiO)의 조합으로 구현해 두 금속 산화물의 전하 전달 현상을 효과적으로 유도했으며, 광범위한 에너지 레벨 조절 능력 및 최대 2.4배의 전기전도도 향상을 달성했다. 이를 녹색과 청색 OLED에 적용했고 기존의 상용 유기 소재를 적용한 소자보다 32% 더 우수한 외부양자효율을 달성함으로 높은 범용성과 성능을 입증했다.
신소재공학과 정연식 교수는 "이번 기술은 핵심 소재의 성능 제어 방법을 혁신함으로써, 실감형 메타버스 구현에 꼭 필요한 최첨단 디스플레이 구현에 기여할 것ˮ이라고 전망했다.
이번 연구는 과학기술정보통신부 및 한국연구재단이 추진하는 미래소재디스커버리지원사업(단장 최성율), 글로벌프런티어 사업(단장 김광호) 및 나노·소재기술개발사업, 그리고 산업통상자원부에서 추진하는 소재부품장비혁신 Lab기술개발사업의 지원을 받아 수행됐다.
2022.01.24 조회수 15125
전하 전달 복합체를 이용한 신개념 디스플레이 소재 개발
우리 대학 신소재공학과 정연식 교수, 전덕영 명예교수, 한국전자통신연구원(ETRI) 권병화 박사 공동 연구팀이 차세대 디스플레이 소자에 적용 가능한 신개념 금속 산화물 복합 나노소재 개발에 성공했다고 19일 밝혔다.
KAIST-ETRI 공동 연구팀은 특정 금속 산화물 나노입자가 다른 산화물 내부에서 나노미터(nm) 크기로 분산될 경우, 접촉면(인터페이스)에서 전하가 교환되면서 전하 전달 복합체(Charge transfer complex)를 형성하는 새로운 현상을 발견했다. 연구팀은 이를 유기발광다이오드(OLED) 등 고부가가치 디스플레이에 적용해 기존 상용 유기 소재 기반의 소자 성능을 뛰어넘는 데 성공했다.
오는 2월에 우리 대학 신소재공학 박사학위 취득 예정인 김무현 연구원이 주도하고 조남명 박사, ETRI 주철웅 선임연구원 등이 참여한 이번 연구는 국제학술지 `네이처 커뮤니케이션스(Nature Communications)' 1월 10일 字 온라인판에 게재됐다. (논문명: Metal Oxide Charge Transfer Complex for Effective Energy Band Tailoring in Multilayer Optoelectronics)
디스플레이 발광 셀 등 다층구조를 가지는 광전자소자에서 금속 산화물은 우수한 전기적 특성 및 안정성 덕분에 전하 수송 및 주입 층으로 널리 활용되고 있다. 하지만, 유기 발광 다이오드(OLED)에서 퀀텀닷 발광다이오드(QLED), 페로브스카이트 발광다이오드(PeLED)로 이어지는 미래 디스플레이 산업에서 이러한 금속 산화물 소재를 더 유용하게 활용하기 위해서는 에너지 레벨 및 전기전도도와 같은 특성들이 더 넓은 범위에서 제어될 수 있어야 한다.
이는 유기 발광 소재, 퀀텀닷, 페로브스카이트 등으로 발광층 소재가 매우 다양해짐에 따라 디스플레이 소자들의 성능을 극대화하기 위해서는 각각의 시스템에 최적화된 전기적 특성을 제공해야 하기 때문이다.
연구팀은 에너지 레벨 차이가 있는 두 금속 산화물 사이에서 일어나는 전하 전달(Charge transfer) 현상에 주목했다. 전하 전달 복합체는 마치 건포도 빵의 형태와 유사한 구조로 되어 있는데, 건포도(나노입자)를 더 넣게 되면 더 많은 당분(전하)이 빵(매트릭스)으로 이동하여 빵 전체가 더 달콤해지는 원리로 비유될 수 있다.
이 새로운 개념을 산화 몰리브덴(MoO3) 나노입자와 산화니켈(NiO)의 조합으로 구현해 두 금속 산화물의 전하 전달 현상을 효과적으로 유도했으며, 광범위한 에너지 레벨 조절 능력 및 최대 2.4배의 전기전도도 향상을 달성했다. 이를 녹색과 청색 OLED에 적용했고 기존의 상용 유기 소재를 적용한 소자보다 32% 더 우수한 외부양자효율을 달성함으로 높은 범용성과 성능을 입증했다.
신소재공학과 정연식 교수는 "이번 기술은 핵심 소재의 성능 제어 방법을 혁신함으로써, 실감형 메타버스 구현에 꼭 필요한 최첨단 디스플레이 구현에 기여할 것ˮ이라고 전망했다.
이번 연구는 과학기술정보통신부 및 한국연구재단이 추진하는 미래소재디스커버리지원사업(단장 최성율), 글로벌프런티어 사업(단장 김광호) 및 나노·소재기술개발사업, 그리고 산업통상자원부에서 추진하는 소재부품장비혁신 Lab기술개발사업의 지원을 받아 수행됐다.
2022.01.24 조회수 15125 사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
2021.12.08 조회수 12574
사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
2021.12.08 조회수 12574 악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30 조회수 12607
악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30 조회수 12607