%ED%99%94%ED%95%99%EA%B3%BC
-
 ‘슝’ 스스로 움직이는 생명체 세포로봇 개발
현재 전 세계적으로 마이크로 및 나노급의 작은 입자 기반의 비생명체 자가 추진 로봇 기술은 활발하게 연구되고 있는 반면에, 세포와 같은 생명체 구성 요소를 직접 활용한 세포로봇 연구는 아직 초기 단계에 머물러 있다. 우리 연구진이 세포 기반 시스템의 자율적으로 이동하는 세포로봇을 개발하는데 성공했다. 향후 정밀 약물 전달이나 차세대 세포 기반 치료법의 원천기술로 활용될 수 있을 것으로 기대된다.
우리 대학 화학과 최인성 교수 연구팀이 외부 동력 장치나 복잡한 기계 구조 없이, 생체 부산물인 ‘요소(urea)’*를 연료로 사용하는 자가 추진 세포로봇을 개발했다고 30일 밝혔다.
*요소(urea): 사람을 포함한 대부분의 동물 체내에서 단백질을 분해하면서 생기는 노폐물로 생명체 안에서는 단백질 대사 과정에서 암모니아를 독성이 낮은 형태로 전환하여 배출하는 중요한 역할을 함
연구팀이 구현한 세포로봇은 방향성을 갖고 스스로 이동할 수 있으며, 원하는 물질을 운반하거나 주변 환경 제어 기능을 탑재할 수 있는 다기능성 플랫폼으로 설계됐다.
연구팀은 쉽고 안정적으로 얻을 수 있는 생명체이면서 부산물로 생성된 에탄올 활용 가능성이 있고, 인공적인 복잡한 외부 장치 없이 생명체 스스로 만들어내는 물질을 활용할 수 있는 ‘효모’에 주목했다.
제빵과 막걸리 발효에 사용되는 효모(이스트, yeast)는 포도당을 분해해 에너지를 얻는 대사 과정에서 알코올(에탄올)을 부산물로 생성하는데, 연구팀은 이때 생성된 에탄올을 활용해 효모 표면에 생체친화적인 방식으로 나노 껍질을 형성할 수 있는 원천기술을 개발했다.
이를 위해, 알코올산화효소(AOx)와 겨자무과산화효소(HRP)로 구성된 효소 시스템을 도입했다. 이 효소 시스템은 효모의 포도당 분해 반응과 연계된 연쇄적 효소 반응을 유도하며, 그 결과로 멜라닌 계열의 나노껍질이 효모 표면에 형성된다.
특히, 이번에 개발된 화학적 방법론은 효모가 성장하고 분열하는 동안에도 나노껍질 형성이 지속적으로 일어나도록 설계돼 있어서, 세포의 형태 변화에 따라 비대칭적인 세포-껍질 구조가 자연스럽게 생성된다.
예를 들어, 분열 중인 세포 전체를 감싸는 껍질이 형성되기도 하지만, 모세포 부분에는 껍질이 생성되고 딸세포 부분에는 형성되지 않는 구조도 만들어진다.
연구팀은 세포를 감싸는 나노껍질에 우레아제(urease)*를 부착하고 세포로봇의 움직임을 관찰했다. 우레아제는 요소를 분해하는 촉매 역할을 하며 세포로봇이 스스로 움직일 수 있도록 구동력을 만들어내는 핵심 역할을 수행하며 비대칭 구조를 가진 세포로봇이 보다 명확한 방향성을 갖고 자가 추진하는 현상을 확인했다.
*우레아제(urease): 요소를 분해해 암모니아와 이산화탄소를 만드는 효소
이번에 개발된 세포로봇은 세포 주위에 존재하는 물질만으로 자가 추진이 가능하고, 자석이나 레이저 등 복잡한 외부 제어 장치에 의존하지 않아 구동 메커니즘이 훨씬 간단하고 생체친화적이다. 또한, 나노껍질에 다양한 효소를 화학적으로 접합할 수 있어, 다양한 생체 물질을 연료로 활용하는 세포로봇의 확장 개발도 가능하다.
이번 연구의 제1 저자인 화학과 김나영 박사과정은 “자가 추진 세포로봇은 스스로 환경을 감지하고 반응하며 움직이는 능력을 지닌 새로운 개념의 플랫폼으로, 향후 암세포 표적 치료나 정밀 약물전달시스템 등에서 중요한 역할을 할 수 있을 것”이라고 말했다.
이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’에 지난 6월 25일 오후 2시(미국 동부시각) 온라인판에 게재됐다.
※ 논문명 : Autonomous Chemo-Metabolic Construction of Anisotropic Cell-in-Shell Nanobiohybrids in Enzyme-Powered Cell Microrobots; 국문 번역 : 효소 구동 세포 마이크로로봇 구축에서의 자율적인 화학-대사 반응을 통해 형성된 비등방성 세포내껍질 나노바이오하이브리드
※ DOI: https://doi.org/10.1126/sciadv.adu5451
한편, 이번 연구는 한국연구재단 기초연구사업 중견연구과제(제목: 세포대사 연계형 단일세포나노피포화)의 지원을 받아 수행됐다.
2025.06.30 조회수 1039
‘슝’ 스스로 움직이는 생명체 세포로봇 개발
현재 전 세계적으로 마이크로 및 나노급의 작은 입자 기반의 비생명체 자가 추진 로봇 기술은 활발하게 연구되고 있는 반면에, 세포와 같은 생명체 구성 요소를 직접 활용한 세포로봇 연구는 아직 초기 단계에 머물러 있다. 우리 연구진이 세포 기반 시스템의 자율적으로 이동하는 세포로봇을 개발하는데 성공했다. 향후 정밀 약물 전달이나 차세대 세포 기반 치료법의 원천기술로 활용될 수 있을 것으로 기대된다.
우리 대학 화학과 최인성 교수 연구팀이 외부 동력 장치나 복잡한 기계 구조 없이, 생체 부산물인 ‘요소(urea)’*를 연료로 사용하는 자가 추진 세포로봇을 개발했다고 30일 밝혔다.
*요소(urea): 사람을 포함한 대부분의 동물 체내에서 단백질을 분해하면서 생기는 노폐물로 생명체 안에서는 단백질 대사 과정에서 암모니아를 독성이 낮은 형태로 전환하여 배출하는 중요한 역할을 함
연구팀이 구현한 세포로봇은 방향성을 갖고 스스로 이동할 수 있으며, 원하는 물질을 운반하거나 주변 환경 제어 기능을 탑재할 수 있는 다기능성 플랫폼으로 설계됐다.
연구팀은 쉽고 안정적으로 얻을 수 있는 생명체이면서 부산물로 생성된 에탄올 활용 가능성이 있고, 인공적인 복잡한 외부 장치 없이 생명체 스스로 만들어내는 물질을 활용할 수 있는 ‘효모’에 주목했다.
제빵과 막걸리 발효에 사용되는 효모(이스트, yeast)는 포도당을 분해해 에너지를 얻는 대사 과정에서 알코올(에탄올)을 부산물로 생성하는데, 연구팀은 이때 생성된 에탄올을 활용해 효모 표면에 생체친화적인 방식으로 나노 껍질을 형성할 수 있는 원천기술을 개발했다.
이를 위해, 알코올산화효소(AOx)와 겨자무과산화효소(HRP)로 구성된 효소 시스템을 도입했다. 이 효소 시스템은 효모의 포도당 분해 반응과 연계된 연쇄적 효소 반응을 유도하며, 그 결과로 멜라닌 계열의 나노껍질이 효모 표면에 형성된다.
특히, 이번에 개발된 화학적 방법론은 효모가 성장하고 분열하는 동안에도 나노껍질 형성이 지속적으로 일어나도록 설계돼 있어서, 세포의 형태 변화에 따라 비대칭적인 세포-껍질 구조가 자연스럽게 생성된다.
예를 들어, 분열 중인 세포 전체를 감싸는 껍질이 형성되기도 하지만, 모세포 부분에는 껍질이 생성되고 딸세포 부분에는 형성되지 않는 구조도 만들어진다.
연구팀은 세포를 감싸는 나노껍질에 우레아제(urease)*를 부착하고 세포로봇의 움직임을 관찰했다. 우레아제는 요소를 분해하는 촉매 역할을 하며 세포로봇이 스스로 움직일 수 있도록 구동력을 만들어내는 핵심 역할을 수행하며 비대칭 구조를 가진 세포로봇이 보다 명확한 방향성을 갖고 자가 추진하는 현상을 확인했다.
*우레아제(urease): 요소를 분해해 암모니아와 이산화탄소를 만드는 효소
이번에 개발된 세포로봇은 세포 주위에 존재하는 물질만으로 자가 추진이 가능하고, 자석이나 레이저 등 복잡한 외부 제어 장치에 의존하지 않아 구동 메커니즘이 훨씬 간단하고 생체친화적이다. 또한, 나노껍질에 다양한 효소를 화학적으로 접합할 수 있어, 다양한 생체 물질을 연료로 활용하는 세포로봇의 확장 개발도 가능하다.
이번 연구의 제1 저자인 화학과 김나영 박사과정은 “자가 추진 세포로봇은 스스로 환경을 감지하고 반응하며 움직이는 능력을 지닌 새로운 개념의 플랫폼으로, 향후 암세포 표적 치료나 정밀 약물전달시스템 등에서 중요한 역할을 할 수 있을 것”이라고 말했다.
이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’에 지난 6월 25일 오후 2시(미국 동부시각) 온라인판에 게재됐다.
※ 논문명 : Autonomous Chemo-Metabolic Construction of Anisotropic Cell-in-Shell Nanobiohybrids in Enzyme-Powered Cell Microrobots; 국문 번역 : 효소 구동 세포 마이크로로봇 구축에서의 자율적인 화학-대사 반응을 통해 형성된 비등방성 세포내껍질 나노바이오하이브리드
※ DOI: https://doi.org/10.1126/sciadv.adu5451
한편, 이번 연구는 한국연구재단 기초연구사업 중견연구과제(제목: 세포대사 연계형 단일세포나노피포화)의 지원을 받아 수행됐다.
2025.06.30 조회수 1039 -
 폐타이어를 고무·나일론 원료로 전환 성공
전 세계적으로 매년 수십억 개의 타이어가 폐기되며, 이는 심각한 환경오염의 주요 원인 중 하나로 지목되고 있다. 우리 연구진이 폐타이어를 고무나 나일론 섬유 원료로 쓰이는 고부가가치 화학 원료인 고순도의 고리형 알켄으로 선택적 전환하는 데 성공했다. 이는 폐타이어 재활용 분야의 새로운 전환점으로 평가된다.
우리 대학 화학과 홍순혁 교수 연구팀이 이중 촉매 기반 연속 반응 시스템을 개발해 폐타이어 문제를 효과적으로 해결했다고 26일 밝혔다.
폐타이어는 합성고무와 천연고무의 복합체로 구성되며, 실리카, 카본블랙, 산화방지제 등의 첨가제를 포함해 물리적 강도와 내구성이 극대화되어 있다. 특히 가황 공정을 통해 고무 사슬 간의 가교가 형성돼 열과 압력에 강한 구조를 갖게 되는데, 이는 폐타이어의 화학적 재활용을 어렵게 만드는 주요 원인 중 하나다.
그동안 폐타이어의 재활용은 주로 열분해 방식이나 물리적 분쇄 재활용에 의존해 왔다. 열분해 방식은 350~800°C의 고온 환경에서 고분자 사슬을 분해해 연료유로 전환하는 기술이나, 높은 에너지 소비, 낮은 선택성, 그리고 저품질의 탄화수소 혼합물 생성이라는 한계가 명확히 존재한다.
연구팀은 이런 문제를 해결하고자 두 가지 촉매를 활용해 폐고무를 유용한 화학물질로 바꾸는 방법을 개발하였다. 첫 번째 촉매는 고무 분자 안의 결합 구조를 바꿔 분해가 잘 되도록 돕고, 두 번째 촉매는 고리를 닫는 반응을 통해 고리 모양의 화합물을 만들어낸다.
이 과정은 최대 92%의 높은 선택성과 82%의 수율을 보여준다. 만들어진 고리형 펜텐은 다시 고무로 재활용할 수 있고, 고리형 헥센은 나일론 섬유의 원료로 쓰이는 등 산업적으로 매우 가치가 높다.
연구팀은 개발한 시스템을 실제 폐기물로 버려진 폐타이어에 적용해, 고순도의 고리형 알켄으로 선택적 전환하는 데 성공했다. 이는 기존 열분해 방식과 달리 저온의 정밀 촉매 반응을 통해 고부가가치 화학 원료를 생산할 수 있다는 점에서 폐타이어 재활용 분야의 새로운 전환점으로 평가된다.
또한, 이번 기술은 다양한 종류의 합성고무와 폐고무에 폭넓게 적용될 수 있어, 자원 순환형 경제 실현에 기여할 수 있는 핵심 원천기술로 주목받고 있다.
홍순혁 교수는 “이번 연구는 폐타이어의 화학적 재활용에 대한 혁신적인 해법을 제시한 것이며, 경제성을 높이기 위해 차세대 고효율 촉매 개발, 상용화를 위한 기반을 마련해 나갈 예정이다”며, “기초화학을 통해 폐플라스틱 문제 해결에 기여하는 것이 목표”라고 밝혔다.
우리 대학 화학과 박범순, 조경일, 최경민 연구원이 참여한 이번 연구는 한국연구재단의 지원으로 수행됐으며, 국제 저명 학술지 ‘Chem’에 6월 18일 자로 온라인 게재됐다.
※논문명: Catalytic and Selective Chemical Recycling of Post-Consumer Rubbers into Cycloalkenes
※DOI: 10.1016/j.chempr.2025.102625
2025.06.26 조회수 1044
폐타이어를 고무·나일론 원료로 전환 성공
전 세계적으로 매년 수십억 개의 타이어가 폐기되며, 이는 심각한 환경오염의 주요 원인 중 하나로 지목되고 있다. 우리 연구진이 폐타이어를 고무나 나일론 섬유 원료로 쓰이는 고부가가치 화학 원료인 고순도의 고리형 알켄으로 선택적 전환하는 데 성공했다. 이는 폐타이어 재활용 분야의 새로운 전환점으로 평가된다.
우리 대학 화학과 홍순혁 교수 연구팀이 이중 촉매 기반 연속 반응 시스템을 개발해 폐타이어 문제를 효과적으로 해결했다고 26일 밝혔다.
폐타이어는 합성고무와 천연고무의 복합체로 구성되며, 실리카, 카본블랙, 산화방지제 등의 첨가제를 포함해 물리적 강도와 내구성이 극대화되어 있다. 특히 가황 공정을 통해 고무 사슬 간의 가교가 형성돼 열과 압력에 강한 구조를 갖게 되는데, 이는 폐타이어의 화학적 재활용을 어렵게 만드는 주요 원인 중 하나다.
그동안 폐타이어의 재활용은 주로 열분해 방식이나 물리적 분쇄 재활용에 의존해 왔다. 열분해 방식은 350~800°C의 고온 환경에서 고분자 사슬을 분해해 연료유로 전환하는 기술이나, 높은 에너지 소비, 낮은 선택성, 그리고 저품질의 탄화수소 혼합물 생성이라는 한계가 명확히 존재한다.
연구팀은 이런 문제를 해결하고자 두 가지 촉매를 활용해 폐고무를 유용한 화학물질로 바꾸는 방법을 개발하였다. 첫 번째 촉매는 고무 분자 안의 결합 구조를 바꿔 분해가 잘 되도록 돕고, 두 번째 촉매는 고리를 닫는 반응을 통해 고리 모양의 화합물을 만들어낸다.
이 과정은 최대 92%의 높은 선택성과 82%의 수율을 보여준다. 만들어진 고리형 펜텐은 다시 고무로 재활용할 수 있고, 고리형 헥센은 나일론 섬유의 원료로 쓰이는 등 산업적으로 매우 가치가 높다.
연구팀은 개발한 시스템을 실제 폐기물로 버려진 폐타이어에 적용해, 고순도의 고리형 알켄으로 선택적 전환하는 데 성공했다. 이는 기존 열분해 방식과 달리 저온의 정밀 촉매 반응을 통해 고부가가치 화학 원료를 생산할 수 있다는 점에서 폐타이어 재활용 분야의 새로운 전환점으로 평가된다.
또한, 이번 기술은 다양한 종류의 합성고무와 폐고무에 폭넓게 적용될 수 있어, 자원 순환형 경제 실현에 기여할 수 있는 핵심 원천기술로 주목받고 있다.
홍순혁 교수는 “이번 연구는 폐타이어의 화학적 재활용에 대한 혁신적인 해법을 제시한 것이며, 경제성을 높이기 위해 차세대 고효율 촉매 개발, 상용화를 위한 기반을 마련해 나갈 예정이다”며, “기초화학을 통해 폐플라스틱 문제 해결에 기여하는 것이 목표”라고 밝혔다.
우리 대학 화학과 박범순, 조경일, 최경민 연구원이 참여한 이번 연구는 한국연구재단의 지원으로 수행됐으며, 국제 저명 학술지 ‘Chem’에 6월 18일 자로 온라인 게재됐다.
※논문명: Catalytic and Selective Chemical Recycling of Post-Consumer Rubbers into Cycloalkenes
※DOI: 10.1016/j.chempr.2025.102625
2025.06.26 조회수 1044 -
 21개 화학반응 동시 분석..AI 신약 개발 판 바꾼다
임산부의 입덧 완화 목적으로 사용됐던 약물인 탈리도마이드(Thalidomide)는 생체 내에서는 광학 이성질체*의 특성으로 한쪽 이성질체는 진정 효과를 나타내지만, 다른 쪽은 기형 유발이라는 심각한 부작용을 일으킨다. 이런 예처럼, 신약 개발에서는 원하는 광학 이성질체만을 선택적으로 합성하는 정밀 유기합성 기술이 중요하다. 하지만, 여러 반응물을 동시에 분석하는 것 자체가 어려웠던 기존 방식을 극복하고, 우리 연구진이 세계 최초로 21종의 반응물을 동시에 정밀 분석하는 기술을 개발해, AI와 로봇을 활용하는 신약 개발에 획기적인 기여가 기대된다.
*광학 이성질체: 동일한 화학식을 가지며 거울상 관계에 있으면서 서로 겹칠 수 없는 비대칭 구조로 존재하는 분자 쌍을 말한다. 이는 왼손과 오른손처럼 형태는 유사하지만 포개어지지 않는 관계와 유사하다.
우리 대학 화학과 김현우 교수 연구팀이 인공지능 기반 자율합성* 시대에 적합한 혁신적인 광학이성질체 분석 기술을 개발했다고 16일 밝혔다. 이번 연구는 다수의 반응물을 동시에 투입해 진행하는 비대칭 촉매 반응을 고해상도 불소 핵자기공명분광기(19F NMR)를 활용해 정밀 분석한 세계 최초의 기술로, 신약 개발 및 촉매 최적화 등 다양한 분야에 획기적인 기여가 기대된다.
* 인공지능 기반 자율합성: 인공지능(AI)을 활용해 화학 물질 합성 과정을 자동화하고 최적화하는 첨단 기술로, 미래 실험실의 자동화 및 지능형 연구 환경을 구현할 핵심 요소로 주목받고 있다. AI가 실험 조건을 예측·조절하고 결과를 해석해 후속 실험을 스스로 설계함으로써 반복 실험 수행 시 인간 개입을 최소화해 연구 효율성과 혁신성을 크게 높인다.
현재 자율합성 시스템은 반응 설계부터 수행까지는 자동화가 가능하지만, 반응 결과 분석은 전통적 장비를 활용한 개별 처리 방식에 의존하고 있어 속도 저하와 병목 현상이 발생하며 고속 반복 실험에는 적합하지 않다는 문제점이 제기돼 왔다.
또한, 1990년대에 제안된 다기질 동시 스크리닝 기법은 반응 분석의 효율을 극대화할 전략으로 주목받았지만, 기존 크로마토그래피 기반 분석법의 한계로 인해 적용 가능한 기질 수가 제한적이었다. 특히 원하는 광학 이성질체만 선택하여 합성하는 비대칭 합성 반응에서는 10종 이상의 기질을 동시에 분석하는 것이 불가능에 가까웠다.
이러한 한계를 극복하기 위해, 연구팀은 다수의 반응물을 하나의 반응 용기에 투입하여 동시에 비대칭 촉매 반응을 수행한 뒤 불소 작용기를 생성물에 도입하고, 자체 개발한 카이랄 코발트 시약을 적용해 모든 광학 이성질체를 명확하게 정량 분석할 수 있는 불소 핵자기공명분광기(19F NMR) 기반 다기질 동시 스크리닝 기술을 구현했다.
연구팀은 19F NMR의 우수한 분해능과 민감도를 활용해, 21종 기질의 비대칭 합성 반응을 단일 반응 용기에서 동시에 수행하고 생성물의 수율과 광학 이성질체 비율을 별도의 분리 과정 없이 정량 측정하는 데 성공했다.
김현우 교수는 “여러 기질을 한 반응기에 넣고 비대칭 합성 반응을 동시에 수행하는 것은 누구나 할 수 있지만, 생성물 전체를 정확하게 분석하는 것은 지금까지 풀기 어려운 과제였다”며, “세계 최고 수준의 다기질 스크리닝 분석 기술을 구현함으로써 AI 기반 자율합성 플랫폼의 분석 역량 향상에 크게 기여할 수 있을 것으로 기대된다”고 말했다.
이어 “이번 연구는 신약 개발에 필수적인 비대칭 촉매 반응의 효율성과 선택성을 신속히 검증할 수 있는 기술로, AI 기반 자율화 연구의 핵심 분석 도구로 활용될 전망이다”라고 밝혔다.
이번 연구에는 우리 대학 화학과 김동훈 석박통합과정 학생(제1 저자), 최경선 석박통합과정 학생(제2 저자) 가 참여했으며, 화학 분야 세계적 권위의 국제 학술지 미국화학회지(Journal of the American Chemical Society) 에 2025년 5월 27일 자 온라인 게재됐다.
※ 논문명: One-pot Multisubstrate Screening for Asymmetric Catalysis Enabled by 19F NMR-based Simultaneous Chiral Analysis
※ DOI: 10.1021/jacs.5c03446
이번 연구는 한국연구재단 중견연구자 지원사업, 비대칭 촉매반응 디자인센터, KAIST KC30 프로젝트의 지원을 받아 수행됐다.
2025.06.16 조회수 2462
21개 화학반응 동시 분석..AI 신약 개발 판 바꾼다
임산부의 입덧 완화 목적으로 사용됐던 약물인 탈리도마이드(Thalidomide)는 생체 내에서는 광학 이성질체*의 특성으로 한쪽 이성질체는 진정 효과를 나타내지만, 다른 쪽은 기형 유발이라는 심각한 부작용을 일으킨다. 이런 예처럼, 신약 개발에서는 원하는 광학 이성질체만을 선택적으로 합성하는 정밀 유기합성 기술이 중요하다. 하지만, 여러 반응물을 동시에 분석하는 것 자체가 어려웠던 기존 방식을 극복하고, 우리 연구진이 세계 최초로 21종의 반응물을 동시에 정밀 분석하는 기술을 개발해, AI와 로봇을 활용하는 신약 개발에 획기적인 기여가 기대된다.
*광학 이성질체: 동일한 화학식을 가지며 거울상 관계에 있으면서 서로 겹칠 수 없는 비대칭 구조로 존재하는 분자 쌍을 말한다. 이는 왼손과 오른손처럼 형태는 유사하지만 포개어지지 않는 관계와 유사하다.
우리 대학 화학과 김현우 교수 연구팀이 인공지능 기반 자율합성* 시대에 적합한 혁신적인 광학이성질체 분석 기술을 개발했다고 16일 밝혔다. 이번 연구는 다수의 반응물을 동시에 투입해 진행하는 비대칭 촉매 반응을 고해상도 불소 핵자기공명분광기(19F NMR)를 활용해 정밀 분석한 세계 최초의 기술로, 신약 개발 및 촉매 최적화 등 다양한 분야에 획기적인 기여가 기대된다.
* 인공지능 기반 자율합성: 인공지능(AI)을 활용해 화학 물질 합성 과정을 자동화하고 최적화하는 첨단 기술로, 미래 실험실의 자동화 및 지능형 연구 환경을 구현할 핵심 요소로 주목받고 있다. AI가 실험 조건을 예측·조절하고 결과를 해석해 후속 실험을 스스로 설계함으로써 반복 실험 수행 시 인간 개입을 최소화해 연구 효율성과 혁신성을 크게 높인다.
현재 자율합성 시스템은 반응 설계부터 수행까지는 자동화가 가능하지만, 반응 결과 분석은 전통적 장비를 활용한 개별 처리 방식에 의존하고 있어 속도 저하와 병목 현상이 발생하며 고속 반복 실험에는 적합하지 않다는 문제점이 제기돼 왔다.
또한, 1990년대에 제안된 다기질 동시 스크리닝 기법은 반응 분석의 효율을 극대화할 전략으로 주목받았지만, 기존 크로마토그래피 기반 분석법의 한계로 인해 적용 가능한 기질 수가 제한적이었다. 특히 원하는 광학 이성질체만 선택하여 합성하는 비대칭 합성 반응에서는 10종 이상의 기질을 동시에 분석하는 것이 불가능에 가까웠다.
이러한 한계를 극복하기 위해, 연구팀은 다수의 반응물을 하나의 반응 용기에 투입하여 동시에 비대칭 촉매 반응을 수행한 뒤 불소 작용기를 생성물에 도입하고, 자체 개발한 카이랄 코발트 시약을 적용해 모든 광학 이성질체를 명확하게 정량 분석할 수 있는 불소 핵자기공명분광기(19F NMR) 기반 다기질 동시 스크리닝 기술을 구현했다.
연구팀은 19F NMR의 우수한 분해능과 민감도를 활용해, 21종 기질의 비대칭 합성 반응을 단일 반응 용기에서 동시에 수행하고 생성물의 수율과 광학 이성질체 비율을 별도의 분리 과정 없이 정량 측정하는 데 성공했다.
김현우 교수는 “여러 기질을 한 반응기에 넣고 비대칭 합성 반응을 동시에 수행하는 것은 누구나 할 수 있지만, 생성물 전체를 정확하게 분석하는 것은 지금까지 풀기 어려운 과제였다”며, “세계 최고 수준의 다기질 스크리닝 분석 기술을 구현함으로써 AI 기반 자율합성 플랫폼의 분석 역량 향상에 크게 기여할 수 있을 것으로 기대된다”고 말했다.
이어 “이번 연구는 신약 개발에 필수적인 비대칭 촉매 반응의 효율성과 선택성을 신속히 검증할 수 있는 기술로, AI 기반 자율화 연구의 핵심 분석 도구로 활용될 전망이다”라고 밝혔다.
이번 연구에는 우리 대학 화학과 김동훈 석박통합과정 학생(제1 저자), 최경선 석박통합과정 학생(제2 저자) 가 참여했으며, 화학 분야 세계적 권위의 국제 학술지 미국화학회지(Journal of the American Chemical Society) 에 2025년 5월 27일 자 온라인 게재됐다.
※ 논문명: One-pot Multisubstrate Screening for Asymmetric Catalysis Enabled by 19F NMR-based Simultaneous Chiral Analysis
※ DOI: 10.1021/jacs.5c03446
이번 연구는 한국연구재단 중견연구자 지원사업, 비대칭 촉매반응 디자인센터, KAIST KC30 프로젝트의 지원을 받아 수행됐다.
2025.06.16 조회수 2462 -
 세계 최초 플라빈 빛 파장 설계 성공, 의료·환경 혁신
플라빈은 우리 몸 등 생명체 내의 에너지 생산과 생화학 반응에 관여하는 중요한 조효소이자 특정 색의 빛을 방출하는 형광 분자다. 하지만 자연계의 플라빈은 대부분 파란색에서 초록색 영역까지 짧은 파장의 빛을 낼 수 있어, 그보다 긴 파장인 적외선 영역까지는 확장되기 어렵다. KAIST 연구진이 기존 한계를 극복하고 플라빈이 내뿜는 형광 파장을 근적외선까지 확장하여 의료·환경·에너지 분야의 새로운 가능성을 제시했다.
우리 대학 화학과 백윤정 교수 연구팀은 근적외선 파장에서 발광이 가능한 5개의 고리 구조를 가진 새로운 오환형 플라빈 분자를 세계 최초로 개발하는 데 성공했다.
백윤정 교수 연구팀은 전통적으로 세 개의 고리를 갖는 플라빈 구조에서 플라빈의 핵심 구조를 5개의 고리로 확장하고, 여기에 산소 및 황 등 이종 원자를 정교하게 도입함으로써 분자의 전자 구조를 정밀하게 조절하는 새로운 합성 전략을 제시했다.
특히 이번에 개발된 분자는 적외선에 가까운 짙은 붉은색 및 근적외선 영역의 빛을 낼 수 있어, 기존 플라빈 색소가 낼 수 있었던 색의 범위를 획기적으로 확장했다는 평가를 받고 있다.
그 결과, 황이 포함된 구조체는 772 nm에 달하는 근적외선 영역에서 발광하며, 이는 지금까지 보고된 플라빈 유도체 중 가장 긴 파장이다. 또한 이 분자는 기존의 플라빈에서 드물게 관찰되던 준가역적인 산화 특성을 나타내어 전기화학적 기능성까지 동시에 갖춘 다기능성 분자 플랫폼으로 주목받고 있다.
연구팀은 분자의 구조를 미세하게 조절함으로써, 빛을 어떻게 흡수하고 방출할지를 원하는 대로 설계할 수 있게 되었고, 전기 신호를 전달하거나 변환하는 능력 또한 함께 제어할 수 있음을 입증했다.
이번 연구는 기존 플라빈의 한계를 뛰어넘어 빛의 파장을 바꿈으로서 활용 기술과 응용 범위를 넓힐 수 있다는 것을 보여줬다. 예를 들어, 근적외선(NIR) 같은 긴 파장의 빛을 통해 몸 속 더 깊이 정확하게 진단·치료하게 하며, 오염이나 독성물질이 특정 빛에 반응하도록 설계도 가능하며, 긴 파장의 빛을 흡수해서 친환경 에너지로 만들게 하는 등 발광 파장과 전자 특성을 정밀하게 제어하는 새로운 플랫폼을 제시하였다.
백윤정 교수는 “플라빈의 빛 파장을 바꿀 수 있다는 것은 우리가 원하는 상황에 맞게 빛을 자유롭게 설계하고 활용할 수 있다는 뜻으로, 앞으로 우리 손으로 원하는 색과 성질을 가진 분자를 정밀하게 디자인하고 만들수 있다는 가능성을 보여준 것”이라며, “이는 의료, 환경, 에너지 등 빛 기반 기술이 적용되는 수많은 분야에서 게임 체인저가 될 수 있는 기반 기술이 될 것”이라고 말했다.
해당 성과는 세계적인 국제 학술지 Nature사가 발행하는 `네이처 커뮤니케이션즈(Nature Communications)'에 4월 15일자로 게재되었다.
※ 논문명 : Expanding the Chemical Space of Flavins with Pentacyclic architecture
※ 저자 정보 : 서다영 (KAIST, 제1 저자), 권성연 (기초과학연구원, 공동 제2 저자), 윤가혜 (KAIST, 공동 제2 저자), 손태일 (KAIST, 공동 제2 저자), 원창현 (KAIST, 제3 저자), Neetu Singh (KAIST, 제4 저자), 김동욱 (기초과학연구원, 제5 저자) 및 백윤정 (KAIST, 교신저자) 포함 총 8 명 DOI: 10.1038/s41467-025-58957-2
한편, 이번 연구는 과기정통부가 지원하는 개인기초연구사업의‘우수신진연구’와 산업통상자원부가 지원하는‘소재부품개발사업’과제의 지원을 받아 수행됐다.
2025.04.23 조회수 3024
세계 최초 플라빈 빛 파장 설계 성공, 의료·환경 혁신
플라빈은 우리 몸 등 생명체 내의 에너지 생산과 생화학 반응에 관여하는 중요한 조효소이자 특정 색의 빛을 방출하는 형광 분자다. 하지만 자연계의 플라빈은 대부분 파란색에서 초록색 영역까지 짧은 파장의 빛을 낼 수 있어, 그보다 긴 파장인 적외선 영역까지는 확장되기 어렵다. KAIST 연구진이 기존 한계를 극복하고 플라빈이 내뿜는 형광 파장을 근적외선까지 확장하여 의료·환경·에너지 분야의 새로운 가능성을 제시했다.
우리 대학 화학과 백윤정 교수 연구팀은 근적외선 파장에서 발광이 가능한 5개의 고리 구조를 가진 새로운 오환형 플라빈 분자를 세계 최초로 개발하는 데 성공했다.
백윤정 교수 연구팀은 전통적으로 세 개의 고리를 갖는 플라빈 구조에서 플라빈의 핵심 구조를 5개의 고리로 확장하고, 여기에 산소 및 황 등 이종 원자를 정교하게 도입함으로써 분자의 전자 구조를 정밀하게 조절하는 새로운 합성 전략을 제시했다.
특히 이번에 개발된 분자는 적외선에 가까운 짙은 붉은색 및 근적외선 영역의 빛을 낼 수 있어, 기존 플라빈 색소가 낼 수 있었던 색의 범위를 획기적으로 확장했다는 평가를 받고 있다.
그 결과, 황이 포함된 구조체는 772 nm에 달하는 근적외선 영역에서 발광하며, 이는 지금까지 보고된 플라빈 유도체 중 가장 긴 파장이다. 또한 이 분자는 기존의 플라빈에서 드물게 관찰되던 준가역적인 산화 특성을 나타내어 전기화학적 기능성까지 동시에 갖춘 다기능성 분자 플랫폼으로 주목받고 있다.
연구팀은 분자의 구조를 미세하게 조절함으로써, 빛을 어떻게 흡수하고 방출할지를 원하는 대로 설계할 수 있게 되었고, 전기 신호를 전달하거나 변환하는 능력 또한 함께 제어할 수 있음을 입증했다.
이번 연구는 기존 플라빈의 한계를 뛰어넘어 빛의 파장을 바꿈으로서 활용 기술과 응용 범위를 넓힐 수 있다는 것을 보여줬다. 예를 들어, 근적외선(NIR) 같은 긴 파장의 빛을 통해 몸 속 더 깊이 정확하게 진단·치료하게 하며, 오염이나 독성물질이 특정 빛에 반응하도록 설계도 가능하며, 긴 파장의 빛을 흡수해서 친환경 에너지로 만들게 하는 등 발광 파장과 전자 특성을 정밀하게 제어하는 새로운 플랫폼을 제시하였다.
백윤정 교수는 “플라빈의 빛 파장을 바꿀 수 있다는 것은 우리가 원하는 상황에 맞게 빛을 자유롭게 설계하고 활용할 수 있다는 뜻으로, 앞으로 우리 손으로 원하는 색과 성질을 가진 분자를 정밀하게 디자인하고 만들수 있다는 가능성을 보여준 것”이라며, “이는 의료, 환경, 에너지 등 빛 기반 기술이 적용되는 수많은 분야에서 게임 체인저가 될 수 있는 기반 기술이 될 것”이라고 말했다.
해당 성과는 세계적인 국제 학술지 Nature사가 발행하는 `네이처 커뮤니케이션즈(Nature Communications)'에 4월 15일자로 게재되었다.
※ 논문명 : Expanding the Chemical Space of Flavins with Pentacyclic architecture
※ 저자 정보 : 서다영 (KAIST, 제1 저자), 권성연 (기초과학연구원, 공동 제2 저자), 윤가혜 (KAIST, 공동 제2 저자), 손태일 (KAIST, 공동 제2 저자), 원창현 (KAIST, 제3 저자), Neetu Singh (KAIST, 제4 저자), 김동욱 (기초과학연구원, 제5 저자) 및 백윤정 (KAIST, 교신저자) 포함 총 8 명 DOI: 10.1038/s41467-025-58957-2
한편, 이번 연구는 과기정통부가 지원하는 개인기초연구사업의‘우수신진연구’와 산업통상자원부가 지원하는‘소재부품개발사업’과제의 지원을 받아 수행됐다.
2025.04.23 조회수 3024 -
 고성능 촉매 개발, 반도체 핫전자 기술을 통해 해결하다
우리 대학 화학과 박정영 석좌교수, 신소재공학과 정연식 교수, 그리고 KIST 김동훈 박사 공동 연구팀이 반도체 기술을 활용하여 촉매 성능에 특정 변인이 미치는 영향을 정량적으로 분석할 수 있는 새로운 플랫폼을 성공적으로 구현했다. 이를 통해 대표적인 다경로 화학 반응인 메탄올 산화 반응에서 메틸 포르메이트 선택성을 크게 향상시켰으며, 이번 연구는 차세대 고성능 이종 촉매 개발을 앞당기는 데 기여할 것으로 기대된다고 1일 밝혔다.
다경로 화학 반응에서는 반응성과 선택성의 상충 관계로 인해 특정 생성물의 선택성을 높이는 것이 어려운 문제로 남아 있다. 특히, 메탄올 산화 반응에서는 이산화탄소와 더불어 고부가 가치 생성물인 메틸 포르메이트가 생성되므로, 메틸 포르메이트의 선택성을 극대화하는 것이 중요하다.
그러나 기존 불규칙적인 구조의 이종 촉매에서는 금속-산화물 계면 밀도를 비롯한 여러 변인이 동시에 촉매 성능에 영향을 미치기 때문에 특정 변수가 개별적으로 미치는 영향을 분석하는 것이 어렵다. 이에 KAIST-KIST 공동 연구팀은 균일하게 정렬된 금속산화물 나노 패턴을 구현할 수 있는 반도체 기술을 활용하여 이종 촉매 성능에 영향을 미칠 수 있는 다른 변인을 통제하고, 오로지 금속산화물의 물성만이 촉매 성능에 미치는 영향을 정량적으로 분석하였다. 구체적으로, 산소 공극 (Oxygen Vacancy)의 양을 조절하기 위해 다양한 환경에서 열처리한 세륨 산화물 (CeOx) 나노 패턴을 제작하고, 이를 백금(Pt) 박막 촉매 위에 전사하여 금속산화물의 산소 공극이 메틸 포르메이트 선택성에 미치는 영향을 분석했다.
연구 결과, 산소 공극이 가장 풍부하게 생성된 진공 환경에서 열처리한 CeOx-Pt 이종 촉매의 경우, 열처리를 하지 않은 CeO2-Pt 이종 촉매 대비 약 50% 향상된 메틸 포르메이트 선택성을 보였으며, 이는 반응 중 발생하는 핫 전자의 검출을 통해 실시간으로도 확인되었다. 또한, 연구팀은 양자역학 기반의 DFT 시뮬레이션을 통해 금속산화물 내부의 산소 공극이 이종 촉매의 성능에 미치는 영향을 이론적으로 규명하였다. 시뮬레이션 결과, 산소 공극은 금속/산화물 계면에 많은 양의 전자를 축적시키면서 반응 중간체 간 결합을 촉진하였고, 이로 인해 메틸 포르메이트 선택성이 향상됨을 확인하였다.
이에 대해 박정영 교수는 “이번에 개발한 반도체기반 플랫폼을 통해 핫전하와 촉매 선택성의 정량적 분석이 가능해짐에 따라 핫전하 기반의 광촉매 센서의 상용화 개발 및 핫전하 기반 광열촉매 시스템의 상용화 개발로 이어질 수 있다.”고 언급했다. 신소재공학과 정연식 교수는 “기존의 무작위 구조를 가진 촉매에서는 특정 변수의 영향을 정량적으로 분석하는 것이 어려웠으나, 반도체 기술을 활용한 이번 연구를 통해 보다 효율적인 이종 촉매 설계와 선택성 조절 전략을 제시할 수 있을 것으로 기대된다”고 밝혔다.
신소재공학과 이규락 박사, 화학과 송경재 박사, KIST 홍두선 박사가 공동 제 1 저자로 참여한 이번 연구는 국제학술지 ‘네이처 커뮤니케이션스 (Nature Communications)’에 3월 25일 자로 온라인 게재됐다. (논문 제목: Unraveling Oxygen Vacancy-Driven Catalytic Selectivity and Hot Electron Generation on Heterointerfaces using Nanostructured Platform)
이번 연구는 산업통상자원부 에너지혁신인재양성사업, 과학기술정보통신부 중견연구자지원사업, 그리고 과학기술정보통신부 국가전략기술소재개발사업 등의 지원을 받아 수행됐다.
2025.04.01 조회수 3883
고성능 촉매 개발, 반도체 핫전자 기술을 통해 해결하다
우리 대학 화학과 박정영 석좌교수, 신소재공학과 정연식 교수, 그리고 KIST 김동훈 박사 공동 연구팀이 반도체 기술을 활용하여 촉매 성능에 특정 변인이 미치는 영향을 정량적으로 분석할 수 있는 새로운 플랫폼을 성공적으로 구현했다. 이를 통해 대표적인 다경로 화학 반응인 메탄올 산화 반응에서 메틸 포르메이트 선택성을 크게 향상시켰으며, 이번 연구는 차세대 고성능 이종 촉매 개발을 앞당기는 데 기여할 것으로 기대된다고 1일 밝혔다.
다경로 화학 반응에서는 반응성과 선택성의 상충 관계로 인해 특정 생성물의 선택성을 높이는 것이 어려운 문제로 남아 있다. 특히, 메탄올 산화 반응에서는 이산화탄소와 더불어 고부가 가치 생성물인 메틸 포르메이트가 생성되므로, 메틸 포르메이트의 선택성을 극대화하는 것이 중요하다.
그러나 기존 불규칙적인 구조의 이종 촉매에서는 금속-산화물 계면 밀도를 비롯한 여러 변인이 동시에 촉매 성능에 영향을 미치기 때문에 특정 변수가 개별적으로 미치는 영향을 분석하는 것이 어렵다. 이에 KAIST-KIST 공동 연구팀은 균일하게 정렬된 금속산화물 나노 패턴을 구현할 수 있는 반도체 기술을 활용하여 이종 촉매 성능에 영향을 미칠 수 있는 다른 변인을 통제하고, 오로지 금속산화물의 물성만이 촉매 성능에 미치는 영향을 정량적으로 분석하였다. 구체적으로, 산소 공극 (Oxygen Vacancy)의 양을 조절하기 위해 다양한 환경에서 열처리한 세륨 산화물 (CeOx) 나노 패턴을 제작하고, 이를 백금(Pt) 박막 촉매 위에 전사하여 금속산화물의 산소 공극이 메틸 포르메이트 선택성에 미치는 영향을 분석했다.
연구 결과, 산소 공극이 가장 풍부하게 생성된 진공 환경에서 열처리한 CeOx-Pt 이종 촉매의 경우, 열처리를 하지 않은 CeO2-Pt 이종 촉매 대비 약 50% 향상된 메틸 포르메이트 선택성을 보였으며, 이는 반응 중 발생하는 핫 전자의 검출을 통해 실시간으로도 확인되었다. 또한, 연구팀은 양자역학 기반의 DFT 시뮬레이션을 통해 금속산화물 내부의 산소 공극이 이종 촉매의 성능에 미치는 영향을 이론적으로 규명하였다. 시뮬레이션 결과, 산소 공극은 금속/산화물 계면에 많은 양의 전자를 축적시키면서 반응 중간체 간 결합을 촉진하였고, 이로 인해 메틸 포르메이트 선택성이 향상됨을 확인하였다.
이에 대해 박정영 교수는 “이번에 개발한 반도체기반 플랫폼을 통해 핫전하와 촉매 선택성의 정량적 분석이 가능해짐에 따라 핫전하 기반의 광촉매 센서의 상용화 개발 및 핫전하 기반 광열촉매 시스템의 상용화 개발로 이어질 수 있다.”고 언급했다. 신소재공학과 정연식 교수는 “기존의 무작위 구조를 가진 촉매에서는 특정 변수의 영향을 정량적으로 분석하는 것이 어려웠으나, 반도체 기술을 활용한 이번 연구를 통해 보다 효율적인 이종 촉매 설계와 선택성 조절 전략을 제시할 수 있을 것으로 기대된다”고 밝혔다.
신소재공학과 이규락 박사, 화학과 송경재 박사, KIST 홍두선 박사가 공동 제 1 저자로 참여한 이번 연구는 국제학술지 ‘네이처 커뮤니케이션스 (Nature Communications)’에 3월 25일 자로 온라인 게재됐다. (논문 제목: Unraveling Oxygen Vacancy-Driven Catalytic Selectivity and Hot Electron Generation on Heterointerfaces using Nanostructured Platform)
이번 연구는 산업통상자원부 에너지혁신인재양성사업, 과학기술정보통신부 중견연구자지원사업, 그리고 과학기술정보통신부 국가전략기술소재개발사업 등의 지원을 받아 수행됐다.
2025.04.01 조회수 3883 -
 6밀리초에 단백질 반응 순간 포착 성공
생명현상을 이해하고 나아가 신약 개발을 위해 단백질 상호 작용 및 효소-기질 반응 등 마이크로초(micro-second)~밀리초(milli-second) 수준의 짧은 시간 동안 일어난 현상을 이해하는 것이 핵심이다. KAIST 연구진이 생명 현상을 이해하는데 필수적인 생화학 반응의 변화를 수 밀리초 수준에서 정지시키고 분석하는 방법을 개발했다.
우리 대학 화학과 강진영 교수와 물리학과 이원희 교수의 공동 연구팀이 초고속 생화학 반응 연구를 위한 ‘패릴렌(parylene)’* 기반 박막 미세유체 혼합-분사 장치’를 개발했다고 24일 밝혔다.
*패릴렌: 단백질 반응을 초고속으로 관찰하기 위한 미세유체(microfluidics) 장치를 만드는 핵심 재료로 수 마이크로미터의 얇은 박막형태로 스프레이 제작이 가능하게 만든 소재임
이번 연구는 기존에 제시됐던 시간 분해 초저온 전자현미경(이하 TRCEM, Time-resolved cryo-electron microscopy) 기법의 한계를 극복해 기존 대비 시료 소모량을 1/3 수준으로 줄이면서 분석가능한 최소 반응시간을 기존 기술 대비 수십 배 향상하여 6밀리초(1,000분의 6초)까지 단축했다.
시간 분해 초저온 전자현미경은 단백질 복합체의 반응 중간 상태를 초저온에서 빠르게 냉동해 구조를 분석하는 기술로 최근 특별히 많은 주목을 받고 있다.
통상적인 초저온 전자현미경 분석에서는 짧은시간 존재하고 사라지는 반응 중간체를 포착하기 어려웠다. 이를 해결하기 위해 다양한 TRCEM 기법이 개발됐으나, 기존 기술은 많은 시료 소비와 제한된 시간 해상도 등의 한계로 어려움이 있었다. 연구침은 이를 극복하기 위해 초박막 패릴렌 소재를 적용한 새로운 혼합-분사장치를 개발했다.
본 장치는 시료의 양을 기존 대비 1/3 수준으로 줄여 실질적인 연구의 어려움을 개선했으며, 미세유체역학 소자 내에서 반응 개시에 드는 시료 혼합 시간을 0.5밀리초로 줄여 전체 반응시간을 6밀리초까지 줄였다. 연구팀은 또한 소자의 일체형 설계를 통해 실험의 정밀도와 재현성을 향상했다.
강진영 교수는 “이번 연구는 TRCEM 기법을 더욱 실용적으로 만들었으며, 구조 생물학 및 신약 개발, 효소 반응연구, 바이오 센서 개발 등 다양한 생명과학 및 의약 분야에서 패럴린 박막 소자의 폭넓은 활용 가능성을 제시했다”고 연구의 의의를 설명했다.
이원희 교수는 “연구팀은 앞으로 이를 활용한 생화학 반응 연구와 더 빠른 반응 분석을 위한 성능 향상을 목표로 연구를 이어갈 계획이다”라고 밝혔다.
이번 연구 결과는 화학과 석·박통합과정 황혜랑 연구원이 제 1저자로 국제학술지 어드밴스드 펑셔널 머티리얼즈(Advanced Functional Materials) 2025년 1월 28일 자에 온라인 게재됐다. (논문명: Integrated Parylene-Based Thin-Film Microfluidic Device for Time-Resolved Cryo-Electron Microscopy, doi.org/10.1002/adfm.202418224).
한편 이번 연구는 한국연구재단과 삼성미래기술육성재단, CELINE 컨소시엄의 지원을 받아 수행됐다.
2025.03.24 조회수 3832
6밀리초에 단백질 반응 순간 포착 성공
생명현상을 이해하고 나아가 신약 개발을 위해 단백질 상호 작용 및 효소-기질 반응 등 마이크로초(micro-second)~밀리초(milli-second) 수준의 짧은 시간 동안 일어난 현상을 이해하는 것이 핵심이다. KAIST 연구진이 생명 현상을 이해하는데 필수적인 생화학 반응의 변화를 수 밀리초 수준에서 정지시키고 분석하는 방법을 개발했다.
우리 대학 화학과 강진영 교수와 물리학과 이원희 교수의 공동 연구팀이 초고속 생화학 반응 연구를 위한 ‘패릴렌(parylene)’* 기반 박막 미세유체 혼합-분사 장치’를 개발했다고 24일 밝혔다.
*패릴렌: 단백질 반응을 초고속으로 관찰하기 위한 미세유체(microfluidics) 장치를 만드는 핵심 재료로 수 마이크로미터의 얇은 박막형태로 스프레이 제작이 가능하게 만든 소재임
이번 연구는 기존에 제시됐던 시간 분해 초저온 전자현미경(이하 TRCEM, Time-resolved cryo-electron microscopy) 기법의 한계를 극복해 기존 대비 시료 소모량을 1/3 수준으로 줄이면서 분석가능한 최소 반응시간을 기존 기술 대비 수십 배 향상하여 6밀리초(1,000분의 6초)까지 단축했다.
시간 분해 초저온 전자현미경은 단백질 복합체의 반응 중간 상태를 초저온에서 빠르게 냉동해 구조를 분석하는 기술로 최근 특별히 많은 주목을 받고 있다.
통상적인 초저온 전자현미경 분석에서는 짧은시간 존재하고 사라지는 반응 중간체를 포착하기 어려웠다. 이를 해결하기 위해 다양한 TRCEM 기법이 개발됐으나, 기존 기술은 많은 시료 소비와 제한된 시간 해상도 등의 한계로 어려움이 있었다. 연구침은 이를 극복하기 위해 초박막 패릴렌 소재를 적용한 새로운 혼합-분사장치를 개발했다.
본 장치는 시료의 양을 기존 대비 1/3 수준으로 줄여 실질적인 연구의 어려움을 개선했으며, 미세유체역학 소자 내에서 반응 개시에 드는 시료 혼합 시간을 0.5밀리초로 줄여 전체 반응시간을 6밀리초까지 줄였다. 연구팀은 또한 소자의 일체형 설계를 통해 실험의 정밀도와 재현성을 향상했다.
강진영 교수는 “이번 연구는 TRCEM 기법을 더욱 실용적으로 만들었으며, 구조 생물학 및 신약 개발, 효소 반응연구, 바이오 센서 개발 등 다양한 생명과학 및 의약 분야에서 패럴린 박막 소자의 폭넓은 활용 가능성을 제시했다”고 연구의 의의를 설명했다.
이원희 교수는 “연구팀은 앞으로 이를 활용한 생화학 반응 연구와 더 빠른 반응 분석을 위한 성능 향상을 목표로 연구를 이어갈 계획이다”라고 밝혔다.
이번 연구 결과는 화학과 석·박통합과정 황혜랑 연구원이 제 1저자로 국제학술지 어드밴스드 펑셔널 머티리얼즈(Advanced Functional Materials) 2025년 1월 28일 자에 온라인 게재됐다. (논문명: Integrated Parylene-Based Thin-Film Microfluidic Device for Time-Resolved Cryo-Electron Microscopy, doi.org/10.1002/adfm.202418224).
한편 이번 연구는 한국연구재단과 삼성미래기술육성재단, CELINE 컨소시엄의 지원을 받아 수행됐다.
2025.03.24 조회수 3832 -
 빛을 전기로, 에너지전환 핵심, 핫홀을 잡다
빛이 금속 나노 구조체에 닿으면 순간적으로 생성되는 플라즈모닉 핫전하(plasmonic hot carrier)는 광에너지를 전기 및 화학에너지 같은 고부가가치 에너지원으로 변환하는 중요한 매개체이다. 이 중 핫홀(hot hole)은 광전기화학 반응에 효율을 증폭시키지만 피코초(1조분의 1초) 수준의 극초단 시간 내에 열적으로 소멸되어 실용적인 응용이 되기 어려웠다. 한국 연구진이 핫홀을 더 오래 유지하고 흐름을 증폭시키는 기술을 개발하면서 차세대 고효율 광에너지 전환 기술의 상용화를 앞당기는 성과를 거두었다.
우리 대학 화학과 박정영 석좌교수 연구팀은 인하대 신소재공학과 이문상 교수 연구팀과 공동연구를 통해, 핫홀(hot hole) 흐름을 증폭시키고 이를 실시간으로 국소 전류 분포 맵핑을 하여 광전류 향상 메커니즘을 성공적으로 규명했다고 12일 밝혔다.
연구팀은 금속 나노 그물망을 특수한 반도체 소재(p형 질화갈륨) 기판 위에 배치한 나노 다이오드 구조를 만들어 기판 표면이 핫홀 추출을 촉진하도록 설계했다. 그 결과, 핫홀 추출 방향과 동일한 질화갈륨 기판에서는 다른 방향의 질화갈륨 기판보다 핫홀의 흐름 증폭 효과가 약 2배 증가시키는 데 성공했다.
또한, 광전도성 원자힘 현미경(Photoconductive Atomic Force Microscopy, pc-AFM) 기반의 광전류 맵핑 시스템을 활용해 나노미터(머리카락 두께의 10만 분의 1) 수준에서 핫홀의 흐름을 실시간 분석했다. 핫홀의 흐름이 주로 금 나노 그물망에 빛이 국소적으로 집중되는 ‘핫스팟’ 에서 강하게 활성화되지만, 질화갈륨 기판의 성장방향을 바꿈에 따라 핫스팟 이외의 영역에서도 핫홀의 흐름이 활성화되는 현상을 확인했다.
이 연구를 통해 연구진은 빛을 전기 및 화학 에너지로 변환하는 효율적인 방법을 찾았으며, 이를 활용하면 차세대 태양전지, 광촉매, 수소 생산 기술 등이 크게 발전할 것으로 기대된다.
박정영 교수는 “나노 다이오드기법을 이용하여 핫홀의 흐름을 처음으로 제어할 수 있었고 이를 이용하여 다양한 광전소자 및 광촉매 응용에 혁신적인 기여를 할 수 있을 것이다. 예를 들면 태양광을 이용한 에너지 변환 기술(태양전지, 수소 생성 등)에 획기적인 발전을 기대할 수 있으며 실시간 분석 기술을 개발하여 초소형 광전소자(광센서, 나노 반도체 소자) 개발에 응용이 가능”하다고 말했다.
화학과 이현화 박사와 텍사스 오스틴 대학 화학공학과 박유진 박사후연구원이 제1 저자로, 인하대학교 신소재공학과 이문상 교수와 KAIST 화학과 박정영 교수가 공동 교신저자로 참여한 이번 연구성과는 국제학술지‘사이언스 어드밴시스(Science Advances)’에 3월 7일 자로 온라인 게재됐다.
(논문 제목: Reconfiguring hot-hole flux via polarity modulation of p-GaN in plasmonic Schottky architectures)
DOI : https://www.science.org/doi/10.1126/sciadv.adu0086
한편, 이 연구과제는 한국연구재단(NRF)의 지원을 받았다.
2025.03.12 조회수 3475
빛을 전기로, 에너지전환 핵심, 핫홀을 잡다
빛이 금속 나노 구조체에 닿으면 순간적으로 생성되는 플라즈모닉 핫전하(plasmonic hot carrier)는 광에너지를 전기 및 화학에너지 같은 고부가가치 에너지원으로 변환하는 중요한 매개체이다. 이 중 핫홀(hot hole)은 광전기화학 반응에 효율을 증폭시키지만 피코초(1조분의 1초) 수준의 극초단 시간 내에 열적으로 소멸되어 실용적인 응용이 되기 어려웠다. 한국 연구진이 핫홀을 더 오래 유지하고 흐름을 증폭시키는 기술을 개발하면서 차세대 고효율 광에너지 전환 기술의 상용화를 앞당기는 성과를 거두었다.
우리 대학 화학과 박정영 석좌교수 연구팀은 인하대 신소재공학과 이문상 교수 연구팀과 공동연구를 통해, 핫홀(hot hole) 흐름을 증폭시키고 이를 실시간으로 국소 전류 분포 맵핑을 하여 광전류 향상 메커니즘을 성공적으로 규명했다고 12일 밝혔다.
연구팀은 금속 나노 그물망을 특수한 반도체 소재(p형 질화갈륨) 기판 위에 배치한 나노 다이오드 구조를 만들어 기판 표면이 핫홀 추출을 촉진하도록 설계했다. 그 결과, 핫홀 추출 방향과 동일한 질화갈륨 기판에서는 다른 방향의 질화갈륨 기판보다 핫홀의 흐름 증폭 효과가 약 2배 증가시키는 데 성공했다.
또한, 광전도성 원자힘 현미경(Photoconductive Atomic Force Microscopy, pc-AFM) 기반의 광전류 맵핑 시스템을 활용해 나노미터(머리카락 두께의 10만 분의 1) 수준에서 핫홀의 흐름을 실시간 분석했다. 핫홀의 흐름이 주로 금 나노 그물망에 빛이 국소적으로 집중되는 ‘핫스팟’ 에서 강하게 활성화되지만, 질화갈륨 기판의 성장방향을 바꿈에 따라 핫스팟 이외의 영역에서도 핫홀의 흐름이 활성화되는 현상을 확인했다.
이 연구를 통해 연구진은 빛을 전기 및 화학 에너지로 변환하는 효율적인 방법을 찾았으며, 이를 활용하면 차세대 태양전지, 광촉매, 수소 생산 기술 등이 크게 발전할 것으로 기대된다.
박정영 교수는 “나노 다이오드기법을 이용하여 핫홀의 흐름을 처음으로 제어할 수 있었고 이를 이용하여 다양한 광전소자 및 광촉매 응용에 혁신적인 기여를 할 수 있을 것이다. 예를 들면 태양광을 이용한 에너지 변환 기술(태양전지, 수소 생성 등)에 획기적인 발전을 기대할 수 있으며 실시간 분석 기술을 개발하여 초소형 광전소자(광센서, 나노 반도체 소자) 개발에 응용이 가능”하다고 말했다.
화학과 이현화 박사와 텍사스 오스틴 대학 화학공학과 박유진 박사후연구원이 제1 저자로, 인하대학교 신소재공학과 이문상 교수와 KAIST 화학과 박정영 교수가 공동 교신저자로 참여한 이번 연구성과는 국제학술지‘사이언스 어드밴시스(Science Advances)’에 3월 7일 자로 온라인 게재됐다.
(논문 제목: Reconfiguring hot-hole flux via polarity modulation of p-GaN in plasmonic Schottky architectures)
DOI : https://www.science.org/doi/10.1126/sciadv.adu0086
한편, 이 연구과제는 한국연구재단(NRF)의 지원을 받았다.
2025.03.12 조회수 3475 -
 폴리페놀 코팅 기술로 탈모 예방 가능성 입증
탈모는 전 세계적으로 수억 명이 겪고 있는 문제로 심리적·사회적 영향을 크게 미치고 있다. KAIST 연구진이 천연 폴리페놀(polyphenol)의 일종인 탄닌산이 탈모 예방에 기여할 가능성에 주목하고 연구를 통해 탄닌산이 단순한 코팅제가 아니라, 탈모를 완화시키는 ‘접착 중재자(adhesion mediator)’ 역할을 한다는 점을 밝혀냈다.
우리 대학 화학과 이해신 교수 연구팀이 탄닌산 기반 코팅 기술을 활용해 탈모 완화 기능성 성분을 서서히 방출하는 새로운 탈모 예방 기술을 개발했다고 6일 밝혔다.
탈모에는 안드로겐 탈모증(androgenetic alopecia, AGA) 및 휴지기 탈모(telogen effluvium, TE)가 있는데 유전적, 호르몬적, 환경적 요인이 복합적으로 작용하며, 현재까지도 효과적이면서 부작용이 적은 치료법이 부족한 실정이다.
대표적인 탈모 치료제인 미녹시딜(minoxidil)과 피나스테라이드(finasteride) 는 일정 효과를 보이지만, 장기적인 사용이 필요하고, 체질에 따라 효능이 다르게 나타날 뿐만 아니라 일부 사용자는 부작용을 경험하기도 한다.
이해신 교수 연구팀은 탄닌산이 모발의 주요 단백질인 케라틴과 강하게 결합해 모발 표면에 지속적으로 부착될 수 있음을 입증했으며, 이를 활용해 특정 기능성 성분을 제어된 방식으로 방출할 수 있음을 확인했다.
특히 연구팀은 살리실산(salicylic acid, SCA), 니아신아마이드(niacinamide, N), 덱스판테놀(dexpanthenol, DAL) 등 탈모 완화 기능성 성분을 포함한 조합을 개발하고, 이를 ‘스캔달(SCANDAL)’이라 명명했다. 연구 결과, 탄닌산과 결합된 스캔달 복합체는 수분과 접촉하면 점진적으로 방출되며, 모발 표면을 따라 모낭으로 전달되는 것으로 나타났다.
굿모나의원(원장: 이건민) 연구팀은 탄닌산/스캔달 복합체가 포함된 샴푸를 12명의 탈모 환자에게 7일간 적용한 결과, 임상자 모두에게 유의미한 탈모 감소 효과가 관찰됐다. 실험 결과, 평균적으로 56.2%의 모발 탈락 감소 효과가 나타났으며, 최대 90.2%까지 탈모가 감소하는 사례도 확인됐다.
이는 탄닌산이 모발 표면에서 스캔달 성분을 안정적으로 유지하고, 서서히 방출되면서 모낭까지 전달되는 방식이 탈모 완화에 효과적일 수 있음을 시사한다.
이해신 교수는 “천연 폴리페놀(polyphenol)의 일종인 탄닌산은 강력한 항산화 효과를 가지며, 단백질과 강하게 결합하는 특성이 있어 생체 접착제(bioadhesive) 역할을 할 수 있다는 것을 입증하는데 성공했다.”고 말했다.
이어 이 교수는 “기존 연구에서도 피부 및 단백질 코팅 소재로 활용된 사례가 있지만, 이번 연구는 모발과의 결합 및 탈모 완화 성분 전달을 위한 최초 사례로 교원창업기업 폴리페놀팩토리(주)를 통해 제품화한 ‘그래비티 (Grabity)’샴푸에 적용하였다. 앞으로도 끊어지는 얇은 헤어의 강도를 획기적으로 늘리는 샴푸, 곱슬머리를 펴 주는 제품 등 더 다양한 연구 결과에 따른 제품화를 위해 노력하고 있다”고 강조했다.
화학과 김은우 박사과정이 제1 저자로, 이해신 교수가 교신저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 머티리얼 인터페이스Advanced Materials Interfaces’ 1월 6일 온라인판에 게재됐다. (논문명: Leveraging Multifaceted Polyphenol Interactions: An Approach for Hair Loss Mitigation) DOI: 10.1002/admi.202400851
한편 이번 연구는 KAIST 교원 창업 기업인 폴리페놀팩토리(주)의 지원을 받아 수행됐다.
2025.02.06 조회수 7499
폴리페놀 코팅 기술로 탈모 예방 가능성 입증
탈모는 전 세계적으로 수억 명이 겪고 있는 문제로 심리적·사회적 영향을 크게 미치고 있다. KAIST 연구진이 천연 폴리페놀(polyphenol)의 일종인 탄닌산이 탈모 예방에 기여할 가능성에 주목하고 연구를 통해 탄닌산이 단순한 코팅제가 아니라, 탈모를 완화시키는 ‘접착 중재자(adhesion mediator)’ 역할을 한다는 점을 밝혀냈다.
우리 대학 화학과 이해신 교수 연구팀이 탄닌산 기반 코팅 기술을 활용해 탈모 완화 기능성 성분을 서서히 방출하는 새로운 탈모 예방 기술을 개발했다고 6일 밝혔다.
탈모에는 안드로겐 탈모증(androgenetic alopecia, AGA) 및 휴지기 탈모(telogen effluvium, TE)가 있는데 유전적, 호르몬적, 환경적 요인이 복합적으로 작용하며, 현재까지도 효과적이면서 부작용이 적은 치료법이 부족한 실정이다.
대표적인 탈모 치료제인 미녹시딜(minoxidil)과 피나스테라이드(finasteride) 는 일정 효과를 보이지만, 장기적인 사용이 필요하고, 체질에 따라 효능이 다르게 나타날 뿐만 아니라 일부 사용자는 부작용을 경험하기도 한다.
이해신 교수 연구팀은 탄닌산이 모발의 주요 단백질인 케라틴과 강하게 결합해 모발 표면에 지속적으로 부착될 수 있음을 입증했으며, 이를 활용해 특정 기능성 성분을 제어된 방식으로 방출할 수 있음을 확인했다.
특히 연구팀은 살리실산(salicylic acid, SCA), 니아신아마이드(niacinamide, N), 덱스판테놀(dexpanthenol, DAL) 등 탈모 완화 기능성 성분을 포함한 조합을 개발하고, 이를 ‘스캔달(SCANDAL)’이라 명명했다. 연구 결과, 탄닌산과 결합된 스캔달 복합체는 수분과 접촉하면 점진적으로 방출되며, 모발 표면을 따라 모낭으로 전달되는 것으로 나타났다.
굿모나의원(원장: 이건민) 연구팀은 탄닌산/스캔달 복합체가 포함된 샴푸를 12명의 탈모 환자에게 7일간 적용한 결과, 임상자 모두에게 유의미한 탈모 감소 효과가 관찰됐다. 실험 결과, 평균적으로 56.2%의 모발 탈락 감소 효과가 나타났으며, 최대 90.2%까지 탈모가 감소하는 사례도 확인됐다.
이는 탄닌산이 모발 표면에서 스캔달 성분을 안정적으로 유지하고, 서서히 방출되면서 모낭까지 전달되는 방식이 탈모 완화에 효과적일 수 있음을 시사한다.
이해신 교수는 “천연 폴리페놀(polyphenol)의 일종인 탄닌산은 강력한 항산화 효과를 가지며, 단백질과 강하게 결합하는 특성이 있어 생체 접착제(bioadhesive) 역할을 할 수 있다는 것을 입증하는데 성공했다.”고 말했다.
이어 이 교수는 “기존 연구에서도 피부 및 단백질 코팅 소재로 활용된 사례가 있지만, 이번 연구는 모발과의 결합 및 탈모 완화 성분 전달을 위한 최초 사례로 교원창업기업 폴리페놀팩토리(주)를 통해 제품화한 ‘그래비티 (Grabity)’샴푸에 적용하였다. 앞으로도 끊어지는 얇은 헤어의 강도를 획기적으로 늘리는 샴푸, 곱슬머리를 펴 주는 제품 등 더 다양한 연구 결과에 따른 제품화를 위해 노력하고 있다”고 강조했다.
화학과 김은우 박사과정이 제1 저자로, 이해신 교수가 교신저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 머티리얼 인터페이스Advanced Materials Interfaces’ 1월 6일 온라인판에 게재됐다. (논문명: Leveraging Multifaceted Polyphenol Interactions: An Approach for Hair Loss Mitigation) DOI: 10.1002/admi.202400851
한편 이번 연구는 KAIST 교원 창업 기업인 폴리페놀팩토리(주)의 지원을 받아 수행됐다.
2025.02.06 조회수 7499 -
 펨토초보다 짧은 순간 전이상태 분자구조를 밝히다
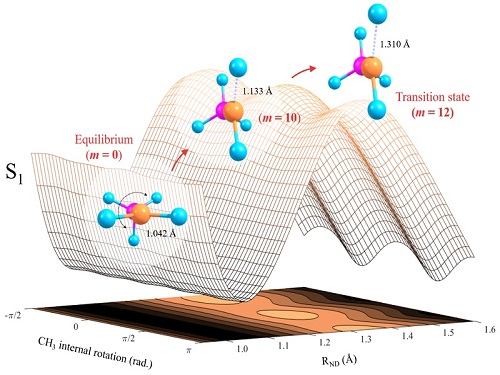
즈웨일 교수(1999년 노벨화학상)가 창출한 펨토화학을 통해 화학반응 중 일어나는 분자구조 변화를 실시간에서 관측할 수 있는 길이 열렸지만, 엄밀한 의미에서 에너지에 따른 전이상태 (Transition-State) 구조 변화를 직접 관측한 예는 매우 드물다. KAIST 연구진은, 광분해 화학반응 전이상태의 분자구조 변화를 분광학 기법*으로 정확하게 측정하는데 세계 최초로 성공했다.
*분광학 기법: 빛과 분자의 상호작용을 통해 양자역학적 분자구조를 정확하게 알아냄
우리 대학 화학과 김상규 교수 연구팀이 화학반응의 전이상태 (Transition-State) 구조를 실험적으로 밝히는 데 성공했다고 4일 밝혔다.
화학반응 속도론이 개발되면서, 가장 중요한 핵심으로 자리잡은 개념이 ‘전이상태 (Transition-State)’다. 전이상태 이론(Transition State Theory, 이하 TST) 에서는 반응물과 생성물 중간에 위치한 전이상태의 분자구조 및 동역학적 특성에 의해 반응속도, 생성물의 상대적 수율, 에너지 분포 등이 결정된다. TST는 지난 1세기 동안, 모든 환경에서의 연소, 유기, 생화학 반응 등에 널리 응용 되어온 가장 보편적인 반응속도론이다.
그러나, 전이상태는 펨토초(10-15 second)보다 더 짧은 시간 동안만 존재하므로, 전이상태를 직접 실험적으로 관찰하는 것은 매우 어려운 일이며 항상 도전적인 과제로 남아있었다.
김상규 교수 연구팀에서 관측한 전이상태는 특별한 의미를 갖는다. 분광학적 기법을 통해, 분자가 전이상태로 접근하면서 가지는 구조 변화를 매우 정확하게 측정할 수 있었던 첫 번째 예라는 점이다.
분광학 기법으로 측정된 정확한 전이상태 분자구조 변화에 따라 관찰된 반응속도의 급격한 변화를 통해서, 분자구조와 화학반응성 간 긴밀한 상관관계도 아울러 증명되었다.
김상규 교수는 “복잡한 분자의 화학반응에서 전이상태에 접근하면서 급격하게 변화하는 분자구조를 분광학 및 반응동역학 기법으로 밝힌 것은 처음이며, 향후 많은 이론 및 실험적 연구를 촉진할 것으로 기대된다. 특히, 전이상태 구조는 특정 화학반응을 선택적으로 빠르게 할 수 있는 고효율 촉매 설계에 가장 근원적인 정보를 제공할 것이다.”라고 말했다.
이번 연구 결과는 김정길 박사 (제 1 저자), 강민석 박사과정 학생, 윤준호 박사(現 LG화학)가 공동 저자로 2025년 1월 ‘네이처 커뮤니케이션즈(Nature Communications, Vol. 16, 210) 에 대표적(Featured) 연구 성과로 발표됐다.
또한 매우 이례적으로 분광학 분야 최고 권위자인 MIT의 로버트 필드(Robert Field) 교수 및 이스라엘 벤구리온 대학 바라밴 (Baraban) 교수가 공동작성한 하이라이트 커멘트(Nature Communications, 16, 76)를 통해, 이번 연구 결과가 가지는 독창성과 시사성, 중요성 및 향후 실험물리화학 분야에서의 임팩트가 강조됐다.
한편 이번 연구는 한국연구재단의 중견연구사업 및 기초과학 4.0 중점연구소 (자연과학연구소)에서 지원받아 수행됐다.
2025.02.04 조회수 4651
펨토초보다 짧은 순간 전이상태 분자구조를 밝히다
즈웨일 교수(1999년 노벨화학상)가 창출한 펨토화학을 통해 화학반응 중 일어나는 분자구조 변화를 실시간에서 관측할 수 있는 길이 열렸지만, 엄밀한 의미에서 에너지에 따른 전이상태 (Transition-State) 구조 변화를 직접 관측한 예는 매우 드물다. KAIST 연구진은, 광분해 화학반응 전이상태의 분자구조 변화를 분광학 기법*으로 정확하게 측정하는데 세계 최초로 성공했다.
*분광학 기법: 빛과 분자의 상호작용을 통해 양자역학적 분자구조를 정확하게 알아냄
우리 대학 화학과 김상규 교수 연구팀이 화학반응의 전이상태 (Transition-State) 구조를 실험적으로 밝히는 데 성공했다고 4일 밝혔다.
화학반응 속도론이 개발되면서, 가장 중요한 핵심으로 자리잡은 개념이 ‘전이상태 (Transition-State)’다. 전이상태 이론(Transition State Theory, 이하 TST) 에서는 반응물과 생성물 중간에 위치한 전이상태의 분자구조 및 동역학적 특성에 의해 반응속도, 생성물의 상대적 수율, 에너지 분포 등이 결정된다. TST는 지난 1세기 동안, 모든 환경에서의 연소, 유기, 생화학 반응 등에 널리 응용 되어온 가장 보편적인 반응속도론이다.
그러나, 전이상태는 펨토초(10-15 second)보다 더 짧은 시간 동안만 존재하므로, 전이상태를 직접 실험적으로 관찰하는 것은 매우 어려운 일이며 항상 도전적인 과제로 남아있었다.
김상규 교수 연구팀에서 관측한 전이상태는 특별한 의미를 갖는다. 분광학적 기법을 통해, 분자가 전이상태로 접근하면서 가지는 구조 변화를 매우 정확하게 측정할 수 있었던 첫 번째 예라는 점이다.
분광학 기법으로 측정된 정확한 전이상태 분자구조 변화에 따라 관찰된 반응속도의 급격한 변화를 통해서, 분자구조와 화학반응성 간 긴밀한 상관관계도 아울러 증명되었다.
김상규 교수는 “복잡한 분자의 화학반응에서 전이상태에 접근하면서 급격하게 변화하는 분자구조를 분광학 및 반응동역학 기법으로 밝힌 것은 처음이며, 향후 많은 이론 및 실험적 연구를 촉진할 것으로 기대된다. 특히, 전이상태 구조는 특정 화학반응을 선택적으로 빠르게 할 수 있는 고효율 촉매 설계에 가장 근원적인 정보를 제공할 것이다.”라고 말했다.
이번 연구 결과는 김정길 박사 (제 1 저자), 강민석 박사과정 학생, 윤준호 박사(現 LG화학)가 공동 저자로 2025년 1월 ‘네이처 커뮤니케이션즈(Nature Communications, Vol. 16, 210) 에 대표적(Featured) 연구 성과로 발표됐다.
또한 매우 이례적으로 분광학 분야 최고 권위자인 MIT의 로버트 필드(Robert Field) 교수 및 이스라엘 벤구리온 대학 바라밴 (Baraban) 교수가 공동작성한 하이라이트 커멘트(Nature Communications, 16, 76)를 통해, 이번 연구 결과가 가지는 독창성과 시사성, 중요성 및 향후 실험물리화학 분야에서의 임팩트가 강조됐다.
한편 이번 연구는 한국연구재단의 중견연구사업 및 기초과학 4.0 중점연구소 (자연과학연구소)에서 지원받아 수행됐다.
2025.02.04 조회수 4651 -
 버려지는 이산화탄소를 되살릴 수 있다면
세계적으로 기후 변화와 탄소 배출 문제의 심각성이 대두되면서 이산화탄소(CO2)를 화학 연료와 화합물 등의 자원으로 전환해서 활용하는 기술이 절실한 상황이다. 우리 대학 화학과 박정영 교수 연구팀이 한국재료연구원 나노재료연구본부 박다희 박사 연구팀과 공동연구를 통해 이산화탄소(CO2) 전환 효율을 크게 향상하는 촉매 기술을 개발했다.
기존의 이산화탄소(CO2) 전환 기술은 높은 에너지를 소비하는 것에 비해 효율은 낮아 상용화가 어렵다. 특히, 단원자 촉매(SACs)는 촉매 합성이 복잡하고, 금속 산화물 지지체(촉매 입자를 안정적으로 유지하거나 내구성을 높이는 역할)와 결합 안정성을 유지하기 어려워 촉매 성능이 떨어졌다.
이러한 한계를 극복하기 위해 연구팀은 단일 및 이중 단원자 촉매 기술을 개발하고 간단한 공정으로 촉매 효율을 높이는 기술을 선보였다. 본 성과는 이중 단원자 촉매(DSACs)로 금속 간 전자 상호작용을 적극 활용해 기존보다 50% 이상 높은 전환율과 우수한 선택성(촉매가 원하는 생성물을 많이 생성할 수 있도록 유도하는 능력)을 구현했다.
본 기술은 금속 산화물 지지체 내 산소 공공(Oxygen Vacancy)과 결함 구조를 정밀하게 제어해 이산화탄소(CO2) 전환 반응의 효율과 선택성을 획기적으로 높이는 촉매 설계 기술이다. 산소 공공이 촉매 표면에 이산화탄소가 잘 흡착되도록 돕고, 단원자 및 이중 단원자는 수소(H2)가 흡착되도록 돕는다. 산소 공공과 단원자 및 이중 단원자가 함께 작용하면서 이산화탄소(CO2)가 수소(H2)와 만나 원하는 화합물로 쉽게 전환되는 것이다. 특히, 이중 단원자 촉매(DSACs)는 두 금속 원자 간의 전자 상호작용을 적극 활용해 반응 경로를 조절하고 효율을 극대화했다.
연구팀은 에어로졸 분무 열분해법(Aerosol-Assisted Spray Pyrolysis)을 적용해 간단한 공정으로 촉매를 합성하고 대량 생산 가능성도 확보했다. 이는 복잡한 중간 과정 없이 액체 상태의 재료를 에어로졸(안개 같은 작은 입자)로 만든 후 뜨거운 챔버에 보내면 촉매가 완성되는 간단한 공정 방식이다. 해당 방식은 금속 산화물 지지체 내부에 금속 원자를 균일하게 분산시키고, 결함 구조를 정밀하게 조절할 수 있도록 돕는다. 이처럼 금속 산화물 지지체의 결함 구조를 정밀하게 제어함으로써 단일 및 이중 단원자 촉매를 안정적으로 형성하고 이중 단원자 촉매(DSACs)를 활용해 기존 단일 원자 촉매 사용량을 약 50% 줄이면서도 이산화탄소(CO2) 전환 효율을 기존 대비 약 두 배 이상 향상시키고, 99% 이상의 높은 선택성을 구현했다.
본 기술은 화학 연료 합성, 수소 생산, 청정에너지 산업 등 다양한 분야에 활용할 수 있다. 또한, 촉매 합성법(에어로졸 분무 열분해법)이 간단하고 생산 효율도 높아서 상용화될 가능성이 매우 크다.
연구책임자인 박다희 선임연구원은 "본 기술은 이산화탄소(CO2) 전환 촉매의 성능을 획기적으로 향상하는 동시에 간단한 공정을 통해 상용화를 가능하게 한 중요한 성과”라며, "탄소중립 실현을 위한 핵심 기술로 활용될 수 있을 것으로 기대된다.”라고 밝혔다. 또한 박정영 교수는 “본 연구는 새로운 종류의 단원자 촉매를 상대적으로 쉽게 합성할 수 있어 다양한 화학 반응에 쓰일 수 있고, 온실가스로 인한 지구온난화 문제 해결에 가장 시급한 연구 분야인 이산화탄소 분해/활용 촉매개발에 중요한 단초를 제공한다.”라고 언급했다.
본 연구는 한국재료연구원의 주요사업과 과학기술정보통신부, 산업통상자원부, 국가과학기술연구회의 지원을 받아 수행되었다. 연구 결과는 촉매 및 에너지 분야에서 권위 있는 저널인 어플라이드 카탈러시스 비: 인바이런멘탈 앤 에너지(Applied Catalysis B: Environmental and Energy(JCR 상위 1%, IF 20.3))에 온라인 게재됐다.
*논문(Applied Catalysis B: Environmental and Energy)
DOI 주소 https://doi.org/10.1016/j.apcatb.2024.124987
2025.01.23 조회수 4169
버려지는 이산화탄소를 되살릴 수 있다면
세계적으로 기후 변화와 탄소 배출 문제의 심각성이 대두되면서 이산화탄소(CO2)를 화학 연료와 화합물 등의 자원으로 전환해서 활용하는 기술이 절실한 상황이다. 우리 대학 화학과 박정영 교수 연구팀이 한국재료연구원 나노재료연구본부 박다희 박사 연구팀과 공동연구를 통해 이산화탄소(CO2) 전환 효율을 크게 향상하는 촉매 기술을 개발했다.
기존의 이산화탄소(CO2) 전환 기술은 높은 에너지를 소비하는 것에 비해 효율은 낮아 상용화가 어렵다. 특히, 단원자 촉매(SACs)는 촉매 합성이 복잡하고, 금속 산화물 지지체(촉매 입자를 안정적으로 유지하거나 내구성을 높이는 역할)와 결합 안정성을 유지하기 어려워 촉매 성능이 떨어졌다.
이러한 한계를 극복하기 위해 연구팀은 단일 및 이중 단원자 촉매 기술을 개발하고 간단한 공정으로 촉매 효율을 높이는 기술을 선보였다. 본 성과는 이중 단원자 촉매(DSACs)로 금속 간 전자 상호작용을 적극 활용해 기존보다 50% 이상 높은 전환율과 우수한 선택성(촉매가 원하는 생성물을 많이 생성할 수 있도록 유도하는 능력)을 구현했다.
본 기술은 금속 산화물 지지체 내 산소 공공(Oxygen Vacancy)과 결함 구조를 정밀하게 제어해 이산화탄소(CO2) 전환 반응의 효율과 선택성을 획기적으로 높이는 촉매 설계 기술이다. 산소 공공이 촉매 표면에 이산화탄소가 잘 흡착되도록 돕고, 단원자 및 이중 단원자는 수소(H2)가 흡착되도록 돕는다. 산소 공공과 단원자 및 이중 단원자가 함께 작용하면서 이산화탄소(CO2)가 수소(H2)와 만나 원하는 화합물로 쉽게 전환되는 것이다. 특히, 이중 단원자 촉매(DSACs)는 두 금속 원자 간의 전자 상호작용을 적극 활용해 반응 경로를 조절하고 효율을 극대화했다.
연구팀은 에어로졸 분무 열분해법(Aerosol-Assisted Spray Pyrolysis)을 적용해 간단한 공정으로 촉매를 합성하고 대량 생산 가능성도 확보했다. 이는 복잡한 중간 과정 없이 액체 상태의 재료를 에어로졸(안개 같은 작은 입자)로 만든 후 뜨거운 챔버에 보내면 촉매가 완성되는 간단한 공정 방식이다. 해당 방식은 금속 산화물 지지체 내부에 금속 원자를 균일하게 분산시키고, 결함 구조를 정밀하게 조절할 수 있도록 돕는다. 이처럼 금속 산화물 지지체의 결함 구조를 정밀하게 제어함으로써 단일 및 이중 단원자 촉매를 안정적으로 형성하고 이중 단원자 촉매(DSACs)를 활용해 기존 단일 원자 촉매 사용량을 약 50% 줄이면서도 이산화탄소(CO2) 전환 효율을 기존 대비 약 두 배 이상 향상시키고, 99% 이상의 높은 선택성을 구현했다.
본 기술은 화학 연료 합성, 수소 생산, 청정에너지 산업 등 다양한 분야에 활용할 수 있다. 또한, 촉매 합성법(에어로졸 분무 열분해법)이 간단하고 생산 효율도 높아서 상용화될 가능성이 매우 크다.
연구책임자인 박다희 선임연구원은 "본 기술은 이산화탄소(CO2) 전환 촉매의 성능을 획기적으로 향상하는 동시에 간단한 공정을 통해 상용화를 가능하게 한 중요한 성과”라며, "탄소중립 실현을 위한 핵심 기술로 활용될 수 있을 것으로 기대된다.”라고 밝혔다. 또한 박정영 교수는 “본 연구는 새로운 종류의 단원자 촉매를 상대적으로 쉽게 합성할 수 있어 다양한 화학 반응에 쓰일 수 있고, 온실가스로 인한 지구온난화 문제 해결에 가장 시급한 연구 분야인 이산화탄소 분해/활용 촉매개발에 중요한 단초를 제공한다.”라고 언급했다.
본 연구는 한국재료연구원의 주요사업과 과학기술정보통신부, 산업통상자원부, 국가과학기술연구회의 지원을 받아 수행되었다. 연구 결과는 촉매 및 에너지 분야에서 권위 있는 저널인 어플라이드 카탈러시스 비: 인바이런멘탈 앤 에너지(Applied Catalysis B: Environmental and Energy(JCR 상위 1%, IF 20.3))에 온라인 게재됐다.
*논문(Applied Catalysis B: Environmental and Energy)
DOI 주소 https://doi.org/10.1016/j.apcatb.2024.124987
2025.01.23 조회수 4169 -
 천연물 최초 합성으로부터 신개념 광스위치 개발
자연에서 일어나는 대부분의 화학 반응은 에너지적으로 안정한 형태를 취하는 방향으로 진행된다. 그렇기에 상대적으로 불안정한 구조를 가진 세큐린진 B의 합성은 매우 도전적인 과제다. 우리 연구진이 천연물 합성 원리를 바탕으로 빛으로 on/off가 가능한 분자 스위치 신소재 원천기술을 확보했다.
우리 대학 화학과 한순규 교수와 윤동기 교수 공동연구팀이 항암 및 퇴행성 뇌 질환 치료 효과로 학계의 꾸준한 관심을 받고있는 세큐리네가 알칼로이드 천연물 군에 속하는 세큐린진(securingine) B의 합성 방법을 세계 최초로 밝혀내고, 이 과정에서 발견한 화학적 반응성을 응용해 새로운 타입의 분자 광스위치를 개발했다고 11일 밝혔다.
한 교수 연구팀은 천연물 합성에 머무르지 않고 이 분자 재배열 원리를 바탕으로 서로 다른 파장의 빛을 통해 가역적으로 형태와 성질이 바뀌는 분자 광스위치를 고안했다.
천연물에 전자주개 치환기*를 달자 가시광선 영역의 빛을 흡수하면서, 무색인 기본 천연물과 달리 신물질은 노란색을 띠었다. 이렇게 새로 만든 천연물 유래 소재에 파란색 빛을 쬐었더니 수 초 뒤 색이 없어졌다. 빛에 의해 분자구조가 변형되면서 물질의 성질이 바뀌어 더 이상 색을 띄지 않게 된 것이다. 게다가 이 변형된 구조의 물질에 310나노미터(nm) 파장의 자외선을 쬐었더니 다시 구조가 원래대로 돌아오면서 노란색이 됐다.
*전자주개 치환기: 상대적으로 전자밀도가 풍부하여 전자가 부족한 시스템을 안정화시킬 수 있는 탄화수소의 모체 사슬 상의 한 개 이상의 수소 원자를 대체하는 원자 또는 원자단
한 교수 연구팀은 새로이 개발한 광 감응 물질을 고분자에도 적용했다. 연구팀은 PDMS(polydimethylsiloxane, 연성고분자의 일종) 고분자에 분자 광스위치 물질을 혼합하고 굳혀서 427 nm 파장의 파란색 가시광선을 쬐어쬐어주면 무색이 되고 310 nm 파장의 자외선을 쬐어주면 노란색으로 변하는 젤리 물질을 개발하였다.
연구팀은 새로 개발한 광스위치 소재를 광학재료 분야에 접목하고자 같은 학과 윤동기 교수 연구팀과 광 감응 카이랄* 혼입제 개발에 착수했다. 디스플레이 분야에 적용하기 위해 액정 물질에 파란색 빛을 쬐었을 때 카이랄 액정의 꼬임 주기가 변하면서 광스위치의 성질도 여전히 가지는 것을 관찰했다.
*카이랄: 왼손과 오른손처럼 서로 거울 쌍을 이루지만, 둘이 서로 겹쳐지지 않는 성질로 화학의 핵심 개념이자 물질의 광학적 특성을 결정하는 근본 요소 중 하나.
이번에 개발한 광스위치는 분자 내에서 결합이 이동해 분자구조가 바뀌는 혁신적인 작동 원리에 기반해 분자 광스위치 관련 분야 연구자의 눈길을 끌었다. 파장에 따른 색 변화뿐 아니라 형광의 on/off도 가능하기 때문에 형광 탐침자로써 생물학 분야에도 응용가능하다.
한 교수는 “이번 성과는 천연물 합성이라는 기초과학 연구 과정에서 발견한 원리를 다양하게 응용 가능한 새로운 분자 광스위치 개발로 연결한 사례”라며 “새로운 기술의 개발을 위해서는 자연현상의 작동 원리를 탐구하는 기초과학 연구가 굉장히 중요하다는 것을 다시 한번 일깨워준 계기가 되었다”라고 밝혔다.
화학과 박상빈 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 ‘셀 프레스(Cell Press)’에서 발간하는 국제 학술지 ‘켐(Chem)’에 10월 31일 字 게재됐다. (논문명: Synthesis of securingine B enables photoresponsive materials design)
이번 연구는 한국연구재단이 지원하는 선도연구센터인 KAIST 멀티스케일 카이랄 구조체 연구센터에(센터장: 이희승 교수) 속한 한순규-윤동기 교수 연구팀의 공동연구로 진행됐다.
이 밖에도 이번 연구는 한국연구재단의 개인기초연구사업과 KAIST의 도약연구(UP) 사업, KC30 사업, 그리고 초세대 협업연구실 프로젝트의 지원을 받아 수행됐다.
2024.11.11 조회수 4395
천연물 최초 합성으로부터 신개념 광스위치 개발
자연에서 일어나는 대부분의 화학 반응은 에너지적으로 안정한 형태를 취하는 방향으로 진행된다. 그렇기에 상대적으로 불안정한 구조를 가진 세큐린진 B의 합성은 매우 도전적인 과제다. 우리 연구진이 천연물 합성 원리를 바탕으로 빛으로 on/off가 가능한 분자 스위치 신소재 원천기술을 확보했다.
우리 대학 화학과 한순규 교수와 윤동기 교수 공동연구팀이 항암 및 퇴행성 뇌 질환 치료 효과로 학계의 꾸준한 관심을 받고있는 세큐리네가 알칼로이드 천연물 군에 속하는 세큐린진(securingine) B의 합성 방법을 세계 최초로 밝혀내고, 이 과정에서 발견한 화학적 반응성을 응용해 새로운 타입의 분자 광스위치를 개발했다고 11일 밝혔다.
한 교수 연구팀은 천연물 합성에 머무르지 않고 이 분자 재배열 원리를 바탕으로 서로 다른 파장의 빛을 통해 가역적으로 형태와 성질이 바뀌는 분자 광스위치를 고안했다.
천연물에 전자주개 치환기*를 달자 가시광선 영역의 빛을 흡수하면서, 무색인 기본 천연물과 달리 신물질은 노란색을 띠었다. 이렇게 새로 만든 천연물 유래 소재에 파란색 빛을 쬐었더니 수 초 뒤 색이 없어졌다. 빛에 의해 분자구조가 변형되면서 물질의 성질이 바뀌어 더 이상 색을 띄지 않게 된 것이다. 게다가 이 변형된 구조의 물질에 310나노미터(nm) 파장의 자외선을 쬐었더니 다시 구조가 원래대로 돌아오면서 노란색이 됐다.
*전자주개 치환기: 상대적으로 전자밀도가 풍부하여 전자가 부족한 시스템을 안정화시킬 수 있는 탄화수소의 모체 사슬 상의 한 개 이상의 수소 원자를 대체하는 원자 또는 원자단
한 교수 연구팀은 새로이 개발한 광 감응 물질을 고분자에도 적용했다. 연구팀은 PDMS(polydimethylsiloxane, 연성고분자의 일종) 고분자에 분자 광스위치 물질을 혼합하고 굳혀서 427 nm 파장의 파란색 가시광선을 쬐어쬐어주면 무색이 되고 310 nm 파장의 자외선을 쬐어주면 노란색으로 변하는 젤리 물질을 개발하였다.
연구팀은 새로 개발한 광스위치 소재를 광학재료 분야에 접목하고자 같은 학과 윤동기 교수 연구팀과 광 감응 카이랄* 혼입제 개발에 착수했다. 디스플레이 분야에 적용하기 위해 액정 물질에 파란색 빛을 쬐었을 때 카이랄 액정의 꼬임 주기가 변하면서 광스위치의 성질도 여전히 가지는 것을 관찰했다.
*카이랄: 왼손과 오른손처럼 서로 거울 쌍을 이루지만, 둘이 서로 겹쳐지지 않는 성질로 화학의 핵심 개념이자 물질의 광학적 특성을 결정하는 근본 요소 중 하나.
이번에 개발한 광스위치는 분자 내에서 결합이 이동해 분자구조가 바뀌는 혁신적인 작동 원리에 기반해 분자 광스위치 관련 분야 연구자의 눈길을 끌었다. 파장에 따른 색 변화뿐 아니라 형광의 on/off도 가능하기 때문에 형광 탐침자로써 생물학 분야에도 응용가능하다.
한 교수는 “이번 성과는 천연물 합성이라는 기초과학 연구 과정에서 발견한 원리를 다양하게 응용 가능한 새로운 분자 광스위치 개발로 연결한 사례”라며 “새로운 기술의 개발을 위해서는 자연현상의 작동 원리를 탐구하는 기초과학 연구가 굉장히 중요하다는 것을 다시 한번 일깨워준 계기가 되었다”라고 밝혔다.
화학과 박상빈 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 ‘셀 프레스(Cell Press)’에서 발간하는 국제 학술지 ‘켐(Chem)’에 10월 31일 字 게재됐다. (논문명: Synthesis of securingine B enables photoresponsive materials design)
이번 연구는 한국연구재단이 지원하는 선도연구센터인 KAIST 멀티스케일 카이랄 구조체 연구센터에(센터장: 이희승 교수) 속한 한순규-윤동기 교수 연구팀의 공동연구로 진행됐다.
이 밖에도 이번 연구는 한국연구재단의 개인기초연구사업과 KAIST의 도약연구(UP) 사업, KC30 사업, 그리고 초세대 협업연구실 프로젝트의 지원을 받아 수행됐다.
2024.11.11 조회수 4395 -
 인공지능 화학 학습으로 새로운 소재 개발 가능
새로운 물질을 설계하거나 물질의 물성을 예측하는 데 인공지능을 활용하기도 한다. 한미 공동 연구진이 기본 인공지능 모델보다 발전되어 화학 개념 학습을 하고 소재 예측, 새로운 물질 설계, 물질의 물성 예측에 더 높은 정확도를 제공하는 인공지능을 개발하는 데 성공했다.
우리 대학 화학과 이억균 명예교수와 김형준 교수 공동 연구팀이 창원대학교 생물학화학융합학부 김원준 교수, 미국 UC 머세드(Merced) 응용수학과의 김창호 교수 연구팀과 공동연구를 통해, 새로운 인공지능(AI) 기술인 ‘프로핏-넷(이하 PROFiT-Net)’을 개발하는 데 성공했다고 9일 밝혔다.
연구팀이 개발한 인공지능은 유전율, 밴드갭, 형성 에너지 등의 주요한 소재 물성 예측 정확도에 있어서 이번 기술은 기존 딥러닝 모델의 오차를 최소 10%, 최대 40% 줄일 수 있는 것으로 보여 주목받고 있다.
PROFiT-Net의 가장 큰 특징은 화학의 기본 개념을 학습해 예측 성능을 크게 높였다는 점이다. 최외각 전자 배치, 이온화 에너지, 전기 음성도와 같은 내용은 화학을 배울 때 가장 먼저 배우는 기본 개념 중 하나다.
기존 AI 모델과 달리, PROFiT-Net은 이러한 기본 화학적 속성과 이들 간의 상호작용을 직접적으로 학습함으로써 더욱 정밀한 예측을 할 수 있다. 이는 특히 새로운 물질을 설계하거나 물질의 물성을 예측하는 데 있어 더 높은 정확도를 제공하며, 화학 및 소재 과학 분야에서 크게 기여할 것으로 기대된다.
김형준 교수는 "AI 기술이 기초 화학 개념을 바탕으로 한층 더 발전할 수 있다는 가능성을 보여주었다ˮ고 말했으며 “추후 반도체 소재나 기능성 소재 개발과 같은 다양한 응용 분야에서 AI가 중요한 도구로 자리 잡을 수 있는 발판을 마련했다ˮ고 말했다.
이번 연구는 KAIST의 김세준 박사가 제1 저자로 참여하였고, 국제 학술지 `미국화학회지(Journal of the American Chemical Society)' 에 지난 9월 25일 字 게재됐다.
(논문명: PROFiT-Net: Property-networking deep learning model for materials, PROFiT-Net 링크: https://github.com/sejunkim6370/PROFiT-Net)
한편 이번 연구는 한국연구재단(NRF)의 나노·소재 기술개발(In-memory 컴퓨팅용 강유전체 개발을 위한 전주기 AI 기술)과 탑-티어 연구기관 간 협력 플랫폼 구축 및 공동연구 지원사업으로 진행됐다.
2024.10.10 조회수 8854
인공지능 화학 학습으로 새로운 소재 개발 가능
새로운 물질을 설계하거나 물질의 물성을 예측하는 데 인공지능을 활용하기도 한다. 한미 공동 연구진이 기본 인공지능 모델보다 발전되어 화학 개념 학습을 하고 소재 예측, 새로운 물질 설계, 물질의 물성 예측에 더 높은 정확도를 제공하는 인공지능을 개발하는 데 성공했다.
우리 대학 화학과 이억균 명예교수와 김형준 교수 공동 연구팀이 창원대학교 생물학화학융합학부 김원준 교수, 미국 UC 머세드(Merced) 응용수학과의 김창호 교수 연구팀과 공동연구를 통해, 새로운 인공지능(AI) 기술인 ‘프로핏-넷(이하 PROFiT-Net)’을 개발하는 데 성공했다고 9일 밝혔다.
연구팀이 개발한 인공지능은 유전율, 밴드갭, 형성 에너지 등의 주요한 소재 물성 예측 정확도에 있어서 이번 기술은 기존 딥러닝 모델의 오차를 최소 10%, 최대 40% 줄일 수 있는 것으로 보여 주목받고 있다.
PROFiT-Net의 가장 큰 특징은 화학의 기본 개념을 학습해 예측 성능을 크게 높였다는 점이다. 최외각 전자 배치, 이온화 에너지, 전기 음성도와 같은 내용은 화학을 배울 때 가장 먼저 배우는 기본 개념 중 하나다.
기존 AI 모델과 달리, PROFiT-Net은 이러한 기본 화학적 속성과 이들 간의 상호작용을 직접적으로 학습함으로써 더욱 정밀한 예측을 할 수 있다. 이는 특히 새로운 물질을 설계하거나 물질의 물성을 예측하는 데 있어 더 높은 정확도를 제공하며, 화학 및 소재 과학 분야에서 크게 기여할 것으로 기대된다.
김형준 교수는 "AI 기술이 기초 화학 개념을 바탕으로 한층 더 발전할 수 있다는 가능성을 보여주었다ˮ고 말했으며 “추후 반도체 소재나 기능성 소재 개발과 같은 다양한 응용 분야에서 AI가 중요한 도구로 자리 잡을 수 있는 발판을 마련했다ˮ고 말했다.
이번 연구는 KAIST의 김세준 박사가 제1 저자로 참여하였고, 국제 학술지 `미국화학회지(Journal of the American Chemical Society)' 에 지난 9월 25일 字 게재됐다.
(논문명: PROFiT-Net: Property-networking deep learning model for materials, PROFiT-Net 링크: https://github.com/sejunkim6370/PROFiT-Net)
한편 이번 연구는 한국연구재단(NRF)의 나노·소재 기술개발(In-memory 컴퓨팅용 강유전체 개발을 위한 전주기 AI 기술)과 탑-티어 연구기관 간 협력 플랫폼 구축 및 공동연구 지원사업으로 진행됐다.
2024.10.10 조회수 8854