%EB%B0%94%EC%9D%B4%EC%98%A4%EC%9D%98%EB%A3%8C%EA%B8%B0%EC%88%A0%EA%B0%9C%EB%B0%9C%EC%82%AC%EC%97%85
-
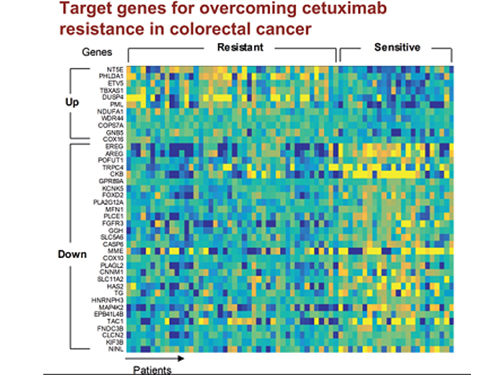 조광현 교수, 대장암 항암제 내성 극복할 병용 치료타겟 발굴
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암의 항암제 내성을 극복할 수 있는 새로운 병용치료 타겟을 발굴하는 데 성공했다.
연구팀은 암세포의 복잡한 생체데이터를 분자 네트워크 관점에서 분석하는 시스템생물학 접근법의 중요성을 제시했다. 이 방법을 통해 암세포가 가지는 약제 내성의 원리를 시스템 차원에서 파악하고, 새로운 약물 타겟을 체계적으로 발굴할 수 있을 것으로 기대된다.
박상민 박사과정, 황채영 박사 등이 참여한 이번 연구결과는 국제학술지 ‘유럽생화학회저널(FEBS Journal)’의 4월호 표지논문으로 게재됐다. (논문명 : Systems analysis identifies potential target genes to overcome cetuximab resistance in colorectal cancer cells)
암은 흔하게 발생하는 대표적인 난치병으로 특히 대장암은 전 세계적으로 환자 수가 100만 명을 넘어섰고, 국내의 경우 서구화된 식습관과 비만 등으로 인해 발병률 증가 속도가 10년간 가장 높게 나타났다. 최근 급격한 고령화에 따라 대장암 환자의 발생률 및 사망률이 가파르게 증가할 것으로 예상되고 있다.
최근 암세포의 특정 분자만을 표적으로 하는 표적항암제가 개발돼 부작용을 크게 줄이고 효과를 높일 수 있지만, 여전히 약물에 반응하는 환자가 매우 제한적이며 그나마 반응을 보이더라도 표적 항암치료 후 약물에 대한 내성이 생겨 암이 재발하는 문제를 안고 있다.
또한, 환자별로 항암제에 대한 반응이 매우 달라 환자의 암 조직 내 유전자 변이의 특징에 따라 적합한 치료를 선택하는 정밀의학의 필요성이 커지고 있다. 대장암 역시 약물의 효과를 예측할 수 있는 유전자 바이오마커의 여부에 따라 적합한 표적항암제를 처방하는 시도가 이뤄지고 있다.
FDA 승인을 받은 대표적인 대장암 치료제인 세툭시맙(cetuximab)의 경우 약물 반응성을 예측하는 바이오마커로 KRAS 유전자 돌연변이의 유무가 활용되고 있는데 이 유전자 돌연변이가 없는 환자에게 처방을 권고하고 있다.
그러나 KRAS 돌연변이가 없는 환자도 세툭시맙 반응률은 절반 정도에 불과하고 기존 항암 화학요법 단독시행과 비교해도 평균 5개월의 수명을 연장하는 데 그치고 있다. 오히려 KRAS 돌연변이가 있는 환자에게서 반응성이 있는 경우가 보고되고 있다.
따라서 KRAS 돌연변이 유무 이외의 새 바이오마커가 요구되고 있으며 KRAS 돌연변이가 존재해도 내성을 극복할 수 있는 병용치료 타겟의 발굴이 필요하다.
조 교수 연구팀은 유전체 데이터 분석, 수학 모델링, 컴퓨터 시뮬레이션 분석과 암 세포주 실험을 융합한 시스템생물학 연구를 통해 세툭시맙 반응성에 대한 바이오마커로 다섯 개의 새로운 유전자(DUSP4, ETV5, GNB5, NT5E, PHLDA1)를 찾아냈다.
그리고 대장암세포에서 각 유전자를 실험적으로 억제한 결과 KRAS 정상 세포에서 발생하는 세툭시맙 내성을 모두 극복할 수 있었다.
특히 GNB5를 억제하면 KRAS 돌연변이가 있는 세포주에서도 세툭시맙 처리에 따른 약물내성을 극복할 수 있음을 밝혔다. 따라서 GNB5의 억제를 통해 대장암 환자의 KRAS 돌연변이 유무와 관계없이 세툭시맙에 대한 내성을 극복할 수 있어 GNB5가 효과적인 병용치료 분자 타겟이 될 수 있음을 증명했다.
연구팀이 제시한 유전자를 바이오마커로 활용하면 세툭시맙에 잘 반응할 수 있는 민감 환자군을 미리 선별해 치료할 수 있는 정밀의학의 실현을 앞당길 수 있다.
또한, 발굴된 유전자들을 표적화하는 신약개발을 통해 내성을 가지는 환자군에 대해서도 새로운 치료전략을 제시할 수 있다. 특히 세툭시맙 치료 대상에서 제외됐던 KRAS 돌연변이가 있는 환자군에 대해서도 GNB5의 억제를 통해 치료 효과를 가져올 수 있을 것으로 기대된다.
조 교수는 “지금껏 GNB5 유전자 조절을 대장암의 조합치료에 활용한 예는 없었다”라며 “시스템생물학으로 암세포가 가지는 약제 내성의 원리를 밝히고, 내성 환자군에 대한 바이오마커 동정 및 내성 극복을 위한 병행치료 타겟 발굴을 통해 정밀의학을 실현할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유럽생화학회저널 4월 표지
2019.05.07 조회수 24758
조광현 교수, 대장암 항암제 내성 극복할 병용 치료타겟 발굴
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암의 항암제 내성을 극복할 수 있는 새로운 병용치료 타겟을 발굴하는 데 성공했다.
연구팀은 암세포의 복잡한 생체데이터를 분자 네트워크 관점에서 분석하는 시스템생물학 접근법의 중요성을 제시했다. 이 방법을 통해 암세포가 가지는 약제 내성의 원리를 시스템 차원에서 파악하고, 새로운 약물 타겟을 체계적으로 발굴할 수 있을 것으로 기대된다.
박상민 박사과정, 황채영 박사 등이 참여한 이번 연구결과는 국제학술지 ‘유럽생화학회저널(FEBS Journal)’의 4월호 표지논문으로 게재됐다. (논문명 : Systems analysis identifies potential target genes to overcome cetuximab resistance in colorectal cancer cells)
암은 흔하게 발생하는 대표적인 난치병으로 특히 대장암은 전 세계적으로 환자 수가 100만 명을 넘어섰고, 국내의 경우 서구화된 식습관과 비만 등으로 인해 발병률 증가 속도가 10년간 가장 높게 나타났다. 최근 급격한 고령화에 따라 대장암 환자의 발생률 및 사망률이 가파르게 증가할 것으로 예상되고 있다.
최근 암세포의 특정 분자만을 표적으로 하는 표적항암제가 개발돼 부작용을 크게 줄이고 효과를 높일 수 있지만, 여전히 약물에 반응하는 환자가 매우 제한적이며 그나마 반응을 보이더라도 표적 항암치료 후 약물에 대한 내성이 생겨 암이 재발하는 문제를 안고 있다.
또한, 환자별로 항암제에 대한 반응이 매우 달라 환자의 암 조직 내 유전자 변이의 특징에 따라 적합한 치료를 선택하는 정밀의학의 필요성이 커지고 있다. 대장암 역시 약물의 효과를 예측할 수 있는 유전자 바이오마커의 여부에 따라 적합한 표적항암제를 처방하는 시도가 이뤄지고 있다.
FDA 승인을 받은 대표적인 대장암 치료제인 세툭시맙(cetuximab)의 경우 약물 반응성을 예측하는 바이오마커로 KRAS 유전자 돌연변이의 유무가 활용되고 있는데 이 유전자 돌연변이가 없는 환자에게 처방을 권고하고 있다.
그러나 KRAS 돌연변이가 없는 환자도 세툭시맙 반응률은 절반 정도에 불과하고 기존 항암 화학요법 단독시행과 비교해도 평균 5개월의 수명을 연장하는 데 그치고 있다. 오히려 KRAS 돌연변이가 있는 환자에게서 반응성이 있는 경우가 보고되고 있다.
따라서 KRAS 돌연변이 유무 이외의 새 바이오마커가 요구되고 있으며 KRAS 돌연변이가 존재해도 내성을 극복할 수 있는 병용치료 타겟의 발굴이 필요하다.
조 교수 연구팀은 유전체 데이터 분석, 수학 모델링, 컴퓨터 시뮬레이션 분석과 암 세포주 실험을 융합한 시스템생물학 연구를 통해 세툭시맙 반응성에 대한 바이오마커로 다섯 개의 새로운 유전자(DUSP4, ETV5, GNB5, NT5E, PHLDA1)를 찾아냈다.
그리고 대장암세포에서 각 유전자를 실험적으로 억제한 결과 KRAS 정상 세포에서 발생하는 세툭시맙 내성을 모두 극복할 수 있었다.
특히 GNB5를 억제하면 KRAS 돌연변이가 있는 세포주에서도 세툭시맙 처리에 따른 약물내성을 극복할 수 있음을 밝혔다. 따라서 GNB5의 억제를 통해 대장암 환자의 KRAS 돌연변이 유무와 관계없이 세툭시맙에 대한 내성을 극복할 수 있어 GNB5가 효과적인 병용치료 분자 타겟이 될 수 있음을 증명했다.
연구팀이 제시한 유전자를 바이오마커로 활용하면 세툭시맙에 잘 반응할 수 있는 민감 환자군을 미리 선별해 치료할 수 있는 정밀의학의 실현을 앞당길 수 있다.
또한, 발굴된 유전자들을 표적화하는 신약개발을 통해 내성을 가지는 환자군에 대해서도 새로운 치료전략을 제시할 수 있다. 특히 세툭시맙 치료 대상에서 제외됐던 KRAS 돌연변이가 있는 환자군에 대해서도 GNB5의 억제를 통해 치료 효과를 가져올 수 있을 것으로 기대된다.
조 교수는 “지금껏 GNB5 유전자 조절을 대장암의 조합치료에 활용한 예는 없었다”라며 “시스템생물학으로 암세포가 가지는 약제 내성의 원리를 밝히고, 내성 환자군에 대한 바이오마커 동정 및 내성 극복을 위한 병행치료 타겟 발굴을 통해 정밀의학을 실현할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유럽생화학회저널 4월 표지
2019.05.07 조회수 24758 -
 조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 24213
조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 24213 -
 조광현 교수, 뇌파 생성, 변조 담당하는 신경회로 원리 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌파의 생성 및 변조를 담당하는 핵심 신경회로를 규명하는 데 성공했다.
이를 통해 뇌의 동작원리를 밝힐 뿐 아니라 향후 여러 뇌질환 환자에게서 발생하는 비정상적 뇌파활동을 신경세포 네트워크 수준에서 규명하는 데 활용 가능할 것으로 기대된다. 이번 연구는 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명했다는 의미를 갖는다.
이병욱 박사과정, 신동관 박사, 스티븐 그로스 박사가 함께 참여한 이번 연구는 국제 학술지 ‘셀 리포트(Cell Reports)’ 11월 6일자 온라인 판에 게재됐다.
뇌의 다양한 기능은 신경세포(뉴런) 사이의 복잡한 상호작용을 통해 이뤄진다. 특히 뉴런들의 동시다발적인 발화에 의해 형성되는 뇌파는 뇌의 활동 상태를 측정하는 가장 중요한 지표이며, 특정 기능을 수행하기 위해 영역 간 선택적 통신의 매개체 역할을 하는 것으로 알려져 있다.
또한 뇌파의 비정상적인 생성 및 변조 현상은 다양한 뇌질환과 밀접한 관계를 갖는 것으로 밝혀지고 있다. 이에 따라 전 세계 신경생물학 연구자들은 뇌파의 생성 및 변조 원리를 파악하기 위해 노력해 왔다.
그러나 뇌파의 생성 및 변조는 수많은 뉴런 사이의 복잡한 상호작용을 통해 발생하는 예측할 수 없는 창발적 특성(emergent property)을 갖기 때문에 기존의 신경 생물학 실험을 통해 그 원리를 규명하기에는 한계가 있었다.
조 교수 연구팀은 시스템생물학 기반의 연구방법을 통해 뇌파의 생성 및 변조 원리를 분석했다. 연구팀은 여러 뇌 영역 중 특히 감각 피질(sensory cortex)에 주목했다. 감각 피질은 외부 감각 정보를 처리하고 통합, 조절하는 핵심 영역으로 여러 주파수 대역의 뇌파와 변조를 관측할 수 있다.
연구팀은 최근 커넥토믹스 (connectomics) 연구를 통해 밝혀진 쥐의 감각피질 내 뉴런의 종류 및 뉴런 간 연결성 정보를 이용해 감각피질을 구성하는 뉴런들과 이들을 연결하는 시냅스를 수학 모델을 통해 표현하고 이로부터 신경회로를 구축해 뇌파의 생성 및 변조 과정을 분석했다.
연구팀은 대규모 컴퓨터 시뮬레이션 분석을 통해 흥분성 뉴런과 억제성 뉴런으로 구성된 양성피드백과 음성피드백의 중첩된 구조(interlinked positive and negative feedback)가 뇌파의 생성 및 주파수 변조 현상의 핵심회로임을 최초로 규명했다.
특히 연구팀은 기존의 전기생리학 실험을 통해 측정된 뉴런 간 시냅스의 특정 연결강도가 신경회로의 뇌파 생성 및 변조 기능을 극대화시킬 수 있는 최적의 조합임을 밝혀냈다.
이번에 개발한 수학모형을 활용하면 전통적 생물학 실험을 통해 파악이 어려웠던 뉴런들 간의 다양한 상호작용을 이해하고 신경회로의 복잡한 설계원리를 파악할 수 있을 것으로 기대된다.
또한 여러 뇌질환 환자의 뇌에서 관측되는 비정상적인 뇌파 활동을 신경네트워크 차원에서 분석하고 규명할 수 있을 것으로 예상된다.
시스템생물학 접근을 통한 신경회로의 구조 및 기능 분석은 인공지능의 발전에도 기여할 것으로 기대된다. 두뇌 신경회로의 작동원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다. 자폐증이나 집중력 조절장애 등과 관련된 신경회로 규명, 두뇌 치료 기술 개발 등의 원천 의료기술 개발에도 혁신으로 이어질 수 있다.
조 교수는 “지금껏 뇌파의 생성 및 변조를 담당하는 핵심 신경회로가 밝혀진 바가 없었다”며 “이번 연구에서는 최근 커넥토믹스 (connectomcis) 연구를 통해 점차 밝혀지고 있는 뉴런간의 복잡한 연결성에 숨겨진 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작원리를 파악할 수 있는 새로운 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, 그리고 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뉴런 간 연결 강도에 내제된 기능적 설계원리 파악
그림2. 뇌파의 생성 및 변조를 담당하는 핵심 신경회로
2018.11.14 조회수 21104
조광현 교수, 뇌파 생성, 변조 담당하는 신경회로 원리 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌파의 생성 및 변조를 담당하는 핵심 신경회로를 규명하는 데 성공했다.
이를 통해 뇌의 동작원리를 밝힐 뿐 아니라 향후 여러 뇌질환 환자에게서 발생하는 비정상적 뇌파활동을 신경세포 네트워크 수준에서 규명하는 데 활용 가능할 것으로 기대된다. 이번 연구는 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명했다는 의미를 갖는다.
이병욱 박사과정, 신동관 박사, 스티븐 그로스 박사가 함께 참여한 이번 연구는 국제 학술지 ‘셀 리포트(Cell Reports)’ 11월 6일자 온라인 판에 게재됐다.
뇌의 다양한 기능은 신경세포(뉴런) 사이의 복잡한 상호작용을 통해 이뤄진다. 특히 뉴런들의 동시다발적인 발화에 의해 형성되는 뇌파는 뇌의 활동 상태를 측정하는 가장 중요한 지표이며, 특정 기능을 수행하기 위해 영역 간 선택적 통신의 매개체 역할을 하는 것으로 알려져 있다.
또한 뇌파의 비정상적인 생성 및 변조 현상은 다양한 뇌질환과 밀접한 관계를 갖는 것으로 밝혀지고 있다. 이에 따라 전 세계 신경생물학 연구자들은 뇌파의 생성 및 변조 원리를 파악하기 위해 노력해 왔다.
그러나 뇌파의 생성 및 변조는 수많은 뉴런 사이의 복잡한 상호작용을 통해 발생하는 예측할 수 없는 창발적 특성(emergent property)을 갖기 때문에 기존의 신경 생물학 실험을 통해 그 원리를 규명하기에는 한계가 있었다.
조 교수 연구팀은 시스템생물학 기반의 연구방법을 통해 뇌파의 생성 및 변조 원리를 분석했다. 연구팀은 여러 뇌 영역 중 특히 감각 피질(sensory cortex)에 주목했다. 감각 피질은 외부 감각 정보를 처리하고 통합, 조절하는 핵심 영역으로 여러 주파수 대역의 뇌파와 변조를 관측할 수 있다.
연구팀은 최근 커넥토믹스 (connectomics) 연구를 통해 밝혀진 쥐의 감각피질 내 뉴런의 종류 및 뉴런 간 연결성 정보를 이용해 감각피질을 구성하는 뉴런들과 이들을 연결하는 시냅스를 수학 모델을 통해 표현하고 이로부터 신경회로를 구축해 뇌파의 생성 및 변조 과정을 분석했다.
연구팀은 대규모 컴퓨터 시뮬레이션 분석을 통해 흥분성 뉴런과 억제성 뉴런으로 구성된 양성피드백과 음성피드백의 중첩된 구조(interlinked positive and negative feedback)가 뇌파의 생성 및 주파수 변조 현상의 핵심회로임을 최초로 규명했다.
특히 연구팀은 기존의 전기생리학 실험을 통해 측정된 뉴런 간 시냅스의 특정 연결강도가 신경회로의 뇌파 생성 및 변조 기능을 극대화시킬 수 있는 최적의 조합임을 밝혀냈다.
이번에 개발한 수학모형을 활용하면 전통적 생물학 실험을 통해 파악이 어려웠던 뉴런들 간의 다양한 상호작용을 이해하고 신경회로의 복잡한 설계원리를 파악할 수 있을 것으로 기대된다.
또한 여러 뇌질환 환자의 뇌에서 관측되는 비정상적인 뇌파 활동을 신경네트워크 차원에서 분석하고 규명할 수 있을 것으로 예상된다.
시스템생물학 접근을 통한 신경회로의 구조 및 기능 분석은 인공지능의 발전에도 기여할 것으로 기대된다. 두뇌 신경회로의 작동원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다. 자폐증이나 집중력 조절장애 등과 관련된 신경회로 규명, 두뇌 치료 기술 개발 등의 원천 의료기술 개발에도 혁신으로 이어질 수 있다.
조 교수는 “지금껏 뇌파의 생성 및 변조를 담당하는 핵심 신경회로가 밝혀진 바가 없었다”며 “이번 연구에서는 최근 커넥토믹스 (connectomcis) 연구를 통해 점차 밝혀지고 있는 뉴런간의 복잡한 연결성에 숨겨진 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작원리를 파악할 수 있는 새로운 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업, 그리고 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뉴런 간 연결 강도에 내제된 기능적 설계원리 파악
그림2. 뇌파의 생성 및 변조를 담당하는 핵심 신경회로
2018.11.14 조회수 21104 -
 김준 교수, 난치성 유전질환인 섬모병증 치료제 후보 발굴
〈 김준 교수, 김용준 박사과정 〉
우리 대학 의과학대학원 김준 교수가 연세대학교 생명공학과 권호정 교수 연구팀과의 공동 연구를 통해 난치성 유전질환인 섬모병증의 치료제 후보를 개발했다.
이번 연구 결과는 섬모병증 치료제 개발을 위한 기반이 될 것으로 기대되며 유사한 난치성 유전질환에 대한 저분자 화합물 약물 개발 플랫폼으로도 활용 가능할 것으로 예상된다.
김용준 박사과정이 1저자로 참여하고 정인지, 김성수, 정유주 연구원이 공동 저자로 참여한 이번 연구는 의, 과학 분야 국제 학술지 ‘저널 오브 클리니컬 인베스티게이션(Journal of Clinical Investigation)’ 7월 23일자 온라인 판에 게재됐다.(논문명 Eupatilin rescues ciliary transition zone defects to ameliorate ciliopathy-related phenotypes)
세포 소기관인 일차섬모는 배아가 발생하는 과정에서 세포 간 신호전달에 관여하고 망막 광수용체 세포가 기능하는 역할을 하는 등 인체에 중요한 기관이다.
섬모병증은 이러한 섬모의 형성에 필수적인 유전자들의 돌연변이로 인해 발생되며 소뇌발달 및 신장 이상, 망막 퇴행 등의 증상을 보인다.
현재 섬모병증을 치료하는 약물은 개발되지 않았다. 섬모병증 뿐 아니라 기능손실 유전자 돌연변이가 원인이 되는 대부분의 희귀유전질환은 유전자 치료를 제외하고는 치료 약물의 개발이 이뤄지지 않았다.
연구팀은 문제 해결을 위해 섬모병증 원인의 하나인 CEP290 유전자 돌연변이를 유전자 편집기법으로 모사한 세포를 구축한 뒤 화합물 라이브러리 스크리닝 기법을 통해 섬모병증에서 나타나는 섬모형성 부진 현상을 극복할 수 있는 천연 저분자 화합물을 발굴했다.
발굴된 화합물은 CEP290 단백질과 복합체를 이뤄 섬모형성과 기능에 관여하는 단백질(NPHP5)에 작용하는 것으로 밝혀졌다. CEP290 단백질이 유전자 돌연변이로 인해 만들어지지 않는 경우 NPHP5 단백질도 정상적으로 작용하지 못하는데 이 화합물은 NPHP5의 기능을 정상화시켜 복합체가 담당하던 기능의 일부를 회복함을 확인했다.
또한 연구팀은 발굴한 화합물을 섬모병증 증상을 갖는 동물 모델에 주입했고 망막 퇴행 현상을 지연시키는 효과를 입증했다.
1저자인 김용준 박사과정은 “이번 연구는 기능손실 유전자 돌연변이로 인해 발생하는 유전질환도 저분자 화합물 약물로 치료가 가능함을 규명했다는 의미를 갖는다”고 말했다.
김준 교수는 “발굴된 후보약물의 효과를 동물실험을 통해 확인했기 때문에 인체에서의 효과 또한 증명하는 후속 연구를 진행할 예정이다”고 말했다.
이번 연구는 보건복지부 희귀질환연구센터지원사업, 한국연구재단 바이오의료기술개발사업, 글로벌연구실 사업의 지원으로 수행됐다.
□ 그림 설명
그림1.섬모형성 이상을 회복시키는 약물 발굴
그림2. 발굴된 약물에 의해 섬모병증 모델 생쥐의 망막퇴행이 지연되는 효과 확인
2018.07.30 조회수 15754
김준 교수, 난치성 유전질환인 섬모병증 치료제 후보 발굴
〈 김준 교수, 김용준 박사과정 〉
우리 대학 의과학대학원 김준 교수가 연세대학교 생명공학과 권호정 교수 연구팀과의 공동 연구를 통해 난치성 유전질환인 섬모병증의 치료제 후보를 개발했다.
이번 연구 결과는 섬모병증 치료제 개발을 위한 기반이 될 것으로 기대되며 유사한 난치성 유전질환에 대한 저분자 화합물 약물 개발 플랫폼으로도 활용 가능할 것으로 예상된다.
김용준 박사과정이 1저자로 참여하고 정인지, 김성수, 정유주 연구원이 공동 저자로 참여한 이번 연구는 의, 과학 분야 국제 학술지 ‘저널 오브 클리니컬 인베스티게이션(Journal of Clinical Investigation)’ 7월 23일자 온라인 판에 게재됐다.(논문명 Eupatilin rescues ciliary transition zone defects to ameliorate ciliopathy-related phenotypes)
세포 소기관인 일차섬모는 배아가 발생하는 과정에서 세포 간 신호전달에 관여하고 망막 광수용체 세포가 기능하는 역할을 하는 등 인체에 중요한 기관이다.
섬모병증은 이러한 섬모의 형성에 필수적인 유전자들의 돌연변이로 인해 발생되며 소뇌발달 및 신장 이상, 망막 퇴행 등의 증상을 보인다.
현재 섬모병증을 치료하는 약물은 개발되지 않았다. 섬모병증 뿐 아니라 기능손실 유전자 돌연변이가 원인이 되는 대부분의 희귀유전질환은 유전자 치료를 제외하고는 치료 약물의 개발이 이뤄지지 않았다.
연구팀은 문제 해결을 위해 섬모병증 원인의 하나인 CEP290 유전자 돌연변이를 유전자 편집기법으로 모사한 세포를 구축한 뒤 화합물 라이브러리 스크리닝 기법을 통해 섬모병증에서 나타나는 섬모형성 부진 현상을 극복할 수 있는 천연 저분자 화합물을 발굴했다.
발굴된 화합물은 CEP290 단백질과 복합체를 이뤄 섬모형성과 기능에 관여하는 단백질(NPHP5)에 작용하는 것으로 밝혀졌다. CEP290 단백질이 유전자 돌연변이로 인해 만들어지지 않는 경우 NPHP5 단백질도 정상적으로 작용하지 못하는데 이 화합물은 NPHP5의 기능을 정상화시켜 복합체가 담당하던 기능의 일부를 회복함을 확인했다.
또한 연구팀은 발굴한 화합물을 섬모병증 증상을 갖는 동물 모델에 주입했고 망막 퇴행 현상을 지연시키는 효과를 입증했다.
1저자인 김용준 박사과정은 “이번 연구는 기능손실 유전자 돌연변이로 인해 발생하는 유전질환도 저분자 화합물 약물로 치료가 가능함을 규명했다는 의미를 갖는다”고 말했다.
김준 교수는 “발굴된 후보약물의 효과를 동물실험을 통해 확인했기 때문에 인체에서의 효과 또한 증명하는 후속 연구를 진행할 예정이다”고 말했다.
이번 연구는 보건복지부 희귀질환연구센터지원사업, 한국연구재단 바이오의료기술개발사업, 글로벌연구실 사업의 지원으로 수행됐다.
□ 그림 설명
그림1.섬모형성 이상을 회복시키는 약물 발굴
그림2. 발굴된 약물에 의해 섬모병증 모델 생쥐의 망막퇴행이 지연되는 효과 확인
2018.07.30 조회수 15754 -
 전상용 교수, 건선,아토피 치료용 펩타이드 개발
우리 대학 생명과학과 전상용 교수 연구팀이 피부 전달을 통해 건선을 치료할 수 있는 펩타이드 치료제를 개발했다.
연구팀은 수 년 전 발견한 펩타이드를 나노입자로 제작해 피부를 통해 전달함으로써 동물 모델에서 건선을 치료하는 데 성공했다.
김진용 박사가 1저자로 참여한 이번 연구는 나노분야 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 6월 27일자 온라인 판에 게재됐다.(논문명 :Nanoparticle-Assisted Transcutaneous Delivery of a Signal Transducer and Activator of Transcription 3-Inhibiting Peptide Ameliorates Psoriasis-like Skin Inflammation)
건선은 대표적인 만성 염증성 피부질환으로 전 세계 성인의 약 3%가 앓고 있는 자가 면역질환 중 하나이다. 최근 건선의 원인에 STAT3라는 단백질이 핵심 역할을 한다는 사실이 밝혀졌다.
연구팀은 수 년 전 STAT3라는 단백질의 기능을 저하시킬 수 있는 펩타이드를 최초로 발견해 항암 치료제로 개발한 바 있다. 그러나 건선 피부는 각질층이 매우 두껍기 때문에 피부를 통해 펩타이드를 투과시켜 표적 약물 치료를 하는 데에는 기술적인 한계가 존재했다.
연구팀은 이번 연구에서 길이가 서로 다른 두 개의 인지질과 STAT3 억제 펩타이드가 특정 조건에서 약 30나노미터 크기의 매우 작은 원반 모양의 나노입자를 안정적으로 형성함을 발견했다.
연구팀은 특수 지질성분으로 이뤄진 제형(劑形)을 통해 수십 나노미터 크기의 원판형 나노입자로 이뤄진 STAT3 억제용 펩타이드를 제조했다.
연구팀이 개발한 STAT3 억제 펩타이드는 건선 피부를 가진 동물 모델에 투여했을 때 뛰어난 항염증 효과를 보였고, 건선 발병의 핵심 요소인 각질세포의 과증식과 염증성 싸이토카인인 IL-17 등의 분비를 막는 역할을 했다.
연구팀은 의과학대학원 김필한 교수와의 공동 연구를 통해 펩타이드가 피부 속으로 얼마나 깊이 투과되는지 관찰했고, 이를 통해 나노입자가 각질층을 통과해 진피층 상부까지 전달됨을 확인했다.
전상용 교수는 “STAT3 억제 앱타이드가 난치성 염증성 피부질환인 건선에 대해 우수한 치료 효과를 보이는 바이오 신약 후보물질이 될 수 있음을 확인했다.”며 “효율적인 피부 전달이 가능한 시스템을 구축했다는 점에서 큰 의미가 있으며 향후 임상 적용이 될 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 글로벌연구실사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 앱타이드-지질 나노복합체의 건선 유발 생쥐 귀 모델에서의 치료효능 평가
그림2. 앱타이드-지질 나노복합체의 건선 유발 생쥐모델에서의 피부투과 효능 평가
2018.07.17 조회수 19283
전상용 교수, 건선,아토피 치료용 펩타이드 개발
우리 대학 생명과학과 전상용 교수 연구팀이 피부 전달을 통해 건선을 치료할 수 있는 펩타이드 치료제를 개발했다.
연구팀은 수 년 전 발견한 펩타이드를 나노입자로 제작해 피부를 통해 전달함으로써 동물 모델에서 건선을 치료하는 데 성공했다.
김진용 박사가 1저자로 참여한 이번 연구는 나노분야 국제 학술지 ‘에이시에스 나노(ACS Nano)’ 6월 27일자 온라인 판에 게재됐다.(논문명 :Nanoparticle-Assisted Transcutaneous Delivery of a Signal Transducer and Activator of Transcription 3-Inhibiting Peptide Ameliorates Psoriasis-like Skin Inflammation)
건선은 대표적인 만성 염증성 피부질환으로 전 세계 성인의 약 3%가 앓고 있는 자가 면역질환 중 하나이다. 최근 건선의 원인에 STAT3라는 단백질이 핵심 역할을 한다는 사실이 밝혀졌다.
연구팀은 수 년 전 STAT3라는 단백질의 기능을 저하시킬 수 있는 펩타이드를 최초로 발견해 항암 치료제로 개발한 바 있다. 그러나 건선 피부는 각질층이 매우 두껍기 때문에 피부를 통해 펩타이드를 투과시켜 표적 약물 치료를 하는 데에는 기술적인 한계가 존재했다.
연구팀은 이번 연구에서 길이가 서로 다른 두 개의 인지질과 STAT3 억제 펩타이드가 특정 조건에서 약 30나노미터 크기의 매우 작은 원반 모양의 나노입자를 안정적으로 형성함을 발견했다.
연구팀은 특수 지질성분으로 이뤄진 제형(劑形)을 통해 수십 나노미터 크기의 원판형 나노입자로 이뤄진 STAT3 억제용 펩타이드를 제조했다.
연구팀이 개발한 STAT3 억제 펩타이드는 건선 피부를 가진 동물 모델에 투여했을 때 뛰어난 항염증 효과를 보였고, 건선 발병의 핵심 요소인 각질세포의 과증식과 염증성 싸이토카인인 IL-17 등의 분비를 막는 역할을 했다.
연구팀은 의과학대학원 김필한 교수와의 공동 연구를 통해 펩타이드가 피부 속으로 얼마나 깊이 투과되는지 관찰했고, 이를 통해 나노입자가 각질층을 통과해 진피층 상부까지 전달됨을 확인했다.
전상용 교수는 “STAT3 억제 앱타이드가 난치성 염증성 피부질환인 건선에 대해 우수한 치료 효과를 보이는 바이오 신약 후보물질이 될 수 있음을 확인했다.”며 “효율적인 피부 전달이 가능한 시스템을 구축했다는 점에서 큰 의미가 있으며 향후 임상 적용이 될 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 글로벌연구실사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 앱타이드-지질 나노복합체의 건선 유발 생쥐 귀 모델에서의 치료효능 평가
그림2. 앱타이드-지질 나노복합체의 건선 유발 생쥐모델에서의 피부투과 효능 평가
2018.07.17 조회수 19283 -
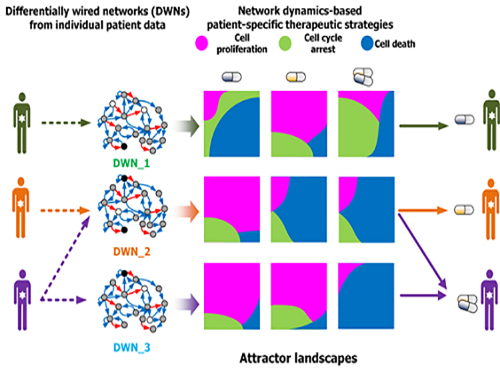 조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
2017.12.07 조회수 24856
조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
2017.12.07 조회수 24856 -
 조광현 교수, 대장암 유발하는 돌연변이 유전자의 네트워크 원리 규명
〈 왼쪽위부터 시계방향으로 이종훈 박사과정, 공정렬 박사과정, 조광현 교수, 신동관 연구교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암이 발병하는 과정에서 생기는 유전자 네트워크의 원리를 규명하는 데 성공했다.
이를 통해 대장암의 근본적인 발병 원리를 밝혀낼 뿐 아니라 향후 새로운 개념의 효과적인 항암제의 분자표적을 찾는데 활용될 것으로 기대된다. 또한 4차 산업혁명의 핵심 기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명해냈다는 의의를 갖는다.
신동관 박사, 이종훈, 공정렬 학생연구원 등이 함께 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 2일자 온라인 판에 게재됐다.
인간의 암은 유전자 돌연변이에 의해 발생한다. 이 돌연변이의 빈도는 암종에 따라 차이가 나는데 백혈병, 소아암은 10여 개 정도이지만 성인 고형암은 평균 50여 개, 폐암 등의 외부인자로 인한 경우는 수백 개에 이른다.
전 세계 암연구자들은 암 치료를 위해 환자들에게서 빈번하게 발견되는 유전자 돌연변이들을 파악하고 이 중 주요 암 유발 유전자를 찾아내 표적 항암제를 개발하고자 노력했다.
그러나 유전자 돌연변이는 해당 유전자의 기능에만 영향을 주는 게 아니라 그 유전자와 상호작용하는 다른 유전자에게도 영향을 끼친다. 따라서 이러한 유전자 네트워크의 원리를 모른 채 소수의 암 유발 유전자를 대상으로 하는 현재의 치료법은 일부에게만 효과가 있고 쉽게 약물의 내성을 일으키는 한계가 있다.
조 교수 연구팀은 대장암 환자의 대규모 유전체 데이터를 이용해 유전자 상호작용 네트워크에서 나타나는 다중 돌연변이의 협력적 효과에 대한 수학모형을 구축했다.
이는 국제 암유전체컨소시엄에서 발표한 전암 유전체데이터베이스(TCGA: The Cancer Genome Atlas)를 토대로 구축한 것으로, 유전자 네트워크에서 나타나는 돌연변이의 영향력을 정량화하고 이를 이용해 대장암 환자 군을 임상 특징에 따라 군집화 하는데 성공했다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 암 발생 과정에서 나타나는 임계전이(critical transition) 현상을 밝혀내 숨겨진 유전자 네트워크의 원리를 최초로 규명했다.
임계전이란 상전이와 같이 물질의 상태가 갑작스럽게 변화하는 현상을 말한다. 암 발생 과정에서는 유전자 돌연변이의 발생 순서를 추적하기 어렵기 때문에 전이 현상이 존재하는지 확인할 수 없었다.
연구팀은 시스템생물학 기반의 연구방법을 이용해 확인한 결과 기존의 대장암에서 잘 알려진 암 유발 유전자 돌연변이의 발생 순서를 따르는 경우에 임계전이 현상을 보임을 발견했다.
이번에 개발한 수학모형을 활용하면 암환자에게 발생하는 다수 유전자 돌연변이의 영향을 가장 효과적으로 저해할 수 있는 새로운 항암 표적 약물이 개발될 것으로 기대된다.
특히 주요 암 유발 유전자 뿐 아니라 돌연변이의 영향을 받는 다른 모든 유전자들을 대상으로 종합적으로 평가해 효과적인 약물 표적을 찾아낼 수 있다.
조 교수는 “지금껏 다수 유전자들의 돌연변이가 암 발생에 어떻게 기여하는지 밝혀진 바가 없었다”며 “이번 연구에서는 시스템생물학으로 암세포의 발달과정에서 유전자 네트워크의 원리를 최초로 밝힘으로써 새로운 차원의 항암제 표적을 발굴할 수 있는 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유전자 돌연변이의 영향력 전파에 의한 거대 클러스터의 형성
그림2. 암발생 과정에서 돌연변이 협력효과의 임계전이 현상
2017.11.07 조회수 25292
조광현 교수, 대장암 유발하는 돌연변이 유전자의 네트워크 원리 규명
〈 왼쪽위부터 시계방향으로 이종훈 박사과정, 공정렬 박사과정, 조광현 교수, 신동관 연구교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 대장암이 발병하는 과정에서 생기는 유전자 네트워크의 원리를 규명하는 데 성공했다.
이를 통해 대장암의 근본적인 발병 원리를 밝혀낼 뿐 아니라 향후 새로운 개념의 효과적인 항암제의 분자표적을 찾는데 활용될 것으로 기대된다. 또한 4차 산업혁명의 핵심 기술로 주목받는 IT와 BT의 융합연구인 시스템생물학 연구로 규명해냈다는 의의를 갖는다.
신동관 박사, 이종훈, 공정렬 학생연구원 등이 함께 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 2일자 온라인 판에 게재됐다.
인간의 암은 유전자 돌연변이에 의해 발생한다. 이 돌연변이의 빈도는 암종에 따라 차이가 나는데 백혈병, 소아암은 10여 개 정도이지만 성인 고형암은 평균 50여 개, 폐암 등의 외부인자로 인한 경우는 수백 개에 이른다.
전 세계 암연구자들은 암 치료를 위해 환자들에게서 빈번하게 발견되는 유전자 돌연변이들을 파악하고 이 중 주요 암 유발 유전자를 찾아내 표적 항암제를 개발하고자 노력했다.
그러나 유전자 돌연변이는 해당 유전자의 기능에만 영향을 주는 게 아니라 그 유전자와 상호작용하는 다른 유전자에게도 영향을 끼친다. 따라서 이러한 유전자 네트워크의 원리를 모른 채 소수의 암 유발 유전자를 대상으로 하는 현재의 치료법은 일부에게만 효과가 있고 쉽게 약물의 내성을 일으키는 한계가 있다.
조 교수 연구팀은 대장암 환자의 대규모 유전체 데이터를 이용해 유전자 상호작용 네트워크에서 나타나는 다중 돌연변이의 협력적 효과에 대한 수학모형을 구축했다.
이는 국제 암유전체컨소시엄에서 발표한 전암 유전체데이터베이스(TCGA: The Cancer Genome Atlas)를 토대로 구축한 것으로, 유전자 네트워크에서 나타나는 돌연변이의 영향력을 정량화하고 이를 이용해 대장암 환자 군을 임상 특징에 따라 군집화 하는데 성공했다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 암 발생 과정에서 나타나는 임계전이(critical transition) 현상을 밝혀내 숨겨진 유전자 네트워크의 원리를 최초로 규명했다.
임계전이란 상전이와 같이 물질의 상태가 갑작스럽게 변화하는 현상을 말한다. 암 발생 과정에서는 유전자 돌연변이의 발생 순서를 추적하기 어렵기 때문에 전이 현상이 존재하는지 확인할 수 없었다.
연구팀은 시스템생물학 기반의 연구방법을 이용해 확인한 결과 기존의 대장암에서 잘 알려진 암 유발 유전자 돌연변이의 발생 순서를 따르는 경우에 임계전이 현상을 보임을 발견했다.
이번에 개발한 수학모형을 활용하면 암환자에게 발생하는 다수 유전자 돌연변이의 영향을 가장 효과적으로 저해할 수 있는 새로운 항암 표적 약물이 개발될 것으로 기대된다.
특히 주요 암 유발 유전자 뿐 아니라 돌연변이의 영향을 받는 다른 모든 유전자들을 대상으로 종합적으로 평가해 효과적인 약물 표적을 찾아낼 수 있다.
조 교수는 “지금껏 다수 유전자들의 돌연변이가 암 발생에 어떻게 기여하는지 밝혀진 바가 없었다”며 “이번 연구에서는 시스템생물학으로 암세포의 발달과정에서 유전자 네트워크의 원리를 최초로 밝힘으로써 새로운 차원의 항암제 표적을 발굴할 수 있는 가능성을 제시했다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 유전자 돌연변이의 영향력 전파에 의한 거대 클러스터의 형성
그림2. 암발생 과정에서 돌연변이 협력효과의 임계전이 현상
2017.11.07 조회수 25292 -
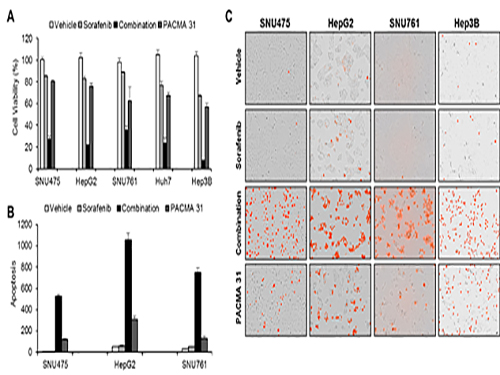 조광현 교수, 간암 표적 치료제 내성 극복 위한 최적 약물조합 발견
〈 조 광 현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 간암 약물 치료의 효과를 높이는 새로운 방법을 찾아냈다. 특히 이번 연구는 바이오분야의 4차 산업혁명을 견인하고 있는 IT와 BT의 융합연구인 시스템생물학(Systems Biology) 연구로 이뤄졌다.
서울대병원 내과 윤정환 교수팀과 공동연구를 통해 이루어낸 이번 연구 결과는 국제 간 전문지인 헤파톨로지(Hepatology)에 게재됐다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오의료기술개발사업과 중견연구자지원사업의 지원을 받아 수행됐다.
간암은 전 세계적으로 남성에게는 다섯 번째, 여성에게는 일곱 번째로 발생률이 높은 암이며 암 사망원인의 두 번째를 차지한다. 특히 우리나라의 간암 사망률은 인구 10만 명 당 28.4명으로 경제협력개발기구(OECD) 국가 중 압도적인 1위이며 2위인 일본의 2배에 이르고 있다.
우리나라에서만 간암 환자가 매년 평균 1만 6000명이 새로 발생하고 있지만 5년 생존율이 12%에 미치지 못한다. 국가암정보센터에 따르면 지난해 암으로 사망한 사람 가운데 폐암이 1만 7399명으로 가장 많았고 간암은 1만 1311명으로 그 뒤를 이었다.
간암은 우리나라의 암 가운데 사회적 비용이 1위인 암이다. 그 이유는 다른 암에 비해 사망자가 많고 더 젊은 나이(40, 50대)에 사망하기 때문이다. 이에 부작용이 적고 생존율을 높여줄 수 있는 새로운 치료법 개발이 시급한 실정이다.
간암의 치료로는 수술 및 색전술, 약물 치료가 있지만 수술이 어려운 진행성 간암에서는 치료 방법이 극히 제한적이다.
진행성 간암의 표적 항암제로 소라페닙(Sorafenib)이 유일하게 승인돼 임상에서 쓰이고 있는데 국내에서만 매년 200억 원 이상 처방되고 있지만 일부 환자에서만 효능을 나타내며 또한 대부분의 경우 약제 내성이 발생한다.
소라페닙은 말기 간암 환자의 생존 기간을 약 3개월 정도 밖에 늘리지 못하지만 다국적 제약회사에 의해 개발된 많은 후발주자 약물들이 그 효과를 뛰어 넘는데 실패했다.
소라페닙은 다중타겟을 치료표적으로 하여 그 작용 기전이 모호하고 따라서 약제의 내성기전 또한 아직 잘 알려져 있지 않다.
조광현 교수가 이끈 융합 연구팀은 소라페닙 작용 및 내성 기전을 규명하기 위해 소라페닙을 간암 세포에 처리하였을 때 세포내 분자 발현이 변화하는 것을 분석했다.
이를 통해 암세포가 소라페닙에 대항하는 기전을 알아냈고 시스템생물학적 분석을 실시하여 암세포내 단백질 이황화 이성질화 효소(protein disulfide isomerase, PDI)가 암세포가 소라페닙에 대항하는데 핵심적 역할을 하는 것을 발견했으며 이 효소를 차단했을 때 소라페닙의 효능이 훨씬 증가함을 관찰했다.
공동연구를 수행한 서울대병원 내과 윤정환 교수 연구팀은 쥐를 이용한 동물실험에서 소라페닙과 단백질 이황화 이성질화 효소 차단제를 같이 처리하면 간암 증식 억제에 시너지가 있음을 관찰하였고 소라페닙에 저항성을 가진 간암 환자의 조직에서 이 효소가 증가되어 있음을 관찰하여, 향후 임상 적용을 위한 가능성을 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 IT와 BT의 융합연구인 시스템생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암에 대한 표적 치료제 작용을 네트워크 차원에서 분석하여 내성을 극복할 수 있는 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 말했다.
□ 사진 설명
사진1. 간암세포를 이용한 세포실험을 이용해 시뮬레이션 결과를 확인
사진2. 구축된 ER stress 네트워크를 이용한 네트워크 분석 및 컴퓨터 시뮬레이션 결과
사진3. 간암 세포가 소라페닙에 반응할 때 전사체 변화를 분석하여 ER stress 반응이 주요하게 나타남을 발견하게 된 ER stress 네트워크 모델
2017.08.24 조회수 22590
조광현 교수, 간암 표적 치료제 내성 극복 위한 최적 약물조합 발견
〈 조 광 현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 간암 약물 치료의 효과를 높이는 새로운 방법을 찾아냈다. 특히 이번 연구는 바이오분야의 4차 산업혁명을 견인하고 있는 IT와 BT의 융합연구인 시스템생물학(Systems Biology) 연구로 이뤄졌다.
서울대병원 내과 윤정환 교수팀과 공동연구를 통해 이루어낸 이번 연구 결과는 국제 간 전문지인 헤파톨로지(Hepatology)에 게재됐다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 바이오의료기술개발사업과 중견연구자지원사업의 지원을 받아 수행됐다.
간암은 전 세계적으로 남성에게는 다섯 번째, 여성에게는 일곱 번째로 발생률이 높은 암이며 암 사망원인의 두 번째를 차지한다. 특히 우리나라의 간암 사망률은 인구 10만 명 당 28.4명으로 경제협력개발기구(OECD) 국가 중 압도적인 1위이며 2위인 일본의 2배에 이르고 있다.
우리나라에서만 간암 환자가 매년 평균 1만 6000명이 새로 발생하고 있지만 5년 생존율이 12%에 미치지 못한다. 국가암정보센터에 따르면 지난해 암으로 사망한 사람 가운데 폐암이 1만 7399명으로 가장 많았고 간암은 1만 1311명으로 그 뒤를 이었다.
간암은 우리나라의 암 가운데 사회적 비용이 1위인 암이다. 그 이유는 다른 암에 비해 사망자가 많고 더 젊은 나이(40, 50대)에 사망하기 때문이다. 이에 부작용이 적고 생존율을 높여줄 수 있는 새로운 치료법 개발이 시급한 실정이다.
간암의 치료로는 수술 및 색전술, 약물 치료가 있지만 수술이 어려운 진행성 간암에서는 치료 방법이 극히 제한적이다.
진행성 간암의 표적 항암제로 소라페닙(Sorafenib)이 유일하게 승인돼 임상에서 쓰이고 있는데 국내에서만 매년 200억 원 이상 처방되고 있지만 일부 환자에서만 효능을 나타내며 또한 대부분의 경우 약제 내성이 발생한다.
소라페닙은 말기 간암 환자의 생존 기간을 약 3개월 정도 밖에 늘리지 못하지만 다국적 제약회사에 의해 개발된 많은 후발주자 약물들이 그 효과를 뛰어 넘는데 실패했다.
소라페닙은 다중타겟을 치료표적으로 하여 그 작용 기전이 모호하고 따라서 약제의 내성기전 또한 아직 잘 알려져 있지 않다.
조광현 교수가 이끈 융합 연구팀은 소라페닙 작용 및 내성 기전을 규명하기 위해 소라페닙을 간암 세포에 처리하였을 때 세포내 분자 발현이 변화하는 것을 분석했다.
이를 통해 암세포가 소라페닙에 대항하는 기전을 알아냈고 시스템생물학적 분석을 실시하여 암세포내 단백질 이황화 이성질화 효소(protein disulfide isomerase, PDI)가 암세포가 소라페닙에 대항하는데 핵심적 역할을 하는 것을 발견했으며 이 효소를 차단했을 때 소라페닙의 효능이 훨씬 증가함을 관찰했다.
공동연구를 수행한 서울대병원 내과 윤정환 교수 연구팀은 쥐를 이용한 동물실험에서 소라페닙과 단백질 이황화 이성질화 효소 차단제를 같이 처리하면 간암 증식 억제에 시너지가 있음을 관찰하였고 소라페닙에 저항성을 가진 간암 환자의 조직에서 이 효소가 증가되어 있음을 관찰하여, 향후 임상 적용을 위한 가능성을 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 IT와 BT의 융합연구인 시스템생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암에 대한 표적 치료제 작용을 네트워크 차원에서 분석하여 내성을 극복할 수 있는 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 말했다.
□ 사진 설명
사진1. 간암세포를 이용한 세포실험을 이용해 시뮬레이션 결과를 확인
사진2. 구축된 ER stress 네트워크를 이용한 네트워크 분석 및 컴퓨터 시뮬레이션 결과
사진3. 간암 세포가 소라페닙에 반응할 때 전사체 변화를 분석하여 ER stress 반응이 주요하게 나타남을 발견하게 된 ER stress 네트워크 모델
2017.08.24 조회수 22590 -
 김일두 교수, 동물 단백질 촉매로 활용한 질병진단센서 개발
〈 김 일 두 교수 〉
우리 대학 신소재공학과 김일두 교수 연구팀이 동물의 단백질을 촉매로 활용해 호흡으로 질병을 진단할 수 있는 센서를 개발했다.
이는 사람의 날숨에 포함된 다양한 질병과 관련된 바이오마커 가스들에 대한 패턴 인식을 통해 질병을 조기 모니터링 할 수 있는 기술이다.
이번 기술은 다양한 단일 금속입자 뿐만 아니라 어떠한 조합의 이종입자도 2 nm 크기로 합성할 수 있는 장점을 갖는다. 연구팀은 기존에도 호흡으로 질병을 진단하는 센서를 개발했으나 이번 기술은 더욱 정확하고 높은 감도를 갖는다는 특징이 있다.
김상준, 최선진 박사가 1저자로 참여한 이번 연구 결과는 미국 화학회의 화학분야 국제 학술지 ‘어카운트 오브 케미칼 리서치(Accounts of Chemical Research)’ 7월호 표지논문으로 선정됐고, 독일 와일리 국제 학술지인 ‘어드밴스드 머터리얼즈(Advanced Materials)’에도 게재가 확정됐다.
혈액 체취나 영상 촬영 없이 내뱉는 숨(호기)만으로 각종 질병 여부를 파악하는 호흡 지문 센서 기술은 핵심 미래 기술이다. 호기 속 특정 가스들의 농도변화를 체크해 건강 이상 여부를 판단할 수 있다.
호기가스 성분에는 수분 외에도 수소, 아세톤, 톨루엔, 암모니아, 황화수소, 일산화질소 등이 포함된다. 이 가스들은 천식, 폐암, 1형 당뇨병, 구취 등 특정 질병 환자에게서 높은 농도로 배출되는 바이오마커 가스이다.
호흡을 이용한 질병 진단은 마치 음주측정기처럼 테들라(Tedlar) 백에 포집된 날숨 가스를 소형 센서 장치로 주입한 후 빠른 속도로 분석되기 때문에 쉽고 간편하게 질병을 진단할 수 있다. 또한 질병 대사가 일어나는 시점에서 검출이 가능해 조기 진단이 가능하다.
하지만 매우 경미한 수준인 10억분의 1(ppb)에서 100만분의 1(ppm) 수준으로 발생하는 가스를 호흡 속에서 정확히 분석하기 위해서는 기술의 진보가 필요하다. 특히 수분을 포함한 수백 종의 방해 가스는 특정 질병 관련 바이오마커 가스를 선택적으로 분석하는 저항 변화식 센서의 취약점으로 남아 있다.
기존의 가스 센서는 백금, 팔라듐 등 특정 촉매를 결합해 감지 특성을 높이려고 시도했으나 ppb 농도에서는 생체지표 가스 감지 특성이 높지 않다는 한계가 있었다.
연구팀은 기존 센서의 한계 극복을 위해 동물의 조직에 존재하는 나노크기의 단백질을 희생층으로 이용해 속이 비어있는 단백질 껍질 안에 석출된 이종촉매(Heterogeneous catalyst) 입자를 합성하는데 성공했다.
이번 연구에 사용된 나노크기의 단백질은 주기율표에 존재하는 원소물질을 조합해 어떠한 형태의 이종촉매도 다양하게 구현할 수 있다는 큰 장점을 갖는다.
특히 이종 원소간 조성비를 쉽게 조절할 수 있고 금속간화합물도 제조할 수 있어 신조성을 갖는 촉매 합성 측면에서 매우 획기적인 방법이다.
예를 들어 백금이 기준 촉매일 때 백금팔라듐(PtPd), 백금니켈(PtNi), 백금루테늄(PdRu), 백금이트륨(PtY3) 등 다양한 이종 합금촉매로 확장할 수 있다.
연구팀은 개발된 이종촉매 입자를 넓은 비표면적과 다공성 구조를 갖는 금속산화물 나노섬유에 결착시켜 특정 생체지표 기체에만 선택적으로 반응하는 감지소재를 개발했다. 이종촉매가 결착된 나노섬유 센서는 기존에 촉매 활성이 가장 뛰어나다고 알려진 백금이나 팔라듐 촉매보다 약 3~4배 이상 감지 특성이 향상됨을 확인했다.
특히 아세톤이나 황화수소 가스는 1ppm에서 감도가 100배 수준으로 바뀌는 최고 수준의 감도 특성이 관찰됐다.
연구팀은 다양한 종류의 감지 소재가 적용된 복합 센서 배치(sensor array) 시스템을 이용해 사람의 지문을 인식하듯 개개인의 호흡을 패턴 인식해 일반인도 쉽게 건강 이상을 판별할 수 있는 질병진단 플랫폼을 개발했다.
16종의 다른 선택성을 갖는 센서를 어레이화하는데 성공했으며, 환자의 건강상태에 따라 날숨 농도변화가 다르게 나타나기 때문에 날숨 속 가스 정보를 지문처럼 패턴화하여 개인의 건강 변화를 지속적으로 모니터링 하는 헬스케어 기기에 적용할 수 있다.
김 교수는 “기존에 센서에 사용된 적이 없는 2 nm 크기의 이종촉매를 단백질을 이용하여 적용함으로써, 질병과 연관된 생체지표 가스에 고감도 및 고 선택성으로 반응하는 센서소재 라이브러리를 구현할 수 있다”며 “앞으로 다양한 촉매 군을 확보하면 수많은 질병을 진단할 수 있는 센서를 개발할 수 있다”고 말했다.
또한 “호흡으로 질병을 진단하는 센서는 누구나 손쉽게 스스로 진단할 수 있는 자가 진단 기기의 시작으로 의료비 지출 상승을 막고 지속적 건강관리에 큰 도움이 될 것이다”고 말했다.
이번 기술과 관련된 특허들은 지난 3월과 6월 각각 벤처기업과 중소기업에 기술이전 됐다.
본 연구는 미래창조 과학부 웨어러블 플랫폼소재 기술센터 과제와 바이오의료기술개발사업 과제의 지원으로 이루어졌다.
□ 그림 설명
그림1. 어카운트 오브 케미칼 리서치 표지 이미지
그림2. 다종 입자 촉매
그림3. 함금촉매 합성
그림4. 다종센서 어레이_날숨 분석 센서
2017.07.18 조회수 35488
김일두 교수, 동물 단백질 촉매로 활용한 질병진단센서 개발
〈 김 일 두 교수 〉
우리 대학 신소재공학과 김일두 교수 연구팀이 동물의 단백질을 촉매로 활용해 호흡으로 질병을 진단할 수 있는 센서를 개발했다.
이는 사람의 날숨에 포함된 다양한 질병과 관련된 바이오마커 가스들에 대한 패턴 인식을 통해 질병을 조기 모니터링 할 수 있는 기술이다.
이번 기술은 다양한 단일 금속입자 뿐만 아니라 어떠한 조합의 이종입자도 2 nm 크기로 합성할 수 있는 장점을 갖는다. 연구팀은 기존에도 호흡으로 질병을 진단하는 센서를 개발했으나 이번 기술은 더욱 정확하고 높은 감도를 갖는다는 특징이 있다.
김상준, 최선진 박사가 1저자로 참여한 이번 연구 결과는 미국 화학회의 화학분야 국제 학술지 ‘어카운트 오브 케미칼 리서치(Accounts of Chemical Research)’ 7월호 표지논문으로 선정됐고, 독일 와일리 국제 학술지인 ‘어드밴스드 머터리얼즈(Advanced Materials)’에도 게재가 확정됐다.
혈액 체취나 영상 촬영 없이 내뱉는 숨(호기)만으로 각종 질병 여부를 파악하는 호흡 지문 센서 기술은 핵심 미래 기술이다. 호기 속 특정 가스들의 농도변화를 체크해 건강 이상 여부를 판단할 수 있다.
호기가스 성분에는 수분 외에도 수소, 아세톤, 톨루엔, 암모니아, 황화수소, 일산화질소 등이 포함된다. 이 가스들은 천식, 폐암, 1형 당뇨병, 구취 등 특정 질병 환자에게서 높은 농도로 배출되는 바이오마커 가스이다.
호흡을 이용한 질병 진단은 마치 음주측정기처럼 테들라(Tedlar) 백에 포집된 날숨 가스를 소형 센서 장치로 주입한 후 빠른 속도로 분석되기 때문에 쉽고 간편하게 질병을 진단할 수 있다. 또한 질병 대사가 일어나는 시점에서 검출이 가능해 조기 진단이 가능하다.
하지만 매우 경미한 수준인 10억분의 1(ppb)에서 100만분의 1(ppm) 수준으로 발생하는 가스를 호흡 속에서 정확히 분석하기 위해서는 기술의 진보가 필요하다. 특히 수분을 포함한 수백 종의 방해 가스는 특정 질병 관련 바이오마커 가스를 선택적으로 분석하는 저항 변화식 센서의 취약점으로 남아 있다.
기존의 가스 센서는 백금, 팔라듐 등 특정 촉매를 결합해 감지 특성을 높이려고 시도했으나 ppb 농도에서는 생체지표 가스 감지 특성이 높지 않다는 한계가 있었다.
연구팀은 기존 센서의 한계 극복을 위해 동물의 조직에 존재하는 나노크기의 단백질을 희생층으로 이용해 속이 비어있는 단백질 껍질 안에 석출된 이종촉매(Heterogeneous catalyst) 입자를 합성하는데 성공했다.
이번 연구에 사용된 나노크기의 단백질은 주기율표에 존재하는 원소물질을 조합해 어떠한 형태의 이종촉매도 다양하게 구현할 수 있다는 큰 장점을 갖는다.
특히 이종 원소간 조성비를 쉽게 조절할 수 있고 금속간화합물도 제조할 수 있어 신조성을 갖는 촉매 합성 측면에서 매우 획기적인 방법이다.
예를 들어 백금이 기준 촉매일 때 백금팔라듐(PtPd), 백금니켈(PtNi), 백금루테늄(PdRu), 백금이트륨(PtY3) 등 다양한 이종 합금촉매로 확장할 수 있다.
연구팀은 개발된 이종촉매 입자를 넓은 비표면적과 다공성 구조를 갖는 금속산화물 나노섬유에 결착시켜 특정 생체지표 기체에만 선택적으로 반응하는 감지소재를 개발했다. 이종촉매가 결착된 나노섬유 센서는 기존에 촉매 활성이 가장 뛰어나다고 알려진 백금이나 팔라듐 촉매보다 약 3~4배 이상 감지 특성이 향상됨을 확인했다.
특히 아세톤이나 황화수소 가스는 1ppm에서 감도가 100배 수준으로 바뀌는 최고 수준의 감도 특성이 관찰됐다.
연구팀은 다양한 종류의 감지 소재가 적용된 복합 센서 배치(sensor array) 시스템을 이용해 사람의 지문을 인식하듯 개개인의 호흡을 패턴 인식해 일반인도 쉽게 건강 이상을 판별할 수 있는 질병진단 플랫폼을 개발했다.
16종의 다른 선택성을 갖는 센서를 어레이화하는데 성공했으며, 환자의 건강상태에 따라 날숨 농도변화가 다르게 나타나기 때문에 날숨 속 가스 정보를 지문처럼 패턴화하여 개인의 건강 변화를 지속적으로 모니터링 하는 헬스케어 기기에 적용할 수 있다.
김 교수는 “기존에 센서에 사용된 적이 없는 2 nm 크기의 이종촉매를 단백질을 이용하여 적용함으로써, 질병과 연관된 생체지표 가스에 고감도 및 고 선택성으로 반응하는 센서소재 라이브러리를 구현할 수 있다”며 “앞으로 다양한 촉매 군을 확보하면 수많은 질병을 진단할 수 있는 센서를 개발할 수 있다”고 말했다.
또한 “호흡으로 질병을 진단하는 센서는 누구나 손쉽게 스스로 진단할 수 있는 자가 진단 기기의 시작으로 의료비 지출 상승을 막고 지속적 건강관리에 큰 도움이 될 것이다”고 말했다.
이번 기술과 관련된 특허들은 지난 3월과 6월 각각 벤처기업과 중소기업에 기술이전 됐다.
본 연구는 미래창조 과학부 웨어러블 플랫폼소재 기술센터 과제와 바이오의료기술개발사업 과제의 지원으로 이루어졌다.
□ 그림 설명
그림1. 어카운트 오브 케미칼 리서치 표지 이미지
그림2. 다종 입자 촉매
그림3. 함금촉매 합성
그림4. 다종센서 어레이_날숨 분석 센서
2017.07.18 조회수 35488