%EC%95%8C%EC%B8%A0%ED%95%98%EC%9D%B4%EB%A8%B8
-
 알츠하이머 발병 과정을 관찰하다
퇴행성 질환을 유발하는 아밀로이드 섬유 단백질의 초기 불안정한 움직임과 같은 생명 현상을 분자 수준에서 실시간 관찰이 가능한 기술이 개발되었다. 이를 통해 알츠하이머나 파킨슨 병과 같은 퇴행성 질환의 발병 과정에 대한 실마리를 제공할 수 있을 것으로 기대된다.
우리 대학 신소재공학과 육종민 교수 연구팀이 한국기초과학지원연구원, 포항산업과학연구원, 성균관대학교 약학대학 연구팀과 함께 그래핀을 이용해 알츠하이머 질병을 유발한다고 알려진 아밀로이드 섬유 단백질의 실시간 거동을 관찰할 수 있는 새로운 단분자 관찰 기술(single-molecule technique)을 개발했다고 30일 밝혔다.
단분자 관찰 기술은 단일 분자 수준에서 발생하는 현상을 관찰할 수 있는 기법을 말한다. 생체 과정에서 수반되는 단백질 간의 상호작용, 접힘, 조립 과정 등을 이해하는 데 핵심적인 기술이다. 현재까지 단분자 관찰 기술로는 특정 분자를 식별하기 위한 형광 현미경을 이용해 관찰하거나, 단백질을 급속 냉동시켜 움직임을 고정해 분자 구조를 해석하는 초저온 전자현미경 기법이 활용 돼왔다.
하지만, 자연 그대로의 단백질을 특별한 전처리 없이 분자 단위에서 실시간으로 관찰할 수 있는 기술은 여전히 부재한 상황이었다.
최근 이에 대한 대안으로 물질을 얼리지 않고 상온 상태에서 관찰하는 액상 전자현미경 기술이 최근 주목을 받고 있다. 이 기술은 얇은 투과막을 이용해 액체를 감싸 전자현미경 내에서 물질의 변화를 관찰할 수 있는 기술이지만, 두꺼운 투과 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성은 해결해야 하는 숙제였다.
육종민 교수 연구팀은 차세대 소재로 주목받고 있는 그래핀을 이용해 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성 문제를 해결하며, 단백질의 거동을 실시간 관찰할 수 있는 단분자 그래핀 액상 셀 전자현미경 기술을 개발했다. [그림 1]
이번 연구에서 투과 막으로 이용한 그래핀은 원자 단위의 두께를 가지고 있어 분자 수준 관찰을 가능하게 할 뿐만 아니라, 전자빔에 의한 단백질의 산화를 방지하는 산화 방지 역할을 해 기존 대비 40배 가량 변성을 억제해 단백질의 거동을 실시간으로 관찰할 수 있게 했다.
연구팀은 개발한 전자현미경 기술을 활용해, 알츠하이머 질병을 유발한다고 알려진 아밀로이드 베타 섬유의 초기 성장 과정에서 발현되는 분자 불안정성을 세계 최초로 관찰했다. [그림 2]
이 전자현미경 기술은 온전한 단백질의 다양한 거동들을 분자 수준에서 관찰을 가능하게 하므로, 코로나19와 같은 바이러스성 단백질의 감염 과정, 퇴행성 질환을 일으키는 아밀로이드성 단백질의 섬유화/응집 거동 등과 같이 단백질의 상호작용에 의한 생명 현상을 이해하는 데 활용될 수 있을 것으로 기대된다.
육 교수는 "현미경 기술의 발전은 생명과학 및 공학 기술 발전의 토대가 되는 것으로, 분자 단위의 현상을 관찰할 수 있다면 단백질들의 상호작용을 이해하고 조절할 수 있는 실마리를 제공할 수 있으며, 이를 통해 알츠하이머와 같은 퇴행성 질환의 신약 개발에 도움을 줄 수 있을 것으로 기대한다ˮ 라고 말했다.
우리 대학 신소재공학과 졸업생 박정재 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 머티리얼스(Advanced Materials)' 지난 11월 온라인으로 발표됐다. (논문명 : Single-Molecule Graphene Liquid Cell Electron Microscopy for Instability of Intermediate Amyloid Fibrils).
이번 연구는 한국연구재단의 중견연구자지원사업(MIST) (NRF-2022R1A2C2008929)과 나노 및 소재 기술개발사업(MIST)(NRF-2021M3H4A6A02050365)의 지원을 받아 수행됐다.
2024.01.30 조회수 7781
알츠하이머 발병 과정을 관찰하다
퇴행성 질환을 유발하는 아밀로이드 섬유 단백질의 초기 불안정한 움직임과 같은 생명 현상을 분자 수준에서 실시간 관찰이 가능한 기술이 개발되었다. 이를 통해 알츠하이머나 파킨슨 병과 같은 퇴행성 질환의 발병 과정에 대한 실마리를 제공할 수 있을 것으로 기대된다.
우리 대학 신소재공학과 육종민 교수 연구팀이 한국기초과학지원연구원, 포항산업과학연구원, 성균관대학교 약학대학 연구팀과 함께 그래핀을 이용해 알츠하이머 질병을 유발한다고 알려진 아밀로이드 섬유 단백질의 실시간 거동을 관찰할 수 있는 새로운 단분자 관찰 기술(single-molecule technique)을 개발했다고 30일 밝혔다.
단분자 관찰 기술은 단일 분자 수준에서 발생하는 현상을 관찰할 수 있는 기법을 말한다. 생체 과정에서 수반되는 단백질 간의 상호작용, 접힘, 조립 과정 등을 이해하는 데 핵심적인 기술이다. 현재까지 단분자 관찰 기술로는 특정 분자를 식별하기 위한 형광 현미경을 이용해 관찰하거나, 단백질을 급속 냉동시켜 움직임을 고정해 분자 구조를 해석하는 초저온 전자현미경 기법이 활용 돼왔다.
하지만, 자연 그대로의 단백질을 특별한 전처리 없이 분자 단위에서 실시간으로 관찰할 수 있는 기술은 여전히 부재한 상황이었다.
최근 이에 대한 대안으로 물질을 얼리지 않고 상온 상태에서 관찰하는 액상 전자현미경 기술이 최근 주목을 받고 있다. 이 기술은 얇은 투과막을 이용해 액체를 감싸 전자현미경 내에서 물질의 변화를 관찰할 수 있는 기술이지만, 두꺼운 투과 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성은 해결해야 하는 숙제였다.
육종민 교수 연구팀은 차세대 소재로 주목받고 있는 그래핀을 이용해 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성 문제를 해결하며, 단백질의 거동을 실시간 관찰할 수 있는 단분자 그래핀 액상 셀 전자현미경 기술을 개발했다. [그림 1]
이번 연구에서 투과 막으로 이용한 그래핀은 원자 단위의 두께를 가지고 있어 분자 수준 관찰을 가능하게 할 뿐만 아니라, 전자빔에 의한 단백질의 산화를 방지하는 산화 방지 역할을 해 기존 대비 40배 가량 변성을 억제해 단백질의 거동을 실시간으로 관찰할 수 있게 했다.
연구팀은 개발한 전자현미경 기술을 활용해, 알츠하이머 질병을 유발한다고 알려진 아밀로이드 베타 섬유의 초기 성장 과정에서 발현되는 분자 불안정성을 세계 최초로 관찰했다. [그림 2]
이 전자현미경 기술은 온전한 단백질의 다양한 거동들을 분자 수준에서 관찰을 가능하게 하므로, 코로나19와 같은 바이러스성 단백질의 감염 과정, 퇴행성 질환을 일으키는 아밀로이드성 단백질의 섬유화/응집 거동 등과 같이 단백질의 상호작용에 의한 생명 현상을 이해하는 데 활용될 수 있을 것으로 기대된다.
육 교수는 "현미경 기술의 발전은 생명과학 및 공학 기술 발전의 토대가 되는 것으로, 분자 단위의 현상을 관찰할 수 있다면 단백질들의 상호작용을 이해하고 조절할 수 있는 실마리를 제공할 수 있으며, 이를 통해 알츠하이머와 같은 퇴행성 질환의 신약 개발에 도움을 줄 수 있을 것으로 기대한다ˮ 라고 말했다.
우리 대학 신소재공학과 졸업생 박정재 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 머티리얼스(Advanced Materials)' 지난 11월 온라인으로 발표됐다. (논문명 : Single-Molecule Graphene Liquid Cell Electron Microscopy for Instability of Intermediate Amyloid Fibrils).
이번 연구는 한국연구재단의 중견연구자지원사업(MIST) (NRF-2022R1A2C2008929)과 나노 및 소재 기술개발사업(MIST)(NRF-2021M3H4A6A02050365)의 지원을 받아 수행됐다.
2024.01.30 조회수 7781 -
 알츠하이머 조기 진단하는 센서단백질 디자인하다
고정된 3차원 구조가 없는 상태로 존재하는 비정형 단백질((Intrinsically disordered protein)은 알츠하이머, 파킨슨병과 같은 신경계 질환부터 암, 심혈관계 질환, 대사질환을 유발하는 것으로 알려져 있다. 따라서, 이들을 신속하게 검출하고 분석할 수 있다면 조기 진단을 통해 질병의 진행을 막고 환자의 예후를 개선할 수 있을 뿐 아니라, 병리기전을 밝히고 나아가 치료제를 개발하는 데 큰 도움이 될 수 있다.
우리 대학 생명과학과 김학성 교수 연구팀이 이러한 비정형 단백질을 간단하게 검출할 수 있는 센서 단백질을 디자인하는 데에 성공했다고 8일 밝혔다.
단백질은 특정한 3차원 구조를 가지며 생체 내 다양한 기능을 수행하는 데 실제 인간 단백질 중 44%는 상황에 따라 구조가 변화는 비정형 단백질로 고정된 구조를 갖는 일반 단백질보다 더욱 다양한 기능을 수행한다. 그러나, 비정형 단백질은 고정된 구조가 없어서 이들 단백질의 분석과 기능 연구가 매우 어려웠다.
연구팀은 비정형 단백질이 단백질 2차 구조인 베타 스트랜드(β-strand)를 형성하는 특정 아미노산 서열을 갖고 있다는 점에 착안하여 이러한 특정 서열과 상보적으로 결합할 경우에만 신호를 방출하는 새로운 형태의 센서 단백질 디자인 방법을 정립하였다.
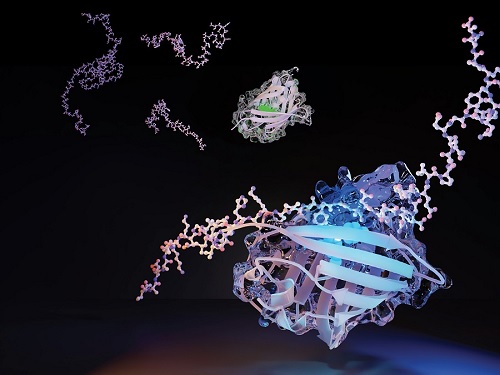
연구팀은 자연계에 존재하는 녹색 형광 단백질(Green Fluorescent Protein, GFP)의 베타 스트랜드 하나를 제거한 후, 비정형 단백질의 특정 서열이 결합하면 형광 단백질 발색단(chromophore)의 파장 스펙트럼이 변화하는 센서 단백질을 컴퓨터 및 방향적 진화 방법을 이용하여 성공적으로 개발하였다. (그림 1)
연구팀은 대표적 비정형 단백질의 하나로 알츠하이머를 유발하는 세포 내 베타-아밀로이드(β-amyloid)를 검출할 수 있는 센서 단백질을 개발하여 실시간으로 세포막과의 상호작용을 추적하고 영상화할 수 있었다. 기존에는 비정형 단백질을 분석하기 위해 복잡한 여러 단계의 전처리 과정이 필요하였고 이로 인해 비정형 단백질 자체가 크게 변형되어 실제 비정형 단백질의 분석과 기능 연구에 많은 제약이 있었다. 그러나, 이번에 개발된 센서 단백질은 단순히 비정형 단백질과 섞어줌으로써 매우 간편하고 빠르게 비정형 단백질을 검출할 수 있어서 향후 비정형 단백질 분석 및 관련 질병 연구에 크게 기여할 것으로 기대된다.
생명과학과 유태근 박사가 제1 저자로 참여하고 이진수 박사 (허원도 교수 연구실)와 윤정민 박사(송지준 교수 연구실)가 공동으로 진행한 이번 연구는 국제 학술지 '잭스 골드 (JACS Au)'에 지난 10월 26일 자 3권 11호에 출판됐으며, 표지 논문으로 선정됐다. (그림 2) (논문명 : Engineering of a Fluorescent Protein for a Sensing of an Intrinsically Disordered Protein through Transition in the Chromophore State)
제1 저자인 유태근 박사는 “고정된 구조가 없는 비정형 단백질은 일반적 단백질에 비해 센서 단백질의 디자인과 개발이 매우 어려운 표적이었다”라며 “이번 연구가 비정형 단백질의 분석과 관련 병리기전의 연구에 새로운 방법과 전략을 제시할 수 있을 것이다”라고 말했다.
한편 이번 연구는 한국연구재단 기초연구사업과 중견연구자지원사업의 지원을 받아 수행됐다.
2023.12.08 조회수 6612
알츠하이머 조기 진단하는 센서단백질 디자인하다
고정된 3차원 구조가 없는 상태로 존재하는 비정형 단백질((Intrinsically disordered protein)은 알츠하이머, 파킨슨병과 같은 신경계 질환부터 암, 심혈관계 질환, 대사질환을 유발하는 것으로 알려져 있다. 따라서, 이들을 신속하게 검출하고 분석할 수 있다면 조기 진단을 통해 질병의 진행을 막고 환자의 예후를 개선할 수 있을 뿐 아니라, 병리기전을 밝히고 나아가 치료제를 개발하는 데 큰 도움이 될 수 있다.
우리 대학 생명과학과 김학성 교수 연구팀이 이러한 비정형 단백질을 간단하게 검출할 수 있는 센서 단백질을 디자인하는 데에 성공했다고 8일 밝혔다.
단백질은 특정한 3차원 구조를 가지며 생체 내 다양한 기능을 수행하는 데 실제 인간 단백질 중 44%는 상황에 따라 구조가 변화는 비정형 단백질로 고정된 구조를 갖는 일반 단백질보다 더욱 다양한 기능을 수행한다. 그러나, 비정형 단백질은 고정된 구조가 없어서 이들 단백질의 분석과 기능 연구가 매우 어려웠다.
연구팀은 비정형 단백질이 단백질 2차 구조인 베타 스트랜드(β-strand)를 형성하는 특정 아미노산 서열을 갖고 있다는 점에 착안하여 이러한 특정 서열과 상보적으로 결합할 경우에만 신호를 방출하는 새로운 형태의 센서 단백질 디자인 방법을 정립하였다.
연구팀은 자연계에 존재하는 녹색 형광 단백질(Green Fluorescent Protein, GFP)의 베타 스트랜드 하나를 제거한 후, 비정형 단백질의 특정 서열이 결합하면 형광 단백질 발색단(chromophore)의 파장 스펙트럼이 변화하는 센서 단백질을 컴퓨터 및 방향적 진화 방법을 이용하여 성공적으로 개발하였다. (그림 1)
연구팀은 대표적 비정형 단백질의 하나로 알츠하이머를 유발하는 세포 내 베타-아밀로이드(β-amyloid)를 검출할 수 있는 센서 단백질을 개발하여 실시간으로 세포막과의 상호작용을 추적하고 영상화할 수 있었다. 기존에는 비정형 단백질을 분석하기 위해 복잡한 여러 단계의 전처리 과정이 필요하였고 이로 인해 비정형 단백질 자체가 크게 변형되어 실제 비정형 단백질의 분석과 기능 연구에 많은 제약이 있었다. 그러나, 이번에 개발된 센서 단백질은 단순히 비정형 단백질과 섞어줌으로써 매우 간편하고 빠르게 비정형 단백질을 검출할 수 있어서 향후 비정형 단백질 분석 및 관련 질병 연구에 크게 기여할 것으로 기대된다.
생명과학과 유태근 박사가 제1 저자로 참여하고 이진수 박사 (허원도 교수 연구실)와 윤정민 박사(송지준 교수 연구실)가 공동으로 진행한 이번 연구는 국제 학술지 '잭스 골드 (JACS Au)'에 지난 10월 26일 자 3권 11호에 출판됐으며, 표지 논문으로 선정됐다. (그림 2) (논문명 : Engineering of a Fluorescent Protein for a Sensing of an Intrinsically Disordered Protein through Transition in the Chromophore State)
제1 저자인 유태근 박사는 “고정된 구조가 없는 비정형 단백질은 일반적 단백질에 비해 센서 단백질의 디자인과 개발이 매우 어려운 표적이었다”라며 “이번 연구가 비정형 단백질의 분석과 관련 병리기전의 연구에 새로운 방법과 전략을 제시할 수 있을 것이다”라고 말했다.
한편 이번 연구는 한국연구재단 기초연구사업과 중견연구자지원사업의 지원을 받아 수행됐다.
2023.12.08 조회수 6612 -
 알츠하이머병 유발하는 독성 단백질 발굴
알츠하이머병은 가장 대표적인 신경퇴행성 질환으로, 기억력 감퇴와 인지능력 저하를 유발한다. 알츠하이머병의 발병 인구가 급속히 증가하고 있으나, 현재까지 발병 원인이 명확히 밝혀진 바 없고, 이에 따라 효과적인 치료제 개발 또한 굉장히 더디게 진행되고 있다.
우리 대학 화학과 임미희 교수(금속신경단백질연구단 단장) 연구팀이 한국기초과학지원연구원 바이오융합연구부 이영호 박사 연구팀, 우리 대학 화학과 백무현 교수 연구팀, 의과학대학원 한진주 교수 연구팀과의 공동연구와 한국생명공학연구원 희귀난치질환연구센터 이다용 박사 연구팀과 공동연구를 통해 알츠하이머병 유발인자의 독성을 촉진하는 세포 내 단백질을 발굴함으로써, 알츠하이머병과 관련된 새로운 병리적 네트워크를 제시했다고 20일 밝혔다.
알츠하이머병 환자들의 뇌에서 대표적으로 나타나는 병리적 현상은 노인성 반점 축적이다. 노인성 반점의 주된 구성분은 아밀로이드-베타 펩타이드로인 응집체로 세포 내 물질들과 결합해 세포 손상을 유발한다. 따라서, 이들 응집체와 세포 사멸 간의 상관관계가 활발히 연구되고 있다. 그러나, 아밀로이드-베타와 세포 사멸 유발 인자들 간의 직접적인 상호작용에 관해서는 아직 많은 부분이 밝혀진 바 없다.
최근 미국 FDA에서 승인한 알츠하이머병 신약은 노인성 반점을 나타내는 아밀로이드-베타 펩타이드의 응집체의 세포 손상을 주요 타깃으로 하여 개발됐다. 하지만, 제한된 사용 여부(특히, 부작용)로 그 신약 개발의 방향 전환 및 개선이 필요함을 연구자들은 절실히 느끼고 있다.
임미희 교수 연구팀은 알츠하이머병에서 과발현되며 원인 미상의 신경세포 사멸을 유발하는 ‘아밀로이드 전구체 C 말단 절단체’ 단백질이 아밀로이드-베타 및 금속-아밀로이드-베타 복합체와 결합해 응집을 촉진하고 독성 촉진제 역할을 함을 세계 최초로 증명하는 연구 내용을 발표했다.
이번 연구 결과는 아밀로이드 전구체 C 말단 절단체 자체 또는 아밀로이드-베타과 결합한 복합체가 새로운 알츠하이머병의 새로운 바이오마커로 작용할 수 있고, 또한 그들이 새로운 신약개발 타깃이 될 수 있음을 제시하고 있다.
임미희 교수 연구팀의 남은주 박사(KAIST 화학과 박사 졸업, 現 브리검 여성 병원 및 하버드 의과대학 연구원)가 제1 저자로 참여한 이번 연구는 세포 내 단백질 미세주입 기술을 통해 세포 안에서 아밀로이드 전구체 C 말단 절단체가 아밀로이드-베타 응집 촉진에 미치는 역할을 연구팀은 확인했다. 더 나아가, 뉴런 세포 및 설치류의 뇌에서 아밀로이드-베타와 관련된 세포 사멸, 뉴런 손상, 염증반응이 아밀로이드 전구체 C 말단 절단체에 의해 더욱 증가하는 현상을 최초로 확인해 세계적으로 주목받고 있다.
임미희 교수는 “이번 연구 결과는 알츠하이머병에서 기존에 알려지지 않은 생체 내 아밀로이드-베타 응집 및 독성 촉진제 발굴에 큰 의의가 있다”고 말하며, “이 연구 성과는 새로운 바이오마커 및 치료타깃을 제안하고 있다”고 밝혔다.
이번 연구는 국제 저명 학술지인 `어드밴스드 사이언스(Advanced Science, Impact factor: 15.1)'에 11월 10일 자 게재됐다. (논문명: APP-C31: An Intracellular Promoter of Both Metal-Free and Metal-Bound Amyloid-β40 Aggregation and Toxicity in Alzheimer’s Disease) Adv. Sci. 2023, 2307182 (https://doi.org/10.1002/advs.202307182)
이번 연구는 한국연구재단 기초연구사업(특히, 리더연구), KBSI, 국가과학기술연구회(NST), IBS 및 KAIST의 지원을 받아 진행됐다.
2023.11.20 조회수 7533
알츠하이머병 유발하는 독성 단백질 발굴
알츠하이머병은 가장 대표적인 신경퇴행성 질환으로, 기억력 감퇴와 인지능력 저하를 유발한다. 알츠하이머병의 발병 인구가 급속히 증가하고 있으나, 현재까지 발병 원인이 명확히 밝혀진 바 없고, 이에 따라 효과적인 치료제 개발 또한 굉장히 더디게 진행되고 있다.
우리 대학 화학과 임미희 교수(금속신경단백질연구단 단장) 연구팀이 한국기초과학지원연구원 바이오융합연구부 이영호 박사 연구팀, 우리 대학 화학과 백무현 교수 연구팀, 의과학대학원 한진주 교수 연구팀과의 공동연구와 한국생명공학연구원 희귀난치질환연구센터 이다용 박사 연구팀과 공동연구를 통해 알츠하이머병 유발인자의 독성을 촉진하는 세포 내 단백질을 발굴함으로써, 알츠하이머병과 관련된 새로운 병리적 네트워크를 제시했다고 20일 밝혔다.
알츠하이머병 환자들의 뇌에서 대표적으로 나타나는 병리적 현상은 노인성 반점 축적이다. 노인성 반점의 주된 구성분은 아밀로이드-베타 펩타이드로인 응집체로 세포 내 물질들과 결합해 세포 손상을 유발한다. 따라서, 이들 응집체와 세포 사멸 간의 상관관계가 활발히 연구되고 있다. 그러나, 아밀로이드-베타와 세포 사멸 유발 인자들 간의 직접적인 상호작용에 관해서는 아직 많은 부분이 밝혀진 바 없다.
최근 미국 FDA에서 승인한 알츠하이머병 신약은 노인성 반점을 나타내는 아밀로이드-베타 펩타이드의 응집체의 세포 손상을 주요 타깃으로 하여 개발됐다. 하지만, 제한된 사용 여부(특히, 부작용)로 그 신약 개발의 방향 전환 및 개선이 필요함을 연구자들은 절실히 느끼고 있다.
임미희 교수 연구팀은 알츠하이머병에서 과발현되며 원인 미상의 신경세포 사멸을 유발하는 ‘아밀로이드 전구체 C 말단 절단체’ 단백질이 아밀로이드-베타 및 금속-아밀로이드-베타 복합체와 결합해 응집을 촉진하고 독성 촉진제 역할을 함을 세계 최초로 증명하는 연구 내용을 발표했다.
이번 연구 결과는 아밀로이드 전구체 C 말단 절단체 자체 또는 아밀로이드-베타과 결합한 복합체가 새로운 알츠하이머병의 새로운 바이오마커로 작용할 수 있고, 또한 그들이 새로운 신약개발 타깃이 될 수 있음을 제시하고 있다.
임미희 교수 연구팀의 남은주 박사(KAIST 화학과 박사 졸업, 現 브리검 여성 병원 및 하버드 의과대학 연구원)가 제1 저자로 참여한 이번 연구는 세포 내 단백질 미세주입 기술을 통해 세포 안에서 아밀로이드 전구체 C 말단 절단체가 아밀로이드-베타 응집 촉진에 미치는 역할을 연구팀은 확인했다. 더 나아가, 뉴런 세포 및 설치류의 뇌에서 아밀로이드-베타와 관련된 세포 사멸, 뉴런 손상, 염증반응이 아밀로이드 전구체 C 말단 절단체에 의해 더욱 증가하는 현상을 최초로 확인해 세계적으로 주목받고 있다.
임미희 교수는 “이번 연구 결과는 알츠하이머병에서 기존에 알려지지 않은 생체 내 아밀로이드-베타 응집 및 독성 촉진제 발굴에 큰 의의가 있다”고 말하며, “이 연구 성과는 새로운 바이오마커 및 치료타깃을 제안하고 있다”고 밝혔다.
이번 연구는 국제 저명 학술지인 `어드밴스드 사이언스(Advanced Science, Impact factor: 15.1)'에 11월 10일 자 게재됐다. (논문명: APP-C31: An Intracellular Promoter of Both Metal-Free and Metal-Bound Amyloid-β40 Aggregation and Toxicity in Alzheimer’s Disease) Adv. Sci. 2023, 2307182 (https://doi.org/10.1002/advs.202307182)
이번 연구는 한국연구재단 기초연구사업(특히, 리더연구), KBSI, 국가과학기술연구회(NST), IBS 및 KAIST의 지원을 받아 진행됐다.
2023.11.20 조회수 7533 -
 심각한 염증 부작용 없앤 새로운 알츠하이머병 치료제 개발
우리 대학 생명과학과 김찬혁, 정원석 교수 공동연구팀이 알츠하이머병에 대한 새로운 형태의 단백질 치료제를 개발했다고 22일 밝혔다.
연구팀은 세포 포식작용에 관여하는 단백질을 응용한 `Gas6 융합단백질'을 제작하고 이를 통해 알츠하이머병을 유발하는 베타 아밀로이드 플라크(단백질 응집체)를 제거할 수 있는 새로운 형태의 치료제를 개발했다. 기존의 베타 아밀로이드를 표적으로 하는 항체 기반 치료제가 불확실한 치료 효과와 더불어 심각한 부작용을 일으키는 것이 보고되고 있는 가운데, 이를 근본적으로 극복할 수 있는 새로운 방식의 치료제를 연구팀은 제작한 것이다. 또한 해당 접근법은 향후 다양한 퇴행성 뇌 질환 및 자가면역질환 치료에 폭넓게 응용될 수 있을 것으로 기대된다.
생명과학과 박사과정 정현철, 이세영 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 메디슨 (Nature Medicine)' 8월 4일 字 온라인 출판됐다. (논문명 : Anti-inflammatory clearance of amyloid beta by a chimeric Gas6 fusion protein).
알츠하이머병은 기억상실과 인지장애를 동반하는 노인성 치매의 대표적 원인이다. 최근 국내 언론에 잘못 알려진 바와는 달리, 알츠하이머병은 뇌에 쌓이는 베타 아밀로이드 응집체 (비정상적으로 39~43개의 아미노산으로 잘려진 아밀로이드 조각들의 응집체)에 의한 시냅스 손상과 세포 독성으로 발병한다는 것이 학계 및 의료계의 정설이다. 이러한 정설에 의구심이 일었던 것은 아직까지 수많은 노력에도 불구하고 베타 아밀로이드를 제거하는 알츠하이머병 치료제가 성공적으로 개발되지 못했기 때문이었다. 최근 베타 아밀로이드를 표적으로 하는 항체 기반 치료제인 아두헬름이 사상 처음으로 알츠하이머병의 근원 치료제로써 2021년 6월 미국에서 FDA 승인이 이뤄졌으나, 치료 효과 및 부작용에 관한 논란이 여전히 지속되고 있다.
아두헬름과 같은 항체 기반의 치료제를 처방받은 알츠하이머병 환자들에게서 나타나는 가장 큰 부작용은 뇌 부종 (ARIA-E) 및 뇌 미세혈관출혈 (ARIA-H)이다. 이러한 부작용은 뇌 염증과 밀접하게 관련돼 있는데, 이는 항체 기반 치료제들이 면역세포에서 발현되는 Fc 수용체를 통해 필연적으로 염증반응을 일으키기 때문으로 알려져 있다. 이 Fc 수용체는 다른 한편으로는 면역세포가 항체에 의한 포식작용을 통해 베타 아밀로이드 응집체를 제거하는데 필수적인 기능을 한다. 따라서 심각한 염증 부작용을 근본적으로 예방하면서 베타 아밀로이드 응집체를 효과적으로 제거하는 치료제를 개발하는 것은 알츠하이머병 치료의 오랜 딜레마였다.
연구팀은 이러한 문제를 기존 항체의 틀에서 벗어나 새로운 기전의 단백질 치료제를 디자인함으로써 해결했다. 우리 몸에는 끊임없이 죽어 나가는 세포들을 제거하기 위한 특수한 포식작용 경로가 존재하는데, 연구팀은 이에 관여하는 Gas6라는 단백질을 인위적으로 조작해 베타 아밀로이드를 표적으로 하는 융합단백질을 제작했다. 연구팀은 실험을 통해 이 융합단백질(anti-Abeta-Gas6)이 뇌 안에서 선택적으로 베타 아밀로이드를 제거함과 동시에 염증반응을 오히려 억제한다는 것을 증명했다.
또한 알츠하이머 질병 쥐 모델을 통해 연구팀이 개발한 융합단백질이 미세아교세포와 별아교세포를 동시에 활용해 뇌 속에 축적된 베타 아밀로이드의 양을 현저하게 줄이는 것을 발견했다. 이는 기존의 항체 치료제가 미세아교세포를 통해서만 베타 아밀로이드를 줄일 수 있는 것에 비해 뚜렷한 이점으로 보인다. 동시에 연구팀은 Gas6 융합단백질이 항체 치료제에 의해서 더 악화되는 미세아교세포에 의한 과도한 시냅스 제거 현상을 획기적으로 억제할 수 있음을 밝혔다. 더 나아가, Gas6 융합단백질을 주입한 알츠하이머 질병 쥐 모델에서는 손상된 인지능력 및 기억력이 항체 치료제보다도 높은 수준으로 회복되는 결과도 확인했다.
추가로 기존의 항체 기반 치료제를 처방받은 알츠하이머 환자에게서 나타났던 부작용인 뇌 미세혈관 출혈도, Gas6 융합단백질을 주입한 알츠하이머 질병 쥐 모델에서는 현저하게 감소하는 것을 연구팀은 증명했다.
따라서 연구팀이 개발한 융합단백질은 새로운 형태의 작용기전을 적용한 최초의 알츠하이머 질병 치료제이며, 이러한 형태의 치료제는 다양한 퇴행성 뇌 질환 및 자가 면역질환에 적용될 수 있을 것으로 기대된다.
연구팀은 "지금까지 많은 항체 기반 치료제가 성공하지 못했던 이유는 뇌 조직 및 혈관에 쌓이는 베타 아밀로이드가 올바른 방식으로 청소되지 않았기 때문ˮ이라며 "Gas6 융합단백질을 통해서는 베타 아밀로이드가 염증반응 없이 청소되기 때문에 부작용이 낮을 뿐만 아니라 높은 인지기능의 향상도 기대할 수 있을 것ˮ이라고 말했다.
연구팀은 이번 Gas6 융합단백질 치료기술을 기반으로 2021년 8월에 일리미스테라퓨틱스(Illimis Therapeutics, 대표이사: 박상훈)를 설립했고, 향후 이를 통해 베타 아밀로이드를 표적으로 하는 알츠하이머 치료제(GAIA-Abeta, ILM01) 개발뿐 아니라, 표적을 타우 등으로 치환하는 치료제도 개발하여 다양한 확장 및 임상 개발을 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 사업(프렙과제) 및 치매극복연구개발사업단 (KDRC, 단장: 묵인희)의 지원을 받아 수행됐다.
2022.08.22 조회수 10425
심각한 염증 부작용 없앤 새로운 알츠하이머병 치료제 개발
우리 대학 생명과학과 김찬혁, 정원석 교수 공동연구팀이 알츠하이머병에 대한 새로운 형태의 단백질 치료제를 개발했다고 22일 밝혔다.
연구팀은 세포 포식작용에 관여하는 단백질을 응용한 `Gas6 융합단백질'을 제작하고 이를 통해 알츠하이머병을 유발하는 베타 아밀로이드 플라크(단백질 응집체)를 제거할 수 있는 새로운 형태의 치료제를 개발했다. 기존의 베타 아밀로이드를 표적으로 하는 항체 기반 치료제가 불확실한 치료 효과와 더불어 심각한 부작용을 일으키는 것이 보고되고 있는 가운데, 이를 근본적으로 극복할 수 있는 새로운 방식의 치료제를 연구팀은 제작한 것이다. 또한 해당 접근법은 향후 다양한 퇴행성 뇌 질환 및 자가면역질환 치료에 폭넓게 응용될 수 있을 것으로 기대된다.
생명과학과 박사과정 정현철, 이세영 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 메디슨 (Nature Medicine)' 8월 4일 字 온라인 출판됐다. (논문명 : Anti-inflammatory clearance of amyloid beta by a chimeric Gas6 fusion protein).
알츠하이머병은 기억상실과 인지장애를 동반하는 노인성 치매의 대표적 원인이다. 최근 국내 언론에 잘못 알려진 바와는 달리, 알츠하이머병은 뇌에 쌓이는 베타 아밀로이드 응집체 (비정상적으로 39~43개의 아미노산으로 잘려진 아밀로이드 조각들의 응집체)에 의한 시냅스 손상과 세포 독성으로 발병한다는 것이 학계 및 의료계의 정설이다. 이러한 정설에 의구심이 일었던 것은 아직까지 수많은 노력에도 불구하고 베타 아밀로이드를 제거하는 알츠하이머병 치료제가 성공적으로 개발되지 못했기 때문이었다. 최근 베타 아밀로이드를 표적으로 하는 항체 기반 치료제인 아두헬름이 사상 처음으로 알츠하이머병의 근원 치료제로써 2021년 6월 미국에서 FDA 승인이 이뤄졌으나, 치료 효과 및 부작용에 관한 논란이 여전히 지속되고 있다.
아두헬름과 같은 항체 기반의 치료제를 처방받은 알츠하이머병 환자들에게서 나타나는 가장 큰 부작용은 뇌 부종 (ARIA-E) 및 뇌 미세혈관출혈 (ARIA-H)이다. 이러한 부작용은 뇌 염증과 밀접하게 관련돼 있는데, 이는 항체 기반 치료제들이 면역세포에서 발현되는 Fc 수용체를 통해 필연적으로 염증반응을 일으키기 때문으로 알려져 있다. 이 Fc 수용체는 다른 한편으로는 면역세포가 항체에 의한 포식작용을 통해 베타 아밀로이드 응집체를 제거하는데 필수적인 기능을 한다. 따라서 심각한 염증 부작용을 근본적으로 예방하면서 베타 아밀로이드 응집체를 효과적으로 제거하는 치료제를 개발하는 것은 알츠하이머병 치료의 오랜 딜레마였다.
연구팀은 이러한 문제를 기존 항체의 틀에서 벗어나 새로운 기전의 단백질 치료제를 디자인함으로써 해결했다. 우리 몸에는 끊임없이 죽어 나가는 세포들을 제거하기 위한 특수한 포식작용 경로가 존재하는데, 연구팀은 이에 관여하는 Gas6라는 단백질을 인위적으로 조작해 베타 아밀로이드를 표적으로 하는 융합단백질을 제작했다. 연구팀은 실험을 통해 이 융합단백질(anti-Abeta-Gas6)이 뇌 안에서 선택적으로 베타 아밀로이드를 제거함과 동시에 염증반응을 오히려 억제한다는 것을 증명했다.
또한 알츠하이머 질병 쥐 모델을 통해 연구팀이 개발한 융합단백질이 미세아교세포와 별아교세포를 동시에 활용해 뇌 속에 축적된 베타 아밀로이드의 양을 현저하게 줄이는 것을 발견했다. 이는 기존의 항체 치료제가 미세아교세포를 통해서만 베타 아밀로이드를 줄일 수 있는 것에 비해 뚜렷한 이점으로 보인다. 동시에 연구팀은 Gas6 융합단백질이 항체 치료제에 의해서 더 악화되는 미세아교세포에 의한 과도한 시냅스 제거 현상을 획기적으로 억제할 수 있음을 밝혔다. 더 나아가, Gas6 융합단백질을 주입한 알츠하이머 질병 쥐 모델에서는 손상된 인지능력 및 기억력이 항체 치료제보다도 높은 수준으로 회복되는 결과도 확인했다.
추가로 기존의 항체 기반 치료제를 처방받은 알츠하이머 환자에게서 나타났던 부작용인 뇌 미세혈관 출혈도, Gas6 융합단백질을 주입한 알츠하이머 질병 쥐 모델에서는 현저하게 감소하는 것을 연구팀은 증명했다.
따라서 연구팀이 개발한 융합단백질은 새로운 형태의 작용기전을 적용한 최초의 알츠하이머 질병 치료제이며, 이러한 형태의 치료제는 다양한 퇴행성 뇌 질환 및 자가 면역질환에 적용될 수 있을 것으로 기대된다.
연구팀은 "지금까지 많은 항체 기반 치료제가 성공하지 못했던 이유는 뇌 조직 및 혈관에 쌓이는 베타 아밀로이드가 올바른 방식으로 청소되지 않았기 때문ˮ이라며 "Gas6 융합단백질을 통해서는 베타 아밀로이드가 염증반응 없이 청소되기 때문에 부작용이 낮을 뿐만 아니라 높은 인지기능의 향상도 기대할 수 있을 것ˮ이라고 말했다.
연구팀은 이번 Gas6 융합단백질 치료기술을 기반으로 2021년 8월에 일리미스테라퓨틱스(Illimis Therapeutics, 대표이사: 박상훈)를 설립했고, 향후 이를 통해 베타 아밀로이드를 표적으로 하는 알츠하이머 치료제(GAIA-Abeta, ILM01) 개발뿐 아니라, 표적을 타우 등으로 치환하는 치료제도 개발하여 다양한 확장 및 임상 개발을 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 사업(프렙과제) 및 치매극복연구개발사업단 (KDRC, 단장: 묵인희)의 지원을 받아 수행됐다.
2022.08.22 조회수 10425 -
 신경전달물질 소마토스타틴의 알츠하이머 독성 개선효과 발견
우리 대학 화학과 임미희 교수 연구팀, 생명과학과 이승희 교수 연구팀, 화학과 박기영 교수 연구팀이 단백질 기반 신경전달물질인 소마토스타틴(성장 억제 호르몬)이 알츠하이머 발병 메커니즘에서 독성을 개선할 수 있다는 새로운 역할을 발굴했다고 25일 밝혔다.
이 연구는 국제 저명 학술지인 `네이처 케미스트리(Nature Chemistry, Impact factor: 24.427, 화학 분야 상위 3.9%)'에 7월 게재됐다. (논문명: Conformational and functional changes of the native neuropeptide somatostatin occur in the presence of copper and amyloid-β)
전 세계적으로 치매 인구는 5,000만 명에 육박하고, 그중 알츠하이머병은 가장 흔한 신경퇴행성 질환으로 언어 구사 능력과 기억력 등 전반적인 사고 능력 손상이 대표적인 증상으로 여겨진다. 장노년 인구의 급격한 증가와 기대 수명 연장에 따라 치료제 개발의 중요성이 대두되고 있으나, 현재까지 그 발병 원인조차 명확하게 밝혀지지 않은 실상이다.
아밀로이드 가설에 따르면 아밀로이드 베타 단백질의 비정상적인 침적은 신경세포의 사멸을 일으킨다. 아밀로이드 베타 응집체는 섬유화를 거쳐 노인성 플라크의 대부분을 차지하는데, 최근 연구에 따르면 특히 알츠하이머 환자의 플라크에서 고농도의 전이 금속이 검출된다. 이는 금속 이온과 아밀로이드 베타 간의 긴밀한 상호작용 가능성을 시사한다. 금속 이온은 아밀로이드 베타와 상호작용해 단백질의 섬유화를 촉진하며, 특히 산화환원 활성 전이 금속인 구리의 경우에는 활성 산소를 다량 생성해 세포 소기관에 심각한 산화 스트레스를 일으킬 수 있다.
아밀로이드 베타 단백질과 전이 금속은 시냅스(신경세포 접합부)에서 신경전달물질과 밀접하게 상호작용할 수 있으나, 아직 이러한 병적 요인들이 신경전달물질의 구조 및 신호 전달 기능에 직접적으로 미치는 영향에 관해서는 자세히 연구된 바 없다.
연구팀은 구리, 아밀로이드 베타, 금속-아밀로이드 베타 복합체에 의해 단백질 기반 신경전달물질인 소마토스타틴이 자가 응집되는 동시에 세포 신호 전달과 같은 본연의 기능을 잃는 대신, 금속-아밀로이드 베타의 응집과 독성을 조절한다는 연구 내용을 발표했다.
화학과 한지연 박사가 제1 저자로 참여한 이번 연구는 구리와 소마토스타틴의 배위 구조 후보군을 분자적 수준에서 밝혀 응집 메커니즘을 제안하고, 소마토스타틴이 아밀로이드 베타의 응집 경로에 미치는 영향을 금속의 유무에 따라 규명했다. 더 나아가 실제 신경모세포종에서 소마토스타틴의 수용체 결합, 세포막 상호 작용, 세포 독성 변화를 최초로 입증하여 세계적으로 주목받고 있다.
임미희 교수는 “이번 연구 결과는 알츠하이머 질환의 발병 기전 내 신경전달물질의 새로운 역할을 규명한 데에 큰 의의가 있다”고 말하며, “이 연구 성과는 노화에 의한 신경퇴행성 질환의 병적 네트워크를 규명하는 데에 실마리를 제공하고, 향후 바이오마커 및 치료제 개발에도 크게 기여할 것으로 기대된다”고 밝혔다.
한편 이번 연구는 한국연구재단 기초연구사업과 KAIST의 지원을 받아 진행됐다.
2022.07.25 조회수 8185
신경전달물질 소마토스타틴의 알츠하이머 독성 개선효과 발견
우리 대학 화학과 임미희 교수 연구팀, 생명과학과 이승희 교수 연구팀, 화학과 박기영 교수 연구팀이 단백질 기반 신경전달물질인 소마토스타틴(성장 억제 호르몬)이 알츠하이머 발병 메커니즘에서 독성을 개선할 수 있다는 새로운 역할을 발굴했다고 25일 밝혔다.
이 연구는 국제 저명 학술지인 `네이처 케미스트리(Nature Chemistry, Impact factor: 24.427, 화학 분야 상위 3.9%)'에 7월 게재됐다. (논문명: Conformational and functional changes of the native neuropeptide somatostatin occur in the presence of copper and amyloid-β)
전 세계적으로 치매 인구는 5,000만 명에 육박하고, 그중 알츠하이머병은 가장 흔한 신경퇴행성 질환으로 언어 구사 능력과 기억력 등 전반적인 사고 능력 손상이 대표적인 증상으로 여겨진다. 장노년 인구의 급격한 증가와 기대 수명 연장에 따라 치료제 개발의 중요성이 대두되고 있으나, 현재까지 그 발병 원인조차 명확하게 밝혀지지 않은 실상이다.
아밀로이드 가설에 따르면 아밀로이드 베타 단백질의 비정상적인 침적은 신경세포의 사멸을 일으킨다. 아밀로이드 베타 응집체는 섬유화를 거쳐 노인성 플라크의 대부분을 차지하는데, 최근 연구에 따르면 특히 알츠하이머 환자의 플라크에서 고농도의 전이 금속이 검출된다. 이는 금속 이온과 아밀로이드 베타 간의 긴밀한 상호작용 가능성을 시사한다. 금속 이온은 아밀로이드 베타와 상호작용해 단백질의 섬유화를 촉진하며, 특히 산화환원 활성 전이 금속인 구리의 경우에는 활성 산소를 다량 생성해 세포 소기관에 심각한 산화 스트레스를 일으킬 수 있다.
아밀로이드 베타 단백질과 전이 금속은 시냅스(신경세포 접합부)에서 신경전달물질과 밀접하게 상호작용할 수 있으나, 아직 이러한 병적 요인들이 신경전달물질의 구조 및 신호 전달 기능에 직접적으로 미치는 영향에 관해서는 자세히 연구된 바 없다.
연구팀은 구리, 아밀로이드 베타, 금속-아밀로이드 베타 복합체에 의해 단백질 기반 신경전달물질인 소마토스타틴이 자가 응집되는 동시에 세포 신호 전달과 같은 본연의 기능을 잃는 대신, 금속-아밀로이드 베타의 응집과 독성을 조절한다는 연구 내용을 발표했다.
화학과 한지연 박사가 제1 저자로 참여한 이번 연구는 구리와 소마토스타틴의 배위 구조 후보군을 분자적 수준에서 밝혀 응집 메커니즘을 제안하고, 소마토스타틴이 아밀로이드 베타의 응집 경로에 미치는 영향을 금속의 유무에 따라 규명했다. 더 나아가 실제 신경모세포종에서 소마토스타틴의 수용체 결합, 세포막 상호 작용, 세포 독성 변화를 최초로 입증하여 세계적으로 주목받고 있다.
임미희 교수는 “이번 연구 결과는 알츠하이머 질환의 발병 기전 내 신경전달물질의 새로운 역할을 규명한 데에 큰 의의가 있다”고 말하며, “이 연구 성과는 노화에 의한 신경퇴행성 질환의 병적 네트워크를 규명하는 데에 실마리를 제공하고, 향후 바이오마커 및 치료제 개발에도 크게 기여할 것으로 기대된다”고 밝혔다.
한편 이번 연구는 한국연구재단 기초연구사업과 KAIST의 지원을 받아 진행됐다.
2022.07.25 조회수 8185 -
 저주파 자기장 반응성 나노입자 개발해 알츠하이머 원인물질 분해 성공
우리 대학 신소재공학과 박찬범 교수 연구팀이 저주파 자기장 반응성 나노입자를 개발하는 데 성공했다고 16일 밝혔다. 연구팀은 이를 이용해 알츠하이머질환을 유발하는 베타-아밀로이드 펩타이드(아미노산 화합물) 응집체를 자기장으로 분해할 수 있다고 밝혔다.
신소재공학과 장진형 박사과정이 제1 저자로 참여한 이번 연구는 국제학술지 `사이언스 어드밴시스(Science Advances)' 5월 13일 字에 게재됐다. (논문명: Magnetoelectric dissociation of Alzheimer's β-amyloid aggregates)
자기 전기(Magnetoelectric) 소재는 자성과 전기성이 결합한 물성을 가지며 스핀트로닉스(Spintronics) 소자, 트랜스듀서(Transducer) 등 다양한 전자기기를 구성하는 핵심 물질이다. 그러나 자기 전기 소재는 원자 내 전자의 회전과 궤도 운동을 방해하는 양성자의 정전기적 상호작용(스핀-오빗 상호작용)으로 인해 성능 향상에 한계를 지닌다.
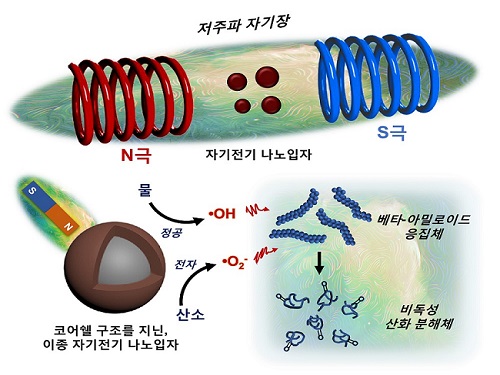
연구팀은 자기 전기 소재의 일종이며, 반도체 및 배터리 분야에 주로 쓰이는 코발트 페라이트(Cobalt ferrite)와 비스무스 페라이트(Bismuth ferrite)를 코어쉘(Core-shell) 구조로 접합시킴으로써 이종(Heterogeneous) 자기 전기 나노입자를 개발했다. 서로 다른 자기 전기 소재의 균일한 접합을 통해 이들의 경계면에서 저주파 자기장에 반응하는 자기-압전효과(Magneto-piezoelectric effect)를 일으킬 수 있었다.
특히, 나노입자가 저주파 자기장에 반응해 전하 운반체를 생성할 때 열을 방출하지 않는 현상에 연구팀은 주목했다. 자기장은 뇌 조직을 손상 없이 투과할 수 있으며 자기공명영상(MRI, Magnetic Resonance Imaging) 등에서 활용돼 의료적 안전성이 이미 검증된 바가 있다.
연구팀이 개발한 나노입자에 저주파 자기장을 쏘았을 때 베타-아밀로이드 펩타이드(Beta-amyloid peptide)를 산화시킴으로써 그 응집체의 결합력을 약화시켜 분해했고, 신경독성도 중화시킬 수 있음을 연구팀은 관찰했다.
아밀로이드 응집체는 알츠하이머병 등 다양한 퇴행성 신경질환들에서 공통적으로 관찰되며, 규칙적인 수소 결합을 통해 매우 안정적인 단백질 이차구조(Secondary structure)를 가져 분해가 어렵다고 알려져 왔다.
박찬범 교수는 "저주파 자기장 반응성 나노소재는 독성이 낮으며 자기장과 반응해 아밀로이드 응집체를 효율적으로 분해할 수 있기에 의료분야로 확장할 수 있는 잠재력이 있다ˮ면서, "이를 검증하기 위해 향후 알츠하이머 형질변환 마우스 등을 이용한 동물실험 등이 우선적으로 필요하다ˮ고 말했다.
한편 이번 연구는 한편 이번 연구는 과학기술정보통신부 리더연구자지원사업(창의연구)의 지원을 받아 수행됐다.
2022.05.16 조회수 9182
저주파 자기장 반응성 나노입자 개발해 알츠하이머 원인물질 분해 성공
우리 대학 신소재공학과 박찬범 교수 연구팀이 저주파 자기장 반응성 나노입자를 개발하는 데 성공했다고 16일 밝혔다. 연구팀은 이를 이용해 알츠하이머질환을 유발하는 베타-아밀로이드 펩타이드(아미노산 화합물) 응집체를 자기장으로 분해할 수 있다고 밝혔다.
신소재공학과 장진형 박사과정이 제1 저자로 참여한 이번 연구는 국제학술지 `사이언스 어드밴시스(Science Advances)' 5월 13일 字에 게재됐다. (논문명: Magnetoelectric dissociation of Alzheimer's β-amyloid aggregates)
자기 전기(Magnetoelectric) 소재는 자성과 전기성이 결합한 물성을 가지며 스핀트로닉스(Spintronics) 소자, 트랜스듀서(Transducer) 등 다양한 전자기기를 구성하는 핵심 물질이다. 그러나 자기 전기 소재는 원자 내 전자의 회전과 궤도 운동을 방해하는 양성자의 정전기적 상호작용(스핀-오빗 상호작용)으로 인해 성능 향상에 한계를 지닌다.
연구팀은 자기 전기 소재의 일종이며, 반도체 및 배터리 분야에 주로 쓰이는 코발트 페라이트(Cobalt ferrite)와 비스무스 페라이트(Bismuth ferrite)를 코어쉘(Core-shell) 구조로 접합시킴으로써 이종(Heterogeneous) 자기 전기 나노입자를 개발했다. 서로 다른 자기 전기 소재의 균일한 접합을 통해 이들의 경계면에서 저주파 자기장에 반응하는 자기-압전효과(Magneto-piezoelectric effect)를 일으킬 수 있었다.
특히, 나노입자가 저주파 자기장에 반응해 전하 운반체를 생성할 때 열을 방출하지 않는 현상에 연구팀은 주목했다. 자기장은 뇌 조직을 손상 없이 투과할 수 있으며 자기공명영상(MRI, Magnetic Resonance Imaging) 등에서 활용돼 의료적 안전성이 이미 검증된 바가 있다.
연구팀이 개발한 나노입자에 저주파 자기장을 쏘았을 때 베타-아밀로이드 펩타이드(Beta-amyloid peptide)를 산화시킴으로써 그 응집체의 결합력을 약화시켜 분해했고, 신경독성도 중화시킬 수 있음을 연구팀은 관찰했다.
아밀로이드 응집체는 알츠하이머병 등 다양한 퇴행성 신경질환들에서 공통적으로 관찰되며, 규칙적인 수소 결합을 통해 매우 안정적인 단백질 이차구조(Secondary structure)를 가져 분해가 어렵다고 알려져 왔다.
박찬범 교수는 "저주파 자기장 반응성 나노소재는 독성이 낮으며 자기장과 반응해 아밀로이드 응집체를 효율적으로 분해할 수 있기에 의료분야로 확장할 수 있는 잠재력이 있다ˮ면서, "이를 검증하기 위해 향후 알츠하이머 형질변환 마우스 등을 이용한 동물실험 등이 우선적으로 필요하다ˮ고 말했다.
한편 이번 연구는 한편 이번 연구는 과학기술정보통신부 리더연구자지원사업(창의연구)의 지원을 받아 수행됐다.
2022.05.16 조회수 9182 -
 하이드로젤 기반 유연성 뇌-기계 인터페이스 개발
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이 메사추세츠 공과대학(MIT) 폴리나 아니키바(Polina Anikeeva) 교수, 쏸허 자오(Xuanhe Zhao) 교수, 육현우 박사 공동 연구팀과 함께 *하이드로젤 기반의 유연성 뇌-기계 인터페이스를 개발하는 데 성공했다고 21일 밝혔다.
☞ 하이드로젤: 물과 젤리가 합쳐진 합성어이며 주로 필러, 보톡스, 화장품에 쓰이는 반고체 상태의 물질이다. 인공적인 인체 조직을 만드는 원료로 적합해 의학적으로도 널리 쓰인다.
이번 연구 결과는 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)'에 2021년 6월 8일 字로 출판됐다. (논문명: Adaptive and multifunctional hydrogel hybrid probes for long-term sensing and modulation of neural activity)
뇌 구조를 연구하거나 뇌 신경 질환의 메커니즘을 파악, 치료하기 위해서는, 실시간으로 뇌를 자극하고 신호를 측정할 수 있는 인터페이스의 개발이 필수적이다. 그러나 기존의 신경 인터페이스는 기계적, 화학적 특성이 뇌 조직과 너무 달라서 일어나는 이물 반응(foreign body response) 때문에, 주변에 절연세포층이 형성돼 그 수명이 매우 짧아진다는 문제점을 가지고 있었다.
연구팀은 해당 문제의 해결을 위해, 직접 제작한 다기능성 파이버 다발을 하이드로젤 몸체에 넣는 방법을 이용해 `뇌 모사형 신경 인터페이스'를 제작했다. 해당 장치는 빛으로 특정 신경세포종만을 자극할 수 있는 광유전학 기술을 적용하기 위한 광섬유뿐만 아니라, 뇌에서 신호를 읽을 수 있는 전극 다발, 약물을 뇌 속으로 전달할 수 있는 미세 유체 채널을 모두 보유하고 있다.
해당 인터페이스는 하이드로젤 몸체를 건조시킨 상태에서는 단단한 성질이 고분자와 유사해 몸체에 삽입하기가 쉽다. 하지만 몸에 들어가면 체내의 수분을 빠르게 흡수해. 부드럽고 수분이 풍부한 주변 조직과 유사한 상태가 되므로 이물 반응을 최소화할 수 있다.
연구팀은 이러한 특성을 가진 장치를 동물 모델에 직접 적용해, 기존의 기록을 훨씬 뛰어넘는 삽입 후 6개월까지도 뇌 신호를 측정할 수 있음을 보였다. 또한 자유롭게 움직이는 쥐를 대상으로 초장기간 광유전학 실험, 행동 실험 등이 가능하며, 이물 반응에 의한 아교세포 및 면역세포의 발현이 기존 장치보다 현저히 줄어듦을 증명했다.
박성준 교수는 "이번 연구는 최초로 하이드로젤을 다기능 신경 인터페이스의 구성물질로 사용해 그 수명을 대폭 상승시켰다는 데에 의의가 있으며, 해당 연구를 통해 향후 알츠하이머병, 파킨슨병 등 초장기간 관찰이 필요한 뇌 신경 질환 연구가 더욱 발전할 수 있을 것으로 기대된다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 신진연구사업, 범부처의료기기개발 사업, 나노소재원천기술개발사업, 차세대 지능형 반도체 개발사업, KK-JRC 스마트 프로젝트, 카이스트 글로벌 이니셔티브 프로그램, 포스트 인공지능(Post-AI) 프로젝트 사업의 지원을 받아 수행됐다.
2021.06.21 조회수 32681
하이드로젤 기반 유연성 뇌-기계 인터페이스 개발
우리 대학 바이오및뇌공학과 박성준 교수 연구팀이 메사추세츠 공과대학(MIT) 폴리나 아니키바(Polina Anikeeva) 교수, 쏸허 자오(Xuanhe Zhao) 교수, 육현우 박사 공동 연구팀과 함께 *하이드로젤 기반의 유연성 뇌-기계 인터페이스를 개발하는 데 성공했다고 21일 밝혔다.
☞ 하이드로젤: 물과 젤리가 합쳐진 합성어이며 주로 필러, 보톡스, 화장품에 쓰이는 반고체 상태의 물질이다. 인공적인 인체 조직을 만드는 원료로 적합해 의학적으로도 널리 쓰인다.
이번 연구 결과는 국제 학술지 `네이처 커뮤니케이션즈(Nature Communications)'에 2021년 6월 8일 字로 출판됐다. (논문명: Adaptive and multifunctional hydrogel hybrid probes for long-term sensing and modulation of neural activity)
뇌 구조를 연구하거나 뇌 신경 질환의 메커니즘을 파악, 치료하기 위해서는, 실시간으로 뇌를 자극하고 신호를 측정할 수 있는 인터페이스의 개발이 필수적이다. 그러나 기존의 신경 인터페이스는 기계적, 화학적 특성이 뇌 조직과 너무 달라서 일어나는 이물 반응(foreign body response) 때문에, 주변에 절연세포층이 형성돼 그 수명이 매우 짧아진다는 문제점을 가지고 있었다.
연구팀은 해당 문제의 해결을 위해, 직접 제작한 다기능성 파이버 다발을 하이드로젤 몸체에 넣는 방법을 이용해 `뇌 모사형 신경 인터페이스'를 제작했다. 해당 장치는 빛으로 특정 신경세포종만을 자극할 수 있는 광유전학 기술을 적용하기 위한 광섬유뿐만 아니라, 뇌에서 신호를 읽을 수 있는 전극 다발, 약물을 뇌 속으로 전달할 수 있는 미세 유체 채널을 모두 보유하고 있다.
해당 인터페이스는 하이드로젤 몸체를 건조시킨 상태에서는 단단한 성질이 고분자와 유사해 몸체에 삽입하기가 쉽다. 하지만 몸에 들어가면 체내의 수분을 빠르게 흡수해. 부드럽고 수분이 풍부한 주변 조직과 유사한 상태가 되므로 이물 반응을 최소화할 수 있다.
연구팀은 이러한 특성을 가진 장치를 동물 모델에 직접 적용해, 기존의 기록을 훨씬 뛰어넘는 삽입 후 6개월까지도 뇌 신호를 측정할 수 있음을 보였다. 또한 자유롭게 움직이는 쥐를 대상으로 초장기간 광유전학 실험, 행동 실험 등이 가능하며, 이물 반응에 의한 아교세포 및 면역세포의 발현이 기존 장치보다 현저히 줄어듦을 증명했다.
박성준 교수는 "이번 연구는 최초로 하이드로젤을 다기능 신경 인터페이스의 구성물질로 사용해 그 수명을 대폭 상승시켰다는 데에 의의가 있으며, 해당 연구를 통해 향후 알츠하이머병, 파킨슨병 등 초장기간 관찰이 필요한 뇌 신경 질환 연구가 더욱 발전할 수 있을 것으로 기대된다ˮ 라고 말했다.
한편 이번 연구는 한국연구재단 신진연구사업, 범부처의료기기개발 사업, 나노소재원천기술개발사업, 차세대 지능형 반도체 개발사업, KK-JRC 스마트 프로젝트, 카이스트 글로벌 이니셔티브 프로그램, 포스트 인공지능(Post-AI) 프로젝트 사업의 지원을 받아 수행됐다.
2021.06.21 조회수 32681 -
 초고감도 생체 분자 검출용 디지털 라만 분광 기술 개발
우리 대학 바이오및뇌공학과 정기훈 교수 연구팀이 생체 분자의 광학 검출의 기술적 장벽인 신호대잡음비를 1,000배 이상, 검출한계를 기존 대비 10억 배인 아토몰(10-18 mole) 단위까지 향상시키는 디지털 코드 *라만 분광 기술을 세계 최초로 개발했다고 15일 밝혔다.
☞ 라만 분광법(Raman spectroscopy): 특정 분자에 레이저를 쏘았을 때, 그 분자 전자의 에너지준위 차이만큼 에너지를 흡수하는 현상을 통해 분자의 종류를 알아내는 방법이다.
연구진은 통신 분야에서 잘 알려진 대역 확산기술(CDMA)을 생분자화합물의 라만 분광 검출법에 세계 최초로 적용했다. 디지털 코드화된 레이저광원을 이용해 모든 잡음신호를 제거하고, 생화합물의 고순도 라만 분광 신호를 복원함으로써, 극저농도의 생분자화합물을 형광 표지 없이 정확하게 분석했다. 이러한 디지털 코드 라만 분광 기술은 다양한 분자진단, 약물 및 암 치료 모니터링뿐 아니라 현장 진단용 광학 진단기기나 모바일 헬스케어 기기에도 활용이 가능할 것으로 크게 기대된다.
우리 대학 바이오및뇌공학과 이원경 박사과정이 제 1저자로 참여한 이번 연구는 세계적 권위의 과학전문지 `네이처(nature)'의 자매지인 `네이처 커뮤니케이션스(Nature Communications)'에 1월 8일 字 온라인판에 발표됐다. (논문명: Spread Spectrum SERS allows label-free detection of attomolar neurotransmitters)
알츠하이머병, 파킨슨병, 우울증 등의 뇌세포와 관련된 신경 질환은 뇌세포에서 만들어지는 신경전달물질이 적절히 분비되지 않거나 불균형으로 분비돼 발생하는 질병으로, 최근에는 발병과 직간접적인 사망자가 급증하고 있으나 치료가 쉽지 않다. 신경전달물질은 뉴런의 축색 돌기 말단에서 분비돼 시냅스 갭을 통과한 후 다른 뉴런에 신호를 전달하는 물질로, 결합하는 수용체의 화학적 성질에 따라 기능이 다르고, 발생하는 질병도 다양하다.
알츠하이머병 환자들은 신경전달물질 가운데 아세틸콜린이 부족하거나 글루탐산염이 높은 특징이 있고, 도파민이 부족하면 몸이 굳어지며 떨리는 파킨슨병에 걸리기 쉽고 조현병이나 주의력 결핍 과잉 행동장애와 같은 정신질환의 원인이 된다. 신경전달물질과 관련된 신경 질환은 특정 수용체 작용제나 수용체 길항체로 치료를 하는데, 효과는 그다지 성공적이지 않다. 따라서 알츠하이머병이나 파킨슨병과 같은 신경 질환의 조기 진단을 위해서 적절한 신경전달물질의 적절한 분비를 위한 지속적인 신경전달물질 농도 변화를 모니터링하는 것이 매우 중요하다.
극저농도의 신경전달물질을 간편하면서도 정확하게 측정할 수 있다면 신경계 질환의 조기 진단율을 크게 높일 수 있고 신경 질환 환자의 치료 추적 관리에 큰 도움을 줄 수 있다. 하지만 신경전달물질 기반의 기존 신경 질환 진단기술은 양전자 방출 단층촬영(PET), 표면증강라만분광(SERS), 고성능 액체 크로마토그래피(HPLC), 형광 표지 기반 센서로 측정해 분석하는 방식이다. 이러한 기존 신경 질환 진단기술은 검출한계가 나노몰(10-9 mole) 이상에 그치며, 시료 전처리 단계가 복잡하고 측정 시간이 오래 걸리는 한계가 있다.
연구팀은 문제 해결을 위해 대역확산 통신기술의 뛰어난 잡음 제거 기술을 생체 분자 검출에 적용해 레이저 출력 변동, 수신기 자체 잡음 등의 시스템 잡음과 표적 분자 이외의 분자 신호를 효율적으로 제거하고 표적 생체 분자 신호만 선택적으로 복원했다. 그 결과 생체 분자 신호의 신호대잡음비를 증가시켜 더욱 정밀한 검출한계를 달성했다.
대역확산 기반 디지털 코드 분광 기술은 직교성을 가지는 확산 코드로 암호화된 빛으로 생체 분자를 높은 에너지로 이동시켜 생체 분자에서 산란돼 나오는 빛을 다시 확산 코드로 복호화한다. 이러한 과정을 거쳐 표적 생체 분자의 산란 신호를 복원해 질병 및 건강 진단 지표, 유전 물질 검출 등에 응용할 수 있다.
또한 직교성을 가지는 확산 코드는 기존의 다른 신호처리 기술보다 잡음을 제거하는 성능이 우수해 신호대잡음비와 검출한계, 시간해상도를 최고 수준으로 끌어올릴 수 있다.
연구팀이 개발한 대역확산 라만 분광 기술은 물질의 고유진동 지문을 측정하는 성분 분석과 전처리가 필요하지 않다는 라만 분광 기술의 장점을 그대로 유지하면서 기존의 기술적 한계인 낮은 신호대잡음비와 검출한계를 극복하는 기술로, 바이오 이미징, 현미경, 바이오 마커 센서, 약물 모니터링, 암 조직 검사 등의 다양한 분야에 활용될 수 있다.
연구팀은 대역확산 분광 기술과 표면증강 라만 분광법(Surface-enhanced Raman spectroscopy)을 접목시켜 별도의 표지 없이도 5종의 신경전달물질을 아토 몰 농도에서 검출해 기존 검출한계를 10억(109)배 향상시켰으며, 신호대잡음비가 1,000배 이상 증가함을 확인했다.
제1 저자인 이원경 박사과정은 "고감도 분자 진단을 위해 통신 분야의 최첨단 기술인 대역확산 기술을 접목한 차세대 디지털 코드 라만 분광 기술을 최초로 제안했으며, 이 방법으로 기존 생체 분자 검출 기술의 장벽을 해결하고 기존 기술의 신경전달물질 검출한계를 획기적으로 향상시켰다ˮ며 "고감도 소형 분광기로 신속하고 간단하게 현장 진단이 가능하고 다양한 분야에 활용될 수 있어 파급효과가 크다ˮ고 말했다.
정기훈 교수는 "이번 결과를 바탕으로 향후 휴대용으로 소형화를 진행하면 낮은 비용으로 무표지 초고감도 생체 분자 분석 및 신속한 현장 진단이 가능해질 것이다ˮ며 "또한 신경전달물질뿐 아니라 다양한 생화합물 검출, 바이러스 검출, 신약평가분야에 크게 활용될수 있을 것이다ˮ고 말했다.
한편, 이번 연구는 한국연구재단 바이오기술개발사업, KAIST 코로나대응 과학기술뉴딜사업단과 범부처 전주기 의료기기 사업, 과학기술정보통신부 ETRI 연구개발지원사업의 지원을 받아 수행됐다.
2021.01.18 조회수 79790
초고감도 생체 분자 검출용 디지털 라만 분광 기술 개발
우리 대학 바이오및뇌공학과 정기훈 교수 연구팀이 생체 분자의 광학 검출의 기술적 장벽인 신호대잡음비를 1,000배 이상, 검출한계를 기존 대비 10억 배인 아토몰(10-18 mole) 단위까지 향상시키는 디지털 코드 *라만 분광 기술을 세계 최초로 개발했다고 15일 밝혔다.
☞ 라만 분광법(Raman spectroscopy): 특정 분자에 레이저를 쏘았을 때, 그 분자 전자의 에너지준위 차이만큼 에너지를 흡수하는 현상을 통해 분자의 종류를 알아내는 방법이다.
연구진은 통신 분야에서 잘 알려진 대역 확산기술(CDMA)을 생분자화합물의 라만 분광 검출법에 세계 최초로 적용했다. 디지털 코드화된 레이저광원을 이용해 모든 잡음신호를 제거하고, 생화합물의 고순도 라만 분광 신호를 복원함으로써, 극저농도의 생분자화합물을 형광 표지 없이 정확하게 분석했다. 이러한 디지털 코드 라만 분광 기술은 다양한 분자진단, 약물 및 암 치료 모니터링뿐 아니라 현장 진단용 광학 진단기기나 모바일 헬스케어 기기에도 활용이 가능할 것으로 크게 기대된다.
우리 대학 바이오및뇌공학과 이원경 박사과정이 제 1저자로 참여한 이번 연구는 세계적 권위의 과학전문지 `네이처(nature)'의 자매지인 `네이처 커뮤니케이션스(Nature Communications)'에 1월 8일 字 온라인판에 발표됐다. (논문명: Spread Spectrum SERS allows label-free detection of attomolar neurotransmitters)
알츠하이머병, 파킨슨병, 우울증 등의 뇌세포와 관련된 신경 질환은 뇌세포에서 만들어지는 신경전달물질이 적절히 분비되지 않거나 불균형으로 분비돼 발생하는 질병으로, 최근에는 발병과 직간접적인 사망자가 급증하고 있으나 치료가 쉽지 않다. 신경전달물질은 뉴런의 축색 돌기 말단에서 분비돼 시냅스 갭을 통과한 후 다른 뉴런에 신호를 전달하는 물질로, 결합하는 수용체의 화학적 성질에 따라 기능이 다르고, 발생하는 질병도 다양하다.
알츠하이머병 환자들은 신경전달물질 가운데 아세틸콜린이 부족하거나 글루탐산염이 높은 특징이 있고, 도파민이 부족하면 몸이 굳어지며 떨리는 파킨슨병에 걸리기 쉽고 조현병이나 주의력 결핍 과잉 행동장애와 같은 정신질환의 원인이 된다. 신경전달물질과 관련된 신경 질환은 특정 수용체 작용제나 수용체 길항체로 치료를 하는데, 효과는 그다지 성공적이지 않다. 따라서 알츠하이머병이나 파킨슨병과 같은 신경 질환의 조기 진단을 위해서 적절한 신경전달물질의 적절한 분비를 위한 지속적인 신경전달물질 농도 변화를 모니터링하는 것이 매우 중요하다.
극저농도의 신경전달물질을 간편하면서도 정확하게 측정할 수 있다면 신경계 질환의 조기 진단율을 크게 높일 수 있고 신경 질환 환자의 치료 추적 관리에 큰 도움을 줄 수 있다. 하지만 신경전달물질 기반의 기존 신경 질환 진단기술은 양전자 방출 단층촬영(PET), 표면증강라만분광(SERS), 고성능 액체 크로마토그래피(HPLC), 형광 표지 기반 센서로 측정해 분석하는 방식이다. 이러한 기존 신경 질환 진단기술은 검출한계가 나노몰(10-9 mole) 이상에 그치며, 시료 전처리 단계가 복잡하고 측정 시간이 오래 걸리는 한계가 있다.
연구팀은 문제 해결을 위해 대역확산 통신기술의 뛰어난 잡음 제거 기술을 생체 분자 검출에 적용해 레이저 출력 변동, 수신기 자체 잡음 등의 시스템 잡음과 표적 분자 이외의 분자 신호를 효율적으로 제거하고 표적 생체 분자 신호만 선택적으로 복원했다. 그 결과 생체 분자 신호의 신호대잡음비를 증가시켜 더욱 정밀한 검출한계를 달성했다.
대역확산 기반 디지털 코드 분광 기술은 직교성을 가지는 확산 코드로 암호화된 빛으로 생체 분자를 높은 에너지로 이동시켜 생체 분자에서 산란돼 나오는 빛을 다시 확산 코드로 복호화한다. 이러한 과정을 거쳐 표적 생체 분자의 산란 신호를 복원해 질병 및 건강 진단 지표, 유전 물질 검출 등에 응용할 수 있다.
또한 직교성을 가지는 확산 코드는 기존의 다른 신호처리 기술보다 잡음을 제거하는 성능이 우수해 신호대잡음비와 검출한계, 시간해상도를 최고 수준으로 끌어올릴 수 있다.
연구팀이 개발한 대역확산 라만 분광 기술은 물질의 고유진동 지문을 측정하는 성분 분석과 전처리가 필요하지 않다는 라만 분광 기술의 장점을 그대로 유지하면서 기존의 기술적 한계인 낮은 신호대잡음비와 검출한계를 극복하는 기술로, 바이오 이미징, 현미경, 바이오 마커 센서, 약물 모니터링, 암 조직 검사 등의 다양한 분야에 활용될 수 있다.
연구팀은 대역확산 분광 기술과 표면증강 라만 분광법(Surface-enhanced Raman spectroscopy)을 접목시켜 별도의 표지 없이도 5종의 신경전달물질을 아토 몰 농도에서 검출해 기존 검출한계를 10억(109)배 향상시켰으며, 신호대잡음비가 1,000배 이상 증가함을 확인했다.
제1 저자인 이원경 박사과정은 "고감도 분자 진단을 위해 통신 분야의 최첨단 기술인 대역확산 기술을 접목한 차세대 디지털 코드 라만 분광 기술을 최초로 제안했으며, 이 방법으로 기존 생체 분자 검출 기술의 장벽을 해결하고 기존 기술의 신경전달물질 검출한계를 획기적으로 향상시켰다ˮ며 "고감도 소형 분광기로 신속하고 간단하게 현장 진단이 가능하고 다양한 분야에 활용될 수 있어 파급효과가 크다ˮ고 말했다.
정기훈 교수는 "이번 결과를 바탕으로 향후 휴대용으로 소형화를 진행하면 낮은 비용으로 무표지 초고감도 생체 분자 분석 및 신속한 현장 진단이 가능해질 것이다ˮ며 "또한 신경전달물질뿐 아니라 다양한 생화합물 검출, 바이러스 검출, 신약평가분야에 크게 활용될수 있을 것이다ˮ고 말했다.
한편, 이번 연구는 한국연구재단 바이오기술개발사업, KAIST 코로나대응 과학기술뉴딜사업단과 범부처 전주기 의료기기 사업, 과학기술정보통신부 ETRI 연구개발지원사업의 지원을 받아 수행됐다.
2021.01.18 조회수 79790 -
 시스템생물학 이용 세계 최초 알츠하이머성 치매 환자 맞춤형 치료 효능 예측 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀 (장소영 박사과정(제1저자), 강의룡 박사과정, 장홍준 박사과정)은 서울대학교 의과대학 묵인희 교수 연구팀과 공동연구를 통해 시스템생물학*과 알츠하이머 환자 유래 뇌 오가노이드** 모델의 융합으로 환자 맞춤형 약물 효능평가 플랫폼(Drug-screening platform)을 세계 최초로 개발했다고 13일 밝혔다.
* 시스템생물학: IT의 수학모델링 및 컴퓨터시뮬레이션과 BT의 분자세포생물학 실험을 융합하여 복잡한 생명현상을 규명하고 설명하는 연구 패러다임
** 뇌 오가노이드: 환자의 역분화 줄기세포(iPSC) 유래 인공 미니 뇌
알츠하이머병은 치매의 약 70%를 차지하는 대표적 치매 질환이나 현재까지 발병 원인이 불명확하며, 근본적인 치료제도 없는 인류가 극복하지 못한 질병 중 하나다.
알츠하이머병 치료제 개발 난제 중 하나는 실제 살아있는 환자의 뇌를 직접 실험 샘플로 사용할 수 없다는 것이었다. 이는 수많은 치료제 후보군의 약물 효능을 정확히 평가하기가 어려워 치료제 개발의 걸림돌로 작용해왔다.
조광현 교수 공동 연구팀은 실제 치매환자에서 유래한 뇌 오가노이드 기반으로 생물학적 메커니즘에 대한 수학 모델링을 융합하여 약물효능 예측이 가능한 플랫폼을 세계 최초로 개발했다. 환자 혈액으로부터 역분화줄기세포(Induced-pluripotent stem cell)*를 구축 후 이를 이용하여 3D 뇌 오가노이드를 제작해 실제 환자의 뇌와 유사한 환경 구축을 통해 실험적 한계를 극복했다.
* 역분화줄기세포: 다능성이 없는 혈액 면역세포에 역분화를 일으키는 4가지 특정 유전자를 도입하여 배아 줄기세포와 같이 모든 종류의 세포로 분화할 수 있는 성질(다능성)을 가진 줄기세포
또한, 시스템생물학 기반 수학 모델링 기법으로 알츠하이머병의 신경세포 특이적 네트워크망을 구축하고, 이를 실제 알츠하이머병 환자 및 정상군 유래 뇌 오가노이드를 통하여 신경세포 컴퓨터 모델의 실효성을 검증했다.
이 연구결과는 알츠하이머병의 시스템생물학 기반 신경세포 컴퓨터 모델을 실제 환자 유래 뇌 오가노이드로 검증한 세계 최초의 사례이다. 이는 환자 맞춤형 치료(Precision medicine)의 불모지로 여겨졌던 뇌 질환분야에서도 알츠하이머병 환자의 유전형에 따른 최적의 약물 효능 예측이 가능하게 됨을 의미하며 향후 약물 타겟 발굴에 기여할 것으로 기대된다.
조광현 교수는 “이번에 개발한 시스템생물학 기반 알츠하이머성 치매환자 약물 효능평가 플랫폼을 통해 향후 치매 치료제 개발 경쟁에서 우리나라가 국가적 우위를 선점할 수 있을 것으로 기대한다”고 밝혔다.
이번 연구는 보건복지부 한국보건산업진흥원의 국가치매극복기술개발 사업 및 한국연구재단의 중견연구자지원사업으로 수행됐으며, 연구성과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications)의 2021년 1월 12일자 논문으로 게재됐다.
(https://www.nature.com/articles/s41467-020-20440-5)
2021.01.13 조회수 75462
시스템생물학 이용 세계 최초 알츠하이머성 치매 환자 맞춤형 치료 효능 예측 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀 (장소영 박사과정(제1저자), 강의룡 박사과정, 장홍준 박사과정)은 서울대학교 의과대학 묵인희 교수 연구팀과 공동연구를 통해 시스템생물학*과 알츠하이머 환자 유래 뇌 오가노이드** 모델의 융합으로 환자 맞춤형 약물 효능평가 플랫폼(Drug-screening platform)을 세계 최초로 개발했다고 13일 밝혔다.
* 시스템생물학: IT의 수학모델링 및 컴퓨터시뮬레이션과 BT의 분자세포생물학 실험을 융합하여 복잡한 생명현상을 규명하고 설명하는 연구 패러다임
** 뇌 오가노이드: 환자의 역분화 줄기세포(iPSC) 유래 인공 미니 뇌
알츠하이머병은 치매의 약 70%를 차지하는 대표적 치매 질환이나 현재까지 발병 원인이 불명확하며, 근본적인 치료제도 없는 인류가 극복하지 못한 질병 중 하나다.
알츠하이머병 치료제 개발 난제 중 하나는 실제 살아있는 환자의 뇌를 직접 실험 샘플로 사용할 수 없다는 것이었다. 이는 수많은 치료제 후보군의 약물 효능을 정확히 평가하기가 어려워 치료제 개발의 걸림돌로 작용해왔다.
조광현 교수 공동 연구팀은 실제 치매환자에서 유래한 뇌 오가노이드 기반으로 생물학적 메커니즘에 대한 수학 모델링을 융합하여 약물효능 예측이 가능한 플랫폼을 세계 최초로 개발했다. 환자 혈액으로부터 역분화줄기세포(Induced-pluripotent stem cell)*를 구축 후 이를 이용하여 3D 뇌 오가노이드를 제작해 실제 환자의 뇌와 유사한 환경 구축을 통해 실험적 한계를 극복했다.
* 역분화줄기세포: 다능성이 없는 혈액 면역세포에 역분화를 일으키는 4가지 특정 유전자를 도입하여 배아 줄기세포와 같이 모든 종류의 세포로 분화할 수 있는 성질(다능성)을 가진 줄기세포
또한, 시스템생물학 기반 수학 모델링 기법으로 알츠하이머병의 신경세포 특이적 네트워크망을 구축하고, 이를 실제 알츠하이머병 환자 및 정상군 유래 뇌 오가노이드를 통하여 신경세포 컴퓨터 모델의 실효성을 검증했다.
이 연구결과는 알츠하이머병의 시스템생물학 기반 신경세포 컴퓨터 모델을 실제 환자 유래 뇌 오가노이드로 검증한 세계 최초의 사례이다. 이는 환자 맞춤형 치료(Precision medicine)의 불모지로 여겨졌던 뇌 질환분야에서도 알츠하이머병 환자의 유전형에 따른 최적의 약물 효능 예측이 가능하게 됨을 의미하며 향후 약물 타겟 발굴에 기여할 것으로 기대된다.
조광현 교수는 “이번에 개발한 시스템생물학 기반 알츠하이머성 치매환자 약물 효능평가 플랫폼을 통해 향후 치매 치료제 개발 경쟁에서 우리나라가 국가적 우위를 선점할 수 있을 것으로 기대한다”고 밝혔다.
이번 연구는 보건복지부 한국보건산업진흥원의 국가치매극복기술개발 사업 및 한국연구재단의 중견연구자지원사업으로 수행됐으며, 연구성과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications)의 2021년 1월 12일자 논문으로 게재됐다.
(https://www.nature.com/articles/s41467-020-20440-5)
2021.01.13 조회수 75462 -
 알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
2020.09.28 조회수 27043
알츠하이머병을 유발하는 새로운 유전인자 발견
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 알츠하이머병을 유발하는 새로운 유전인자를 발견했다고 28일 밝혔다.
정 교수 연구팀은 환자의 뇌 영상·유전자와 함께 뇌척수액 데이터를 이용해 알츠하이머병의 새로운 유전인자를 발견했다. 연구팀은 새로 발견한 이 유전인자가 알츠하이머병의 원인 단백질로 알려진 아밀로이드 및 타우 단백질과는 별도로 환자의 인지 저하를 발생하는 사실과 함께 이 유전자가 항산화 효소 대사와 관련됐음을 입증했다. 이번 연구를 계기로 전 세계 약 1억5000만 명에 달하는 알츠하이머병 환자의 병태생리학적 규명은 물론 새로운 치료제 개발에 기여할 것으로 큰 기대를 모으고 있다.
우리 대학 의과학대학원김항래 박사가 제1 저자로 참여한 이번 연구 논문은 9월 16일 字 신경학 분야 저명 학술지인 '신경학(Neurology)'에 게재됐다. (논문명 : Genetic variants beyond amyloid and tau associated with cognitive decline: A cohort study)
알츠하이머병은 치매의 가장 흔한 원인인데 고령화에 따라 전 세계적으로 환자 수가 급속히 늘고 있다. 알츠하이머병을 유발하는 주요 원인 단백질로는 아밀로이드 및 타우 단백질이 알려져 있다. 따라서 이러한 주원인 단백질을 대상으로 하는 치료제가 많이 개발되는 추세다. 그러나 연이은 신약 개발의 실패로 인해 알츠하이머병에 대한 새로운 병태생리와 치료 대상에 관한 연구에 관심이 증가하고 있다.
정 교수 연구팀은 이번 연구를 위해 미국과 캐나다에 소재한 63개 지역 연구기관으로부터 얻은 정상인, 경도인지장애 관련 자료를 그리고 알츠하이머치매 환자로부터 얻은 뇌 영상·유전자·뇌척수액 데이터를 활용했다.(Alzheimer's Disease Neuroimaging Initiative, ADNI, http://adni.loni.usc.edu)
연구팀은 이와 함께 총 414명의 알츠하이머병 스펙트럼 환자(아밀로이드 단백질 양성 환자)를 대상으로 약 620만 개의 단일염기 다형성(Single Nucleotide Polymorphism, SNP)을 확인하는 과정에서 아밀로이드 및 타우 단백질과 별도로 환자의 인지기능에 영향을 주는 새로운 유전인자를 찾아냈다.
연구팀은 특히 독립된 데이터에서도 해당 유전자분석 결과의 재현에도 성공해 생물 정보학 분석을 통해서도 해당 유전인자가 항산화 효소 대사와 관련된 유전인자임을 입증했다. 연구팀은 실험을 통해 뇌 자기공명영상(Magnetic Resonance Imaging, MRI)으로 계산한 대뇌피질위축 데이터와 구조방정식 모델을 통해 해당 유전자가 뇌의 두정엽과 후두엽의 뇌 위축을 유발한다는 사실을 확인한 것이다. 이 패턴은 아밀로이드 및 타우 단백질에 의한 기존의 뇌 위축 패턴 현상과는 다른 것으로 나타났다.
제1 저자인 김항래 박사는 "이번 연구결과를 바탕으로 해당 유전인자가 있는 환자를 대상으로 항산화 치료의 효율성을 검증하는 추가 연구를 진행할 계획ˮ 이라고 밝혔다. 한편 이번 연구는 보건복지부 치매극복사업과 과학기술정보통신부 뇌과학원천기술사업의 지원을 받아 수행됐다.
2020.09.28 조회수 27043 -
 알츠하이머 치료제 개발을 위한 새로운 가능성 제시
우리 연구진이 알츠하이머 발병 원인을 동시다발적으로 억제 가능한 치료제 개발 원리를 증명하고 또 동물실험에서 효능을 입증하는 등 알츠하이머병에 관한 새로운 치료제 개발에 대한 가능성을 제시함으로써 많은 주목을 받고 있다.
우리 대학 화학과 임미희 교수 연구팀이 알츠하이머 발병의 원인으로 알려진 ‘활성 산소종’과 ‘아밀로이드 베타’, ‘금속 이온’ 등을 손쉽고도 동시다발적으로 억제할 수 있는 치료제 개발 원리를 새롭게 증명하고 알츠하이머 질환에 걸린 동물 모델(실험용 쥐) 치료를 통해 이를 입증하는 데 성공했다고 11일 밝혔다.
이번 연구에는 KAIST 백무현 교수와 서울아산병원 이주영 교수도 함께 참여했으며 저명 국제 학술지인 미국 화학회지(Journal of the American Chemical Society) 4월 1일 字에 게재됐다. 이 논문은 특히 4월 26일 字 ‘편집장 선정 우수 논문(Editors’Choice Paper)’으로 꼽혀 많은 주목을 받고 있다. (논문명 : Minimalistic Principles for Designing Small Molecules with Multiple Reactivities against Pathological Factors in Dementia)
알츠하이머병은 치매를 일으키는 대표적인 뇌 질환이다. 이 질환의 원인으로 다양한 요소들이 제시됐지만, 원인 인자들 사이의 원리들은 아직도 명확하게 밝혀지지 않고 있다.
알츠하이머병을 일으키는 대표적인 원인 인자로는, 활성 산소종과 아밀로이드 베타, 금속 이온이 알려져 있다. 이 요인들은 개별적으로 질병을 유발할 뿐만 아니라, 상호 작용을 통해 뇌 질환을 더욱 악화시킬 수 있다. 예를 들어, 금속 이온들은 아밀로이드 베타와 결합해 아밀로이드 베타의 응집 속도를 촉진시킬 뿐만 아니라, 활성 산소종들을 과다하게 생성하여 신경독성을 유발할 수 있다. 따라서 이처럼 복잡하게 얽힌 여러 원인 인자들을 동시에 겨냥할 수 있는 새로운 알츠하이머병 치료제 개발이 필요하다.
임 교수 연구팀은 단순한 저분자 화합물의 산화 환원 반응을 이용해 알츠하이머병의 원인 인자들을 손쉽게 조절할 수 있음을 증명했다. 임 교수팀은 산화되는 정도가 다른 화합물들의 합리적 설계를 통해 쉽게 산화되는 화합물들은 알츠하이머 질병의 여러 원인 인자들을 한꺼번에 조절할 수 있다는 사실을 확인했다.
연구 결과, 임 교수 연구팀은 저분자 화합물의 산화 환원 반응으로 활성 산소종에 대한 항산화 작용의 가능성을 확인했을 뿐만 아니라 아밀로이드 베타 또는 금속-아밀로이드 베타의 응집 및 섬유 형성 정도 또한 확연히 감소되는 것을 실험적으로 증명했다.
이 밖에 알츠하이머병에 걸린 동물 모델(실험용 쥐)에 체외 반응성이 좋고 바이오 응용에 적합한 성질을 가지고 있는 대표 저분자 화합물을 주입한 한 결과, 뇌 속에 축적된 아밀로이드 베타의 양이 크게 줄어드는 현상과 함께 알츠하이머 동물 모델의 손상된 인지 능력과 기억력이 향상되는 결과를 확인했다.
이번 연구가 크게 주목받는 이유는 알츠하이머병을 치료하기 위한 화합물을 개발하는 데 있어 아주 단순한 방향족 저분자 화합물의 구조변화를 통해 산화 환원 정도를 조절하여 여러 원인 인자들을 동시에 조절할 수 있고 이러한 간단한 원리를 통해 누구나 손쉽게 치료제를 디자인할 수 있기 때문이다.
임미희 교수는“이번 연구는 아주 단순한 방향족 저분자 화합물의 산화 정도의 차이를 이용해 여러 원인 인자들과의 반응성 유무를 확연히 구분할 수 있다는 점을 증명한 데 의미가 있다”며, “이 방법을 신약 개발의 디자인 방법으로 사용한다면, 비용과 시간을 훨씬 단축시켜 최대의 효과를 가질 수 있다”고 덧붙였다. 임 교수는 이와 함께 “제시된 치료제의 디자인 방법은 다양한 퇴행성 뇌 질환 치료제들의 개발 성공 가능성을 높일 것으로 기대된다”라고 강조했다.
한편 이번 연구는 한국연구재단, 기초과학연구원과 서울아산병원 등의 지원을 받아 수행됐다.
2020.05.11 조회수 19400
알츠하이머 치료제 개발을 위한 새로운 가능성 제시
우리 연구진이 알츠하이머 발병 원인을 동시다발적으로 억제 가능한 치료제 개발 원리를 증명하고 또 동물실험에서 효능을 입증하는 등 알츠하이머병에 관한 새로운 치료제 개발에 대한 가능성을 제시함으로써 많은 주목을 받고 있다.
우리 대학 화학과 임미희 교수 연구팀이 알츠하이머 발병의 원인으로 알려진 ‘활성 산소종’과 ‘아밀로이드 베타’, ‘금속 이온’ 등을 손쉽고도 동시다발적으로 억제할 수 있는 치료제 개발 원리를 새롭게 증명하고 알츠하이머 질환에 걸린 동물 모델(실험용 쥐) 치료를 통해 이를 입증하는 데 성공했다고 11일 밝혔다.
이번 연구에는 KAIST 백무현 교수와 서울아산병원 이주영 교수도 함께 참여했으며 저명 국제 학술지인 미국 화학회지(Journal of the American Chemical Society) 4월 1일 字에 게재됐다. 이 논문은 특히 4월 26일 字 ‘편집장 선정 우수 논문(Editors’Choice Paper)’으로 꼽혀 많은 주목을 받고 있다. (논문명 : Minimalistic Principles for Designing Small Molecules with Multiple Reactivities against Pathological Factors in Dementia)
알츠하이머병은 치매를 일으키는 대표적인 뇌 질환이다. 이 질환의 원인으로 다양한 요소들이 제시됐지만, 원인 인자들 사이의 원리들은 아직도 명확하게 밝혀지지 않고 있다.
알츠하이머병을 일으키는 대표적인 원인 인자로는, 활성 산소종과 아밀로이드 베타, 금속 이온이 알려져 있다. 이 요인들은 개별적으로 질병을 유발할 뿐만 아니라, 상호 작용을 통해 뇌 질환을 더욱 악화시킬 수 있다. 예를 들어, 금속 이온들은 아밀로이드 베타와 결합해 아밀로이드 베타의 응집 속도를 촉진시킬 뿐만 아니라, 활성 산소종들을 과다하게 생성하여 신경독성을 유발할 수 있다. 따라서 이처럼 복잡하게 얽힌 여러 원인 인자들을 동시에 겨냥할 수 있는 새로운 알츠하이머병 치료제 개발이 필요하다.
임 교수 연구팀은 단순한 저분자 화합물의 산화 환원 반응을 이용해 알츠하이머병의 원인 인자들을 손쉽게 조절할 수 있음을 증명했다. 임 교수팀은 산화되는 정도가 다른 화합물들의 합리적 설계를 통해 쉽게 산화되는 화합물들은 알츠하이머 질병의 여러 원인 인자들을 한꺼번에 조절할 수 있다는 사실을 확인했다.
연구 결과, 임 교수 연구팀은 저분자 화합물의 산화 환원 반응으로 활성 산소종에 대한 항산화 작용의 가능성을 확인했을 뿐만 아니라 아밀로이드 베타 또는 금속-아밀로이드 베타의 응집 및 섬유 형성 정도 또한 확연히 감소되는 것을 실험적으로 증명했다.
이 밖에 알츠하이머병에 걸린 동물 모델(실험용 쥐)에 체외 반응성이 좋고 바이오 응용에 적합한 성질을 가지고 있는 대표 저분자 화합물을 주입한 한 결과, 뇌 속에 축적된 아밀로이드 베타의 양이 크게 줄어드는 현상과 함께 알츠하이머 동물 모델의 손상된 인지 능력과 기억력이 향상되는 결과를 확인했다.
이번 연구가 크게 주목받는 이유는 알츠하이머병을 치료하기 위한 화합물을 개발하는 데 있어 아주 단순한 방향족 저분자 화합물의 구조변화를 통해 산화 환원 정도를 조절하여 여러 원인 인자들을 동시에 조절할 수 있고 이러한 간단한 원리를 통해 누구나 손쉽게 치료제를 디자인할 수 있기 때문이다.
임미희 교수는“이번 연구는 아주 단순한 방향족 저분자 화합물의 산화 정도의 차이를 이용해 여러 원인 인자들과의 반응성 유무를 확연히 구분할 수 있다는 점을 증명한 데 의미가 있다”며, “이 방법을 신약 개발의 디자인 방법으로 사용한다면, 비용과 시간을 훨씬 단축시켜 최대의 효과를 가질 수 있다”고 덧붙였다. 임 교수는 이와 함께 “제시된 치료제의 디자인 방법은 다양한 퇴행성 뇌 질환 치료제들의 개발 성공 가능성을 높일 것으로 기대된다”라고 강조했다.
한편 이번 연구는 한국연구재단, 기초과학연구원과 서울아산병원 등의 지원을 받아 수행됐다.
2020.05.11 조회수 19400 -
 두뇌 인지 기능 조절하는 신경 펩타이드 발견
우리 대학 생명과학과 이승희 교수 연구팀이 두뇌에 존재하는 신경 펩타이드 중 하나인 소마토스타틴(somatostatin)이 두뇌 인지 기능을 높일 수 있음을 밝혔다.
이 교수 연구팀은 특정 가바(뇌세포 대사 기능을 억제 신경 안정 작용을 하는 신경 전달 억제 물질) 분비 신경 세포에서 분비되는 펩타이드 중 하나인 소마토스태틴이 시각 피질의 정보 처리 과정을 조절하고 높일 수 있음을 규명했다. 이번 연구 성과는 치매 등의 뇌 질환에서 인지 능력 회복을 위한 치료제 개발의 계기가 될 것으로 기대된다.
생명과학과 송유향 박사, 황양선 석사, 바이오및뇌공학과 김관수 박사과정, 서울대학교 의과학대학 이형로 박사과정이 공동 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘사이언스 어드밴시스 (Science Advances)’ 4월 22일 자 온라인판에 게재됐다(논문명 : Somatostatin enhances visual processing and perception by modulating excitatory inputs to the parvalbumin-positive interneurons in V1).
2019년 기준 국내 65세 이상 노인 중 10명 중 1명은 치매 질환을 갖고 있다. 치매는 기억력 손실, 인지 기능 및 운동기능 저하 등의 일상생활 장애를 유발해 그 심각성은 나날이 두드러지고 있다.
이승희 교수 연구팀은 치매의 한 종류인 알츠하이머 질환 환자의 뇌척수액에서 소마토스타틴의 발현율이 현저히 감소했다는 점에 주목해 소마토스타틴에 의한 인지 능력 회복 가능성을 밝히는 연구를 수행했다.
소마토스타틴은 인간을 포함한 포유류의 중추신경계에서 존재한다. 특히 정상적인 포유류의 대뇌 피질에서 소마토스타틴을 발현하는 신경 세포인 가바(GABA, γ-aminobutyric acid)를 신경전달물질로 분비해 흥분성 신경 세포의 활성을 억제함으로써 정보 처리 정도를 조율한다.
그러나 기존 연구는 가바의 효과에만 국한돼, 동시에 분비될 수 있는 신경 펩타이드인 소마토스타틴의 고유한 효과 관련 연구는 부족한 상황이다.
연구팀은 자유롭게 움직이는 실험용 생쥐에서 시각정보 인지 및 식별 능력을 측정할 수 있는 실험 장비를 개발 및 도입했다. 이를 통해 생쥐의 시각피질 또는 뇌척수액에 소마토스타틴을 직접 주입한 후 이를 관찰해 생쥐의 시각정보 인지 능력이 현저히 증가함을 발견했다.
나아가 소마토스타틴의 처리에 따른 생체 내 또는 뇌 절편에서의 신경 세포 간 신경전달 효율의 변화를 측정하고, 해당 신경망을 연속 볼록면 주사전자현미경(SBEM)으로 관찰해 소마토스타틴에 의한 시각인지 기능의 향상이 이루어지는 생체 내 신경 생리적 원리를 규명했다.
이러한 연구 성과는 향후 인간을 비롯한 포유류의 두뇌 인지 기능을 조절 가능할 수 있을 뿐 아니라 퇴행성 뇌 질환 등에서 나타나는 인지 기능 장애 치료에 폭넓게 응용 및 적용될 수 있을 것으로 기대된다.
이승희 교수는 “이번 연구는 두뇌 기능을 높이고, 뇌 질환을 치료할 수 있는 새로운 약물 개발로 이어질 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단 중견연구자 지원사업의 지원을 받아 수행됐다.
2020.04.23 조회수 17519
두뇌 인지 기능 조절하는 신경 펩타이드 발견
우리 대학 생명과학과 이승희 교수 연구팀이 두뇌에 존재하는 신경 펩타이드 중 하나인 소마토스타틴(somatostatin)이 두뇌 인지 기능을 높일 수 있음을 밝혔다.
이 교수 연구팀은 특정 가바(뇌세포 대사 기능을 억제 신경 안정 작용을 하는 신경 전달 억제 물질) 분비 신경 세포에서 분비되는 펩타이드 중 하나인 소마토스태틴이 시각 피질의 정보 처리 과정을 조절하고 높일 수 있음을 규명했다. 이번 연구 성과는 치매 등의 뇌 질환에서 인지 능력 회복을 위한 치료제 개발의 계기가 될 것으로 기대된다.
생명과학과 송유향 박사, 황양선 석사, 바이오및뇌공학과 김관수 박사과정, 서울대학교 의과학대학 이형로 박사과정이 공동 1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘사이언스 어드밴시스 (Science Advances)’ 4월 22일 자 온라인판에 게재됐다(논문명 : Somatostatin enhances visual processing and perception by modulating excitatory inputs to the parvalbumin-positive interneurons in V1).
2019년 기준 국내 65세 이상 노인 중 10명 중 1명은 치매 질환을 갖고 있다. 치매는 기억력 손실, 인지 기능 및 운동기능 저하 등의 일상생활 장애를 유발해 그 심각성은 나날이 두드러지고 있다.
이승희 교수 연구팀은 치매의 한 종류인 알츠하이머 질환 환자의 뇌척수액에서 소마토스타틴의 발현율이 현저히 감소했다는 점에 주목해 소마토스타틴에 의한 인지 능력 회복 가능성을 밝히는 연구를 수행했다.
소마토스타틴은 인간을 포함한 포유류의 중추신경계에서 존재한다. 특히 정상적인 포유류의 대뇌 피질에서 소마토스타틴을 발현하는 신경 세포인 가바(GABA, γ-aminobutyric acid)를 신경전달물질로 분비해 흥분성 신경 세포의 활성을 억제함으로써 정보 처리 정도를 조율한다.
그러나 기존 연구는 가바의 효과에만 국한돼, 동시에 분비될 수 있는 신경 펩타이드인 소마토스타틴의 고유한 효과 관련 연구는 부족한 상황이다.
연구팀은 자유롭게 움직이는 실험용 생쥐에서 시각정보 인지 및 식별 능력을 측정할 수 있는 실험 장비를 개발 및 도입했다. 이를 통해 생쥐의 시각피질 또는 뇌척수액에 소마토스타틴을 직접 주입한 후 이를 관찰해 생쥐의 시각정보 인지 능력이 현저히 증가함을 발견했다.
나아가 소마토스타틴의 처리에 따른 생체 내 또는 뇌 절편에서의 신경 세포 간 신경전달 효율의 변화를 측정하고, 해당 신경망을 연속 볼록면 주사전자현미경(SBEM)으로 관찰해 소마토스타틴에 의한 시각인지 기능의 향상이 이루어지는 생체 내 신경 생리적 원리를 규명했다.
이러한 연구 성과는 향후 인간을 비롯한 포유류의 두뇌 인지 기능을 조절 가능할 수 있을 뿐 아니라 퇴행성 뇌 질환 등에서 나타나는 인지 기능 장애 치료에 폭넓게 응용 및 적용될 수 있을 것으로 기대된다.
이승희 교수는 “이번 연구는 두뇌 기능을 높이고, 뇌 질환을 치료할 수 있는 새로운 약물 개발로 이어질 수 있을 것으로 기대한다”라고 말했다.
이번 연구는 한국연구재단 중견연구자 지원사업의 지원을 받아 수행됐다.
2020.04.23 조회수 17519