-
 종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.07.16
조회수 6578
-
 맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.06.27
조회수 6279
-
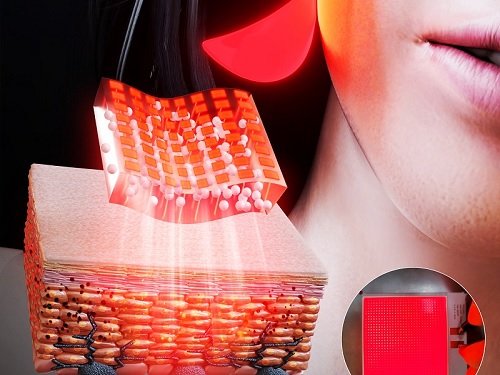 면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
2022.11.10
조회수 9408
-
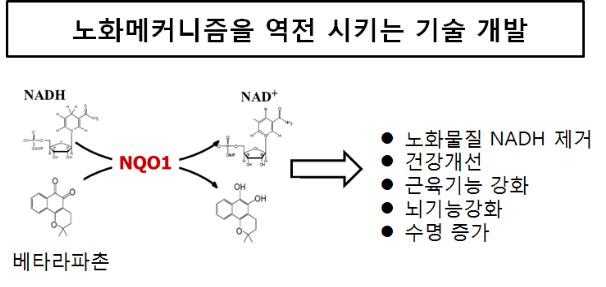 노화를 억제하면서 건강히 장수할 수 있도록 돕는 新물질 발견
김대수 교수
- PLoS One 발표,“암, 치매 및 파킨슨병 예방․치료에 한걸음 다가가”-
노화를 억제하면서 건강히 오래살 수 있도록 돕는 새로운 물질이 국내 연구진에 의해 발견됨에 따라, 건강한 삶을 오래 유지하고 싶은 인류의 꿈에 한걸음 다가서게 되었다.
우리 학교 생명과학과 김대수 교수(43세) 연구팀과 충남대 의과대학 및 산업체와의 공동연구로 진행된 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(전략연구)의 지원으로 수행되었고, 생물학 분야의 권위 있는 학술지인 ‘플로스 원(PLoS One)’ 최신호(10월 11일자)에 게재되었다.(논문명: Beta-lapachone, a modulator of NAD metabolism, prevents health declines in aged mice)
사람이 건강하게 오래 살 수 있는 효과적인 방법은 식사량을 줄이거나(小食) 달리기와 같은 유산소운동을 하는 것이다.
김대수 교수 연구팀은 우선 소식이나 유산소운동이 보조효소(NAD+*)를 증가시켜 세포의 노화를 억제한다는 점에 착안하였다. 연구팀은 천연화합물(베타-라파촌)로 효소(NQO1)를 활성화시키면, 적게 먹거나 별도의 운동을 하지 않아도 NAD+의 양이 증가됨을 규명하였다.
*) NAD+(니코틴아미드 디욱시뉴클레오타이드) : 이 보조효소가 세포내에서 증가하면 노화방지 효과가 있는 것으로 알려져 있음
**) 베타-라파촌(beta-lapachon) : 라파초 나무, 단삼 등 식물에 고농도로 함유된 천연화합물
또한 이미 노화가 진행된 생쥐들에게 베타-라파촌을 사료에 섞여 먹인 결과, 3개월이 경과되면 운동기능과 뇌기능이 모두 향상되어 건강하게 오래살 수 있음을 확인하였다. 특히 베타-라파촌은 동․서양에서 오랜 기간 사용해 온 약초의 주성분으로 만들어져, 머지않아 쉽게 상용화할 수 있는 것이 특징이다.
김대수 교수는 “지금까지 노화를 억제하는 약물들이 다수 개발되었지만, 사람에게 적용하는데 한계가 있었다. 우리 연구팀이 찾아낸 새로운 물질은 소식이나 운동으로 나타나는 효과를 그대로 모방하여 밝혀낸 것으로서, 향후 암, 치매 및 파킨슨병과 같은 노인성 질환을 예방하고 치료하는데 크게 기여할 것으로 기대한다”고 연구의의를 밝혔다.
노화를 억제하면서 건강히 장수할 수 있도록 돕는 新물질 발견
김대수 교수
- PLoS One 발표,“암, 치매 및 파킨슨병 예방․치료에 한걸음 다가가”-
노화를 억제하면서 건강히 오래살 수 있도록 돕는 새로운 물질이 국내 연구진에 의해 발견됨에 따라, 건강한 삶을 오래 유지하고 싶은 인류의 꿈에 한걸음 다가서게 되었다.
우리 학교 생명과학과 김대수 교수(43세) 연구팀과 충남대 의과대학 및 산업체와의 공동연구로 진행된 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(전략연구)의 지원으로 수행되었고, 생물학 분야의 권위 있는 학술지인 ‘플로스 원(PLoS One)’ 최신호(10월 11일자)에 게재되었다.(논문명: Beta-lapachone, a modulator of NAD metabolism, prevents health declines in aged mice)
사람이 건강하게 오래 살 수 있는 효과적인 방법은 식사량을 줄이거나(小食) 달리기와 같은 유산소운동을 하는 것이다.
김대수 교수 연구팀은 우선 소식이나 유산소운동이 보조효소(NAD+*)를 증가시켜 세포의 노화를 억제한다는 점에 착안하였다. 연구팀은 천연화합물(베타-라파촌)로 효소(NQO1)를 활성화시키면, 적게 먹거나 별도의 운동을 하지 않아도 NAD+의 양이 증가됨을 규명하였다.
*) NAD+(니코틴아미드 디욱시뉴클레오타이드) : 이 보조효소가 세포내에서 증가하면 노화방지 효과가 있는 것으로 알려져 있음
**) 베타-라파촌(beta-lapachon) : 라파초 나무, 단삼 등 식물에 고농도로 함유된 천연화합물
또한 이미 노화가 진행된 생쥐들에게 베타-라파촌을 사료에 섞여 먹인 결과, 3개월이 경과되면 운동기능과 뇌기능이 모두 향상되어 건강하게 오래살 수 있음을 확인하였다. 특히 베타-라파촌은 동․서양에서 오랜 기간 사용해 온 약초의 주성분으로 만들어져, 머지않아 쉽게 상용화할 수 있는 것이 특징이다.
김대수 교수는 “지금까지 노화를 억제하는 약물들이 다수 개발되었지만, 사람에게 적용하는데 한계가 있었다. 우리 연구팀이 찾아낸 새로운 물질은 소식이나 운동으로 나타나는 효과를 그대로 모방하여 밝혀낸 것으로서, 향후 암, 치매 및 파킨슨병과 같은 노인성 질환을 예방하고 치료하는데 크게 기여할 것으로 기대한다”고 연구의의를 밝혔다.
2012.10.24
조회수 22727
 종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.07.16 조회수 6578
종양모델 칩으로 다조건 항암제 동시 평가
실제 인체에 항암제가 투여되면 약물 분자는 혈류를 따라 수송된다. 이 약물 분자들은 혈관 벽을 투과하고 확산한다. 확산한 분자는 종양 덩어리 내부까지 점차 침투해 약물 효능이 나타나게 된다. 우리 연구진이 바이오프린팅 기술로 36가지의 종양 미세환경을 유체채널 내부에 모사하여 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는데 성공하여 화제다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 기존 바이오프린팅* 및 랩온어칩** 기술의 한계점을 극복하고 장점을 극대화하여 복잡한 종양 미세환경이 구현된 랩온어칩을 개발하여 여러 분석 변수가 반영된 약물 스크리닝을 수행하는 데 성공했다고 16일 밝혔다.
* 바이오프린팅(bioprinting): 세포와 생체재료로 구성된 바이오 잉크를 활용하여 생체조직 및 기관과 유사한 기능적 구조물을 제작하는 3D 프린팅 기술
** 랩온어칩(lab-on-a-chip): “칩 위의 실험실”이란 개념을 갖고 있으며 각종 시료분석에 필요한 전처리, 분리, 희석, 혼합, 반응, 검출 기능 등을 미세유체 회로로 이루어진 채널 내에서 일괄적으로 수행할 수 있도록 만들어진 미세유체 소자 및 시스템
바이오프린팅은 조직이나 장기의 복잡한 형상과 조성을 체외환경에서 재현할 수 있는 생체모사 기술이지만, 제작된 생체모델의 배양 환경 제어와 분석이 어렵다. 반면, 랩온어칩은 미세 유체채널 내에서의 유체 제어 기술에 기반해 배양 환경의 정교한 제어와 다양한 분석 수행이 가능하지만, 미세한 유체 통로 내부에 생체 환경을 모사하는 데 한계가 있었다.
연구진은 바이오프린팅 기술로 서로 다른 조성으로 구성된 총 36개의 종양 모델을 랩온어칩 내에 형성한 후, 동일한 소자 내에서 12가지 실험 조건에 따른 항암제 효능을 동시에 평가하는 데 성공했다.
연구팀은 바이오프린팅의 우수한 공간적 자유도와 다양한 생체재료를 활용할 수 있다는 장점을 이용해, 세 가지 서로 다른 조성으로 이루어진 36개의 종양 모델을 하나의 미세 유체소자에 집적시켰다. 세포를 유동 배양해 물질 수송에 핵심 구조물인 혈관 벽과 종양 덩어리를 모사하여 네 가지 농도의 항암제를 종양 모델에 유입함으로써, 하나의 소자에서 12가지 실험 조건의 약물 평가를 수행했다.
또한 연구팀은 혈관 벽에 의해 약물 분자의 수송이 저해되고 종양 덩어리 내부까지 침투되는 현상을 관찰할 수 있었고, 체내 수송 과정을 모사하지 못했던 기존 종양 모델과 약물 효능에 큰 차이를 보인다는 것을 확인했다.
이처럼 바이오프린팅-랩온어칩 통합기술을 활용해 모델 복잡성, 모델 수, 모델 처리량 등 다양한 변수를 고려한 체외 종양 모델을 제작할 수 있었고, 더욱 신뢰성 있는 약물 평가를 수행할 수 있었다.
연구를 주도한 박제균 교수는 “바이오프린팅과 랩온어칩의 통합기술로 제작된 미세 유체 세포배양 및 분석 플랫폼의 개발에 따른 신뢰성 있는 약물 평가 모델에 대한 성과”임을 강조하며, “향후 다양한 조직 및 장기 특성을 모사하고 생물학적 분석과 약물 효능 평가를 고효율로 수행할 수 있는 동물실험 대체용 차세대 체외 세포배양 및 분석 기술로 활용될 수 있을 것”이라고 말했다.
바이오및뇌공학과 이기현 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 '어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)'에 2024년 6월 3일 자로 온라인판에 게재됐다.
(https://doi.org/10.1002/adhm.202303716. 논문명: Bioprinted multi-composition array mimicking tumor microenvironment to evaluate drug efficacy with multivariable analysis).
또한, 이번 논문은 와일리-VCH(Wiley-VCH) 출판사의 ‘핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)’세션과 ‘핫 토픽: 미세유체공학(Hot Topic: Microfluidics)’세션에 동시 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.07.16 조회수 6578 맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.06.27 조회수 6279
맞춤형 종양 모델 구축 스페로이드 플랫폼 개발
세포들이 뭉쳐 생성된 구형 집합체인 스페로이드(spheroid)의 제작 기술은 현재 단일 조건의 스페로이드를 대규모로 생성하는 것까지는 가능하나, 체내 조직의 기능을 모사할 수 있는 최적의 크기 및 세포 조성 범위의 탐색이 어렵고, 다중 약물 스크리닝에 적합하지 않다는 문제가 있었다. 우리 연구진이 단 3번의 세포 주입으로 10가지 세포 조성을 갖는 100개의 스페로이드를 제작하고, 25가지 약물 조합을 동시에 처리할 수 있는 플랫폼을 구축하는 데 성공했다.
우리 대학 바이오및뇌공학과 박제균 교수 연구팀이 다양한 스페로이드 어레이(배열)를 맞춤형으로 손쉽게 제작하고 이를 구획화해 다중 시약 처리를 수행할 수 있는 조립형 마이크로어레이 플랫폼을 개발했다고 27일 밝혔다.
기존 단일 조건의 스페로이드를 대규모로 제작하는 방법은 다중 약물 스크리닝이 어렵고, 다중 약물 스크리닝이 가능한 방법은 대규모 제작이 어려워, 두 가지 장점을 동시에 만족하는 플랫폼이 개발되지 않은 실정이었다.
* 다중 약물 스크리닝: 암 치료의 식별 및 약물 안전성 평가를 위해 약물의 종류, 농도 등 다양한 실험 조건 변화에 따른 세포 및 조직의 반응을 평가하는 방법
연구팀은 조립식 플랫폼의 핵심기술인 행잉드롭 마이크로어레이*, 그래디언트(gradient) 블록**, 오목 기둥 마이크로어레이***를 개발하고, 이들의 조립 방식에 따라 달라지는 여러 가지 스페로이드 어레이 기반 종양 모델의 제작 방법과 분석 방법을 발표했다.
* 행잉드롭 마이크로어레이: 고드름과 같이 표면에 매달린 형태의 물방울을 의미하는 행잉드롭 내에 세포가 존재하면 중력에 의해 세포들이 응집되어 스페로이드가 만들어짐. 행잉드롭 마이크로어레이는 바닥 면에 구멍이 2차원으로 배열되어, 단 한 번의 세포 혼합용액 주입으로 행잉드롭을 어레이 형태로 형성할 수 있어, 균일한 스페로이드 어레이를 제작할 수 있음
** 그래디언트 블록: 경사면을 가지는 블록으로, 행잉드롭 마이크로어레이와 조립하게 되면 각각의 어레이 구멍에 가라앉는 세포의 수가 선형으로 변화하게 되어 이를 통해 크기가 규칙적으로 변화하는 스페로이드 어레이를 제작할 수 있음
***오목 기둥 마이크로어레이: 행잉드롭과 접촉하여 스페로이드를 기둥 상부에 안착시켜 회수할 수 있는 구조를 갖고 있어, 스페로이드 어레이를 개별적으로 분리하고 이동시킬 수 있음
연구팀은 10가지의 다른 세포 조성을 가지며, 조성 별로 10개의 스페로이드가 존재하는, 총 100개의 삼중 배양 스페로이드로 구성된 어레이를 단 세 번의 세포 혼합용액 주입으로 생성시키는데 성공했다.
또한 연구팀은 행잉드롭 마이크로어레이와 오목 기둥 마이크로어레이의 조립을 통해 대규모로 생성된 스페로이드를 작은물방울 형태로 각각 분리하고, 구획화된 행잉드롭 마이크로어레이로 옮겨 스페로이드 어레이를 구획화시키는 방법을 새롭게 선보였다. 이를 통해 스페로이드 어레이의 순차적 다중 시약 처리 및 일괄적 형광 염색이 가능하게 되어 스페로이드 분석 및 실험 과정이 획기적으로 개선됐다.
연구를 주도한 박제균 교수는 “이번 연구는 다양한 크기와 조성을 갖는 스페로이드 어레이를 대규모로 제작하고, 원하는 대로 이동시켜 일괄 또는 다중 시약 처리가 가능한 고효율 스크리닝 플랫폼의 개발 성과”임을 강조하며, “간단하면서도 우수한 편의성을 갖춘 플랫폼이기에, 향후 다른 연구자들도 스페로이드 및 오가노이드의 크기와 조성에 따른 변화 연구와 다양한 세포 조성으로 이루어진 복잡한 스페로이드, 오가노이드 어레이를 이용한 고효율 약물 스크리닝 등에 활용할 수 있을 것”이라고 말했다.
우리 대학 바이오및뇌공학과 김휘수 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘어드밴스드 헬스케어 머티리얼즈(Advanced Healthcare Materials)’에 2024년 5월 30일 자로 온라인판에 게재됐다.(https://doi.org/10.1002/adhm.202400501. 논문명: Reconfigurable Hanging Drop Microarray Platform for On-demand Preparation and Analysis of Spheroid Array) 또한 상기 논문은 와일리-VCH(Wiley-VCH) 출판사의 “핫 토픽: 종양과 암(Hot Topic: Tumors and Cancer)” 세션에도 선정됐다.
한편 이번 연구는 한국연구재단 기초연구사업(중견연구)의 지원을 받아 수행됐다.
2024.06.27 조회수 6279 면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
2022.11.10 조회수 9408
면 발광 마이크로 LED 패치 개발로 피부 미백에 획기적 효과
우리 대학 신소재공학과 이건재 교수팀과 세브란스 오상호 교수팀이 멜라닌 생성 억제를 위한 *면 발광 마이크로 LED 피부 패치를 개발했다고 10일 밝혔다.
☞ 면 발광 마이크로 LED 피부 패치: 인간의 머리카락의 ~1/100 의 두께를 가지는 매우 작은 LED 칩을 사용하여 제작한 인체에 부착 가능한 광치료 패치다. 기존의 점 발광의 특성을 가지는 LED와 달리, 구형 실리카 입자를 이용한 빛의 산란을 통해 면 발광의 특성을 갖는다.
멜라닌은 피부 내 존재하는 갈색 또는 흑색 색소로, 자외선 혹은 스트레스와 같은 외부 요인에 의해 비정상적으로 합성될 경우, 기미, 주근깨, 검버섯 등의 질환 형태로 나타나기 때문에 정상적으로 치료할 필요가 있다.
최근 피부질환 치료 및 미용을 위한 LED 기기들이 지속적으로 출시되고 있지만, 치료 효과에 있어서는 여전히 논란이 있다. 이는 LED가 피부에 밀착될 수 없어, 거리에 따른 광 손실 및 발열 문제로 인하여 역효과를 낼 수 있기 때문이다. 유의미한 피부 미용 효과를 얻기 위해서는 LED 광원을 피부에 밀착하여 조사함으로써, 균일한 빛을 피부 진피 내까지 효과적으로 전달해야 한다.
이에, 이건재 교수팀은 천여 개의 마이크로 LED를 4×4 cm2의 플라스틱 기판 위에서 구현하고, 빛의 확산을 위한 실리카 입자를 코팅함으로써 피부에 밀착하여 붙일 수 있는 면 발광 마이크로 LED 패치를 제작했다. 100 마이크로미터(μm) 크기의 마이크로 LED는 매우 작아 유연성을 가지며, 수직으로 배열된 전극은 LED의 발열을 줄여, 인간 피부 위에서 열적 손상 없이 장시간 구동 가능하다.
연구팀은 인간 피부 세포와 쥐의 등 피부에 면 발광 마이크로 LED 패치를 밀착시키고 조사하여 멜라닌 생성 억제 효능을 확인하였으며, 기존 상용 LED 대비, 피부 조직에 미치는 독성이 적을 뿐만 아니라, 효과적이고 일관된 경향으로 멜라닌 생성량을 감소시키는 데 성공했다. 또한, 피부 조직 분석을 통하여 멜라닌 생성에 관여하는 MITF (microphthalmia-associated transcription factor), Melan-A, 티로시나아제를 포함하는 단백질 및 효소 발현의 억제가 확인되었다.
이건재 교수는 "이번에 개발한 무기물 기반 면 발광 마이크로 LED 패치는 광 효율, 신뢰성, 수명 등이 우수하며, 기존 광 치료 기기와 달리 부작용은 줄이고 치료 효과를 극대화하여 코스메틱 분야에 큰 영향을 줄 것”이라고 말했다. 면 발광 마이크로 LED 패치는 현재 이 교수가 교원 창업한 ㈜프로닉스에 기술이전되어, 양산 장비를 갖추고 내년 3월 제품 출시를 앞두고 있다.
이번 연구는 웨어러블플랫폼 소재기술센터, 휴먼플러스 융합연구개발사업의 지원을 받아 수행됐으며, 국제 학술지 `어드밴스드 헬스케어 메터리얼즈(Advanced Healthcare Materials)'에 11월 게재됐다.
2022.11.10 조회수 9408 노화를 억제하면서 건강히 장수할 수 있도록 돕는 新물질 발견
김대수 교수
- PLoS One 발표,“암, 치매 및 파킨슨병 예방․치료에 한걸음 다가가”-
노화를 억제하면서 건강히 오래살 수 있도록 돕는 새로운 물질이 국내 연구진에 의해 발견됨에 따라, 건강한 삶을 오래 유지하고 싶은 인류의 꿈에 한걸음 다가서게 되었다.
우리 학교 생명과학과 김대수 교수(43세) 연구팀과 충남대 의과대학 및 산업체와의 공동연구로 진행된 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(전략연구)의 지원으로 수행되었고, 생물학 분야의 권위 있는 학술지인 ‘플로스 원(PLoS One)’ 최신호(10월 11일자)에 게재되었다.(논문명: Beta-lapachone, a modulator of NAD metabolism, prevents health declines in aged mice)
사람이 건강하게 오래 살 수 있는 효과적인 방법은 식사량을 줄이거나(小食) 달리기와 같은 유산소운동을 하는 것이다.
김대수 교수 연구팀은 우선 소식이나 유산소운동이 보조효소(NAD+*)를 증가시켜 세포의 노화를 억제한다는 점에 착안하였다. 연구팀은 천연화합물(베타-라파촌)로 효소(NQO1)를 활성화시키면, 적게 먹거나 별도의 운동을 하지 않아도 NAD+의 양이 증가됨을 규명하였다.
*) NAD+(니코틴아미드 디욱시뉴클레오타이드) : 이 보조효소가 세포내에서 증가하면 노화방지 효과가 있는 것으로 알려져 있음
**) 베타-라파촌(beta-lapachon) : 라파초 나무, 단삼 등 식물에 고농도로 함유된 천연화합물
또한 이미 노화가 진행된 생쥐들에게 베타-라파촌을 사료에 섞여 먹인 결과, 3개월이 경과되면 운동기능과 뇌기능이 모두 향상되어 건강하게 오래살 수 있음을 확인하였다. 특히 베타-라파촌은 동․서양에서 오랜 기간 사용해 온 약초의 주성분으로 만들어져, 머지않아 쉽게 상용화할 수 있는 것이 특징이다.
김대수 교수는 “지금까지 노화를 억제하는 약물들이 다수 개발되었지만, 사람에게 적용하는데 한계가 있었다. 우리 연구팀이 찾아낸 새로운 물질은 소식이나 운동으로 나타나는 효과를 그대로 모방하여 밝혀낸 것으로서, 향후 암, 치매 및 파킨슨병과 같은 노인성 질환을 예방하고 치료하는데 크게 기여할 것으로 기대한다”고 연구의의를 밝혔다.
2012.10.24 조회수 22727
노화를 억제하면서 건강히 장수할 수 있도록 돕는 新물질 발견
김대수 교수
- PLoS One 발표,“암, 치매 및 파킨슨병 예방․치료에 한걸음 다가가”-
노화를 억제하면서 건강히 오래살 수 있도록 돕는 새로운 물질이 국내 연구진에 의해 발견됨에 따라, 건강한 삶을 오래 유지하고 싶은 인류의 꿈에 한걸음 다가서게 되었다.
우리 학교 생명과학과 김대수 교수(43세) 연구팀과 충남대 의과대학 및 산업체와의 공동연구로 진행된 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(전략연구)의 지원으로 수행되었고, 생물학 분야의 권위 있는 학술지인 ‘플로스 원(PLoS One)’ 최신호(10월 11일자)에 게재되었다.(논문명: Beta-lapachone, a modulator of NAD metabolism, prevents health declines in aged mice)
사람이 건강하게 오래 살 수 있는 효과적인 방법은 식사량을 줄이거나(小食) 달리기와 같은 유산소운동을 하는 것이다.
김대수 교수 연구팀은 우선 소식이나 유산소운동이 보조효소(NAD+*)를 증가시켜 세포의 노화를 억제한다는 점에 착안하였다. 연구팀은 천연화합물(베타-라파촌)로 효소(NQO1)를 활성화시키면, 적게 먹거나 별도의 운동을 하지 않아도 NAD+의 양이 증가됨을 규명하였다.
*) NAD+(니코틴아미드 디욱시뉴클레오타이드) : 이 보조효소가 세포내에서 증가하면 노화방지 효과가 있는 것으로 알려져 있음
**) 베타-라파촌(beta-lapachon) : 라파초 나무, 단삼 등 식물에 고농도로 함유된 천연화합물
또한 이미 노화가 진행된 생쥐들에게 베타-라파촌을 사료에 섞여 먹인 결과, 3개월이 경과되면 운동기능과 뇌기능이 모두 향상되어 건강하게 오래살 수 있음을 확인하였다. 특히 베타-라파촌은 동․서양에서 오랜 기간 사용해 온 약초의 주성분으로 만들어져, 머지않아 쉽게 상용화할 수 있는 것이 특징이다.
김대수 교수는 “지금까지 노화를 억제하는 약물들이 다수 개발되었지만, 사람에게 적용하는데 한계가 있었다. 우리 연구팀이 찾아낸 새로운 물질은 소식이나 운동으로 나타나는 효과를 그대로 모방하여 밝혀낸 것으로서, 향후 암, 치매 및 파킨슨병과 같은 노인성 질환을 예방하고 치료하는데 크게 기여할 것으로 기대한다”고 연구의의를 밝혔다.
2012.10.24 조회수 22727