%EA%B9%80%EC%9C%A0%EC%8B%9D
-
 바이러스 면역반응‘켰다 껐다’단백질 스위치 발견
팬데믹 이후에도 다양한 신종 감염병이 출현하며 우리는 여전히 강력하고 지속적인 면역 방어를 요구하는 바이러스 위협에 직면해 있다. 동시에 과잉으로 면역 체계가 반응하면 오히려 몸의 조직을 해치는 부작용이 생기기도 한다. KAIST·국제 연구진이 이런 바이러스에 면역 반응을 조절하는 스위치 역할의 단백질을 찾아내는데 성공했다. 향후 감염병 대응과 자가면역질환 치료의 새로운 기반을 마련할 것으로 기대된다.
우리 대학 생명화학공학과 김유식 교수와 미국 플로리다주립대 차승희 교수 공동 연구팀이 세포 내 미토콘드리아에서 유래한 이중나선 RNA가 면역반응을 증폭시키는 메커니즘을 규명하고, 이를 조절하는 단백질 슬러프(SLIRP)가 바이러스 감염과 자가면역질환 양쪽에서 ‘면역 스위치’ 역할을 수행하는 것을 밝혀냈다.
자가면역질환은 면역 체계가 외부 침입자와 자기 조직을 구분하지 못하고 스스로를 공격하는 질환으로, 쉐그렌 증후군, 전신홍반루푸스 등으로 아직 명확한 발병 원인도 밝혀지지 않고, 효과적인 치료제도 드물다.
따라서 면역 과활성화를 유도하는 분자적 기전을 규명하고, 이를 조절할 수 있는 인자를 찾아내고자 생명화학공학과 김유식 교수 연구팀은 세포 내 기관에서 만들어지는 유전물질인 미토콘드리아 이중나선 RNA (mitochondrial double-stranded RNA, 이하 mt-dsRNA)에 주목했다.
엠티 디에스알엔에이(mt-dsRNA)는 바이러스 RNA와 유사하여 감염 바이러스가 없어도 우리 몸에서는 바이러스로 착각하고 면역반응을 유도할 수 있다는 점에 착안했다.
연구진은 면역 반응을 증폭시키는 단백질 슬러프를 발견하였고 실제로 다양한 자가면역질환 환자의 조직과 바이러스 자극을 모사한 실험 모델에서 슬러프 발현이 증가하는 것으로 확인했고, 반대로 슬러프를 억제했을 때는 면역반응이 현저히 감소되는것을 확인했다.
실험 결과, 슬러프가 면역 증폭의 핵심 인자임을 입증했고, 슬러프 단백질이 mt-dsRNA를 안정화시키고 축적시키는 역할을 하여, 이로 인해 면역반응이 증폭된다는 사실을 알아냈다.
이번 연구는 슬러프 단백질의 기능을 바이러스 감염 및 자가면역질환이라는 상반된 환경에서도 검증했다. 인간 베타 코로나바이러스 OC43과 뇌심근염 바이러스 EMCV에 감염된 세포에서 슬러프를 억제했을 때 항바이러스 반응이 감소하고, 바이러스 복제가 증가함을 확인했다.
반면, 대표적인 자가면역질환인 쉐그렌 증후군 환자의 혈액과 침샘 세포에서는 슬러프와 엠티 디에스알엔에이의 발현이 높게 나타났고, 슬러프를 억제했을 때 비정상적인 면역반응이 완화되는 경향도 관찰되었다.
이는 슬러프가 감염과 자가면역질환 모두에서 면역반응을 조절하는 중요한 분자 스위치라는 사실음 뒷받침한다.
생명화학공학과 김유식 교수는 "이번 연구를 통해 슬러프 단백질이 엠티 디에스알엔에이(mt-dsRNA)를 기반으로 면역반응의 증폭을 유도하는 핵심 인자임을 규명했다ˮ면서 "특히, 슬러프가 자가면역질환과 바이러스 감염에서 공통적으로 작동하는 면역 조절자라는 점에서, 슬러프를 타깃으로 한 면역 균형 조절 전략이 다양한 질환에 적용될 수 있을 것으로 기대된다ˮ라고 말했다.
생명화학공학과 박사과정 구도영(제1저자), 석사과정 양예원 학생(제2저자)이 참여한 이번 연구는 국제학술지 `셀 리포츠 (Cell Reports)'에 지난 4월 19일 온라인 게재됐다.
※ 논문명 : SLIRP amplifies antiviral signaling via positive feedback regulation and contributes to autoimmune diseases https://doi.org/10.1016/j.celrep.2025.115588
※ 주저자: 구도영(KAIST, 제1저자), 양예원(KAIST, 제2저자), 차승희(플로리다 주립대, 교신저자), 김유식(KAIST, 교신저자)
이번 연구는 보건복지부의 공익적 의료기술연구사업과 미국 국립보건연구원 (NIH)의 연구과제(R01) 지원을 받아 수행됐다.
2025.05.14 조회수 3352
바이러스 면역반응‘켰다 껐다’단백질 스위치 발견
팬데믹 이후에도 다양한 신종 감염병이 출현하며 우리는 여전히 강력하고 지속적인 면역 방어를 요구하는 바이러스 위협에 직면해 있다. 동시에 과잉으로 면역 체계가 반응하면 오히려 몸의 조직을 해치는 부작용이 생기기도 한다. KAIST·국제 연구진이 이런 바이러스에 면역 반응을 조절하는 스위치 역할의 단백질을 찾아내는데 성공했다. 향후 감염병 대응과 자가면역질환 치료의 새로운 기반을 마련할 것으로 기대된다.
우리 대학 생명화학공학과 김유식 교수와 미국 플로리다주립대 차승희 교수 공동 연구팀이 세포 내 미토콘드리아에서 유래한 이중나선 RNA가 면역반응을 증폭시키는 메커니즘을 규명하고, 이를 조절하는 단백질 슬러프(SLIRP)가 바이러스 감염과 자가면역질환 양쪽에서 ‘면역 스위치’ 역할을 수행하는 것을 밝혀냈다.
자가면역질환은 면역 체계가 외부 침입자와 자기 조직을 구분하지 못하고 스스로를 공격하는 질환으로, 쉐그렌 증후군, 전신홍반루푸스 등으로 아직 명확한 발병 원인도 밝혀지지 않고, 효과적인 치료제도 드물다.
따라서 면역 과활성화를 유도하는 분자적 기전을 규명하고, 이를 조절할 수 있는 인자를 찾아내고자 생명화학공학과 김유식 교수 연구팀은 세포 내 기관에서 만들어지는 유전물질인 미토콘드리아 이중나선 RNA (mitochondrial double-stranded RNA, 이하 mt-dsRNA)에 주목했다.
엠티 디에스알엔에이(mt-dsRNA)는 바이러스 RNA와 유사하여 감염 바이러스가 없어도 우리 몸에서는 바이러스로 착각하고 면역반응을 유도할 수 있다는 점에 착안했다.
연구진은 면역 반응을 증폭시키는 단백질 슬러프를 발견하였고 실제로 다양한 자가면역질환 환자의 조직과 바이러스 자극을 모사한 실험 모델에서 슬러프 발현이 증가하는 것으로 확인했고, 반대로 슬러프를 억제했을 때는 면역반응이 현저히 감소되는것을 확인했다.
실험 결과, 슬러프가 면역 증폭의 핵심 인자임을 입증했고, 슬러프 단백질이 mt-dsRNA를 안정화시키고 축적시키는 역할을 하여, 이로 인해 면역반응이 증폭된다는 사실을 알아냈다.
이번 연구는 슬러프 단백질의 기능을 바이러스 감염 및 자가면역질환이라는 상반된 환경에서도 검증했다. 인간 베타 코로나바이러스 OC43과 뇌심근염 바이러스 EMCV에 감염된 세포에서 슬러프를 억제했을 때 항바이러스 반응이 감소하고, 바이러스 복제가 증가함을 확인했다.
반면, 대표적인 자가면역질환인 쉐그렌 증후군 환자의 혈액과 침샘 세포에서는 슬러프와 엠티 디에스알엔에이의 발현이 높게 나타났고, 슬러프를 억제했을 때 비정상적인 면역반응이 완화되는 경향도 관찰되었다.
이는 슬러프가 감염과 자가면역질환 모두에서 면역반응을 조절하는 중요한 분자 스위치라는 사실음 뒷받침한다.
생명화학공학과 김유식 교수는 "이번 연구를 통해 슬러프 단백질이 엠티 디에스알엔에이(mt-dsRNA)를 기반으로 면역반응의 증폭을 유도하는 핵심 인자임을 규명했다ˮ면서 "특히, 슬러프가 자가면역질환과 바이러스 감염에서 공통적으로 작동하는 면역 조절자라는 점에서, 슬러프를 타깃으로 한 면역 균형 조절 전략이 다양한 질환에 적용될 수 있을 것으로 기대된다ˮ라고 말했다.
생명화학공학과 박사과정 구도영(제1저자), 석사과정 양예원 학생(제2저자)이 참여한 이번 연구는 국제학술지 `셀 리포츠 (Cell Reports)'에 지난 4월 19일 온라인 게재됐다.
※ 논문명 : SLIRP amplifies antiviral signaling via positive feedback regulation and contributes to autoimmune diseases https://doi.org/10.1016/j.celrep.2025.115588
※ 주저자: 구도영(KAIST, 제1저자), 양예원(KAIST, 제2저자), 차승희(플로리다 주립대, 교신저자), 김유식(KAIST, 교신저자)
이번 연구는 보건복지부의 공익적 의료기술연구사업과 미국 국립보건연구원 (NIH)의 연구과제(R01) 지원을 받아 수행됐다.
2025.05.14 조회수 3352 -
 미토콘드리아로 퇴행성 질환까지 제어 가능하다
우리 대학 생명화학공학과 김유식 교수 연구팀이 비정상적 면역 활성을 유발해 염증반응이 동반된 세포 사멸을 일으키는 미토콘드리아 이중나선 RNA의 새로운 조절 기전을 찾아냈다고 22일 밝혔다.
최근 미토콘드리아 이중나선 RNA가 스트레스 환경에서 세포질로 빠져나가 비정상적 면역 활성 및 세포 사멸을 유발한다는 것이 밝혀졌다. 또한 이러한 미토콘드리아 이중나선 RNA로 촉발되는 면역 활성은 관절염 및 헌팅턴 무도병을 비롯한 염증반응이 동반된 퇴행성 질환과 자가면역질환 중 하나인 쇼그렌 증후군의 발병 및 진행에 핵심적인 역할을 한다는 것이 보고됐다.
아직 미토콘드리아 이중나선 RNA의 분자적 조절 기전에 대해서는 보고된 바 없다는 점을 착안해서 연구팀은 미토콘드리아 내에 존재하며 RNA와 결합할 수 있는 단백질에 대해 유전자 가위를 이용해 각 단백질의 발현을 억제한 후 미토콘드리아 이중나선 RNA의 발현량을 조사했다.
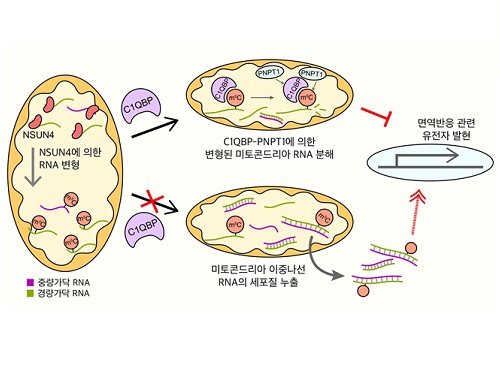
이 과정에서 RNA의 구성 물질 중 하나인 시토신의 화학적 변형을 유발하는 엔썬4(NSUN4)*이라는 단백질의 발현을 줄였을 때 미토콘드리아 이중나선 RNA의 발현이 유의미하게 증가하는 것을 확인했다.
*엔썬4 (NSUN4): NOP2/Sun RNA 메틸트랜스퍼라제 4
나아가, 연구팀은 단백질을 생산하지 않는 미토콘드리아 비암호화 RNA의 변형을 가속시키는 것이 동 단백질 엔썬4에 의해서라고 최초로 제시했다.
연구팀은 추가 연구를 통해 미토콘드리아 RNA 단백질들의 발현 감소로 축적된 미토콘드리아 이중나선 RNA의 양이 증가했으며 세포질로 누출된 미토콘드리아 이중나선 RNA는 면역반응을 활성화시켰다. 이를 통해 연구팀은 새로운 세포 내 면역 유발인자로 최근 주목받기 시작한 미토콘드리아 이중나선 RNA의 변형에 의한 발현 조절 기전을 제시했다.
생명화학공학과 김유식 교수는 “이번 연구를 통해 비정상적 면역 활성 유발 인자로 최근 주목받고 있는 미토콘드리아 이중나선 RNA의 형성 및 조절 기전을 밝혔다”면서 “이번 연구의 결과를 바탕으로 면역 계통 질환을 비롯해 다양한 퇴행성 질환의 발병 및 진행 과정을 효과적으로 제어할 수 있는 전략을 제시할 수 있을 것”이라고 말했다.
생명화학공학과 김수진 박사(現 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학(Harvard Medical School) 박사후연구원)와 탄 스테파니(Tan Stephanie) 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 7월 16일 字에 온라인 게재됐다. (논문명 : RNA 5-methylcytosine marks mitochondrial double-stranded RNAs for degradation and cytosolic release).
한편 이번 연구는 한국연구재단 우수신진연구지원사업과 미국 국립보건원의 지원으로 수행됐다.
2024.07.22 조회수 5383
미토콘드리아로 퇴행성 질환까지 제어 가능하다
우리 대학 생명화학공학과 김유식 교수 연구팀이 비정상적 면역 활성을 유발해 염증반응이 동반된 세포 사멸을 일으키는 미토콘드리아 이중나선 RNA의 새로운 조절 기전을 찾아냈다고 22일 밝혔다.
최근 미토콘드리아 이중나선 RNA가 스트레스 환경에서 세포질로 빠져나가 비정상적 면역 활성 및 세포 사멸을 유발한다는 것이 밝혀졌다. 또한 이러한 미토콘드리아 이중나선 RNA로 촉발되는 면역 활성은 관절염 및 헌팅턴 무도병을 비롯한 염증반응이 동반된 퇴행성 질환과 자가면역질환 중 하나인 쇼그렌 증후군의 발병 및 진행에 핵심적인 역할을 한다는 것이 보고됐다.
아직 미토콘드리아 이중나선 RNA의 분자적 조절 기전에 대해서는 보고된 바 없다는 점을 착안해서 연구팀은 미토콘드리아 내에 존재하며 RNA와 결합할 수 있는 단백질에 대해 유전자 가위를 이용해 각 단백질의 발현을 억제한 후 미토콘드리아 이중나선 RNA의 발현량을 조사했다.
이 과정에서 RNA의 구성 물질 중 하나인 시토신의 화학적 변형을 유발하는 엔썬4(NSUN4)*이라는 단백질의 발현을 줄였을 때 미토콘드리아 이중나선 RNA의 발현이 유의미하게 증가하는 것을 확인했다.
*엔썬4 (NSUN4): NOP2/Sun RNA 메틸트랜스퍼라제 4
나아가, 연구팀은 단백질을 생산하지 않는 미토콘드리아 비암호화 RNA의 변형을 가속시키는 것이 동 단백질 엔썬4에 의해서라고 최초로 제시했다.
연구팀은 추가 연구를 통해 미토콘드리아 RNA 단백질들의 발현 감소로 축적된 미토콘드리아 이중나선 RNA의 양이 증가했으며 세포질로 누출된 미토콘드리아 이중나선 RNA는 면역반응을 활성화시켰다. 이를 통해 연구팀은 새로운 세포 내 면역 유발인자로 최근 주목받기 시작한 미토콘드리아 이중나선 RNA의 변형에 의한 발현 조절 기전을 제시했다.
생명화학공학과 김유식 교수는 “이번 연구를 통해 비정상적 면역 활성 유발 인자로 최근 주목받고 있는 미토콘드리아 이중나선 RNA의 형성 및 조절 기전을 밝혔다”면서 “이번 연구의 결과를 바탕으로 면역 계통 질환을 비롯해 다양한 퇴행성 질환의 발병 및 진행 과정을 효과적으로 제어할 수 있는 전략을 제시할 수 있을 것”이라고 말했다.
생명화학공학과 김수진 박사(現 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학(Harvard Medical School) 박사후연구원)와 탄 스테파니(Tan Stephanie) 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 7월 16일 字에 온라인 게재됐다. (논문명 : RNA 5-methylcytosine marks mitochondrial double-stranded RNAs for degradation and cytosolic release).
한편 이번 연구는 한국연구재단 우수신진연구지원사업과 미국 국립보건원의 지원으로 수행됐다.
2024.07.22 조회수 5383 -
 암, 루게릭병 등 난치성 질환 발병 기전 밝혀
단백질 정보를 가진 mRNA 유전자 조절 기전에서 알루 요소(Alu)의 중요성을 제시하고, 나아가 종양 형성, 퇴행성 뇌질환 등 mRNA가 변화하는 다양한 질환에서 역방향 알루 반복구조(IRAlus)라는 새로운 발병 원인을 최초로 제시함으로써 질병 치료에 획기적인 방안을 제시하였다.
우리 대학 생명화학공학과 김유식 교수와 바이오및뇌공학과 이영석 교수 공동 연구팀이 종양 형성과 퇴행성 뇌질환을 유발하는 새로운 유전자 조절 기전을 찾아냈다고 6일 밝혔다.
인간 유전체의 약 10%를 차지하는 반복서열인 알루 요소(Alu element, Alu)는 단백질 정보를 가지는 전령 RNA(messenger RNA, mRNA)의 단백질 생산 효율을 조절할 수 있다. 특히, mRNA가 2개의 알루 요소로 형성된 역방향 알루 반복 구조(Inverted Alu repeats, IRAlus)를 가지게 되면 mRNA의 세포 내 이동이 방해되어 단백질 생산이 감소한다.
연구팀은 질환 특이적으로 mRNA가 변화하는 과정에서 주요 mRNA가 역방향 알루 반복 구조(IRAlus)에 의해 조절받게 하고 이는 mRNA가 가지고 있는 유전자 발현 억제로 이어져 질환을 일으킨다는 새로운 발병 기전을 밝혔다.
알루(Alu)는 유전체의 단백질 정보를 가지고 있지만 유전체 상에서 본인의 서열만을 복제하는 성질이 있어 ‘이기적 서열’로 알려져 있었다. 최근 연구에 의하면 mRNA 내의 존재하는 역방향 알루 반복 구조(IRAlus)는 숙주 mRNA의 세포질로의 이동을 방해하여 해당 유전자의 단백질 번역을 억제한다. 그러나, 해당 유전자 발현 조절 기전의 생물학적 중요성에 대해서는 보고된 바가 없었다.
연구팀은 역방향 알루 반복 구조(IRAlus)를 인지할 수 있는 항체를 활용한 차세대 염기서열 분석법을 사용해 특정 세포 내 활성화된, 기능적인 역방향 알루 반복 구조(IRAlus)를 가지고 있어 역방향 알루 반복 구조(IRAlus)에 의해 단백질 합성이 억제될 수 있는 mRNA 유전자 목록을 완성했다.
종양 형성 과정에서 역방향 알루 반복 구조(IRAlus)의 유전자 조절 기전의 영향을 분석했다. 연구팀은 대표적인 종양억제유전자를 억제하는 종양 유전자 조절을 하고 이는 단백질 발현 증가로 이어지며 결과적으로 종양억제유전자 활성이 억제됨으로써 암 발달을 촉진할 수 있다.
나아가, 특정 mRNA 서열과 상보적으로 결합해 mRNA의 기능을 억제해 다양한 질병 치료 및 조절 도구로 현재 연구되고 있는 혁신 RNA 치료제인 안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, 이하 ASO)를 활용해 단백질 발현을 복구하는 암 치료 전략을 탐색했다.
연구팀은 신경계 세포에서 역방향 알루 반복 구조(IRAlus)로 인한 유전자 조절이 활발하다는 것을 확인했다. 또한, 해당 현상의 과도한 활성과 루게릭병으로 알려진 근위축성 측삭경화증을 비롯한 퇴행성 뇌질환 간의 연관성을 최초로 제시했다.
생명화학공학과 김유식 교수는 “이번 연구는 인간 유전체 내 반복서열인 역방향 알루 반복 구조(IRAlus)를 가지는 유전자를 목록화하는 것을 넘어서 해당 유전자 발현 조절이 인간 질환, 특히 종양 형성 및 퇴행성 뇌질환 발병과정에서 핵심적인 역할을 하는 것을 최초로 확인했다”면서 “이번 연구에서 제시한 역방향 알루 반복 구조(IRAlus)라는 새로운 타겟 물질을 활용하면 종양과 노화를 비롯해 다양한 퇴행성 질환의 발병 기전 분석에 근본적이고 효과적인 치료전략을 마련하는 데 유용할 것”이라고 말했다.
생명화학공학과 구자영 박사(현 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학 (Harvard Medical School) 박사후연구원)와 이건용 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 2월 2일 字에 온라인 게재됐다. (논문명 : Alternative Polyadenylation Determines the Functional Landscape of Inverted Alu Repeats).
우리 대학 생명과학과 임정훈 교수 연구팀과 의과학대학원 한진주 교수 연구팀이 참여한 이번 연구는 한국연구재단 기초연구실 지원사업과 KAIST 도약연구사업의 지원을 받아 수행됐다.
2024.02.06 조회수 6511
암, 루게릭병 등 난치성 질환 발병 기전 밝혀
단백질 정보를 가진 mRNA 유전자 조절 기전에서 알루 요소(Alu)의 중요성을 제시하고, 나아가 종양 형성, 퇴행성 뇌질환 등 mRNA가 변화하는 다양한 질환에서 역방향 알루 반복구조(IRAlus)라는 새로운 발병 원인을 최초로 제시함으로써 질병 치료에 획기적인 방안을 제시하였다.
우리 대학 생명화학공학과 김유식 교수와 바이오및뇌공학과 이영석 교수 공동 연구팀이 종양 형성과 퇴행성 뇌질환을 유발하는 새로운 유전자 조절 기전을 찾아냈다고 6일 밝혔다.
인간 유전체의 약 10%를 차지하는 반복서열인 알루 요소(Alu element, Alu)는 단백질 정보를 가지는 전령 RNA(messenger RNA, mRNA)의 단백질 생산 효율을 조절할 수 있다. 특히, mRNA가 2개의 알루 요소로 형성된 역방향 알루 반복 구조(Inverted Alu repeats, IRAlus)를 가지게 되면 mRNA의 세포 내 이동이 방해되어 단백질 생산이 감소한다.
연구팀은 질환 특이적으로 mRNA가 변화하는 과정에서 주요 mRNA가 역방향 알루 반복 구조(IRAlus)에 의해 조절받게 하고 이는 mRNA가 가지고 있는 유전자 발현 억제로 이어져 질환을 일으킨다는 새로운 발병 기전을 밝혔다.
알루(Alu)는 유전체의 단백질 정보를 가지고 있지만 유전체 상에서 본인의 서열만을 복제하는 성질이 있어 ‘이기적 서열’로 알려져 있었다. 최근 연구에 의하면 mRNA 내의 존재하는 역방향 알루 반복 구조(IRAlus)는 숙주 mRNA의 세포질로의 이동을 방해하여 해당 유전자의 단백질 번역을 억제한다. 그러나, 해당 유전자 발현 조절 기전의 생물학적 중요성에 대해서는 보고된 바가 없었다.
연구팀은 역방향 알루 반복 구조(IRAlus)를 인지할 수 있는 항체를 활용한 차세대 염기서열 분석법을 사용해 특정 세포 내 활성화된, 기능적인 역방향 알루 반복 구조(IRAlus)를 가지고 있어 역방향 알루 반복 구조(IRAlus)에 의해 단백질 합성이 억제될 수 있는 mRNA 유전자 목록을 완성했다.
종양 형성 과정에서 역방향 알루 반복 구조(IRAlus)의 유전자 조절 기전의 영향을 분석했다. 연구팀은 대표적인 종양억제유전자를 억제하는 종양 유전자 조절을 하고 이는 단백질 발현 증가로 이어지며 결과적으로 종양억제유전자 활성이 억제됨으로써 암 발달을 촉진할 수 있다.
나아가, 특정 mRNA 서열과 상보적으로 결합해 mRNA의 기능을 억제해 다양한 질병 치료 및 조절 도구로 현재 연구되고 있는 혁신 RNA 치료제인 안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, 이하 ASO)를 활용해 단백질 발현을 복구하는 암 치료 전략을 탐색했다.
연구팀은 신경계 세포에서 역방향 알루 반복 구조(IRAlus)로 인한 유전자 조절이 활발하다는 것을 확인했다. 또한, 해당 현상의 과도한 활성과 루게릭병으로 알려진 근위축성 측삭경화증을 비롯한 퇴행성 뇌질환 간의 연관성을 최초로 제시했다.
생명화학공학과 김유식 교수는 “이번 연구는 인간 유전체 내 반복서열인 역방향 알루 반복 구조(IRAlus)를 가지는 유전자를 목록화하는 것을 넘어서 해당 유전자 발현 조절이 인간 질환, 특히 종양 형성 및 퇴행성 뇌질환 발병과정에서 핵심적인 역할을 하는 것을 최초로 확인했다”면서 “이번 연구에서 제시한 역방향 알루 반복 구조(IRAlus)라는 새로운 타겟 물질을 활용하면 종양과 노화를 비롯해 다양한 퇴행성 질환의 발병 기전 분석에 근본적이고 효과적인 치료전략을 마련하는 데 유용할 것”이라고 말했다.
생명화학공학과 구자영 박사(현 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학 (Harvard Medical School) 박사후연구원)와 이건용 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 2월 2일 字에 온라인 게재됐다. (논문명 : Alternative Polyadenylation Determines the Functional Landscape of Inverted Alu Repeats).
우리 대학 생명과학과 임정훈 교수 연구팀과 의과학대학원 한진주 교수 연구팀이 참여한 이번 연구는 한국연구재단 기초연구실 지원사업과 KAIST 도약연구사업의 지원을 받아 수행됐다.
2024.02.06 조회수 6511 -
 RNA를 활용한 자가면역질환 조기진단 및 치료제 개발 앞장설 것
우리 대학 생명화학공학과 김유식 교수와 임성갑 교수, 분당서울대병원 류마티스내과 이윤종 교수 그리고 미국 플로리다주립대 차승희 교수 공동 연구팀이 희귀난치성 자가면역질환인 쉐그렌 증후군(Sjögren’s Syndrome)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
원인불명의 만성 전신 염증 질환인 쉐그렌 증후군은 눈물샘 및 침샘 등 외분비샘을 주로 침범하는 자가면역질환이다. 안구 및 구강건조증 등 외분비샘 기능 저하가 가장 흔한 증상이지만, 외분비샘 외 장기 침범이 다양하고 악성 림프종 합병증에 대한 위험이 특징적으로 수반되고 있다. 주로 중년 여성에게 나타나며 환자 중 약 3분의 1은 림프종, 관절염, 간 손상, 기관지염 등의 다양한 전신증상을 겪으며, 악성 림프종 및 폐 섬유화 합병증으로 조기 사망할 수 있는 무서운 질환이다.
연구팀은 쉐그렌 증후군에서 비정상적인 면역 활성을 유발해 외분비샘 조직 손상을 일으키는 물질로 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)를 제시했다.
이번 연구는 mt-dsRNA라는 쉐그렌 증후군 증상 조절 인자를 최초로 확립해 비침습성 조기 진단법 및 치료제 개발을 위한 이론적 기반을 제공할 것으로 기대된다.
우리 대학 생명화학공학과 윤지민 박사과정생과 이민석 박사가 공동 제1 저자로 참여한 이번 연구는 국제학술지 `몰레큘러 테라피 뉴클레익 에시드(Molecular Therapy – Nucleic Acids)'에 지난 9월 27일 게재됐다. (논문명 : Mitochondrial double-stranded RNAs as a pivotal mediator in the pathogenesis of Sjögren’s syndrome)
쉐그렌 증후군은 질병의 심각성에도 불구하고 지금까지 질환의 병태생리를 대변하는 유전자 마커 없이 환자의 증상을 기반으로 진단이 이뤄지고 있으며 치료제 또한 존재하지 않는 희귀성 난치질환이다. 또한, 쉐그렌 증후군 진단은 이미 외분비샘 조직 손상이 상당히 진행된 후에 가능하고 진단법 역시 증상을 기반으로 해 낮은 질병 특이도를 갖고 있다. 이러한 한계점을 극복하기 위해 연구팀은 질병의 발병 및 진행 메커니즘을 분석해 쉐그렌 증후군의 조기 진단과 치료 효과를 기대할 수 있는 신규 면역 제어 표적 물질을 확립하고자 했다.
쉐그렌 증후군 환자에게서는 특히 이중나선 RNA(dsRNA)를 인지하는 선천성 면역 반응 단백질의 과활성화 그리고 이에 의한 항바이러스성 인터페론 반응이 관찰됐다. 하지만 지금까지 dsRNA가 실제 질환에 관여하는지는 보고된 바 없으며 dsRNA를 표적으로 하는 진단법 및 치료 방향을 탐색한 연구 또한 존재하지 않는다.
세포 내 자연적으로 존재하는 RNA도 dsRNA를 형성해 선천성 면역반응을 조절할 수 있다. 세포 내재 dsRNA를 생성하는 대표적인 세포 내 소기관은 미토콘드리아이며 mt-dsRNA 또한 선천성 면역반응 단백질에 의해 인지되어 인터페론 반응을 유도할 수 있다. 연구팀은 쉐그렌 증후군 환자에서 관찰된 과도한 면역 활성의 특징과 미토콘드리아 기능 이상 등을 고려해 mt-dsRNA가 질환 발병에서 중요한 기능을 할 것이라는 가설을 세우고 연구를 수행했다.
연구팀은 쉐그렌 증후군 환자의 누액과 타액을 분석한 결과 환자 특이적으로 mt-dsRNA의 과발현 현상을 확인했다. 이는 환자의 일차 세포 및 쉐그렌 증후군 모델 생쥐의 손상된 침샘에서도 확인됐다. 연구팀은 이에 mt-dsRNA의 기능을 분석하기 위해 세포 실험을 진행했다. 특히, 타액선 세포주의 3차원 스페로이드 배양 시스템을 구축해 보다 정확한 질병 환경을 모사했다. 그 결과 mt-dsRNA의 발현이 면역 활성이 유발되는 스트레스 상황에서 증가하며 이는 면역 활성의 촉진제 역할을 한다는 것을 연구팀은 규명했다. 특히, mt-dsRNA의 발현을 억제했을 때 면역 활성이 감소하며 질환의 특징이 일부 복원되는 것을 확인했다.
나아가 연구팀은 쉐그렌 증후군 환자의 증상 완화에 활용되는 필로카핀의 치료 메커니즘에서 mt-dsRNA의 기능을 분석했다. 연구팀은 M3R 수용체 작용제인 아세틸콜린이 mt-dsRNA 조절을 통해 면역 활성을 억제하며 쉐그렌 증후군 환자에서 추출된 자가항체가 아세틸콜린을 억제해 과도한 면역 활성을 유발한다는 것을 확인했다. 필로카핀이 아세틸콜린을 모방하는 M3R 작용제임을 고려했을 때, 연구팀은 약물의 효과를 대변할 수 있는 마커로서 mt-dsRNA의 기능성을 검증했다.
생명화학공학과 김유식 교수는 "이번 연구를 통해 난치병으로 인식되고 있는 쉐그렌 증후군에서 mt-dsRNA라는 새로운 병인을 제시했다ˮ면서 "특히, mt-dsRNA 발현량 조절을 통한 면역 과활성화의 완화 효과를 고려했을 때 쉐그렌 증후군 외 기타 자가면역질환에서도 mt-dsRNA라는 새로운 생태 병리학적 마커를 활용해 진단 및 치료 전략을 마련할 수 있을 것ˮ이라고 말했다.
이번 연구는 KAIST-SNUBH End Run 협업 과제, 보건복지부 공익적 의료기술연구사업 및 산업통상자원부 기술혁신프로그램사업의 지원을 받아 수행됐다.
2022.10.31 조회수 10463
RNA를 활용한 자가면역질환 조기진단 및 치료제 개발 앞장설 것
우리 대학 생명화학공학과 김유식 교수와 임성갑 교수, 분당서울대병원 류마티스내과 이윤종 교수 그리고 미국 플로리다주립대 차승희 교수 공동 연구팀이 희귀난치성 자가면역질환인 쉐그렌 증후군(Sjögren’s Syndrome)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
원인불명의 만성 전신 염증 질환인 쉐그렌 증후군은 눈물샘 및 침샘 등 외분비샘을 주로 침범하는 자가면역질환이다. 안구 및 구강건조증 등 외분비샘 기능 저하가 가장 흔한 증상이지만, 외분비샘 외 장기 침범이 다양하고 악성 림프종 합병증에 대한 위험이 특징적으로 수반되고 있다. 주로 중년 여성에게 나타나며 환자 중 약 3분의 1은 림프종, 관절염, 간 손상, 기관지염 등의 다양한 전신증상을 겪으며, 악성 림프종 및 폐 섬유화 합병증으로 조기 사망할 수 있는 무서운 질환이다.
연구팀은 쉐그렌 증후군에서 비정상적인 면역 활성을 유발해 외분비샘 조직 손상을 일으키는 물질로 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)를 제시했다.
이번 연구는 mt-dsRNA라는 쉐그렌 증후군 증상 조절 인자를 최초로 확립해 비침습성 조기 진단법 및 치료제 개발을 위한 이론적 기반을 제공할 것으로 기대된다.
우리 대학 생명화학공학과 윤지민 박사과정생과 이민석 박사가 공동 제1 저자로 참여한 이번 연구는 국제학술지 `몰레큘러 테라피 뉴클레익 에시드(Molecular Therapy – Nucleic Acids)'에 지난 9월 27일 게재됐다. (논문명 : Mitochondrial double-stranded RNAs as a pivotal mediator in the pathogenesis of Sjögren’s syndrome)
쉐그렌 증후군은 질병의 심각성에도 불구하고 지금까지 질환의 병태생리를 대변하는 유전자 마커 없이 환자의 증상을 기반으로 진단이 이뤄지고 있으며 치료제 또한 존재하지 않는 희귀성 난치질환이다. 또한, 쉐그렌 증후군 진단은 이미 외분비샘 조직 손상이 상당히 진행된 후에 가능하고 진단법 역시 증상을 기반으로 해 낮은 질병 특이도를 갖고 있다. 이러한 한계점을 극복하기 위해 연구팀은 질병의 발병 및 진행 메커니즘을 분석해 쉐그렌 증후군의 조기 진단과 치료 효과를 기대할 수 있는 신규 면역 제어 표적 물질을 확립하고자 했다.
쉐그렌 증후군 환자에게서는 특히 이중나선 RNA(dsRNA)를 인지하는 선천성 면역 반응 단백질의 과활성화 그리고 이에 의한 항바이러스성 인터페론 반응이 관찰됐다. 하지만 지금까지 dsRNA가 실제 질환에 관여하는지는 보고된 바 없으며 dsRNA를 표적으로 하는 진단법 및 치료 방향을 탐색한 연구 또한 존재하지 않는다.
세포 내 자연적으로 존재하는 RNA도 dsRNA를 형성해 선천성 면역반응을 조절할 수 있다. 세포 내재 dsRNA를 생성하는 대표적인 세포 내 소기관은 미토콘드리아이며 mt-dsRNA 또한 선천성 면역반응 단백질에 의해 인지되어 인터페론 반응을 유도할 수 있다. 연구팀은 쉐그렌 증후군 환자에서 관찰된 과도한 면역 활성의 특징과 미토콘드리아 기능 이상 등을 고려해 mt-dsRNA가 질환 발병에서 중요한 기능을 할 것이라는 가설을 세우고 연구를 수행했다.
연구팀은 쉐그렌 증후군 환자의 누액과 타액을 분석한 결과 환자 특이적으로 mt-dsRNA의 과발현 현상을 확인했다. 이는 환자의 일차 세포 및 쉐그렌 증후군 모델 생쥐의 손상된 침샘에서도 확인됐다. 연구팀은 이에 mt-dsRNA의 기능을 분석하기 위해 세포 실험을 진행했다. 특히, 타액선 세포주의 3차원 스페로이드 배양 시스템을 구축해 보다 정확한 질병 환경을 모사했다. 그 결과 mt-dsRNA의 발현이 면역 활성이 유발되는 스트레스 상황에서 증가하며 이는 면역 활성의 촉진제 역할을 한다는 것을 연구팀은 규명했다. 특히, mt-dsRNA의 발현을 억제했을 때 면역 활성이 감소하며 질환의 특징이 일부 복원되는 것을 확인했다.
나아가 연구팀은 쉐그렌 증후군 환자의 증상 완화에 활용되는 필로카핀의 치료 메커니즘에서 mt-dsRNA의 기능을 분석했다. 연구팀은 M3R 수용체 작용제인 아세틸콜린이 mt-dsRNA 조절을 통해 면역 활성을 억제하며 쉐그렌 증후군 환자에서 추출된 자가항체가 아세틸콜린을 억제해 과도한 면역 활성을 유발한다는 것을 확인했다. 필로카핀이 아세틸콜린을 모방하는 M3R 작용제임을 고려했을 때, 연구팀은 약물의 효과를 대변할 수 있는 마커로서 mt-dsRNA의 기능성을 검증했다.
생명화학공학과 김유식 교수는 "이번 연구를 통해 난치병으로 인식되고 있는 쉐그렌 증후군에서 mt-dsRNA라는 새로운 병인을 제시했다ˮ면서 "특히, mt-dsRNA 발현량 조절을 통한 면역 과활성화의 완화 효과를 고려했을 때 쉐그렌 증후군 외 기타 자가면역질환에서도 mt-dsRNA라는 새로운 생태 병리학적 마커를 활용해 진단 및 치료 전략을 마련할 수 있을 것ˮ이라고 말했다.
이번 연구는 KAIST-SNUBH End Run 협업 과제, 보건복지부 공익적 의료기술연구사업 및 산업통상자원부 기술혁신프로그램사업의 지원을 받아 수행됐다.
2022.10.31 조회수 10463 -
 RNA 활용해 퇴행성 관절염 획기적 조기진단 가능성 열어
우리 대학 생명화학공학과 김유식 교수와 분당서울대병원 류마티스내과 이윤종 교수 공동 연구팀이 골관절염(Osteoarthritis)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
골관절염은 뼈의 관절면을 감싸고 있는 관절 연골이 마모돼 연골 밑의 뼈가 노출되고, 관절 주변 활액막에 염증이 생겨서 통증과 변형이 발생하는 질환이다. 흔히 퇴행성 관절염이라고도 불리며, 관절 질환 중에서 가장 많이 발생하는 질환이다.
연구팀은 골관절염의 발병 과정 중 손상된 연골에서 염증을 일으켜 세포사멸을 촉진하는 물질이 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)라는 것을 밝혔다.
이번 연구는 골관절염에서 발견되는 다양한 증상들의 원인을 mt-dsRNA라는 개념을 통해 하나로 통합함으로써 골관절염 진단 및 치료에 획기적인 방안을 제시할 것으로 기대된다.
생명화학공학과 박사과정에 재학 중인 김수진 학생과 이건용 학생이 공동 제1 저자로 참여한 이번 연구는 국제학술지 `셀 리포트(Cell Reports)' 지난 8월 9일 字에 게재됐다. (논문명 : Mitochondrial double-stranded RNAs govern the stress response in chondrocytes to promote osteoarthritis development)
골관절염은 우리나라 70세 이상의 여성 인구에서 약 50%의 유병률을 보이는 매우 흔한 질환이다. 골관절염은 일반적으로 노화와 함께 진행되기 때문에 초기에 이들을 구분하는 데 한계가 있다. 골관절염의 진행을 늦추기 위해 증상의 심각성에 따라 약물을 활용한 보존적 치료 혹은 수술을 비롯한 다양한 시도를 활발히 하고 있지만, 기존 접근방법으로 골관절염이 완치될 것이라는 기대를 하기는 어려운 상황이다. 연구팀은 질병의 발병 및 진행 메커니즘을 분석함으로써 골관절염의 조기진단과 완치에 한 걸음 다가갈 수 있는 완전히 새로운 표적 물질을 찾고자 했다.
이중나선 RNA(dsRNA)는 비정상적인 면역반응을 유발해 세포사멸 및 염증반응을 촉진한다고 알려져 있다. dsRNA의 과발현은 다양한 퇴행성 질환과 밀접한 관련이 있어 dsRNA의 조절은 건강한 세포를 유지하기 위해 필수적이다. 세포에서 dsRNA를 생성하는 대표적인 기관은 세포에 에너지를 제공한다고 알려진 미토콘드리아다. 미토콘드리아는 자체 생산하는 dsRNA를 세포질로부터 분리해 dsRNA의 노출과 이에 따른 면역반응을 막는다. 하지만 자극 혹은 세포 스트레스에 의해 mt-dsRNA가 세포질에 노출되면 RNA가 면역반응 단백질에 의해 인지돼 비정상적인 면역반응을 일으킬 수 있다.
연구팀은 골관절염에서 미토콘드리아의 손상과 원인을 알 수 없는 면역반응 단백질의 활성화가 관찰된다는 점에 착안해 mt-dsRNA가 골관절염 발병에서 중요한 기능을 할 것이라는 가설을 세웠다.
연구팀은 연골세포에서 구축한 골관절염 모사 환경에서 mt-dsRNA가 미토콘드리아 외부로 노출돼 선천성 면역반응 단백질에 의해 인지됨에 따라 면역반응을 일으킨다는 것을 확인했다. 또한 골관절염 환자들의 무릎 활막액 및 연골 조직과 골관절염 생쥐 모델의 연골에서도 mt-dsRNA가 유의미하게 증가해 있는 것을 확인했다.
특히, 다른 관절 질환인 류마티스 관절염과 통풍 환자들의 활막액과 비교했을 때 골관절염 환자들의 활막액에서 더 많은 양의 mt-dsRNA가 검출됐다. 또한 초기 골관절염을 앓고 있는 환자들의 연골에서 mt-dsRNA가 많이 증가했다. 따라서 연구팀은 골관절염을 특이적으로 조기진단 할 수 있는 바이오마커로서 mt-dsRNA의 가능성을 제시했다.
더 나아가 연구팀은 골관절염의 전도유망한 치료법 중 하나인 자가포식(Autophagy)의 치료 메커니즘에서 mt-dsRNA의 역할을 규명했다. 연구팀은 자가포식이 세포질에서 mt-dsRNA를 제거함으로써 골관절염의 증상을 완화할 수 있다는 사실을 밝힘으로써 골관절염 치료를 위한 신개념의 표적 물질로서 mt-dsRNA을 제시했다.
생명화학공학과 김유식 교수는 "이번 연구는 세포 수준의 골관절염 모사 환경에서 mt-dsRNA의 기능 규명을 넘어서 실제 골관절염 생쥐 모델의 연골 및 환자의 인체유래물에서 mt-dsRNA의 특이적인 발현 증가를 검증했다ˮ면서 "골관절염처럼 미토콘드리아 손상이 관찰되는 알츠하이머를 비롯한 퇴행성 질환의 발병 메커니즘 분석에 mt-dsRNA를 활용한다면 효과적인 치료전략을 마련하는데 유용할 것ˮ이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 박사과정생 연구장려금 지원사업의 지원을 받아 수행했다.
2022.08.31 조회수 8587
RNA 활용해 퇴행성 관절염 획기적 조기진단 가능성 열어
우리 대학 생명화학공학과 김유식 교수와 분당서울대병원 류마티스내과 이윤종 교수 공동 연구팀이 골관절염(Osteoarthritis)을 유발하는 주요 인자를 찾아냈다고 31일 밝혔다.
골관절염은 뼈의 관절면을 감싸고 있는 관절 연골이 마모돼 연골 밑의 뼈가 노출되고, 관절 주변 활액막에 염증이 생겨서 통증과 변형이 발생하는 질환이다. 흔히 퇴행성 관절염이라고도 불리며, 관절 질환 중에서 가장 많이 발생하는 질환이다.
연구팀은 골관절염의 발병 과정 중 손상된 연골에서 염증을 일으켜 세포사멸을 촉진하는 물질이 미토콘드리아 이중나선 RNA(mitochondrial double-stranded RNA, 이하 mt-dsRNA)라는 것을 밝혔다.
이번 연구는 골관절염에서 발견되는 다양한 증상들의 원인을 mt-dsRNA라는 개념을 통해 하나로 통합함으로써 골관절염 진단 및 치료에 획기적인 방안을 제시할 것으로 기대된다.
생명화학공학과 박사과정에 재학 중인 김수진 학생과 이건용 학생이 공동 제1 저자로 참여한 이번 연구는 국제학술지 `셀 리포트(Cell Reports)' 지난 8월 9일 字에 게재됐다. (논문명 : Mitochondrial double-stranded RNAs govern the stress response in chondrocytes to promote osteoarthritis development)
골관절염은 우리나라 70세 이상의 여성 인구에서 약 50%의 유병률을 보이는 매우 흔한 질환이다. 골관절염은 일반적으로 노화와 함께 진행되기 때문에 초기에 이들을 구분하는 데 한계가 있다. 골관절염의 진행을 늦추기 위해 증상의 심각성에 따라 약물을 활용한 보존적 치료 혹은 수술을 비롯한 다양한 시도를 활발히 하고 있지만, 기존 접근방법으로 골관절염이 완치될 것이라는 기대를 하기는 어려운 상황이다. 연구팀은 질병의 발병 및 진행 메커니즘을 분석함으로써 골관절염의 조기진단과 완치에 한 걸음 다가갈 수 있는 완전히 새로운 표적 물질을 찾고자 했다.
이중나선 RNA(dsRNA)는 비정상적인 면역반응을 유발해 세포사멸 및 염증반응을 촉진한다고 알려져 있다. dsRNA의 과발현은 다양한 퇴행성 질환과 밀접한 관련이 있어 dsRNA의 조절은 건강한 세포를 유지하기 위해 필수적이다. 세포에서 dsRNA를 생성하는 대표적인 기관은 세포에 에너지를 제공한다고 알려진 미토콘드리아다. 미토콘드리아는 자체 생산하는 dsRNA를 세포질로부터 분리해 dsRNA의 노출과 이에 따른 면역반응을 막는다. 하지만 자극 혹은 세포 스트레스에 의해 mt-dsRNA가 세포질에 노출되면 RNA가 면역반응 단백질에 의해 인지돼 비정상적인 면역반응을 일으킬 수 있다.
연구팀은 골관절염에서 미토콘드리아의 손상과 원인을 알 수 없는 면역반응 단백질의 활성화가 관찰된다는 점에 착안해 mt-dsRNA가 골관절염 발병에서 중요한 기능을 할 것이라는 가설을 세웠다.
연구팀은 연골세포에서 구축한 골관절염 모사 환경에서 mt-dsRNA가 미토콘드리아 외부로 노출돼 선천성 면역반응 단백질에 의해 인지됨에 따라 면역반응을 일으킨다는 것을 확인했다. 또한 골관절염 환자들의 무릎 활막액 및 연골 조직과 골관절염 생쥐 모델의 연골에서도 mt-dsRNA가 유의미하게 증가해 있는 것을 확인했다.
특히, 다른 관절 질환인 류마티스 관절염과 통풍 환자들의 활막액과 비교했을 때 골관절염 환자들의 활막액에서 더 많은 양의 mt-dsRNA가 검출됐다. 또한 초기 골관절염을 앓고 있는 환자들의 연골에서 mt-dsRNA가 많이 증가했다. 따라서 연구팀은 골관절염을 특이적으로 조기진단 할 수 있는 바이오마커로서 mt-dsRNA의 가능성을 제시했다.
더 나아가 연구팀은 골관절염의 전도유망한 치료법 중 하나인 자가포식(Autophagy)의 치료 메커니즘에서 mt-dsRNA의 역할을 규명했다. 연구팀은 자가포식이 세포질에서 mt-dsRNA를 제거함으로써 골관절염의 증상을 완화할 수 있다는 사실을 밝힘으로써 골관절염 치료를 위한 신개념의 표적 물질로서 mt-dsRNA을 제시했다.
생명화학공학과 김유식 교수는 "이번 연구는 세포 수준의 골관절염 모사 환경에서 mt-dsRNA의 기능 규명을 넘어서 실제 골관절염 생쥐 모델의 연골 및 환자의 인체유래물에서 mt-dsRNA의 특이적인 발현 증가를 검증했다ˮ면서 "골관절염처럼 미토콘드리아 손상이 관찰되는 알츠하이머를 비롯한 퇴행성 질환의 발병 메커니즘 분석에 mt-dsRNA를 활용한다면 효과적인 치료전략을 마련하는데 유용할 것ˮ이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 박사과정생 연구장려금 지원사업의 지원을 받아 수행했다.
2022.08.31 조회수 8587 -
 개인 맞춤형 암 치료에 한 발짝 다가서
우리 연구진이 급성골수성백혈병(Acute myeloid leukemia)과 골수이형성증후군(Myelodysplastic syndromes) 치료에 사용되는 항암 화학 치료제 중 하나인 데시타빈(decitabine)의 인체 내 작용 메커니즘을 규명해 항암제 효과가 있는 환자와 없는 환자를 구별해 낼 수 있는 유전자 발굴에 성공했다.
이번 연구를 통해 환자별로 적합한 치료를 받을 수 있게 되면 환자들이 치료에 드는 경제적 지출과 시간적 소비 또한 확연하게 줄일 수 있을 것으로 기대된다.
우리 대학 생명화학공학과 김유식 교수와 서울대병원 혈액암센터 홍준식 교수 공동 연구팀이 항암 화학치료에서 작용하는 주요 인자를 찾아냈다고 7일 밝혔다.
생명화학공학과 박사과정에 재학 중인 구용석 학생, 서울대병원 박주환 연구원 그리고 우리 대학 조령은 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `미국국립과학원회보(PNAS)' 3월 30일 字에 게재됐다. (논문명: Noncanonical immune response to the inhibition of DNA methylation via stabilization of endogenous retrovirus dsRNAs)
데시타빈과 같은 DNA 탈메틸화제(DNA demethylating agent)는 DNA 복제과정에 참여하고 DNA상에 존재하는 메틸기(-CH₃)를 제거해 유전자 발현을 조절한다. 특히 암세포에는 일반 세포보다 많은 양의 DNA가 메틸화돼 있으며, 이는 DNA에서 RNA를 생성하는 전사 과정을 억제하는 역할을 한다. 세포에 탈메틸화제 처리를 하면 DNA상에 메틸기가 제거돼 세포 내에 수많은 종류의 RNA들이 생성된다.
이렇게 데시타빈에 의해 조절되는 RNA 중에는 이중나선 RNA (double-stranded RNA, 이하 dsRNA)가 있다. 원래 dsRNA는 바이러스에 감염된 세포에서 많이 생산되며, 인간 세포는 바이러스에서 유래된 dsRNA를 외부 물질로 인지해 면역반응을 일으킨다.
특이하게도 dsRNA를 인지하는 인간의 선천성 면역반응 시스템은 핵산 서열 정보를 무시한 채 dsRNA의 길이나 말단 형태와 같은 구조적 특징을 이용해 dsRNA와 반응한다. 이와 같은 특징 때문에 꼭 바이러스에서 유래된 dsRNA가 아니라 체내에서 생성된 dsRNA 또한 외부 물질로 오인돼 비정상적인 면역반응을 일으킬 수 있다. 암 치료에서는 DNA 탈메틸화제 처리로 dsRNA의 발현량을 증가시키고 이는 dsRNA에 의한 면역 활성으로 이어져 암세포만의 세포사멸이 일어나게 된다.
연구팀은 이러한 데시타빈에 의한 dsRNA 발현증가 그리고 dsRNA에 의한 세포사멸을 조절하는 유전자를 연구했다. 특히, DNA 탈메틸화제를 투여받은 환자 중 많은 수의 환자가 약물의 효과를 보지 못한다는 점에 착안해 dsRNA와 상호작용하는 다양한 dsRNA 결합 단백질을 분석했다.
그 결과로 dsRNA와 직접 결합해 dsRNA의 안정성을 조절하는 단백질인 `스타우펜1(이하 Staufen1)'이 데시타빈에 의한 세포 반응에 중요한 기능을 한다는 것을 최초로 규명했다. Staufen1의 발현이 억제된 세포에서는 dsRNA가 빠르게 제거돼 하위 면역반응이 일어나지 않았으며 암세포의 사멸도 관찰되지 않았다.
연구팀은 데시타빈 뿐만 아니라 아자시티딘(azacitidine)과 같은 DNA 탈메틸화제를 투여받은 급성골수성백혈병과 골수이형성증후군 환자 46명의 골수추출액에서 Staufen1 유전자의 발현양상을 분석했고, 그 결과 약물의 효과를 보지 못한 환자에게서는 Staufen1의 발현이 유의미하게 감소해 있다는 것을 확인했다. 또한, Staufen1의 발현이 낮은 환자는 생존율(overall survival)과 무진행 생존율(progression-free survival)이 모두 낮아 환자의 예후가 좋지 않다는 것을 확인했다.
생명화학공학과 김유식 교수는 "이번 연구에서는 단순 데시타빈 항암제의 작용기전 규명을 넘어서 실제 데시타빈을 투여받은 환자의 검체에서도 그 효과를 검증했다ˮ면서 "추후 이번에 찾은 유전자의 바이오마커화를 통해 데시타빈과 아자시티딘과 같은 DNA 탈메틸화제의 효과를 예측할 수 있어 효과적인 맞춤형 암 치료전략을 마련하는데 유용할 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원을 받아 수행됐다.
2021.04.07 조회수 80304
개인 맞춤형 암 치료에 한 발짝 다가서
우리 연구진이 급성골수성백혈병(Acute myeloid leukemia)과 골수이형성증후군(Myelodysplastic syndromes) 치료에 사용되는 항암 화학 치료제 중 하나인 데시타빈(decitabine)의 인체 내 작용 메커니즘을 규명해 항암제 효과가 있는 환자와 없는 환자를 구별해 낼 수 있는 유전자 발굴에 성공했다.
이번 연구를 통해 환자별로 적합한 치료를 받을 수 있게 되면 환자들이 치료에 드는 경제적 지출과 시간적 소비 또한 확연하게 줄일 수 있을 것으로 기대된다.
우리 대학 생명화학공학과 김유식 교수와 서울대병원 혈액암센터 홍준식 교수 공동 연구팀이 항암 화학치료에서 작용하는 주요 인자를 찾아냈다고 7일 밝혔다.
생명화학공학과 박사과정에 재학 중인 구용석 학생, 서울대병원 박주환 연구원 그리고 우리 대학 조령은 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `미국국립과학원회보(PNAS)' 3월 30일 字에 게재됐다. (논문명: Noncanonical immune response to the inhibition of DNA methylation via stabilization of endogenous retrovirus dsRNAs)
데시타빈과 같은 DNA 탈메틸화제(DNA demethylating agent)는 DNA 복제과정에 참여하고 DNA상에 존재하는 메틸기(-CH₃)를 제거해 유전자 발현을 조절한다. 특히 암세포에는 일반 세포보다 많은 양의 DNA가 메틸화돼 있으며, 이는 DNA에서 RNA를 생성하는 전사 과정을 억제하는 역할을 한다. 세포에 탈메틸화제 처리를 하면 DNA상에 메틸기가 제거돼 세포 내에 수많은 종류의 RNA들이 생성된다.
이렇게 데시타빈에 의해 조절되는 RNA 중에는 이중나선 RNA (double-stranded RNA, 이하 dsRNA)가 있다. 원래 dsRNA는 바이러스에 감염된 세포에서 많이 생산되며, 인간 세포는 바이러스에서 유래된 dsRNA를 외부 물질로 인지해 면역반응을 일으킨다.
특이하게도 dsRNA를 인지하는 인간의 선천성 면역반응 시스템은 핵산 서열 정보를 무시한 채 dsRNA의 길이나 말단 형태와 같은 구조적 특징을 이용해 dsRNA와 반응한다. 이와 같은 특징 때문에 꼭 바이러스에서 유래된 dsRNA가 아니라 체내에서 생성된 dsRNA 또한 외부 물질로 오인돼 비정상적인 면역반응을 일으킬 수 있다. 암 치료에서는 DNA 탈메틸화제 처리로 dsRNA의 발현량을 증가시키고 이는 dsRNA에 의한 면역 활성으로 이어져 암세포만의 세포사멸이 일어나게 된다.
연구팀은 이러한 데시타빈에 의한 dsRNA 발현증가 그리고 dsRNA에 의한 세포사멸을 조절하는 유전자를 연구했다. 특히, DNA 탈메틸화제를 투여받은 환자 중 많은 수의 환자가 약물의 효과를 보지 못한다는 점에 착안해 dsRNA와 상호작용하는 다양한 dsRNA 결합 단백질을 분석했다.
그 결과로 dsRNA와 직접 결합해 dsRNA의 안정성을 조절하는 단백질인 `스타우펜1(이하 Staufen1)'이 데시타빈에 의한 세포 반응에 중요한 기능을 한다는 것을 최초로 규명했다. Staufen1의 발현이 억제된 세포에서는 dsRNA가 빠르게 제거돼 하위 면역반응이 일어나지 않았으며 암세포의 사멸도 관찰되지 않았다.
연구팀은 데시타빈 뿐만 아니라 아자시티딘(azacitidine)과 같은 DNA 탈메틸화제를 투여받은 급성골수성백혈병과 골수이형성증후군 환자 46명의 골수추출액에서 Staufen1 유전자의 발현양상을 분석했고, 그 결과 약물의 효과를 보지 못한 환자에게서는 Staufen1의 발현이 유의미하게 감소해 있다는 것을 확인했다. 또한, Staufen1의 발현이 낮은 환자는 생존율(overall survival)과 무진행 생존율(progression-free survival)이 모두 낮아 환자의 예후가 좋지 않다는 것을 확인했다.
생명화학공학과 김유식 교수는 "이번 연구에서는 단순 데시타빈 항암제의 작용기전 규명을 넘어서 실제 데시타빈을 투여받은 환자의 검체에서도 그 효과를 검증했다ˮ면서 "추후 이번에 찾은 유전자의 바이오마커화를 통해 데시타빈과 아자시티딘과 같은 DNA 탈메틸화제의 효과를 예측할 수 있어 효과적인 맞춤형 암 치료전략을 마련하는데 유용할 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원을 받아 수행됐다.
2021.04.07 조회수 80304 -
 다양한 바이러스 감염병을 쉽고 빠르게 찾아내는 만능 진단기술 개발
우리 연구진이 감염된 세포의 용해액만으로도 바이러스의 존재 여부를 핵산 증폭 없이 판독이 가능한 신기술을 개발했다. 이 기술은 바이러스의 특이적으로 존재한다고 알려진 ‘이중나선 RNA(이하 dsRNA)’검출을 기반으로 한다.
이 기술이 실용화되면 현재의 유전자 증폭(PCR) 검사와는 달리 시료 준비나 핵산 증폭, RNA 핵산 서열 정보가 필요 없어 각종 바이러스 감염병이나 신·변종 바이러스를 쉽고 빠르게 진단하는 기술이나 키트(Kit) 등을 개발하는 데 큰 도움이 될 것으로 기대된다.
우리 대학 생명화학공학과 리섕·김유식 교수 공동연구팀은 바이러스의 특징을 이용해 다양한 종류의 바이러스를 검출할 수 있는 만능 진단기술을 개발했다고 28일 밝혔다. 생명화학공학과 박사과정에 재학 중인 구자영, 김수라 학생이 공동 제1 저자로 참여한 이번 연구결과는 국제 학술지 `바이오마크로몰레큘스(Biomacromolecules' 4월 9일 字 온라인 판에 게재됐다. (논문명: Reactive Polymer Targeting dsRNA as Universal Virus Detection Platform with Enhanced Sensitivity).
RNA(리보핵산)는 일반적으로 DNA(디옥시리보핵산)가 가진 유전정보를 운반해 단백질을 생산하게 한다. 그러나 단백질을 만들지 않는 다양한 `비번역 RNA(non-coding RNA)'가 존재하는데 이들은 세포 내 신호전달, 유전자 발현 조절, 그리고 RNA 효소적 작용 등의 다양한 역할을 맡는다. 이러한 비번역 RNA들에 상보적인 핵산 서열을 가지는 RNA가 결합해 형성된 `dsRNA'는 특히 바이러스에서 특이적으로 많이 발견된다.
dsRNA는 DNA 바이러스의 전사 또는 RNA 바이러스의 복제 과정에서 생산되는데, 인간 세포는 바이러스 dsRNA를 외부 물질로 인지해 면역반응을 일으킨다. 특이하게도 바이러스 dsRNA를 인지하는 인간의 선천성 면역반응시스템은 핵산 서열 정보를 무시한 채 dsRNA의 길이나 말단 구조와 같은 형태적 특징을 이용해 dsRNA와 반응한다. 인간 면역체계가 다양한 종류의 바이러스에 대처를 가능케 하는 이유다.
공동연구팀은 이런 인간 면역체계의 원리에 착안해 바이러스의 특징인 길이가 긴 dsRNA를 검출할 수 있는 기판 제작을 통해 다양한 종류의 바이러스를 핵산 서열 정보 없이 검출할 수 있도록 했다. 실리카 기판 표면에는 펜타 플루오르 페닐 아크릴레이트(PPFPA) 반응성 고분자를 코팅해 높은 효율로 빠르고 간편하게 dsRNA를 인지하는 항체를 고정시켰다. 이렇게 개발된 기판에서 면역반응을 일으키는 76bp(base pair, 염기 쌍 개수를 의미하는 길이 단위) 이상의 긴 길이를 가지는 dsRNA를 검출할 수 있었다. 또한, 감염이 되지 않은 세포에서 발견되는 단일 가닥 RNA와 함께 19bp의 짧은 dsRNA는 전혀 검출되지 않아 바이러스 감염 진단용으로 활용 가능성을 확인했다.
연구팀은 이어 바이러스 dsRNA의 긴 길이를 활용한 2단계 검출 방법을 찾기 위해 많은 도전 끝에 특이도 및 민감도가 향상된 바이러스 dsRNA 검출기술을 개발하는 데 성공했다.
연구팀은 이와 함께 시료 준비과정도 대폭 간편화시켜 세포에서 RNA를 분리하거나 정제 작업 없이 감염된 세포의 용해액만을 이용해 바이러스 dsRNA를 검출할 수 있는 기술을 개발했다. 이 기술을 A형과 C형 간염 바이러스에 감염된 세포에 적용한 결과, 바이러스 dsRNA의 존재 여부를 핵산 증폭 없이 판독하는 데에도 성공했다.
KAIST 생명화학공학과 리섕 교수는 "이번 연구에서는 A형 간염과 C형 간염 dsRNA만을 검출했지만, 바이러스 dsRNA는 다양한 종류의 바이러스에서 발견된다ˮ 면서 "이번에 개발한 dsRNA 검출기술은 다양한 바이러스에 적용 가능해 만능 감염병 진단기술로 발전될 수 있고, 특히 공항·학교 등 공공장소에서도 쉽고 빠르게 감염병을 검출할 수 있어 효과적인 방역대책을 마련하는데 유용할 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 국방과학연구소 순수기초연구 용역사업에 지원을 받아 수행됐다.
2020.06.01 조회수 16647
다양한 바이러스 감염병을 쉽고 빠르게 찾아내는 만능 진단기술 개발
우리 연구진이 감염된 세포의 용해액만으로도 바이러스의 존재 여부를 핵산 증폭 없이 판독이 가능한 신기술을 개발했다. 이 기술은 바이러스의 특이적으로 존재한다고 알려진 ‘이중나선 RNA(이하 dsRNA)’검출을 기반으로 한다.
이 기술이 실용화되면 현재의 유전자 증폭(PCR) 검사와는 달리 시료 준비나 핵산 증폭, RNA 핵산 서열 정보가 필요 없어 각종 바이러스 감염병이나 신·변종 바이러스를 쉽고 빠르게 진단하는 기술이나 키트(Kit) 등을 개발하는 데 큰 도움이 될 것으로 기대된다.
우리 대학 생명화학공학과 리섕·김유식 교수 공동연구팀은 바이러스의 특징을 이용해 다양한 종류의 바이러스를 검출할 수 있는 만능 진단기술을 개발했다고 28일 밝혔다. 생명화학공학과 박사과정에 재학 중인 구자영, 김수라 학생이 공동 제1 저자로 참여한 이번 연구결과는 국제 학술지 `바이오마크로몰레큘스(Biomacromolecules' 4월 9일 字 온라인 판에 게재됐다. (논문명: Reactive Polymer Targeting dsRNA as Universal Virus Detection Platform with Enhanced Sensitivity).
RNA(리보핵산)는 일반적으로 DNA(디옥시리보핵산)가 가진 유전정보를 운반해 단백질을 생산하게 한다. 그러나 단백질을 만들지 않는 다양한 `비번역 RNA(non-coding RNA)'가 존재하는데 이들은 세포 내 신호전달, 유전자 발현 조절, 그리고 RNA 효소적 작용 등의 다양한 역할을 맡는다. 이러한 비번역 RNA들에 상보적인 핵산 서열을 가지는 RNA가 결합해 형성된 `dsRNA'는 특히 바이러스에서 특이적으로 많이 발견된다.
dsRNA는 DNA 바이러스의 전사 또는 RNA 바이러스의 복제 과정에서 생산되는데, 인간 세포는 바이러스 dsRNA를 외부 물질로 인지해 면역반응을 일으킨다. 특이하게도 바이러스 dsRNA를 인지하는 인간의 선천성 면역반응시스템은 핵산 서열 정보를 무시한 채 dsRNA의 길이나 말단 구조와 같은 형태적 특징을 이용해 dsRNA와 반응한다. 인간 면역체계가 다양한 종류의 바이러스에 대처를 가능케 하는 이유다.
공동연구팀은 이런 인간 면역체계의 원리에 착안해 바이러스의 특징인 길이가 긴 dsRNA를 검출할 수 있는 기판 제작을 통해 다양한 종류의 바이러스를 핵산 서열 정보 없이 검출할 수 있도록 했다. 실리카 기판 표면에는 펜타 플루오르 페닐 아크릴레이트(PPFPA) 반응성 고분자를 코팅해 높은 효율로 빠르고 간편하게 dsRNA를 인지하는 항체를 고정시켰다. 이렇게 개발된 기판에서 면역반응을 일으키는 76bp(base pair, 염기 쌍 개수를 의미하는 길이 단위) 이상의 긴 길이를 가지는 dsRNA를 검출할 수 있었다. 또한, 감염이 되지 않은 세포에서 발견되는 단일 가닥 RNA와 함께 19bp의 짧은 dsRNA는 전혀 검출되지 않아 바이러스 감염 진단용으로 활용 가능성을 확인했다.
연구팀은 이어 바이러스 dsRNA의 긴 길이를 활용한 2단계 검출 방법을 찾기 위해 많은 도전 끝에 특이도 및 민감도가 향상된 바이러스 dsRNA 검출기술을 개발하는 데 성공했다.
연구팀은 이와 함께 시료 준비과정도 대폭 간편화시켜 세포에서 RNA를 분리하거나 정제 작업 없이 감염된 세포의 용해액만을 이용해 바이러스 dsRNA를 검출할 수 있는 기술을 개발했다. 이 기술을 A형과 C형 간염 바이러스에 감염된 세포에 적용한 결과, 바이러스 dsRNA의 존재 여부를 핵산 증폭 없이 판독하는 데에도 성공했다.
KAIST 생명화학공학과 리섕 교수는 "이번 연구에서는 A형 간염과 C형 간염 dsRNA만을 검출했지만, 바이러스 dsRNA는 다양한 종류의 바이러스에서 발견된다ˮ 면서 "이번에 개발한 dsRNA 검출기술은 다양한 바이러스에 적용 가능해 만능 감염병 진단기술로 발전될 수 있고, 특히 공항·학교 등 공공장소에서도 쉽고 빠르게 감염병을 검출할 수 있어 효과적인 방역대책을 마련하는데 유용할 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 국방과학연구소 순수기초연구 용역사업에 지원을 받아 수행됐다.
2020.06.01 조회수 16647 -
 암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
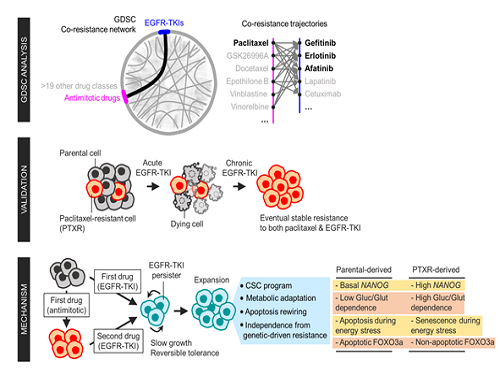
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17 조회수 15014
암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17 조회수 15014