%EB%B0%95%ED%85%8C%EB%A6%AC%EC%95%84
-
 슈퍼박테리아 방패 ‘바이오필름’ 무력화 치료 플랫폼 개발
병원 내 감염의 주요 원인 중 하나로 알려진 슈퍼박테리아 ‘메티실린 내성 황색포도상구균(MRSA, 이하 포도상구균)’은 기존 항생제에 대한 높은 내성뿐 아니라 강력한 미생물막인 바이오필름(biofilm)을 형성함으로써 외부 치료제를 효과적으로 차단한다. 이에 우리 연구진은 국제 연구진과 함께 미세방울(microbubble)을 이용해 유전자 표적 나노입자를 전달하여 바이오필름을 무너뜨리고 기존 항생제가 무력한 감염증에 대한 혁신적 해결책을 제시하는 플랫폼 개발에 성공했다.
우리 대학 생명과학과 정현정 교수 연구팀이 미국 일리노이대 공현준 교수팀과의 공동연구를 통해, 포도상구균이 형성한 세균성 바이오필름을 효과적으로 제거하기 위해 유전자 억제제를 세균 내부로 정확하게 전달하는 미세방울 기반 나노-유전자 전달 플랫폼(BTN‑MB)를 개발했다고 29일 밝혔다.
연구팀은 먼저, 포도상구균의 주요 유전자 3종<바이오필름 형성(icaA), 세포 분열(ftsZ), 항생제 내성(mecA)>을 동시에 억제하는 짧은 DNA 조각(oligonucleotide)을 설계하고, 이를 탑재해 균내로 효과적으로 전달할 수 있는 나노입자(BTN)를 고안했다.
여기에 더해, 미세방울(microbubble, 이하 MB)을 사용해 포도상구균이 형성한 바이오필름인 미생물막의 투과성을 높인다. 연구팀은 두 가지 기술을 병용해, 세균의 증식과 내성 획득을 원천적으로 차단하는 이중 타격 전략을 구현했다.
이 치료 시스템은 두 단계로 작동한다. 먼저, 미세방울(MB)이 포도상구균이 형성한 세균성 생체막내 압력 변화로 나노입자(BTN)의 침투를 가능하게 만든다. 이어서, BTN이 생체막의 틈을 타 세균 내부로 침투해 유전자 억제제를 정확하게 전달한다. 이를 통해 포도상구균의 유전자 조절을 일으켜 생체막 재형성, 세포 증식, 그리고 항생제 내성 발현이 동시에 차단된다.
돼지 피부 감염 생체막 모델과 포도상구균 감염 마우스 상처 모델에서 시행한 실험 결과, BTN‑MB 치료군은 생체막 두께가 크게 감소했으며, 세균 수와 염증 반응도 현저히 줄어드는 뛰어난 치료 효과를 확인할 수 있었다.
이러한 결과는 기존 항생제 단독 치료로는 달성하기 어려운 수준이며, 향후 다양한 내성균 감염 치료에도 적용할 수 있는 가능성을 보여준다.
연구를 주도한 정현정 교수는 “이번 연구는 기존 항생제로는 해결할 수 없는 슈퍼박테리아 감염에 대해 나노기술, 유전자 억제, 물리적 접근법을 융합해 새로운 치료 해법을 제시한 것”이라며, “향후 전신 적용 및 다양한 감염 질환으로의 확장을 목표로 연구를 지속할 것”이라고 설명했다.
해당 연구는 우리 대학 생명과학과 정주연 학생과 일리노이대 안유진 박사가 제1 저자로 참여했으며, 국제학술지‘어드밴스드 펑셔널 머터리얼스(Advanced Functional Materials)’에 5월 19일 자로 온라인 게재됐다.
※ 논문 제목: Microbubble-Controlled Delivery of Biofilm-Targeting Nanoparticles to Treat MRSA Infection
※ DOI: https://doi.org/10.1002/adfm.202508291
한편, 이번 연구는 한국연구재단과 보건복지부의 지원을 받아 수행됐다.
2025.05.29 조회수 2018
슈퍼박테리아 방패 ‘바이오필름’ 무력화 치료 플랫폼 개발
병원 내 감염의 주요 원인 중 하나로 알려진 슈퍼박테리아 ‘메티실린 내성 황색포도상구균(MRSA, 이하 포도상구균)’은 기존 항생제에 대한 높은 내성뿐 아니라 강력한 미생물막인 바이오필름(biofilm)을 형성함으로써 외부 치료제를 효과적으로 차단한다. 이에 우리 연구진은 국제 연구진과 함께 미세방울(microbubble)을 이용해 유전자 표적 나노입자를 전달하여 바이오필름을 무너뜨리고 기존 항생제가 무력한 감염증에 대한 혁신적 해결책을 제시하는 플랫폼 개발에 성공했다.
우리 대학 생명과학과 정현정 교수 연구팀이 미국 일리노이대 공현준 교수팀과의 공동연구를 통해, 포도상구균이 형성한 세균성 바이오필름을 효과적으로 제거하기 위해 유전자 억제제를 세균 내부로 정확하게 전달하는 미세방울 기반 나노-유전자 전달 플랫폼(BTN‑MB)를 개발했다고 29일 밝혔다.
연구팀은 먼저, 포도상구균의 주요 유전자 3종<바이오필름 형성(icaA), 세포 분열(ftsZ), 항생제 내성(mecA)>을 동시에 억제하는 짧은 DNA 조각(oligonucleotide)을 설계하고, 이를 탑재해 균내로 효과적으로 전달할 수 있는 나노입자(BTN)를 고안했다.
여기에 더해, 미세방울(microbubble, 이하 MB)을 사용해 포도상구균이 형성한 바이오필름인 미생물막의 투과성을 높인다. 연구팀은 두 가지 기술을 병용해, 세균의 증식과 내성 획득을 원천적으로 차단하는 이중 타격 전략을 구현했다.
이 치료 시스템은 두 단계로 작동한다. 먼저, 미세방울(MB)이 포도상구균이 형성한 세균성 생체막내 압력 변화로 나노입자(BTN)의 침투를 가능하게 만든다. 이어서, BTN이 생체막의 틈을 타 세균 내부로 침투해 유전자 억제제를 정확하게 전달한다. 이를 통해 포도상구균의 유전자 조절을 일으켜 생체막 재형성, 세포 증식, 그리고 항생제 내성 발현이 동시에 차단된다.
돼지 피부 감염 생체막 모델과 포도상구균 감염 마우스 상처 모델에서 시행한 실험 결과, BTN‑MB 치료군은 생체막 두께가 크게 감소했으며, 세균 수와 염증 반응도 현저히 줄어드는 뛰어난 치료 효과를 확인할 수 있었다.
이러한 결과는 기존 항생제 단독 치료로는 달성하기 어려운 수준이며, 향후 다양한 내성균 감염 치료에도 적용할 수 있는 가능성을 보여준다.
연구를 주도한 정현정 교수는 “이번 연구는 기존 항생제로는 해결할 수 없는 슈퍼박테리아 감염에 대해 나노기술, 유전자 억제, 물리적 접근법을 융합해 새로운 치료 해법을 제시한 것”이라며, “향후 전신 적용 및 다양한 감염 질환으로의 확장을 목표로 연구를 지속할 것”이라고 설명했다.
해당 연구는 우리 대학 생명과학과 정주연 학생과 일리노이대 안유진 박사가 제1 저자로 참여했으며, 국제학술지‘어드밴스드 펑셔널 머터리얼스(Advanced Functional Materials)’에 5월 19일 자로 온라인 게재됐다.
※ 논문 제목: Microbubble-Controlled Delivery of Biofilm-Targeting Nanoparticles to Treat MRSA Infection
※ DOI: https://doi.org/10.1002/adfm.202508291
한편, 이번 연구는 한국연구재단과 보건복지부의 지원을 받아 수행됐다.
2025.05.29 조회수 2018 -
 당뇨병 만성상처 추적 스마트 헬스케어 기기 개발
우리 대학 연구팀이 당뇨병 등 상처 부위의 시공간 온도 변화 및 열전달 특성 추적을 통해 상처 치유 과정을 효과적으로 모니터링할 수 있는 무선 시스템을 개발했다.
전기및전자공학부 권경하 교수팀이 중앙대학교 류한준 교수와 상처 치유 과정을 실시간으로 추적해 적절한 치료를 제공할 수 있게 해주는 디지털 헬스케어 기술을 개발했다고 5일 밝혔다.
피부는 유해 물질로부터 인체를 보호하는 장벽 기능을 한다. 피부 손상은 집중 치료가 필요한 환자들에게 감염과 관련된 심각한 건강 위험을 초래할 수 있다. 특히 당뇨병 환자의 경우, 정상적인 혈액 순환과 상처 치유 과정에 문제가 생겨 만성 상처가 쉽게 발생한다. 이러한 만성 상처의 재생을 위해 미국에서만 매년 수백억 달러의 의료 비용이 지출되고 있다. 상처 치유를 촉진하는 다양한 방법이 있지만, 환자별 상처 상태에 따라 맞춤 관리가 필요하다.
이에 연구팀은 상처 부위와 주변 건강한 피부 사이의 온도 차이를 활용해 상처 내 발열 반응을 추적했으며, 열 전송 특성을 측정해 피부 표면 근처의 수분 변화를 관찰함으로써 흉터 조직의 형성 과정을 파악할 수 있는 기반으로 활용했다. 연구팀은 당뇨병이 있는 쥐를 통해 병적 상태에서 상처 치유가 지연되는 과정에서 실험을 진행했고, 수집된 데이터가 상처 치유 과정과 흉터 조직 형성을 정확히 추적할 수 있음을 입증했다.
해당 시스템은 상처가 치유된 후에 기기를 제거하는 과정에서 발생할 수 있는 조직 손상을 최소화하기 위해, 체내에서 자연 분해가 가능한 생분해성 센서 모듈과 통합됐다. 이 생분해성 모듈은 사용 후 별도로 제거할 필요 없이 몸속에서 저절로 분해되어 사라지므로, 추가적인 불편함이나 조직 손상의 위험을 최소화한다. 생분해성 재료를 사용한 이 장치는 사용 후 제거할 필요가 없으므로 상처 부위 내부에서도 모니터링할 수 있는 가능성을 제시한다.
연구를 주도한 권경하 교수는 "상처 부위의 온도와 열전달 특성을 지속적으로 모니터링함으로써, 의료 전문가들이 당뇨병 환자의 상처 상태를 더 정확하게 파악하고 적절한 치료를 제공할 수 있게 될 것으로 기대된다ˮ면서 "생분해성 센서를 사용해 상처 치유가 완료된 후 장치를 제거할 필요 없이 안전하게 분해될 수 있어, 병원뿐만 아니라 가정에서도 실시간 모니터링이 가능해질 것ˮ이라고 말했다.
연구팀은 향후 이 기기를 항균 특성을 가진 재료와 통합해, 염증 반응, 박테리아 감염 및 기타 병변을 관측 및 예방하는 기술로 확장할 계획이다. 온도 및 열전달 특성 변화를 통해 감염 수준을 감지 함으로써 병원이나 가정에서 실시간으로 사용할 수 있는 항균, 범용 상처 모니터링 플랫폼을 제공하는 것을 목표로 한다.
이번 연구 결과는 국제 학술지 `어드밴스드 헬스케어 머티리얼스(Advanced Healthcare Materials)'에 지난 2월 19일 발표됐으며, 표지 논문(Inside Back Cover Journal)으로 선정됐다. (논문명 : Materials and Device Designs for Wireless Monitoring of Temperature and Thermal Transport Properties of Wound Beds during Healing)
한편, 이번 연구는 한국연구재단의 기초연구사업, 지역혁신선도연구센터사업 및 BK21의 지원을 받아 수행됐다.
2024.03.05 조회수 8009
당뇨병 만성상처 추적 스마트 헬스케어 기기 개발
우리 대학 연구팀이 당뇨병 등 상처 부위의 시공간 온도 변화 및 열전달 특성 추적을 통해 상처 치유 과정을 효과적으로 모니터링할 수 있는 무선 시스템을 개발했다.
전기및전자공학부 권경하 교수팀이 중앙대학교 류한준 교수와 상처 치유 과정을 실시간으로 추적해 적절한 치료를 제공할 수 있게 해주는 디지털 헬스케어 기술을 개발했다고 5일 밝혔다.
피부는 유해 물질로부터 인체를 보호하는 장벽 기능을 한다. 피부 손상은 집중 치료가 필요한 환자들에게 감염과 관련된 심각한 건강 위험을 초래할 수 있다. 특히 당뇨병 환자의 경우, 정상적인 혈액 순환과 상처 치유 과정에 문제가 생겨 만성 상처가 쉽게 발생한다. 이러한 만성 상처의 재생을 위해 미국에서만 매년 수백억 달러의 의료 비용이 지출되고 있다. 상처 치유를 촉진하는 다양한 방법이 있지만, 환자별 상처 상태에 따라 맞춤 관리가 필요하다.
이에 연구팀은 상처 부위와 주변 건강한 피부 사이의 온도 차이를 활용해 상처 내 발열 반응을 추적했으며, 열 전송 특성을 측정해 피부 표면 근처의 수분 변화를 관찰함으로써 흉터 조직의 형성 과정을 파악할 수 있는 기반으로 활용했다. 연구팀은 당뇨병이 있는 쥐를 통해 병적 상태에서 상처 치유가 지연되는 과정에서 실험을 진행했고, 수집된 데이터가 상처 치유 과정과 흉터 조직 형성을 정확히 추적할 수 있음을 입증했다.
해당 시스템은 상처가 치유된 후에 기기를 제거하는 과정에서 발생할 수 있는 조직 손상을 최소화하기 위해, 체내에서 자연 분해가 가능한 생분해성 센서 모듈과 통합됐다. 이 생분해성 모듈은 사용 후 별도로 제거할 필요 없이 몸속에서 저절로 분해되어 사라지므로, 추가적인 불편함이나 조직 손상의 위험을 최소화한다. 생분해성 재료를 사용한 이 장치는 사용 후 제거할 필요가 없으므로 상처 부위 내부에서도 모니터링할 수 있는 가능성을 제시한다.
연구를 주도한 권경하 교수는 "상처 부위의 온도와 열전달 특성을 지속적으로 모니터링함으로써, 의료 전문가들이 당뇨병 환자의 상처 상태를 더 정확하게 파악하고 적절한 치료를 제공할 수 있게 될 것으로 기대된다ˮ면서 "생분해성 센서를 사용해 상처 치유가 완료된 후 장치를 제거할 필요 없이 안전하게 분해될 수 있어, 병원뿐만 아니라 가정에서도 실시간 모니터링이 가능해질 것ˮ이라고 말했다.
연구팀은 향후 이 기기를 항균 특성을 가진 재료와 통합해, 염증 반응, 박테리아 감염 및 기타 병변을 관측 및 예방하는 기술로 확장할 계획이다. 온도 및 열전달 특성 변화를 통해 감염 수준을 감지 함으로써 병원이나 가정에서 실시간으로 사용할 수 있는 항균, 범용 상처 모니터링 플랫폼을 제공하는 것을 목표로 한다.
이번 연구 결과는 국제 학술지 `어드밴스드 헬스케어 머티리얼스(Advanced Healthcare Materials)'에 지난 2월 19일 발표됐으며, 표지 논문(Inside Back Cover Journal)으로 선정됐다. (논문명 : Materials and Device Designs for Wireless Monitoring of Temperature and Thermal Transport Properties of Wound Beds during Healing)
한편, 이번 연구는 한국연구재단의 기초연구사업, 지역혁신선도연구센터사업 및 BK21의 지원을 받아 수행됐다.
2024.03.05 조회수 8009 -
 산업 균주 제작 및 병원균 억제 범용기술 개발
박테리아는 우리 일상에서 김치, 된장, 술 등 식품에 활용되어 왔을 뿐만 아니라 최근에는 대사 공학을 통해 플라스틱, 영양제, 사료, 의약품 등을 생산하는 산업용 세포 공장으로 활약하고 있다. 하지만 유익한 박테리아 외에도 다양한 감염성 질병을 일으키는 폐렴균, 살모넬라균 등 병원균이 있어 대사공학적 기법을 통해 유해한 병원균은 병원성을 억제하거나 사멸을 유도하고, 유익한 산업용 박테리아는 고부가가치 물질을 고효율로 생산할 수 있도록 조작하는 것이 중요하다.
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 그람 음성균과 양성균 모두를 포함한 다양한 박테리아에서 표적 유전자를 효과적으로 억제할 수 있는 신규 sRNA 도구를 개발했다고 10일 밝혔다. 해당 연구 결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)'에 4월 24일 字 온라인 게재됐다.
※ 논문명 : Targeted and high-throughput gene knockdown in diverse bacteria using synthetic sRNAs
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), 조재성(한국과학기술원, 현 MIT 박사후연구원, 공동 제1저자), 양동수(한국과학기술원, 현 고려대학교 조교수, 공동 제1저자), Cindy Prabowo (한국과학기술원, 공동저자), Mohammad Ghiffary (한국과학기술원, 공동저자), 한태희 (한국과학기술원, 공동저자), 최경록 (한국과학기술원, 공동저자), 문천우 (한국과학기술원, 공동저자), Hengrui Zhou (한국과학기술원, 공동저자), 류재용 (한국과학기술원, 현 덕성여자대학교 조교수, 공동저자), 김현욱 (한국과학기술원, 공동저자) - 총 11명
sRNA는 대장균에서 표적 유전자를 억제하기 위해 합성 조절하는 효과적인 도구이지만 그동안 대장균과 같은 그람 음성균 외에 산업적으로 유용한 고초균이나 코리네박테리움 같은 그람 양성균에서는 적용이 어려웠다.
이에 생명화학공학과 이상엽 특훈교수 연구팀은 그람 음성균과 양성균 모두를 포함한 다양한 박테리아에서 표적 유전자를 효과적으로 억제할 수 있는 신규 sRNA 도구를 개발했다. 연구팀은 우선 미생물 데이터베이스를 이용해 수천 종의 미생물 유래 sRNA 시스템을 검토했고, 그중 가장 높은 유전자 억제능을 보여준 `고초균(Bacillus subtilis)' 박테리아 유래 sRNA 시스템을 최종 선정했고 이를 ’광범위 미생물 적용 sRNA‘(Broad-Host-Range sRNA, 이하 BHR-sRNA)라고 명명했다.
sRNA와 유사한 시스템으로는 유전자 가위로 잘 알려진 크리스퍼(CRISPR)를 개량한 크리스퍼 간섭(CRISPR interference, CRISPRi) 시스템이 있다. 유전자 가위의 핵심인 Cas9 단백질에 돌연변이를 일으켜 DNA를 자르지 않으면서 유전자 전사 과정만을 억제해 유전자 발현을 억제하는 시스템인데, Cas9 단백질의 분자량이 매우 높아 몇몇 박테리아에서 성장을 저해하는 현상이 보고됐다. 하지만 이번 연구에서 개발한 BHR-sRNA 시스템은 박테리아의 성장에 전혀 영향을 끼치지 않으면서도 CRISPR 간섭과 유사한 유전자 억제능을 보였다.
BHR-sRNA 시스템의 범용성을 검증하기 위해 연구팀은 다양한 그람 음성균 및 그람 양성균 16종을 선정하여 테스트했고, 그중 15종의 박테리아에서 BHR-sRNA 시스템이 성공적으로 작동함을 증명했다. 또한, 10종의 박테리아에서 기존의 대장균 기반 sRNA 시스템보다 유전자 억제능이 뛰어남을 증명했다. 이와 같이 BHR-sRNA 시스템은 다양한 박테리아에서 효과적으로 유전자 발현을 억제할 수 있는 범용 도구임을 입증했다.
최근 점차 심각해져 가는 항생제 내성 병원균 문제를 해결하기 위해, 연구팀은 BHR-sRNA를 이용해 독성인자를 생산하는 유전자를 억제하고, 결과적으로 병원성을 억제하고자 했다. 특히 BHR-sRNA를 활용해 병원 발생 감염균인 표피포도상 구균(Staphylococcus epidermidis)에서 항생제 내성의 원인 중 하나인 바이오필름 형성을 73% 억제할 수 있었고, 폐렴균인 폐렴막대균(Klebsiella pneumoniae)에서 항생제 내성을 58% 약화하는 결과를 보였다. 연구팀은 또한, BHR-sRNA를 산업용 박테리아에 적용해 표적 물질을 고효율로 생산하고자 했다. 특히 폴리아마이드 고분자의 원재료인 발레로락탐(valerolactam), 포도향 첨가제인 메틸안트라닐산(methyl anthranilate), 그리고 청색 천연염료인 인디고이딘(indigoidine)을 최고 농도로 생산할 수 있었다.
이번 연구를 통해 개발한 BHR-sRNA를 활용해 다양한 산업공정으로의 응용이 기대되며, 항생제 내성 병원균 퇴치를 통한 연구에도 활용될 수 있으리라 기대된다. 교신저자인 이상엽 특훈교수는 “기존에는 각각의 박테리아마다 유전자 억제 도구를 새로 개발해야 했는데, 이번 연구를 통해 다양한 박테리아에서 범용으로 작동하는 도구를 개발했다”며 “앞으로 합성생물학과 대사공학, 그리고 병원균 대응연구 발전에 큰 도움이 될 것”이라고 밝혔다.
한편, 이번 연구는 과기정통부가 지원하는 석유대체 친환경 화학기술개발사업의 바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발 과제의 지원을 받아 수행됐다.
2023.05.10 조회수 9374
산업 균주 제작 및 병원균 억제 범용기술 개발
박테리아는 우리 일상에서 김치, 된장, 술 등 식품에 활용되어 왔을 뿐만 아니라 최근에는 대사 공학을 통해 플라스틱, 영양제, 사료, 의약품 등을 생산하는 산업용 세포 공장으로 활약하고 있다. 하지만 유익한 박테리아 외에도 다양한 감염성 질병을 일으키는 폐렴균, 살모넬라균 등 병원균이 있어 대사공학적 기법을 통해 유해한 병원균은 병원성을 억제하거나 사멸을 유도하고, 유익한 산업용 박테리아는 고부가가치 물질을 고효율로 생산할 수 있도록 조작하는 것이 중요하다.
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 그람 음성균과 양성균 모두를 포함한 다양한 박테리아에서 표적 유전자를 효과적으로 억제할 수 있는 신규 sRNA 도구를 개발했다고 10일 밝혔다. 해당 연구 결과는 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)'에 4월 24일 字 온라인 게재됐다.
※ 논문명 : Targeted and high-throughput gene knockdown in diverse bacteria using synthetic sRNAs
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), 조재성(한국과학기술원, 현 MIT 박사후연구원, 공동 제1저자), 양동수(한국과학기술원, 현 고려대학교 조교수, 공동 제1저자), Cindy Prabowo (한국과학기술원, 공동저자), Mohammad Ghiffary (한국과학기술원, 공동저자), 한태희 (한국과학기술원, 공동저자), 최경록 (한국과학기술원, 공동저자), 문천우 (한국과학기술원, 공동저자), Hengrui Zhou (한국과학기술원, 공동저자), 류재용 (한국과학기술원, 현 덕성여자대학교 조교수, 공동저자), 김현욱 (한국과학기술원, 공동저자) - 총 11명
sRNA는 대장균에서 표적 유전자를 억제하기 위해 합성 조절하는 효과적인 도구이지만 그동안 대장균과 같은 그람 음성균 외에 산업적으로 유용한 고초균이나 코리네박테리움 같은 그람 양성균에서는 적용이 어려웠다.
이에 생명화학공학과 이상엽 특훈교수 연구팀은 그람 음성균과 양성균 모두를 포함한 다양한 박테리아에서 표적 유전자를 효과적으로 억제할 수 있는 신규 sRNA 도구를 개발했다. 연구팀은 우선 미생물 데이터베이스를 이용해 수천 종의 미생물 유래 sRNA 시스템을 검토했고, 그중 가장 높은 유전자 억제능을 보여준 `고초균(Bacillus subtilis)' 박테리아 유래 sRNA 시스템을 최종 선정했고 이를 ’광범위 미생물 적용 sRNA‘(Broad-Host-Range sRNA, 이하 BHR-sRNA)라고 명명했다.
sRNA와 유사한 시스템으로는 유전자 가위로 잘 알려진 크리스퍼(CRISPR)를 개량한 크리스퍼 간섭(CRISPR interference, CRISPRi) 시스템이 있다. 유전자 가위의 핵심인 Cas9 단백질에 돌연변이를 일으켜 DNA를 자르지 않으면서 유전자 전사 과정만을 억제해 유전자 발현을 억제하는 시스템인데, Cas9 단백질의 분자량이 매우 높아 몇몇 박테리아에서 성장을 저해하는 현상이 보고됐다. 하지만 이번 연구에서 개발한 BHR-sRNA 시스템은 박테리아의 성장에 전혀 영향을 끼치지 않으면서도 CRISPR 간섭과 유사한 유전자 억제능을 보였다.
BHR-sRNA 시스템의 범용성을 검증하기 위해 연구팀은 다양한 그람 음성균 및 그람 양성균 16종을 선정하여 테스트했고, 그중 15종의 박테리아에서 BHR-sRNA 시스템이 성공적으로 작동함을 증명했다. 또한, 10종의 박테리아에서 기존의 대장균 기반 sRNA 시스템보다 유전자 억제능이 뛰어남을 증명했다. 이와 같이 BHR-sRNA 시스템은 다양한 박테리아에서 효과적으로 유전자 발현을 억제할 수 있는 범용 도구임을 입증했다.
최근 점차 심각해져 가는 항생제 내성 병원균 문제를 해결하기 위해, 연구팀은 BHR-sRNA를 이용해 독성인자를 생산하는 유전자를 억제하고, 결과적으로 병원성을 억제하고자 했다. 특히 BHR-sRNA를 활용해 병원 발생 감염균인 표피포도상 구균(Staphylococcus epidermidis)에서 항생제 내성의 원인 중 하나인 바이오필름 형성을 73% 억제할 수 있었고, 폐렴균인 폐렴막대균(Klebsiella pneumoniae)에서 항생제 내성을 58% 약화하는 결과를 보였다. 연구팀은 또한, BHR-sRNA를 산업용 박테리아에 적용해 표적 물질을 고효율로 생산하고자 했다. 특히 폴리아마이드 고분자의 원재료인 발레로락탐(valerolactam), 포도향 첨가제인 메틸안트라닐산(methyl anthranilate), 그리고 청색 천연염료인 인디고이딘(indigoidine)을 최고 농도로 생산할 수 있었다.
이번 연구를 통해 개발한 BHR-sRNA를 활용해 다양한 산업공정으로의 응용이 기대되며, 항생제 내성 병원균 퇴치를 통한 연구에도 활용될 수 있으리라 기대된다. 교신저자인 이상엽 특훈교수는 “기존에는 각각의 박테리아마다 유전자 억제 도구를 새로 개발해야 했는데, 이번 연구를 통해 다양한 박테리아에서 범용으로 작동하는 도구를 개발했다”며 “앞으로 합성생물학과 대사공학, 그리고 병원균 대응연구 발전에 큰 도움이 될 것”이라고 밝혔다.
한편, 이번 연구는 과기정통부가 지원하는 석유대체 친환경 화학기술개발사업의 바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발 과제의 지원을 받아 수행됐다.
2023.05.10 조회수 9374 -
 인공지능 이용해 3차원 홀로그래피 현미경의 박테리아 신속 식별 기술 개발
우리 대학 물리학과 박용근 교수 연구팀이 홀로그래피 현미경과 인공지능을 이용한 신속 박테리아 병원균 식별 기술을 개발했다고 27일 밝혔다.
병원균의 조기 식별은 감염질환 치료에 필수적이다. 치명적인 상태로 진행되기 전에 감염균에 맞는 효과적인 항생제의 선택과 투여가 가능해지기 때문이다. 하지만 현재의 일상적 병원균 식별은 통상 수일이 소요된다. 이로 인해 감염 초기 식별 결과 없이 실증적인 처방으로 항생제를 투여하는 사례가 빈번하며, 이로 인해 패혈증의 경우 치명률이 50%에 달하며 항생제 남용으로 인한 슈퍼박테리아 문제도 발생한다.
기존 방법으로 병원균 식별이 오래 걸리는 원인은 긴 박테리아 배양 시간이다. 질량 분석기로 대표되는 식별 기술들은 일정량 이상의 박테리아 표본이 확보되어야 균종과 관련된 분자적 신호를 검출할 수 있다. 이로 인해, 환자에서 추출한 시편을 하루 이상 배양해야만 검출이 될 정도의 박테리아 개수가 확보된다.
광학 분야의 저명 학술지인 `빛: 과학과 응용(Light: Science & Applications), (IF = 17.782)'에 게재된 이번 연구(논문명: Rapid species identification of pathogenic bacteria from a minute quantity exploiting three-dimensional quantitative phase imaging and artificial neural network)에서 박용근 교수 연구팀은 3차원 홀로그래피 현미경과 인공지능 알고리즘을 활용해서 단일 세포 수준의 표본으로도 병원균의 균종을 정확히 알아낼 수 있음을 입증했다.
홀로그래피 현미경으로 측정되는 3차원 굴절률 영상 정보에 내재된 균종과 관련된 특성을 인공지능 알고리즘으로 학습해 종을 구분하는 것이 핵심 아이디어다. 연구팀은 종별로 500개 이상의 박테리아의 3차원 굴절률 영상을 측정했고, 이를 인공지능 신경망을 통해 학습시켰다.
연구팀은 개발한 방법을 이용해 주요한 혈액 감염균을 신속하게 식별함으로써 실제 진단에도 응용될 가능성을 검증했다. 구체적으로 그람 음성 및 양성, 구균 및 간균을 모두 포함한 총 19가지 균종으로 혈액 감염 사례의 90% 이상의 원인이 되는 균들이다. 한 개의 병원균 혹은 병원균 덩어리를 측정한 단일 3차원 굴절률 영상에서는 약 82.5%의 정확도로 균종 판별이 가능했다. 연구팀은 또한 여러 영상을 확보할 수 있을 때 정확도가 증가해, 7개의 박테리아 영상이 확보된다면 99.9%의 정확도를 얻을 수 있었다.
연구진의 책임자이자 논문의 교신저자인 박용근 교수는 "홀로그래피 현미경의 세포 감별 능력을 인공지능으로 극대화해 감염 진단 기술로서의 가능성을 확인한 것이 의미ˮ라고 말했다. 제1 저자인 물리학과 김건 박사과정 학생은 "100,000분의 1 수준의 표본량으로도 질량 분석기의 균종 검출률과 비슷한 정확도를 얻었고 환자 시편에서 다양한 병원균을 식별하는 플랫폼 기술이 될 것으로 기대된다ˮ라고 덧붙였다.
이번 연구는 KAIST-삼성서울병원-토모큐브 팀의 수년간의 공동 연구를 통해 진행됐다. 물리학과 박용근 교수 연구팀의 기술에 다양한 기관의 경험과 비전을 반영함으로써 완성할 수 있었다. 삼성서울병원 진단검사의학과 이남용 교수, 진단검사의학과 허희재 교수, 감염내과 정두련 교수 연구팀, 서울성모병원 진단검사의학과 유인영 교수, 분당 차병원 응급의학과 김규석 교수, 우리 대학 나노과학기술대학원 정현정 교수 등 다양한 분야와 기관이 모여, 실험적 검증을 효과적으로 진행할 수 있었다. 또한 KAIST 교원 창업 기업인 ㈜토모큐브의 3차원 홀로그래피 기술 지원도 필수적인 역할을 했다.
한편 이번 연구는 한국연구재단 창의연구사업, 과학기술일자리진흥원의 지원을 받아 수행됐다.
2022.06.27 조회수 10634
인공지능 이용해 3차원 홀로그래피 현미경의 박테리아 신속 식별 기술 개발
우리 대학 물리학과 박용근 교수 연구팀이 홀로그래피 현미경과 인공지능을 이용한 신속 박테리아 병원균 식별 기술을 개발했다고 27일 밝혔다.
병원균의 조기 식별은 감염질환 치료에 필수적이다. 치명적인 상태로 진행되기 전에 감염균에 맞는 효과적인 항생제의 선택과 투여가 가능해지기 때문이다. 하지만 현재의 일상적 병원균 식별은 통상 수일이 소요된다. 이로 인해 감염 초기 식별 결과 없이 실증적인 처방으로 항생제를 투여하는 사례가 빈번하며, 이로 인해 패혈증의 경우 치명률이 50%에 달하며 항생제 남용으로 인한 슈퍼박테리아 문제도 발생한다.
기존 방법으로 병원균 식별이 오래 걸리는 원인은 긴 박테리아 배양 시간이다. 질량 분석기로 대표되는 식별 기술들은 일정량 이상의 박테리아 표본이 확보되어야 균종과 관련된 분자적 신호를 검출할 수 있다. 이로 인해, 환자에서 추출한 시편을 하루 이상 배양해야만 검출이 될 정도의 박테리아 개수가 확보된다.
광학 분야의 저명 학술지인 `빛: 과학과 응용(Light: Science & Applications), (IF = 17.782)'에 게재된 이번 연구(논문명: Rapid species identification of pathogenic bacteria from a minute quantity exploiting three-dimensional quantitative phase imaging and artificial neural network)에서 박용근 교수 연구팀은 3차원 홀로그래피 현미경과 인공지능 알고리즘을 활용해서 단일 세포 수준의 표본으로도 병원균의 균종을 정확히 알아낼 수 있음을 입증했다.
홀로그래피 현미경으로 측정되는 3차원 굴절률 영상 정보에 내재된 균종과 관련된 특성을 인공지능 알고리즘으로 학습해 종을 구분하는 것이 핵심 아이디어다. 연구팀은 종별로 500개 이상의 박테리아의 3차원 굴절률 영상을 측정했고, 이를 인공지능 신경망을 통해 학습시켰다.
연구팀은 개발한 방법을 이용해 주요한 혈액 감염균을 신속하게 식별함으로써 실제 진단에도 응용될 가능성을 검증했다. 구체적으로 그람 음성 및 양성, 구균 및 간균을 모두 포함한 총 19가지 균종으로 혈액 감염 사례의 90% 이상의 원인이 되는 균들이다. 한 개의 병원균 혹은 병원균 덩어리를 측정한 단일 3차원 굴절률 영상에서는 약 82.5%의 정확도로 균종 판별이 가능했다. 연구팀은 또한 여러 영상을 확보할 수 있을 때 정확도가 증가해, 7개의 박테리아 영상이 확보된다면 99.9%의 정확도를 얻을 수 있었다.
연구진의 책임자이자 논문의 교신저자인 박용근 교수는 "홀로그래피 현미경의 세포 감별 능력을 인공지능으로 극대화해 감염 진단 기술로서의 가능성을 확인한 것이 의미ˮ라고 말했다. 제1 저자인 물리학과 김건 박사과정 학생은 "100,000분의 1 수준의 표본량으로도 질량 분석기의 균종 검출률과 비슷한 정확도를 얻었고 환자 시편에서 다양한 병원균을 식별하는 플랫폼 기술이 될 것으로 기대된다ˮ라고 덧붙였다.
이번 연구는 KAIST-삼성서울병원-토모큐브 팀의 수년간의 공동 연구를 통해 진행됐다. 물리학과 박용근 교수 연구팀의 기술에 다양한 기관의 경험과 비전을 반영함으로써 완성할 수 있었다. 삼성서울병원 진단검사의학과 이남용 교수, 진단검사의학과 허희재 교수, 감염내과 정두련 교수 연구팀, 서울성모병원 진단검사의학과 유인영 교수, 분당 차병원 응급의학과 김규석 교수, 우리 대학 나노과학기술대학원 정현정 교수 등 다양한 분야와 기관이 모여, 실험적 검증을 효과적으로 진행할 수 있었다. 또한 KAIST 교원 창업 기업인 ㈜토모큐브의 3차원 홀로그래피 기술 지원도 필수적인 역할을 했다.
한편 이번 연구는 한국연구재단 창의연구사업, 과학기술일자리진흥원의 지원을 받아 수행됐다.
2022.06.27 조회수 10634 -
 디스플레이 소재로 빛 이용해 친환경 암모니아 합성법 제시
우리 대학 생명화학공학과 이도창 교수, 이상엽 특훈교수, 박영신 연구교수 연구팀이 디스플레이 소재인 양자점(퀀텀닷)을 이용해 *질소 고정 박테리아의 암모니아 생산 효율을 대폭 늘렸다고 16일 밝혔다.
☞ 질소 고정(Nitrogen Fixation) : 공기 중 질소 기체 분자(N₂)를 암모니아(NH₃)를 비롯한 질소화합물로 전환하는 과정을 말한다.
이 교수 연구팀은 양자점에 의해 흡수된 빛 에너지가 박테리아의 암모니아 합성 반응에 사용되도록 설계했으며, 그 결과 박테리아의 암모니아 생산량을 큰 폭으로 증가시킬 수 있었다. 이를 위해 연구팀은 양자점을 질소고정 박테리아 안에 더 많이 넣을 수 있는 방법을 제시했다.
생명화학공학과 고성준 박사가 제1저자로 참여한 이번 연구의 결과는 국제 학술지 `미국 화학회지(JACS)'에 표지 논문으로 선정돼 출판됐다. (논문명 : Light-Driven Ammonia Production by Azotobacter vinelandii Cultured in Medium Containing Colloidal Quantum Dots).
질소 고정 박테리아는 질소 고정 효소를 이용해 대기 중 질소를 암모니아로 전환하여 생장에 필요한 단백질을 생산한다. 이러한 질소 고정 반응은 화학적 암모니아 합성법인 하버-보슈 공정에 비해 에너지 소비와 이산화탄소 배출이 현저하게 적다.
하지만, 박테리아는 생장에 필요한 만큼만 암모니아를 생산하도록 진화돼 질소 고정 효소의 반응이 느리기에 이를 산업적으로 활용하기 어렵다. 질소 고정 반응이 느린 이유는 효소의 두 가지 구성요소(전자 전달부, 촉매 반응부)의 비효율적인 상호작용 때문이다. 전자 전달부가 촉매 반응부에 전자를 공급한 후, 반드시 탈착돼야만 촉매 반응부가 새로운 전자를 추가로 공급받아 암모니아를 생성할 수 있다.
연구팀은 문제 해결을 위해 빛을 흡수하는 양자점을 박테리아의 질소 고정 반응에 전자 공급원으로 활용해 나노·바이오 복합 시스템을 구축했다. 양자점은 수 나노미터의 작은 크기를 갖는 반도체 나노입자이며 디스플레이 소재로 많이 알려진 물질이다. 하지만, 양자점이 흡수한 빛 에너지를 표면에 쉽게 전달할 수 있도록 입자의 구조 및 표면을 제어하면 광 감응 및 광 촉매 소재로도 우수한 특성을 보인다. 연구팀은 질소 고정 효소의 전자 전달부 역할을 양자점으로 대체하기 위해 양자점의 코어/쉘 구조를 전자 전달에 유리하게 설계했다. 또한, 양자점이 생물학적 시스템에 결합할 수 있도록 표면 화학 특성을 제어해 수(水)분산 특성을 확보했다.
연구팀은 구조 및 표면이 제어된 양자점을 질소 고정 박테리아의 대사활동이 가장 활발한 성장기에 추가해, 박테리아의 능동적인 양자점 흡수를 유도했다. 이렇게 제작된 양자점-박테리아 복합 시스템에 빛을 조사한 결과, 질소고정 반응 속도가 증가하며 암모니아 생산량이 대폭 증가함을 확인했다. 고성준 박사는 "디스플레이 소재와 미생물의 장점을 합해 빛 에너지를 이용한 새로운 방식의 암모니아 합성법을 제시한 결과ˮ라며 "이번 연구를 활용한 그린 암모니아 생산 플랫폼을 구축한다면, 환경 및 에너지 문제에 적극적으로 대응할 수 있을 것이다ˮ라고 말했다.
한편 이번 연구는 삼성미래기술육성사업의 지원을 받아 수행됐다.
2022.06.16 조회수 11897
디스플레이 소재로 빛 이용해 친환경 암모니아 합성법 제시
우리 대학 생명화학공학과 이도창 교수, 이상엽 특훈교수, 박영신 연구교수 연구팀이 디스플레이 소재인 양자점(퀀텀닷)을 이용해 *질소 고정 박테리아의 암모니아 생산 효율을 대폭 늘렸다고 16일 밝혔다.
☞ 질소 고정(Nitrogen Fixation) : 공기 중 질소 기체 분자(N₂)를 암모니아(NH₃)를 비롯한 질소화합물로 전환하는 과정을 말한다.
이 교수 연구팀은 양자점에 의해 흡수된 빛 에너지가 박테리아의 암모니아 합성 반응에 사용되도록 설계했으며, 그 결과 박테리아의 암모니아 생산량을 큰 폭으로 증가시킬 수 있었다. 이를 위해 연구팀은 양자점을 질소고정 박테리아 안에 더 많이 넣을 수 있는 방법을 제시했다.
생명화학공학과 고성준 박사가 제1저자로 참여한 이번 연구의 결과는 국제 학술지 `미국 화학회지(JACS)'에 표지 논문으로 선정돼 출판됐다. (논문명 : Light-Driven Ammonia Production by Azotobacter vinelandii Cultured in Medium Containing Colloidal Quantum Dots).
질소 고정 박테리아는 질소 고정 효소를 이용해 대기 중 질소를 암모니아로 전환하여 생장에 필요한 단백질을 생산한다. 이러한 질소 고정 반응은 화학적 암모니아 합성법인 하버-보슈 공정에 비해 에너지 소비와 이산화탄소 배출이 현저하게 적다.
하지만, 박테리아는 생장에 필요한 만큼만 암모니아를 생산하도록 진화돼 질소 고정 효소의 반응이 느리기에 이를 산업적으로 활용하기 어렵다. 질소 고정 반응이 느린 이유는 효소의 두 가지 구성요소(전자 전달부, 촉매 반응부)의 비효율적인 상호작용 때문이다. 전자 전달부가 촉매 반응부에 전자를 공급한 후, 반드시 탈착돼야만 촉매 반응부가 새로운 전자를 추가로 공급받아 암모니아를 생성할 수 있다.
연구팀은 문제 해결을 위해 빛을 흡수하는 양자점을 박테리아의 질소 고정 반응에 전자 공급원으로 활용해 나노·바이오 복합 시스템을 구축했다. 양자점은 수 나노미터의 작은 크기를 갖는 반도체 나노입자이며 디스플레이 소재로 많이 알려진 물질이다. 하지만, 양자점이 흡수한 빛 에너지를 표면에 쉽게 전달할 수 있도록 입자의 구조 및 표면을 제어하면 광 감응 및 광 촉매 소재로도 우수한 특성을 보인다. 연구팀은 질소 고정 효소의 전자 전달부 역할을 양자점으로 대체하기 위해 양자점의 코어/쉘 구조를 전자 전달에 유리하게 설계했다. 또한, 양자점이 생물학적 시스템에 결합할 수 있도록 표면 화학 특성을 제어해 수(水)분산 특성을 확보했다.
연구팀은 구조 및 표면이 제어된 양자점을 질소 고정 박테리아의 대사활동이 가장 활발한 성장기에 추가해, 박테리아의 능동적인 양자점 흡수를 유도했다. 이렇게 제작된 양자점-박테리아 복합 시스템에 빛을 조사한 결과, 질소고정 반응 속도가 증가하며 암모니아 생산량이 대폭 증가함을 확인했다. 고성준 박사는 "디스플레이 소재와 미생물의 장점을 합해 빛 에너지를 이용한 새로운 방식의 암모니아 합성법을 제시한 결과ˮ라며 "이번 연구를 활용한 그린 암모니아 생산 플랫폼을 구축한다면, 환경 및 에너지 문제에 적극적으로 대응할 수 있을 것이다ˮ라고 말했다.
한편 이번 연구는 삼성미래기술육성사업의 지원을 받아 수행됐다.
2022.06.16 조회수 11897 -
 살아있는 미생물 내 바이오 플라스틱 생성 관찰 최초 성공
우리 대학 생명화학공학과 이상엽 특훈교수(연구부총장)와 물리학과 박용근 석좌교수 공동연구팀이 ‘3차원 홀로그래픽 현미경 기술을 통한 미생물의 바이오 플라스틱 과립 생산 특징 규명’에 성공했다고 27일 밝혔다.
이번 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 7월 27일 字 온라인 게재됐다.
※ 논문명 : Three-dimensional label-free visualization and quantification of polyhydroxyalkanoates in individual bacterial cell in its native state
※ 저자 정보 : 이상엽(KAIST, 교신저자), 박용근(KAIST, 교신저자), 최소영(KAIST, 공동 제1 저자), 오정훈(KAIST, 공동 제1저자), 정재황(KAIST, 공동 제1저자) - 총 5명
전 세계적으로 폐플라스틱으로 인한 환경오염 및 생태계 파괴, 미세 플라스틱의 인류 보건 위협 등의 문제가 심각해짐에 따라 다양한 규제 및 대안 기술들이 연구되고 있다. 그중 미생물로부터 만들어지는 폴리에스테르인 폴리하이드록시알카노에이트 (polyhydroxyalkanoate, 이하 PHA)가 기존 합성 플라스틱을 대체할 친환경 바이오 플라스틱으로 많은 관심을 받고 있다.
PHA는 폴리에틸렌이나 폴리프로필렌과 같은 범용 플라스틱과 유사한 물성을 가지고 있어 용기 포장재, 비닐, 일회용품 등의 다양한 활용이 가능하며, 토양이나 해양 환경에서 생분해가 가능한 고분자라는 가장 중요한 장점을 갖고 있다.
PHA는 몇몇 미생물 내에 불용성의 과립(granule) 형태로 발견되는 고분자 물질로, 미생물이 환경 변화 및 세포 상태에 따라 탄소원, 에너지원으로 세포 내에 축적하게 된다. PHA가 세포 내에 축적되는 원리를 관찰하기 위해 여러 연구가 진행돼왔다.
형광 현미경, 투과전자현미경, 전자 저온 촬영 등의 기술이 이용됐는데, 이는 2차원상의 이미지만을 제시하거나 형광 물질과 같은 별도의 표식이나 세포의 고정/절편 제작 과정이 있어야 하여, 세포 원래 그대로의 상태에서의 관측이 어려웠다. 따라서 기술적 한계로 인해 세포 내에서 PHA 과립 형성에 대한 완전한 이해가 어려웠고, 관측 결과에 기반을 둔 여러 형성 메커니즘 모델만이 제안돼왔다.
이에 이상엽 특훈교수와 박용근 석좌교수 공동연구팀은 최근 떠오르고 있는 *3차원 홀로그래픽 현미경 기술을 통해 PHA 생산 박테리아의 심층 관찰 및 정량/정성 분석 연구를 수행했다.
*3차원 홀로그래픽 현미경 기술은 물질의 굴절률(refractive index)을 활용하는 이미징 방법으로, 염색 등 준비 과정을 필요로 하지 않기 때문에 살아 있는 세포의 3차원 정보를 정량적으로 측정 가능하다.
연구팀은 PHA의 한 종류인 *PHB 생산 미생물로 잘 알려진 쿠프리아비두스 네카토르(Cupriavidus necator)와 이 미생물의 PHB 합성 대사회로 유전자를 가진 재조합 대장균을 이용해 비교·분석을 수행했다.
*PHA는 현재까지 약 150여 가지의 하이드록시산 화합물들이 단량체로 보고되었으며, PHA 중 가장 대표적이며 많은 연구가 이루어진 것이 poly(3-hydroxybutyrate) [PHB]임
연구팀은 재구성된 세포의 3차원 굴절률 분포로 단일세포 수준에서 세포와 세포 내 과립의 3차원 시각화 및 이를 통한 부피, 질량, 밀도, 분포 등의 정량 분석에 성공했다. 수백 개의 단일 세포들과 세포 내의 PHA 과립에 대한 정량 및 이의 통계 분석을 통해 두 미생물에서의 PHA 과립 형성의 차이점을 도출해냈다.
특히, 단일세포 내의 PHA 과립의 밀도의 개념을 새롭게 제시했으며, 두 미생물에서의 PHA 과립의 밀도의 차이 및 세포 내 분포 형태 및 위치에 대한 특이적인 차이를 발견했다. 더 나아가서, 두 미생물의 PHA 과립 형성의 차이를 나타내게 하는 핵심 단백질을 규명해, 재조합 대장균의 PHA 과립 형성의 양상을 쿠프리아비두스 네카토르와 유사하게 변화시킬 수 있었다.
또한, 실시간 모니터링을 통해 최대 약 8시간 동안의 세포와 세포 내 PHA 과립의 성장 과정을 보여주는 3차원 영상을 제작할 수 있었다. 이는 미생물이 살아있는 상태에서 별도의 처리 과정이 없는 자연 상태 조건 하에, 세포 내 PHA 과립의 형성과 세포 분열과 연계된 이동을 3차원에서 실시간으로 관측한 세계 최초의 결과라는 데 큰 의의가 있다.
이상엽 특훈교수는 “이번 연구를 통해 미생물의 PHA 생산 원리에 대해 더욱 깊은 이해가 가능해졌고, 이는 생물학과 물리학의 융합 연구로서 이뤄진 성과라는 데에 큰 의의가 있으며, 향후 다양한 바이오 플라스틱 생산 공정 개발에 큰 도움이 될 것”이라고 말했다.
한편 이번 연구는 과기정통부가 지원하는 기후변화대응기술개발사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2021.07.28 조회수 16624
살아있는 미생물 내 바이오 플라스틱 생성 관찰 최초 성공
우리 대학 생명화학공학과 이상엽 특훈교수(연구부총장)와 물리학과 박용근 석좌교수 공동연구팀이 ‘3차원 홀로그래픽 현미경 기술을 통한 미생물의 바이오 플라스틱 과립 생산 특징 규명’에 성공했다고 27일 밝혔다.
이번 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 7월 27일 字 온라인 게재됐다.
※ 논문명 : Three-dimensional label-free visualization and quantification of polyhydroxyalkanoates in individual bacterial cell in its native state
※ 저자 정보 : 이상엽(KAIST, 교신저자), 박용근(KAIST, 교신저자), 최소영(KAIST, 공동 제1 저자), 오정훈(KAIST, 공동 제1저자), 정재황(KAIST, 공동 제1저자) - 총 5명
전 세계적으로 폐플라스틱으로 인한 환경오염 및 생태계 파괴, 미세 플라스틱의 인류 보건 위협 등의 문제가 심각해짐에 따라 다양한 규제 및 대안 기술들이 연구되고 있다. 그중 미생물로부터 만들어지는 폴리에스테르인 폴리하이드록시알카노에이트 (polyhydroxyalkanoate, 이하 PHA)가 기존 합성 플라스틱을 대체할 친환경 바이오 플라스틱으로 많은 관심을 받고 있다.
PHA는 폴리에틸렌이나 폴리프로필렌과 같은 범용 플라스틱과 유사한 물성을 가지고 있어 용기 포장재, 비닐, 일회용품 등의 다양한 활용이 가능하며, 토양이나 해양 환경에서 생분해가 가능한 고분자라는 가장 중요한 장점을 갖고 있다.
PHA는 몇몇 미생물 내에 불용성의 과립(granule) 형태로 발견되는 고분자 물질로, 미생물이 환경 변화 및 세포 상태에 따라 탄소원, 에너지원으로 세포 내에 축적하게 된다. PHA가 세포 내에 축적되는 원리를 관찰하기 위해 여러 연구가 진행돼왔다.
형광 현미경, 투과전자현미경, 전자 저온 촬영 등의 기술이 이용됐는데, 이는 2차원상의 이미지만을 제시하거나 형광 물질과 같은 별도의 표식이나 세포의 고정/절편 제작 과정이 있어야 하여, 세포 원래 그대로의 상태에서의 관측이 어려웠다. 따라서 기술적 한계로 인해 세포 내에서 PHA 과립 형성에 대한 완전한 이해가 어려웠고, 관측 결과에 기반을 둔 여러 형성 메커니즘 모델만이 제안돼왔다.
이에 이상엽 특훈교수와 박용근 석좌교수 공동연구팀은 최근 떠오르고 있는 *3차원 홀로그래픽 현미경 기술을 통해 PHA 생산 박테리아의 심층 관찰 및 정량/정성 분석 연구를 수행했다.
*3차원 홀로그래픽 현미경 기술은 물질의 굴절률(refractive index)을 활용하는 이미징 방법으로, 염색 등 준비 과정을 필요로 하지 않기 때문에 살아 있는 세포의 3차원 정보를 정량적으로 측정 가능하다.
연구팀은 PHA의 한 종류인 *PHB 생산 미생물로 잘 알려진 쿠프리아비두스 네카토르(Cupriavidus necator)와 이 미생물의 PHB 합성 대사회로 유전자를 가진 재조합 대장균을 이용해 비교·분석을 수행했다.
*PHA는 현재까지 약 150여 가지의 하이드록시산 화합물들이 단량체로 보고되었으며, PHA 중 가장 대표적이며 많은 연구가 이루어진 것이 poly(3-hydroxybutyrate) [PHB]임
연구팀은 재구성된 세포의 3차원 굴절률 분포로 단일세포 수준에서 세포와 세포 내 과립의 3차원 시각화 및 이를 통한 부피, 질량, 밀도, 분포 등의 정량 분석에 성공했다. 수백 개의 단일 세포들과 세포 내의 PHA 과립에 대한 정량 및 이의 통계 분석을 통해 두 미생물에서의 PHA 과립 형성의 차이점을 도출해냈다.
특히, 단일세포 내의 PHA 과립의 밀도의 개념을 새롭게 제시했으며, 두 미생물에서의 PHA 과립의 밀도의 차이 및 세포 내 분포 형태 및 위치에 대한 특이적인 차이를 발견했다. 더 나아가서, 두 미생물의 PHA 과립 형성의 차이를 나타내게 하는 핵심 단백질을 규명해, 재조합 대장균의 PHA 과립 형성의 양상을 쿠프리아비두스 네카토르와 유사하게 변화시킬 수 있었다.
또한, 실시간 모니터링을 통해 최대 약 8시간 동안의 세포와 세포 내 PHA 과립의 성장 과정을 보여주는 3차원 영상을 제작할 수 있었다. 이는 미생물이 살아있는 상태에서 별도의 처리 과정이 없는 자연 상태 조건 하에, 세포 내 PHA 과립의 형성과 세포 분열과 연계된 이동을 3차원에서 실시간으로 관측한 세계 최초의 결과라는 데 큰 의의가 있다.
이상엽 특훈교수는 “이번 연구를 통해 미생물의 PHA 생산 원리에 대해 더욱 깊은 이해가 가능해졌고, 이는 생물학과 물리학의 융합 연구로서 이뤄진 성과라는 데에 큰 의의가 있으며, 향후 다양한 바이오 플라스틱 생산 공정 개발에 큰 도움이 될 것”이라고 말했다.
한편 이번 연구는 과기정통부가 지원하는 기후변화대응기술개발사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2021.07.28 조회수 16624 -
 도파민의 성질로 박테리아 생장의 실시간 탐지 기술 개발
우리 몸의 신경전달물질인 도파민의 성질을 이용해 박테리아(병원균)를 쉽게 검출할 수 있는 기술이 우리 대학 연구진에 의해 개발됐다.
생명과학과 정현정 교수, 화학과 이해신 교수 공동연구팀이 도파민의 반응을 이용해 병원균의 생장과 항생제 내성을 광학적으로 측정하고 맨눈으로 실시간 검출하는 기술을 개발했다고 7일 밝혔다.
박테리아의 항생제 내성 문제는 현대인의 건강을 위협하는 위험요인으로 꼽히고 있다. 항생제 내성에 대한 적절한 대처가 없다면 30년 이내에 항생제 내성균에 의한 피해가 암보다 더 현대인의 수명을 줄일 수 있다는 보고서가 발표되기도 했다. 항생제 내성균의 종류가 점차 늘어나면서 미국 질병통제예방센터(CDC)는 연간 최소 200만 명 이상의 환자가 항생제 내성 병원균에 의해 발생하고 있다고 보고했다.
도파민은 대다수 생명체에서 신경전달물질로 사용되며, 산소가 존재하는 환경에서 다른 물질의 도움 없이 자체 중합반응(두 개 이상 결합해 큰 화합물이 되는 일)이 일어난다. 이렇게 중합된 도파민 고분자는 짙은 갈색을 나타내고, 다양한 물질 표면에 흡착해 층을 형성한다.
연구팀은 이러한 도파민의 성질을 이용해 병원균이 생장하는지와 항생제 내성을 갖는지를 육안과 형광으로 동시에 탐지 가능한 기술을 개발했다. 이 기술은 현재 사용되는 디스크 확산 검사나 균 배양 분석에 대비해 시간이 짧고 중합효소 연쇄 반응(PCR 검사)과 비교할 때도 전처리 과정이 필요 없는 간편한 기술이라는 점이 큰 장점이다.
우리 대학 나노과학기술대학원 석박사통합과정 이주훈 학생이 제1 저자로, 나노과학기술대학원 석박사통합과정 류제성 학생과 생명과학과 강유경 박사가 공동 저자로 참여한 이번 연구 결과는 재료과학 분야 국제학술지 `어드밴스드 펑셔널 머티리얼즈(Advanced Functional Materials, IF 16.836)'에 11월 3일 字 온라인 게재됐다. (논문명 : Polydopamine Sensors of Bacterial Hypoxia via Fluorescence Coupling)
도파민의 자체 중합반응에서는 개시제 역할을 하는 산소가 필수적인 존재다. 연구팀은 박테리아가 생장함에 따라 용액 내의 산소를 소모하는 현상을 이용, 박테리아의 생장 정도를 도파민의 중합반응과 연관 지어 관측하는 방법을 개발했다.
또 박테리아의 생장에 영향을 끼치지 않는 소재인 덱스트란으로 형광나노입자를 제조해 실험에 사용했다. 도파민의 자체 중합반응은 용액 내에 존재하는 형광나노입자 표면에 흡착하고 층을 형성해 입자의 화학적, 물리적 성질에 큰 변화를 일으키고 기존에 발생하던 강한 형광 신호를 약하게 만든다. 또한, 도파민과 나노입자가 첨가된 용액 내에서는 도파민의 산화와 자체 중합반응 때문에 용액의 색이 짙은 갈색으로 변한다.
하지만 박테리아가 용액 내에 존재하는 경우 박테리아 생장 때문에 산소가 소모돼 도파민의 자체 중합반응은 저해되고 용액의 색깔은 투명하게 유지된다. 나노입자의 형광 신호 역시 원래의 신호를 유지하게 된다.
연구팀은 이러한 현상을 박테리아의 생장 및 항생제 내성을 탐지하는데 적용할 수 있다는 점에 착안, 항생제에 내성을 가지는 `뉴 델리 메탈로-베타락타마제 1 (NDM-1)'을 발현하는 대장균(E. coli)을 대상으로 실험을 진행했다.
일반적인 대장균의 경우 카바페넴 계열의 항생제인 암피실린에 의해 생장이 크게 저해되는데, 항생제에 내성을 갖는 대장균은 생장이 잘 이뤄진다. 즉 항생제 내성을 가지는지에 따라 소모하는 산소의 양이 달라지고, 이 차이 때문에 도파민의 중합반응 여부를 육안과 광학적 측정으로 확인할 수 있다.
이렇게 살아있는 세포의 활성에 따라 일어나는 도파민의 자체 중합반응은 실제로 인체에 존재하는 다양한 `카테콜아민' 물질에서 나타나는 반응과 깊은 관련이 있다. 일례로 피부에 존재하는 카테콜아민은 자체 중합반응이 왕성하게 일어나 피부의 색에 큰 영향을 주는 멜라닌 색소를 형성하게 되는데 신경계에 존재하는 카테콜아민은 자체 중합반응이 거의 일어나지 않고 단일분자 형태로 존재하여 작용하는 것으로 알려져 있다. 연구팀은 이번 연구 결과를 향후 생체 내에서 도파민 등 카테콜아민의 역할과 작용을 다양한 생체 모델에서 밝히는 연구로 발전시킨다면 매우 흥미로운 연구 결과를 얻을 것으로 기대하고 있다.
정현정 교수는 “이번 연구는 도파민의 자체 중합반응을 생체 시스템에서 규명한 연구로 큰 의미를 가지며, 이를 박테리아 생장 및 항생제 내성의 실시간 검출에 적용할 수 있어 기존의 미생물 배양법보다 신속하게, 그리고 PCR 검사보다 간편하게 진단이 가능해 감염병 확산 예방에 크게 기여할 것으로 기대된다”고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업 및 KAIST 그랜드 챌린지 사업의 지원을 통해 이뤄졌다.
2020.12.07 조회수 47267
도파민의 성질로 박테리아 생장의 실시간 탐지 기술 개발
우리 몸의 신경전달물질인 도파민의 성질을 이용해 박테리아(병원균)를 쉽게 검출할 수 있는 기술이 우리 대학 연구진에 의해 개발됐다.
생명과학과 정현정 교수, 화학과 이해신 교수 공동연구팀이 도파민의 반응을 이용해 병원균의 생장과 항생제 내성을 광학적으로 측정하고 맨눈으로 실시간 검출하는 기술을 개발했다고 7일 밝혔다.
박테리아의 항생제 내성 문제는 현대인의 건강을 위협하는 위험요인으로 꼽히고 있다. 항생제 내성에 대한 적절한 대처가 없다면 30년 이내에 항생제 내성균에 의한 피해가 암보다 더 현대인의 수명을 줄일 수 있다는 보고서가 발표되기도 했다. 항생제 내성균의 종류가 점차 늘어나면서 미국 질병통제예방센터(CDC)는 연간 최소 200만 명 이상의 환자가 항생제 내성 병원균에 의해 발생하고 있다고 보고했다.
도파민은 대다수 생명체에서 신경전달물질로 사용되며, 산소가 존재하는 환경에서 다른 물질의 도움 없이 자체 중합반응(두 개 이상 결합해 큰 화합물이 되는 일)이 일어난다. 이렇게 중합된 도파민 고분자는 짙은 갈색을 나타내고, 다양한 물질 표면에 흡착해 층을 형성한다.
연구팀은 이러한 도파민의 성질을 이용해 병원균이 생장하는지와 항생제 내성을 갖는지를 육안과 형광으로 동시에 탐지 가능한 기술을 개발했다. 이 기술은 현재 사용되는 디스크 확산 검사나 균 배양 분석에 대비해 시간이 짧고 중합효소 연쇄 반응(PCR 검사)과 비교할 때도 전처리 과정이 필요 없는 간편한 기술이라는 점이 큰 장점이다.
우리 대학 나노과학기술대학원 석박사통합과정 이주훈 학생이 제1 저자로, 나노과학기술대학원 석박사통합과정 류제성 학생과 생명과학과 강유경 박사가 공동 저자로 참여한 이번 연구 결과는 재료과학 분야 국제학술지 `어드밴스드 펑셔널 머티리얼즈(Advanced Functional Materials, IF 16.836)'에 11월 3일 字 온라인 게재됐다. (논문명 : Polydopamine Sensors of Bacterial Hypoxia via Fluorescence Coupling)
도파민의 자체 중합반응에서는 개시제 역할을 하는 산소가 필수적인 존재다. 연구팀은 박테리아가 생장함에 따라 용액 내의 산소를 소모하는 현상을 이용, 박테리아의 생장 정도를 도파민의 중합반응과 연관 지어 관측하는 방법을 개발했다.
또 박테리아의 생장에 영향을 끼치지 않는 소재인 덱스트란으로 형광나노입자를 제조해 실험에 사용했다. 도파민의 자체 중합반응은 용액 내에 존재하는 형광나노입자 표면에 흡착하고 층을 형성해 입자의 화학적, 물리적 성질에 큰 변화를 일으키고 기존에 발생하던 강한 형광 신호를 약하게 만든다. 또한, 도파민과 나노입자가 첨가된 용액 내에서는 도파민의 산화와 자체 중합반응 때문에 용액의 색이 짙은 갈색으로 변한다.
하지만 박테리아가 용액 내에 존재하는 경우 박테리아 생장 때문에 산소가 소모돼 도파민의 자체 중합반응은 저해되고 용액의 색깔은 투명하게 유지된다. 나노입자의 형광 신호 역시 원래의 신호를 유지하게 된다.
연구팀은 이러한 현상을 박테리아의 생장 및 항생제 내성을 탐지하는데 적용할 수 있다는 점에 착안, 항생제에 내성을 가지는 `뉴 델리 메탈로-베타락타마제 1 (NDM-1)'을 발현하는 대장균(E. coli)을 대상으로 실험을 진행했다.
일반적인 대장균의 경우 카바페넴 계열의 항생제인 암피실린에 의해 생장이 크게 저해되는데, 항생제에 내성을 갖는 대장균은 생장이 잘 이뤄진다. 즉 항생제 내성을 가지는지에 따라 소모하는 산소의 양이 달라지고, 이 차이 때문에 도파민의 중합반응 여부를 육안과 광학적 측정으로 확인할 수 있다.
이렇게 살아있는 세포의 활성에 따라 일어나는 도파민의 자체 중합반응은 실제로 인체에 존재하는 다양한 `카테콜아민' 물질에서 나타나는 반응과 깊은 관련이 있다. 일례로 피부에 존재하는 카테콜아민은 자체 중합반응이 왕성하게 일어나 피부의 색에 큰 영향을 주는 멜라닌 색소를 형성하게 되는데 신경계에 존재하는 카테콜아민은 자체 중합반응이 거의 일어나지 않고 단일분자 형태로 존재하여 작용하는 것으로 알려져 있다. 연구팀은 이번 연구 결과를 향후 생체 내에서 도파민 등 카테콜아민의 역할과 작용을 다양한 생체 모델에서 밝히는 연구로 발전시킨다면 매우 흥미로운 연구 결과를 얻을 것으로 기대하고 있다.
정현정 교수는 “이번 연구는 도파민의 자체 중합반응을 생체 시스템에서 규명한 연구로 큰 의미를 가지며, 이를 박테리아 생장 및 항생제 내성의 실시간 검출에 적용할 수 있어 기존의 미생물 배양법보다 신속하게, 그리고 PCR 검사보다 간편하게 진단이 가능해 감염병 확산 예방에 크게 기여할 것으로 기대된다”고 말했다.
한편 이번 연구는 한국연구재단 중견연구자지원사업 및 KAIST 그랜드 챌린지 사업의 지원을 통해 이뤄졌다.
2020.12.07 조회수 47267 -
 김재경 교수, 수학 모델 통해 세포 상호작용 원리 규명
〈김재경 교수〉
우리 대학 수리과학과 김재경 교수와 라이스 대학 매튜 베넷(Matthew Bennett), 휴스턴 대학 크레시미르 조식(Kresimir Josic) 교수 공동 연구팀이 합성생물학과 수학적 모델을 이용해 세포들이 넓은 공간에서 효과적으로 의사소통하는 방법을 발견했다.
이번 연구 결과는 국제 학술지 ‘네이처 케미컬 바이올로지(Nature Chemical Biology)’ 10월 14일 자 온라인판에 게재됐다. (논문명 :Long-range temporal coordination of gene expression in synthetic microbial consortia)
〈박테리아들의 복잡한 상호작용을 수학을 이용해 원위의 점들의 상호작용으로 단순화한 모식도〉
세포들은 신호 전달 분자(Signalling molecule)를 이용해 의사소통하는데 이 신호는 보통 아주 짧은 거리만 도달할 수 있다. 그런데도 세포들은 넓은 공간에서도 상호작용하며 동기화를 이뤄낸다.
이는 마치 넓은 축구장에 수만 명의 사람이 주변 3~4명의 박수 소리만 들을 수 있는데도 불구하고 모두가 같은 박자로 손뼉을 치는 것과 비슷한 상황이다. 이러한 현상이 가능한 이유는 무엇일까?
연구팀은 합성생물학을 이용해 만든 전사 회로(Transcriptional circuit)를 박테리아(E. coli)에 구축해 주기적으로 신호 전달 분자를 방출할 수 있도록 했다. 처음엔 제각기 다른 시간에 신호 전달 분자를 방출하던 박테리아들은 의사소통을 통해 같은 시간에 주기적으로 분자를 방출하는 동기화를 이뤄냈다.
하지만 박테리아를 넓은 공간으로 옮겼을 땐 이러한 동기화가 각 박테리아의 신호 전달 분자 전사 회로에 전사적 양성 피드백 룹 (Transcriptional positive feedback loop)이 있을 때만 가능하다는 것을 발견했다.
양성 피드백 룹은 단백질이 스스로 유전자 발현을 유도하는 시스템으로, 전달받은 신호를 증폭하는 역할을 한다. 연구팀은 이러한 역할을 자세히 이해하기 위해 편미분방정식(Partial differential equation)을 이용해 세포 내 신호 전달 분자의 생성과 세포 간 의사소통을 정확하게 묘사하는 수학적 모델을 개발했다.
그러나 전사 회로를 구성하는 다양한 종류의 분자들 사이의 상호작용을 묘사하기 위해서는 고차원의 편미분방정식이 필요했고 이를 분석하기는 쉽지 않았다.
이를 극복하기 위해 연구팀은 시스템이 주기적인 패턴을 반복한다는 점에 착안해 고차원 시스템을 1차원 원 위의 움직임으로 단순화했다. 달은 고차원인 우주 공간에서 움직이지만, 궤도를 따라 주기적으로 움직이기에 달의 움직임을 1차원 원 위에서 나타낼 수 있는 것과 같은 원리이다.
이를 통해 연구팀은 박테리아 사이의 복잡한 상호작용을 원 위를 주기적으로 움직이는 두 점의 상호작용으로 단순화할 수 있었다.
연구팀은 양성 피드백 룹이 있으면 두 점의 위치 차이가 커도 시간이 지날수록 점점 차이가 줄어들어 결국 동시에 움직이는 것을 확인했다. 연구팀은 이러한 수학적 분석 결과를 실험을 통해서 검증함으로써 넓은 공간에서 세포가 효과적으로 상호작용하는 방식을 규명했다.
김재경 교수는 “세포들이 자신의 목소리는 낮추고 상대방의 목소리에는 더 귀 기울일 때만 한목소리를 낼 수 있다는 점이 인상적이다”라며 “이러한 원리는 수학을 이용한 복잡한 시스템의 단순화 없이는 찾지 못했을 것이다. 복잡한 것을 단순하게 볼 수 있도록 해주는 것이 수학의 힘이다”라고 말했다.
2019.10.15 조회수 16273
김재경 교수, 수학 모델 통해 세포 상호작용 원리 규명
〈김재경 교수〉
우리 대학 수리과학과 김재경 교수와 라이스 대학 매튜 베넷(Matthew Bennett), 휴스턴 대학 크레시미르 조식(Kresimir Josic) 교수 공동 연구팀이 합성생물학과 수학적 모델을 이용해 세포들이 넓은 공간에서 효과적으로 의사소통하는 방법을 발견했다.
이번 연구 결과는 국제 학술지 ‘네이처 케미컬 바이올로지(Nature Chemical Biology)’ 10월 14일 자 온라인판에 게재됐다. (논문명 :Long-range temporal coordination of gene expression in synthetic microbial consortia)
〈박테리아들의 복잡한 상호작용을 수학을 이용해 원위의 점들의 상호작용으로 단순화한 모식도〉
세포들은 신호 전달 분자(Signalling molecule)를 이용해 의사소통하는데 이 신호는 보통 아주 짧은 거리만 도달할 수 있다. 그런데도 세포들은 넓은 공간에서도 상호작용하며 동기화를 이뤄낸다.
이는 마치 넓은 축구장에 수만 명의 사람이 주변 3~4명의 박수 소리만 들을 수 있는데도 불구하고 모두가 같은 박자로 손뼉을 치는 것과 비슷한 상황이다. 이러한 현상이 가능한 이유는 무엇일까?
연구팀은 합성생물학을 이용해 만든 전사 회로(Transcriptional circuit)를 박테리아(E. coli)에 구축해 주기적으로 신호 전달 분자를 방출할 수 있도록 했다. 처음엔 제각기 다른 시간에 신호 전달 분자를 방출하던 박테리아들은 의사소통을 통해 같은 시간에 주기적으로 분자를 방출하는 동기화를 이뤄냈다.
하지만 박테리아를 넓은 공간으로 옮겼을 땐 이러한 동기화가 각 박테리아의 신호 전달 분자 전사 회로에 전사적 양성 피드백 룹 (Transcriptional positive feedback loop)이 있을 때만 가능하다는 것을 발견했다.
양성 피드백 룹은 단백질이 스스로 유전자 발현을 유도하는 시스템으로, 전달받은 신호를 증폭하는 역할을 한다. 연구팀은 이러한 역할을 자세히 이해하기 위해 편미분방정식(Partial differential equation)을 이용해 세포 내 신호 전달 분자의 생성과 세포 간 의사소통을 정확하게 묘사하는 수학적 모델을 개발했다.
그러나 전사 회로를 구성하는 다양한 종류의 분자들 사이의 상호작용을 묘사하기 위해서는 고차원의 편미분방정식이 필요했고 이를 분석하기는 쉽지 않았다.
이를 극복하기 위해 연구팀은 시스템이 주기적인 패턴을 반복한다는 점에 착안해 고차원 시스템을 1차원 원 위의 움직임으로 단순화했다. 달은 고차원인 우주 공간에서 움직이지만, 궤도를 따라 주기적으로 움직이기에 달의 움직임을 1차원 원 위에서 나타낼 수 있는 것과 같은 원리이다.
이를 통해 연구팀은 박테리아 사이의 복잡한 상호작용을 원 위를 주기적으로 움직이는 두 점의 상호작용으로 단순화할 수 있었다.
연구팀은 양성 피드백 룹이 있으면 두 점의 위치 차이가 커도 시간이 지날수록 점점 차이가 줄어들어 결국 동시에 움직이는 것을 확인했다. 연구팀은 이러한 수학적 분석 결과를 실험을 통해서 검증함으로써 넓은 공간에서 세포가 효과적으로 상호작용하는 방식을 규명했다.
김재경 교수는 “세포들이 자신의 목소리는 낮추고 상대방의 목소리에는 더 귀 기울일 때만 한목소리를 낼 수 있다는 점이 인상적이다”라며 “이러한 원리는 수학을 이용한 복잡한 시스템의 단순화 없이는 찾지 못했을 것이다. 복잡한 것을 단순하게 볼 수 있도록 해주는 것이 수학의 힘이다”라고 말했다.
2019.10.15 조회수 16273 -
 전성윤 교수, 8시간 안에 항생제 조합 성능 확인하는 기술 개발
〈 김승규 연구원, 전성윤 교수 〉
우리 대학 기계공학과 전성윤 교수 연구팀(바이오미세유체 연구실)이 미세유체 칩을 이용해 두 개의 항생제 간 시너지 효과를 8시간 만에 검사할 수 있는 기술을 개발했다.
이번 연구는 항생제의 시너지 효과 검사에 최소 24시간 소요돼 활용이 어려웠던 기존 기술을 크게 개선한 것으로, 향후 환자들에게 적절한 항생제 조합치료를 할 수 있는 기반 기술이 될 것으로 기대된다.
김승규 석박사통합과정이 1 저자로 참여하고 생명과학과 정현정 교수 연구팀과 공동으로 수행한 이번 연구는 영국 왕립화학회(Royal Society of Chemistry)에서 발행하는 ‘랩온어칩(Lab on a Chip)’ 3월 21일 자 뒤표지 논문으로 게재됐다. (논문명 : On-chip phenotypic investigation of combinatory antibiotic effects by generating orthogonal concentration gradients, 직교 농도구배 형성을 통한 칩 상 항생제 조합 효과 검사)
항생제에 매우 높은 저항성을 갖는 ‘슈퍼박테리아’의 등장은 세계적으로 병원 및 관련 기관에 큰 위협으로 떠오르고 있다. 지난 2014년에는 세계보건기구(WHO)가 병원균의 항생제에 대한 내성이 심각한 수준에 도달했다고 공식적으로 처음 보고하기도 했다.
이러한 항생제 저항성 병원균을 효과적으로 억제하기 위해 두 종류 이상의 항생제를 섞어 처리하는 ‘항생제 조합 치료’가 주목받고 있지만, 항생제의 종류와 적정한 농도 범위가 큰 영향을 미쳐 정확한 조합을 해야 할뿐더러 치료가 항상 효과적이지는 않다는 문제점이 있다.
따라서 미지의 항생제 저항성 병원균을 대상으로 체외 항생제 조합 검사를 통해 적합한 항생제 조합과 농도 범위를 찾는 것은 매우 중요한 과정이다. 하지만 기존 검사 방식은 항생제 희석 및 샘플 준비 과정이 불편하고 결과 도출까지 24시간 이상이 걸려 대부분 경험적 치료에 의존하고 있다.
연구팀은 문제 해결을 위해 필요한 샘플 양이 수십 마이크로리터에 불과한 미세유체 칩을 이용했다. 머리카락 굵기 수준의 좁은 미세채널에서 유체 흐름을 제어할 수 있는 시스템인 미세유체 칩을 통해 두 개의 항생제 간 농도조합 121개를 단 35분 만에 자동으로 형성했다.
연구팀은 박테리아 샘플을 아가로스 젤과 섞어 미세채널에 주입해 굳힌 뒤 이를 둘러싸는 미세채널들에 각 항생제가 포함된 시약과 항생제가 포함되지 않은 시약을 주입했다.
항생제가 첨가된 채널로부터 항생제가 없는 채널로 항생제 분자들의 확산이 이뤄지고 결국 두 항생제의 조합이 박테리아가 굳혀있는 아가로스 젤에 35분 만에 형성된다. 연구팀은 이후 6시간 동안 억제되는 박테리아의 성장을 현미경을 통해 관찰했다.
연구팀은 서로 다른 항균 원리를 갖는 다섯 종류의 항생제를 두 개씩 조합해 녹농균(Pseudomonas aeruginosa)을 대상으로 항생제 조합 효능 검사를 시행했다. 그 결과 항생제 짝에 따라 각기 다른 항균효과를 확인할 수 있었고 검사한 항생제 짝의 시너지 관계를 분류할 수 있었다.
연구팀의 미세유체 칩 기반의 검사 방식은 번거로운 희석과정과 긴 검사 시간으로 인해 불편했던 기존 검사 방식을 크게 개선했다.
이전에도 전 교수 연구팀은 ‘미세유체 칩 기반의 항생제 효능 신속검사 기술’을 개발해 지난 2월 5일 ‘바이오마이크로플루이딕스(Biomicrofluidics)’지에 피처 기사로 게재한 바 있다. 이번 논문은 그 후속 연구로 미세유체 칩이 차세대 약물 검사 플랫폼으로 활용될 가능성을 제시했다는 의의가 있다.
연구책임자인 전 교수는 “미세유체 칩의 약물 검사 플랫폼으로써의 발전 가능성은 무궁무진하다”라며 “개발한 미세유체 칩이 상용화돼 실제 현장에서 항생제 조합치료를 위해 활용되기를 기대한다”라고 말했다.
이번 연구는 EEWS 기후변화연구허브사업과 교육부 이공분야기초연구사업 및 BK21 플러스프로그램의 지원을 받아 수행됐다.
그림 설명
그림1. Lab on a Chip 표지 이미지
그림2. 본 연구의 미세유체 칩과 분석결과 예시
2019.04.05 조회수 25749
전성윤 교수, 8시간 안에 항생제 조합 성능 확인하는 기술 개발
〈 김승규 연구원, 전성윤 교수 〉
우리 대학 기계공학과 전성윤 교수 연구팀(바이오미세유체 연구실)이 미세유체 칩을 이용해 두 개의 항생제 간 시너지 효과를 8시간 만에 검사할 수 있는 기술을 개발했다.
이번 연구는 항생제의 시너지 효과 검사에 최소 24시간 소요돼 활용이 어려웠던 기존 기술을 크게 개선한 것으로, 향후 환자들에게 적절한 항생제 조합치료를 할 수 있는 기반 기술이 될 것으로 기대된다.
김승규 석박사통합과정이 1 저자로 참여하고 생명과학과 정현정 교수 연구팀과 공동으로 수행한 이번 연구는 영국 왕립화학회(Royal Society of Chemistry)에서 발행하는 ‘랩온어칩(Lab on a Chip)’ 3월 21일 자 뒤표지 논문으로 게재됐다. (논문명 : On-chip phenotypic investigation of combinatory antibiotic effects by generating orthogonal concentration gradients, 직교 농도구배 형성을 통한 칩 상 항생제 조합 효과 검사)
항생제에 매우 높은 저항성을 갖는 ‘슈퍼박테리아’의 등장은 세계적으로 병원 및 관련 기관에 큰 위협으로 떠오르고 있다. 지난 2014년에는 세계보건기구(WHO)가 병원균의 항생제에 대한 내성이 심각한 수준에 도달했다고 공식적으로 처음 보고하기도 했다.
이러한 항생제 저항성 병원균을 효과적으로 억제하기 위해 두 종류 이상의 항생제를 섞어 처리하는 ‘항생제 조합 치료’가 주목받고 있지만, 항생제의 종류와 적정한 농도 범위가 큰 영향을 미쳐 정확한 조합을 해야 할뿐더러 치료가 항상 효과적이지는 않다는 문제점이 있다.
따라서 미지의 항생제 저항성 병원균을 대상으로 체외 항생제 조합 검사를 통해 적합한 항생제 조합과 농도 범위를 찾는 것은 매우 중요한 과정이다. 하지만 기존 검사 방식은 항생제 희석 및 샘플 준비 과정이 불편하고 결과 도출까지 24시간 이상이 걸려 대부분 경험적 치료에 의존하고 있다.
연구팀은 문제 해결을 위해 필요한 샘플 양이 수십 마이크로리터에 불과한 미세유체 칩을 이용했다. 머리카락 굵기 수준의 좁은 미세채널에서 유체 흐름을 제어할 수 있는 시스템인 미세유체 칩을 통해 두 개의 항생제 간 농도조합 121개를 단 35분 만에 자동으로 형성했다.
연구팀은 박테리아 샘플을 아가로스 젤과 섞어 미세채널에 주입해 굳힌 뒤 이를 둘러싸는 미세채널들에 각 항생제가 포함된 시약과 항생제가 포함되지 않은 시약을 주입했다.
항생제가 첨가된 채널로부터 항생제가 없는 채널로 항생제 분자들의 확산이 이뤄지고 결국 두 항생제의 조합이 박테리아가 굳혀있는 아가로스 젤에 35분 만에 형성된다. 연구팀은 이후 6시간 동안 억제되는 박테리아의 성장을 현미경을 통해 관찰했다.
연구팀은 서로 다른 항균 원리를 갖는 다섯 종류의 항생제를 두 개씩 조합해 녹농균(Pseudomonas aeruginosa)을 대상으로 항생제 조합 효능 검사를 시행했다. 그 결과 항생제 짝에 따라 각기 다른 항균효과를 확인할 수 있었고 검사한 항생제 짝의 시너지 관계를 분류할 수 있었다.
연구팀의 미세유체 칩 기반의 검사 방식은 번거로운 희석과정과 긴 검사 시간으로 인해 불편했던 기존 검사 방식을 크게 개선했다.
이전에도 전 교수 연구팀은 ‘미세유체 칩 기반의 항생제 효능 신속검사 기술’을 개발해 지난 2월 5일 ‘바이오마이크로플루이딕스(Biomicrofluidics)’지에 피처 기사로 게재한 바 있다. 이번 논문은 그 후속 연구로 미세유체 칩이 차세대 약물 검사 플랫폼으로 활용될 가능성을 제시했다는 의의가 있다.
연구책임자인 전 교수는 “미세유체 칩의 약물 검사 플랫폼으로써의 발전 가능성은 무궁무진하다”라며 “개발한 미세유체 칩이 상용화돼 실제 현장에서 항생제 조합치료를 위해 활용되기를 기대한다”라고 말했다.
이번 연구는 EEWS 기후변화연구허브사업과 교육부 이공분야기초연구사업 및 BK21 플러스프로그램의 지원을 받아 수행됐다.
그림 설명
그림1. Lab on a Chip 표지 이미지
그림2. 본 연구의 미세유체 칩과 분석결과 예시
2019.04.05 조회수 25749 -
 이상엽 특훈교수, 병원균이 항생제에 내성을 갖는 원리 규명
〈 이 상 엽 교수 〉
우리 대학 생명화학공학과 이상엽 교수와 덴마크 공대(DTU) 노보 노르디스크 바이오지속가능센터(Novo Nordist Foundation Center for Biosustainability) 공동 연구팀이 박테리아 병원균이 항생제에 대한 내성을 획득하는 작동 원리를 밝혔다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 7일자 온라인 판에 게재됐다.
항생제 남용 등으로 인해 항생제 내성균이 점점 더 늘어나고 있다. 이는 인류의 생존을 위협하는 문제로 그 심각성이 전 세계적으로 점점 커지고 있다.
인체 감염균이 항생제 내성을 갖는 방식에는 항생제를 분해하는 효소를 갖거나 다시 뱉어내는 등 다양한 방식이 있다. 그 중 대표적인 것은 항생제 내성 유전자를 획득해 항생제를 무용지물로 만드는 것이다.
내성 유전자는 보통 항생제를 생산하는 곰팡이나 악티노박테리아에서 발견된다. 이는 해당 항생제를 만드는 곰팡이와 박테리아가 자기 스스로를 항생제로부터 보호하기 위해 갖고 있는 것이다.
이 내성 유전자를 인체 감염균이 획득하면 항생제 내성을 갖게 된다. 이러한 사실은 게놈 정보 등을 통해 이미 알려져 있는 사실이다.
그러나 어떤 방식으로 항생제 내성 유전자들이 인체 감염균에 전달되는지는 밝혀지지 않았다.
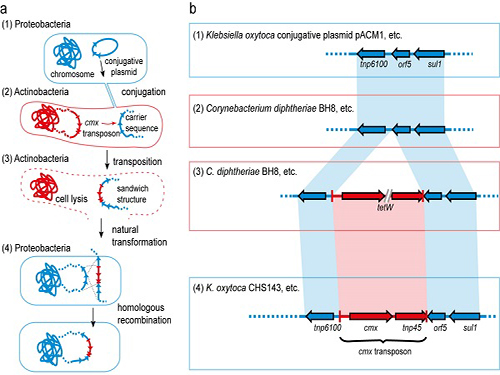
이상엽 교수와 덴마크 공대 공동 연구팀은 항생제 내성 유전자가 직접적으로 인체 감염균에 전달되는 것이 아니라 연구팀이 캐리백(carry-back)이라고 이름 지은 복잡한 과정을 통해 이뤄지는 것을 규명했다.
우선 인체 감염균과 방선균이 박테리아간의 성교에 해당하는 접합(conjugation)에 의해 인체 감염균의 DNA 일부가 방선균으로 들어간다.
그 와중에 항생제 내성 유전자 양쪽 주위에도 감염균의 DNA가 들어가는경우가 생긴다. 이 상태에서 방선균이 죽어 세포가 깨지면 항생제 내성 유전자와 감염균의 DNA 조각이 포함된 DNA들도 함께 나오게 된다.
이렇게 배출된 항생제 내성 유전자에는 인체 감염균의 일부 DNA가 양쪽에 공존하고 있다. 이 때문에 인체 감염균은 자신의 게놈에 재삽입이 가능해지고 이를 통해 항생제 내성을 획득한다.
연구팀은 생물정보학적 분석과 실제 실험을 통해 이를 증명했다.
이 교수는 “이번 연구결과는 인체 감염 유해균들이 항생제 내성을 획득하는 방식 중 한 가지를 제시한 것이다”며 “병원 내, 외부의 감염과 예방 관리시스템, 항생제의 올바른 사용에 대해 다시 한 번 생각할 수 있는 기회를 제공할 것이다”고 말했다.
이번 연구는 노보 노르디스크 재단과 미래창조과학부 원천기술과(바이오리파이너리를 위한 시스템대사공학 연구사업)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 항생제 내성 유전자가 전달되는 캐리백 현상의 모식도
2017.06.19 조회수 23860
이상엽 특훈교수, 병원균이 항생제에 내성을 갖는 원리 규명
〈 이 상 엽 교수 〉
우리 대학 생명화학공학과 이상엽 교수와 덴마크 공대(DTU) 노보 노르디스크 바이오지속가능센터(Novo Nordist Foundation Center for Biosustainability) 공동 연구팀이 박테리아 병원균이 항생제에 대한 내성을 획득하는 작동 원리를 밝혔다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 7일자 온라인 판에 게재됐다.
항생제 남용 등으로 인해 항생제 내성균이 점점 더 늘어나고 있다. 이는 인류의 생존을 위협하는 문제로 그 심각성이 전 세계적으로 점점 커지고 있다.
인체 감염균이 항생제 내성을 갖는 방식에는 항생제를 분해하는 효소를 갖거나 다시 뱉어내는 등 다양한 방식이 있다. 그 중 대표적인 것은 항생제 내성 유전자를 획득해 항생제를 무용지물로 만드는 것이다.
내성 유전자는 보통 항생제를 생산하는 곰팡이나 악티노박테리아에서 발견된다. 이는 해당 항생제를 만드는 곰팡이와 박테리아가 자기 스스로를 항생제로부터 보호하기 위해 갖고 있는 것이다.
이 내성 유전자를 인체 감염균이 획득하면 항생제 내성을 갖게 된다. 이러한 사실은 게놈 정보 등을 통해 이미 알려져 있는 사실이다.
그러나 어떤 방식으로 항생제 내성 유전자들이 인체 감염균에 전달되는지는 밝혀지지 않았다.
이상엽 교수와 덴마크 공대 공동 연구팀은 항생제 내성 유전자가 직접적으로 인체 감염균에 전달되는 것이 아니라 연구팀이 캐리백(carry-back)이라고 이름 지은 복잡한 과정을 통해 이뤄지는 것을 규명했다.
우선 인체 감염균과 방선균이 박테리아간의 성교에 해당하는 접합(conjugation)에 의해 인체 감염균의 DNA 일부가 방선균으로 들어간다.
그 와중에 항생제 내성 유전자 양쪽 주위에도 감염균의 DNA가 들어가는경우가 생긴다. 이 상태에서 방선균이 죽어 세포가 깨지면 항생제 내성 유전자와 감염균의 DNA 조각이 포함된 DNA들도 함께 나오게 된다.
이렇게 배출된 항생제 내성 유전자에는 인체 감염균의 일부 DNA가 양쪽에 공존하고 있다. 이 때문에 인체 감염균은 자신의 게놈에 재삽입이 가능해지고 이를 통해 항생제 내성을 획득한다.
연구팀은 생물정보학적 분석과 실제 실험을 통해 이를 증명했다.
이 교수는 “이번 연구결과는 인체 감염 유해균들이 항생제 내성을 획득하는 방식 중 한 가지를 제시한 것이다”며 “병원 내, 외부의 감염과 예방 관리시스템, 항생제의 올바른 사용에 대해 다시 한 번 생각할 수 있는 기회를 제공할 것이다”고 말했다.
이번 연구는 노보 노르디스크 재단과 미래창조과학부 원천기술과(바이오리파이너리를 위한 시스템대사공학 연구사업)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 항생제 내성 유전자가 전달되는 캐리백 현상의 모식도
2017.06.19 조회수 23860 -
 김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 21341
김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 21341 -
 대사공학적으로 개량된 박테리아로 범용 플라스틱 생산기술 개발
- 이상엽 교수팀과 LG 화학 연구팀 공동개발
- 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지 게재예정
생명화학공학과 이상엽(李相燁, 45세, LG화학 석좌교수, 생명과학기술대학 학장) 특훈교수팀과 LG화학 기술연구원(원장 유진녕) 박시재, 양택호박사팀이 4년여 간의 공동연구를 통해 박테리아를 이용하여 재생 가능한 바이오매스로부터 플라스틱을 생산하는 기술을 최근 개발했다.
교육과학기술부 시스템생물학 연구개발 사업과 LG화학 석좌교수 연구비로 지원된 이번 연구에서는 시스템 대사공학과 효소공학 기법을 접목, 자연적으로는 생성되지 않는 플라스틱(unnatural polymer)의 일종으로 최근 각광을 받고 있는 폴리유산(Polylactic acid, PLA)을 효율적으로 생산할 수 있는 대장균을 개발한 것이다.
이번 연구 결과는 바이오공학 분야 최고 전통의 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지에 게재 승인됐으며 스포트라이트 논문(Spotlight paper)으로 선정돼 2010년 1월호에 두 편의 연속 논문으로 게재될 예정이다.
두 논문의 제목은 ‘개량된 프로피오네이트 코엔자임 에이 트랜스퍼레이즈와 폴리하이드록시알카노에이트 중합효소를 이용한 폴리유산과 그의 공중합체의 생합성(Biosynthesis of Polylactic acid and its Copolymers Using Evolved Propionate CoA Transferase and PHA Synthase)’과 ‘폴리유산과 그의 공중합체의 생산을 위한 대장균의 대사공학(Metabolic Engineering of Escherichia coli for the Production of Polylactic Acid and its Copolymers)’이다. 19건의 특허가 전 세계 출원 중이다.
기존의 복잡한 2단계 공정을 통해 생산되던 폴리유산을 재생가능한 원료로부터 미생물의 직접 발효에 의해 생산이 가능하도록 한 혁신적인 본 연구 전략은 앞으로 석유 유래 플라스틱을 대체할 수 있는 다양한 비자연 고분자(unnatural polymer)들의 생산에 활용될 획기적인 기술로 평가되고 있다.
폴리유산 (Polylactic acid, PLA)은 많은 바이오매스 유래 고분자들 중에서도 생분해성, 생체적합성, 구조적 안정성, 그리고 낮은 독성과 같은 뛰어난 물성으로 인해 석유 유래 플라스틱의 대체물로서 대두되고 있다.
그러나, 폴리유산은 현재 두 단계 공정으로 합성된다. 우선, 미생물 발효를 통해 유산(락트산, Lactic acid)을 생산, 정제한 후 여러 가지 시약, 용매 및 촉매가 첨가되는 복잡한 공정의 화학적 중합반응에 의해 폴리유산이 합성된다.
또한, 폴리유산의 물성을 다양하게 개선하기 위해 폴리하이드록시알카노에이트 (Polyhydroxyalkanoate, PHA)와 같은 다른 고분자들과의 공중합이나 혼합반응 등의 연구가 이루어지고 있다.
이러한 노력에도 불구하고, 공중합 반응에 사용되는 락톤계 모노머들의 가용성과 비용을 고려했을 때, 기존의 화학적 합성 방법은 효과적이지 않다. 이에, 미생물 유래 고분자인 폴리하이드록시알카노에이트의 생합성 시스템을 기반으로, 폴리유산과 그의 공중합체들의 생합성이 가능할 수 있는 대사경로를 효소공학을 통해 구축했다.
그러나, 외래 대사경로의 도입 및 조작만으로는 폴리유산 단일 중합체와 유산의 함량이 높은 공중합체의 생산이 효율적이지 않아, 시스템 수준으로 세포 내 대사흐름을 증가시킬 필요성을 인지했다. 이에, 대장균 균주의 인실리코 게놈 수준의 시뮬레이션을 이용한 대사흐름분석 기법을 활용하여 고분자 생산을 위한 주요 전구체의 대사 흐름을 논리적으로 강화시킴으로써, 세포성장과 함께 목적 고분자의 효율적 생산이 가능하도록 했다.
따라서, 효소공학을 통한 고분자 합성 경로의 직접적 조작 및 강화 뿐 아니라, 시스템 대사공학을 통한 논리적 접근으로 조작된 대사흐름을 바탕으로 다양한 폴리유산 플라스틱을 보다 효율적으로 생산할 수 있었다.
이는 시스템 대사공학과 효소공학을 접목시킨 고기술 전략으로 비자연 고분자를 효율적으로 생산한 최초의 성공적인 예로서, 재생가능한 자원으로부터 폴리유산뿐 아니라 석유유래 플라스틱을 대체할 수 있는 다른 비자연 고분자들의 일단계 생산을 위한 기반 기술을 마련해줌으로써, 플라스틱 생산 공정에 있어 새로운 전략을 제시했다.
李 교수는 “자연계에 없는 고분자를 미생물로 생산하는 것이 과연 될까? 라는 의문을 갖고 시작했다. 우리 KAIST 연구실의 정유경박사와 LG화학 기술연구원 연구팀원 10여명이 4년간의 끈질긴 노력 끝에 성공했다”며, “이번 연구는 대장균의 가상세포 시뮬레이션을 통해 세포 내 대사흐름을 목적한 고분자 생산에 유리하도록 논리적으로 조작하고, 고분자 생합성 경로를 구성하는 외래 효소들을 새롭게 만들어 도입함으로써, 강화된 대사흐름을 이용해 보다 효율적으로 목적 고분자를 생산할 수 있는 균주를 개발하는데 성공한 세계 첫 번째 케이스다. 특히, 유산이 단량체로 함유된 공중합체의 경우에는 세계최초로 만든 것이 되어 물질특허들로 출원중이다”라고 밝혔다.
한편, 이 혁신적인 연구 성과는 22일 미국 CNN 홈페이지의 Top기사 등 해외언론의 주요기사로 소개됐다. 주요내용은 한국의 KAIST 이상엽 교수팀과 LG화학 연구팀이 전 세계적으로 석유고갈, 지구온난화 및 환경오염 문제로 재생가능한 자원을 이용한 바이오매스 기반 기술의 개발이 시급한 현 시대의 흐름에 부응하면서, 재생가능한 자원으로부터 효율적으로 바이오공학을 통한 플라스틱 (Bioengineered plastics) 폴리유산의 생산이 가능한 대장균 균주를 개발했다는 내용이다.
2009.11.24 조회수 26504
대사공학적으로 개량된 박테리아로 범용 플라스틱 생산기술 개발
- 이상엽 교수팀과 LG 화학 연구팀 공동개발
- 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지 게재예정
생명화학공학과 이상엽(李相燁, 45세, LG화학 석좌교수, 생명과학기술대학 학장) 특훈교수팀과 LG화학 기술연구원(원장 유진녕) 박시재, 양택호박사팀이 4년여 간의 공동연구를 통해 박테리아를 이용하여 재생 가능한 바이오매스로부터 플라스틱을 생산하는 기술을 최근 개발했다.
교육과학기술부 시스템생물학 연구개발 사업과 LG화학 석좌교수 연구비로 지원된 이번 연구에서는 시스템 대사공학과 효소공학 기법을 접목, 자연적으로는 생성되지 않는 플라스틱(unnatural polymer)의 일종으로 최근 각광을 받고 있는 폴리유산(Polylactic acid, PLA)을 효율적으로 생산할 수 있는 대장균을 개발한 것이다.
이번 연구 결과는 바이오공학 분야 최고 전통의 바이오테크놀로지 바이오엔지니어링(Biotechnology and Bioengineering)지에 게재 승인됐으며 스포트라이트 논문(Spotlight paper)으로 선정돼 2010년 1월호에 두 편의 연속 논문으로 게재될 예정이다.
두 논문의 제목은 ‘개량된 프로피오네이트 코엔자임 에이 트랜스퍼레이즈와 폴리하이드록시알카노에이트 중합효소를 이용한 폴리유산과 그의 공중합체의 생합성(Biosynthesis of Polylactic acid and its Copolymers Using Evolved Propionate CoA Transferase and PHA Synthase)’과 ‘폴리유산과 그의 공중합체의 생산을 위한 대장균의 대사공학(Metabolic Engineering of Escherichia coli for the Production of Polylactic Acid and its Copolymers)’이다. 19건의 특허가 전 세계 출원 중이다.
기존의 복잡한 2단계 공정을 통해 생산되던 폴리유산을 재생가능한 원료로부터 미생물의 직접 발효에 의해 생산이 가능하도록 한 혁신적인 본 연구 전략은 앞으로 석유 유래 플라스틱을 대체할 수 있는 다양한 비자연 고분자(unnatural polymer)들의 생산에 활용될 획기적인 기술로 평가되고 있다.
폴리유산 (Polylactic acid, PLA)은 많은 바이오매스 유래 고분자들 중에서도 생분해성, 생체적합성, 구조적 안정성, 그리고 낮은 독성과 같은 뛰어난 물성으로 인해 석유 유래 플라스틱의 대체물로서 대두되고 있다.
그러나, 폴리유산은 현재 두 단계 공정으로 합성된다. 우선, 미생물 발효를 통해 유산(락트산, Lactic acid)을 생산, 정제한 후 여러 가지 시약, 용매 및 촉매가 첨가되는 복잡한 공정의 화학적 중합반응에 의해 폴리유산이 합성된다.
또한, 폴리유산의 물성을 다양하게 개선하기 위해 폴리하이드록시알카노에이트 (Polyhydroxyalkanoate, PHA)와 같은 다른 고분자들과의 공중합이나 혼합반응 등의 연구가 이루어지고 있다.
이러한 노력에도 불구하고, 공중합 반응에 사용되는 락톤계 모노머들의 가용성과 비용을 고려했을 때, 기존의 화학적 합성 방법은 효과적이지 않다. 이에, 미생물 유래 고분자인 폴리하이드록시알카노에이트의 생합성 시스템을 기반으로, 폴리유산과 그의 공중합체들의 생합성이 가능할 수 있는 대사경로를 효소공학을 통해 구축했다.
그러나, 외래 대사경로의 도입 및 조작만으로는 폴리유산 단일 중합체와 유산의 함량이 높은 공중합체의 생산이 효율적이지 않아, 시스템 수준으로 세포 내 대사흐름을 증가시킬 필요성을 인지했다. 이에, 대장균 균주의 인실리코 게놈 수준의 시뮬레이션을 이용한 대사흐름분석 기법을 활용하여 고분자 생산을 위한 주요 전구체의 대사 흐름을 논리적으로 강화시킴으로써, 세포성장과 함께 목적 고분자의 효율적 생산이 가능하도록 했다.
따라서, 효소공학을 통한 고분자 합성 경로의 직접적 조작 및 강화 뿐 아니라, 시스템 대사공학을 통한 논리적 접근으로 조작된 대사흐름을 바탕으로 다양한 폴리유산 플라스틱을 보다 효율적으로 생산할 수 있었다.
이는 시스템 대사공학과 효소공학을 접목시킨 고기술 전략으로 비자연 고분자를 효율적으로 생산한 최초의 성공적인 예로서, 재생가능한 자원으로부터 폴리유산뿐 아니라 석유유래 플라스틱을 대체할 수 있는 다른 비자연 고분자들의 일단계 생산을 위한 기반 기술을 마련해줌으로써, 플라스틱 생산 공정에 있어 새로운 전략을 제시했다.
李 교수는 “자연계에 없는 고분자를 미생물로 생산하는 것이 과연 될까? 라는 의문을 갖고 시작했다. 우리 KAIST 연구실의 정유경박사와 LG화학 기술연구원 연구팀원 10여명이 4년간의 끈질긴 노력 끝에 성공했다”며, “이번 연구는 대장균의 가상세포 시뮬레이션을 통해 세포 내 대사흐름을 목적한 고분자 생산에 유리하도록 논리적으로 조작하고, 고분자 생합성 경로를 구성하는 외래 효소들을 새롭게 만들어 도입함으로써, 강화된 대사흐름을 이용해 보다 효율적으로 목적 고분자를 생산할 수 있는 균주를 개발하는데 성공한 세계 첫 번째 케이스다. 특히, 유산이 단량체로 함유된 공중합체의 경우에는 세계최초로 만든 것이 되어 물질특허들로 출원중이다”라고 밝혔다.
한편, 이 혁신적인 연구 성과는 22일 미국 CNN 홈페이지의 Top기사 등 해외언론의 주요기사로 소개됐다. 주요내용은 한국의 KAIST 이상엽 교수팀과 LG화학 연구팀이 전 세계적으로 석유고갈, 지구온난화 및 환경오염 문제로 재생가능한 자원을 이용한 바이오매스 기반 기술의 개발이 시급한 현 시대의 흐름에 부응하면서, 재생가능한 자원으로부터 효율적으로 바이오공학을 통한 플라스틱 (Bioengineered plastics) 폴리유산의 생산이 가능한 대장균 균주를 개발했다는 내용이다.
2009.11.24 조회수 26504