%ED%95%99%EB%AC%B8%ED%9B%84%EC%86%8D%EC%84%B8%EB%8C%80%EC%96%91%EC%84%B1%EC%82%AC%EC%97%85
-
 신경세포 연결해주는 접착단백질 결합구조 규명
국내 연구진이 신경세포 연결을 주관하는 시냅스접착단백질**의 3차원 복합체 구조를 규명함으로써, 시냅스* 형성초기 기전을 제시하였다. 시냅스 이상으로 인한 강박증이나 조울증 등 다양한 뇌질환의 발병기전 규명과 치료제 개발에 활용될 것으로 기대된다.
* 시냅스 : 신경전달물질의 분비와 흡수가 일어나는 1,000억 여 개에 달하는 신경세포의 접합부위로 학습과 기억, 감각, 운동 등을 조절하는 뇌 활동의 기본단위이다. ** 시냅스접착단백질 : 벨크로처럼 두 개의 신경세포를 단단하게 연결해 시냅스 형성을 돕는 신경세포막에 존재하는 단백질
우리 학교 의과학대학원 김호민 교수와 연세대 생화학과 고재원 교수 (이상 교신저자)가 주도하고, 연세대 엄지원 연구교수, KAIST 김기훈 석사과정 연구원 및 을지대 박범석 교수(이상 제1저자)가 참여한 이번 연구는 미래창조과학부와 한국연구재단이 지원하는 신진연구자지원사업, 중견연구자지원사업(핵심연구) 및 교육부 학문후속세대양성사업의 지원으로 수행되었고 자연과학 분야 국제학술지 네이처 커뮤니케이션스(Nature Communications)지 온라인판 11월 14일자에 게재되었다. (논문명 : Structural basis for LAR-RPTP/Slitrk complex-mediated synaptic adhesion)
신경세포막에 존재하는 단백질 슬릿트랙*은 다른 신경세포의 막에 존재하는 단백질 LAR-RPTP**와 복합체를 이뤄 초기 시냅스 형성과 신경세포의 흥분과 억제간의 균형 유지에 관여하는 것으로 알려져 있었다.
* 슬릿트랙(Slitrk) : 뇌의 중추신경계에서 강하게 발현되는 단백질. 이 유전자가 결핍된 형질전환생쥐의 경우 다양한 뇌질환 표현형을 나타냄. 최근 LAR-RPTP와 결합하여 시냅스 형성을 조절하는 시냅스접착단백질임이 밝혀짐
** LAR-RPTP : 신경세포의 초기 발달과정에서 중요한 역할을 하는 단백질 군. 최근 시냅스 형성에 관계된 주요 기능들이 조금씩 밝혀지면서 새롭게 주목 받기 시작한시냅스접착단백질
이들 두 단백질의 이상은 시냅스의 기능이상을 유발해 자폐증, 정신분열증, 간질, 강박증 및 조울증 같은 다양한 신경·정신질환을 유발하는 것으로 알려져 있지만 두 단백질의 결합구조와 구체적인 작용기전이 규명되지 않아 치료제 개발에 한계가 있었다.
연구팀은 단백질 결정학기술과 바이오투과전자현미경을 활용해 두 시냅스접착단백질(슬릿트랙(Slitrk)과 LAR-RPTP)이 결합된 3차원 구조를 밝혀내고 이들 상호간의 결합의 핵심이 되는 부위를 찾아냈다.
나아가 두 시냅스접착 단백질이 결합한 후 클러스터를 형성하면서 시냅스 생성이 유도된다는 것을 규명하였다.
김호민 교수는 “시냅스접착단백질의 기능 이상으로 나타나는 다양한 뇌질환의 발병기전 이해에 큰 밑거름이 될 것. 특히, 단백질 구조생물학과 신경생물학의 유기적인 협력연구를 통하여 우수한 성과를 거둔 대표적 사례가 될 것”이라고 밝혔다. 고재원 교수는 “시냅스접착단백질 분자기전을 이해함으로써 시냅스 형성 관련 연구의 새로운 방향을 제시할 것”이라고 연구의의를 밝혔다.
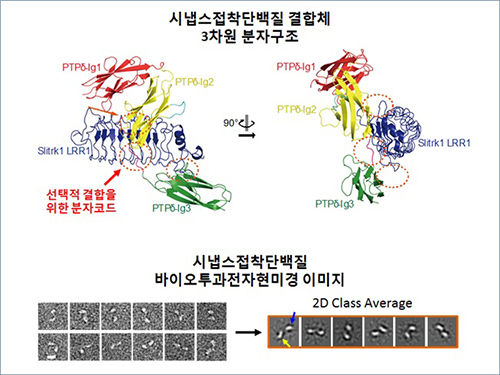
그림 1. 시냅스접착단백질 결합체 구조 및 슬릿트랫 바이오투과전자현미경 이미지
(위) 시냅스접착단백질 슬릿트랙(Slitrk)과 LAR-RPTP 결합체 분자구조
단백질결정학을 통해 시냅스접착단백질 결합체 분자구조를 분석한 결과 두 시냅스접착단백질의 결합에 중추적인 역할을 하는 핵심적인 아미노산을 도출할 수 있었다.
특히 LAR-RPTP 단백질에 위치한 선택적 접합(Alternative splicing) 부위(붉은색 화살표)가 슬릿트랙 (Slitrk)과 선택적으로 결합하기 위한 분자코드임을 규명하였다.
(아래) 슬릿트랙의 바이오투과전자현미경 이미지 단백질결정학으로는 규명이 어려운 전체 슬릿트랙 단백질 구조(세포막 바깥쪽부위)를 바이오투과전자현미경을 사용하여 분석하였다. 그림에서 보듯 전체 슬릿트랙은 땅콩처럼 생긴 비슷한 두 개의 단백질 모듈(푸른색, 노란색 화살표)로 구성되어 있고, 이들 중 한 부분(파란색 화살표)만 LAR-RPTP와 결합하게 된다는 것을 규명하였다.
그림 2. 시냅스접착단백질 결합에 의해 유도되는 시냅스형성 분자기전
전시냅스의 LAR-RPTP과 후시냅스의 슬릿트랙(Slitrk)의 결합이 단순한 결합에 그치는 것이 아니라 결합 이후 신경세포 막에서의 배열변화를 통해 단백질 클러스터 형성을 유도할 수 있음을 보였다.
그림 3. 시냅스 및 시냅스접착단백질 개요
시냅스는 1000 억여 개에 달하는 신경세포들의 접합 부위인 뇌기능의 기본단위로서 신경세포 간 교환되는 신경전달물질들에 의하여 학습 및 기억, 감각, 운동 등이 원활히 조절된다. 시냅스에는 약 1,000여종 단백질이 존재하며, 이들 중 신경세포 막에 존재하며 벨크로처럼 두 개의 신경세포를 단단하게 연결하여 시냅스 형성을 돕는 단백질을 시냅스접착단백질이라 한다. 현재 불과 10여개의 시냅스접착단백질만이 밝혀져 있고, 이중 최근에 주목받기 시작한 시냅스접착단백질이 슬릿트랫과 LAR-RPTP이다.
2014.11.20 조회수 20565
신경세포 연결해주는 접착단백질 결합구조 규명
국내 연구진이 신경세포 연결을 주관하는 시냅스접착단백질**의 3차원 복합체 구조를 규명함으로써, 시냅스* 형성초기 기전을 제시하였다. 시냅스 이상으로 인한 강박증이나 조울증 등 다양한 뇌질환의 발병기전 규명과 치료제 개발에 활용될 것으로 기대된다.
* 시냅스 : 신경전달물질의 분비와 흡수가 일어나는 1,000억 여 개에 달하는 신경세포의 접합부위로 학습과 기억, 감각, 운동 등을 조절하는 뇌 활동의 기본단위이다. ** 시냅스접착단백질 : 벨크로처럼 두 개의 신경세포를 단단하게 연결해 시냅스 형성을 돕는 신경세포막에 존재하는 단백질
우리 학교 의과학대학원 김호민 교수와 연세대 생화학과 고재원 교수 (이상 교신저자)가 주도하고, 연세대 엄지원 연구교수, KAIST 김기훈 석사과정 연구원 및 을지대 박범석 교수(이상 제1저자)가 참여한 이번 연구는 미래창조과학부와 한국연구재단이 지원하는 신진연구자지원사업, 중견연구자지원사업(핵심연구) 및 교육부 학문후속세대양성사업의 지원으로 수행되었고 자연과학 분야 국제학술지 네이처 커뮤니케이션스(Nature Communications)지 온라인판 11월 14일자에 게재되었다. (논문명 : Structural basis for LAR-RPTP/Slitrk complex-mediated synaptic adhesion)
신경세포막에 존재하는 단백질 슬릿트랙*은 다른 신경세포의 막에 존재하는 단백질 LAR-RPTP**와 복합체를 이뤄 초기 시냅스 형성과 신경세포의 흥분과 억제간의 균형 유지에 관여하는 것으로 알려져 있었다.
* 슬릿트랙(Slitrk) : 뇌의 중추신경계에서 강하게 발현되는 단백질. 이 유전자가 결핍된 형질전환생쥐의 경우 다양한 뇌질환 표현형을 나타냄. 최근 LAR-RPTP와 결합하여 시냅스 형성을 조절하는 시냅스접착단백질임이 밝혀짐
** LAR-RPTP : 신경세포의 초기 발달과정에서 중요한 역할을 하는 단백질 군. 최근 시냅스 형성에 관계된 주요 기능들이 조금씩 밝혀지면서 새롭게 주목 받기 시작한시냅스접착단백질
이들 두 단백질의 이상은 시냅스의 기능이상을 유발해 자폐증, 정신분열증, 간질, 강박증 및 조울증 같은 다양한 신경·정신질환을 유발하는 것으로 알려져 있지만 두 단백질의 결합구조와 구체적인 작용기전이 규명되지 않아 치료제 개발에 한계가 있었다.
연구팀은 단백질 결정학기술과 바이오투과전자현미경을 활용해 두 시냅스접착단백질(슬릿트랙(Slitrk)과 LAR-RPTP)이 결합된 3차원 구조를 밝혀내고 이들 상호간의 결합의 핵심이 되는 부위를 찾아냈다.
나아가 두 시냅스접착 단백질이 결합한 후 클러스터를 형성하면서 시냅스 생성이 유도된다는 것을 규명하였다.
김호민 교수는 “시냅스접착단백질의 기능 이상으로 나타나는 다양한 뇌질환의 발병기전 이해에 큰 밑거름이 될 것. 특히, 단백질 구조생물학과 신경생물학의 유기적인 협력연구를 통하여 우수한 성과를 거둔 대표적 사례가 될 것”이라고 밝혔다. 고재원 교수는 “시냅스접착단백질 분자기전을 이해함으로써 시냅스 형성 관련 연구의 새로운 방향을 제시할 것”이라고 연구의의를 밝혔다.
그림 1. 시냅스접착단백질 결합체 구조 및 슬릿트랫 바이오투과전자현미경 이미지
(위) 시냅스접착단백질 슬릿트랙(Slitrk)과 LAR-RPTP 결합체 분자구조
단백질결정학을 통해 시냅스접착단백질 결합체 분자구조를 분석한 결과 두 시냅스접착단백질의 결합에 중추적인 역할을 하는 핵심적인 아미노산을 도출할 수 있었다.
특히 LAR-RPTP 단백질에 위치한 선택적 접합(Alternative splicing) 부위(붉은색 화살표)가 슬릿트랙 (Slitrk)과 선택적으로 결합하기 위한 분자코드임을 규명하였다.
(아래) 슬릿트랙의 바이오투과전자현미경 이미지 단백질결정학으로는 규명이 어려운 전체 슬릿트랙 단백질 구조(세포막 바깥쪽부위)를 바이오투과전자현미경을 사용하여 분석하였다. 그림에서 보듯 전체 슬릿트랙은 땅콩처럼 생긴 비슷한 두 개의 단백질 모듈(푸른색, 노란색 화살표)로 구성되어 있고, 이들 중 한 부분(파란색 화살표)만 LAR-RPTP와 결합하게 된다는 것을 규명하였다.
그림 2. 시냅스접착단백질 결합에 의해 유도되는 시냅스형성 분자기전
전시냅스의 LAR-RPTP과 후시냅스의 슬릿트랙(Slitrk)의 결합이 단순한 결합에 그치는 것이 아니라 결합 이후 신경세포 막에서의 배열변화를 통해 단백질 클러스터 형성을 유도할 수 있음을 보였다.
그림 3. 시냅스 및 시냅스접착단백질 개요
시냅스는 1000 억여 개에 달하는 신경세포들의 접합 부위인 뇌기능의 기본단위로서 신경세포 간 교환되는 신경전달물질들에 의하여 학습 및 기억, 감각, 운동 등이 원활히 조절된다. 시냅스에는 약 1,000여종 단백질이 존재하며, 이들 중 신경세포 막에 존재하며 벨크로처럼 두 개의 신경세포를 단단하게 연결하여 시냅스 형성을 돕는 단백질을 시냅스접착단백질이라 한다. 현재 불과 10여개의 시냅스접착단백질만이 밝혀져 있고, 이중 최근에 주목받기 시작한 시냅스접착단백질이 슬릿트랫과 LAR-RPTP이다.
2014.11.20 조회수 20565 -
 단백질 나노튜브의 자기조립 분자스위치 발견
- 한국, 미국, 이스라엘 국제 공동 연구 성과 -
- 암 치료와 뇌 질환 메커니즘 단서 -
우리 학교 바이오및뇌공학과 최명철 교수와 송채연 연구교수는 미국
산타바바라 캘리포니아대학교, 이스라엘 히브리대학교와 공동으로 세포분열과 세포간 물질수송에 열쇠가 되는 단백질 나노튜브의 자기조립
구조를 제어하는 분자스위치를 발견했다.
연구 결과는 세계적 학술지 ‘네이처 머티리얼즈(Nature Materials, IF=35.7)’ 19일자에 게재됐다.
마이크로튜불(microtubule, 미세소관)은 사람의 몸속에서 세포분열·세포골격·세포간 물질수송 도구로 사용되는 튜브 형태의 단백질로 굵기가 25나노미터(1나노미터는 머리카락 굵기의 10만분의 1)에 불과하다.
대부분의 암 치료 약물은 마이크로튜불의 형성을 교란해 암세포 분열을
억제하는 것으로 작용 메커니즘이 알려져 있다. 알츠하이머병은 세포간 물질수송을 담당하는 마이크로튜불의 구조적 안정성이 떨어지면서
신경세포에서의 신호전달이 제대로 이루어지지 않아 생기는 대표적 뇌질환이다.
연구팀은 싱크로트론 X선 산란장치(synchrotron x-ray
scattering: 전자를 빛의 속도에 가깝게 가속시켜 강력한 X선을 발생시키는 장치)와 투과전자현미경을 이용해 단백질
나노튜브의 자기조립 구조를 서브나노미터(1나노미터 미만)의 정확도로 측정했다.
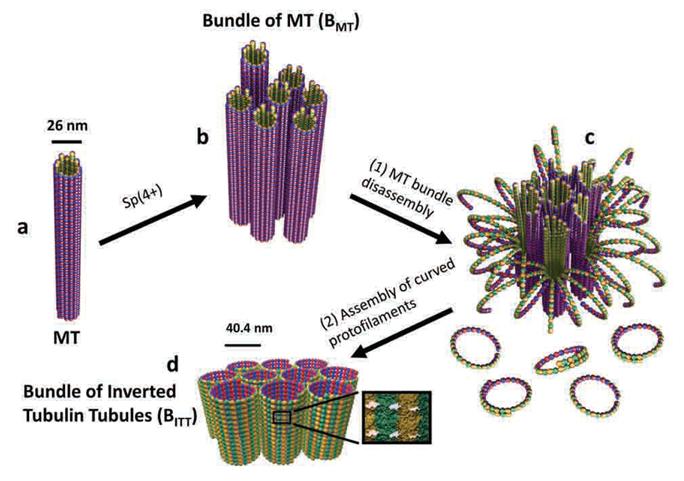
연구팀은 이번 연구를 분자 레벨에서 레고 블록을 쌓아 올리는 것에 비유해
가로×세로×폭이 각각 4×5×8 나노미터인 단백질 블록을 쌓아 올려 25나노미터 굵기의 튜브를 형성하는 메커니즘을 추적했다. 이
과정에서 연구팀은 레고 블록의 형태를 제어하는 분자스위치를 발견했다. 또 지금까지 보고된 바 없는 전혀 새로운 크기와 형태의
단백질 튜브 구조를 만들어 내는데 성공했다.
최명철 교수는 “인간의 생명 시스템은 고도의 자기조립 구조체를 형성해 복잡한 생물학적 기능을 하고 있지만 한편으로는 극히 단순한 물리학적 원리에 의해 제어가 가능하다는 새로운 패러다임을 제시했다”고 이 연구의 의의를 밝혔다.
또 “이번 연구는 암 치료와 뇌질환 메커니즘을 규명하고자하는 작은 발걸음이며 앞으로 바이오 나노튜브를 이용한 공학적 응용이 무궁무진할 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 국제협력사업, 신진연구자지원사업, 학문후속세대양성사업, KAIST 고위험 고수익 프로젝트(High Risk High Return Project)의 지원으로 수행됐다.
2014.01.21 조회수 25273
단백질 나노튜브의 자기조립 분자스위치 발견
- 한국, 미국, 이스라엘 국제 공동 연구 성과 -
- 암 치료와 뇌 질환 메커니즘 단서 -
우리 학교 바이오및뇌공학과 최명철 교수와 송채연 연구교수는 미국
산타바바라 캘리포니아대학교, 이스라엘 히브리대학교와 공동으로 세포분열과 세포간 물질수송에 열쇠가 되는 단백질 나노튜브의 자기조립
구조를 제어하는 분자스위치를 발견했다.
연구 결과는 세계적 학술지 ‘네이처 머티리얼즈(Nature Materials, IF=35.7)’ 19일자에 게재됐다.
마이크로튜불(microtubule, 미세소관)은 사람의 몸속에서 세포분열·세포골격·세포간 물질수송 도구로 사용되는 튜브 형태의 단백질로 굵기가 25나노미터(1나노미터는 머리카락 굵기의 10만분의 1)에 불과하다.
대부분의 암 치료 약물은 마이크로튜불의 형성을 교란해 암세포 분열을
억제하는 것으로 작용 메커니즘이 알려져 있다. 알츠하이머병은 세포간 물질수송을 담당하는 마이크로튜불의 구조적 안정성이 떨어지면서
신경세포에서의 신호전달이 제대로 이루어지지 않아 생기는 대표적 뇌질환이다.
연구팀은 싱크로트론 X선 산란장치(synchrotron x-ray
scattering: 전자를 빛의 속도에 가깝게 가속시켜 강력한 X선을 발생시키는 장치)와 투과전자현미경을 이용해 단백질
나노튜브의 자기조립 구조를 서브나노미터(1나노미터 미만)의 정확도로 측정했다.
연구팀은 이번 연구를 분자 레벨에서 레고 블록을 쌓아 올리는 것에 비유해
가로×세로×폭이 각각 4×5×8 나노미터인 단백질 블록을 쌓아 올려 25나노미터 굵기의 튜브를 형성하는 메커니즘을 추적했다. 이
과정에서 연구팀은 레고 블록의 형태를 제어하는 분자스위치를 발견했다. 또 지금까지 보고된 바 없는 전혀 새로운 크기와 형태의
단백질 튜브 구조를 만들어 내는데 성공했다.
최명철 교수는 “인간의 생명 시스템은 고도의 자기조립 구조체를 형성해 복잡한 생물학적 기능을 하고 있지만 한편으로는 극히 단순한 물리학적 원리에 의해 제어가 가능하다는 새로운 패러다임을 제시했다”고 이 연구의 의의를 밝혔다.
또 “이번 연구는 암 치료와 뇌질환 메커니즘을 규명하고자하는 작은 발걸음이며 앞으로 바이오 나노튜브를 이용한 공학적 응용이 무궁무진할 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 국제협력사업, 신진연구자지원사업, 학문후속세대양성사업, KAIST 고위험 고수익 프로젝트(High Risk High Return Project)의 지원으로 수행됐다.
2014.01.21 조회수 25273 -
 스트레스에 의해 생긴 잔주름의 숨겨진 비밀을 밝혀내다
- Nature Materials 표지논문 선정, ‘자연을 닮은 구조물’ 제작에 새로운 가능성 열어-
신진 여성과학자가 스트레스에 의해 생긴 잔주름이 성장하면서 깊은 주름으로 발전하는 전 과정을 가시화하여 그 원인을 규명함으로써 표면주름 제어기술 개발에 새로운 전기를 마련하였다.
카이스트 김필남 연구교수가 주도한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 직무대행 김병국)이 추진하는 학문후속세대양성사업(박사후 국외연수)의 지원을 받아 미국 프린스턴 대학에서 수행되었고, 연구결과는 세계 최고 권위의 과학전문지 ‘네이처(Nature)’의 대표적인 자매지인 ‘Nature Materials" 12월호(12월 1일자)에 표지논문으로 선정되는 영예를 얻었다.
김필남 박사 연구팀은 얇은 박막이 극심한 스트레스를 받으면서 생기는 잔주름이 깊은 골짜기 형태의 접힌 구조물로 변형해가는 일련의 과정을 밝히고, 이를 통해 자연계에서 나타날 수 있는 다양한 복합 구조물을 모방해내는 기반기술을 개발하는데 성공하였다.
표면주름은 여러 개로 적층된 구조에서 그 중 어느 한 층이 극도로 빠른 팽창(또는 수축)이 일어날 때 그 불안정성으로 나타나는 구조이다. 이러한 불안정성을 갖는 적층구조는 동․식물의 표피(피부)와 같은 생물의 조직뿐만 아니라, 최근 활발히 연구되고 있는 구겨지는 플렉시블 디스플레이(또는 소자)에서도 흔히 나타난다.
특히 생체조직에서는 주름이 지속적으로 성장하는 과정을 겪는데, 지금까지 이러한 이차원적인 표면에서 잔주름의 성장이 만들어내는 삼차원적인 구조의 변형에 대해서는 밝혀진 바가 없다. 이번 연구를 통해서 김 박사팀은 주름(wrinkle)이 곡률이 극심한 접힘(fold)이라는 구조로 변형되어가는 메커니즘을 규명하였다.
또한 연구팀은 실시간 분석을 통해 잔주름 구조물이 일련의 자기조직화 과정*을 거쳐 궁극적으로 그물망 형태의 접힘 구조물로 변형된다는 사실을 밝혀냈다. *) 자기 조직화 과정 : 계층적 방식(Hierarchical process), 자발적 제어과정 (Self-regulation process), 연속적인 구획화(Subdivision process) 및 분지화(Branching process) 등
흥미롭게도 연구팀은 이 과정을 통해 만들어진 구조는 건조한 땅이 갈라지면서 만들어내는 균열구조와 매우 흡사하고, 나뭇잎에서 볼 수 있는 맥관구조 뿐만 아니라, 인체에서 볼 수 있는 혈관 네트워크와도 매우 흡사한 구조를 가지고 있다는 사실을 발견하였다.
이번 연구는 무생물뿐만 아니라 생물계에서 보여주는 다양하지만 일관된 구조(그물망 구조 등)의 발생 원리를 기계적․물리학적 입장에서 재해석할 수 있음을 보여주는 결과이다. 따라서 이번 연구 결과는 모든 발생과정을 볼 수 없는 생물계에서의 구조화, 패턴화를 이해하는데 크게 기여할 것으로 평가된다.
김필남 박사는 “이번 연구는 오랫동안 연구되어왔던 ‘주름 또는 접힘’이라는 생물학적, 자연발생적 구조물을 이해하고 직접 제어․조절하여 ‘자연을 닮은 구조물’을 보다 쉽게 만들어 낼 수 있는 새로운 가능성을 제시하였다”고 연구의의를 밝혔다.
2011.12.20 조회수 20335
스트레스에 의해 생긴 잔주름의 숨겨진 비밀을 밝혀내다
- Nature Materials 표지논문 선정, ‘자연을 닮은 구조물’ 제작에 새로운 가능성 열어-
신진 여성과학자가 스트레스에 의해 생긴 잔주름이 성장하면서 깊은 주름으로 발전하는 전 과정을 가시화하여 그 원인을 규명함으로써 표면주름 제어기술 개발에 새로운 전기를 마련하였다.
카이스트 김필남 연구교수가 주도한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 직무대행 김병국)이 추진하는 학문후속세대양성사업(박사후 국외연수)의 지원을 받아 미국 프린스턴 대학에서 수행되었고, 연구결과는 세계 최고 권위의 과학전문지 ‘네이처(Nature)’의 대표적인 자매지인 ‘Nature Materials" 12월호(12월 1일자)에 표지논문으로 선정되는 영예를 얻었다.
김필남 박사 연구팀은 얇은 박막이 극심한 스트레스를 받으면서 생기는 잔주름이 깊은 골짜기 형태의 접힌 구조물로 변형해가는 일련의 과정을 밝히고, 이를 통해 자연계에서 나타날 수 있는 다양한 복합 구조물을 모방해내는 기반기술을 개발하는데 성공하였다.
표면주름은 여러 개로 적층된 구조에서 그 중 어느 한 층이 극도로 빠른 팽창(또는 수축)이 일어날 때 그 불안정성으로 나타나는 구조이다. 이러한 불안정성을 갖는 적층구조는 동․식물의 표피(피부)와 같은 생물의 조직뿐만 아니라, 최근 활발히 연구되고 있는 구겨지는 플렉시블 디스플레이(또는 소자)에서도 흔히 나타난다.
특히 생체조직에서는 주름이 지속적으로 성장하는 과정을 겪는데, 지금까지 이러한 이차원적인 표면에서 잔주름의 성장이 만들어내는 삼차원적인 구조의 변형에 대해서는 밝혀진 바가 없다. 이번 연구를 통해서 김 박사팀은 주름(wrinkle)이 곡률이 극심한 접힘(fold)이라는 구조로 변형되어가는 메커니즘을 규명하였다.
또한 연구팀은 실시간 분석을 통해 잔주름 구조물이 일련의 자기조직화 과정*을 거쳐 궁극적으로 그물망 형태의 접힘 구조물로 변형된다는 사실을 밝혀냈다. *) 자기 조직화 과정 : 계층적 방식(Hierarchical process), 자발적 제어과정 (Self-regulation process), 연속적인 구획화(Subdivision process) 및 분지화(Branching process) 등
흥미롭게도 연구팀은 이 과정을 통해 만들어진 구조는 건조한 땅이 갈라지면서 만들어내는 균열구조와 매우 흡사하고, 나뭇잎에서 볼 수 있는 맥관구조 뿐만 아니라, 인체에서 볼 수 있는 혈관 네트워크와도 매우 흡사한 구조를 가지고 있다는 사실을 발견하였다.
이번 연구는 무생물뿐만 아니라 생물계에서 보여주는 다양하지만 일관된 구조(그물망 구조 등)의 발생 원리를 기계적․물리학적 입장에서 재해석할 수 있음을 보여주는 결과이다. 따라서 이번 연구 결과는 모든 발생과정을 볼 수 없는 생물계에서의 구조화, 패턴화를 이해하는데 크게 기여할 것으로 평가된다.
김필남 박사는 “이번 연구는 오랫동안 연구되어왔던 ‘주름 또는 접힘’이라는 생물학적, 자연발생적 구조물을 이해하고 직접 제어․조절하여 ‘자연을 닮은 구조물’을 보다 쉽게 만들어 낼 수 있는 새로운 가능성을 제시하였다”고 연구의의를 밝혔다.
2011.12.20 조회수 20335