%EA%B9%80%ED%95%84%ED%95%9C
-
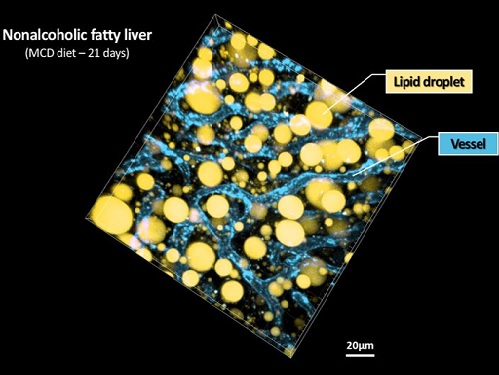 비알콜성 지방간 진행 영상화 기술 개발
우리 대학 의과학대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 비알콜성 지방간에서 간세포 내 *지방구 형성과 미세혈관계를 동시에 고해상도의 영상으로 촬영하는 데 성공했다고 14일 밝혔다.
☞ 지방구(Lipid droplet): 지방 방울이라고도 하며, 간세포의 세포질에 구 형태로 축적된 지방을 뜻한다.
김 교수 연구팀은 이에 앞서 살아있는 비알콜성 지방간 동물모델에서 질환이 진행될수록 간세포 내의 지방구가 축적되며 크기가 증가하는 과정에서 개개의 지방구를 3차원으로 정밀하게 분석할 수 있는 생체현미경 기술을 개발, 이번 연구에 활용했다.
비알콜성 지방간은 서구화된 식습관 및 비만율 증가로 국내에서 급속히 증가하고 있는데 단순 지방간부터 만성 지방간염 및 간경변증(간경화)에 이르는 넓은 범위의 간 질환을 포함한다. 정상인에게서도 최대 24%, 비만인에서는 최대 74%까지 높은 유병률이 보고되고 있어 심각한 간 질환으로 진행되지 않도록 적극적인 관리가 요구된다.
그동안 비알콜성 지방간 질환 연구들은 대부분이 절제된 간 조직을 사용한 조직병리학적 분석을 통해 이뤄졌다. 하지만 이 같은 방식으로는 질환이 장기간에 걸쳐 진행되는 동안 간 내부의 간세포와 주변 미세환경에서 일어나는 다양한 분자세포 수준의 변화를 3차원으로 정밀하게 분석하고 그 원리를 밝히는 것이 어려웠다. 글로벌 차원의 집중적인 연구개발 투자에도 불구하고 비알콜성 지방간 질환의 새로운 치료제의 개발이 지연되고 주된 이유다.
김필한 교수 연구팀은 독자적으로 개발한 초고속 레이저 공초점·이광자 생체현미경을 사용해 살아있는 비알콜성 지방간 질환 동물모델에서 질환 진행에 따른 간세포 내 지방구의 형성 및 축적과 주변 미세 간 혈관계를 동시에 고해상도를 지닌 3차원 영상으로 촬영하는 데 성공했다.
연구팀이 개발한 생체현미경 시스템은 시속 380Km 이상의 초고속으로 회전하는 다각 거울을 이용해 살아있는 생체 내부 간 조직의 움직임을 실시간으로 추적하고 보정이 가능해 크기가 마이크로미터(μm·100만분의 1미터) 이하인 극히 작은 지방구까지 고해상도로 영상화가 가능하다.
연구팀은 또 비알콜성 간 질환에서 질환 진행으로 간세포 내 지방구의 축적률이 증가하고 개개의 지방구 크기가 증가하는 현상을 영상화하는 데 성공했다. 이와 함께 지방구의 크기 증가가 간세포 핵의 위치변화를 일으키고 결국 간세포 모양의 변화를 일으키는 현상을 고해상도 영상화를 통해 확인했다.
김 연구팀이 독자적으로 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 생체 내부 간의 미세환경을 이루는 다양한 구성성분(세포, 혈관, 지질, 콜라겐 외 생체분자)들을 동시에 실시간으로 영상촬영이 가능해 비알콜성 지방간 질환을 비롯한 다양한 간 질환 연구와 치료제 개발과정에 다양하게 활용될 것으로 기대된다.
특히 이 3차원 생체현미경 기술은 우리 대학 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올 인원 생체현미경 모델명인 'IVM-CM'과 'IVM-MS'로 2019년 10월부터 출시되고 있는데 기초 의·생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장의 핵심 장비로 벌써부터 주목받고 있다.
※ MCD diet는 지방간을 유도하기 위한 특수 사료를 의미하며 생쥐에게 섭취시키면 빠르게 지방간이 생긴다.
김 교수는 "비알콜성 지방간을 포함한 다양한 질환의 3차원 생체현미경을 이용한 실시간 고해상도 영상기술은 질환의 진행에 따른 세포 수준의 다양한 변화의 정밀한 관찰이 가능하다ˮ라며 "3차원 생체현미경은 미래 바이오헬스 산업에서 여러 인간 질환의 진단 및 치료제 개발에 획기적인 도움을 줄 것ˮ이라고 말했다.
나노과학기술대학원 문지은 박사과정 학생이 제1 저자로 참여한 연구팀 논문은 미국광학회가 발간하는 국제 학술지 '바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express)' 誌 8월 19일 字에 실리는 한편 편집장 선정(Editor's pick) 우수 논문으로 주목받았다. (논문명 : Intravital longitudinal imaging of hepatic lipid droplet accumulation in a murine model for nonalcoholic fatty liver disease)
한편 이번 연구는 과학기술정보통신부의 이공분야기초연구사업의 지원을 받아 이뤄졌다.
2020.09.14 조회수 30206
비알콜성 지방간 진행 영상화 기술 개발
우리 대학 의과학대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 비알콜성 지방간에서 간세포 내 *지방구 형성과 미세혈관계를 동시에 고해상도의 영상으로 촬영하는 데 성공했다고 14일 밝혔다.
☞ 지방구(Lipid droplet): 지방 방울이라고도 하며, 간세포의 세포질에 구 형태로 축적된 지방을 뜻한다.
김 교수 연구팀은 이에 앞서 살아있는 비알콜성 지방간 동물모델에서 질환이 진행될수록 간세포 내의 지방구가 축적되며 크기가 증가하는 과정에서 개개의 지방구를 3차원으로 정밀하게 분석할 수 있는 생체현미경 기술을 개발, 이번 연구에 활용했다.
비알콜성 지방간은 서구화된 식습관 및 비만율 증가로 국내에서 급속히 증가하고 있는데 단순 지방간부터 만성 지방간염 및 간경변증(간경화)에 이르는 넓은 범위의 간 질환을 포함한다. 정상인에게서도 최대 24%, 비만인에서는 최대 74%까지 높은 유병률이 보고되고 있어 심각한 간 질환으로 진행되지 않도록 적극적인 관리가 요구된다.
그동안 비알콜성 지방간 질환 연구들은 대부분이 절제된 간 조직을 사용한 조직병리학적 분석을 통해 이뤄졌다. 하지만 이 같은 방식으로는 질환이 장기간에 걸쳐 진행되는 동안 간 내부의 간세포와 주변 미세환경에서 일어나는 다양한 분자세포 수준의 변화를 3차원으로 정밀하게 분석하고 그 원리를 밝히는 것이 어려웠다. 글로벌 차원의 집중적인 연구개발 투자에도 불구하고 비알콜성 지방간 질환의 새로운 치료제의 개발이 지연되고 주된 이유다.
김필한 교수 연구팀은 독자적으로 개발한 초고속 레이저 공초점·이광자 생체현미경을 사용해 살아있는 비알콜성 지방간 질환 동물모델에서 질환 진행에 따른 간세포 내 지방구의 형성 및 축적과 주변 미세 간 혈관계를 동시에 고해상도를 지닌 3차원 영상으로 촬영하는 데 성공했다.
연구팀이 개발한 생체현미경 시스템은 시속 380Km 이상의 초고속으로 회전하는 다각 거울을 이용해 살아있는 생체 내부 간 조직의 움직임을 실시간으로 추적하고 보정이 가능해 크기가 마이크로미터(μm·100만분의 1미터) 이하인 극히 작은 지방구까지 고해상도로 영상화가 가능하다.
연구팀은 또 비알콜성 간 질환에서 질환 진행으로 간세포 내 지방구의 축적률이 증가하고 개개의 지방구 크기가 증가하는 현상을 영상화하는 데 성공했다. 이와 함께 지방구의 크기 증가가 간세포 핵의 위치변화를 일으키고 결국 간세포 모양의 변화를 일으키는 현상을 고해상도 영상화를 통해 확인했다.
김 연구팀이 독자적으로 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 생체 내부 간의 미세환경을 이루는 다양한 구성성분(세포, 혈관, 지질, 콜라겐 외 생체분자)들을 동시에 실시간으로 영상촬영이 가능해 비알콜성 지방간 질환을 비롯한 다양한 간 질환 연구와 치료제 개발과정에 다양하게 활용될 것으로 기대된다.
특히 이 3차원 생체현미경 기술은 우리 대학 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올 인원 생체현미경 모델명인 'IVM-CM'과 'IVM-MS'로 2019년 10월부터 출시되고 있는데 기초 의·생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장의 핵심 장비로 벌써부터 주목받고 있다.
※ MCD diet는 지방간을 유도하기 위한 특수 사료를 의미하며 생쥐에게 섭취시키면 빠르게 지방간이 생긴다.
김 교수는 "비알콜성 지방간을 포함한 다양한 질환의 3차원 생체현미경을 이용한 실시간 고해상도 영상기술은 질환의 진행에 따른 세포 수준의 다양한 변화의 정밀한 관찰이 가능하다ˮ라며 "3차원 생체현미경은 미래 바이오헬스 산업에서 여러 인간 질환의 진단 및 치료제 개발에 획기적인 도움을 줄 것ˮ이라고 말했다.
나노과학기술대학원 문지은 박사과정 학생이 제1 저자로 참여한 연구팀 논문은 미국광학회가 발간하는 국제 학술지 '바이오메디컬 옵틱스 익스프레스(Biomedical Optics Express)' 誌 8월 19일 字에 실리는 한편 편집장 선정(Editor's pick) 우수 논문으로 주목받았다. (논문명 : Intravital longitudinal imaging of hepatic lipid droplet accumulation in a murine model for nonalcoholic fatty liver disease)
한편 이번 연구는 과학기술정보통신부의 이공분야기초연구사업의 지원을 받아 이뤄졌다.
2020.09.14 조회수 30206 -
 김필한 교수, 패혈증 환자의 폐 손상 원인 밝혀
〈 김필한 교수 〉
우리 대학 의과학대학원/나노과학기술대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 패혈증 폐에서 모세혈관과 혈액 내 순환 세포를 고해상도 촬영하는 데 성공했다.
연구팀은 패혈증 폐의 모세혈관 내부에서 백혈구의 일종인 호중구(好中球, neutrophil)들이 서로 응집하며 혈액 미세순환의 저해를 유발하고, 나아가 피가 통하지 않는 사강(死腔, dead space)을 형성함을 규명했다.
연구팀은 이 현상이 패혈증 모델의 폐손상으로 이어지는 조직 저산소증 유발의 원인이 되며, 호중구 응집을 해소하면 미세순환이 개선되며 저산소증도 함께 호전됨을 증명했다.
박인원 박사(현 분당서울대학교병원 응급의학과)가 주도한 이번 연구결과는 의학 분야 국제 학술지 ‘유럽호흡기학회지(European Respiratory Journal)’에 3월 28일 자에 게재됐다.
폐는 호흡을 통해 생명 유지의 필수 작용인 산소와 이산화탄소 간 가스 교환을 하는 기관으로 이는 적혈구들이 순환하는 수많은 모세혈관으로 둘러싸인 폐포(肺胞)에서 이뤄진다.
폐포의 미세순환 관찰을 위해 연구자들이 지속적인 노력을 하고 있으나 호흡을 위해 항상 움직이는 폐 안의 모세혈관과 적혈구의 미세순환을 고해상도로 촬영하는 것은 매우 어려웠다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 폐의 호흡 상태를 보존하면서 움직임을 최소화할 수 있는 영상 챔버를 새롭게 제작했다. 이를 통해 패혈증 동물모델의 폐에서 모세혈관 내부의 적혈구 순환 촬영에 성공했다.
이 과정에서 패혈증 모델의 폐에서 적혈구들이 순환하지 않는 공간인 사강이 증가하며 이곳에서 저산소증이 유발되는 것을 발견했다. 이는 혈액 내부의 호중구들이 모세혈관과 세동맥 내부에서 서로 응집하며 갇히는 현상으로 인해 발생함을 밝혔다. 갇힌 호중구들은 미세순환 저해, 활성산소의 다량 생산 등 패혈증 모델의 폐 조직 손상을 유발하는 것도 확인했다.
연구팀은 추가 연구를 통해 폐혈관 내부의 응집한 호중구가 전신을 순환하는 호중구에 비해 세포 간 부착에 관여하는 Mac-1 수용체(CD11b/CD18)가 높게 발현함을 증명했다. 이어 Mac-1 저해제를 패혈증 모델에 사용하여 호중구 응집으로 저해된 미세순환을 개선하고 저산소증의 호전과 폐부종 감소를 증명했다.
연구팀이 독자 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 폐 안 세포들의 실시간 영상촬영이 가능해 패혈증을 포함한 여러 폐 질환의 연구에 다양하게 활용될 것으로 기대된다.
연구팀의 폐 미세순환 영상촬영 및 정밀 분석 기법은 향후 미세순환과 연관된 다양한 질환들의 연구뿐 아니라 새로운 진단기술 개발 및 치료제의 평가를 위한 원천기술로 활용될 것으로 보인다.
김 교수 연구팀의 3차원 생체현미경 기술은 KAIST 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올인원 생체현미경 모델 ‘IVM-CM’과 ‘IVM-C’로 출시됐으며 여러 인간 질환의 복잡한 발생 과정을 밝히기 위한 기초 의․생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장에 핵심 장비로 활용될 예정이다.
김 교수는 “패혈증으로 인한 급성 폐손상 모델에서 폐 미세순환의 저해가 호중구로 인하여 발생하며, 이를 제어하면 미세순환 개선을 통해 저산소증 및 폐부종을 해소할 수 있어 패혈증 환자를 치료하는 새로운 전략이 될 수 있음을 새롭게 밝혀냈다.”고 말했다.
이번 연구는 의과학대학원 졸업생 박인원 박사가 1저자로 참여했고 유한재단 보건장학회, 교육부 글로벌박사펠로우쉽사업, 과학기술정보통신부의 글로벌프론티어사업과 이공분야기초연구사업, 그리고 보건복지부의 질환극복기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 초고속 레이저주사 3차원 생체현미경 시스템
그림2. 생체 내 폐 이미징 기술 개념도 및 사진
2019.04.01 조회수 23399
김필한 교수, 패혈증 환자의 폐 손상 원인 밝혀
〈 김필한 교수 〉
우리 대학 의과학대학원/나노과학기술대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 패혈증 폐에서 모세혈관과 혈액 내 순환 세포를 고해상도 촬영하는 데 성공했다.
연구팀은 패혈증 폐의 모세혈관 내부에서 백혈구의 일종인 호중구(好中球, neutrophil)들이 서로 응집하며 혈액 미세순환의 저해를 유발하고, 나아가 피가 통하지 않는 사강(死腔, dead space)을 형성함을 규명했다.
연구팀은 이 현상이 패혈증 모델의 폐손상으로 이어지는 조직 저산소증 유발의 원인이 되며, 호중구 응집을 해소하면 미세순환이 개선되며 저산소증도 함께 호전됨을 증명했다.
박인원 박사(현 분당서울대학교병원 응급의학과)가 주도한 이번 연구결과는 의학 분야 국제 학술지 ‘유럽호흡기학회지(European Respiratory Journal)’에 3월 28일 자에 게재됐다.
폐는 호흡을 통해 생명 유지의 필수 작용인 산소와 이산화탄소 간 가스 교환을 하는 기관으로 이는 적혈구들이 순환하는 수많은 모세혈관으로 둘러싸인 폐포(肺胞)에서 이뤄진다.
폐포의 미세순환 관찰을 위해 연구자들이 지속적인 노력을 하고 있으나 호흡을 위해 항상 움직이는 폐 안의 모세혈관과 적혈구의 미세순환을 고해상도로 촬영하는 것은 매우 어려웠다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 폐의 호흡 상태를 보존하면서 움직임을 최소화할 수 있는 영상 챔버를 새롭게 제작했다. 이를 통해 패혈증 동물모델의 폐에서 모세혈관 내부의 적혈구 순환 촬영에 성공했다.
이 과정에서 패혈증 모델의 폐에서 적혈구들이 순환하지 않는 공간인 사강이 증가하며 이곳에서 저산소증이 유발되는 것을 발견했다. 이는 혈액 내부의 호중구들이 모세혈관과 세동맥 내부에서 서로 응집하며 갇히는 현상으로 인해 발생함을 밝혔다. 갇힌 호중구들은 미세순환 저해, 활성산소의 다량 생산 등 패혈증 모델의 폐 조직 손상을 유발하는 것도 확인했다.
연구팀은 추가 연구를 통해 폐혈관 내부의 응집한 호중구가 전신을 순환하는 호중구에 비해 세포 간 부착에 관여하는 Mac-1 수용체(CD11b/CD18)가 높게 발현함을 증명했다. 이어 Mac-1 저해제를 패혈증 모델에 사용하여 호중구 응집으로 저해된 미세순환을 개선하고 저산소증의 호전과 폐부종 감소를 증명했다.
연구팀이 독자 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 폐 안 세포들의 실시간 영상촬영이 가능해 패혈증을 포함한 여러 폐 질환의 연구에 다양하게 활용될 것으로 기대된다.
연구팀의 폐 미세순환 영상촬영 및 정밀 분석 기법은 향후 미세순환과 연관된 다양한 질환들의 연구뿐 아니라 새로운 진단기술 개발 및 치료제의 평가를 위한 원천기술로 활용될 것으로 보인다.
김 교수 연구팀의 3차원 생체현미경 기술은 KAIST 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올인원 생체현미경 모델 ‘IVM-CM’과 ‘IVM-C’로 출시됐으며 여러 인간 질환의 복잡한 발생 과정을 밝히기 위한 기초 의․생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장에 핵심 장비로 활용될 예정이다.
김 교수는 “패혈증으로 인한 급성 폐손상 모델에서 폐 미세순환의 저해가 호중구로 인하여 발생하며, 이를 제어하면 미세순환 개선을 통해 저산소증 및 폐부종을 해소할 수 있어 패혈증 환자를 치료하는 새로운 전략이 될 수 있음을 새롭게 밝혀냈다.”고 말했다.
이번 연구는 의과학대학원 졸업생 박인원 박사가 1저자로 참여했고 유한재단 보건장학회, 교육부 글로벌박사펠로우쉽사업, 과학기술정보통신부의 글로벌프론티어사업과 이공분야기초연구사업, 그리고 보건복지부의 질환극복기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 초고속 레이저주사 3차원 생체현미경 시스템
그림2. 생체 내 폐 이미징 기술 개념도 및 사진
2019.04.01 조회수 23399 -
 김필한 교수 교원창업기업, 3차원 생체현미경 IVM-CM 출시
〈김필한 교수, 아이빔테크놀로지 김인선 CEO〉
우리 대학 나노과학기술대학원/의과학대학원 김필한 교수 연구팀이 소속된 교원창업기업 아이빔테크놀로지(IVIM Technology, Inc)가 3차원 올인원 생체 현미경 ‘IVM-CM’과 ‘IVM-C’를 개발했다.
이는 김필한 교수 연구팀의 혁신적 생체현미경(IntraVital Microscopy, IVM) 원천기술을 토대로 개발한 것으로 미래 글로벌 바이오헬스 시장에 활용될 예정이다.
세계적 현미경 제조사들의 기술을 넘어 혁신적 원천 기술을 기반으로 개발된 ‘IVM-C’와 ‘IVM-CM’은 여러 인간 질환의 복잡한 발생 과정을 밝히기 위한 기초 의․생명 연구의 차세대 첨단 영상장비가 될 것으로 기대된다.
생체현미경은 바이오제약 분야에서 크게 주목받고 있다. 최근 바이오제약 산업은 단순 합성약물개발보다 생체의 미세 구성단위인 세포 수준에서 복합적으로 작용하는 면역치료제, 세포치료제, 유전자치료제, 항체치료제 등 새로운 개념의 바이오의약품 개발에 집중하고 있기 때문이다.
인체는 수없이 많은 세포들이 복잡한 상호작용을 통해 동작한다. 그러나 현재 신약개발 전임상 단계에서는 시험관 내(in-vitro)와 생체 외(ex-vivo) 실험처럼 상호작용이 일어나지 않는 방식의 연구가 주로 수행되고 있다.
이러한 실험 결과들로만 얻은 결과로 임상시험에 진입한다면 오류와 실패의 가능성이 높아진다. 따라서 신약개발을 위한 임상시험 전 마지막 단계에서 반드시 살아있는 동물에서의 생체 내(in-vivo) 실험으로 효능 분석이 진행돼야 한다.
생체현미경 기술은 바로 이 과정에서 살아있는 동물 내부의 목표로 하는 세포, 단백질과 주입된 물질의 움직임을 동시에 3차원 고해상도 영상으로 직접 관찰할 수 있어 시험 결과의 오류, 시간, 비용을 현저히 줄일 수 있다.
기존 현미경 기술을 살아있는 생체에 적용하려면 영상획득 과정 동안 생체를 유지하기 위한 여러 추가적인 장비가 필요하다. 또한 영상 속도와 해상도의 한계로 인해 생체 내부의 세포를 직접 관찰하기 어려웠다.
아이빔테크놀로지의 ‘IVM-C’와 ‘IVM-CM’모델은 최초의 올인원 3차원 생체현미경 제품으로 살아있는 생체 내부조직을 구성하는 세포들을 고해상도로 직접 관찰할 수 있다.
기존 MRI나 CT 등으로 불가능했던 신체의 다양한 장기 내부에서 움직이는 세포들을 하나하나 구별해 관찰하는 것이 가능하다. 이를 통해 다양한 질병이 몸속에서 발생하는 과정에 대해 자세한 세포단위 영상 정보를 제공할 수 있다.
특히 ‘IVM-C’와 ‘IVM-CM’모델은 독보적인 초고속 레이저스캐닝 기술을 이용해 기존 기술수준을 크게 뛰어넘는 고해상도와 정밀도로 살아있는 생체 내부의 다양한 세포 및 주변 미세 환경과 단백질 등의 분자를 동시에 영상화하는 것이 가능하다.
‘IVM-C’모델은 살아있는 생체 내부의 고해상도 공초점 영상을 총 4가지 색으로 동시에 획득할 수 있으며, ‘IVM-CM’모델은 공초점 영상과 더불어 고속펄스레이저를 이용한 다중광자 영상까지 획득할 수 있다.
최고기술책임자(CTO) 김필한 교수는 “‘IVM-C’와 ‘IVM-CM’은 세포치료제, 면역치료제, 신약 및 선도물질 효능 분석 시 다양한 세포들이 존재하는 생체 내 환경에서 단일 세포 단위의 정밀한 효능 분석이 가능한 유일한 장비로 생명 현상을 보다 정밀하게 종합 분석하기 위한 혁신적 원천 기술로 급성장할 글로벌 바이오헬스 시장을 개척할 수 있는 차세대 의료, 의약 기술 발전을 가속화할 핵심 기술이 될 것이다”고 말했다.
아이빔테크놀로지는 시장성과 성장 가능성을 높게 평가받아 창업 후 3개월 만인 작년 9월 30억 원의 투자 유치를 달성한 바 있다.
대표이사는 김인선 전 제넥신 경영지원본부장, 최고기술책임자는 김필한 교수, 영업 및 마케팅 총괄은 독일 광학 기업인 칼자이스에서 14년간 경험을 쌓은 박수진 이사가 맡고 있다.
또한 우리 대학 박사 출신들로 구성된 기술개발팀과 연구서비스팀이 차세대 후속 장비 개발과 글로벌 바이오헬스 시장 활성화를 위해 노력하고 있다.
김필한 교수 연구팀은 창업원 엔드-런(End-Run) 사업화도약과제에 참여했으며, 아이빔테크놀로지는 창업원의 지원을 받아 설립됐다.
□ 사진 설명
사진1. IVM-CM 장비사진
사진2. IVM-CM 생체영상결과 사진
사진3. IVM-CM 생체 내부 세포 추적 사진
2018.09.05 조회수 15418
김필한 교수 교원창업기업, 3차원 생체현미경 IVM-CM 출시
〈김필한 교수, 아이빔테크놀로지 김인선 CEO〉
우리 대학 나노과학기술대학원/의과학대학원 김필한 교수 연구팀이 소속된 교원창업기업 아이빔테크놀로지(IVIM Technology, Inc)가 3차원 올인원 생체 현미경 ‘IVM-CM’과 ‘IVM-C’를 개발했다.
이는 김필한 교수 연구팀의 혁신적 생체현미경(IntraVital Microscopy, IVM) 원천기술을 토대로 개발한 것으로 미래 글로벌 바이오헬스 시장에 활용될 예정이다.
세계적 현미경 제조사들의 기술을 넘어 혁신적 원천 기술을 기반으로 개발된 ‘IVM-C’와 ‘IVM-CM’은 여러 인간 질환의 복잡한 발생 과정을 밝히기 위한 기초 의․생명 연구의 차세대 첨단 영상장비가 될 것으로 기대된다.
생체현미경은 바이오제약 분야에서 크게 주목받고 있다. 최근 바이오제약 산업은 단순 합성약물개발보다 생체의 미세 구성단위인 세포 수준에서 복합적으로 작용하는 면역치료제, 세포치료제, 유전자치료제, 항체치료제 등 새로운 개념의 바이오의약품 개발에 집중하고 있기 때문이다.
인체는 수없이 많은 세포들이 복잡한 상호작용을 통해 동작한다. 그러나 현재 신약개발 전임상 단계에서는 시험관 내(in-vitro)와 생체 외(ex-vivo) 실험처럼 상호작용이 일어나지 않는 방식의 연구가 주로 수행되고 있다.
이러한 실험 결과들로만 얻은 결과로 임상시험에 진입한다면 오류와 실패의 가능성이 높아진다. 따라서 신약개발을 위한 임상시험 전 마지막 단계에서 반드시 살아있는 동물에서의 생체 내(in-vivo) 실험으로 효능 분석이 진행돼야 한다.
생체현미경 기술은 바로 이 과정에서 살아있는 동물 내부의 목표로 하는 세포, 단백질과 주입된 물질의 움직임을 동시에 3차원 고해상도 영상으로 직접 관찰할 수 있어 시험 결과의 오류, 시간, 비용을 현저히 줄일 수 있다.
기존 현미경 기술을 살아있는 생체에 적용하려면 영상획득 과정 동안 생체를 유지하기 위한 여러 추가적인 장비가 필요하다. 또한 영상 속도와 해상도의 한계로 인해 생체 내부의 세포를 직접 관찰하기 어려웠다.
아이빔테크놀로지의 ‘IVM-C’와 ‘IVM-CM’모델은 최초의 올인원 3차원 생체현미경 제품으로 살아있는 생체 내부조직을 구성하는 세포들을 고해상도로 직접 관찰할 수 있다.
기존 MRI나 CT 등으로 불가능했던 신체의 다양한 장기 내부에서 움직이는 세포들을 하나하나 구별해 관찰하는 것이 가능하다. 이를 통해 다양한 질병이 몸속에서 발생하는 과정에 대해 자세한 세포단위 영상 정보를 제공할 수 있다.
특히 ‘IVM-C’와 ‘IVM-CM’모델은 독보적인 초고속 레이저스캐닝 기술을 이용해 기존 기술수준을 크게 뛰어넘는 고해상도와 정밀도로 살아있는 생체 내부의 다양한 세포 및 주변 미세 환경과 단백질 등의 분자를 동시에 영상화하는 것이 가능하다.
‘IVM-C’모델은 살아있는 생체 내부의 고해상도 공초점 영상을 총 4가지 색으로 동시에 획득할 수 있으며, ‘IVM-CM’모델은 공초점 영상과 더불어 고속펄스레이저를 이용한 다중광자 영상까지 획득할 수 있다.
최고기술책임자(CTO) 김필한 교수는 “‘IVM-C’와 ‘IVM-CM’은 세포치료제, 면역치료제, 신약 및 선도물질 효능 분석 시 다양한 세포들이 존재하는 생체 내 환경에서 단일 세포 단위의 정밀한 효능 분석이 가능한 유일한 장비로 생명 현상을 보다 정밀하게 종합 분석하기 위한 혁신적 원천 기술로 급성장할 글로벌 바이오헬스 시장을 개척할 수 있는 차세대 의료, 의약 기술 발전을 가속화할 핵심 기술이 될 것이다”고 말했다.
아이빔테크놀로지는 시장성과 성장 가능성을 높게 평가받아 창업 후 3개월 만인 작년 9월 30억 원의 투자 유치를 달성한 바 있다.
대표이사는 김인선 전 제넥신 경영지원본부장, 최고기술책임자는 김필한 교수, 영업 및 마케팅 총괄은 독일 광학 기업인 칼자이스에서 14년간 경험을 쌓은 박수진 이사가 맡고 있다.
또한 우리 대학 박사 출신들로 구성된 기술개발팀과 연구서비스팀이 차세대 후속 장비 개발과 글로벌 바이오헬스 시장 활성화를 위해 노력하고 있다.
김필한 교수 연구팀은 창업원 엔드-런(End-Run) 사업화도약과제에 참여했으며, 아이빔테크놀로지는 창업원의 지원을 받아 설립됐다.
□ 사진 설명
사진1. IVM-CM 장비사진
사진2. IVM-CM 생체영상결과 사진
사진3. IVM-CM 생체 내부 세포 추적 사진
2018.09.05 조회수 15418 -
 김필한 교수, 초고속 레이저 생체현미경 개발
〈 김 필 한 교수 〉
우리 대학 나노과학기술대학원 김필한 교수 연구팀이 개발한 초고속 생체현미경(IVM: IntraVital Microscopy)을 통해 미래 글로벌 바이오헬스 시장을 겨냥한 상용화에 나선다.
김 교수는 (재)의약바이오컨버젼스연구단, 서울대학교 김성훈 교수와의 공동 연구를 통해 개발한 최첨단 초고속 레이저스캐닝 3차원 생체현미경 기술을 토대로 아이빔테크놀로지(주)(IVIM Technology, Inc)를 창업했다.
이 생체현미경(IntraVital Microscopy : IVM)은 수많은 세포들 간 상호작용을 통해 나타나는 생명 현상을 탐구하고 여러 질환의 복잡한 발생 과정을 밝힘으로써 기초 의생명 연구의 차세대 첨단 영상장비가 될 것으로 기대된다.
연구팀의 기술은 살아있는 생체 내부조직을 구성하는 세포의 움직임을 직접 관찰할 수 있다. MRI나 CT 등 기존 생체영상 기술로는 불가능한 신체 다양한 장기 내부의 수많은 세포 하나하나를 구별하고 각 세포들의 움직임을 3차원으로 즉시 확인 가능하다.
이를 통해 다양한 질병이 몸속에서 발생하는 과정에 대해 자세한 세포단위 영상 정보를 제공할 수 있다.
특히 초고속 생체현미경 기술은 여러 색의 레이저 빔을 이용해 기존의 조직분석 기술로는 불가능했던 살아있는 생체 내부의 다양한 세포 및 주변 미세 환경과 단백질 등의 분자를 동시에 영상화할 수 있다.
이를 활용하면 생체 외부에서 수집한 데이터로 수립한 가정을 실제 살아있는 생체 내 환경에서 세포 단위로 검증하고 분석할 수 있다.
생체현미경은 바이오제약 분야에서도 주목받고 있다. 최근 바이오제약 산업은 단순 합성약물개발보다 생체의 미세 구성단위인 세포 수준에서 복합적으로 작용하는 면역치료제, 세포치료제, 유전자치료제, 항체치료제 등 새로운 개념의 바이오의약품 개발에 집중하고 있기 때문이다.
연구팀의 생체현미경은 동물실험에서 목표로 하는 세포, 단백질과 주입된 물질의 움직임을 동시에 3차원 동영상으로 관찰할 수 있다. 현재 (재)의약바이오컨버젼스연구단과 함께 차세대 신약개발을 위한 핵심기술로 발전시키기 위해 노력 중이다.
김 교수가 창업한 회사는 시장성과 성장가능성을 높게 평가받아 벤처기업으로서는 이례적으로 빠르게 창업 3개월 만에 LB인베스트먼트와 에이티넘인베스트먼트로부터 총 30억 원의 투자를 유치했다.
김 교수는 “이 기술은 다양한 생명 현상을 보다 정밀하게 종합 분석하기 위한 원천기술이다”며 “고령화 사회의 도래와 함께 급성장할 글로벌 바이오헬스 시장을 개척할 수 있는 차세대 의료, 의약 기술의 발전을 가속화할 핵심 기술이 될 것으로 확신한다”고 말했다.
김 교수 연구팀의 연구는 창업원의 엔드런(End-Run) 사업과 과학기술정보통신부가 추진하는 글로벌프론티어사업의 혁신형의약바이오컨버전스사업의 지원을 받아 수행됐다.
□ 사진 설명
사진1. 초고속 레이저 생체현미경 (IVM) 사진1
사진2. 초고속 레이저 생체현미경 (IVM) 사진2
사진3. 생체 내부 세포수준 변화의 IVM 영상 결과
사진4. 생체 내부 다양한 장기의 세포수준 IVM 영상 결과
2017.11.21 조회수 25821
김필한 교수, 초고속 레이저 생체현미경 개발
〈 김 필 한 교수 〉
우리 대학 나노과학기술대학원 김필한 교수 연구팀이 개발한 초고속 생체현미경(IVM: IntraVital Microscopy)을 통해 미래 글로벌 바이오헬스 시장을 겨냥한 상용화에 나선다.
김 교수는 (재)의약바이오컨버젼스연구단, 서울대학교 김성훈 교수와의 공동 연구를 통해 개발한 최첨단 초고속 레이저스캐닝 3차원 생체현미경 기술을 토대로 아이빔테크놀로지(주)(IVIM Technology, Inc)를 창업했다.
이 생체현미경(IntraVital Microscopy : IVM)은 수많은 세포들 간 상호작용을 통해 나타나는 생명 현상을 탐구하고 여러 질환의 복잡한 발생 과정을 밝힘으로써 기초 의생명 연구의 차세대 첨단 영상장비가 될 것으로 기대된다.
연구팀의 기술은 살아있는 생체 내부조직을 구성하는 세포의 움직임을 직접 관찰할 수 있다. MRI나 CT 등 기존 생체영상 기술로는 불가능한 신체 다양한 장기 내부의 수많은 세포 하나하나를 구별하고 각 세포들의 움직임을 3차원으로 즉시 확인 가능하다.
이를 통해 다양한 질병이 몸속에서 발생하는 과정에 대해 자세한 세포단위 영상 정보를 제공할 수 있다.
특히 초고속 생체현미경 기술은 여러 색의 레이저 빔을 이용해 기존의 조직분석 기술로는 불가능했던 살아있는 생체 내부의 다양한 세포 및 주변 미세 환경과 단백질 등의 분자를 동시에 영상화할 수 있다.
이를 활용하면 생체 외부에서 수집한 데이터로 수립한 가정을 실제 살아있는 생체 내 환경에서 세포 단위로 검증하고 분석할 수 있다.
생체현미경은 바이오제약 분야에서도 주목받고 있다. 최근 바이오제약 산업은 단순 합성약물개발보다 생체의 미세 구성단위인 세포 수준에서 복합적으로 작용하는 면역치료제, 세포치료제, 유전자치료제, 항체치료제 등 새로운 개념의 바이오의약품 개발에 집중하고 있기 때문이다.
연구팀의 생체현미경은 동물실험에서 목표로 하는 세포, 단백질과 주입된 물질의 움직임을 동시에 3차원 동영상으로 관찰할 수 있다. 현재 (재)의약바이오컨버젼스연구단과 함께 차세대 신약개발을 위한 핵심기술로 발전시키기 위해 노력 중이다.
김 교수가 창업한 회사는 시장성과 성장가능성을 높게 평가받아 벤처기업으로서는 이례적으로 빠르게 창업 3개월 만에 LB인베스트먼트와 에이티넘인베스트먼트로부터 총 30억 원의 투자를 유치했다.
김 교수는 “이 기술은 다양한 생명 현상을 보다 정밀하게 종합 분석하기 위한 원천기술이다”며 “고령화 사회의 도래와 함께 급성장할 글로벌 바이오헬스 시장을 개척할 수 있는 차세대 의료, 의약 기술의 발전을 가속화할 핵심 기술이 될 것으로 확신한다”고 말했다.
김 교수 연구팀의 연구는 창업원의 엔드런(End-Run) 사업과 과학기술정보통신부가 추진하는 글로벌프론티어사업의 혁신형의약바이오컨버전스사업의 지원을 받아 수행됐다.
□ 사진 설명
사진1. 초고속 레이저 생체현미경 (IVM) 사진1
사진2. 초고속 레이저 생체현미경 (IVM) 사진2
사진3. 생체 내부 세포수준 변화의 IVM 영상 결과
사진4. 생체 내부 다양한 장기의 세포수준 IVM 영상 결과
2017.11.21 조회수 25821 -
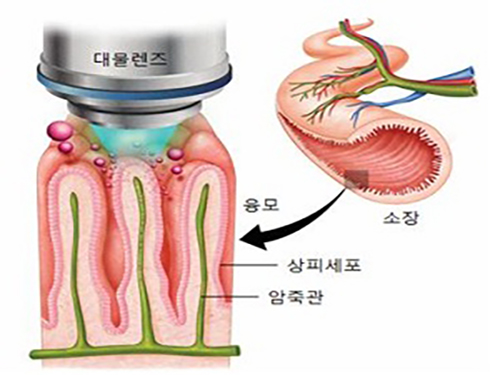 소장 내 지방 흡수과정의 비밀 밝혀
김 필 한 교수
우리 대학 나노과학기술대학원 김필한 교수와 의과학대학원 고규영 교수 공동 연구팀이 소장에서 지방이 흡수되는 과정의 고해상도 촬영에 성공했다.
이번 연구는 나노과학기술대학원 최기백 박사과정 학생, 의과학대학원 장전엽 박사, 박인태 박사과정 학생이 1저자로 참여했다.
이를 통해 소장의 융모로 흡수된 지방의 전달 통로인 암죽관의 수축현상을 최초로 발견했다.
이번 연구결과는 의생명과학 분야 국제 학술지인 ‘임상연구(The Journal of Clinical Investigation, Impact Factor 13.261)’ 10월 5일자 온라인판에 게재됐다. 또한 11월에는 이달의 주목할 만한 연구로 ‘JCI This month’에도 소개될 예정이다. (논문명 : Intravital imaging of intestinal lacteals unveils lipid drainage through contractility)
소장은 영양분을 흡수하는 기관이다. 소장의 관찰을 위해 많은 학자들이 노력했지만 소장은 항상 쉬지 않고 움직이기 때문에 고해상도 촬영에 한계가 있었다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 소장 의 상태를 보존하고 내벽을 고정할 수 있는 영상 챔버를 이용해 동물 모델의 소장 내벽에서 지방산이 흡수되는 과정을 촬영했다.
이 과정에서 지방의 흡수 통로인 암죽관이 일정 주기로 수축 및 이완하는 현상을 발견했다. 또한 암죽관의 수축 정도가 소장에서의 지방산 흡수 속도에 영향을 미치는 것을 발견했다.
연구팀은 이 암죽관의 움직임이 융모 내부에 다량 존재하는 민무늬근세포에 의해 발생하고, 이는 체내에 분포된 자율신경계를 통해 조절됨을 밝혔다.
이번 연구를 통해 개발된 최첨단 고해상도 생체영상기술로 소장 내 다양한 물질 흡수 과정의 실시간 모니터링이 가능해질 것으로 예상된다.
또한 이 기술은 신약개발 과정에서 지용성 약물이 소장 내 암죽관으로 흡수되게 해 간 독성을 최소화하는 새로운 약물전달 방법 확립에 기여할 것으로 기대된다.
김 교수는 “우리가 섭취하는 다량의 지용성 영양소가 체내로 흡수되는 과정에서 자율신경계로 조절되는 융모 내부의 암죽관 제어 메커니즘이 존재함을 새롭게 밝혀냈다”고 말했다.
이번 연구는 미래창조과학부의 글로벌프론티어사업 및 신기술융합형 성장동력사업의 지원을 받아 수행됐다.
그림 설명
그림1. 소장 내벽에 존재하는 융모에서 지방산이 흡수되는 과정을 광학현미경으로 영상화하는 과정 모식도
그림2. 소장 융모에서 지방산(적색)이 암죽관(녹색)을 통해 흡수되는 과정
그림3. 암죽관(녹색)의 반복적인 이완과 수축 운동. 0초, 2.7초에 이완. 1.6초, 4초에 암죽관의 수축
2015.10.14 조회수 20345
소장 내 지방 흡수과정의 비밀 밝혀
김 필 한 교수
우리 대학 나노과학기술대학원 김필한 교수와 의과학대학원 고규영 교수 공동 연구팀이 소장에서 지방이 흡수되는 과정의 고해상도 촬영에 성공했다.
이번 연구는 나노과학기술대학원 최기백 박사과정 학생, 의과학대학원 장전엽 박사, 박인태 박사과정 학생이 1저자로 참여했다.
이를 통해 소장의 융모로 흡수된 지방의 전달 통로인 암죽관의 수축현상을 최초로 발견했다.
이번 연구결과는 의생명과학 분야 국제 학술지인 ‘임상연구(The Journal of Clinical Investigation, Impact Factor 13.261)’ 10월 5일자 온라인판에 게재됐다. 또한 11월에는 이달의 주목할 만한 연구로 ‘JCI This month’에도 소개될 예정이다. (논문명 : Intravital imaging of intestinal lacteals unveils lipid drainage through contractility)
소장은 영양분을 흡수하는 기관이다. 소장의 관찰을 위해 많은 학자들이 노력했지만 소장은 항상 쉬지 않고 움직이기 때문에 고해상도 촬영에 한계가 있었다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 소장 의 상태를 보존하고 내벽을 고정할 수 있는 영상 챔버를 이용해 동물 모델의 소장 내벽에서 지방산이 흡수되는 과정을 촬영했다.
이 과정에서 지방의 흡수 통로인 암죽관이 일정 주기로 수축 및 이완하는 현상을 발견했다. 또한 암죽관의 수축 정도가 소장에서의 지방산 흡수 속도에 영향을 미치는 것을 발견했다.
연구팀은 이 암죽관의 움직임이 융모 내부에 다량 존재하는 민무늬근세포에 의해 발생하고, 이는 체내에 분포된 자율신경계를 통해 조절됨을 밝혔다.
이번 연구를 통해 개발된 최첨단 고해상도 생체영상기술로 소장 내 다양한 물질 흡수 과정의 실시간 모니터링이 가능해질 것으로 예상된다.
또한 이 기술은 신약개발 과정에서 지용성 약물이 소장 내 암죽관으로 흡수되게 해 간 독성을 최소화하는 새로운 약물전달 방법 확립에 기여할 것으로 기대된다.
김 교수는 “우리가 섭취하는 다량의 지용성 영양소가 체내로 흡수되는 과정에서 자율신경계로 조절되는 융모 내부의 암죽관 제어 메커니즘이 존재함을 새롭게 밝혀냈다”고 말했다.
이번 연구는 미래창조과학부의 글로벌프론티어사업 및 신기술융합형 성장동력사업의 지원을 받아 수행됐다.
그림 설명
그림1. 소장 내벽에 존재하는 융모에서 지방산이 흡수되는 과정을 광학현미경으로 영상화하는 과정 모식도
그림2. 소장 융모에서 지방산(적색)이 암죽관(녹색)을 통해 흡수되는 과정
그림3. 암죽관(녹색)의 반복적인 이완과 수축 운동. 0초, 2.7초에 이완. 1.6초, 4초에 암죽관의 수축
2015.10.14 조회수 20345 -
 테라헤르츠파 생체 부작용 첫 발견
인체에 무해하면서도 X선보다 활용분야가 다양해 꿈의 전자파로 불리는 ‘테라헤르츠파’의 생체 부작용이 세계 최초로 밝혀졌다.
우리 학교 나노과학기술대학원 김필한 교수와 한국원자력연구원 정영욱 박사 공동연구팀은 테라헤르츠파가 동물의 피부조직에서 염증반응을 일으키는 현상을 관찰했다.
연구결과는 광학 분야의 세계적 학술지인 ‘옵틱스 익스프레스(Optics Express)’ 온라인 판(5월 19일자)에 게재됐다.
테라헤르츠파는 0.1THz~10THz(테라헤르츠, 1조헤르츠) 대역의 전자기파로 가시광선이나 적외선보다 파장이 길어 X선처럼 물체의 내부를 투과해 볼 수 있지만 에너지가 낮아 인체에 해를 입히지 않는다고 알려져 왔다.
보안검색, 차세대 무선통신, 의료영상기술 등 다양한 분야에 활용되고 있으나 생체에 어떤 영향을 미치는지에 대한 연구는 거의 이뤄지지 않았다.
또 기존에 수행된 테라헤르츠 전자파의 영향에 관한 연구는 주로 인위적으로 배양된 세포만을 대상으로 수행해 복잡하고 다양한 구조의 생명체 조직에 미치는 영향을 예측하는 것은 불가능했다.
한국원자력연구원 연구팀은 먼저 살아있는 생체에 적용할 수 있는 고출력 테라헤르츠 전자파 발생기를 개발했다. 통신 분야에서 사용되는 것보다 10배 많은 출력량으로 바이오센서 등에 상용화하기 위해서는 지금보다 출력을 대폭 늘려야하기 때문이다.
이와 함께 KAIST 연구팀은 살아있는 생체조직 내부의 세포를 구분할 수 있는 고해상도의 3차원 영상 초고속 레이저 현미경을 개발했다.
공동연구팀은 고출력 테라헤르츠파를 유전자조작 생쥐의 피부에 30분간 조사한 결과 6시간 후 피부조직에서 염증세포의 수가 기존보다 6배 이상 증가한 것을 발견했다.
인체에 손상을 주지 않고 상피암 등 피부표면에 발생하는 질병을 효과적으로 확인할 수 있을 것으로 기대를 모으고 있는 ‘테라헤르츠파’의 생체 부작용이 세계에서 처음으로 보고된 것이다.
김필한 교수는 “이번 연구 결과는 현재 다양한 분야에 활용되고 있는 테라헤르츠 전자파를 어떻게 하면 더 안전하게 사용할 수 있는가에 대한 기준을 제시한 것”이라며 “향후 일상생활에서 쓰이는 다른 종류의 전자파의 생체 영향에 대한 정확한 이해 및 분석에도 활용될 것”이라고 말했다.
한편, 이번 연구는 미래창조과학부의 재원으로 한국연구재단을 통해 세계수준의 연구센터(WCI) 및 선도연구센터(ERC) 사업의 지원을 받아 수행됐다.
그림 1. KAIST의 초고속 레이저스캐닝 공초점현미경 사진
그림 2. 한국원자력 연구원의 테라헤르츠 전자파 발생장치
그림 3. 살아있는 동물의 피부조직 세포수준 영상 획득 사진
그림 4. 테라헤르츠 전자파에 의해 유도된 염증세포 영상화 사진
2014.06.18 조회수 19959
테라헤르츠파 생체 부작용 첫 발견
인체에 무해하면서도 X선보다 활용분야가 다양해 꿈의 전자파로 불리는 ‘테라헤르츠파’의 생체 부작용이 세계 최초로 밝혀졌다.
우리 학교 나노과학기술대학원 김필한 교수와 한국원자력연구원 정영욱 박사 공동연구팀은 테라헤르츠파가 동물의 피부조직에서 염증반응을 일으키는 현상을 관찰했다.
연구결과는 광학 분야의 세계적 학술지인 ‘옵틱스 익스프레스(Optics Express)’ 온라인 판(5월 19일자)에 게재됐다.
테라헤르츠파는 0.1THz~10THz(테라헤르츠, 1조헤르츠) 대역의 전자기파로 가시광선이나 적외선보다 파장이 길어 X선처럼 물체의 내부를 투과해 볼 수 있지만 에너지가 낮아 인체에 해를 입히지 않는다고 알려져 왔다.
보안검색, 차세대 무선통신, 의료영상기술 등 다양한 분야에 활용되고 있으나 생체에 어떤 영향을 미치는지에 대한 연구는 거의 이뤄지지 않았다.
또 기존에 수행된 테라헤르츠 전자파의 영향에 관한 연구는 주로 인위적으로 배양된 세포만을 대상으로 수행해 복잡하고 다양한 구조의 생명체 조직에 미치는 영향을 예측하는 것은 불가능했다.
한국원자력연구원 연구팀은 먼저 살아있는 생체에 적용할 수 있는 고출력 테라헤르츠 전자파 발생기를 개발했다. 통신 분야에서 사용되는 것보다 10배 많은 출력량으로 바이오센서 등에 상용화하기 위해서는 지금보다 출력을 대폭 늘려야하기 때문이다.
이와 함께 KAIST 연구팀은 살아있는 생체조직 내부의 세포를 구분할 수 있는 고해상도의 3차원 영상 초고속 레이저 현미경을 개발했다.
공동연구팀은 고출력 테라헤르츠파를 유전자조작 생쥐의 피부에 30분간 조사한 결과 6시간 후 피부조직에서 염증세포의 수가 기존보다 6배 이상 증가한 것을 발견했다.
인체에 손상을 주지 않고 상피암 등 피부표면에 발생하는 질병을 효과적으로 확인할 수 있을 것으로 기대를 모으고 있는 ‘테라헤르츠파’의 생체 부작용이 세계에서 처음으로 보고된 것이다.
김필한 교수는 “이번 연구 결과는 현재 다양한 분야에 활용되고 있는 테라헤르츠 전자파를 어떻게 하면 더 안전하게 사용할 수 있는가에 대한 기준을 제시한 것”이라며 “향후 일상생활에서 쓰이는 다른 종류의 전자파의 생체 영향에 대한 정확한 이해 및 분석에도 활용될 것”이라고 말했다.
한편, 이번 연구는 미래창조과학부의 재원으로 한국연구재단을 통해 세계수준의 연구센터(WCI) 및 선도연구센터(ERC) 사업의 지원을 받아 수행됐다.
그림 1. KAIST의 초고속 레이저스캐닝 공초점현미경 사진
그림 2. 한국원자력 연구원의 테라헤르츠 전자파 발생장치
그림 3. 살아있는 동물의 피부조직 세포수준 영상 획득 사진
그림 4. 테라헤르츠 전자파에 의해 유도된 염증세포 영상화 사진
2014.06.18 조회수 19959