-
 숨 쉬는 헤어셀 구조의 피부부착형 맥파 센서 개발
우리 대학 바이오및뇌공학과 조영호 교수 연구팀이 피부에서 발생하는 땀을 실시간으로 투과시키며 피부와의 접촉면적을 획기적으로 개선한 다공성 헤어셀 구조의 맥파※ 센서를 개발했다고 17일 밝혔다.
※ 맥파: 심장이 박동할 때 발생하는 파동을 말한다.
헤어셀 구조란 피부의 섬모와 같이 다공성 표면 위에 여러 개의 섬모가 형성돼있는 구조를 말한다.
새로 개발된 다공성 헤어셀 구조의 맥파 센서 기술은 맥파 외 피부 온도, 피부 전도도 등 타 생체신호 센서들의 결합을 통해, 인간의 정신건강 상태를 상시 장기적으로 판별하는 연구에 적용하고 있다.
바이오및뇌공학과 석민호 박사과정의 주도로 개발한 이번 연구는 국제 학술지 `나노스케일 어드벤시스(Nanoscale Advances)' 7월 27일 字 온라인판에 게재됐다. 논문명: A Porous PDMS Pulsewave Sensor with Haircell Structures for Water Vapor Transmission Rate and Signal-to-Noise Ratio Enhancement)
기존 폴리머 기반 맥파 센서는 땀 투과도가 피부의 하루 평균 땀 발생량 (432g/m2) 보다 낮아 장기간 부착 시 접촉성 피부염, 가려움 등의 피부 문제를 일으키는 단점이 있으며, 피부에 안정적으로 접촉할 수 있는 면적이 낮아 맥파 신호의 정확도가 떨어지는 문제를 지닌다.
조영호 교수 연구팀은 문제 해결을 위해, 폴리디메틸실록산(PDMS) 고분자 내에 구연산을 결정화 후 에탄올로 녹여 작고 균일한 공극을 형성함으로써 맥파 센서의 땀 투과도를 높였으며, 이러한 다공성 고분자 표면에 헤어셀 구조를 형성해 피부와의 접촉면적을 획기적으로 넓혀 맥파 센서의 측정 정확도를 개선한 다공성 헤어셀 구조의 맥파 센서를 제작했다.
이번 다공성 헤어셀 구조의 맥파 센서의 땀 투과도는 하루 486g/m2을 보여 피부의 하루 평균 땀 발생량보다 많고, 기존 기술 대비 72% 증가함을 보였다. 또한 피부에 장기간 부착 시에도 피부 트러블이 발생하지 않음을 7일간의 연속 부착 실험을 통해 입증했다. 측정 정확도(≈신호대잡음비※)는 22.89를 보여, 기존 기술 대비 측정 정확도를 약 9배 높였다.
※ 신호대잡음비: 잡음의 크기 대비 맥파 신호의 크기 정도를 말한다.
조영호 교수는 "이번 연구를 통해 피부 트러블 없이 인간의 건강 상태를 상시 모니터링할 수 있는 웨어러블 센서를 개발했고 인공피부로서의 상시 사용성 역시 확립했다ˮ고 말했다.
한편, 이번 연구는 알키미스트 프로젝트 사업의 지원을 통해 수행됐다.
숨 쉬는 헤어셀 구조의 피부부착형 맥파 센서 개발
우리 대학 바이오및뇌공학과 조영호 교수 연구팀이 피부에서 발생하는 땀을 실시간으로 투과시키며 피부와의 접촉면적을 획기적으로 개선한 다공성 헤어셀 구조의 맥파※ 센서를 개발했다고 17일 밝혔다.
※ 맥파: 심장이 박동할 때 발생하는 파동을 말한다.
헤어셀 구조란 피부의 섬모와 같이 다공성 표면 위에 여러 개의 섬모가 형성돼있는 구조를 말한다.
새로 개발된 다공성 헤어셀 구조의 맥파 센서 기술은 맥파 외 피부 온도, 피부 전도도 등 타 생체신호 센서들의 결합을 통해, 인간의 정신건강 상태를 상시 장기적으로 판별하는 연구에 적용하고 있다.
바이오및뇌공학과 석민호 박사과정의 주도로 개발한 이번 연구는 국제 학술지 `나노스케일 어드벤시스(Nanoscale Advances)' 7월 27일 字 온라인판에 게재됐다. 논문명: A Porous PDMS Pulsewave Sensor with Haircell Structures for Water Vapor Transmission Rate and Signal-to-Noise Ratio Enhancement)
기존 폴리머 기반 맥파 센서는 땀 투과도가 피부의 하루 평균 땀 발생량 (432g/m2) 보다 낮아 장기간 부착 시 접촉성 피부염, 가려움 등의 피부 문제를 일으키는 단점이 있으며, 피부에 안정적으로 접촉할 수 있는 면적이 낮아 맥파 신호의 정확도가 떨어지는 문제를 지닌다.
조영호 교수 연구팀은 문제 해결을 위해, 폴리디메틸실록산(PDMS) 고분자 내에 구연산을 결정화 후 에탄올로 녹여 작고 균일한 공극을 형성함으로써 맥파 센서의 땀 투과도를 높였으며, 이러한 다공성 고분자 표면에 헤어셀 구조를 형성해 피부와의 접촉면적을 획기적으로 넓혀 맥파 센서의 측정 정확도를 개선한 다공성 헤어셀 구조의 맥파 센서를 제작했다.
이번 다공성 헤어셀 구조의 맥파 센서의 땀 투과도는 하루 486g/m2을 보여 피부의 하루 평균 땀 발생량보다 많고, 기존 기술 대비 72% 증가함을 보였다. 또한 피부에 장기간 부착 시에도 피부 트러블이 발생하지 않음을 7일간의 연속 부착 실험을 통해 입증했다. 측정 정확도(≈신호대잡음비※)는 22.89를 보여, 기존 기술 대비 측정 정확도를 약 9배 높였다.
※ 신호대잡음비: 잡음의 크기 대비 맥파 신호의 크기 정도를 말한다.
조영호 교수는 "이번 연구를 통해 피부 트러블 없이 인간의 건강 상태를 상시 모니터링할 수 있는 웨어러블 센서를 개발했고 인공피부로서의 상시 사용성 역시 확립했다ˮ고 말했다.
한편, 이번 연구는 알키미스트 프로젝트 사업의 지원을 통해 수행됐다.
2021.08.18
조회수 9716
-
 효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2021.01.06
조회수 56245
-
 육종민 교수팀, 살아있는 세포의 전자현미경 관찰 성공
우리 대학 신소재공학과 육종민 교수 연구팀이 경북대학교(총장 김상동) ITA 융합대학원 한영기 교수 연구팀과 공동연구를 통해 살아 있는 세포를 전자현미경을 통해 실시간으로 관찰하는 데 성공했다고 29일 밝혔다.
이번 연구를 통해 살아 있는 다양한 세포의 실시간 분자 단위 관찰이 가능해져, 그동안 관찰하지 못했던 살아 있는 세포의 전이·감염에 관한 전 과정을 규명할 수 있게 돼 신약 개발 등을 더욱 촉진할 수 있을 것으로 기대된다.
신소재공학과 구건모 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `나노 레터스(Nano Letters)' 5월 5일 字 온라인판에 게재됐으며 6월 호 표지논문으로 선정됐다. (논문명: Live-Cell Electron Microscopy Using Graphene Veils)
전 세계적으로 대유행하고 있는 코로나바이러스감염증(COVID-19) 등은 수십~수백 나노미터(nm, 1 나노미터는 100만 분의 1밀리미터) 크기의 바이러스로 인해 일어나는 질병이다. 바이러스의 전이·감염 과정을 분석하고 이에 대처하는 신약 개발을 위해서는 바이러스의 미시적인 행동을 실시간으로 관찰하는 것이 매우 중요하다.
수십~수백 나노미터 크기의 바이러스 등을 비롯해 세포와 세포를 이루는 기관들은 가시광선을 이용하는 일반 광학현미경으로는 관찰이 어려워 해상력이 매우 높은 전자선을 이용하는 전자현미경 기술을 이용한다.
그렇지만 전자현미경 기술은 효율적인 작동을 위해 매우 강력한 진공상태가 필요하며 또 가시광선보다 수천 배 이상 높은 에너지를 가지는 전자를 이용하기 때문에 관찰 시 세포의 구조적인 손상이 불가피하다. 따라서 현재로서는 2017년 노벨화학상을 수상한 기술인 극저온 전자현미경을 통해 고정 작업 및 안정화 작업을 거친 표본만 관찰이 가능하다.
최근 학계에서는 사멸해 고정된 것이 아닌 온전한 상태의 살아 있는 세포등 다양한 생체물질을 전자현미경을 이용해 분자 단위로 관찰 가능한지에 대한 논쟁이 전개되고 있다. 육 교수 연구팀은 지난 2012년 개발한 그래핀 액상 셀 전자현미경 기술을 응용해 전자현미경으로도 살아있는 대장균 세포를 관찰하는데 성공했고, 이를 재배양시킴으로써 전자와 진공에 노출됐음에도 불구하고 대장균 세포가 생존한다는 사실을 밝혀냈다.
육 교수 연구팀이 이번 연구에서 활용한 그래핀은 층상 구조인 흑연에서 분리하는 등의 방법으로 얻어내는 약 0.2 나노미터(nm) 두께의 원자 막이다. 여러 분야에서 차세대 소재로 주목받고 있는 그래핀은 강철보다 200배 강한 강도와 높은 전기 전도성을 가지며, 물질을 투과시키지 않는 성질을 가진다. 육 교수 연구팀은 이러한 그래핀 성질을 이용, 세포 등을 액체와 함께 감싸주면, 고진공의 전자현미경 내부에서 탈수에 의한 세포의 구조변화를 막아줄 수 있음을 밝혀냈다. 뿐만 아니라, 그래핀이 전자빔에 의해 공격성이 높아진 활성 산소들을 분해하는 효과도 지니고 있어 그래핀으로 덮어주지 않은 세포보다 100배 강한 전자에 노출되더라도 세포가 활성을 잃지 않는다는 결과를 확인했다.
육 교수는 "이번 연구 결과는 세포보다 더 작은 단백질이나 DNA의 실시간 전자현미경 관찰로까지 확대될 수 있어, 앞으로 다양한 생명 현상의 기작을 근본적으로 밝힐 수 있을 것이라 기대한다ˮ고 밝혔다.
한편, 이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
육종민 교수팀, 살아있는 세포의 전자현미경 관찰 성공
우리 대학 신소재공학과 육종민 교수 연구팀이 경북대학교(총장 김상동) ITA 융합대학원 한영기 교수 연구팀과 공동연구를 통해 살아 있는 세포를 전자현미경을 통해 실시간으로 관찰하는 데 성공했다고 29일 밝혔다.
이번 연구를 통해 살아 있는 다양한 세포의 실시간 분자 단위 관찰이 가능해져, 그동안 관찰하지 못했던 살아 있는 세포의 전이·감염에 관한 전 과정을 규명할 수 있게 돼 신약 개발 등을 더욱 촉진할 수 있을 것으로 기대된다.
신소재공학과 구건모 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `나노 레터스(Nano Letters)' 5월 5일 字 온라인판에 게재됐으며 6월 호 표지논문으로 선정됐다. (논문명: Live-Cell Electron Microscopy Using Graphene Veils)
전 세계적으로 대유행하고 있는 코로나바이러스감염증(COVID-19) 등은 수십~수백 나노미터(nm, 1 나노미터는 100만 분의 1밀리미터) 크기의 바이러스로 인해 일어나는 질병이다. 바이러스의 전이·감염 과정을 분석하고 이에 대처하는 신약 개발을 위해서는 바이러스의 미시적인 행동을 실시간으로 관찰하는 것이 매우 중요하다.
수십~수백 나노미터 크기의 바이러스 등을 비롯해 세포와 세포를 이루는 기관들은 가시광선을 이용하는 일반 광학현미경으로는 관찰이 어려워 해상력이 매우 높은 전자선을 이용하는 전자현미경 기술을 이용한다.
그렇지만 전자현미경 기술은 효율적인 작동을 위해 매우 강력한 진공상태가 필요하며 또 가시광선보다 수천 배 이상 높은 에너지를 가지는 전자를 이용하기 때문에 관찰 시 세포의 구조적인 손상이 불가피하다. 따라서 현재로서는 2017년 노벨화학상을 수상한 기술인 극저온 전자현미경을 통해 고정 작업 및 안정화 작업을 거친 표본만 관찰이 가능하다.
최근 학계에서는 사멸해 고정된 것이 아닌 온전한 상태의 살아 있는 세포등 다양한 생체물질을 전자현미경을 이용해 분자 단위로 관찰 가능한지에 대한 논쟁이 전개되고 있다. 육 교수 연구팀은 지난 2012년 개발한 그래핀 액상 셀 전자현미경 기술을 응용해 전자현미경으로도 살아있는 대장균 세포를 관찰하는데 성공했고, 이를 재배양시킴으로써 전자와 진공에 노출됐음에도 불구하고 대장균 세포가 생존한다는 사실을 밝혀냈다.
육 교수 연구팀이 이번 연구에서 활용한 그래핀은 층상 구조인 흑연에서 분리하는 등의 방법으로 얻어내는 약 0.2 나노미터(nm) 두께의 원자 막이다. 여러 분야에서 차세대 소재로 주목받고 있는 그래핀은 강철보다 200배 강한 강도와 높은 전기 전도성을 가지며, 물질을 투과시키지 않는 성질을 가진다. 육 교수 연구팀은 이러한 그래핀 성질을 이용, 세포 등을 액체와 함께 감싸주면, 고진공의 전자현미경 내부에서 탈수에 의한 세포의 구조변화를 막아줄 수 있음을 밝혀냈다. 뿐만 아니라, 그래핀이 전자빔에 의해 공격성이 높아진 활성 산소들을 분해하는 효과도 지니고 있어 그래핀으로 덮어주지 않은 세포보다 100배 강한 전자에 노출되더라도 세포가 활성을 잃지 않는다는 결과를 확인했다.
육 교수는 "이번 연구 결과는 세포보다 더 작은 단백질이나 DNA의 실시간 전자현미경 관찰로까지 확대될 수 있어, 앞으로 다양한 생명 현상의 기작을 근본적으로 밝힐 수 있을 것이라 기대한다ˮ고 밝혔다.
한편, 이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
2020.06.29
조회수 22131
-
 포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2020.03.11
조회수 16128
-
 빛으로 RNA 이동과 단백질 합성 조절한다
빛으로 세포 내 특정 RNA 이동과 단백질 합성을 조절할 수 있는 기술이 개발됐다. 생명과학과 허원도 교수 연구팀이 빛을 이용해 유전정보를 전달하는 전령RNA와 단백질을 생성하는 리보솜의 결합을 제어해 단백질 합성을 조절하는데 성공했다.
이번 연구성과는 네이처 셀 바이올로지(Nature Cell Biology, IF 17.728)에 2월 18일 오전 1시(한국시간)자 온라인 판에 실렸으며, Nature Reviews Genetics에 하이라이트 논문으로 소개됐다.
DNA의 유전정보는 RNA를 거쳐 단백질로 전달된다. 이때 중간에서 유전정보를 전달하는 RNA를 ‘전령RNA’라고 한다. 단백질 생성공장인 리보솜이 전령RNA의 유전정보를 읽어 단백질을 합성한다. 단백질 합성에 있어 전령RNA는 DNA 유전정보의 중간 전달자, 리보솜은 생성공장, 단백질은 완성품인 셈이다.
이전에는 화학물질을 처리해 전령RNA를 조절하는 방법으로 모든 전령RNA를 한꺼번에 조절하기 때문에 특정 종류의 전령RNA만을 세밀하게 조절하기 어려웠다. 이번 연구에서는 살아있는 세포에 청색광을 비춰줌으로써 세포 내 특정 전령RNA 이동 및 단백질 합성을 시공간 특이적으로 조절하는 mRNA-LARIAT 광유전학 기술을 개발했다.
연구팀은 이전 연구로 개발한 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술과 RNA 이미징 기술을 융합해 mRNA-LARIAT 기술을 개발했다. mRNA-LARIAT 광유전학 기술을 이용하면 빛의 유무에 따라 라리아트 올가미에 전령RNA를 가두거나 분리하고, 이를 실시간으로 관찰하는 것이 가능하다.
연구팀은 헬라 세포에 청색광을 비춰주면 라리아트 올가미에 전령RNA가 가둬지면서 리보솜과 격리되고 단백질 합성이 감소함을 관찰했다. 이어 청색광을 차단하면 라리아트 올가미로부터 전령RNA가 빠져나오면서 리보솜과 단백질 합성을 다시 시작함을 확인했다. 이는 mRNA-LARIAT 광유전학 기술로 빛의 유무에 따라 매우 빠르고 가역적으로 단백질 합성을 조절할 수 있음을 의미한다.
대부분 단백질은 전령RNA와 리보솜에 의해 합성된 후, 각 단백질이 작용하는 위치로 이동한다. 하지만 전령RNA가 라리아트 올가미에 가둬지면 전령RNA가 향후 단백질이 작용하는 위치까지 이동이 멈추고 단백질 합성이 차단된다. 전령RNA는 단백질보다 비교적 작은 분자로, 세포 내 이동이 더 효율적이고 빠르다. 이처럼 mRNA-LARIAT 광유전학 기술로 전령RNA 이동 및 단백질 합성을 빛으로 조절하면 살아있는 세포에서의 RNA의 위치 및 합성되는 신생 단백질의 기능을 효율적으로 연구할 수 있게 되었다.
연구팀은 베타액틴(β-actin) 단백질 합성에 관여하는 전령RNA에 mRNA-LARIAT 기술을 적용했다. 베타액틴 단백질 합성에 관여하는 전령RNA에 청색광을 비추니 세포 골격 구성 및 이동 기능이 제대로 이뤄지지 않음을 관찰했다. 또한 베타액틴 단백질 합성 효율이 최대 90%까지 감소됨을 확인했다.
허원도 교수는 “mRNA-LARIAT 광유전학 기술을 활용하면 암세포, 신경세포 등 다양한 세포 내 전령RNA 이동 및 단백질 합성을 빛으로 조절할 수 있다”라며 “앞으로 암세포 전이, 신경질환 등 전령 RNA 관련 질병 연구에 응용 가능할 것이다”라고 말했다.
빛으로 RNA 이동과 단백질 합성 조절한다
빛으로 세포 내 특정 RNA 이동과 단백질 합성을 조절할 수 있는 기술이 개발됐다. 생명과학과 허원도 교수 연구팀이 빛을 이용해 유전정보를 전달하는 전령RNA와 단백질을 생성하는 리보솜의 결합을 제어해 단백질 합성을 조절하는데 성공했다.
이번 연구성과는 네이처 셀 바이올로지(Nature Cell Biology, IF 17.728)에 2월 18일 오전 1시(한국시간)자 온라인 판에 실렸으며, Nature Reviews Genetics에 하이라이트 논문으로 소개됐다.
DNA의 유전정보는 RNA를 거쳐 단백질로 전달된다. 이때 중간에서 유전정보를 전달하는 RNA를 ‘전령RNA’라고 한다. 단백질 생성공장인 리보솜이 전령RNA의 유전정보를 읽어 단백질을 합성한다. 단백질 합성에 있어 전령RNA는 DNA 유전정보의 중간 전달자, 리보솜은 생성공장, 단백질은 완성품인 셈이다.
이전에는 화학물질을 처리해 전령RNA를 조절하는 방법으로 모든 전령RNA를 한꺼번에 조절하기 때문에 특정 종류의 전령RNA만을 세밀하게 조절하기 어려웠다. 이번 연구에서는 살아있는 세포에 청색광을 비춰줌으로써 세포 내 특정 전령RNA 이동 및 단백질 합성을 시공간 특이적으로 조절하는 mRNA-LARIAT 광유전학 기술을 개발했다.
연구팀은 이전 연구로 개발한 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술과 RNA 이미징 기술을 융합해 mRNA-LARIAT 기술을 개발했다. mRNA-LARIAT 광유전학 기술을 이용하면 빛의 유무에 따라 라리아트 올가미에 전령RNA를 가두거나 분리하고, 이를 실시간으로 관찰하는 것이 가능하다.
연구팀은 헬라 세포에 청색광을 비춰주면 라리아트 올가미에 전령RNA가 가둬지면서 리보솜과 격리되고 단백질 합성이 감소함을 관찰했다. 이어 청색광을 차단하면 라리아트 올가미로부터 전령RNA가 빠져나오면서 리보솜과 단백질 합성을 다시 시작함을 확인했다. 이는 mRNA-LARIAT 광유전학 기술로 빛의 유무에 따라 매우 빠르고 가역적으로 단백질 합성을 조절할 수 있음을 의미한다.
대부분 단백질은 전령RNA와 리보솜에 의해 합성된 후, 각 단백질이 작용하는 위치로 이동한다. 하지만 전령RNA가 라리아트 올가미에 가둬지면 전령RNA가 향후 단백질이 작용하는 위치까지 이동이 멈추고 단백질 합성이 차단된다. 전령RNA는 단백질보다 비교적 작은 분자로, 세포 내 이동이 더 효율적이고 빠르다. 이처럼 mRNA-LARIAT 광유전학 기술로 전령RNA 이동 및 단백질 합성을 빛으로 조절하면 살아있는 세포에서의 RNA의 위치 및 합성되는 신생 단백질의 기능을 효율적으로 연구할 수 있게 되었다.
연구팀은 베타액틴(β-actin) 단백질 합성에 관여하는 전령RNA에 mRNA-LARIAT 기술을 적용했다. 베타액틴 단백질 합성에 관여하는 전령RNA에 청색광을 비추니 세포 골격 구성 및 이동 기능이 제대로 이뤄지지 않음을 관찰했다. 또한 베타액틴 단백질 합성 효율이 최대 90%까지 감소됨을 확인했다.
허원도 교수는 “mRNA-LARIAT 광유전학 기술을 활용하면 암세포, 신경세포 등 다양한 세포 내 전령RNA 이동 및 단백질 합성을 빛으로 조절할 수 있다”라며 “앞으로 암세포 전이, 신경질환 등 전령 RNA 관련 질병 연구에 응용 가능할 것이다”라고 말했다.
2020.02.21
조회수 20888
-
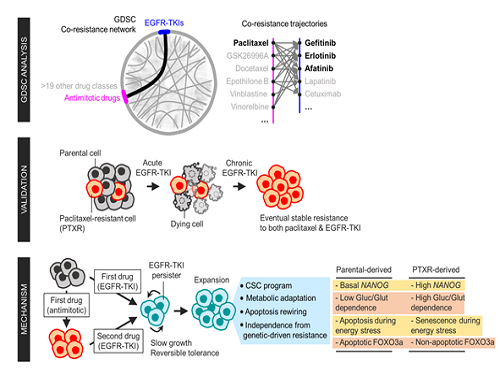 암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17
조회수 14947
-
 김상현 교수, 6만 ppi 초고해상도 디스플레이 제작기술 개발
〈 김상현 교수 연구팀(왼쪽 위 두번째 김상현 교수) 〉
우리 대학 전기및전자공학부 김상현 교수 연구팀이 반도체 공정 기술을 활용해 기존 마이크로 LED 디스플레이의 해상도 한계를 극복할 수 있는 6만 ppi(pixel per inch) 이상의 초고해상도 디스플레이 제작 가능 기술을 개발했다.
금대명 박사가 1 저자로 참여한 이번 연구는 국제학술지 ‘나노스케일(Nanoscale)’ 12월 28일자 표지 논문으로 게재됐다. (논문명 : Strategy toward the fabrication of ultrahigh-resolution micro-LED displays by bonding interface-engineered vertical stacking and surface passivation).
디스플레이의 기본 단위인 LED 중 무기물 LED는 유기물 LED보다 높은 효율, 높은 신뢰성, 고속성을 가져 마이크로 크기의 무기물 LED를 픽셀 화소로 사용하는 디스플레이(마이크로 LED 디스플레이)가 새로운 디스플레이 기술로 주목받고 있다.
무기물 LED를 화소로 사용하기 위해서는 적녹청(R/G/B) 픽셀을 밀집하게 배열해야 하지만, 현재 적색과 녹색, 청색을 낼 수 있는 LED의 물질이 달라 각각 제작한 LED를 디스플레이 기판에 전사해야 한다. 따라서 마이크로 LED 디스플레이에 관련한 대부분 연구가 이런 패키징 측면의 전사 기술 위주로 이루어지고 있다.
그러나 수백만 개의 픽셀을 마이크로미터 크기로 정렬해 세 번의 전사과정으로 화소를 형성하는 것은 전사 시 사용하는 LED 이송헤드의 크기 제한, 기계적 정확도 제한, 그리고 수율 저하 문제 등 해결해야 할 기술적 난제들이 많아 초고해상도 디스플레이에 적용하기에는 한계가 있다.
연구팀은 문제 해결을 위해 적녹청 LED 활성층을 3차원으로 적층한 후, 반도체 패터닝 공정을 이용해 초고해상도 마이크로 LED 디스플레이에 대응할 수 있는 소자 제작 방법을 제안함과 동시에 수직 적층시 문제가 될 수 있는 색의 간섭 문제, 초소형 픽셀에서의 효율 개선 방안을 제시했다.
연구팀은 3차원 적층을 위해 기판 접합 기술을 사용했고, 색 간섭을 최소화하기 위해 접합 면에 필터 특성을 갖는 절연막을 설계해 적색-청색 간섭 광을 97% 제거했다.
이러한 광학 설계를 포함한 접합 매개물을 통해 수직으로 픽셀을 결합해도 빛의 간섭 없이 순도 높은 픽셀을 구현할 수 있음을 확인했다. 연구팀은 수직 결합 후 반도체 패터닝 기술을 이용해 6만 ppi 이상의 해상도 달성 가능성을 증명했다.
또한, 초소형 LED 픽셀에서 문제가 될 수 있는 반도체 표면에서의 비 발광성 재결합 현상을 시간 분해 광발광 분석과 전산모사를 통해 체계적으로 조사해 초소형 LED의 효율을 개선할 수 있는 중요한 방향성을 제시했다.
김상현 교수는 “반도체 공정을 이용해 초고해상도의 픽셀 제작 가능성을 최초로 입증한 연구로, 반도체와 디스플레이 업계 협력의 중요성을 보여주는 연구 결과이다”라며 “후속 연구를 통해 초고해상도 미래 디스플레이의 기술 개발에 힘쓰겠다”라고 말했다.
이번 연구는 한국연구재단 이공분야 기초연구사업 기본연구, 기후변화대응기술개발사업 등의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 1um 크기를 가진 마이크로 단일 LED 가 실제로 배열된 모습을 보여주는 이미지, 1 um, 0.6 um 크기를 가진 LED를 광 여기 방법을 통해 적색 발광이 되는 모습을 보여주는 이미지(작은 사진). 이는 작아진 LED에서도 적색 발광특성이 잘 발현됨을 보여줌.
그림 2. 나노스케일 커버 이미지: 본 제작 방법의 사용 예시를 보여줌
김상현 교수, 6만 ppi 초고해상도 디스플레이 제작기술 개발
〈 김상현 교수 연구팀(왼쪽 위 두번째 김상현 교수) 〉
우리 대학 전기및전자공학부 김상현 교수 연구팀이 반도체 공정 기술을 활용해 기존 마이크로 LED 디스플레이의 해상도 한계를 극복할 수 있는 6만 ppi(pixel per inch) 이상의 초고해상도 디스플레이 제작 가능 기술을 개발했다.
금대명 박사가 1 저자로 참여한 이번 연구는 국제학술지 ‘나노스케일(Nanoscale)’ 12월 28일자 표지 논문으로 게재됐다. (논문명 : Strategy toward the fabrication of ultrahigh-resolution micro-LED displays by bonding interface-engineered vertical stacking and surface passivation).
디스플레이의 기본 단위인 LED 중 무기물 LED는 유기물 LED보다 높은 효율, 높은 신뢰성, 고속성을 가져 마이크로 크기의 무기물 LED를 픽셀 화소로 사용하는 디스플레이(마이크로 LED 디스플레이)가 새로운 디스플레이 기술로 주목받고 있다.
무기물 LED를 화소로 사용하기 위해서는 적녹청(R/G/B) 픽셀을 밀집하게 배열해야 하지만, 현재 적색과 녹색, 청색을 낼 수 있는 LED의 물질이 달라 각각 제작한 LED를 디스플레이 기판에 전사해야 한다. 따라서 마이크로 LED 디스플레이에 관련한 대부분 연구가 이런 패키징 측면의 전사 기술 위주로 이루어지고 있다.
그러나 수백만 개의 픽셀을 마이크로미터 크기로 정렬해 세 번의 전사과정으로 화소를 형성하는 것은 전사 시 사용하는 LED 이송헤드의 크기 제한, 기계적 정확도 제한, 그리고 수율 저하 문제 등 해결해야 할 기술적 난제들이 많아 초고해상도 디스플레이에 적용하기에는 한계가 있다.
연구팀은 문제 해결을 위해 적녹청 LED 활성층을 3차원으로 적층한 후, 반도체 패터닝 공정을 이용해 초고해상도 마이크로 LED 디스플레이에 대응할 수 있는 소자 제작 방법을 제안함과 동시에 수직 적층시 문제가 될 수 있는 색의 간섭 문제, 초소형 픽셀에서의 효율 개선 방안을 제시했다.
연구팀은 3차원 적층을 위해 기판 접합 기술을 사용했고, 색 간섭을 최소화하기 위해 접합 면에 필터 특성을 갖는 절연막을 설계해 적색-청색 간섭 광을 97% 제거했다.
이러한 광학 설계를 포함한 접합 매개물을 통해 수직으로 픽셀을 결합해도 빛의 간섭 없이 순도 높은 픽셀을 구현할 수 있음을 확인했다. 연구팀은 수직 결합 후 반도체 패터닝 기술을 이용해 6만 ppi 이상의 해상도 달성 가능성을 증명했다.
또한, 초소형 LED 픽셀에서 문제가 될 수 있는 반도체 표면에서의 비 발광성 재결합 현상을 시간 분해 광발광 분석과 전산모사를 통해 체계적으로 조사해 초소형 LED의 효율을 개선할 수 있는 중요한 방향성을 제시했다.
김상현 교수는 “반도체 공정을 이용해 초고해상도의 픽셀 제작 가능성을 최초로 입증한 연구로, 반도체와 디스플레이 업계 협력의 중요성을 보여주는 연구 결과이다”라며 “후속 연구를 통해 초고해상도 미래 디스플레이의 기술 개발에 힘쓰겠다”라고 말했다.
이번 연구는 한국연구재단 이공분야 기초연구사업 기본연구, 기후변화대응기술개발사업 등의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 1um 크기를 가진 마이크로 단일 LED 가 실제로 배열된 모습을 보여주는 이미지, 1 um, 0.6 um 크기를 가진 LED를 광 여기 방법을 통해 적색 발광이 되는 모습을 보여주는 이미지(작은 사진). 이는 작아진 LED에서도 적색 발광특성이 잘 발현됨을 보여줌.
그림 2. 나노스케일 커버 이미지: 본 제작 방법의 사용 예시를 보여줌
2020.01.06
조회수 21432
-
 김현우 교수, 알코올 화합물의 광학활성 분석기술 개발
〈 김현우 교수 〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명(NMR) 분광분석기를 통해 알코올 화합물의 광학활성을 간단히 분석할 수 있는 기술을 개발했다.
이 기술은 빠르고 간편한 분석 방법을 가지고 있어 다양한 알코올 화합물의 광학활성뿐만 아니라 비대칭 합성반응의 모니터링까지 폭넓게 응용 및 적용할 수 있을 것으로 기대된다.
장수민 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지 셀의 자매지 ‘아이 사이언스 (iScience)’ 9월 27일 자 온라인판에 게재됐다. (논문명 : A Gallium-Based Chiral Solvating Agent Enables the Use of 1H NMR Spectroscopy to Differentiate Chiral Alcohols)
광학이성질체는 오른손과 왼손의 관계처럼 서로 같은 물질로 이뤄져 있으나 거울상 대칭이 되는 화합물을 말한다. 우리 몸의 필수 구성요소인 아미노산과 당은 하나의 광학이성질체로 이뤄져 있어, 새 화합물이 생체 내에 들어가면 그 화합물의 광학활성에 따라 서로 다른 생리학적 특징을 나타내기 때문에 신약개발에서 광학활성을 조절하고 분석하는 연구가 필수적이다.
광학활성을 분석하는 방법으로 고성능 액체크로마토그래피(HPLC)가 주로 사용되며, 이를 통한 광학활성 분석 시장은 일본이 전체의 50% 이상을 차지하고 있다. 하지만 고성능 액체크로마토그래피는 분석에 30분에서 1시간이 소요되고 분석물이 발색단(發色團)을 가져야 분석 가능하다는 단점이 있다.
이에 비해 화합물의 분자 구조를 분석하는 데 많이 활용되는 핵자기공명(NMR) 분광분석기는 1~5분의 분석시간을 가지고 있으나, 광학활성 화합물의 신호를 분리하는 효과적인 방법이 규명되지 않았다.
김 교수 연구팀은 갈륨금속 중심의 음전하를 띤 금속 화합물을 합성하고 핵자기공명(NMR) 분광분석기를 활용해 효과적인 광학활성의 분석 방법을 개발했다.
연구팀은 금속 화합물과 광학활성 알코올 화합물 간 비공유 상호작용을 통해 핵자기공명 분광분석기의 신호가 구별돼 광학활성을 분석할 수 있는 원리를 이용했다. 기존 핵자기공명(NMR) 분광분석기를 통한 광학활성 분석은 알코올의 상온 분석 방법은 보고되지 않았다.
이번 연구는 다양한 작용기를 포함하고 있는 알코올 화합물의 상온 광학활성을 규명했다는 의의를 갖는다.
이번 연구에서 개발된 방법은 많은 신약 및 신약후보 물질의 광학활성 분석에 활용될 수 있으며, 특히 일본의 의존도가 높은 고성능 액체크로마토그래피(HPLC)를 이용한 광학활성 분석 방법을 대체할 수 있을 것으로 기대된다.
김 교수는 “핵자기공명 분광기를 활용한 광학활성 분석 관련 최고 수준의 기술이며, 신약개발에 필요한 광학활성 분석에 활용될 것으로 기대한다”라고 말했다.
이번 연구는 삼성미래기술육성재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 김현우 교수 연구성과 개념도
김현우 교수, 알코올 화합물의 광학활성 분석기술 개발
〈 김현우 교수 〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명(NMR) 분광분석기를 통해 알코올 화합물의 광학활성을 간단히 분석할 수 있는 기술을 개발했다.
이 기술은 빠르고 간편한 분석 방법을 가지고 있어 다양한 알코올 화합물의 광학활성뿐만 아니라 비대칭 합성반응의 모니터링까지 폭넓게 응용 및 적용할 수 있을 것으로 기대된다.
장수민 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지 셀의 자매지 ‘아이 사이언스 (iScience)’ 9월 27일 자 온라인판에 게재됐다. (논문명 : A Gallium-Based Chiral Solvating Agent Enables the Use of 1H NMR Spectroscopy to Differentiate Chiral Alcohols)
광학이성질체는 오른손과 왼손의 관계처럼 서로 같은 물질로 이뤄져 있으나 거울상 대칭이 되는 화합물을 말한다. 우리 몸의 필수 구성요소인 아미노산과 당은 하나의 광학이성질체로 이뤄져 있어, 새 화합물이 생체 내에 들어가면 그 화합물의 광학활성에 따라 서로 다른 생리학적 특징을 나타내기 때문에 신약개발에서 광학활성을 조절하고 분석하는 연구가 필수적이다.
광학활성을 분석하는 방법으로 고성능 액체크로마토그래피(HPLC)가 주로 사용되며, 이를 통한 광학활성 분석 시장은 일본이 전체의 50% 이상을 차지하고 있다. 하지만 고성능 액체크로마토그래피는 분석에 30분에서 1시간이 소요되고 분석물이 발색단(發色團)을 가져야 분석 가능하다는 단점이 있다.
이에 비해 화합물의 분자 구조를 분석하는 데 많이 활용되는 핵자기공명(NMR) 분광분석기는 1~5분의 분석시간을 가지고 있으나, 광학활성 화합물의 신호를 분리하는 효과적인 방법이 규명되지 않았다.
김 교수 연구팀은 갈륨금속 중심의 음전하를 띤 금속 화합물을 합성하고 핵자기공명(NMR) 분광분석기를 활용해 효과적인 광학활성의 분석 방법을 개발했다.
연구팀은 금속 화합물과 광학활성 알코올 화합물 간 비공유 상호작용을 통해 핵자기공명 분광분석기의 신호가 구별돼 광학활성을 분석할 수 있는 원리를 이용했다. 기존 핵자기공명(NMR) 분광분석기를 통한 광학활성 분석은 알코올의 상온 분석 방법은 보고되지 않았다.
이번 연구는 다양한 작용기를 포함하고 있는 알코올 화합물의 상온 광학활성을 규명했다는 의의를 갖는다.
이번 연구에서 개발된 방법은 많은 신약 및 신약후보 물질의 광학활성 분석에 활용될 수 있으며, 특히 일본의 의존도가 높은 고성능 액체크로마토그래피(HPLC)를 이용한 광학활성 분석 방법을 대체할 수 있을 것으로 기대된다.
김 교수는 “핵자기공명 분광기를 활용한 광학활성 분석 관련 최고 수준의 기술이며, 신약개발에 필요한 광학활성 분석에 활용될 것으로 기대한다”라고 말했다.
이번 연구는 삼성미래기술육성재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 김현우 교수 연구성과 개념도
2019.10.10
조회수 12178
-
 정유성 교수, 인공지능을 통한 소재 역설계 기술 개발
〈 정유성 교수, 노주환 박사과정〉
우리 대학 EEWS대학원/생명화학공학과 정유성 교수 연구팀이 인공지능을 활용해 원하는 물성을 갖는 신소재를 역설계하는 기술을 개발했다.
연구팀은 알고리즘을 통해 수만 개의 물질을 학습시킨 뒤 인공지능을 통해 원하는 물성을 갖는 소재를 역설계하는 방식으로 4종의 신물질을 발견했다. 향후 신소재 개발에 크게 이바지할 수 있을 것으로 기대된다.
노주환 박사과정이 1저자로 참여한 이번 연구 결과는 ‘셀 (Cell)’ 자매지 ‘매터(Matter)’ 10월 2일 자 온라인판에 출판됐다. (논문명 : Inverse Design of Solid State Materials via a Continuous Representation)
소재 연구의 궁극적인 목표는 원하는 물성을 갖는 신소재를 개발하는 것이다. 하지만 현재까지의 신소재 개발은 화학적 직관과 실험적 시행착오를 통한 방법 위주였기 때문에 개발 비용과 시간이 많이 들어 소재 개념화에서부터 상용화에 걸리는 시간이 평균 30년 정도 소요됐다.
기존의 소재 개발 과정은 소재를 시행착오를 통해 합성하고 난 후 물성을 측정해 만들어진 소재가 응용 목적에 맞는 소재인지를 평가하는 방식으로 개발됐다.
정 교수 연구팀은 인공지능 기술과 슈퍼컴퓨터 활용을 융합해 이러한 소재 개발을 기간을 크게 단축할 수 있는 새로운 소재 역설계 방법을 개발했다. 정 교수팀이 개발한 소재 역설계 방법은 기계(알고리즘)로 기존의 수만 개 물질과 그 물질들이 갖는 물성을 학습하게 한 후, 원하는 물성을 갖는 물질을 인공지능 기반 알고리즘이 역으로 생성하는 방식이다.
연구팀이 개발한 소재 역설계 방법은 기존의 컴퓨터 스크리닝을 통해 소재 설계를 가속화 하는 연구와도 차별성이 있다. 스크리닝 기반의 소재 발견 기술은 발견될 물질이 스크리닝 대상이 되는 물질 데이터베이스를 벗어날 수 없다는 한계를 가지고 있다. 따라서 데이터베이스에 존재하지 않는 새로운 형태의 소재를 발견하지 못한다는 단점이 있다.
연구팀이 개발한 신소재 역발견 모델은 인공지능 모델의 한 종류인 생성모델을 이용한 것으로, 생성모델은 이미지 및 음성 처리에 활발하게 활용되고 있는 기술이다. 예를 들어 수천 명의 얼굴들을 기계로 학습하게 해 새로운 사람의 얼굴을 생성해 내는 인공지능 기법이다.
연구팀은 이미지 생성에 주로 쓰이는 생성모델 기반의 인공지능 기법을 알려지지 않은 무기 고체 소재를 생성하는 데 최초로 적용했다. 특히 기존의 생성모델을 고체 소재에 적용하기 위해 역변환이 가능한 3차원 이미지 기반의 표현자를 도입함으로써 현재까지의 소재 역설계 모델의 한계를 극복했고, 이를 iMatGen(image-based Materials Generator) 이라 이름 지었다.
연구팀은 개발된 소재 역설계 기법을 새로운 바나듐 산화물 결정구조를 예측하는데 적용했다. 이 학습 과정에서 기존에 알려진 물질을 제외해 학습하더라도 제외된 물질들을 역으로 재발견할 수 있음을 확인해 개발 모델의 타당성을 검증했다.
최종적으로 개발된 모델을 통해 학습된 연속 잠재공간을 다양한 방법으로 샘플링하고 역변환 함으로써 기존에 존재하지 않는 전혀 새로운 바나듐 산화물 결정구조를 예측할 수 있었다.
정유성 교수는 “이번 연구는 원하는 물성을 갖는 무기 고체 소재를 역으로 설계하는 방법을 데이터 기반 기계학습으로 최초로 보인 예로, 향후 다양한 응용 분야의 신소재 개발에 도움을 줄 수 있을 것으로 기대한다”라고 말했다.
이번 연구 성과는 한국연구재단, 산업통상자원부 산하 에너지기술평가원, 그리고 KISTI의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 개발된 소재 역설계 모델
정유성 교수, 인공지능을 통한 소재 역설계 기술 개발
〈 정유성 교수, 노주환 박사과정〉
우리 대학 EEWS대학원/생명화학공학과 정유성 교수 연구팀이 인공지능을 활용해 원하는 물성을 갖는 신소재를 역설계하는 기술을 개발했다.
연구팀은 알고리즘을 통해 수만 개의 물질을 학습시킨 뒤 인공지능을 통해 원하는 물성을 갖는 소재를 역설계하는 방식으로 4종의 신물질을 발견했다. 향후 신소재 개발에 크게 이바지할 수 있을 것으로 기대된다.
노주환 박사과정이 1저자로 참여한 이번 연구 결과는 ‘셀 (Cell)’ 자매지 ‘매터(Matter)’ 10월 2일 자 온라인판에 출판됐다. (논문명 : Inverse Design of Solid State Materials via a Continuous Representation)
소재 연구의 궁극적인 목표는 원하는 물성을 갖는 신소재를 개발하는 것이다. 하지만 현재까지의 신소재 개발은 화학적 직관과 실험적 시행착오를 통한 방법 위주였기 때문에 개발 비용과 시간이 많이 들어 소재 개념화에서부터 상용화에 걸리는 시간이 평균 30년 정도 소요됐다.
기존의 소재 개발 과정은 소재를 시행착오를 통해 합성하고 난 후 물성을 측정해 만들어진 소재가 응용 목적에 맞는 소재인지를 평가하는 방식으로 개발됐다.
정 교수 연구팀은 인공지능 기술과 슈퍼컴퓨터 활용을 융합해 이러한 소재 개발을 기간을 크게 단축할 수 있는 새로운 소재 역설계 방법을 개발했다. 정 교수팀이 개발한 소재 역설계 방법은 기계(알고리즘)로 기존의 수만 개 물질과 그 물질들이 갖는 물성을 학습하게 한 후, 원하는 물성을 갖는 물질을 인공지능 기반 알고리즘이 역으로 생성하는 방식이다.
연구팀이 개발한 소재 역설계 방법은 기존의 컴퓨터 스크리닝을 통해 소재 설계를 가속화 하는 연구와도 차별성이 있다. 스크리닝 기반의 소재 발견 기술은 발견될 물질이 스크리닝 대상이 되는 물질 데이터베이스를 벗어날 수 없다는 한계를 가지고 있다. 따라서 데이터베이스에 존재하지 않는 새로운 형태의 소재를 발견하지 못한다는 단점이 있다.
연구팀이 개발한 신소재 역발견 모델은 인공지능 모델의 한 종류인 생성모델을 이용한 것으로, 생성모델은 이미지 및 음성 처리에 활발하게 활용되고 있는 기술이다. 예를 들어 수천 명의 얼굴들을 기계로 학습하게 해 새로운 사람의 얼굴을 생성해 내는 인공지능 기법이다.
연구팀은 이미지 생성에 주로 쓰이는 생성모델 기반의 인공지능 기법을 알려지지 않은 무기 고체 소재를 생성하는 데 최초로 적용했다. 특히 기존의 생성모델을 고체 소재에 적용하기 위해 역변환이 가능한 3차원 이미지 기반의 표현자를 도입함으로써 현재까지의 소재 역설계 모델의 한계를 극복했고, 이를 iMatGen(image-based Materials Generator) 이라 이름 지었다.
연구팀은 개발된 소재 역설계 기법을 새로운 바나듐 산화물 결정구조를 예측하는데 적용했다. 이 학습 과정에서 기존에 알려진 물질을 제외해 학습하더라도 제외된 물질들을 역으로 재발견할 수 있음을 확인해 개발 모델의 타당성을 검증했다.
최종적으로 개발된 모델을 통해 학습된 연속 잠재공간을 다양한 방법으로 샘플링하고 역변환 함으로써 기존에 존재하지 않는 전혀 새로운 바나듐 산화물 결정구조를 예측할 수 있었다.
정유성 교수는 “이번 연구는 원하는 물성을 갖는 무기 고체 소재를 역으로 설계하는 방법을 데이터 기반 기계학습으로 최초로 보인 예로, 향후 다양한 응용 분야의 신소재 개발에 도움을 줄 수 있을 것으로 기대한다”라고 말했다.
이번 연구 성과는 한국연구재단, 산업통상자원부 산하 에너지기술평가원, 그리고 KISTI의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 개발된 소재 역설계 모델
2019.10.07
조회수 13026
-
 생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24
조회수 25493
-
 주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03
조회수 24880
-
 조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10
조회수 23612
 숨 쉬는 헤어셀 구조의 피부부착형 맥파 센서 개발
우리 대학 바이오및뇌공학과 조영호 교수 연구팀이 피부에서 발생하는 땀을 실시간으로 투과시키며 피부와의 접촉면적을 획기적으로 개선한 다공성 헤어셀 구조의 맥파※ 센서를 개발했다고 17일 밝혔다.
※ 맥파: 심장이 박동할 때 발생하는 파동을 말한다.
헤어셀 구조란 피부의 섬모와 같이 다공성 표면 위에 여러 개의 섬모가 형성돼있는 구조를 말한다.
새로 개발된 다공성 헤어셀 구조의 맥파 센서 기술은 맥파 외 피부 온도, 피부 전도도 등 타 생체신호 센서들의 결합을 통해, 인간의 정신건강 상태를 상시 장기적으로 판별하는 연구에 적용하고 있다.
바이오및뇌공학과 석민호 박사과정의 주도로 개발한 이번 연구는 국제 학술지 `나노스케일 어드벤시스(Nanoscale Advances)' 7월 27일 字 온라인판에 게재됐다. 논문명: A Porous PDMS Pulsewave Sensor with Haircell Structures for Water Vapor Transmission Rate and Signal-to-Noise Ratio Enhancement)
기존 폴리머 기반 맥파 센서는 땀 투과도가 피부의 하루 평균 땀 발생량 (432g/m2) 보다 낮아 장기간 부착 시 접촉성 피부염, 가려움 등의 피부 문제를 일으키는 단점이 있으며, 피부에 안정적으로 접촉할 수 있는 면적이 낮아 맥파 신호의 정확도가 떨어지는 문제를 지닌다.
조영호 교수 연구팀은 문제 해결을 위해, 폴리디메틸실록산(PDMS) 고분자 내에 구연산을 결정화 후 에탄올로 녹여 작고 균일한 공극을 형성함으로써 맥파 센서의 땀 투과도를 높였으며, 이러한 다공성 고분자 표면에 헤어셀 구조를 형성해 피부와의 접촉면적을 획기적으로 넓혀 맥파 센서의 측정 정확도를 개선한 다공성 헤어셀 구조의 맥파 센서를 제작했다.
이번 다공성 헤어셀 구조의 맥파 센서의 땀 투과도는 하루 486g/m2을 보여 피부의 하루 평균 땀 발생량보다 많고, 기존 기술 대비 72% 증가함을 보였다. 또한 피부에 장기간 부착 시에도 피부 트러블이 발생하지 않음을 7일간의 연속 부착 실험을 통해 입증했다. 측정 정확도(≈신호대잡음비※)는 22.89를 보여, 기존 기술 대비 측정 정확도를 약 9배 높였다.
※ 신호대잡음비: 잡음의 크기 대비 맥파 신호의 크기 정도를 말한다.
조영호 교수는 "이번 연구를 통해 피부 트러블 없이 인간의 건강 상태를 상시 모니터링할 수 있는 웨어러블 센서를 개발했고 인공피부로서의 상시 사용성 역시 확립했다ˮ고 말했다.
한편, 이번 연구는 알키미스트 프로젝트 사업의 지원을 통해 수행됐다.
2021.08.18 조회수 9716
숨 쉬는 헤어셀 구조의 피부부착형 맥파 센서 개발
우리 대학 바이오및뇌공학과 조영호 교수 연구팀이 피부에서 발생하는 땀을 실시간으로 투과시키며 피부와의 접촉면적을 획기적으로 개선한 다공성 헤어셀 구조의 맥파※ 센서를 개발했다고 17일 밝혔다.
※ 맥파: 심장이 박동할 때 발생하는 파동을 말한다.
헤어셀 구조란 피부의 섬모와 같이 다공성 표면 위에 여러 개의 섬모가 형성돼있는 구조를 말한다.
새로 개발된 다공성 헤어셀 구조의 맥파 센서 기술은 맥파 외 피부 온도, 피부 전도도 등 타 생체신호 센서들의 결합을 통해, 인간의 정신건강 상태를 상시 장기적으로 판별하는 연구에 적용하고 있다.
바이오및뇌공학과 석민호 박사과정의 주도로 개발한 이번 연구는 국제 학술지 `나노스케일 어드벤시스(Nanoscale Advances)' 7월 27일 字 온라인판에 게재됐다. 논문명: A Porous PDMS Pulsewave Sensor with Haircell Structures for Water Vapor Transmission Rate and Signal-to-Noise Ratio Enhancement)
기존 폴리머 기반 맥파 센서는 땀 투과도가 피부의 하루 평균 땀 발생량 (432g/m2) 보다 낮아 장기간 부착 시 접촉성 피부염, 가려움 등의 피부 문제를 일으키는 단점이 있으며, 피부에 안정적으로 접촉할 수 있는 면적이 낮아 맥파 신호의 정확도가 떨어지는 문제를 지닌다.
조영호 교수 연구팀은 문제 해결을 위해, 폴리디메틸실록산(PDMS) 고분자 내에 구연산을 결정화 후 에탄올로 녹여 작고 균일한 공극을 형성함으로써 맥파 센서의 땀 투과도를 높였으며, 이러한 다공성 고분자 표면에 헤어셀 구조를 형성해 피부와의 접촉면적을 획기적으로 넓혀 맥파 센서의 측정 정확도를 개선한 다공성 헤어셀 구조의 맥파 센서를 제작했다.
이번 다공성 헤어셀 구조의 맥파 센서의 땀 투과도는 하루 486g/m2을 보여 피부의 하루 평균 땀 발생량보다 많고, 기존 기술 대비 72% 증가함을 보였다. 또한 피부에 장기간 부착 시에도 피부 트러블이 발생하지 않음을 7일간의 연속 부착 실험을 통해 입증했다. 측정 정확도(≈신호대잡음비※)는 22.89를 보여, 기존 기술 대비 측정 정확도를 약 9배 높였다.
※ 신호대잡음비: 잡음의 크기 대비 맥파 신호의 크기 정도를 말한다.
조영호 교수는 "이번 연구를 통해 피부 트러블 없이 인간의 건강 상태를 상시 모니터링할 수 있는 웨어러블 센서를 개발했고 인공피부로서의 상시 사용성 역시 확립했다ˮ고 말했다.
한편, 이번 연구는 알키미스트 프로젝트 사업의 지원을 통해 수행됐다.
2021.08.18 조회수 9716 효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2021.01.06 조회수 56245
효율적 정보 처리를 위한 뇌신경망의 최적화 구조 형성 원리 규명
우리 대학 바이오및뇌공학과 백세범 교수 연구팀이 대뇌 시각 피질 회로가 정보처리에 가장 최적화된 구조를 자발적으로 형성하는 원리를 밝혔다.
이번 연구 결과는 수 십년간의 뇌신경과학 연구에서 그 원리를 명확히 밝혀내지 못했던 시각 피질 기능성 지도들의 복합 구조 형성의 기작을 규명한 것으로, 수학적 모델의 도입을 통해 복잡한 생물학적 신경망 구조의 기원을 찾아낸 성공적인 연구로 평가된다.
연구팀은 망막 신경세포들이 초기 발생 단계에서 일정한 물리적 공간 분포 패턴을 형성하는 과정에서 다양한 종류의 정보 처리 회로가 자발적으로 생성될 뿐만 아니라, 이 패턴으로부터 시각 피질의 기능성 뇌지도들의 규칙적이고 효율적인 복합적 구조가 형성됨을 밝혀냈다.
바이오및뇌공학과 송민 박사과정과 장재선 박사가 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 1월 5일 자에 게재됐다. (논문명: Projection of orthogonal tiling from the retina to the visual cortex).
포유류의 일차시각피질 신경세포들은 눈으로부터 입력된 시각 정보의 색, 물체의 형태를 이루는 선분의 각도, 폭 등의 기본적인 시각 정보를 구별하여 전기적 신호로 부호화 한다. 예를 들어 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 가지는 세포들은 물체의 형태를 구별하기위해 필요한 윤곽선에 대한 정보를 선택적으로 처리한다.
이러한 시각 피질 세포들의 방향 선택성, 공간 주기성등의 성질은 시각 피질 상에서 연속적, 주기적인 형태로 변하는 기능성 지도 (functional map) 구조를 형성하는데, 이 지도들의 구조는 서로 독립적으로 형성되는 것이 아니라 서로 수평, 또는 수직 관계를 이루며 매우 효율적인 짜임새 구조(efficient tiling)를 이룬다. 이를 통해 시각 피질의 모든 국소 영역에서 정보 요소들을 손실없이 효율적으로 부호화할 수 있도록 만드는 대주(hypercolumn) 구조를 형성하는데, 시각 정보처리의 핵심이 되는 이러한 기능성 구조가 어떻게 발생하는지에 대해서는 밝혀진 바가 없었다.
연구팀은 수학적 모델에 기반한 컴퓨터 시뮬레이션을 통하여 포유류의 망막에서 발견되는 신경절 세포들이 단순한 물리적 상호작용을 통해 시각 정보의 입력이 없는 상태에서도 놀라울 정도로 효율적인 공간적 배치를 자발적으로 형성할 수 있음을 확인하였다.
연구팀은 이러한 구조가 시각 피질로 투영되어 시각 피질의 다양한 기능성 뇌지도들을 형성됨과 동시에, 그 지도들 간의 상호 짜임새를 정보처리에 가장 최적화된 형태로 구성할 수 있음을 보였다. 뇌의 주요 정보 처리 회로에 대한 설계도가 이미 망막 단계의 신경망이 형성되는 과정에서 자발적으로 발생함을 증명한 것이다.
백세범 교수는 “시각 정보처리의 핵심 구조인 시각 피질의 기능성 지도가 어떻게 자발적으로 발생하는지 규명하였을 뿐 아니라, 다양한 정보를 처리하는 각각의 뇌신경망 회로 구조가 단순한 물리적 상호작용에 의해 가장 효율적인 형태의 복합 구조를 형성할 수 있음을 처음으로 증명한 연구다" 라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2021.01.06 조회수 56245 육종민 교수팀, 살아있는 세포의 전자현미경 관찰 성공
우리 대학 신소재공학과 육종민 교수 연구팀이 경북대학교(총장 김상동) ITA 융합대학원 한영기 교수 연구팀과 공동연구를 통해 살아 있는 세포를 전자현미경을 통해 실시간으로 관찰하는 데 성공했다고 29일 밝혔다.
이번 연구를 통해 살아 있는 다양한 세포의 실시간 분자 단위 관찰이 가능해져, 그동안 관찰하지 못했던 살아 있는 세포의 전이·감염에 관한 전 과정을 규명할 수 있게 돼 신약 개발 등을 더욱 촉진할 수 있을 것으로 기대된다.
신소재공학과 구건모 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `나노 레터스(Nano Letters)' 5월 5일 字 온라인판에 게재됐으며 6월 호 표지논문으로 선정됐다. (논문명: Live-Cell Electron Microscopy Using Graphene Veils)
전 세계적으로 대유행하고 있는 코로나바이러스감염증(COVID-19) 등은 수십~수백 나노미터(nm, 1 나노미터는 100만 분의 1밀리미터) 크기의 바이러스로 인해 일어나는 질병이다. 바이러스의 전이·감염 과정을 분석하고 이에 대처하는 신약 개발을 위해서는 바이러스의 미시적인 행동을 실시간으로 관찰하는 것이 매우 중요하다.
수십~수백 나노미터 크기의 바이러스 등을 비롯해 세포와 세포를 이루는 기관들은 가시광선을 이용하는 일반 광학현미경으로는 관찰이 어려워 해상력이 매우 높은 전자선을 이용하는 전자현미경 기술을 이용한다.
그렇지만 전자현미경 기술은 효율적인 작동을 위해 매우 강력한 진공상태가 필요하며 또 가시광선보다 수천 배 이상 높은 에너지를 가지는 전자를 이용하기 때문에 관찰 시 세포의 구조적인 손상이 불가피하다. 따라서 현재로서는 2017년 노벨화학상을 수상한 기술인 극저온 전자현미경을 통해 고정 작업 및 안정화 작업을 거친 표본만 관찰이 가능하다.
최근 학계에서는 사멸해 고정된 것이 아닌 온전한 상태의 살아 있는 세포등 다양한 생체물질을 전자현미경을 이용해 분자 단위로 관찰 가능한지에 대한 논쟁이 전개되고 있다. 육 교수 연구팀은 지난 2012년 개발한 그래핀 액상 셀 전자현미경 기술을 응용해 전자현미경으로도 살아있는 대장균 세포를 관찰하는데 성공했고, 이를 재배양시킴으로써 전자와 진공에 노출됐음에도 불구하고 대장균 세포가 생존한다는 사실을 밝혀냈다.
육 교수 연구팀이 이번 연구에서 활용한 그래핀은 층상 구조인 흑연에서 분리하는 등의 방법으로 얻어내는 약 0.2 나노미터(nm) 두께의 원자 막이다. 여러 분야에서 차세대 소재로 주목받고 있는 그래핀은 강철보다 200배 강한 강도와 높은 전기 전도성을 가지며, 물질을 투과시키지 않는 성질을 가진다. 육 교수 연구팀은 이러한 그래핀 성질을 이용, 세포 등을 액체와 함께 감싸주면, 고진공의 전자현미경 내부에서 탈수에 의한 세포의 구조변화를 막아줄 수 있음을 밝혀냈다. 뿐만 아니라, 그래핀이 전자빔에 의해 공격성이 높아진 활성 산소들을 분해하는 효과도 지니고 있어 그래핀으로 덮어주지 않은 세포보다 100배 강한 전자에 노출되더라도 세포가 활성을 잃지 않는다는 결과를 확인했다.
육 교수는 "이번 연구 결과는 세포보다 더 작은 단백질이나 DNA의 실시간 전자현미경 관찰로까지 확대될 수 있어, 앞으로 다양한 생명 현상의 기작을 근본적으로 밝힐 수 있을 것이라 기대한다ˮ고 밝혔다.
한편, 이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
2020.06.29 조회수 22131
육종민 교수팀, 살아있는 세포의 전자현미경 관찰 성공
우리 대학 신소재공학과 육종민 교수 연구팀이 경북대학교(총장 김상동) ITA 융합대학원 한영기 교수 연구팀과 공동연구를 통해 살아 있는 세포를 전자현미경을 통해 실시간으로 관찰하는 데 성공했다고 29일 밝혔다.
이번 연구를 통해 살아 있는 다양한 세포의 실시간 분자 단위 관찰이 가능해져, 그동안 관찰하지 못했던 살아 있는 세포의 전이·감염에 관한 전 과정을 규명할 수 있게 돼 신약 개발 등을 더욱 촉진할 수 있을 것으로 기대된다.
신소재공학과 구건모 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `나노 레터스(Nano Letters)' 5월 5일 字 온라인판에 게재됐으며 6월 호 표지논문으로 선정됐다. (논문명: Live-Cell Electron Microscopy Using Graphene Veils)
전 세계적으로 대유행하고 있는 코로나바이러스감염증(COVID-19) 등은 수십~수백 나노미터(nm, 1 나노미터는 100만 분의 1밀리미터) 크기의 바이러스로 인해 일어나는 질병이다. 바이러스의 전이·감염 과정을 분석하고 이에 대처하는 신약 개발을 위해서는 바이러스의 미시적인 행동을 실시간으로 관찰하는 것이 매우 중요하다.
수십~수백 나노미터 크기의 바이러스 등을 비롯해 세포와 세포를 이루는 기관들은 가시광선을 이용하는 일반 광학현미경으로는 관찰이 어려워 해상력이 매우 높은 전자선을 이용하는 전자현미경 기술을 이용한다.
그렇지만 전자현미경 기술은 효율적인 작동을 위해 매우 강력한 진공상태가 필요하며 또 가시광선보다 수천 배 이상 높은 에너지를 가지는 전자를 이용하기 때문에 관찰 시 세포의 구조적인 손상이 불가피하다. 따라서 현재로서는 2017년 노벨화학상을 수상한 기술인 극저온 전자현미경을 통해 고정 작업 및 안정화 작업을 거친 표본만 관찰이 가능하다.
최근 학계에서는 사멸해 고정된 것이 아닌 온전한 상태의 살아 있는 세포등 다양한 생체물질을 전자현미경을 이용해 분자 단위로 관찰 가능한지에 대한 논쟁이 전개되고 있다. 육 교수 연구팀은 지난 2012년 개발한 그래핀 액상 셀 전자현미경 기술을 응용해 전자현미경으로도 살아있는 대장균 세포를 관찰하는데 성공했고, 이를 재배양시킴으로써 전자와 진공에 노출됐음에도 불구하고 대장균 세포가 생존한다는 사실을 밝혀냈다.
육 교수 연구팀이 이번 연구에서 활용한 그래핀은 층상 구조인 흑연에서 분리하는 등의 방법으로 얻어내는 약 0.2 나노미터(nm) 두께의 원자 막이다. 여러 분야에서 차세대 소재로 주목받고 있는 그래핀은 강철보다 200배 강한 강도와 높은 전기 전도성을 가지며, 물질을 투과시키지 않는 성질을 가진다. 육 교수 연구팀은 이러한 그래핀 성질을 이용, 세포 등을 액체와 함께 감싸주면, 고진공의 전자현미경 내부에서 탈수에 의한 세포의 구조변화를 막아줄 수 있음을 밝혀냈다. 뿐만 아니라, 그래핀이 전자빔에 의해 공격성이 높아진 활성 산소들을 분해하는 효과도 지니고 있어 그래핀으로 덮어주지 않은 세포보다 100배 강한 전자에 노출되더라도 세포가 활성을 잃지 않는다는 결과를 확인했다.
육 교수는 "이번 연구 결과는 세포보다 더 작은 단백질이나 DNA의 실시간 전자현미경 관찰로까지 확대될 수 있어, 앞으로 다양한 생명 현상의 기작을 근본적으로 밝힐 수 있을 것이라 기대한다ˮ고 밝혔다.
한편, 이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
2020.06.29 조회수 22131 포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2020.03.11 조회수 16128
포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2020.03.11 조회수 16128 빛으로 RNA 이동과 단백질 합성 조절한다
빛으로 세포 내 특정 RNA 이동과 단백질 합성을 조절할 수 있는 기술이 개발됐다. 생명과학과 허원도 교수 연구팀이 빛을 이용해 유전정보를 전달하는 전령RNA와 단백질을 생성하는 리보솜의 결합을 제어해 단백질 합성을 조절하는데 성공했다.
이번 연구성과는 네이처 셀 바이올로지(Nature Cell Biology, IF 17.728)에 2월 18일 오전 1시(한국시간)자 온라인 판에 실렸으며, Nature Reviews Genetics에 하이라이트 논문으로 소개됐다.
DNA의 유전정보는 RNA를 거쳐 단백질로 전달된다. 이때 중간에서 유전정보를 전달하는 RNA를 ‘전령RNA’라고 한다. 단백질 생성공장인 리보솜이 전령RNA의 유전정보를 읽어 단백질을 합성한다. 단백질 합성에 있어 전령RNA는 DNA 유전정보의 중간 전달자, 리보솜은 생성공장, 단백질은 완성품인 셈이다.
이전에는 화학물질을 처리해 전령RNA를 조절하는 방법으로 모든 전령RNA를 한꺼번에 조절하기 때문에 특정 종류의 전령RNA만을 세밀하게 조절하기 어려웠다. 이번 연구에서는 살아있는 세포에 청색광을 비춰줌으로써 세포 내 특정 전령RNA 이동 및 단백질 합성을 시공간 특이적으로 조절하는 mRNA-LARIAT 광유전학 기술을 개발했다.
연구팀은 이전 연구로 개발한 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술과 RNA 이미징 기술을 융합해 mRNA-LARIAT 기술을 개발했다. mRNA-LARIAT 광유전학 기술을 이용하면 빛의 유무에 따라 라리아트 올가미에 전령RNA를 가두거나 분리하고, 이를 실시간으로 관찰하는 것이 가능하다.
연구팀은 헬라 세포에 청색광을 비춰주면 라리아트 올가미에 전령RNA가 가둬지면서 리보솜과 격리되고 단백질 합성이 감소함을 관찰했다. 이어 청색광을 차단하면 라리아트 올가미로부터 전령RNA가 빠져나오면서 리보솜과 단백질 합성을 다시 시작함을 확인했다. 이는 mRNA-LARIAT 광유전학 기술로 빛의 유무에 따라 매우 빠르고 가역적으로 단백질 합성을 조절할 수 있음을 의미한다.
대부분 단백질은 전령RNA와 리보솜에 의해 합성된 후, 각 단백질이 작용하는 위치로 이동한다. 하지만 전령RNA가 라리아트 올가미에 가둬지면 전령RNA가 향후 단백질이 작용하는 위치까지 이동이 멈추고 단백질 합성이 차단된다. 전령RNA는 단백질보다 비교적 작은 분자로, 세포 내 이동이 더 효율적이고 빠르다. 이처럼 mRNA-LARIAT 광유전학 기술로 전령RNA 이동 및 단백질 합성을 빛으로 조절하면 살아있는 세포에서의 RNA의 위치 및 합성되는 신생 단백질의 기능을 효율적으로 연구할 수 있게 되었다.
연구팀은 베타액틴(β-actin) 단백질 합성에 관여하는 전령RNA에 mRNA-LARIAT 기술을 적용했다. 베타액틴 단백질 합성에 관여하는 전령RNA에 청색광을 비추니 세포 골격 구성 및 이동 기능이 제대로 이뤄지지 않음을 관찰했다. 또한 베타액틴 단백질 합성 효율이 최대 90%까지 감소됨을 확인했다.
허원도 교수는 “mRNA-LARIAT 광유전학 기술을 활용하면 암세포, 신경세포 등 다양한 세포 내 전령RNA 이동 및 단백질 합성을 빛으로 조절할 수 있다”라며 “앞으로 암세포 전이, 신경질환 등 전령 RNA 관련 질병 연구에 응용 가능할 것이다”라고 말했다.
2020.02.21 조회수 20888
빛으로 RNA 이동과 단백질 합성 조절한다
빛으로 세포 내 특정 RNA 이동과 단백질 합성을 조절할 수 있는 기술이 개발됐다. 생명과학과 허원도 교수 연구팀이 빛을 이용해 유전정보를 전달하는 전령RNA와 단백질을 생성하는 리보솜의 결합을 제어해 단백질 합성을 조절하는데 성공했다.
이번 연구성과는 네이처 셀 바이올로지(Nature Cell Biology, IF 17.728)에 2월 18일 오전 1시(한국시간)자 온라인 판에 실렸으며, Nature Reviews Genetics에 하이라이트 논문으로 소개됐다.
DNA의 유전정보는 RNA를 거쳐 단백질로 전달된다. 이때 중간에서 유전정보를 전달하는 RNA를 ‘전령RNA’라고 한다. 단백질 생성공장인 리보솜이 전령RNA의 유전정보를 읽어 단백질을 합성한다. 단백질 합성에 있어 전령RNA는 DNA 유전정보의 중간 전달자, 리보솜은 생성공장, 단백질은 완성품인 셈이다.
이전에는 화학물질을 처리해 전령RNA를 조절하는 방법으로 모든 전령RNA를 한꺼번에 조절하기 때문에 특정 종류의 전령RNA만을 세밀하게 조절하기 어려웠다. 이번 연구에서는 살아있는 세포에 청색광을 비춰줌으로써 세포 내 특정 전령RNA 이동 및 단백질 합성을 시공간 특이적으로 조절하는 mRNA-LARIAT 광유전학 기술을 개발했다.
연구팀은 이전 연구로 개발한 라리아트 올가미(LARIAT, Light-Activated Reversible Inhibition by Assembled Trap) 기술과 RNA 이미징 기술을 융합해 mRNA-LARIAT 기술을 개발했다. mRNA-LARIAT 광유전학 기술을 이용하면 빛의 유무에 따라 라리아트 올가미에 전령RNA를 가두거나 분리하고, 이를 실시간으로 관찰하는 것이 가능하다.
연구팀은 헬라 세포에 청색광을 비춰주면 라리아트 올가미에 전령RNA가 가둬지면서 리보솜과 격리되고 단백질 합성이 감소함을 관찰했다. 이어 청색광을 차단하면 라리아트 올가미로부터 전령RNA가 빠져나오면서 리보솜과 단백질 합성을 다시 시작함을 확인했다. 이는 mRNA-LARIAT 광유전학 기술로 빛의 유무에 따라 매우 빠르고 가역적으로 단백질 합성을 조절할 수 있음을 의미한다.
대부분 단백질은 전령RNA와 리보솜에 의해 합성된 후, 각 단백질이 작용하는 위치로 이동한다. 하지만 전령RNA가 라리아트 올가미에 가둬지면 전령RNA가 향후 단백질이 작용하는 위치까지 이동이 멈추고 단백질 합성이 차단된다. 전령RNA는 단백질보다 비교적 작은 분자로, 세포 내 이동이 더 효율적이고 빠르다. 이처럼 mRNA-LARIAT 광유전학 기술로 전령RNA 이동 및 단백질 합성을 빛으로 조절하면 살아있는 세포에서의 RNA의 위치 및 합성되는 신생 단백질의 기능을 효율적으로 연구할 수 있게 되었다.
연구팀은 베타액틴(β-actin) 단백질 합성에 관여하는 전령RNA에 mRNA-LARIAT 기술을 적용했다. 베타액틴 단백질 합성에 관여하는 전령RNA에 청색광을 비추니 세포 골격 구성 및 이동 기능이 제대로 이뤄지지 않음을 관찰했다. 또한 베타액틴 단백질 합성 효율이 최대 90%까지 감소됨을 확인했다.
허원도 교수는 “mRNA-LARIAT 광유전학 기술을 활용하면 암세포, 신경세포 등 다양한 세포 내 전령RNA 이동 및 단백질 합성을 빛으로 조절할 수 있다”라며 “앞으로 암세포 전이, 신경질환 등 전령 RNA 관련 질병 연구에 응용 가능할 것이다”라고 말했다.
2020.02.21 조회수 20888 암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17 조회수 14947
암세포의 약물 교차저항 원리 규명
우리 대학 생명화학공학과 김유식 교수 연구팀이 암 치료의 난제 중 하나인 암세포의 다중약물 내성 원리를 규명하는 데 성공했다.
이 연구는 학부생 연구 참여 프로그램(URP: Undergraduate research program)을 통해 마크 보리스 알돈자(Mark Borris Aldonza) 학생이 참여해 그 의미를 더했다. 마크 보리스 알돈자 학부생이 1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 2월 7일 자 온라인판에 게재됐다. (논문명 : Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms).
암 치료과정에서 약물을 장기간 투여하면 세포는 특정 약물에 대해 내성을 갖는다. 이를 극복하기 위한 가장 흔한 방법은 다른 약물을 투여하는 것이다. 하지만 특정 암세포들은 다양한 종류의 약물에 내성을 가지는 교차저항(cross-resistance) 성질을 보인다. 실제로 교차저항으로 인해 활용 가능한 약물의 종류가 줄어들고, 이는 암 재발 원인이 돼 암 극복에 큰 걸림돌이 된다. 따라서 암 극복을 위해선 암세포의 다중 약물 내성 기전의 이해가 필요하다.
연구팀은 폐암 세포가 화학 요법 약물 중 하나인 파크리탁셀에 대한 내성을 가지는 과정에서 표적 치료제인 EGFR-TKI에도 교차저항을 갖는 현상을 발견했다. 1차 약물에 대한 적응과정에서 암세포가 줄기세포화 해 전혀 다른 표적 치료제인 2차 약물에 저항을 가진다는 현상을 확인했다. 이러한 줄기세포화로 인해 포도당 부족에 의한 대사 스트레스 상황에서 암세포는 죽지 않고 활동휴지 상태로 전환된다. 활동휴지 상태인 암세포는 약물에 반응하지 않으며 약물이 없어지고 영양분이 공급되면 다시 빠르게 증식했다.
실제로 세포자살을 주관하는 아포토시스(apoptosis) 신호체계 주요 인자인 FOXO3a가 세포자살을 유도하지 않고, 오히려 세포사멸을 억제하는 방향으로 유전자의 기능이 변화해 세포가 약물을 극복할 수 있게 했다. 연구팀은 이러한 교차저항 세포의 특성을 실제 파크리탁셀 약물을 투여받은 유방암 환자의 검사대상물을 활용해 검증했다. 특히 파크리탁셀에 저항을 갖는 재발환자의 암 조직에서 FOXO3a 유전자의 발현이 증가돼 연구의 임상적 의미를 더했다. 나아가 연구팀은 FOXO3a의 발현을 억제하면 세포가 파크리탁셀과 EGFR-TKI의 저항성을 잃게 돼 교차저항 세포를 극복할 수 있을 것이라는 새 방향을 제시했다.
연구팀이 제시한 약물 교차저항 특성 및 기전은 효과적인 암 약물치료 전략을 개발하는데 이바지할 수 있을 것으로 기대된다. 논문의 제1 저자인 마크 보리스 연구원은 “이 연구가 파크리탁셀과 EGFR-TKI뿐 아니라 다른 약물에 대한 내성 기전 연구에 돌파구를 제시할 수 있을 것으로 기대한다”라며 “암 극복에 효과적인 치료 전략을 개발하는데 적용될 것이다”라고 말했다.
이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 시스템헬스케어 사업의 지원을 받아 수행됐다.
2020.02.17 조회수 14947 김상현 교수, 6만 ppi 초고해상도 디스플레이 제작기술 개발
〈 김상현 교수 연구팀(왼쪽 위 두번째 김상현 교수) 〉
우리 대학 전기및전자공학부 김상현 교수 연구팀이 반도체 공정 기술을 활용해 기존 마이크로 LED 디스플레이의 해상도 한계를 극복할 수 있는 6만 ppi(pixel per inch) 이상의 초고해상도 디스플레이 제작 가능 기술을 개발했다.
금대명 박사가 1 저자로 참여한 이번 연구는 국제학술지 ‘나노스케일(Nanoscale)’ 12월 28일자 표지 논문으로 게재됐다. (논문명 : Strategy toward the fabrication of ultrahigh-resolution micro-LED displays by bonding interface-engineered vertical stacking and surface passivation).
디스플레이의 기본 단위인 LED 중 무기물 LED는 유기물 LED보다 높은 효율, 높은 신뢰성, 고속성을 가져 마이크로 크기의 무기물 LED를 픽셀 화소로 사용하는 디스플레이(마이크로 LED 디스플레이)가 새로운 디스플레이 기술로 주목받고 있다.
무기물 LED를 화소로 사용하기 위해서는 적녹청(R/G/B) 픽셀을 밀집하게 배열해야 하지만, 현재 적색과 녹색, 청색을 낼 수 있는 LED의 물질이 달라 각각 제작한 LED를 디스플레이 기판에 전사해야 한다. 따라서 마이크로 LED 디스플레이에 관련한 대부분 연구가 이런 패키징 측면의 전사 기술 위주로 이루어지고 있다.
그러나 수백만 개의 픽셀을 마이크로미터 크기로 정렬해 세 번의 전사과정으로 화소를 형성하는 것은 전사 시 사용하는 LED 이송헤드의 크기 제한, 기계적 정확도 제한, 그리고 수율 저하 문제 등 해결해야 할 기술적 난제들이 많아 초고해상도 디스플레이에 적용하기에는 한계가 있다.
연구팀은 문제 해결을 위해 적녹청 LED 활성층을 3차원으로 적층한 후, 반도체 패터닝 공정을 이용해 초고해상도 마이크로 LED 디스플레이에 대응할 수 있는 소자 제작 방법을 제안함과 동시에 수직 적층시 문제가 될 수 있는 색의 간섭 문제, 초소형 픽셀에서의 효율 개선 방안을 제시했다.
연구팀은 3차원 적층을 위해 기판 접합 기술을 사용했고, 색 간섭을 최소화하기 위해 접합 면에 필터 특성을 갖는 절연막을 설계해 적색-청색 간섭 광을 97% 제거했다.
이러한 광학 설계를 포함한 접합 매개물을 통해 수직으로 픽셀을 결합해도 빛의 간섭 없이 순도 높은 픽셀을 구현할 수 있음을 확인했다. 연구팀은 수직 결합 후 반도체 패터닝 기술을 이용해 6만 ppi 이상의 해상도 달성 가능성을 증명했다.
또한, 초소형 LED 픽셀에서 문제가 될 수 있는 반도체 표면에서의 비 발광성 재결합 현상을 시간 분해 광발광 분석과 전산모사를 통해 체계적으로 조사해 초소형 LED의 효율을 개선할 수 있는 중요한 방향성을 제시했다.
김상현 교수는 “반도체 공정을 이용해 초고해상도의 픽셀 제작 가능성을 최초로 입증한 연구로, 반도체와 디스플레이 업계 협력의 중요성을 보여주는 연구 결과이다”라며 “후속 연구를 통해 초고해상도 미래 디스플레이의 기술 개발에 힘쓰겠다”라고 말했다.
이번 연구는 한국연구재단 이공분야 기초연구사업 기본연구, 기후변화대응기술개발사업 등의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 1um 크기를 가진 마이크로 단일 LED 가 실제로 배열된 모습을 보여주는 이미지, 1 um, 0.6 um 크기를 가진 LED를 광 여기 방법을 통해 적색 발광이 되는 모습을 보여주는 이미지(작은 사진). 이는 작아진 LED에서도 적색 발광특성이 잘 발현됨을 보여줌.
그림 2. 나노스케일 커버 이미지: 본 제작 방법의 사용 예시를 보여줌
2020.01.06 조회수 21432
김상현 교수, 6만 ppi 초고해상도 디스플레이 제작기술 개발
〈 김상현 교수 연구팀(왼쪽 위 두번째 김상현 교수) 〉
우리 대학 전기및전자공학부 김상현 교수 연구팀이 반도체 공정 기술을 활용해 기존 마이크로 LED 디스플레이의 해상도 한계를 극복할 수 있는 6만 ppi(pixel per inch) 이상의 초고해상도 디스플레이 제작 가능 기술을 개발했다.
금대명 박사가 1 저자로 참여한 이번 연구는 국제학술지 ‘나노스케일(Nanoscale)’ 12월 28일자 표지 논문으로 게재됐다. (논문명 : Strategy toward the fabrication of ultrahigh-resolution micro-LED displays by bonding interface-engineered vertical stacking and surface passivation).
디스플레이의 기본 단위인 LED 중 무기물 LED는 유기물 LED보다 높은 효율, 높은 신뢰성, 고속성을 가져 마이크로 크기의 무기물 LED를 픽셀 화소로 사용하는 디스플레이(마이크로 LED 디스플레이)가 새로운 디스플레이 기술로 주목받고 있다.
무기물 LED를 화소로 사용하기 위해서는 적녹청(R/G/B) 픽셀을 밀집하게 배열해야 하지만, 현재 적색과 녹색, 청색을 낼 수 있는 LED의 물질이 달라 각각 제작한 LED를 디스플레이 기판에 전사해야 한다. 따라서 마이크로 LED 디스플레이에 관련한 대부분 연구가 이런 패키징 측면의 전사 기술 위주로 이루어지고 있다.
그러나 수백만 개의 픽셀을 마이크로미터 크기로 정렬해 세 번의 전사과정으로 화소를 형성하는 것은 전사 시 사용하는 LED 이송헤드의 크기 제한, 기계적 정확도 제한, 그리고 수율 저하 문제 등 해결해야 할 기술적 난제들이 많아 초고해상도 디스플레이에 적용하기에는 한계가 있다.
연구팀은 문제 해결을 위해 적녹청 LED 활성층을 3차원으로 적층한 후, 반도체 패터닝 공정을 이용해 초고해상도 마이크로 LED 디스플레이에 대응할 수 있는 소자 제작 방법을 제안함과 동시에 수직 적층시 문제가 될 수 있는 색의 간섭 문제, 초소형 픽셀에서의 효율 개선 방안을 제시했다.
연구팀은 3차원 적층을 위해 기판 접합 기술을 사용했고, 색 간섭을 최소화하기 위해 접합 면에 필터 특성을 갖는 절연막을 설계해 적색-청색 간섭 광을 97% 제거했다.
이러한 광학 설계를 포함한 접합 매개물을 통해 수직으로 픽셀을 결합해도 빛의 간섭 없이 순도 높은 픽셀을 구현할 수 있음을 확인했다. 연구팀은 수직 결합 후 반도체 패터닝 기술을 이용해 6만 ppi 이상의 해상도 달성 가능성을 증명했다.
또한, 초소형 LED 픽셀에서 문제가 될 수 있는 반도체 표면에서의 비 발광성 재결합 현상을 시간 분해 광발광 분석과 전산모사를 통해 체계적으로 조사해 초소형 LED의 효율을 개선할 수 있는 중요한 방향성을 제시했다.
김상현 교수는 “반도체 공정을 이용해 초고해상도의 픽셀 제작 가능성을 최초로 입증한 연구로, 반도체와 디스플레이 업계 협력의 중요성을 보여주는 연구 결과이다”라며 “후속 연구를 통해 초고해상도 미래 디스플레이의 기술 개발에 힘쓰겠다”라고 말했다.
이번 연구는 한국연구재단 이공분야 기초연구사업 기본연구, 기후변화대응기술개발사업 등의 지원을 받아 수행됐다.
□ 그림 설명
그림 1. 1um 크기를 가진 마이크로 단일 LED 가 실제로 배열된 모습을 보여주는 이미지, 1 um, 0.6 um 크기를 가진 LED를 광 여기 방법을 통해 적색 발광이 되는 모습을 보여주는 이미지(작은 사진). 이는 작아진 LED에서도 적색 발광특성이 잘 발현됨을 보여줌.
그림 2. 나노스케일 커버 이미지: 본 제작 방법의 사용 예시를 보여줌
2020.01.06 조회수 21432 김현우 교수, 알코올 화합물의 광학활성 분석기술 개발
〈 김현우 교수 〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명(NMR) 분광분석기를 통해 알코올 화합물의 광학활성을 간단히 분석할 수 있는 기술을 개발했다.
이 기술은 빠르고 간편한 분석 방법을 가지고 있어 다양한 알코올 화합물의 광학활성뿐만 아니라 비대칭 합성반응의 모니터링까지 폭넓게 응용 및 적용할 수 있을 것으로 기대된다.
장수민 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지 셀의 자매지 ‘아이 사이언스 (iScience)’ 9월 27일 자 온라인판에 게재됐다. (논문명 : A Gallium-Based Chiral Solvating Agent Enables the Use of 1H NMR Spectroscopy to Differentiate Chiral Alcohols)
광학이성질체는 오른손과 왼손의 관계처럼 서로 같은 물질로 이뤄져 있으나 거울상 대칭이 되는 화합물을 말한다. 우리 몸의 필수 구성요소인 아미노산과 당은 하나의 광학이성질체로 이뤄져 있어, 새 화합물이 생체 내에 들어가면 그 화합물의 광학활성에 따라 서로 다른 생리학적 특징을 나타내기 때문에 신약개발에서 광학활성을 조절하고 분석하는 연구가 필수적이다.
광학활성을 분석하는 방법으로 고성능 액체크로마토그래피(HPLC)가 주로 사용되며, 이를 통한 광학활성 분석 시장은 일본이 전체의 50% 이상을 차지하고 있다. 하지만 고성능 액체크로마토그래피는 분석에 30분에서 1시간이 소요되고 분석물이 발색단(發色團)을 가져야 분석 가능하다는 단점이 있다.
이에 비해 화합물의 분자 구조를 분석하는 데 많이 활용되는 핵자기공명(NMR) 분광분석기는 1~5분의 분석시간을 가지고 있으나, 광학활성 화합물의 신호를 분리하는 효과적인 방법이 규명되지 않았다.
김 교수 연구팀은 갈륨금속 중심의 음전하를 띤 금속 화합물을 합성하고 핵자기공명(NMR) 분광분석기를 활용해 효과적인 광학활성의 분석 방법을 개발했다.
연구팀은 금속 화합물과 광학활성 알코올 화합물 간 비공유 상호작용을 통해 핵자기공명 분광분석기의 신호가 구별돼 광학활성을 분석할 수 있는 원리를 이용했다. 기존 핵자기공명(NMR) 분광분석기를 통한 광학활성 분석은 알코올의 상온 분석 방법은 보고되지 않았다.
이번 연구는 다양한 작용기를 포함하고 있는 알코올 화합물의 상온 광학활성을 규명했다는 의의를 갖는다.
이번 연구에서 개발된 방법은 많은 신약 및 신약후보 물질의 광학활성 분석에 활용될 수 있으며, 특히 일본의 의존도가 높은 고성능 액체크로마토그래피(HPLC)를 이용한 광학활성 분석 방법을 대체할 수 있을 것으로 기대된다.
김 교수는 “핵자기공명 분광기를 활용한 광학활성 분석 관련 최고 수준의 기술이며, 신약개발에 필요한 광학활성 분석에 활용될 것으로 기대한다”라고 말했다.
이번 연구는 삼성미래기술육성재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 김현우 교수 연구성과 개념도
2019.10.10 조회수 12178
김현우 교수, 알코올 화합물의 광학활성 분석기술 개발
〈 김현우 교수 〉
우리 대학 화학과 김현우 교수 연구팀이 핵자기공명(NMR) 분광분석기를 통해 알코올 화합물의 광학활성을 간단히 분석할 수 있는 기술을 개발했다.
이 기술은 빠르고 간편한 분석 방법을 가지고 있어 다양한 알코올 화합물의 광학활성뿐만 아니라 비대칭 합성반응의 모니터링까지 폭넓게 응용 및 적용할 수 있을 것으로 기대된다.
장수민 박사과정이 1 저자로 참여한 이번 연구 결과는 국제 학술지 셀의 자매지 ‘아이 사이언스 (iScience)’ 9월 27일 자 온라인판에 게재됐다. (논문명 : A Gallium-Based Chiral Solvating Agent Enables the Use of 1H NMR Spectroscopy to Differentiate Chiral Alcohols)
광학이성질체는 오른손과 왼손의 관계처럼 서로 같은 물질로 이뤄져 있으나 거울상 대칭이 되는 화합물을 말한다. 우리 몸의 필수 구성요소인 아미노산과 당은 하나의 광학이성질체로 이뤄져 있어, 새 화합물이 생체 내에 들어가면 그 화합물의 광학활성에 따라 서로 다른 생리학적 특징을 나타내기 때문에 신약개발에서 광학활성을 조절하고 분석하는 연구가 필수적이다.
광학활성을 분석하는 방법으로 고성능 액체크로마토그래피(HPLC)가 주로 사용되며, 이를 통한 광학활성 분석 시장은 일본이 전체의 50% 이상을 차지하고 있다. 하지만 고성능 액체크로마토그래피는 분석에 30분에서 1시간이 소요되고 분석물이 발색단(發色團)을 가져야 분석 가능하다는 단점이 있다.
이에 비해 화합물의 분자 구조를 분석하는 데 많이 활용되는 핵자기공명(NMR) 분광분석기는 1~5분의 분석시간을 가지고 있으나, 광학활성 화합물의 신호를 분리하는 효과적인 방법이 규명되지 않았다.
김 교수 연구팀은 갈륨금속 중심의 음전하를 띤 금속 화합물을 합성하고 핵자기공명(NMR) 분광분석기를 활용해 효과적인 광학활성의 분석 방법을 개발했다.
연구팀은 금속 화합물과 광학활성 알코올 화합물 간 비공유 상호작용을 통해 핵자기공명 분광분석기의 신호가 구별돼 광학활성을 분석할 수 있는 원리를 이용했다. 기존 핵자기공명(NMR) 분광분석기를 통한 광학활성 분석은 알코올의 상온 분석 방법은 보고되지 않았다.
이번 연구는 다양한 작용기를 포함하고 있는 알코올 화합물의 상온 광학활성을 규명했다는 의의를 갖는다.
이번 연구에서 개발된 방법은 많은 신약 및 신약후보 물질의 광학활성 분석에 활용될 수 있으며, 특히 일본의 의존도가 높은 고성능 액체크로마토그래피(HPLC)를 이용한 광학활성 분석 방법을 대체할 수 있을 것으로 기대된다.
김 교수는 “핵자기공명 분광기를 활용한 광학활성 분석 관련 최고 수준의 기술이며, 신약개발에 필요한 광학활성 분석에 활용될 것으로 기대한다”라고 말했다.
이번 연구는 삼성미래기술육성재단의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 김현우 교수 연구성과 개념도
2019.10.10 조회수 12178 정유성 교수, 인공지능을 통한 소재 역설계 기술 개발
〈 정유성 교수, 노주환 박사과정〉
우리 대학 EEWS대학원/생명화학공학과 정유성 교수 연구팀이 인공지능을 활용해 원하는 물성을 갖는 신소재를 역설계하는 기술을 개발했다.
연구팀은 알고리즘을 통해 수만 개의 물질을 학습시킨 뒤 인공지능을 통해 원하는 물성을 갖는 소재를 역설계하는 방식으로 4종의 신물질을 발견했다. 향후 신소재 개발에 크게 이바지할 수 있을 것으로 기대된다.
노주환 박사과정이 1저자로 참여한 이번 연구 결과는 ‘셀 (Cell)’ 자매지 ‘매터(Matter)’ 10월 2일 자 온라인판에 출판됐다. (논문명 : Inverse Design of Solid State Materials via a Continuous Representation)
소재 연구의 궁극적인 목표는 원하는 물성을 갖는 신소재를 개발하는 것이다. 하지만 현재까지의 신소재 개발은 화학적 직관과 실험적 시행착오를 통한 방법 위주였기 때문에 개발 비용과 시간이 많이 들어 소재 개념화에서부터 상용화에 걸리는 시간이 평균 30년 정도 소요됐다.
기존의 소재 개발 과정은 소재를 시행착오를 통해 합성하고 난 후 물성을 측정해 만들어진 소재가 응용 목적에 맞는 소재인지를 평가하는 방식으로 개발됐다.
정 교수 연구팀은 인공지능 기술과 슈퍼컴퓨터 활용을 융합해 이러한 소재 개발을 기간을 크게 단축할 수 있는 새로운 소재 역설계 방법을 개발했다. 정 교수팀이 개발한 소재 역설계 방법은 기계(알고리즘)로 기존의 수만 개 물질과 그 물질들이 갖는 물성을 학습하게 한 후, 원하는 물성을 갖는 물질을 인공지능 기반 알고리즘이 역으로 생성하는 방식이다.
연구팀이 개발한 소재 역설계 방법은 기존의 컴퓨터 스크리닝을 통해 소재 설계를 가속화 하는 연구와도 차별성이 있다. 스크리닝 기반의 소재 발견 기술은 발견될 물질이 스크리닝 대상이 되는 물질 데이터베이스를 벗어날 수 없다는 한계를 가지고 있다. 따라서 데이터베이스에 존재하지 않는 새로운 형태의 소재를 발견하지 못한다는 단점이 있다.
연구팀이 개발한 신소재 역발견 모델은 인공지능 모델의 한 종류인 생성모델을 이용한 것으로, 생성모델은 이미지 및 음성 처리에 활발하게 활용되고 있는 기술이다. 예를 들어 수천 명의 얼굴들을 기계로 학습하게 해 새로운 사람의 얼굴을 생성해 내는 인공지능 기법이다.
연구팀은 이미지 생성에 주로 쓰이는 생성모델 기반의 인공지능 기법을 알려지지 않은 무기 고체 소재를 생성하는 데 최초로 적용했다. 특히 기존의 생성모델을 고체 소재에 적용하기 위해 역변환이 가능한 3차원 이미지 기반의 표현자를 도입함으로써 현재까지의 소재 역설계 모델의 한계를 극복했고, 이를 iMatGen(image-based Materials Generator) 이라 이름 지었다.
연구팀은 개발된 소재 역설계 기법을 새로운 바나듐 산화물 결정구조를 예측하는데 적용했다. 이 학습 과정에서 기존에 알려진 물질을 제외해 학습하더라도 제외된 물질들을 역으로 재발견할 수 있음을 확인해 개발 모델의 타당성을 검증했다.
최종적으로 개발된 모델을 통해 학습된 연속 잠재공간을 다양한 방법으로 샘플링하고 역변환 함으로써 기존에 존재하지 않는 전혀 새로운 바나듐 산화물 결정구조를 예측할 수 있었다.
정유성 교수는 “이번 연구는 원하는 물성을 갖는 무기 고체 소재를 역으로 설계하는 방법을 데이터 기반 기계학습으로 최초로 보인 예로, 향후 다양한 응용 분야의 신소재 개발에 도움을 줄 수 있을 것으로 기대한다”라고 말했다.
이번 연구 성과는 한국연구재단, 산업통상자원부 산하 에너지기술평가원, 그리고 KISTI의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 개발된 소재 역설계 모델
2019.10.07 조회수 13026
정유성 교수, 인공지능을 통한 소재 역설계 기술 개발
〈 정유성 교수, 노주환 박사과정〉
우리 대학 EEWS대학원/생명화학공학과 정유성 교수 연구팀이 인공지능을 활용해 원하는 물성을 갖는 신소재를 역설계하는 기술을 개발했다.
연구팀은 알고리즘을 통해 수만 개의 물질을 학습시킨 뒤 인공지능을 통해 원하는 물성을 갖는 소재를 역설계하는 방식으로 4종의 신물질을 발견했다. 향후 신소재 개발에 크게 이바지할 수 있을 것으로 기대된다.
노주환 박사과정이 1저자로 참여한 이번 연구 결과는 ‘셀 (Cell)’ 자매지 ‘매터(Matter)’ 10월 2일 자 온라인판에 출판됐다. (논문명 : Inverse Design of Solid State Materials via a Continuous Representation)
소재 연구의 궁극적인 목표는 원하는 물성을 갖는 신소재를 개발하는 것이다. 하지만 현재까지의 신소재 개발은 화학적 직관과 실험적 시행착오를 통한 방법 위주였기 때문에 개발 비용과 시간이 많이 들어 소재 개념화에서부터 상용화에 걸리는 시간이 평균 30년 정도 소요됐다.
기존의 소재 개발 과정은 소재를 시행착오를 통해 합성하고 난 후 물성을 측정해 만들어진 소재가 응용 목적에 맞는 소재인지를 평가하는 방식으로 개발됐다.
정 교수 연구팀은 인공지능 기술과 슈퍼컴퓨터 활용을 융합해 이러한 소재 개발을 기간을 크게 단축할 수 있는 새로운 소재 역설계 방법을 개발했다. 정 교수팀이 개발한 소재 역설계 방법은 기계(알고리즘)로 기존의 수만 개 물질과 그 물질들이 갖는 물성을 학습하게 한 후, 원하는 물성을 갖는 물질을 인공지능 기반 알고리즘이 역으로 생성하는 방식이다.
연구팀이 개발한 소재 역설계 방법은 기존의 컴퓨터 스크리닝을 통해 소재 설계를 가속화 하는 연구와도 차별성이 있다. 스크리닝 기반의 소재 발견 기술은 발견될 물질이 스크리닝 대상이 되는 물질 데이터베이스를 벗어날 수 없다는 한계를 가지고 있다. 따라서 데이터베이스에 존재하지 않는 새로운 형태의 소재를 발견하지 못한다는 단점이 있다.
연구팀이 개발한 신소재 역발견 모델은 인공지능 모델의 한 종류인 생성모델을 이용한 것으로, 생성모델은 이미지 및 음성 처리에 활발하게 활용되고 있는 기술이다. 예를 들어 수천 명의 얼굴들을 기계로 학습하게 해 새로운 사람의 얼굴을 생성해 내는 인공지능 기법이다.
연구팀은 이미지 생성에 주로 쓰이는 생성모델 기반의 인공지능 기법을 알려지지 않은 무기 고체 소재를 생성하는 데 최초로 적용했다. 특히 기존의 생성모델을 고체 소재에 적용하기 위해 역변환이 가능한 3차원 이미지 기반의 표현자를 도입함으로써 현재까지의 소재 역설계 모델의 한계를 극복했고, 이를 iMatGen(image-based Materials Generator) 이라 이름 지었다.
연구팀은 개발된 소재 역설계 기법을 새로운 바나듐 산화물 결정구조를 예측하는데 적용했다. 이 학습 과정에서 기존에 알려진 물질을 제외해 학습하더라도 제외된 물질들을 역으로 재발견할 수 있음을 확인해 개발 모델의 타당성을 검증했다.
최종적으로 개발된 모델을 통해 학습된 연속 잠재공간을 다양한 방법으로 샘플링하고 역변환 함으로써 기존에 존재하지 않는 전혀 새로운 바나듐 산화물 결정구조를 예측할 수 있었다.
정유성 교수는 “이번 연구는 원하는 물성을 갖는 무기 고체 소재를 역으로 설계하는 방법을 데이터 기반 기계학습으로 최초로 보인 예로, 향후 다양한 응용 분야의 신소재 개발에 도움을 줄 수 있을 것으로 기대한다”라고 말했다.
이번 연구 성과는 한국연구재단, 산업통상자원부 산하 에너지기술평가원, 그리고 KISTI의 지원을 통해 수행됐다.
□ 그림 설명
그림1. 개발된 소재 역설계 모델
2019.10.07 조회수 13026 생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24 조회수 25493
생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24 조회수 25493 주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03 조회수 24880
주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03 조회수 24880 조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 23612
조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 23612