-
 스마트 나노센서를 이용한 신약 효능 분석기술 개발
- 사람 몸속에서의 효능을 실시간 모니터링 할 수 있어 - - 나노-바이오-영상-분자화학 등이 융합 -
KAIST가 신약 효능을 분석하는 새로운 기법의 기술을 개발했다.
우리 학교 생명과학과 이상규 박사가 생체나노입자를 사람세포에 적용해 살아있는 세포에서 신약의 효능을 실시간으로 모니터링 하는 기술을 개발했다.
이 기술을 이용하면 사람 몸속에서도 신약의 효능을 보다 정확하게 파악할 수 있을 것으로 기대된다.
지금까지는 신약 후보물질을 몸속으로 투여하고 세포를 추출한 후 효과를 분석했다. 그러나 세포를 용해한 후 세포의 기능이 정지된 상태에서 분석함으로써 예상치 못했던 부작용으로 대부분의 후보물질이 탈락하게 된다. 이 때문에 엄청난 비용과 노력을 들이더라도 신약개발을 성공하기가 매우 어려웠다.
연구팀은 수많은 나노입자가 서로 연결되면 커다란 복합체를 형성할 수 있다는 아이디어에 착안했다. 나노입자를 세포 내부에 적용해 본 결과 실제로 살아있는 세포 안에서 나노입자 간의 결합을 통해 복합체가 빠르게 형성되는 것을 확인했다.
형성된 복합체는 나노센서 역할을 하게 돼 약물이 세포 내에 투여되는 과정에서 약물 타겟과의 결합을 실시간으로 관찰할 수 있었다.
연구팀은 이 나노센서 기술을 ‘스마트한 눈(InCell SMART-i)’이라고 명명했다. 살아있는 세포 안에서 일어나는 신약의 효능작용을 한 눈에 볼 수 있기 때문이다.
이상규 박사는 “이 기술은 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술로 신약개발에 효과적으로 적용 가능한 매우 중요한 기술”이라며 “신약물질의 직접 개발을 원하는 기업으로 기술이 이전돼 상용화가 멀지 않았다”고 말했다.
한편, KAIST 생명과학과 이상규 박사와 리온즈신약연구소(주) 김태국 박사가 개발한 이 기술은 최근 세계적인 화학지인 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 지 9월호에 주목받는 논문(Hot Paper)으로 선정됐다.
그림1. 사람 세포 내에 도입된 스마트 나노 센서가 약물과 약물 타겟 간의 결합에 따라 세포 내에 스팟(같은 나노클러스터)을 형성하고 이를 실시간으로 탐지해 낼 수 있는 원천기술의 모식도
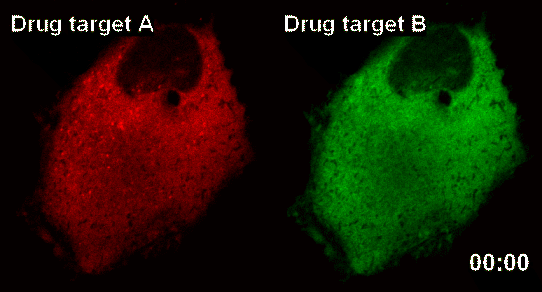
그림2. 약물타겟 A 또는 B가 발현되어 있는 사람세포에 약물을 처리하면 세포 내에서 약물과 약물타겟이 서서히 결합되면서 스마트 나노센서에 의해 이러한 스팟 (같은 나노클러스터) 형태로 실시간으로 센싱-감지된다. 따라서 살아 있는 사람세포 안에서 신약의 효능작용을 실시간으로 마치 비디오를 보는 것처럼 라이브로 모니터링 할 수 있는 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술이다.
스마트 나노센서를 이용한 신약 효능 분석기술 개발
- 사람 몸속에서의 효능을 실시간 모니터링 할 수 있어 - - 나노-바이오-영상-분자화학 등이 융합 -
KAIST가 신약 효능을 분석하는 새로운 기법의 기술을 개발했다.
우리 학교 생명과학과 이상규 박사가 생체나노입자를 사람세포에 적용해 살아있는 세포에서 신약의 효능을 실시간으로 모니터링 하는 기술을 개발했다.
이 기술을 이용하면 사람 몸속에서도 신약의 효능을 보다 정확하게 파악할 수 있을 것으로 기대된다.
지금까지는 신약 후보물질을 몸속으로 투여하고 세포를 추출한 후 효과를 분석했다. 그러나 세포를 용해한 후 세포의 기능이 정지된 상태에서 분석함으로써 예상치 못했던 부작용으로 대부분의 후보물질이 탈락하게 된다. 이 때문에 엄청난 비용과 노력을 들이더라도 신약개발을 성공하기가 매우 어려웠다.
연구팀은 수많은 나노입자가 서로 연결되면 커다란 복합체를 형성할 수 있다는 아이디어에 착안했다. 나노입자를 세포 내부에 적용해 본 결과 실제로 살아있는 세포 안에서 나노입자 간의 결합을 통해 복합체가 빠르게 형성되는 것을 확인했다.
형성된 복합체는 나노센서 역할을 하게 돼 약물이 세포 내에 투여되는 과정에서 약물 타겟과의 결합을 실시간으로 관찰할 수 있었다.
연구팀은 이 나노센서 기술을 ‘스마트한 눈(InCell SMART-i)’이라고 명명했다. 살아있는 세포 안에서 일어나는 신약의 효능작용을 한 눈에 볼 수 있기 때문이다.
이상규 박사는 “이 기술은 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술로 신약개발에 효과적으로 적용 가능한 매우 중요한 기술”이라며 “신약물질의 직접 개발을 원하는 기업으로 기술이 이전돼 상용화가 멀지 않았다”고 말했다.
한편, KAIST 생명과학과 이상규 박사와 리온즈신약연구소(주) 김태국 박사가 개발한 이 기술은 최근 세계적인 화학지인 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 지 9월호에 주목받는 논문(Hot Paper)으로 선정됐다.
그림1. 사람 세포 내에 도입된 스마트 나노 센서가 약물과 약물 타겟 간의 결합에 따라 세포 내에 스팟(같은 나노클러스터)을 형성하고 이를 실시간으로 탐지해 낼 수 있는 원천기술의 모식도
그림2. 약물타겟 A 또는 B가 발현되어 있는 사람세포에 약물을 처리하면 세포 내에서 약물과 약물타겟이 서서히 결합되면서 스마트 나노센서에 의해 이러한 스팟 (같은 나노클러스터) 형태로 실시간으로 센싱-감지된다. 따라서 살아 있는 사람세포 안에서 신약의 효능작용을 실시간으로 마치 비디오를 보는 것처럼 라이브로 모니터링 할 수 있는 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술이다.
2011.09.05
조회수 19594
-
 가상세포 이용해 병원균 잡는 항생제 개발
교육과학기술부는 미래기반기술개발사업(시스템생물학 연구)으로 지원한 우리학교 이상엽 교수팀(전남대 이준행교수, 생명(연), 화학(연) 공동연구)이 항생제에 내성을 가진 병원균 퇴치를 위해 시스템생물학을 기반으로 한 신약발굴 방법론을 개발했다고 밝혔다.
이 교수팀은 병원균이 항생제의 오남용으로 인해 치유가 쉽지 않은 점을 감안하여 내성 병원균의 가상세포를 만들어서 이에 대한 특성을 분석하여 제어하는 방법으로 효과를 입증했다.
이번 연구의 대상은 오염된 어패류에 의해 감염되는 패혈증의 병원균인 비브리오 불니피쿠스(Vibrio vulnificus, 이하 비브리오균) 중 내성균 2개이며, 이에 대한 게놈정보와 생물정보를 토대로 가상세포를 구축하였다.
이러한 가상세포가 생존하기 위해 필요한 화학물질은 193개로 분석되었으며, 이중에서 결정적 역할을 수행하는 5개의 화학물질을 추출하였으며, 이에 관여하는 유전자를 제거함으로써 내성 비브리오균의 성장이 억제되는 효과를 증명하였다.
이 교수팀의 연구결과는 올해 1월 18일 세계적 권위의 네이처 자매지인 ‘분자시스템생물학 (Molecular Systems Biology)지’에 논문으로 게재되어 세계적으로도 연구의 우수성이 인정되었다.
이러한 시스템생물학 기법에 근거한 신약발굴 방법론은 다른 내성 병원균은 물론 다양한 인간 질병에도 적용할 수 있는 토대를 마련한 것으로 기대된다.
가상세포 이용해 병원균 잡는 항생제 개발
교육과학기술부는 미래기반기술개발사업(시스템생물학 연구)으로 지원한 우리학교 이상엽 교수팀(전남대 이준행교수, 생명(연), 화학(연) 공동연구)이 항생제에 내성을 가진 병원균 퇴치를 위해 시스템생물학을 기반으로 한 신약발굴 방법론을 개발했다고 밝혔다.
이 교수팀은 병원균이 항생제의 오남용으로 인해 치유가 쉽지 않은 점을 감안하여 내성 병원균의 가상세포를 만들어서 이에 대한 특성을 분석하여 제어하는 방법으로 효과를 입증했다.
이번 연구의 대상은 오염된 어패류에 의해 감염되는 패혈증의 병원균인 비브리오 불니피쿠스(Vibrio vulnificus, 이하 비브리오균) 중 내성균 2개이며, 이에 대한 게놈정보와 생물정보를 토대로 가상세포를 구축하였다.
이러한 가상세포가 생존하기 위해 필요한 화학물질은 193개로 분석되었으며, 이중에서 결정적 역할을 수행하는 5개의 화학물질을 추출하였으며, 이에 관여하는 유전자를 제거함으로써 내성 비브리오균의 성장이 억제되는 효과를 증명하였다.
이 교수팀의 연구결과는 올해 1월 18일 세계적 권위의 네이처 자매지인 ‘분자시스템생물학 (Molecular Systems Biology)지’에 논문으로 게재되어 세계적으로도 연구의 우수성이 인정되었다.
이러한 시스템생물학 기법에 근거한 신약발굴 방법론은 다른 내성 병원균은 물론 다양한 인간 질병에도 적용할 수 있는 토대를 마련한 것으로 기대된다.
2011.01.19
조회수 16868
-
 심장질환 원인신호전달메커니즘 규명
- 신약개발 및 심장질환 응용연구의 중요한 발판 마련
- IT와 BT를 융합한 시스템생물학 연구 통해 규명
우리학교 바이오및뇌공학과 조광현 교수팀과 생명과학과 허원도 교수팀이 시스템생물학 융합연구를 통해 심장질환 원인신호전달경로의 숨겨진 메커니즘을 규명했다.
심근비대증은 다양한 병인에 의해 심근세포가 비대해지는 병리학적 현상으로써 심부전증과 부정맥 등을 수반하는 주요 심장질환이다.
칼시뉴린-엔팻(calcineurin-NFAT) 신호전달경로는 이러한 심근비대증의 유발에 매우 중요한 역할을 하는 것으로 알려져 있다.
하지만 이 신호전달경로의 주요 조절단백질로 알려진 알캔(RCAN1)의 기능에 대해 많은 논쟁이 이어져 왔고 현재까지 그 구체적인 조절메커니즘이 밝혀지지 않았다.
조광현 교수 융합연구팀은 이러한 복잡한 현상에 대해 수학 모델링과 대규모 컴퓨터시뮬레이션, 그리고 단일세포 분자 이미징 기술을 동원한 시스템생물학 융합연구를 통해 어크(ERK)와 지에스케이(GSK3)로 구성된 스위칭 회로가 칼시뉴린-엔팻 신호전달경로를 조절한다는 것을 새롭게 규명했다.
특히 이 연구에서는 알캔이 세포내 농도가 낮을 때 칼시뉴린(calcineurin)의 기능을 저해하는 억제자로서 기능하지만, 그 농도가 증가하면 어크와 지에스케이에 의한 크로스토크를 통해 칼시뉴린 신호를 오히려 증가시키는 촉진자로서 기능 하도록 세포내 조절회로가 진화적으로 설계되어 있음을 최초로 밝혔다.
지금까지 많은 연구에서 알캔의 상반된 신호조절 역할이 보고되어 학계에서는 과연 무엇이 진실인가에 관한 논쟁이 이어졌다.
또한, 어떻게 동일한 분자가 그와 같이 서로 다른 기능을 보이는 것인지, 이를 유발하는 근본적인 메커니즘은 과연 무엇인지 등이 모두 수수께끼로 남아 있었다.
이번 연구를 통해 학계의 이러한 오랜 질문에 대한 해답이 제시됐으며, 알캔과 칼시뉴린-엔팻 신호전달경로의 근원적인 조절메커니즘이 시스템차원에서 최초로 규명됨으로써 앞으로 이를 표적으로 하는 신약개발 및 관련 심장질환 응용연구의 중요한 발판을 마련하게 되었다.
또한 기존의 실험적 접근만으로는 해결할 수 없는 복잡한 생명현상을 대상으로 IT와 BT의 융합연구인 생체시스템모델링 및 바이오시뮬레이션 연구를 통해 새로운 해결책을 찾을 수 있는 가능성을 제시하게 됐다.
이 연구는 교육과학기술부가 지원하는 한국연구재단의 기초연구실육성사업과 도약연구사업, 그리고 칼슘대사시스템생물학사업의 일환으로 수행됐으며, 연구 결과는 <저널오브셀사이언스(Journal of Cell Science)>의 표지논문으로 선정되어 2011년 1월 1일자(온라인판은 2010년 12월 13일자)에 게재된다.
심장질환 원인신호전달메커니즘 규명
- 신약개발 및 심장질환 응용연구의 중요한 발판 마련
- IT와 BT를 융합한 시스템생물학 연구 통해 규명
우리학교 바이오및뇌공학과 조광현 교수팀과 생명과학과 허원도 교수팀이 시스템생물학 융합연구를 통해 심장질환 원인신호전달경로의 숨겨진 메커니즘을 규명했다.
심근비대증은 다양한 병인에 의해 심근세포가 비대해지는 병리학적 현상으로써 심부전증과 부정맥 등을 수반하는 주요 심장질환이다.
칼시뉴린-엔팻(calcineurin-NFAT) 신호전달경로는 이러한 심근비대증의 유발에 매우 중요한 역할을 하는 것으로 알려져 있다.
하지만 이 신호전달경로의 주요 조절단백질로 알려진 알캔(RCAN1)의 기능에 대해 많은 논쟁이 이어져 왔고 현재까지 그 구체적인 조절메커니즘이 밝혀지지 않았다.
조광현 교수 융합연구팀은 이러한 복잡한 현상에 대해 수학 모델링과 대규모 컴퓨터시뮬레이션, 그리고 단일세포 분자 이미징 기술을 동원한 시스템생물학 융합연구를 통해 어크(ERK)와 지에스케이(GSK3)로 구성된 스위칭 회로가 칼시뉴린-엔팻 신호전달경로를 조절한다는 것을 새롭게 규명했다.
특히 이 연구에서는 알캔이 세포내 농도가 낮을 때 칼시뉴린(calcineurin)의 기능을 저해하는 억제자로서 기능하지만, 그 농도가 증가하면 어크와 지에스케이에 의한 크로스토크를 통해 칼시뉴린 신호를 오히려 증가시키는 촉진자로서 기능 하도록 세포내 조절회로가 진화적으로 설계되어 있음을 최초로 밝혔다.
지금까지 많은 연구에서 알캔의 상반된 신호조절 역할이 보고되어 학계에서는 과연 무엇이 진실인가에 관한 논쟁이 이어졌다.
또한, 어떻게 동일한 분자가 그와 같이 서로 다른 기능을 보이는 것인지, 이를 유발하는 근본적인 메커니즘은 과연 무엇인지 등이 모두 수수께끼로 남아 있었다.
이번 연구를 통해 학계의 이러한 오랜 질문에 대한 해답이 제시됐으며, 알캔과 칼시뉴린-엔팻 신호전달경로의 근원적인 조절메커니즘이 시스템차원에서 최초로 규명됨으로써 앞으로 이를 표적으로 하는 신약개발 및 관련 심장질환 응용연구의 중요한 발판을 마련하게 되었다.
또한 기존의 실험적 접근만으로는 해결할 수 없는 복잡한 생명현상을 대상으로 IT와 BT의 융합연구인 생체시스템모델링 및 바이오시뮬레이션 연구를 통해 새로운 해결책을 찾을 수 있는 가능성을 제시하게 됐다.
이 연구는 교육과학기술부가 지원하는 한국연구재단의 기초연구실육성사업과 도약연구사업, 그리고 칼슘대사시스템생물학사업의 일환으로 수행됐으며, 연구 결과는 <저널오브셀사이언스(Journal of Cell Science)>의 표지논문으로 선정되어 2011년 1월 1일자(온라인판은 2010년 12월 13일자)에 게재된다.
2010.12.20
조회수 16963
-
 이효철 교수팀, 물에 녹은단백질 모양 변화 실시간 관찰 성공
- 관련 논문, 9월 22일(일)자 네이처 메서드(Nature Methods)誌 게재- 단백질의 작동메커니즘 규명에 중요한 도구 역할 및 신약개발에도 큰 도움 줄 것으로 기대
KAIST(총장 서남표) 화학과 이효철(李效澈, 36) 교수팀이 ‘물에서 변하는 단백질 분자구조를 실시간으로 규명’ 하는데 성공했다. 관련 논문은 네이처 자매지인 네이처 메서드(Nature Methods)誌 9월 22일자 온라인 판에 게재됐고 10월호에 출판될 예정이다.
논문의 제목은 “시간분해 엑스선 산란을 이용한 용액상의 단백질의 구조동역학 추적(Tracking the structural dynamics of proteins in solution using time-resolved wide-angle X-ray scattering)”으로 온라인에 게재되는 논문들 중에서도 특히 주목받는 하이라이트 논문으로 소개될 예정이다. 李 교수는 이 논문의 교신저자다.
이번 연구결과는 李 교수팀의 집념의 산물이라 할 수 있다. 李 교수팀은 지난 2005년 5월, 소금처럼 딱딱하게 고체상으로 굳어 있는 상태에서의 단백질의 안정적인 구조만을 볼 수 있는 기존의 방법을 시간분해 엑스선 결정법으로 발전시켜, 정지되어 있는 단백질의 구조뿐 만 아니라 움직이는 단백질의 동영상을 촬영하는데 성공했다. 관련 논문은 미국 국립과학원회보(PNAS, Proceedings of National Academy of Science)에 발표되었으며, 학계의 큰 주목을 받았다.
그러나 이 방법으로도 해결할 수 없는 치명적인 문제는 우리 몸에서 작용하는 일반적인 단백질은 고체상으로 있지 않고 물에 녹아있는 용액상태라는 점이다. 마치 고체 소금이 물에 녹아 소금물이 되는 것과 같은 원리다. 물은 인간의 몸의 약 70% 이상을 차지하고 있고 생명 유지에 필수적인 단백질들은 물에 녹아 있는 상태로 존재한다고 볼 수 있다. 따라서 단백질이 어떻게 기능을 발휘하는 지를 실시간으로 관측하기 위해서는 물에 녹아 있는 단백질 분자의 모양 변화를 실시간으로 추적할 수 있는 기술이 필요하다.
이러한 목표를 향한 첫 열매로 물에 녹아 있는 간단한 유기분자의 구조변화를 실시간 측정하는 데 성공하였으며, 관련 연구논문이 2005년 7월 사이언스(Science)誌에 발표된 바 있다. 당시 이 연구결과는 용액상에서 분자의 움직임을 실시간 추적할 수 있다는 점 때문에 많은 관심을 불러 일으켰는데, 李 교수는 그 기술을 더욱 발전시키면 단백질에도 응용 가능할 것으로 전망했다. 그러나 일반적으로 단백질은 그 당시 성공한 유기분자보다 적어도 1,000배 정도 크고 구조가 훨씬 더 복잡할 뿐 아니라 훨씬 적은 양으로 존재하기 때문에 물에 녹아 있는 단백질에서도 성공할 수 있다는 것에는 많은 과학자들이 회의적으로 생각했다.
이번 네이처 메서드誌에 발표한 연구결과는 그러한 부정적인 생각을 깨고 기존에 성공한 유기분자보다 ‘1,000배 더 큰 단백질 분자가 물에 녹아 있을 때에 이들의 3차원 구조변화를 실시간으로 관측하는데 성공’한 획기적인 연구성과다. 논문에서는 3가지 종류의 단백질에 대한 연구결과를 발표했는데, 우리 몸에서 산소를 이동하는데 중요한 헤모글로빈 단백질과, 근육에서의 산소공급에 관여하는 미오글로빈 단백질 등이다. 이 외에도 단백질은 주로 접혀있어 특정한 구조를 형성하는데 환경이 바뀌면 이 구조가 풀리게 된다. 풀려 있는 단백질은 일반적으로 제 역할을 할 수 없어 이러한 단백질의 접힘-풀림 현상을 이해하는 것은 매우 중요한데 씨토크롬씨라는 단백질이 풀린 상태에서 접히는 과정도 실시간으로 추적하는데 성공하였다.
이 새로운 기술을 사용하면 물에서 움직이는 단백질의 동영상을 촬영할 수도 있어 단백질의 작동메커니즘을 밝히는 데에 중요한 도구가 될 것이며, 앞으로 신약개발을 하는 데에도 큰 도움을 줄 것으로 기대된다. 또한 이 기술은 단백질은 물론이고 나노물질에도 응용이 가능하므로 BT뿐만 아니라 NT분야에도 기여할 수 있을 것으로 전망된다.
이 연구는 교육과학기술부의 창의적연구진흥사업의 연구비 지원으로 진행되었다. 연구결과는 유럽연합방사광가속기센터에서 측정되었으며, 李 교수의 주도하에 이뤄진 국제적인 공동연구의 성과다.
李 교수는 “현재 포항에 있는 제3세대 가속기에 이어 한국에서도 차세대 광원으로 건설이 논의되고 있는 제4세대 방사광가속기(XFEL)가 성공적으로 가동되면, 현재 발표된 데이터보다 적어도 1,000배정도 더 좋은 데이터를 얻을 수 있을 것으로 예상된다.”고 밝혔다.
<이효철 교수 프로필>
■ 학 력
1990 경남과학고 2년 수료, KAIST 화학과 학사과정 입학
1994 KAIST 화학과 학사과정 졸업
1994 Caltech(California Institute of Technology) 박사과정 입학
2001 Caltech 졸업(박사)
2001 시카고 대학 박사 후 연구원(Post Doc.)
2003.8.1-2007.2.28 KAIST 화학과 조교수 2007.3.1-현재 KAIST 화학과 부교수
■ 수상경력
2006 젊은 과학자상(과학기술부/한국과학기술한림원)
2006 과학기술우수논문상(한국과학기술단체총연합회)
2006 KAIST 학술상 2001-2003 美國 대먼 러년 암재단(Damon Runyon Cancer Research Foundation)펠로우쉽
(설명) 시간분해 엑스선 산란의 개념을 예술적으로 표현한 그림
이효철 교수팀, 물에 녹은단백질 모양 변화 실시간 관찰 성공
- 관련 논문, 9월 22일(일)자 네이처 메서드(Nature Methods)誌 게재- 단백질의 작동메커니즘 규명에 중요한 도구 역할 및 신약개발에도 큰 도움 줄 것으로 기대
KAIST(총장 서남표) 화학과 이효철(李效澈, 36) 교수팀이 ‘물에서 변하는 단백질 분자구조를 실시간으로 규명’ 하는데 성공했다. 관련 논문은 네이처 자매지인 네이처 메서드(Nature Methods)誌 9월 22일자 온라인 판에 게재됐고 10월호에 출판될 예정이다.
논문의 제목은 “시간분해 엑스선 산란을 이용한 용액상의 단백질의 구조동역학 추적(Tracking the structural dynamics of proteins in solution using time-resolved wide-angle X-ray scattering)”으로 온라인에 게재되는 논문들 중에서도 특히 주목받는 하이라이트 논문으로 소개될 예정이다. 李 교수는 이 논문의 교신저자다.
이번 연구결과는 李 교수팀의 집념의 산물이라 할 수 있다. 李 교수팀은 지난 2005년 5월, 소금처럼 딱딱하게 고체상으로 굳어 있는 상태에서의 단백질의 안정적인 구조만을 볼 수 있는 기존의 방법을 시간분해 엑스선 결정법으로 발전시켜, 정지되어 있는 단백질의 구조뿐 만 아니라 움직이는 단백질의 동영상을 촬영하는데 성공했다. 관련 논문은 미국 국립과학원회보(PNAS, Proceedings of National Academy of Science)에 발표되었으며, 학계의 큰 주목을 받았다.
그러나 이 방법으로도 해결할 수 없는 치명적인 문제는 우리 몸에서 작용하는 일반적인 단백질은 고체상으로 있지 않고 물에 녹아있는 용액상태라는 점이다. 마치 고체 소금이 물에 녹아 소금물이 되는 것과 같은 원리다. 물은 인간의 몸의 약 70% 이상을 차지하고 있고 생명 유지에 필수적인 단백질들은 물에 녹아 있는 상태로 존재한다고 볼 수 있다. 따라서 단백질이 어떻게 기능을 발휘하는 지를 실시간으로 관측하기 위해서는 물에 녹아 있는 단백질 분자의 모양 변화를 실시간으로 추적할 수 있는 기술이 필요하다.
이러한 목표를 향한 첫 열매로 물에 녹아 있는 간단한 유기분자의 구조변화를 실시간 측정하는 데 성공하였으며, 관련 연구논문이 2005년 7월 사이언스(Science)誌에 발표된 바 있다. 당시 이 연구결과는 용액상에서 분자의 움직임을 실시간 추적할 수 있다는 점 때문에 많은 관심을 불러 일으켰는데, 李 교수는 그 기술을 더욱 발전시키면 단백질에도 응용 가능할 것으로 전망했다. 그러나 일반적으로 단백질은 그 당시 성공한 유기분자보다 적어도 1,000배 정도 크고 구조가 훨씬 더 복잡할 뿐 아니라 훨씬 적은 양으로 존재하기 때문에 물에 녹아 있는 단백질에서도 성공할 수 있다는 것에는 많은 과학자들이 회의적으로 생각했다.
이번 네이처 메서드誌에 발표한 연구결과는 그러한 부정적인 생각을 깨고 기존에 성공한 유기분자보다 ‘1,000배 더 큰 단백질 분자가 물에 녹아 있을 때에 이들의 3차원 구조변화를 실시간으로 관측하는데 성공’한 획기적인 연구성과다. 논문에서는 3가지 종류의 단백질에 대한 연구결과를 발표했는데, 우리 몸에서 산소를 이동하는데 중요한 헤모글로빈 단백질과, 근육에서의 산소공급에 관여하는 미오글로빈 단백질 등이다. 이 외에도 단백질은 주로 접혀있어 특정한 구조를 형성하는데 환경이 바뀌면 이 구조가 풀리게 된다. 풀려 있는 단백질은 일반적으로 제 역할을 할 수 없어 이러한 단백질의 접힘-풀림 현상을 이해하는 것은 매우 중요한데 씨토크롬씨라는 단백질이 풀린 상태에서 접히는 과정도 실시간으로 추적하는데 성공하였다.
이 새로운 기술을 사용하면 물에서 움직이는 단백질의 동영상을 촬영할 수도 있어 단백질의 작동메커니즘을 밝히는 데에 중요한 도구가 될 것이며, 앞으로 신약개발을 하는 데에도 큰 도움을 줄 것으로 기대된다. 또한 이 기술은 단백질은 물론이고 나노물질에도 응용이 가능하므로 BT뿐만 아니라 NT분야에도 기여할 수 있을 것으로 전망된다.
이 연구는 교육과학기술부의 창의적연구진흥사업의 연구비 지원으로 진행되었다. 연구결과는 유럽연합방사광가속기센터에서 측정되었으며, 李 교수의 주도하에 이뤄진 국제적인 공동연구의 성과다.
李 교수는 “현재 포항에 있는 제3세대 가속기에 이어 한국에서도 차세대 광원으로 건설이 논의되고 있는 제4세대 방사광가속기(XFEL)가 성공적으로 가동되면, 현재 발표된 데이터보다 적어도 1,000배정도 더 좋은 데이터를 얻을 수 있을 것으로 예상된다.”고 밝혔다.
<이효철 교수 프로필>
■ 학 력
1990 경남과학고 2년 수료, KAIST 화학과 학사과정 입학
1994 KAIST 화학과 학사과정 졸업
1994 Caltech(California Institute of Technology) 박사과정 입학
2001 Caltech 졸업(박사)
2001 시카고 대학 박사 후 연구원(Post Doc.)
2003.8.1-2007.2.28 KAIST 화학과 조교수 2007.3.1-현재 KAIST 화학과 부교수
■ 수상경력
2006 젊은 과학자상(과학기술부/한국과학기술한림원)
2006 과학기술우수논문상(한국과학기술단체총연합회)
2006 KAIST 학술상 2001-2003 美國 대먼 러년 암재단(Damon Runyon Cancer Research Foundation)펠로우쉽
(설명) 시간분해 엑스선 산란의 개념을 예술적으로 표현한 그림
2008.09.22
조회수 29810
-
 이도헌교수팀, 생물정보학적 연구를 통한 천식 발병 후보 유전자 발견
바이오및뇌공학과 이도헌 교수와 박사과정 황소현씨가 생물정보학 기법을 이용해 기존의 분자생물학적 연구 및 실험 결과에 나타난 천식 관련 단백질들의 상호작용을 분석, 천식 유발에 관여하는 후보 유전자군을 발굴했다.
이 연구결과는 국제학술지 "이론생물학저널(Journal of Theoretical Biology)"에 발표됐으며 기존 연구자료를 새로운 생물정보학 기법으로 분석해 신약 표적유전자를 발굴한 것이어서 신약연구 효율성 향상에 기여할 것으로 전망된다.
연구진은 세계 각국의 분자생물학적 연구자료가 담겨 있는 데이터베이스(OMIM, GEO)에서 천식과 관련 있는 단백질 606개를 찾아내고 이를 시스템 수준에서 연구하기 위해 생물정보학 기술을 이용해 단백질 상호작용 네트워크를 구성했다.
이는 단백질 사이의 상호작용을 연결선으로 표현한 것으로 여러 개의 단백질과 동시에 상호작용을 하는 단백질이 천식유발 단백질 네트워크에서 중요한 역할을 하는 "허브"로 간주된다.
질병과 관련된 질병유전자를 찾기 위해서 기존의 분자생물학적 연구를 통해 몇 가지 유전자들이 밝혀졌지만, 여러 가지 유전적인 요인과 환경적인 요인의 복합적인 작용으로 인해 나타나는 대부분의 복합 질병의 경우는 기존의 분자생물학적인 연구만으로 관련 유전자들을 찾아내기가 어렵다.
이도헌 교수는 "이런 복합적인 질병에서 중요한 역할을 하는 유전자를 찾아내려면 한 두 유전자와 질병의 관계를 조사하기 보다는 그 질병과 관련된 여러 유전자들의 연관성을 살펴보는 시스템 수준의 연구가 필요하다"고 말했다.
이도헌교수팀, 생물정보학적 연구를 통한 천식 발병 후보 유전자 발견
바이오및뇌공학과 이도헌 교수와 박사과정 황소현씨가 생물정보학 기법을 이용해 기존의 분자생물학적 연구 및 실험 결과에 나타난 천식 관련 단백질들의 상호작용을 분석, 천식 유발에 관여하는 후보 유전자군을 발굴했다.
이 연구결과는 국제학술지 "이론생물학저널(Journal of Theoretical Biology)"에 발표됐으며 기존 연구자료를 새로운 생물정보학 기법으로 분석해 신약 표적유전자를 발굴한 것이어서 신약연구 효율성 향상에 기여할 것으로 전망된다.
연구진은 세계 각국의 분자생물학적 연구자료가 담겨 있는 데이터베이스(OMIM, GEO)에서 천식과 관련 있는 단백질 606개를 찾아내고 이를 시스템 수준에서 연구하기 위해 생물정보학 기술을 이용해 단백질 상호작용 네트워크를 구성했다.
이는 단백질 사이의 상호작용을 연결선으로 표현한 것으로 여러 개의 단백질과 동시에 상호작용을 하는 단백질이 천식유발 단백질 네트워크에서 중요한 역할을 하는 "허브"로 간주된다.
질병과 관련된 질병유전자를 찾기 위해서 기존의 분자생물학적 연구를 통해 몇 가지 유전자들이 밝혀졌지만, 여러 가지 유전적인 요인과 환경적인 요인의 복합적인 작용으로 인해 나타나는 대부분의 복합 질병의 경우는 기존의 분자생물학적인 연구만으로 관련 유전자들을 찾아내기가 어렵다.
이도헌 교수는 "이런 복합적인 질병에서 중요한 역할을 하는 유전자를 찾아내려면 한 두 유전자와 질병의 관계를 조사하기 보다는 그 질병과 관련된 여러 유전자들의 연관성을 살펴보는 시스템 수준의 연구가 필요하다"고 말했다.
2008.07.01
조회수 22645
-
 신약개발 원천기술 사이언스지에 발표
자석 이용 신약 개발, 마술같은 기술 "MAGIC" 명명
살아있는 세포내에서 다양한 물질결합 실시간 측정
생명과학과 김태국(金泰國, 41) 교수팀이 (주)씨지케이(CGK, 대표이사 정연철)와 공동으로 개발한 새로운 신약개발 원천기술이 7월1일(금)자 사이언스 誌에 발표됐다.
“살아 있는 세포에서 분자 간 상호작용을 검출하는 자성 나노프로브 기술(A magnetic nanoprobe technology for detecting molecular interactions in live cells)“이라는 제목으로 발표된 이 연구결과는 마술과 같은 기술이라 하여 "MAGIC"으로 명명됐다.
물질의 한쪽 끝에 자성체를 붙여 세포에 넣어준 뒤 자석을 대면 결합된 다른 물질이 같이 끌려나온다는 평범한 원리를 세포내에 적용한 이 기술은 살아있는 세포 내에서 다양한 물질의 결합을 실시간으로 측정 가능해 곧바로 신약개발에 응용될 수 있다. 이미 병원에서도 면역억제제로 사용하고 있는 약물에 같은 실험을 수행하여 사람 세포 내에서 이 약물에 결합한다고 알려진 단백질이 매우 선택적으로 자석에 딸려오는 현상을 실시간으로 확인했다.
金 교수는 "MAGIC 기술은 기존에 생체 내에서의 역할이 명확히 밝혀지지 않은 다양한 약물의 표적 분자를 쉽게 찾을 수 있을 뿐만 아니라, 사람 세포내에서 계속 조절 변화되는 바이오프로그램을 실시간으로 모니터하고 유익하게 재프로그래밍도 할 수 있는 혁신적인 기술"이라며, "특히 신약개발이라는 망망대해에서 더 이상 그물을 치고 기다릴 필요가 없는 셈"이라며 이 기술의 의미를 함축적으로 설명했다.
함께 연구에 참여한 CGK 정연철 대표는 "MAGIC 기술은 그간 발표된 어떤 기술보다 신약개발을 혁신적으로 앞당길 수 있는 상업화에 가장 근접한 기술"이며, "이미 항암제를 포함한 두 종의 신약 후보물질을 찾은 상태이다. 내년까지는 동물 실험을 마칠 것"이라는 계획을 발표했다. 또한 "이미 미국의 회사로부터 이 기술의 사업화를 위한 조인트벤처 설립을 제안 받았으며, 내부적으로 검토중"이라고 밝혔다.
金 교수는 "최근 황우석 교수의 줄기세포 치료법와 더불어 신약 치료법의 원천기술을 국내에 확보하여 확고한 바이오기술의 토대를 확립했다는 것이 무엇보다 의미 있다" 며, "MAGIC 원천기술을 비롯해서 앞으로도 기초연구와 바이오산업을 보다 효과적으로 접목, 국내 산업의 성장동력을 마련하기 위해 열심히 노력 하겠다"는 각오를 밝혔다.
신약개발 원천기술 사이언스지에 발표
자석 이용 신약 개발, 마술같은 기술 "MAGIC" 명명
살아있는 세포내에서 다양한 물질결합 실시간 측정
생명과학과 김태국(金泰國, 41) 교수팀이 (주)씨지케이(CGK, 대표이사 정연철)와 공동으로 개발한 새로운 신약개발 원천기술이 7월1일(금)자 사이언스 誌에 발표됐다.
“살아 있는 세포에서 분자 간 상호작용을 검출하는 자성 나노프로브 기술(A magnetic nanoprobe technology for detecting molecular interactions in live cells)“이라는 제목으로 발표된 이 연구결과는 마술과 같은 기술이라 하여 "MAGIC"으로 명명됐다.
물질의 한쪽 끝에 자성체를 붙여 세포에 넣어준 뒤 자석을 대면 결합된 다른 물질이 같이 끌려나온다는 평범한 원리를 세포내에 적용한 이 기술은 살아있는 세포 내에서 다양한 물질의 결합을 실시간으로 측정 가능해 곧바로 신약개발에 응용될 수 있다. 이미 병원에서도 면역억제제로 사용하고 있는 약물에 같은 실험을 수행하여 사람 세포 내에서 이 약물에 결합한다고 알려진 단백질이 매우 선택적으로 자석에 딸려오는 현상을 실시간으로 확인했다.
金 교수는 "MAGIC 기술은 기존에 생체 내에서의 역할이 명확히 밝혀지지 않은 다양한 약물의 표적 분자를 쉽게 찾을 수 있을 뿐만 아니라, 사람 세포내에서 계속 조절 변화되는 바이오프로그램을 실시간으로 모니터하고 유익하게 재프로그래밍도 할 수 있는 혁신적인 기술"이라며, "특히 신약개발이라는 망망대해에서 더 이상 그물을 치고 기다릴 필요가 없는 셈"이라며 이 기술의 의미를 함축적으로 설명했다.
함께 연구에 참여한 CGK 정연철 대표는 "MAGIC 기술은 그간 발표된 어떤 기술보다 신약개발을 혁신적으로 앞당길 수 있는 상업화에 가장 근접한 기술"이며, "이미 항암제를 포함한 두 종의 신약 후보물질을 찾은 상태이다. 내년까지는 동물 실험을 마칠 것"이라는 계획을 발표했다. 또한 "이미 미국의 회사로부터 이 기술의 사업화를 위한 조인트벤처 설립을 제안 받았으며, 내부적으로 검토중"이라고 밝혔다.
金 교수는 "최근 황우석 교수의 줄기세포 치료법와 더불어 신약 치료법의 원천기술을 국내에 확보하여 확고한 바이오기술의 토대를 확립했다는 것이 무엇보다 의미 있다" 며, "MAGIC 원천기술을 비롯해서 앞으로도 기초연구와 바이오산업을 보다 효과적으로 접목, 국내 산업의 성장동력을 마련하기 위해 열심히 노력 하겠다"는 각오를 밝혔다.
2005.07.01
조회수 22038
 스마트 나노센서를 이용한 신약 효능 분석기술 개발
- 사람 몸속에서의 효능을 실시간 모니터링 할 수 있어 - - 나노-바이오-영상-분자화학 등이 융합 -
KAIST가 신약 효능을 분석하는 새로운 기법의 기술을 개발했다.
우리 학교 생명과학과 이상규 박사가 생체나노입자를 사람세포에 적용해 살아있는 세포에서 신약의 효능을 실시간으로 모니터링 하는 기술을 개발했다.
이 기술을 이용하면 사람 몸속에서도 신약의 효능을 보다 정확하게 파악할 수 있을 것으로 기대된다.
지금까지는 신약 후보물질을 몸속으로 투여하고 세포를 추출한 후 효과를 분석했다. 그러나 세포를 용해한 후 세포의 기능이 정지된 상태에서 분석함으로써 예상치 못했던 부작용으로 대부분의 후보물질이 탈락하게 된다. 이 때문에 엄청난 비용과 노력을 들이더라도 신약개발을 성공하기가 매우 어려웠다.
연구팀은 수많은 나노입자가 서로 연결되면 커다란 복합체를 형성할 수 있다는 아이디어에 착안했다. 나노입자를 세포 내부에 적용해 본 결과 실제로 살아있는 세포 안에서 나노입자 간의 결합을 통해 복합체가 빠르게 형성되는 것을 확인했다.
형성된 복합체는 나노센서 역할을 하게 돼 약물이 세포 내에 투여되는 과정에서 약물 타겟과의 결합을 실시간으로 관찰할 수 있었다.
연구팀은 이 나노센서 기술을 ‘스마트한 눈(InCell SMART-i)’이라고 명명했다. 살아있는 세포 안에서 일어나는 신약의 효능작용을 한 눈에 볼 수 있기 때문이다.
이상규 박사는 “이 기술은 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술로 신약개발에 효과적으로 적용 가능한 매우 중요한 기술”이라며 “신약물질의 직접 개발을 원하는 기업으로 기술이 이전돼 상용화가 멀지 않았다”고 말했다.
한편, KAIST 생명과학과 이상규 박사와 리온즈신약연구소(주) 김태국 박사가 개발한 이 기술은 최근 세계적인 화학지인 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 지 9월호에 주목받는 논문(Hot Paper)으로 선정됐다.
그림1. 사람 세포 내에 도입된 스마트 나노 센서가 약물과 약물 타겟 간의 결합에 따라 세포 내에 스팟(같은 나노클러스터)을 형성하고 이를 실시간으로 탐지해 낼 수 있는 원천기술의 모식도
그림2. 약물타겟 A 또는 B가 발현되어 있는 사람세포에 약물을 처리하면 세포 내에서 약물과 약물타겟이 서서히 결합되면서 스마트 나노센서에 의해 이러한 스팟 (같은 나노클러스터) 형태로 실시간으로 센싱-감지된다. 따라서 살아 있는 사람세포 안에서 신약의 효능작용을 실시간으로 마치 비디오를 보는 것처럼 라이브로 모니터링 할 수 있는 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술이다.
2011.09.05 조회수 19594
스마트 나노센서를 이용한 신약 효능 분석기술 개발
- 사람 몸속에서의 효능을 실시간 모니터링 할 수 있어 - - 나노-바이오-영상-분자화학 등이 융합 -
KAIST가 신약 효능을 분석하는 새로운 기법의 기술을 개발했다.
우리 학교 생명과학과 이상규 박사가 생체나노입자를 사람세포에 적용해 살아있는 세포에서 신약의 효능을 실시간으로 모니터링 하는 기술을 개발했다.
이 기술을 이용하면 사람 몸속에서도 신약의 효능을 보다 정확하게 파악할 수 있을 것으로 기대된다.
지금까지는 신약 후보물질을 몸속으로 투여하고 세포를 추출한 후 효과를 분석했다. 그러나 세포를 용해한 후 세포의 기능이 정지된 상태에서 분석함으로써 예상치 못했던 부작용으로 대부분의 후보물질이 탈락하게 된다. 이 때문에 엄청난 비용과 노력을 들이더라도 신약개발을 성공하기가 매우 어려웠다.
연구팀은 수많은 나노입자가 서로 연결되면 커다란 복합체를 형성할 수 있다는 아이디어에 착안했다. 나노입자를 세포 내부에 적용해 본 결과 실제로 살아있는 세포 안에서 나노입자 간의 결합을 통해 복합체가 빠르게 형성되는 것을 확인했다.
형성된 복합체는 나노센서 역할을 하게 돼 약물이 세포 내에 투여되는 과정에서 약물 타겟과의 결합을 실시간으로 관찰할 수 있었다.
연구팀은 이 나노센서 기술을 ‘스마트한 눈(InCell SMART-i)’이라고 명명했다. 살아있는 세포 안에서 일어나는 신약의 효능작용을 한 눈에 볼 수 있기 때문이다.
이상규 박사는 “이 기술은 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술로 신약개발에 효과적으로 적용 가능한 매우 중요한 기술”이라며 “신약물질의 직접 개발을 원하는 기업으로 기술이 이전돼 상용화가 멀지 않았다”고 말했다.
한편, KAIST 생명과학과 이상규 박사와 리온즈신약연구소(주) 김태국 박사가 개발한 이 기술은 최근 세계적인 화학지인 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 지 9월호에 주목받는 논문(Hot Paper)으로 선정됐다.
그림1. 사람 세포 내에 도입된 스마트 나노 센서가 약물과 약물 타겟 간의 결합에 따라 세포 내에 스팟(같은 나노클러스터)을 형성하고 이를 실시간으로 탐지해 낼 수 있는 원천기술의 모식도
그림2. 약물타겟 A 또는 B가 발현되어 있는 사람세포에 약물을 처리하면 세포 내에서 약물과 약물타겟이 서서히 결합되면서 스마트 나노센서에 의해 이러한 스팟 (같은 나노클러스터) 형태로 실시간으로 센싱-감지된다. 따라서 살아 있는 사람세포 안에서 신약의 효능작용을 실시간으로 마치 비디오를 보는 것처럼 라이브로 모니터링 할 수 있는 나노-바이오-영상-분자화학 등이 융합된 차세대 원천기술이다.
2011.09.05 조회수 19594 가상세포 이용해 병원균 잡는 항생제 개발
교육과학기술부는 미래기반기술개발사업(시스템생물학 연구)으로 지원한 우리학교 이상엽 교수팀(전남대 이준행교수, 생명(연), 화학(연) 공동연구)이 항생제에 내성을 가진 병원균 퇴치를 위해 시스템생물학을 기반으로 한 신약발굴 방법론을 개발했다고 밝혔다.
이 교수팀은 병원균이 항생제의 오남용으로 인해 치유가 쉽지 않은 점을 감안하여 내성 병원균의 가상세포를 만들어서 이에 대한 특성을 분석하여 제어하는 방법으로 효과를 입증했다.
이번 연구의 대상은 오염된 어패류에 의해 감염되는 패혈증의 병원균인 비브리오 불니피쿠스(Vibrio vulnificus, 이하 비브리오균) 중 내성균 2개이며, 이에 대한 게놈정보와 생물정보를 토대로 가상세포를 구축하였다.
이러한 가상세포가 생존하기 위해 필요한 화학물질은 193개로 분석되었으며, 이중에서 결정적 역할을 수행하는 5개의 화학물질을 추출하였으며, 이에 관여하는 유전자를 제거함으로써 내성 비브리오균의 성장이 억제되는 효과를 증명하였다.
이 교수팀의 연구결과는 올해 1월 18일 세계적 권위의 네이처 자매지인 ‘분자시스템생물학 (Molecular Systems Biology)지’에 논문으로 게재되어 세계적으로도 연구의 우수성이 인정되었다.
이러한 시스템생물학 기법에 근거한 신약발굴 방법론은 다른 내성 병원균은 물론 다양한 인간 질병에도 적용할 수 있는 토대를 마련한 것으로 기대된다.
2011.01.19 조회수 16868
가상세포 이용해 병원균 잡는 항생제 개발
교육과학기술부는 미래기반기술개발사업(시스템생물학 연구)으로 지원한 우리학교 이상엽 교수팀(전남대 이준행교수, 생명(연), 화학(연) 공동연구)이 항생제에 내성을 가진 병원균 퇴치를 위해 시스템생물학을 기반으로 한 신약발굴 방법론을 개발했다고 밝혔다.
이 교수팀은 병원균이 항생제의 오남용으로 인해 치유가 쉽지 않은 점을 감안하여 내성 병원균의 가상세포를 만들어서 이에 대한 특성을 분석하여 제어하는 방법으로 효과를 입증했다.
이번 연구의 대상은 오염된 어패류에 의해 감염되는 패혈증의 병원균인 비브리오 불니피쿠스(Vibrio vulnificus, 이하 비브리오균) 중 내성균 2개이며, 이에 대한 게놈정보와 생물정보를 토대로 가상세포를 구축하였다.
이러한 가상세포가 생존하기 위해 필요한 화학물질은 193개로 분석되었으며, 이중에서 결정적 역할을 수행하는 5개의 화학물질을 추출하였으며, 이에 관여하는 유전자를 제거함으로써 내성 비브리오균의 성장이 억제되는 효과를 증명하였다.
이 교수팀의 연구결과는 올해 1월 18일 세계적 권위의 네이처 자매지인 ‘분자시스템생물학 (Molecular Systems Biology)지’에 논문으로 게재되어 세계적으로도 연구의 우수성이 인정되었다.
이러한 시스템생물학 기법에 근거한 신약발굴 방법론은 다른 내성 병원균은 물론 다양한 인간 질병에도 적용할 수 있는 토대를 마련한 것으로 기대된다.
2011.01.19 조회수 16868 심장질환 원인신호전달메커니즘 규명
- 신약개발 및 심장질환 응용연구의 중요한 발판 마련
- IT와 BT를 융합한 시스템생물학 연구 통해 규명
우리학교 바이오및뇌공학과 조광현 교수팀과 생명과학과 허원도 교수팀이 시스템생물학 융합연구를 통해 심장질환 원인신호전달경로의 숨겨진 메커니즘을 규명했다.
심근비대증은 다양한 병인에 의해 심근세포가 비대해지는 병리학적 현상으로써 심부전증과 부정맥 등을 수반하는 주요 심장질환이다.
칼시뉴린-엔팻(calcineurin-NFAT) 신호전달경로는 이러한 심근비대증의 유발에 매우 중요한 역할을 하는 것으로 알려져 있다.
하지만 이 신호전달경로의 주요 조절단백질로 알려진 알캔(RCAN1)의 기능에 대해 많은 논쟁이 이어져 왔고 현재까지 그 구체적인 조절메커니즘이 밝혀지지 않았다.
조광현 교수 융합연구팀은 이러한 복잡한 현상에 대해 수학 모델링과 대규모 컴퓨터시뮬레이션, 그리고 단일세포 분자 이미징 기술을 동원한 시스템생물학 융합연구를 통해 어크(ERK)와 지에스케이(GSK3)로 구성된 스위칭 회로가 칼시뉴린-엔팻 신호전달경로를 조절한다는 것을 새롭게 규명했다.
특히 이 연구에서는 알캔이 세포내 농도가 낮을 때 칼시뉴린(calcineurin)의 기능을 저해하는 억제자로서 기능하지만, 그 농도가 증가하면 어크와 지에스케이에 의한 크로스토크를 통해 칼시뉴린 신호를 오히려 증가시키는 촉진자로서 기능 하도록 세포내 조절회로가 진화적으로 설계되어 있음을 최초로 밝혔다.
지금까지 많은 연구에서 알캔의 상반된 신호조절 역할이 보고되어 학계에서는 과연 무엇이 진실인가에 관한 논쟁이 이어졌다.
또한, 어떻게 동일한 분자가 그와 같이 서로 다른 기능을 보이는 것인지, 이를 유발하는 근본적인 메커니즘은 과연 무엇인지 등이 모두 수수께끼로 남아 있었다.
이번 연구를 통해 학계의 이러한 오랜 질문에 대한 해답이 제시됐으며, 알캔과 칼시뉴린-엔팻 신호전달경로의 근원적인 조절메커니즘이 시스템차원에서 최초로 규명됨으로써 앞으로 이를 표적으로 하는 신약개발 및 관련 심장질환 응용연구의 중요한 발판을 마련하게 되었다.
또한 기존의 실험적 접근만으로는 해결할 수 없는 복잡한 생명현상을 대상으로 IT와 BT의 융합연구인 생체시스템모델링 및 바이오시뮬레이션 연구를 통해 새로운 해결책을 찾을 수 있는 가능성을 제시하게 됐다.
이 연구는 교육과학기술부가 지원하는 한국연구재단의 기초연구실육성사업과 도약연구사업, 그리고 칼슘대사시스템생물학사업의 일환으로 수행됐으며, 연구 결과는 <저널오브셀사이언스(Journal of Cell Science)>의 표지논문으로 선정되어 2011년 1월 1일자(온라인판은 2010년 12월 13일자)에 게재된다.
2010.12.20 조회수 16963
심장질환 원인신호전달메커니즘 규명
- 신약개발 및 심장질환 응용연구의 중요한 발판 마련
- IT와 BT를 융합한 시스템생물학 연구 통해 규명
우리학교 바이오및뇌공학과 조광현 교수팀과 생명과학과 허원도 교수팀이 시스템생물학 융합연구를 통해 심장질환 원인신호전달경로의 숨겨진 메커니즘을 규명했다.
심근비대증은 다양한 병인에 의해 심근세포가 비대해지는 병리학적 현상으로써 심부전증과 부정맥 등을 수반하는 주요 심장질환이다.
칼시뉴린-엔팻(calcineurin-NFAT) 신호전달경로는 이러한 심근비대증의 유발에 매우 중요한 역할을 하는 것으로 알려져 있다.
하지만 이 신호전달경로의 주요 조절단백질로 알려진 알캔(RCAN1)의 기능에 대해 많은 논쟁이 이어져 왔고 현재까지 그 구체적인 조절메커니즘이 밝혀지지 않았다.
조광현 교수 융합연구팀은 이러한 복잡한 현상에 대해 수학 모델링과 대규모 컴퓨터시뮬레이션, 그리고 단일세포 분자 이미징 기술을 동원한 시스템생물학 융합연구를 통해 어크(ERK)와 지에스케이(GSK3)로 구성된 스위칭 회로가 칼시뉴린-엔팻 신호전달경로를 조절한다는 것을 새롭게 규명했다.
특히 이 연구에서는 알캔이 세포내 농도가 낮을 때 칼시뉴린(calcineurin)의 기능을 저해하는 억제자로서 기능하지만, 그 농도가 증가하면 어크와 지에스케이에 의한 크로스토크를 통해 칼시뉴린 신호를 오히려 증가시키는 촉진자로서 기능 하도록 세포내 조절회로가 진화적으로 설계되어 있음을 최초로 밝혔다.
지금까지 많은 연구에서 알캔의 상반된 신호조절 역할이 보고되어 학계에서는 과연 무엇이 진실인가에 관한 논쟁이 이어졌다.
또한, 어떻게 동일한 분자가 그와 같이 서로 다른 기능을 보이는 것인지, 이를 유발하는 근본적인 메커니즘은 과연 무엇인지 등이 모두 수수께끼로 남아 있었다.
이번 연구를 통해 학계의 이러한 오랜 질문에 대한 해답이 제시됐으며, 알캔과 칼시뉴린-엔팻 신호전달경로의 근원적인 조절메커니즘이 시스템차원에서 최초로 규명됨으로써 앞으로 이를 표적으로 하는 신약개발 및 관련 심장질환 응용연구의 중요한 발판을 마련하게 되었다.
또한 기존의 실험적 접근만으로는 해결할 수 없는 복잡한 생명현상을 대상으로 IT와 BT의 융합연구인 생체시스템모델링 및 바이오시뮬레이션 연구를 통해 새로운 해결책을 찾을 수 있는 가능성을 제시하게 됐다.
이 연구는 교육과학기술부가 지원하는 한국연구재단의 기초연구실육성사업과 도약연구사업, 그리고 칼슘대사시스템생물학사업의 일환으로 수행됐으며, 연구 결과는 <저널오브셀사이언스(Journal of Cell Science)>의 표지논문으로 선정되어 2011년 1월 1일자(온라인판은 2010년 12월 13일자)에 게재된다.
2010.12.20 조회수 16963 이효철 교수팀, 물에 녹은단백질 모양 변화 실시간 관찰 성공
- 관련 논문, 9월 22일(일)자 네이처 메서드(Nature Methods)誌 게재- 단백질의 작동메커니즘 규명에 중요한 도구 역할 및 신약개발에도 큰 도움 줄 것으로 기대
KAIST(총장 서남표) 화학과 이효철(李效澈, 36) 교수팀이 ‘물에서 변하는 단백질 분자구조를 실시간으로 규명’ 하는데 성공했다. 관련 논문은 네이처 자매지인 네이처 메서드(Nature Methods)誌 9월 22일자 온라인 판에 게재됐고 10월호에 출판될 예정이다.
논문의 제목은 “시간분해 엑스선 산란을 이용한 용액상의 단백질의 구조동역학 추적(Tracking the structural dynamics of proteins in solution using time-resolved wide-angle X-ray scattering)”으로 온라인에 게재되는 논문들 중에서도 특히 주목받는 하이라이트 논문으로 소개될 예정이다. 李 교수는 이 논문의 교신저자다.
이번 연구결과는 李 교수팀의 집념의 산물이라 할 수 있다. 李 교수팀은 지난 2005년 5월, 소금처럼 딱딱하게 고체상으로 굳어 있는 상태에서의 단백질의 안정적인 구조만을 볼 수 있는 기존의 방법을 시간분해 엑스선 결정법으로 발전시켜, 정지되어 있는 단백질의 구조뿐 만 아니라 움직이는 단백질의 동영상을 촬영하는데 성공했다. 관련 논문은 미국 국립과학원회보(PNAS, Proceedings of National Academy of Science)에 발표되었으며, 학계의 큰 주목을 받았다.
그러나 이 방법으로도 해결할 수 없는 치명적인 문제는 우리 몸에서 작용하는 일반적인 단백질은 고체상으로 있지 않고 물에 녹아있는 용액상태라는 점이다. 마치 고체 소금이 물에 녹아 소금물이 되는 것과 같은 원리다. 물은 인간의 몸의 약 70% 이상을 차지하고 있고 생명 유지에 필수적인 단백질들은 물에 녹아 있는 상태로 존재한다고 볼 수 있다. 따라서 단백질이 어떻게 기능을 발휘하는 지를 실시간으로 관측하기 위해서는 물에 녹아 있는 단백질 분자의 모양 변화를 실시간으로 추적할 수 있는 기술이 필요하다.
이러한 목표를 향한 첫 열매로 물에 녹아 있는 간단한 유기분자의 구조변화를 실시간 측정하는 데 성공하였으며, 관련 연구논문이 2005년 7월 사이언스(Science)誌에 발표된 바 있다. 당시 이 연구결과는 용액상에서 분자의 움직임을 실시간 추적할 수 있다는 점 때문에 많은 관심을 불러 일으켰는데, 李 교수는 그 기술을 더욱 발전시키면 단백질에도 응용 가능할 것으로 전망했다. 그러나 일반적으로 단백질은 그 당시 성공한 유기분자보다 적어도 1,000배 정도 크고 구조가 훨씬 더 복잡할 뿐 아니라 훨씬 적은 양으로 존재하기 때문에 물에 녹아 있는 단백질에서도 성공할 수 있다는 것에는 많은 과학자들이 회의적으로 생각했다.
이번 네이처 메서드誌에 발표한 연구결과는 그러한 부정적인 생각을 깨고 기존에 성공한 유기분자보다 ‘1,000배 더 큰 단백질 분자가 물에 녹아 있을 때에 이들의 3차원 구조변화를 실시간으로 관측하는데 성공’한 획기적인 연구성과다. 논문에서는 3가지 종류의 단백질에 대한 연구결과를 발표했는데, 우리 몸에서 산소를 이동하는데 중요한 헤모글로빈 단백질과, 근육에서의 산소공급에 관여하는 미오글로빈 단백질 등이다. 이 외에도 단백질은 주로 접혀있어 특정한 구조를 형성하는데 환경이 바뀌면 이 구조가 풀리게 된다. 풀려 있는 단백질은 일반적으로 제 역할을 할 수 없어 이러한 단백질의 접힘-풀림 현상을 이해하는 것은 매우 중요한데 씨토크롬씨라는 단백질이 풀린 상태에서 접히는 과정도 실시간으로 추적하는데 성공하였다.
이 새로운 기술을 사용하면 물에서 움직이는 단백질의 동영상을 촬영할 수도 있어 단백질의 작동메커니즘을 밝히는 데에 중요한 도구가 될 것이며, 앞으로 신약개발을 하는 데에도 큰 도움을 줄 것으로 기대된다. 또한 이 기술은 단백질은 물론이고 나노물질에도 응용이 가능하므로 BT뿐만 아니라 NT분야에도 기여할 수 있을 것으로 전망된다.
이 연구는 교육과학기술부의 창의적연구진흥사업의 연구비 지원으로 진행되었다. 연구결과는 유럽연합방사광가속기센터에서 측정되었으며, 李 교수의 주도하에 이뤄진 국제적인 공동연구의 성과다.
李 교수는 “현재 포항에 있는 제3세대 가속기에 이어 한국에서도 차세대 광원으로 건설이 논의되고 있는 제4세대 방사광가속기(XFEL)가 성공적으로 가동되면, 현재 발표된 데이터보다 적어도 1,000배정도 더 좋은 데이터를 얻을 수 있을 것으로 예상된다.”고 밝혔다.
<이효철 교수 프로필>
■ 학 력
1990 경남과학고 2년 수료, KAIST 화학과 학사과정 입학
1994 KAIST 화학과 학사과정 졸업
1994 Caltech(California Institute of Technology) 박사과정 입학
2001 Caltech 졸업(박사)
2001 시카고 대학 박사 후 연구원(Post Doc.)
2003.8.1-2007.2.28 KAIST 화학과 조교수 2007.3.1-현재 KAIST 화학과 부교수
■ 수상경력
2006 젊은 과학자상(과학기술부/한국과학기술한림원)
2006 과학기술우수논문상(한국과학기술단체총연합회)
2006 KAIST 학술상 2001-2003 美國 대먼 러년 암재단(Damon Runyon Cancer Research Foundation)펠로우쉽
(설명) 시간분해 엑스선 산란의 개념을 예술적으로 표현한 그림
2008.09.22 조회수 29810
이효철 교수팀, 물에 녹은단백질 모양 변화 실시간 관찰 성공
- 관련 논문, 9월 22일(일)자 네이처 메서드(Nature Methods)誌 게재- 단백질의 작동메커니즘 규명에 중요한 도구 역할 및 신약개발에도 큰 도움 줄 것으로 기대
KAIST(총장 서남표) 화학과 이효철(李效澈, 36) 교수팀이 ‘물에서 변하는 단백질 분자구조를 실시간으로 규명’ 하는데 성공했다. 관련 논문은 네이처 자매지인 네이처 메서드(Nature Methods)誌 9월 22일자 온라인 판에 게재됐고 10월호에 출판될 예정이다.
논문의 제목은 “시간분해 엑스선 산란을 이용한 용액상의 단백질의 구조동역학 추적(Tracking the structural dynamics of proteins in solution using time-resolved wide-angle X-ray scattering)”으로 온라인에 게재되는 논문들 중에서도 특히 주목받는 하이라이트 논문으로 소개될 예정이다. 李 교수는 이 논문의 교신저자다.
이번 연구결과는 李 교수팀의 집념의 산물이라 할 수 있다. 李 교수팀은 지난 2005년 5월, 소금처럼 딱딱하게 고체상으로 굳어 있는 상태에서의 단백질의 안정적인 구조만을 볼 수 있는 기존의 방법을 시간분해 엑스선 결정법으로 발전시켜, 정지되어 있는 단백질의 구조뿐 만 아니라 움직이는 단백질의 동영상을 촬영하는데 성공했다. 관련 논문은 미국 국립과학원회보(PNAS, Proceedings of National Academy of Science)에 발표되었으며, 학계의 큰 주목을 받았다.
그러나 이 방법으로도 해결할 수 없는 치명적인 문제는 우리 몸에서 작용하는 일반적인 단백질은 고체상으로 있지 않고 물에 녹아있는 용액상태라는 점이다. 마치 고체 소금이 물에 녹아 소금물이 되는 것과 같은 원리다. 물은 인간의 몸의 약 70% 이상을 차지하고 있고 생명 유지에 필수적인 단백질들은 물에 녹아 있는 상태로 존재한다고 볼 수 있다. 따라서 단백질이 어떻게 기능을 발휘하는 지를 실시간으로 관측하기 위해서는 물에 녹아 있는 단백질 분자의 모양 변화를 실시간으로 추적할 수 있는 기술이 필요하다.
이러한 목표를 향한 첫 열매로 물에 녹아 있는 간단한 유기분자의 구조변화를 실시간 측정하는 데 성공하였으며, 관련 연구논문이 2005년 7월 사이언스(Science)誌에 발표된 바 있다. 당시 이 연구결과는 용액상에서 분자의 움직임을 실시간 추적할 수 있다는 점 때문에 많은 관심을 불러 일으켰는데, 李 교수는 그 기술을 더욱 발전시키면 단백질에도 응용 가능할 것으로 전망했다. 그러나 일반적으로 단백질은 그 당시 성공한 유기분자보다 적어도 1,000배 정도 크고 구조가 훨씬 더 복잡할 뿐 아니라 훨씬 적은 양으로 존재하기 때문에 물에 녹아 있는 단백질에서도 성공할 수 있다는 것에는 많은 과학자들이 회의적으로 생각했다.
이번 네이처 메서드誌에 발표한 연구결과는 그러한 부정적인 생각을 깨고 기존에 성공한 유기분자보다 ‘1,000배 더 큰 단백질 분자가 물에 녹아 있을 때에 이들의 3차원 구조변화를 실시간으로 관측하는데 성공’한 획기적인 연구성과다. 논문에서는 3가지 종류의 단백질에 대한 연구결과를 발표했는데, 우리 몸에서 산소를 이동하는데 중요한 헤모글로빈 단백질과, 근육에서의 산소공급에 관여하는 미오글로빈 단백질 등이다. 이 외에도 단백질은 주로 접혀있어 특정한 구조를 형성하는데 환경이 바뀌면 이 구조가 풀리게 된다. 풀려 있는 단백질은 일반적으로 제 역할을 할 수 없어 이러한 단백질의 접힘-풀림 현상을 이해하는 것은 매우 중요한데 씨토크롬씨라는 단백질이 풀린 상태에서 접히는 과정도 실시간으로 추적하는데 성공하였다.
이 새로운 기술을 사용하면 물에서 움직이는 단백질의 동영상을 촬영할 수도 있어 단백질의 작동메커니즘을 밝히는 데에 중요한 도구가 될 것이며, 앞으로 신약개발을 하는 데에도 큰 도움을 줄 것으로 기대된다. 또한 이 기술은 단백질은 물론이고 나노물질에도 응용이 가능하므로 BT뿐만 아니라 NT분야에도 기여할 수 있을 것으로 전망된다.
이 연구는 교육과학기술부의 창의적연구진흥사업의 연구비 지원으로 진행되었다. 연구결과는 유럽연합방사광가속기센터에서 측정되었으며, 李 교수의 주도하에 이뤄진 국제적인 공동연구의 성과다.
李 교수는 “현재 포항에 있는 제3세대 가속기에 이어 한국에서도 차세대 광원으로 건설이 논의되고 있는 제4세대 방사광가속기(XFEL)가 성공적으로 가동되면, 현재 발표된 데이터보다 적어도 1,000배정도 더 좋은 데이터를 얻을 수 있을 것으로 예상된다.”고 밝혔다.
<이효철 교수 프로필>
■ 학 력
1990 경남과학고 2년 수료, KAIST 화학과 학사과정 입학
1994 KAIST 화학과 학사과정 졸업
1994 Caltech(California Institute of Technology) 박사과정 입학
2001 Caltech 졸업(박사)
2001 시카고 대학 박사 후 연구원(Post Doc.)
2003.8.1-2007.2.28 KAIST 화학과 조교수 2007.3.1-현재 KAIST 화학과 부교수
■ 수상경력
2006 젊은 과학자상(과학기술부/한국과학기술한림원)
2006 과학기술우수논문상(한국과학기술단체총연합회)
2006 KAIST 학술상 2001-2003 美國 대먼 러년 암재단(Damon Runyon Cancer Research Foundation)펠로우쉽
(설명) 시간분해 엑스선 산란의 개념을 예술적으로 표현한 그림
2008.09.22 조회수 29810 이도헌교수팀, 생물정보학적 연구를 통한 천식 발병 후보 유전자 발견
바이오및뇌공학과 이도헌 교수와 박사과정 황소현씨가 생물정보학 기법을 이용해 기존의 분자생물학적 연구 및 실험 결과에 나타난 천식 관련 단백질들의 상호작용을 분석, 천식 유발에 관여하는 후보 유전자군을 발굴했다.
이 연구결과는 국제학술지 "이론생물학저널(Journal of Theoretical Biology)"에 발표됐으며 기존 연구자료를 새로운 생물정보학 기법으로 분석해 신약 표적유전자를 발굴한 것이어서 신약연구 효율성 향상에 기여할 것으로 전망된다.
연구진은 세계 각국의 분자생물학적 연구자료가 담겨 있는 데이터베이스(OMIM, GEO)에서 천식과 관련 있는 단백질 606개를 찾아내고 이를 시스템 수준에서 연구하기 위해 생물정보학 기술을 이용해 단백질 상호작용 네트워크를 구성했다.
이는 단백질 사이의 상호작용을 연결선으로 표현한 것으로 여러 개의 단백질과 동시에 상호작용을 하는 단백질이 천식유발 단백질 네트워크에서 중요한 역할을 하는 "허브"로 간주된다.
질병과 관련된 질병유전자를 찾기 위해서 기존의 분자생물학적 연구를 통해 몇 가지 유전자들이 밝혀졌지만, 여러 가지 유전적인 요인과 환경적인 요인의 복합적인 작용으로 인해 나타나는 대부분의 복합 질병의 경우는 기존의 분자생물학적인 연구만으로 관련 유전자들을 찾아내기가 어렵다.
이도헌 교수는 "이런 복합적인 질병에서 중요한 역할을 하는 유전자를 찾아내려면 한 두 유전자와 질병의 관계를 조사하기 보다는 그 질병과 관련된 여러 유전자들의 연관성을 살펴보는 시스템 수준의 연구가 필요하다"고 말했다.
2008.07.01 조회수 22645
이도헌교수팀, 생물정보학적 연구를 통한 천식 발병 후보 유전자 발견
바이오및뇌공학과 이도헌 교수와 박사과정 황소현씨가 생물정보학 기법을 이용해 기존의 분자생물학적 연구 및 실험 결과에 나타난 천식 관련 단백질들의 상호작용을 분석, 천식 유발에 관여하는 후보 유전자군을 발굴했다.
이 연구결과는 국제학술지 "이론생물학저널(Journal of Theoretical Biology)"에 발표됐으며 기존 연구자료를 새로운 생물정보학 기법으로 분석해 신약 표적유전자를 발굴한 것이어서 신약연구 효율성 향상에 기여할 것으로 전망된다.
연구진은 세계 각국의 분자생물학적 연구자료가 담겨 있는 데이터베이스(OMIM, GEO)에서 천식과 관련 있는 단백질 606개를 찾아내고 이를 시스템 수준에서 연구하기 위해 생물정보학 기술을 이용해 단백질 상호작용 네트워크를 구성했다.
이는 단백질 사이의 상호작용을 연결선으로 표현한 것으로 여러 개의 단백질과 동시에 상호작용을 하는 단백질이 천식유발 단백질 네트워크에서 중요한 역할을 하는 "허브"로 간주된다.
질병과 관련된 질병유전자를 찾기 위해서 기존의 분자생물학적 연구를 통해 몇 가지 유전자들이 밝혀졌지만, 여러 가지 유전적인 요인과 환경적인 요인의 복합적인 작용으로 인해 나타나는 대부분의 복합 질병의 경우는 기존의 분자생물학적인 연구만으로 관련 유전자들을 찾아내기가 어렵다.
이도헌 교수는 "이런 복합적인 질병에서 중요한 역할을 하는 유전자를 찾아내려면 한 두 유전자와 질병의 관계를 조사하기 보다는 그 질병과 관련된 여러 유전자들의 연관성을 살펴보는 시스템 수준의 연구가 필요하다"고 말했다.
2008.07.01 조회수 22645 신약개발 원천기술 사이언스지에 발표
자석 이용 신약 개발, 마술같은 기술 "MAGIC" 명명
살아있는 세포내에서 다양한 물질결합 실시간 측정
생명과학과 김태국(金泰國, 41) 교수팀이 (주)씨지케이(CGK, 대표이사 정연철)와 공동으로 개발한 새로운 신약개발 원천기술이 7월1일(금)자 사이언스 誌에 발표됐다.
“살아 있는 세포에서 분자 간 상호작용을 검출하는 자성 나노프로브 기술(A magnetic nanoprobe technology for detecting molecular interactions in live cells)“이라는 제목으로 발표된 이 연구결과는 마술과 같은 기술이라 하여 "MAGIC"으로 명명됐다.
물질의 한쪽 끝에 자성체를 붙여 세포에 넣어준 뒤 자석을 대면 결합된 다른 물질이 같이 끌려나온다는 평범한 원리를 세포내에 적용한 이 기술은 살아있는 세포 내에서 다양한 물질의 결합을 실시간으로 측정 가능해 곧바로 신약개발에 응용될 수 있다. 이미 병원에서도 면역억제제로 사용하고 있는 약물에 같은 실험을 수행하여 사람 세포 내에서 이 약물에 결합한다고 알려진 단백질이 매우 선택적으로 자석에 딸려오는 현상을 실시간으로 확인했다.
金 교수는 "MAGIC 기술은 기존에 생체 내에서의 역할이 명확히 밝혀지지 않은 다양한 약물의 표적 분자를 쉽게 찾을 수 있을 뿐만 아니라, 사람 세포내에서 계속 조절 변화되는 바이오프로그램을 실시간으로 모니터하고 유익하게 재프로그래밍도 할 수 있는 혁신적인 기술"이라며, "특히 신약개발이라는 망망대해에서 더 이상 그물을 치고 기다릴 필요가 없는 셈"이라며 이 기술의 의미를 함축적으로 설명했다.
함께 연구에 참여한 CGK 정연철 대표는 "MAGIC 기술은 그간 발표된 어떤 기술보다 신약개발을 혁신적으로 앞당길 수 있는 상업화에 가장 근접한 기술"이며, "이미 항암제를 포함한 두 종의 신약 후보물질을 찾은 상태이다. 내년까지는 동물 실험을 마칠 것"이라는 계획을 발표했다. 또한 "이미 미국의 회사로부터 이 기술의 사업화를 위한 조인트벤처 설립을 제안 받았으며, 내부적으로 검토중"이라고 밝혔다.
金 교수는 "최근 황우석 교수의 줄기세포 치료법와 더불어 신약 치료법의 원천기술을 국내에 확보하여 확고한 바이오기술의 토대를 확립했다는 것이 무엇보다 의미 있다" 며, "MAGIC 원천기술을 비롯해서 앞으로도 기초연구와 바이오산업을 보다 효과적으로 접목, 국내 산업의 성장동력을 마련하기 위해 열심히 노력 하겠다"는 각오를 밝혔다.
2005.07.01 조회수 22038
신약개발 원천기술 사이언스지에 발표
자석 이용 신약 개발, 마술같은 기술 "MAGIC" 명명
살아있는 세포내에서 다양한 물질결합 실시간 측정
생명과학과 김태국(金泰國, 41) 교수팀이 (주)씨지케이(CGK, 대표이사 정연철)와 공동으로 개발한 새로운 신약개발 원천기술이 7월1일(금)자 사이언스 誌에 발표됐다.
“살아 있는 세포에서 분자 간 상호작용을 검출하는 자성 나노프로브 기술(A magnetic nanoprobe technology for detecting molecular interactions in live cells)“이라는 제목으로 발표된 이 연구결과는 마술과 같은 기술이라 하여 "MAGIC"으로 명명됐다.
물질의 한쪽 끝에 자성체를 붙여 세포에 넣어준 뒤 자석을 대면 결합된 다른 물질이 같이 끌려나온다는 평범한 원리를 세포내에 적용한 이 기술은 살아있는 세포 내에서 다양한 물질의 결합을 실시간으로 측정 가능해 곧바로 신약개발에 응용될 수 있다. 이미 병원에서도 면역억제제로 사용하고 있는 약물에 같은 실험을 수행하여 사람 세포 내에서 이 약물에 결합한다고 알려진 단백질이 매우 선택적으로 자석에 딸려오는 현상을 실시간으로 확인했다.
金 교수는 "MAGIC 기술은 기존에 생체 내에서의 역할이 명확히 밝혀지지 않은 다양한 약물의 표적 분자를 쉽게 찾을 수 있을 뿐만 아니라, 사람 세포내에서 계속 조절 변화되는 바이오프로그램을 실시간으로 모니터하고 유익하게 재프로그래밍도 할 수 있는 혁신적인 기술"이라며, "특히 신약개발이라는 망망대해에서 더 이상 그물을 치고 기다릴 필요가 없는 셈"이라며 이 기술의 의미를 함축적으로 설명했다.
함께 연구에 참여한 CGK 정연철 대표는 "MAGIC 기술은 그간 발표된 어떤 기술보다 신약개발을 혁신적으로 앞당길 수 있는 상업화에 가장 근접한 기술"이며, "이미 항암제를 포함한 두 종의 신약 후보물질을 찾은 상태이다. 내년까지는 동물 실험을 마칠 것"이라는 계획을 발표했다. 또한 "이미 미국의 회사로부터 이 기술의 사업화를 위한 조인트벤처 설립을 제안 받았으며, 내부적으로 검토중"이라고 밝혔다.
金 교수는 "최근 황우석 교수의 줄기세포 치료법와 더불어 신약 치료법의 원천기술을 국내에 확보하여 확고한 바이오기술의 토대를 확립했다는 것이 무엇보다 의미 있다" 며, "MAGIC 원천기술을 비롯해서 앞으로도 기초연구와 바이오산업을 보다 효과적으로 접목, 국내 산업의 성장동력을 마련하기 위해 열심히 노력 하겠다"는 각오를 밝혔다.
2005.07.01 조회수 22038