-
 홍정욱 교수, Elsevier ADES 저널 수석편집장 선임
건설및환경공학과 홍정욱 교수가 세계 최대의 저널 출판사인 Elsevier에서 출간하는 전산역학 분야 권위 학술지인 ‘Advances in Engineering Software’의 수석편집장(Editor-in-Chief)으로 2024년 1월 3일자로 선임됐다.
ADES 저널은 JCR의 공학(Engineering)분야 Q1으로 분류되는 우수한 저널로서 홍정욱 교수는 수석편집장 임무를 통해 투고된 논문의 우수성을 심사하고 다양한 국제적인 활동을 통하여 해당 저널의 수준을 향상시키는 역할을 수행한다.
홍정욱 교수, Elsevier ADES 저널 수석편집장 선임
건설및환경공학과 홍정욱 교수가 세계 최대의 저널 출판사인 Elsevier에서 출간하는 전산역학 분야 권위 학술지인 ‘Advances in Engineering Software’의 수석편집장(Editor-in-Chief)으로 2024년 1월 3일자로 선임됐다.
ADES 저널은 JCR의 공학(Engineering)분야 Q1으로 분류되는 우수한 저널로서 홍정욱 교수는 수석편집장 임무를 통해 투고된 논문의 우수성을 심사하고 다양한 국제적인 활동을 통하여 해당 저널의 수준을 향상시키는 역할을 수행한다.
2024.02.07
조회수 5664
-
 RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
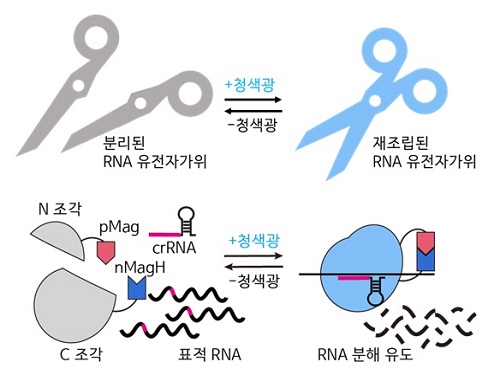
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2024.02.07
조회수 9665
-
 4.55V 고전압 리튬이온전지 전해액 기술 개발
전기차 시대의 가속화에 따라 1회 충전에 긴 주행거리를 가능하게 하는 고용량, 고에너지밀도 이차전지 개발과 더불어 빠르게 충전을 할 수 있는 고속 충전 기술 개발의 중요도가 커지고 있다.
우리 대학 생명화학공학과 최남순 교수 연구팀이 고전압 조건에서 리튬이온전지의 높은 효율과 에너지를 유지하고 고속 충전이 가능한 전해액 설계 기술을 개발했다고 6일 밝혔다. 개발된 전해액은 점도가 낮으면서 고전압에 안정적인 용매를 사용하였으며 안정적인 전극-전해질 계면 반응을 확보할 수 있는 첨가제 기술을 통해 리튬이온전지의 수명 특성을 획기적으로 향상시켰다.
최남순 교수 연구팀은 상용 리튬이온전지에 사용되고 있는 카보네이트 계열의 용매 대신 점도가 낮고 고전압 조건에서 안정적으로 작용할 수 있는 용매 조성 기술과 전극계면 보호 기술을 적용해 기존 연구 결과보다 현저하게 향상된 *가역 효율 (99.9% 이상)을 달성했다.
☞ 가역 효율 : 매 사이클마다 전지의 방전용량을 충전용량으로 나누어 백분율로 나타낸 값으로 배터리의 가역성을 의미함. 가역 효율이 높을수록 매 사이클마다 배터리 용량 손실이 적음을 의미함. 아무리 높은 용량을 구현하는 배터리라도 가역성이 높지 않다면 실용화가 어려움.
또한, 첫 사이클 방전 기준 용량 대비 200 사이클에서의 방전 기준 용량까지를 용량 유지율 측정하였는데 개발된 전해액 기술은 고온 (45도)에서 4.5 V의 충전 전압 조건에서 89.9%의 높은 용량 유지율을 보였으며 4.53 V의 충전 전압 조건에서도 77.0%의 높은 용량 유지율을 보였다. 개발 전해액 조성의 경우 기존 상용 최고 수준 기술 대비 약 10~15% 이상의 높은 용량 유지율을 보여줬다. 뿐만 아니라, 4.55 V의 혁신적인 충전 전압 조건에서도 200회 사이클 후 61.7%의 높은 용량 유지율을 보여주는 등 우수한 수명 특성을 보여줬다.
이번 연구에서 개발된 전해액 설계 기술은 리튬 코발트 산화물 양극을 사용해 4.5 V 이상의 고전압 그리고 1.5C (45분 충전)의 빠른 충전 조건에서 극대화된 성능을 얻었다는 점에서 그 의미가 크다. 여기에 더해 60도 고온 저장에서도 저장 성능이 향상됨도 확인했다. 특히 고에너지밀도 리튬이온전지용 전해액 기준 프레임을 제시한 바, 이는 리튬이차전지 전해액 설계에서 새로운 기준이 될 것이라고 연구진은 설명했다.
이번 논문의 공동 제1 저자인 우리 대학 생명화학공학과 김세훈 박사과정은 “높은 산화안정성 및 저점도 특성을 가지는 용매 적용에 따른 고전압 안정성 및 고속 충전 특성 향상과 전해액 첨가제에 의한 안정적인 전극-전해질 계면 형성의 시너지 효과에 의해 기존에 보고된 리튬이온전지용 전해액 기술 개발의 한계를 뛰어넘는 기술을 개발하게 됐다ˮ라고 말했다. 또한, “상용 리튬이온전지에서 사용하는 수준의 높은 로딩의 리튬 코발트 산화물 양극을 사용하여 전지의 수명 특성을 극대화했기 때문에 산업에의 빠른 적용 및 향후 고에너지밀도 전지 시스템 설계에 있어 이정표로 작용할 수 있을 것이다”라고 전했다.
최남순 교수는 "개발된 전해액 기술은 상용 용매로 사용되고 있는 카보네이트 유기용매의 부족한 고전압 내구성을 에스테르 용매로 획기적으로 극복하였으며 이를 통해 배터리 충전과정에서 가스 발생을 최소화하는 고전압 전해액 시스템을 구축했다ˮ라고 말했다. 또한, "이러한 고전압 용매 조성과 전해액 첨가제 조합 기술은 리튬이온전지의 한계 에너지밀도를 끌어올리기 위한 전해액의 고전압화를 위한 돌파기술이라는 점에서 그 의미가 크다고 하겠다ˮ라고 연구의 의미를 강조했다.
이번 연구에서 생명화학공학과 최남순 교수와 김세훈, 이정아 연구원은 리튬이온전지의 고전압 구동을 위한 새로운 전해액 조성 기술을 개발하고 이에 대한 효과를 검증하였으며 작동 메커니즘을 규명하였다. 경상국립대학교 나노신소재융합공학과 (나노·신소재공학부 고분자공학 전공) 이태경 교수와 이동규, 손준수 연구원은 전해액 용매 및 첨가제의 작동 메커니즘을 계산화학을 통해 구체화하는 연구를 진행하였다. 이번 연구는 저명한 국제 학술지 `에이시에스 에너지 레터즈 (ACS Energy Letters)'에 1월 12일자로 발간되었으며 커버 논문으로 선정되었다 (논문명 : Designing Electrolytes for Stable Operation of High-Voltage LiCoO2 in Lithium-Ion Batteries).
이번 연구 수행은 삼성 에스디아이 (Samsung SDI)의 지원을 받아 수행됐다.
4.55V 고전압 리튬이온전지 전해액 기술 개발
전기차 시대의 가속화에 따라 1회 충전에 긴 주행거리를 가능하게 하는 고용량, 고에너지밀도 이차전지 개발과 더불어 빠르게 충전을 할 수 있는 고속 충전 기술 개발의 중요도가 커지고 있다.
우리 대학 생명화학공학과 최남순 교수 연구팀이 고전압 조건에서 리튬이온전지의 높은 효율과 에너지를 유지하고 고속 충전이 가능한 전해액 설계 기술을 개발했다고 6일 밝혔다. 개발된 전해액은 점도가 낮으면서 고전압에 안정적인 용매를 사용하였으며 안정적인 전극-전해질 계면 반응을 확보할 수 있는 첨가제 기술을 통해 리튬이온전지의 수명 특성을 획기적으로 향상시켰다.
최남순 교수 연구팀은 상용 리튬이온전지에 사용되고 있는 카보네이트 계열의 용매 대신 점도가 낮고 고전압 조건에서 안정적으로 작용할 수 있는 용매 조성 기술과 전극계면 보호 기술을 적용해 기존 연구 결과보다 현저하게 향상된 *가역 효율 (99.9% 이상)을 달성했다.
☞ 가역 효율 : 매 사이클마다 전지의 방전용량을 충전용량으로 나누어 백분율로 나타낸 값으로 배터리의 가역성을 의미함. 가역 효율이 높을수록 매 사이클마다 배터리 용량 손실이 적음을 의미함. 아무리 높은 용량을 구현하는 배터리라도 가역성이 높지 않다면 실용화가 어려움.
또한, 첫 사이클 방전 기준 용량 대비 200 사이클에서의 방전 기준 용량까지를 용량 유지율 측정하였는데 개발된 전해액 기술은 고온 (45도)에서 4.5 V의 충전 전압 조건에서 89.9%의 높은 용량 유지율을 보였으며 4.53 V의 충전 전압 조건에서도 77.0%의 높은 용량 유지율을 보였다. 개발 전해액 조성의 경우 기존 상용 최고 수준 기술 대비 약 10~15% 이상의 높은 용량 유지율을 보여줬다. 뿐만 아니라, 4.55 V의 혁신적인 충전 전압 조건에서도 200회 사이클 후 61.7%의 높은 용량 유지율을 보여주는 등 우수한 수명 특성을 보여줬다.
이번 연구에서 개발된 전해액 설계 기술은 리튬 코발트 산화물 양극을 사용해 4.5 V 이상의 고전압 그리고 1.5C (45분 충전)의 빠른 충전 조건에서 극대화된 성능을 얻었다는 점에서 그 의미가 크다. 여기에 더해 60도 고온 저장에서도 저장 성능이 향상됨도 확인했다. 특히 고에너지밀도 리튬이온전지용 전해액 기준 프레임을 제시한 바, 이는 리튬이차전지 전해액 설계에서 새로운 기준이 될 것이라고 연구진은 설명했다.
이번 논문의 공동 제1 저자인 우리 대학 생명화학공학과 김세훈 박사과정은 “높은 산화안정성 및 저점도 특성을 가지는 용매 적용에 따른 고전압 안정성 및 고속 충전 특성 향상과 전해액 첨가제에 의한 안정적인 전극-전해질 계면 형성의 시너지 효과에 의해 기존에 보고된 리튬이온전지용 전해액 기술 개발의 한계를 뛰어넘는 기술을 개발하게 됐다ˮ라고 말했다. 또한, “상용 리튬이온전지에서 사용하는 수준의 높은 로딩의 리튬 코발트 산화물 양극을 사용하여 전지의 수명 특성을 극대화했기 때문에 산업에의 빠른 적용 및 향후 고에너지밀도 전지 시스템 설계에 있어 이정표로 작용할 수 있을 것이다”라고 전했다.
최남순 교수는 "개발된 전해액 기술은 상용 용매로 사용되고 있는 카보네이트 유기용매의 부족한 고전압 내구성을 에스테르 용매로 획기적으로 극복하였으며 이를 통해 배터리 충전과정에서 가스 발생을 최소화하는 고전압 전해액 시스템을 구축했다ˮ라고 말했다. 또한, "이러한 고전압 용매 조성과 전해액 첨가제 조합 기술은 리튬이온전지의 한계 에너지밀도를 끌어올리기 위한 전해액의 고전압화를 위한 돌파기술이라는 점에서 그 의미가 크다고 하겠다ˮ라고 연구의 의미를 강조했다.
이번 연구에서 생명화학공학과 최남순 교수와 김세훈, 이정아 연구원은 리튬이온전지의 고전압 구동을 위한 새로운 전해액 조성 기술을 개발하고 이에 대한 효과를 검증하였으며 작동 메커니즘을 규명하였다. 경상국립대학교 나노신소재융합공학과 (나노·신소재공학부 고분자공학 전공) 이태경 교수와 이동규, 손준수 연구원은 전해액 용매 및 첨가제의 작동 메커니즘을 계산화학을 통해 구체화하는 연구를 진행하였다. 이번 연구는 저명한 국제 학술지 `에이시에스 에너지 레터즈 (ACS Energy Letters)'에 1월 12일자로 발간되었으며 커버 논문으로 선정되었다 (논문명 : Designing Electrolytes for Stable Operation of High-Voltage LiCoO2 in Lithium-Ion Batteries).
이번 연구 수행은 삼성 에스디아이 (Samsung SDI)의 지원을 받아 수행됐다.
2024.02.06
조회수 9832
-
 암, 루게릭병 등 난치성 질환 발병 기전 밝혀
단백질 정보를 가진 mRNA 유전자 조절 기전에서 알루 요소(Alu)의 중요성을 제시하고, 나아가 종양 형성, 퇴행성 뇌질환 등 mRNA가 변화하는 다양한 질환에서 역방향 알루 반복구조(IRAlus)라는 새로운 발병 원인을 최초로 제시함으로써 질병 치료에 획기적인 방안을 제시하였다.
우리 대학 생명화학공학과 김유식 교수와 바이오및뇌공학과 이영석 교수 공동 연구팀이 종양 형성과 퇴행성 뇌질환을 유발하는 새로운 유전자 조절 기전을 찾아냈다고 6일 밝혔다.
인간 유전체의 약 10%를 차지하는 반복서열인 알루 요소(Alu element, Alu)는 단백질 정보를 가지는 전령 RNA(messenger RNA, mRNA)의 단백질 생산 효율을 조절할 수 있다. 특히, mRNA가 2개의 알루 요소로 형성된 역방향 알루 반복 구조(Inverted Alu repeats, IRAlus)를 가지게 되면 mRNA의 세포 내 이동이 방해되어 단백질 생산이 감소한다.
연구팀은 질환 특이적으로 mRNA가 변화하는 과정에서 주요 mRNA가 역방향 알루 반복 구조(IRAlus)에 의해 조절받게 하고 이는 mRNA가 가지고 있는 유전자 발현 억제로 이어져 질환을 일으킨다는 새로운 발병 기전을 밝혔다.
알루(Alu)는 유전체의 단백질 정보를 가지고 있지만 유전체 상에서 본인의 서열만을 복제하는 성질이 있어 ‘이기적 서열’로 알려져 있었다. 최근 연구에 의하면 mRNA 내의 존재하는 역방향 알루 반복 구조(IRAlus)는 숙주 mRNA의 세포질로의 이동을 방해하여 해당 유전자의 단백질 번역을 억제한다. 그러나, 해당 유전자 발현 조절 기전의 생물학적 중요성에 대해서는 보고된 바가 없었다.
연구팀은 역방향 알루 반복 구조(IRAlus)를 인지할 수 있는 항체를 활용한 차세대 염기서열 분석법을 사용해 특정 세포 내 활성화된, 기능적인 역방향 알루 반복 구조(IRAlus)를 가지고 있어 역방향 알루 반복 구조(IRAlus)에 의해 단백질 합성이 억제될 수 있는 mRNA 유전자 목록을 완성했다.
종양 형성 과정에서 역방향 알루 반복 구조(IRAlus)의 유전자 조절 기전의 영향을 분석했다. 연구팀은 대표적인 종양억제유전자를 억제하는 종양 유전자 조절을 하고 이는 단백질 발현 증가로 이어지며 결과적으로 종양억제유전자 활성이 억제됨으로써 암 발달을 촉진할 수 있다.
나아가, 특정 mRNA 서열과 상보적으로 결합해 mRNA의 기능을 억제해 다양한 질병 치료 및 조절 도구로 현재 연구되고 있는 혁신 RNA 치료제인 안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, 이하 ASO)를 활용해 단백질 발현을 복구하는 암 치료 전략을 탐색했다.
연구팀은 신경계 세포에서 역방향 알루 반복 구조(IRAlus)로 인한 유전자 조절이 활발하다는 것을 확인했다. 또한, 해당 현상의 과도한 활성과 루게릭병으로 알려진 근위축성 측삭경화증을 비롯한 퇴행성 뇌질환 간의 연관성을 최초로 제시했다.
생명화학공학과 김유식 교수는 “이번 연구는 인간 유전체 내 반복서열인 역방향 알루 반복 구조(IRAlus)를 가지는 유전자를 목록화하는 것을 넘어서 해당 유전자 발현 조절이 인간 질환, 특히 종양 형성 및 퇴행성 뇌질환 발병과정에서 핵심적인 역할을 하는 것을 최초로 확인했다”면서 “이번 연구에서 제시한 역방향 알루 반복 구조(IRAlus)라는 새로운 타겟 물질을 활용하면 종양과 노화를 비롯해 다양한 퇴행성 질환의 발병 기전 분석에 근본적이고 효과적인 치료전략을 마련하는 데 유용할 것”이라고 말했다.
생명화학공학과 구자영 박사(현 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학 (Harvard Medical School) 박사후연구원)와 이건용 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 2월 2일 字에 온라인 게재됐다. (논문명 : Alternative Polyadenylation Determines the Functional Landscape of Inverted Alu Repeats).
우리 대학 생명과학과 임정훈 교수 연구팀과 의과학대학원 한진주 교수 연구팀이 참여한 이번 연구는 한국연구재단 기초연구실 지원사업과 KAIST 도약연구사업의 지원을 받아 수행됐다.
암, 루게릭병 등 난치성 질환 발병 기전 밝혀
단백질 정보를 가진 mRNA 유전자 조절 기전에서 알루 요소(Alu)의 중요성을 제시하고, 나아가 종양 형성, 퇴행성 뇌질환 등 mRNA가 변화하는 다양한 질환에서 역방향 알루 반복구조(IRAlus)라는 새로운 발병 원인을 최초로 제시함으로써 질병 치료에 획기적인 방안을 제시하였다.
우리 대학 생명화학공학과 김유식 교수와 바이오및뇌공학과 이영석 교수 공동 연구팀이 종양 형성과 퇴행성 뇌질환을 유발하는 새로운 유전자 조절 기전을 찾아냈다고 6일 밝혔다.
인간 유전체의 약 10%를 차지하는 반복서열인 알루 요소(Alu element, Alu)는 단백질 정보를 가지는 전령 RNA(messenger RNA, mRNA)의 단백질 생산 효율을 조절할 수 있다. 특히, mRNA가 2개의 알루 요소로 형성된 역방향 알루 반복 구조(Inverted Alu repeats, IRAlus)를 가지게 되면 mRNA의 세포 내 이동이 방해되어 단백질 생산이 감소한다.
연구팀은 질환 특이적으로 mRNA가 변화하는 과정에서 주요 mRNA가 역방향 알루 반복 구조(IRAlus)에 의해 조절받게 하고 이는 mRNA가 가지고 있는 유전자 발현 억제로 이어져 질환을 일으킨다는 새로운 발병 기전을 밝혔다.
알루(Alu)는 유전체의 단백질 정보를 가지고 있지만 유전체 상에서 본인의 서열만을 복제하는 성질이 있어 ‘이기적 서열’로 알려져 있었다. 최근 연구에 의하면 mRNA 내의 존재하는 역방향 알루 반복 구조(IRAlus)는 숙주 mRNA의 세포질로의 이동을 방해하여 해당 유전자의 단백질 번역을 억제한다. 그러나, 해당 유전자 발현 조절 기전의 생물학적 중요성에 대해서는 보고된 바가 없었다.
연구팀은 역방향 알루 반복 구조(IRAlus)를 인지할 수 있는 항체를 활용한 차세대 염기서열 분석법을 사용해 특정 세포 내 활성화된, 기능적인 역방향 알루 반복 구조(IRAlus)를 가지고 있어 역방향 알루 반복 구조(IRAlus)에 의해 단백질 합성이 억제될 수 있는 mRNA 유전자 목록을 완성했다.
종양 형성 과정에서 역방향 알루 반복 구조(IRAlus)의 유전자 조절 기전의 영향을 분석했다. 연구팀은 대표적인 종양억제유전자를 억제하는 종양 유전자 조절을 하고 이는 단백질 발현 증가로 이어지며 결과적으로 종양억제유전자 활성이 억제됨으로써 암 발달을 촉진할 수 있다.
나아가, 특정 mRNA 서열과 상보적으로 결합해 mRNA의 기능을 억제해 다양한 질병 치료 및 조절 도구로 현재 연구되고 있는 혁신 RNA 치료제인 안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, 이하 ASO)를 활용해 단백질 발현을 복구하는 암 치료 전략을 탐색했다.
연구팀은 신경계 세포에서 역방향 알루 반복 구조(IRAlus)로 인한 유전자 조절이 활발하다는 것을 확인했다. 또한, 해당 현상의 과도한 활성과 루게릭병으로 알려진 근위축성 측삭경화증을 비롯한 퇴행성 뇌질환 간의 연관성을 최초로 제시했다.
생명화학공학과 김유식 교수는 “이번 연구는 인간 유전체 내 반복서열인 역방향 알루 반복 구조(IRAlus)를 가지는 유전자를 목록화하는 것을 넘어서 해당 유전자 발현 조절이 인간 질환, 특히 종양 형성 및 퇴행성 뇌질환 발병과정에서 핵심적인 역할을 하는 것을 최초로 확인했다”면서 “이번 연구에서 제시한 역방향 알루 반복 구조(IRAlus)라는 새로운 타겟 물질을 활용하면 종양과 노화를 비롯해 다양한 퇴행성 질환의 발병 기전 분석에 근본적이고 효과적인 치료전략을 마련하는 데 유용할 것”이라고 말했다.
생명화학공학과 구자영 박사(현 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학 (Harvard Medical School) 박사후연구원)와 이건용 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 2월 2일 字에 온라인 게재됐다. (논문명 : Alternative Polyadenylation Determines the Functional Landscape of Inverted Alu Repeats).
우리 대학 생명과학과 임정훈 교수 연구팀과 의과학대학원 한진주 교수 연구팀이 참여한 이번 연구는 한국연구재단 기초연구실 지원사업과 KAIST 도약연구사업의 지원을 받아 수행됐다.
2024.02.06
조회수 6437
-
 차세대 2차원 반도체 다기능 전자 소자 개발
공급 전압에 의한 2차원 반도체의 극성 전환을 이용해 새로운 전자 소자로의 응용이 보고된 바 있으나, 모두 누설 전류가 크거나 낮은 전류점멸비로 인해 실제 집적 회로(IC)칩에서 사용하기 어려웠다. 우리 대학 연구팀은 다기능 전자 소자를 통해 프로그램 및 기능성 변환이 가능한 회로 구현의 가능성을 제시하고 IC칩에서의 2차원 반도체의 활용성을 확장하는 기술을 개발하였다.
우리 대학 전기및전자공학부 이가영 교수 연구팀이 양극성 반도체 특성을 가진 2차원 나노 반도체 기반의 다기능 전자 소자를 개발했다고 2일 밝혔다. 다기능 전자 소자란 기존 트랜지스터와 달리 전압에 따라 기능을 변환할 수 있는 소자로, 연구팀의 소자는 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광 감지 소자로 변환 가능하여 폭 넓은 사용이 가능하다.
기존 실리콘 반도체보다 성능이 뛰어난 이황화 몰리브덴(MoS2)는 층상 구조의 2차원 반도체 나노 소재로, 전자가 흐르는 N형 반도체 특성을 가지면서 대기에서 안정적이다. 또한, 기존 실리콘 반도체가 미세화될수록 성능 저하에 취약함에 반해, 이황화 몰리브덴은 관련 문제가 적어 차세대 반도체로서 학계뿐만 아니라 삼성, TSMC, 인텔과 같은 산업계에서의 연구도 활발하다.
그러나 상보적 금속산화막 반도체(CMOS) 구현을 위해서는 음(N) 전하를 띄는 전자뿐만 아니라 양(P) 전하를 띄는 정공 유도도 필요한 데, 이황화 몰리브덴에서는 정공 유도가 어려웠다. 이 문제를 해결하기 위해 이황화 몰리브덴에 추가적인 공정을 도입하거나 다른 P형 물질을 사용하는 방법이 시도됐으나, 공정 난이도가 높다. 이러한 문제점은 현재까지도 이황화 몰리브덴을 상용화하기 위해 해결해야 할 중요한 과제로 남아 있다.
이가영 교수 연구팀은 채널 하부에 전극을 배치하고 금속/반도체 접합 특성을 개선해 전자와 정공 모두 선택적으로 흐를 수 있는 양극성 특성을 구현하는 데 성공했다. 이로써 전류의 점멸 비율을 대폭 높일 뿐만 아니라, 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광감지 소자로 다기능 변조 동작이 가능한 이황화 몰리브덴 전자 소자를 개발했다. 또한 이를 기반으로 집적도가 개선된 논리 연산이 가능함도 보였다.
이번 연구를 주도한 송준기, 이수연 학생은 “기존 실리콘 금속산화막 반도체(CMOS) 공정 호환성이 높은 공정 과정을 통해 차세대 2차원 반도체의 다양한 기능을 구현했다”며 “IC칩에서 이황화 몰리브덴의 전자소자로의 활용성 및 실용성을 넓히는 계기가 될 것이다”라고 덧붙였다.
이가영 교수는 “이번에 개발한 전자 소자는 주어진 전압 특성에 따라 다양한 기능을 수행하면서도 각 기능의 성능이 우수하다”며 “서로 다른 기능의 소자들은 대개 구조와 공정 방법들이 달라 함께 집적시 공정 난이도가 높고 회로 도면 변화에 따른 공정 전환이 까다롭다. 반면, 이번에 개발한 신개념 소자는 하나의 소자에서 다기능을 할 수 있어서 현재 수요가 급증하고 있는 맞춤형 반도체의 제작 및 공정 전환을 용이하게 할 것이다. 목적에 따라 회로 자체의 기능성을 변환할 수 있어 단일 칩 시스템의 소형화에도 기여할 것으로 기대한다”라고 말했다.
우리 대학 전기및전자공학부 송준기 석박통합과정 학생과 이수연 석사과정 학생이 공동 제1 저자로 참여한 이번 연구는 나노과학 분야 저명 국제 학술지 `ACS Nano'에 2024년 1월 26일 온라인판에 출판됐다. (논문명 : Drain-induced multifunctional ambipolar electronics based on junctionless MoS2)
한편 이번 연구는 한국연구재단의 기초연구사업 및 BK21, KAIST의 C2 사업, 그리고 LX 세미콘-KAIST 미래기술센터의 지원을 받아 수행됐다.
차세대 2차원 반도체 다기능 전자 소자 개발
공급 전압에 의한 2차원 반도체의 극성 전환을 이용해 새로운 전자 소자로의 응용이 보고된 바 있으나, 모두 누설 전류가 크거나 낮은 전류점멸비로 인해 실제 집적 회로(IC)칩에서 사용하기 어려웠다. 우리 대학 연구팀은 다기능 전자 소자를 통해 프로그램 및 기능성 변환이 가능한 회로 구현의 가능성을 제시하고 IC칩에서의 2차원 반도체의 활용성을 확장하는 기술을 개발하였다.
우리 대학 전기및전자공학부 이가영 교수 연구팀이 양극성 반도체 특성을 가진 2차원 나노 반도체 기반의 다기능 전자 소자를 개발했다고 2일 밝혔다. 다기능 전자 소자란 기존 트랜지스터와 달리 전압에 따라 기능을 변환할 수 있는 소자로, 연구팀의 소자는 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광 감지 소자로 변환 가능하여 폭 넓은 사용이 가능하다.
기존 실리콘 반도체보다 성능이 뛰어난 이황화 몰리브덴(MoS2)는 층상 구조의 2차원 반도체 나노 소재로, 전자가 흐르는 N형 반도체 특성을 가지면서 대기에서 안정적이다. 또한, 기존 실리콘 반도체가 미세화될수록 성능 저하에 취약함에 반해, 이황화 몰리브덴은 관련 문제가 적어 차세대 반도체로서 학계뿐만 아니라 삼성, TSMC, 인텔과 같은 산업계에서의 연구도 활발하다.
그러나 상보적 금속산화막 반도체(CMOS) 구현을 위해서는 음(N) 전하를 띄는 전자뿐만 아니라 양(P) 전하를 띄는 정공 유도도 필요한 데, 이황화 몰리브덴에서는 정공 유도가 어려웠다. 이 문제를 해결하기 위해 이황화 몰리브덴에 추가적인 공정을 도입하거나 다른 P형 물질을 사용하는 방법이 시도됐으나, 공정 난이도가 높다. 이러한 문제점은 현재까지도 이황화 몰리브덴을 상용화하기 위해 해결해야 할 중요한 과제로 남아 있다.
이가영 교수 연구팀은 채널 하부에 전극을 배치하고 금속/반도체 접합 특성을 개선해 전자와 정공 모두 선택적으로 흐를 수 있는 양극성 특성을 구현하는 데 성공했다. 이로써 전류의 점멸 비율을 대폭 높일 뿐만 아니라, 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광감지 소자로 다기능 변조 동작이 가능한 이황화 몰리브덴 전자 소자를 개발했다. 또한 이를 기반으로 집적도가 개선된 논리 연산이 가능함도 보였다.
이번 연구를 주도한 송준기, 이수연 학생은 “기존 실리콘 금속산화막 반도체(CMOS) 공정 호환성이 높은 공정 과정을 통해 차세대 2차원 반도체의 다양한 기능을 구현했다”며 “IC칩에서 이황화 몰리브덴의 전자소자로의 활용성 및 실용성을 넓히는 계기가 될 것이다”라고 덧붙였다.
이가영 교수는 “이번에 개발한 전자 소자는 주어진 전압 특성에 따라 다양한 기능을 수행하면서도 각 기능의 성능이 우수하다”며 “서로 다른 기능의 소자들은 대개 구조와 공정 방법들이 달라 함께 집적시 공정 난이도가 높고 회로 도면 변화에 따른 공정 전환이 까다롭다. 반면, 이번에 개발한 신개념 소자는 하나의 소자에서 다기능을 할 수 있어서 현재 수요가 급증하고 있는 맞춤형 반도체의 제작 및 공정 전환을 용이하게 할 것이다. 목적에 따라 회로 자체의 기능성을 변환할 수 있어 단일 칩 시스템의 소형화에도 기여할 것으로 기대한다”라고 말했다.
우리 대학 전기및전자공학부 송준기 석박통합과정 학생과 이수연 석사과정 학생이 공동 제1 저자로 참여한 이번 연구는 나노과학 분야 저명 국제 학술지 `ACS Nano'에 2024년 1월 26일 온라인판에 출판됐다. (논문명 : Drain-induced multifunctional ambipolar electronics based on junctionless MoS2)
한편 이번 연구는 한국연구재단의 기초연구사업 및 BK21, KAIST의 C2 사업, 그리고 LX 세미콘-KAIST 미래기술센터의 지원을 받아 수행됐다.
2024.02.05
조회수 7543
-
 입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
2024.02.01
조회수 6297
-
 인공지능으로 인간 추론 능력 극대화시키다
최근 인공지능 기술이 인식, 생성, 제어, 대화와 같은 실제 문제를 빠르게 해결해 나감에 따라 인간의 역할과 일자리 생태계가 변화하고 있다. 인공지능의 발전 속도를 본다면 가까운 미래에는 인공지능이 인간보다 똑똑해질 수도 있다. 이와 반대로 인공지능을 이용해 인간의 사고력 자체를 향상시킬 순 없을까?
우리 대학 뇌인지과학과 이상완 교수(신경과학-인공지능 융합연구센터장) 연구팀이 인간의 빠른 추론 능력을 유도해 인과관계의 학습 효율을 향상할 수 있는 뇌 기반 인공지능 기술 개발에 성공했다고 31일 밝혔다.
우리는 일상생활에서 다양한 사건을 경험하며 세상의 다양한 요소에 대한 인과관계를 학습해 나가고, 공부할 때는 지식 조각들을 조합하며 통합적인 지식을 습득한다. 이러한 과정은 점진적으로 추론하는 베이시안 모델 또는 특정한 상황에서 한 번의 경험으로부터 빠르게 결론을 도출하는 고속추론 또는 원샷 추론이 있다.
연구팀은 이전 연구에서 인간의 원샷 추론 과정을 모델링하고 전두엽과 해마가 이러한 과정에 관여하고 있음을 규명한 바 있다. 이번 연구에서 이 모델에 인간의 원샷 추론 과정을 특정한 상태로 유도하기 위해 알파고에 사용된 바 있는 심층 강화학습 기술을 접목했다. 이는 강화학습 알고리즘이 인간의 원샷 추론 과정을 수없이 시뮬레이션하면서 전두엽과 해마가 가장 효율적으로 학습할 수 있는 최적의 조건을 탐색하는 과정으로 볼 수 있다.
연구팀은 126명의 인간 피험자를 대상으로 한 인과관계 학습 및 추론 실험에서 제안 기술을 사용해 학습했을 때 단순 반복 학습 대비 최대 약 40%까지 학습 효율이 향상됨을 보였다. 더 나아가 오랜 시간에 걸쳐 신중하게 학습하거나 몇 가지 단서만을 조합해 빠르게 결론을 도출하는 것 같은 개인별 학습 성향을 고려한 맞춤형 설계가 가능함을 보였다.
인간의 사고체계에 대한 뇌과학적인 이해를 바탕으로 원샷 추론과 같은 인간의 잠재적 능력을 극대화하는 이 기술은 차세대 인공지능의 중요한 도전과제 중 하나이며, 뇌 기반 인공지능 기술은 인간과 유사한 사고체계를 바탕으로 가치판단을 할 수 있으므로 장기적으로 인간과 인공지능이 협업하는 분야에서 인공지능의 신뢰성 및 윤리성을 높이는 데도 기여할 수 있을 것으로 기대된다.
개발 기술은 스마트 교육, 게임 콘텐츠 개발, 추론 능력 측정, 인지훈련 등 인간의 추론 학습과 관련된 모든 분야에 적용될 수 있다. 기존 기술은 단편적인 기억회상, 특정 인지기능, 정답률 증가와 같은 행동적 측면에 집중해 왔다면, 이번 기술은 인공지능을 이용해 과거의 경험을 일반화시키는 인간의 사고체계 자체를 높이는 가능성을 확인한 최초의 사례로 평가된다.
KAIST에서 연구를 주도한 제1 저자 이지항 교수(현 상명대 서울캠퍼스 조교수)는 "이번 연구를 통해 인간의 인지기능을 인공지능에 이식하여 뇌 기반 인공지능을 실현하는 사례를 보였고, 이를 통해 인간의 고위 수준 인지를 적절한 방향으로 유도할 수 있는 새로운 인간-인공지능 상호작용 패러다임을 제시했다ˮ라고 강조하며, 추후 "인간중심 인공지능 연구 개발뿐만 아니라 바이오메디컬 분야, 특히 정신 건강과 관련된 디지털 치료 분야에 적용했을 때 큰 파급력을 보일 것ˮ이라고 말했다.
연구 책임자인 이상완 교수는 "이번 기술의 잠재력은 인공지능의 방대한 지식을 인간이 빠르게 흡수할 수 있는 형태로 변환할 수 있다는 데 있다ˮ며, "챗 GPT, GPT-4와 같은 언어 인공지능에서 추출되는 다양한 정보를 인간이 빠르게 추론 학습할 수 있게 변환하거나, 게임이나 가상현실의 콘텐츠를 인간의 추론 과정에 맞게 최적화해 몰입도를 높일 수 있고, 반대로 몰입도를 적절한 수준에서 제어할 경우 중독을 완화하는 효과를 기대할 수 있다ˮ라고 말했다.
관련 기술은 국내 및 해외에 특허 출원된 상태이며, KAIST 기술설명회(테크페어)에 소개된 바 있다. 이상완 교수 연구팀은 이러한 뇌 기반 인공지능 원천기술의 파급력을 높이기 위해 2019년 KAIST 신경과학-인공지능 융합연구센터를 설립하고, 구글 딥마인드, 마이크로소프트 연구소, IBM 연구소, 옥스퍼드 대학 등 다양한 해외 연구팀들과 함께 국제공동연구를 수행해 오고 있다.
이번 연구는 `시뮬레이션 기반 실험 디자인을 이용한 인간의 인과관계 추론과정 제어'라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 1월 호 온라인판에 1월 30일 자 게재됐다. (논문명: Controlling human causal inference through in-silico task design)
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 SW스타랩 및 한국연구재단의 지원을 받아 수행됐다.
인공지능으로 인간 추론 능력 극대화시키다
최근 인공지능 기술이 인식, 생성, 제어, 대화와 같은 실제 문제를 빠르게 해결해 나감에 따라 인간의 역할과 일자리 생태계가 변화하고 있다. 인공지능의 발전 속도를 본다면 가까운 미래에는 인공지능이 인간보다 똑똑해질 수도 있다. 이와 반대로 인공지능을 이용해 인간의 사고력 자체를 향상시킬 순 없을까?
우리 대학 뇌인지과학과 이상완 교수(신경과학-인공지능 융합연구센터장) 연구팀이 인간의 빠른 추론 능력을 유도해 인과관계의 학습 효율을 향상할 수 있는 뇌 기반 인공지능 기술 개발에 성공했다고 31일 밝혔다.
우리는 일상생활에서 다양한 사건을 경험하며 세상의 다양한 요소에 대한 인과관계를 학습해 나가고, 공부할 때는 지식 조각들을 조합하며 통합적인 지식을 습득한다. 이러한 과정은 점진적으로 추론하는 베이시안 모델 또는 특정한 상황에서 한 번의 경험으로부터 빠르게 결론을 도출하는 고속추론 또는 원샷 추론이 있다.
연구팀은 이전 연구에서 인간의 원샷 추론 과정을 모델링하고 전두엽과 해마가 이러한 과정에 관여하고 있음을 규명한 바 있다. 이번 연구에서 이 모델에 인간의 원샷 추론 과정을 특정한 상태로 유도하기 위해 알파고에 사용된 바 있는 심층 강화학습 기술을 접목했다. 이는 강화학습 알고리즘이 인간의 원샷 추론 과정을 수없이 시뮬레이션하면서 전두엽과 해마가 가장 효율적으로 학습할 수 있는 최적의 조건을 탐색하는 과정으로 볼 수 있다.
연구팀은 126명의 인간 피험자를 대상으로 한 인과관계 학습 및 추론 실험에서 제안 기술을 사용해 학습했을 때 단순 반복 학습 대비 최대 약 40%까지 학습 효율이 향상됨을 보였다. 더 나아가 오랜 시간에 걸쳐 신중하게 학습하거나 몇 가지 단서만을 조합해 빠르게 결론을 도출하는 것 같은 개인별 학습 성향을 고려한 맞춤형 설계가 가능함을 보였다.
인간의 사고체계에 대한 뇌과학적인 이해를 바탕으로 원샷 추론과 같은 인간의 잠재적 능력을 극대화하는 이 기술은 차세대 인공지능의 중요한 도전과제 중 하나이며, 뇌 기반 인공지능 기술은 인간과 유사한 사고체계를 바탕으로 가치판단을 할 수 있으므로 장기적으로 인간과 인공지능이 협업하는 분야에서 인공지능의 신뢰성 및 윤리성을 높이는 데도 기여할 수 있을 것으로 기대된다.
개발 기술은 스마트 교육, 게임 콘텐츠 개발, 추론 능력 측정, 인지훈련 등 인간의 추론 학습과 관련된 모든 분야에 적용될 수 있다. 기존 기술은 단편적인 기억회상, 특정 인지기능, 정답률 증가와 같은 행동적 측면에 집중해 왔다면, 이번 기술은 인공지능을 이용해 과거의 경험을 일반화시키는 인간의 사고체계 자체를 높이는 가능성을 확인한 최초의 사례로 평가된다.
KAIST에서 연구를 주도한 제1 저자 이지항 교수(현 상명대 서울캠퍼스 조교수)는 "이번 연구를 통해 인간의 인지기능을 인공지능에 이식하여 뇌 기반 인공지능을 실현하는 사례를 보였고, 이를 통해 인간의 고위 수준 인지를 적절한 방향으로 유도할 수 있는 새로운 인간-인공지능 상호작용 패러다임을 제시했다ˮ라고 강조하며, 추후 "인간중심 인공지능 연구 개발뿐만 아니라 바이오메디컬 분야, 특히 정신 건강과 관련된 디지털 치료 분야에 적용했을 때 큰 파급력을 보일 것ˮ이라고 말했다.
연구 책임자인 이상완 교수는 "이번 기술의 잠재력은 인공지능의 방대한 지식을 인간이 빠르게 흡수할 수 있는 형태로 변환할 수 있다는 데 있다ˮ며, "챗 GPT, GPT-4와 같은 언어 인공지능에서 추출되는 다양한 정보를 인간이 빠르게 추론 학습할 수 있게 변환하거나, 게임이나 가상현실의 콘텐츠를 인간의 추론 과정에 맞게 최적화해 몰입도를 높일 수 있고, 반대로 몰입도를 적절한 수준에서 제어할 경우 중독을 완화하는 효과를 기대할 수 있다ˮ라고 말했다.
관련 기술은 국내 및 해외에 특허 출원된 상태이며, KAIST 기술설명회(테크페어)에 소개된 바 있다. 이상완 교수 연구팀은 이러한 뇌 기반 인공지능 원천기술의 파급력을 높이기 위해 2019년 KAIST 신경과학-인공지능 융합연구센터를 설립하고, 구글 딥마인드, 마이크로소프트 연구소, IBM 연구소, 옥스퍼드 대학 등 다양한 해외 연구팀들과 함께 국제공동연구를 수행해 오고 있다.
이번 연구는 `시뮬레이션 기반 실험 디자인을 이용한 인간의 인과관계 추론과정 제어'라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 1월 호 온라인판에 1월 30일 자 게재됐다. (논문명: Controlling human causal inference through in-silico task design)
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 SW스타랩 및 한국연구재단의 지원을 받아 수행됐다.
2024.01.31
조회수 7146
-
 지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
2024.01.30
조회수 9428
-
 알츠하이머 발병 과정을 관찰하다
퇴행성 질환을 유발하는 아밀로이드 섬유 단백질의 초기 불안정한 움직임과 같은 생명 현상을 분자 수준에서 실시간 관찰이 가능한 기술이 개발되었다. 이를 통해 알츠하이머나 파킨슨 병과 같은 퇴행성 질환의 발병 과정에 대한 실마리를 제공할 수 있을 것으로 기대된다.
우리 대학 신소재공학과 육종민 교수 연구팀이 한국기초과학지원연구원, 포항산업과학연구원, 성균관대학교 약학대학 연구팀과 함께 그래핀을 이용해 알츠하이머 질병을 유발한다고 알려진 아밀로이드 섬유 단백질의 실시간 거동을 관찰할 수 있는 새로운 단분자 관찰 기술(single-molecule technique)을 개발했다고 30일 밝혔다.
단분자 관찰 기술은 단일 분자 수준에서 발생하는 현상을 관찰할 수 있는 기법을 말한다. 생체 과정에서 수반되는 단백질 간의 상호작용, 접힘, 조립 과정 등을 이해하는 데 핵심적인 기술이다. 현재까지 단분자 관찰 기술로는 특정 분자를 식별하기 위한 형광 현미경을 이용해 관찰하거나, 단백질을 급속 냉동시켜 움직임을 고정해 분자 구조를 해석하는 초저온 전자현미경 기법이 활용 돼왔다.
하지만, 자연 그대로의 단백질을 특별한 전처리 없이 분자 단위에서 실시간으로 관찰할 수 있는 기술은 여전히 부재한 상황이었다.
최근 이에 대한 대안으로 물질을 얼리지 않고 상온 상태에서 관찰하는 액상 전자현미경 기술이 최근 주목을 받고 있다. 이 기술은 얇은 투과막을 이용해 액체를 감싸 전자현미경 내에서 물질의 변화를 관찰할 수 있는 기술이지만, 두꺼운 투과 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성은 해결해야 하는 숙제였다.
육종민 교수 연구팀은 차세대 소재로 주목받고 있는 그래핀을 이용해 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성 문제를 해결하며, 단백질의 거동을 실시간 관찰할 수 있는 단분자 그래핀 액상 셀 전자현미경 기술을 개발했다. [그림 1]
이번 연구에서 투과 막으로 이용한 그래핀은 원자 단위의 두께를 가지고 있어 분자 수준 관찰을 가능하게 할 뿐만 아니라, 전자빔에 의한 단백질의 산화를 방지하는 산화 방지 역할을 해 기존 대비 40배 가량 변성을 억제해 단백질의 거동을 실시간으로 관찰할 수 있게 했다.
연구팀은 개발한 전자현미경 기술을 활용해, 알츠하이머 질병을 유발한다고 알려진 아밀로이드 베타 섬유의 초기 성장 과정에서 발현되는 분자 불안정성을 세계 최초로 관찰했다. [그림 2]
이 전자현미경 기술은 온전한 단백질의 다양한 거동들을 분자 수준에서 관찰을 가능하게 하므로, 코로나19와 같은 바이러스성 단백질의 감염 과정, 퇴행성 질환을 일으키는 아밀로이드성 단백질의 섬유화/응집 거동 등과 같이 단백질의 상호작용에 의한 생명 현상을 이해하는 데 활용될 수 있을 것으로 기대된다.
육 교수는 "현미경 기술의 발전은 생명과학 및 공학 기술 발전의 토대가 되는 것으로, 분자 단위의 현상을 관찰할 수 있다면 단백질들의 상호작용을 이해하고 조절할 수 있는 실마리를 제공할 수 있으며, 이를 통해 알츠하이머와 같은 퇴행성 질환의 신약 개발에 도움을 줄 수 있을 것으로 기대한다ˮ 라고 말했다.
우리 대학 신소재공학과 졸업생 박정재 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 머티리얼스(Advanced Materials)' 지난 11월 온라인으로 발표됐다. (논문명 : Single-Molecule Graphene Liquid Cell Electron Microscopy for Instability of Intermediate Amyloid Fibrils).
이번 연구는 한국연구재단의 중견연구자지원사업(MIST) (NRF-2022R1A2C2008929)과 나노 및 소재 기술개발사업(MIST)(NRF-2021M3H4A6A02050365)의 지원을 받아 수행됐다.
알츠하이머 발병 과정을 관찰하다
퇴행성 질환을 유발하는 아밀로이드 섬유 단백질의 초기 불안정한 움직임과 같은 생명 현상을 분자 수준에서 실시간 관찰이 가능한 기술이 개발되었다. 이를 통해 알츠하이머나 파킨슨 병과 같은 퇴행성 질환의 발병 과정에 대한 실마리를 제공할 수 있을 것으로 기대된다.
우리 대학 신소재공학과 육종민 교수 연구팀이 한국기초과학지원연구원, 포항산업과학연구원, 성균관대학교 약학대학 연구팀과 함께 그래핀을 이용해 알츠하이머 질병을 유발한다고 알려진 아밀로이드 섬유 단백질의 실시간 거동을 관찰할 수 있는 새로운 단분자 관찰 기술(single-molecule technique)을 개발했다고 30일 밝혔다.
단분자 관찰 기술은 단일 분자 수준에서 발생하는 현상을 관찰할 수 있는 기법을 말한다. 생체 과정에서 수반되는 단백질 간의 상호작용, 접힘, 조립 과정 등을 이해하는 데 핵심적인 기술이다. 현재까지 단분자 관찰 기술로는 특정 분자를 식별하기 위한 형광 현미경을 이용해 관찰하거나, 단백질을 급속 냉동시켜 움직임을 고정해 분자 구조를 해석하는 초저온 전자현미경 기법이 활용 돼왔다.
하지만, 자연 그대로의 단백질을 특별한 전처리 없이 분자 단위에서 실시간으로 관찰할 수 있는 기술은 여전히 부재한 상황이었다.
최근 이에 대한 대안으로 물질을 얼리지 않고 상온 상태에서 관찰하는 액상 전자현미경 기술이 최근 주목을 받고 있다. 이 기술은 얇은 투과막을 이용해 액체를 감싸 전자현미경 내에서 물질의 변화를 관찰할 수 있는 기술이지만, 두꺼운 투과 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성은 해결해야 하는 숙제였다.
육종민 교수 연구팀은 차세대 소재로 주목받고 있는 그래핀을 이용해 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성 문제를 해결하며, 단백질의 거동을 실시간 관찰할 수 있는 단분자 그래핀 액상 셀 전자현미경 기술을 개발했다. [그림 1]
이번 연구에서 투과 막으로 이용한 그래핀은 원자 단위의 두께를 가지고 있어 분자 수준 관찰을 가능하게 할 뿐만 아니라, 전자빔에 의한 단백질의 산화를 방지하는 산화 방지 역할을 해 기존 대비 40배 가량 변성을 억제해 단백질의 거동을 실시간으로 관찰할 수 있게 했다.
연구팀은 개발한 전자현미경 기술을 활용해, 알츠하이머 질병을 유발한다고 알려진 아밀로이드 베타 섬유의 초기 성장 과정에서 발현되는 분자 불안정성을 세계 최초로 관찰했다. [그림 2]
이 전자현미경 기술은 온전한 단백질의 다양한 거동들을 분자 수준에서 관찰을 가능하게 하므로, 코로나19와 같은 바이러스성 단백질의 감염 과정, 퇴행성 질환을 일으키는 아밀로이드성 단백질의 섬유화/응집 거동 등과 같이 단백질의 상호작용에 의한 생명 현상을 이해하는 데 활용될 수 있을 것으로 기대된다.
육 교수는 "현미경 기술의 발전은 생명과학 및 공학 기술 발전의 토대가 되는 것으로, 분자 단위의 현상을 관찰할 수 있다면 단백질들의 상호작용을 이해하고 조절할 수 있는 실마리를 제공할 수 있으며, 이를 통해 알츠하이머와 같은 퇴행성 질환의 신약 개발에 도움을 줄 수 있을 것으로 기대한다ˮ 라고 말했다.
우리 대학 신소재공학과 졸업생 박정재 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 머티리얼스(Advanced Materials)' 지난 11월 온라인으로 발표됐다. (논문명 : Single-Molecule Graphene Liquid Cell Electron Microscopy for Instability of Intermediate Amyloid Fibrils).
이번 연구는 한국연구재단의 중견연구자지원사업(MIST) (NRF-2022R1A2C2008929)과 나노 및 소재 기술개발사업(MIST)(NRF-2021M3H4A6A02050365)의 지원을 받아 수행됐다.
2024.01.30
조회수 7682
-
 양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.01.29
조회수 7288
-
 금이 간 뼈에 ‘뼈 반창고’ 신소재 개발
뼈 재생은 복잡하며 기존의 골 이식 및 성장 인자 전달 등과 같은 재생을 할 경우 높은 단가 발생 등의 한계가 있었는데 뼈조직의 성장을 촉진하기 위한 압전 물질이 개발되었다.
우리 대학 신소재공학과 홍승범 교수 연구팀이 전남대학교 융합바이오시스템기계공학과 김장호 교수 연구팀과 협업을 통해 하이드록시아파타이트(HAp)의 고유한 골 형성 능력을 활용하여 압력을 가했을 때 전기적 신호가 발생하는 생체 모방 지지체를 개발했다고 25일 밝혔다.
하이드록시아파타이트(HAp)란 뼈나 치아에서 발견되는 염기성 인산칼슘으로 생체 친화적인 특징이 있으며, 충치를 예방하는 특성이 있어 치약에도 쓰이는 미네랄 물질이다.
이전의 압전 지지체 관련 연구들은 압전성이 뼈 재생을 촉진하고 골 융합을 향상하는 효과를 다양한 고분자 기반 소재에서 확인했지만, 최적의 골조직 재생에 필요한 복잡한 세포 환경을 모사하는 데 한계가 있었다. 그러나 이번 연구는 하이드록시아파타이트(HAp) 고유의 골 형성 능력을 활용해 생체의 골조직 환경을 모방하는 소재를 개발한 것으로, 연구팀은 새로운 방법을 제시했다.
연구팀은 하이드록시아파타이트(HAp)를 고분자 필름과 융합하는 제조 공정을 개발했다. 이 공정으로 제작된 유연하고 독립적인 지지체는 실험 쥐를 대상으로 한 체외 및 체내 실험에서 뼈 재생을 가속하는 놀라운 잠재력을 입증했다.
또한, 연구팀은 동 지지체의 골 재생 효과의 원인을 다각도로 밝혀냈다. 원자간력 현미경(AFM) 분석을 통해 지지체의 전기적 특성을 조사했으며, 세포 모양과 세포 골격 단백질 형성에 대한 상세한 표면 특성 평가를 진행했다. 또한, 압전 및 표면적 요소가 성장 인자 발현에 어떤 영향을 미치는지 조사했다.
신소재공학과 홍승범 교수는 "뼈의 재생 속도를 가속화시키는 효과를 통해 `뼈 반창고' 같은 역할을 하는 하이드록시아파타이트(HAp) 융합 압전성 복합소재를 개발했다ˮ며, "이번 연구는 생체 재료 설계에 새로운 방향성을 제시하는 데에 그치지 않고, 압전성과 표면적 특성이 뼈 재생에 미치는 영향을 탐구한 데에 의의가 있다ˮ 라고 강조했다.
홍승범 교수 연구팀 소속 주소연 박사과정 학생, 김소연 석사가 공동 제1 저자로 참여한 이번 연구는 2024년 1월 4일 국제학술지 `ACS Applied Materials & Interfaces'에 게재됐다. 또한, 김장호 교수팀의 권용현 박사과정 학생이 공동 제1 저자로, 김장호 교수가 공동교신저자로 기여했다. (논문 제목: Piezoelectrically and Topographically Engineered Scaffolds for Accelerating Bone Regeneration).
해당 연구는 KAIST 연구진흥팀, KUSTAR-KAIST 공동연구센터, KAIST의 글로벌 특이점 사업과 정부의 재원으로 한국연구재단 기초연구사업(NRF2022M3A9E4017151, NRF-2022K1A4A7A04095892, RS2023-00247245, NRF-2021R1A4A3025206)의 지원을 받아 수행됐다.
금이 간 뼈에 ‘뼈 반창고’ 신소재 개발
뼈 재생은 복잡하며 기존의 골 이식 및 성장 인자 전달 등과 같은 재생을 할 경우 높은 단가 발생 등의 한계가 있었는데 뼈조직의 성장을 촉진하기 위한 압전 물질이 개발되었다.
우리 대학 신소재공학과 홍승범 교수 연구팀이 전남대학교 융합바이오시스템기계공학과 김장호 교수 연구팀과 협업을 통해 하이드록시아파타이트(HAp)의 고유한 골 형성 능력을 활용하여 압력을 가했을 때 전기적 신호가 발생하는 생체 모방 지지체를 개발했다고 25일 밝혔다.
하이드록시아파타이트(HAp)란 뼈나 치아에서 발견되는 염기성 인산칼슘으로 생체 친화적인 특징이 있으며, 충치를 예방하는 특성이 있어 치약에도 쓰이는 미네랄 물질이다.
이전의 압전 지지체 관련 연구들은 압전성이 뼈 재생을 촉진하고 골 융합을 향상하는 효과를 다양한 고분자 기반 소재에서 확인했지만, 최적의 골조직 재생에 필요한 복잡한 세포 환경을 모사하는 데 한계가 있었다. 그러나 이번 연구는 하이드록시아파타이트(HAp) 고유의 골 형성 능력을 활용해 생체의 골조직 환경을 모방하는 소재를 개발한 것으로, 연구팀은 새로운 방법을 제시했다.
연구팀은 하이드록시아파타이트(HAp)를 고분자 필름과 융합하는 제조 공정을 개발했다. 이 공정으로 제작된 유연하고 독립적인 지지체는 실험 쥐를 대상으로 한 체외 및 체내 실험에서 뼈 재생을 가속하는 놀라운 잠재력을 입증했다.
또한, 연구팀은 동 지지체의 골 재생 효과의 원인을 다각도로 밝혀냈다. 원자간력 현미경(AFM) 분석을 통해 지지체의 전기적 특성을 조사했으며, 세포 모양과 세포 골격 단백질 형성에 대한 상세한 표면 특성 평가를 진행했다. 또한, 압전 및 표면적 요소가 성장 인자 발현에 어떤 영향을 미치는지 조사했다.
신소재공학과 홍승범 교수는 "뼈의 재생 속도를 가속화시키는 효과를 통해 `뼈 반창고' 같은 역할을 하는 하이드록시아파타이트(HAp) 융합 압전성 복합소재를 개발했다ˮ며, "이번 연구는 생체 재료 설계에 새로운 방향성을 제시하는 데에 그치지 않고, 압전성과 표면적 특성이 뼈 재생에 미치는 영향을 탐구한 데에 의의가 있다ˮ 라고 강조했다.
홍승범 교수 연구팀 소속 주소연 박사과정 학생, 김소연 석사가 공동 제1 저자로 참여한 이번 연구는 2024년 1월 4일 국제학술지 `ACS Applied Materials & Interfaces'에 게재됐다. 또한, 김장호 교수팀의 권용현 박사과정 학생이 공동 제1 저자로, 김장호 교수가 공동교신저자로 기여했다. (논문 제목: Piezoelectrically and Topographically Engineered Scaffolds for Accelerating Bone Regeneration).
해당 연구는 KAIST 연구진흥팀, KUSTAR-KAIST 공동연구센터, KAIST의 글로벌 특이점 사업과 정부의 재원으로 한국연구재단 기초연구사업(NRF2022M3A9E4017151, NRF-2022K1A4A7A04095892, RS2023-00247245, NRF-2021R1A4A3025206)의 지원을 받아 수행됐다.
2024.01.25
조회수 8451
-
 땀에도 강한 웨어러블 로봇 제어 센서 선보이다
노인, 뇌졸중 환자, 외상 환자들의 다양한 재활치료에 활용되는 웨어러블 로봇이 착용자의 땀, 각질 등에도 끄떡없이 장기간 안정적으로 제어 가능하도록 도와주는 근전도 센서 기술이 개발되어 화제다.
우리 대학 전기및전자공학부 정재웅 교수와 기계공학과 김정 교수 연구팀이 공동 연구를 통해 피부 상태에 영향을 받지 않는 고품질의 전기 생리 신호 측정이 가능한 신축·접착성 마이크로니들 센서를 개발하는 데 성공했다고 23일 밝혔다.
다양한 재활치료에 활용되는 웨어러블 로봇이 사람의 움직임 의도를 인식하기 위해서는 몸에서 발생하는 근전도를 정확하게 측정하는 웨어러블 전기 생리 센서가 필요하다. 하지만 기존의 센서들은 시간에 따라 신호의 품질이 떨어지거나, 피부의 털, 각질, 땀 등의 영향을 많이 받고, 나아가 피부보다 단단한 물성으로 움직임 시 피부 변형을 따라갈 수 없어 노이즈(신호 잡음)를 발생시킬 수 있다. 이러한 단점들은 장시간의 신뢰성 높은 웨어러블 로봇 제어를 힘들게 한다.
이번에 개발된 기술은 잘 늘어나며 접착성이 있는 전도성 기판에 피부 각질층을 통과할 수 있는 마이크로니들 어레이를 집적해 불편함 없이 장기간 고품질의 근전도 측정을 가능하게 할 것으로 예상된다. 이와 같은 우수한 성능을 통해 땀, 각질 등을 제거하는 피부 준비 작업을 거치지 않아도 시간에 따른 착용자의 피부 상태 변화에 상관없이 웨어러블 로봇을 안정적으로 제어할 수 있을 것이라 기대된다.
연구팀은 부드러운 실리콘 중합체 기판을 활용해서 마이크로니들을 집적해 신축·접착성 마이크로니들 센서를 제작했다. 단단한 마이크로니들이 높은 저항을 가진 피부의 각질층을 투과해 피부 접촉 저항을 효과적으로 낮춰 털, 각질, 땀, 이물질로 피부가 오염돼도 고품질의 전기 생리 신호를 얻을 수 있다. 동시에 부드러운 전도성 접착 기판이 사람의 움직임으로 인한 피부의 늘어남에 순응해 편안한 착용감을 제공하고 움직임으로 인한 동작 잡음을 최소화할 수 있다.
연구팀은 개발된 신축·접착성 마이크로니들 센서 패치의 효용성을 검증하기 위해 웨어러블 로봇을 이용한 동작 보조 실험을 진행했다. 다리에 부착된 신축·접착성 마이크로니들 센서 패치는 근육에서 발생하는 전기신호를 감지하고 동작 의도를 웨어러블 로봇에 전송해 사람이 무거운 짐을 손쉽게 들어올릴 수 있도록 도와준다.
마이크로니들 센서 패치를 사용했을 때 피부 상태, 신체 움직임의 크기 및 종류와 상관없이 안정적인 근전도 센싱에 기반한 동작 의도 인식을 통해 웨어러블 로봇이 사용자의 동작을 효과적으로 보조할 수 있음을 연구팀은 확인했다.
이번 연구를 주도한 정재웅 교수는 “개발된 신축·접착성 마이크로니들 센서는 피부 상태에 영향받지 않는 안정적인 근전도 센싱을 통해 더욱 정확하고 안정적인 웨어러블 로봇 제어를 가능하게 하여 로봇을 활용하는 환자의 재활을 더 용이하게 할 수 있을 것이다”라고 말했다.
전기및전자공학부 김희수 박사과정과 이주현 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 1월 17일 字에 게재됐다.
(논문명 : Skin-preparation-free, stretchable microneedle adhesive patches for reliable electrophysiological sensing and exoskeleton robot control)
한편 이번 연구는 한국연구재단이 추진하는 생체신호센서융합기술개발사업, 전자약기술개발사업, 4단계 BK21 사업의 지원을 받아 수행됐다.
땀에도 강한 웨어러블 로봇 제어 센서 선보이다
노인, 뇌졸중 환자, 외상 환자들의 다양한 재활치료에 활용되는 웨어러블 로봇이 착용자의 땀, 각질 등에도 끄떡없이 장기간 안정적으로 제어 가능하도록 도와주는 근전도 센서 기술이 개발되어 화제다.
우리 대학 전기및전자공학부 정재웅 교수와 기계공학과 김정 교수 연구팀이 공동 연구를 통해 피부 상태에 영향을 받지 않는 고품질의 전기 생리 신호 측정이 가능한 신축·접착성 마이크로니들 센서를 개발하는 데 성공했다고 23일 밝혔다.
다양한 재활치료에 활용되는 웨어러블 로봇이 사람의 움직임 의도를 인식하기 위해서는 몸에서 발생하는 근전도를 정확하게 측정하는 웨어러블 전기 생리 센서가 필요하다. 하지만 기존의 센서들은 시간에 따라 신호의 품질이 떨어지거나, 피부의 털, 각질, 땀 등의 영향을 많이 받고, 나아가 피부보다 단단한 물성으로 움직임 시 피부 변형을 따라갈 수 없어 노이즈(신호 잡음)를 발생시킬 수 있다. 이러한 단점들은 장시간의 신뢰성 높은 웨어러블 로봇 제어를 힘들게 한다.
이번에 개발된 기술은 잘 늘어나며 접착성이 있는 전도성 기판에 피부 각질층을 통과할 수 있는 마이크로니들 어레이를 집적해 불편함 없이 장기간 고품질의 근전도 측정을 가능하게 할 것으로 예상된다. 이와 같은 우수한 성능을 통해 땀, 각질 등을 제거하는 피부 준비 작업을 거치지 않아도 시간에 따른 착용자의 피부 상태 변화에 상관없이 웨어러블 로봇을 안정적으로 제어할 수 있을 것이라 기대된다.
연구팀은 부드러운 실리콘 중합체 기판을 활용해서 마이크로니들을 집적해 신축·접착성 마이크로니들 센서를 제작했다. 단단한 마이크로니들이 높은 저항을 가진 피부의 각질층을 투과해 피부 접촉 저항을 효과적으로 낮춰 털, 각질, 땀, 이물질로 피부가 오염돼도 고품질의 전기 생리 신호를 얻을 수 있다. 동시에 부드러운 전도성 접착 기판이 사람의 움직임으로 인한 피부의 늘어남에 순응해 편안한 착용감을 제공하고 움직임으로 인한 동작 잡음을 최소화할 수 있다.
연구팀은 개발된 신축·접착성 마이크로니들 센서 패치의 효용성을 검증하기 위해 웨어러블 로봇을 이용한 동작 보조 실험을 진행했다. 다리에 부착된 신축·접착성 마이크로니들 센서 패치는 근육에서 발생하는 전기신호를 감지하고 동작 의도를 웨어러블 로봇에 전송해 사람이 무거운 짐을 손쉽게 들어올릴 수 있도록 도와준다.
마이크로니들 센서 패치를 사용했을 때 피부 상태, 신체 움직임의 크기 및 종류와 상관없이 안정적인 근전도 센싱에 기반한 동작 의도 인식을 통해 웨어러블 로봇이 사용자의 동작을 효과적으로 보조할 수 있음을 연구팀은 확인했다.
이번 연구를 주도한 정재웅 교수는 “개발된 신축·접착성 마이크로니들 센서는 피부 상태에 영향받지 않는 안정적인 근전도 센싱을 통해 더욱 정확하고 안정적인 웨어러블 로봇 제어를 가능하게 하여 로봇을 활용하는 환자의 재활을 더 용이하게 할 수 있을 것이다”라고 말했다.
전기및전자공학부 김희수 박사과정과 이주현 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 1월 17일 字에 게재됐다.
(논문명 : Skin-preparation-free, stretchable microneedle adhesive patches for reliable electrophysiological sensing and exoskeleton robot control)
한편 이번 연구는 한국연구재단이 추진하는 생체신호센서융합기술개발사업, 전자약기술개발사업, 4단계 BK21 사업의 지원을 받아 수행됐다.
2024.01.23
조회수 7786
 홍정욱 교수, Elsevier ADES 저널 수석편집장 선임
건설및환경공학과 홍정욱 교수가 세계 최대의 저널 출판사인 Elsevier에서 출간하는 전산역학 분야 권위 학술지인 ‘Advances in Engineering Software’의 수석편집장(Editor-in-Chief)으로 2024년 1월 3일자로 선임됐다.
ADES 저널은 JCR의 공학(Engineering)분야 Q1으로 분류되는 우수한 저널로서 홍정욱 교수는 수석편집장 임무를 통해 투고된 논문의 우수성을 심사하고 다양한 국제적인 활동을 통하여 해당 저널의 수준을 향상시키는 역할을 수행한다.
2024.02.07 조회수 5664
홍정욱 교수, Elsevier ADES 저널 수석편집장 선임
건설및환경공학과 홍정욱 교수가 세계 최대의 저널 출판사인 Elsevier에서 출간하는 전산역학 분야 권위 학술지인 ‘Advances in Engineering Software’의 수석편집장(Editor-in-Chief)으로 2024년 1월 3일자로 선임됐다.
ADES 저널은 JCR의 공학(Engineering)분야 Q1으로 분류되는 우수한 저널로서 홍정욱 교수는 수석편집장 임무를 통해 투고된 논문의 우수성을 심사하고 다양한 국제적인 활동을 통하여 해당 저널의 수준을 향상시키는 역할을 수행한다.
2024.02.07 조회수 5664 RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2024.02.07 조회수 9665
RNA 유전자 가위 정밀제어기술로 유전자 치료 성큼
최근 유전자 치료제 개발에 있어 중요한 역할을 하는 유전자 가위(CRISPR/Cas) 기술은 DNA 편집을 통해 영구적인 치료 효과를 보일 수 있으나, 비표적 효과에 의한 생체 내 부작용에 의한 돌연변이가 발생하였을 때, 대체할 방안이 불명확하다. DNA 편집의 잠재적인 위험성을 극복하여 특이적으로 인식하고 조절할 수 있는 RNA 대상으로 하는 유전자 가위 시스템이 주목받고 있다.
우리 대학 생명과학과 허원도 교수 연구팀이 세계 최초로 RNA 유전자 가위 기술 (CRISPR/Cas13)의 활성을 화학 유전학 및 광유전학으로 조절해 시간 및 공간적으로 표적 RNA의 염기 편집을 수행하는 기술을 개발했고, 동물 모델에서의 RNA 염기 편집 효과를 입증했다고 7일 밝혔다.
허원도 교수 연구팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해, 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는 데 성공했다. 이를 통해 개발된 에디터 기술로 RNA 분해 및 RNA 염기 편집을 실시간으로 유도할 수 있으며, RNA 염기 편집의 활성을 가역적으로 조절할 수 있음을 확인했다. 또한, 기존 연구자들이 실험에 이용하던 세포모델에서 더 나아가 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 광유전학적으로 RNA 염기 편집이 효과적으로 일어나는 것을 입증했다.
이번 연구는 유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다. 특히 생체 내 전달 목적으로 주로 사용되는데 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있다는 점을 감안하여 DNA 크기 제한을 분할 시스템으로 극복하고, 실험 쥐의 기관 내에서 다양한 모델 시스템 구축을 통해 생체 내 RNA 연구의 적용 범위를 확장할 수 있다.
연구를 주도한 허원도 교수는 “재결합이 가능한 분할 단백질 Cas13 조각을 개발해, 화학적 및 광유전학적으로 특정 시공간에서 정밀하게 조절되는 RNA를 실험적으로 확인했다. 이 기술은 그동안 실험적 한계로 인해 어려웠던 복잡한 RNA 연구를 촉진할 것으로 기대된다.라고 말했다.” 아울러 “유전자 가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로, 질병과 관련된 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구의 적용에 기여할 것으로 기대된다”라고 전했다.
우리 대학 생명과학과 유정혜 박사과정이 제1 저자로 수행한 이번 연구는 저명 국제 학술지 ‘네이처 커뮤니케이션즈 (Nature Communications)’ 2024년 1월 22일 字 온라인판에 게재됐다. (논문명: Programmable RNA base editing with photoactivatable CRISPR-Cas13). (Impact Factor: 17.694). (DOI: https://doi.org/10.1038/s41467-024-44867-2)
한편, 이번 연구는 삼성미래기술육성재단과 정부의 재원으로 한국연구재단 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2024.02.07 조회수 9665 4.55V 고전압 리튬이온전지 전해액 기술 개발
전기차 시대의 가속화에 따라 1회 충전에 긴 주행거리를 가능하게 하는 고용량, 고에너지밀도 이차전지 개발과 더불어 빠르게 충전을 할 수 있는 고속 충전 기술 개발의 중요도가 커지고 있다.
우리 대학 생명화학공학과 최남순 교수 연구팀이 고전압 조건에서 리튬이온전지의 높은 효율과 에너지를 유지하고 고속 충전이 가능한 전해액 설계 기술을 개발했다고 6일 밝혔다. 개발된 전해액은 점도가 낮으면서 고전압에 안정적인 용매를 사용하였으며 안정적인 전극-전해질 계면 반응을 확보할 수 있는 첨가제 기술을 통해 리튬이온전지의 수명 특성을 획기적으로 향상시켰다.
최남순 교수 연구팀은 상용 리튬이온전지에 사용되고 있는 카보네이트 계열의 용매 대신 점도가 낮고 고전압 조건에서 안정적으로 작용할 수 있는 용매 조성 기술과 전극계면 보호 기술을 적용해 기존 연구 결과보다 현저하게 향상된 *가역 효율 (99.9% 이상)을 달성했다.
☞ 가역 효율 : 매 사이클마다 전지의 방전용량을 충전용량으로 나누어 백분율로 나타낸 값으로 배터리의 가역성을 의미함. 가역 효율이 높을수록 매 사이클마다 배터리 용량 손실이 적음을 의미함. 아무리 높은 용량을 구현하는 배터리라도 가역성이 높지 않다면 실용화가 어려움.
또한, 첫 사이클 방전 기준 용량 대비 200 사이클에서의 방전 기준 용량까지를 용량 유지율 측정하였는데 개발된 전해액 기술은 고온 (45도)에서 4.5 V의 충전 전압 조건에서 89.9%의 높은 용량 유지율을 보였으며 4.53 V의 충전 전압 조건에서도 77.0%의 높은 용량 유지율을 보였다. 개발 전해액 조성의 경우 기존 상용 최고 수준 기술 대비 약 10~15% 이상의 높은 용량 유지율을 보여줬다. 뿐만 아니라, 4.55 V의 혁신적인 충전 전압 조건에서도 200회 사이클 후 61.7%의 높은 용량 유지율을 보여주는 등 우수한 수명 특성을 보여줬다.
이번 연구에서 개발된 전해액 설계 기술은 리튬 코발트 산화물 양극을 사용해 4.5 V 이상의 고전압 그리고 1.5C (45분 충전)의 빠른 충전 조건에서 극대화된 성능을 얻었다는 점에서 그 의미가 크다. 여기에 더해 60도 고온 저장에서도 저장 성능이 향상됨도 확인했다. 특히 고에너지밀도 리튬이온전지용 전해액 기준 프레임을 제시한 바, 이는 리튬이차전지 전해액 설계에서 새로운 기준이 될 것이라고 연구진은 설명했다.
이번 논문의 공동 제1 저자인 우리 대학 생명화학공학과 김세훈 박사과정은 “높은 산화안정성 및 저점도 특성을 가지는 용매 적용에 따른 고전압 안정성 및 고속 충전 특성 향상과 전해액 첨가제에 의한 안정적인 전극-전해질 계면 형성의 시너지 효과에 의해 기존에 보고된 리튬이온전지용 전해액 기술 개발의 한계를 뛰어넘는 기술을 개발하게 됐다ˮ라고 말했다. 또한, “상용 리튬이온전지에서 사용하는 수준의 높은 로딩의 리튬 코발트 산화물 양극을 사용하여 전지의 수명 특성을 극대화했기 때문에 산업에의 빠른 적용 및 향후 고에너지밀도 전지 시스템 설계에 있어 이정표로 작용할 수 있을 것이다”라고 전했다.
최남순 교수는 "개발된 전해액 기술은 상용 용매로 사용되고 있는 카보네이트 유기용매의 부족한 고전압 내구성을 에스테르 용매로 획기적으로 극복하였으며 이를 통해 배터리 충전과정에서 가스 발생을 최소화하는 고전압 전해액 시스템을 구축했다ˮ라고 말했다. 또한, "이러한 고전압 용매 조성과 전해액 첨가제 조합 기술은 리튬이온전지의 한계 에너지밀도를 끌어올리기 위한 전해액의 고전압화를 위한 돌파기술이라는 점에서 그 의미가 크다고 하겠다ˮ라고 연구의 의미를 강조했다.
이번 연구에서 생명화학공학과 최남순 교수와 김세훈, 이정아 연구원은 리튬이온전지의 고전압 구동을 위한 새로운 전해액 조성 기술을 개발하고 이에 대한 효과를 검증하였으며 작동 메커니즘을 규명하였다. 경상국립대학교 나노신소재융합공학과 (나노·신소재공학부 고분자공학 전공) 이태경 교수와 이동규, 손준수 연구원은 전해액 용매 및 첨가제의 작동 메커니즘을 계산화학을 통해 구체화하는 연구를 진행하였다. 이번 연구는 저명한 국제 학술지 `에이시에스 에너지 레터즈 (ACS Energy Letters)'에 1월 12일자로 발간되었으며 커버 논문으로 선정되었다 (논문명 : Designing Electrolytes for Stable Operation of High-Voltage LiCoO2 in Lithium-Ion Batteries).
이번 연구 수행은 삼성 에스디아이 (Samsung SDI)의 지원을 받아 수행됐다.
2024.02.06 조회수 9832
4.55V 고전압 리튬이온전지 전해액 기술 개발
전기차 시대의 가속화에 따라 1회 충전에 긴 주행거리를 가능하게 하는 고용량, 고에너지밀도 이차전지 개발과 더불어 빠르게 충전을 할 수 있는 고속 충전 기술 개발의 중요도가 커지고 있다.
우리 대학 생명화학공학과 최남순 교수 연구팀이 고전압 조건에서 리튬이온전지의 높은 효율과 에너지를 유지하고 고속 충전이 가능한 전해액 설계 기술을 개발했다고 6일 밝혔다. 개발된 전해액은 점도가 낮으면서 고전압에 안정적인 용매를 사용하였으며 안정적인 전극-전해질 계면 반응을 확보할 수 있는 첨가제 기술을 통해 리튬이온전지의 수명 특성을 획기적으로 향상시켰다.
최남순 교수 연구팀은 상용 리튬이온전지에 사용되고 있는 카보네이트 계열의 용매 대신 점도가 낮고 고전압 조건에서 안정적으로 작용할 수 있는 용매 조성 기술과 전극계면 보호 기술을 적용해 기존 연구 결과보다 현저하게 향상된 *가역 효율 (99.9% 이상)을 달성했다.
☞ 가역 효율 : 매 사이클마다 전지의 방전용량을 충전용량으로 나누어 백분율로 나타낸 값으로 배터리의 가역성을 의미함. 가역 효율이 높을수록 매 사이클마다 배터리 용량 손실이 적음을 의미함. 아무리 높은 용량을 구현하는 배터리라도 가역성이 높지 않다면 실용화가 어려움.
또한, 첫 사이클 방전 기준 용량 대비 200 사이클에서의 방전 기준 용량까지를 용량 유지율 측정하였는데 개발된 전해액 기술은 고온 (45도)에서 4.5 V의 충전 전압 조건에서 89.9%의 높은 용량 유지율을 보였으며 4.53 V의 충전 전압 조건에서도 77.0%의 높은 용량 유지율을 보였다. 개발 전해액 조성의 경우 기존 상용 최고 수준 기술 대비 약 10~15% 이상의 높은 용량 유지율을 보여줬다. 뿐만 아니라, 4.55 V의 혁신적인 충전 전압 조건에서도 200회 사이클 후 61.7%의 높은 용량 유지율을 보여주는 등 우수한 수명 특성을 보여줬다.
이번 연구에서 개발된 전해액 설계 기술은 리튬 코발트 산화물 양극을 사용해 4.5 V 이상의 고전압 그리고 1.5C (45분 충전)의 빠른 충전 조건에서 극대화된 성능을 얻었다는 점에서 그 의미가 크다. 여기에 더해 60도 고온 저장에서도 저장 성능이 향상됨도 확인했다. 특히 고에너지밀도 리튬이온전지용 전해액 기준 프레임을 제시한 바, 이는 리튬이차전지 전해액 설계에서 새로운 기준이 될 것이라고 연구진은 설명했다.
이번 논문의 공동 제1 저자인 우리 대학 생명화학공학과 김세훈 박사과정은 “높은 산화안정성 및 저점도 특성을 가지는 용매 적용에 따른 고전압 안정성 및 고속 충전 특성 향상과 전해액 첨가제에 의한 안정적인 전극-전해질 계면 형성의 시너지 효과에 의해 기존에 보고된 리튬이온전지용 전해액 기술 개발의 한계를 뛰어넘는 기술을 개발하게 됐다ˮ라고 말했다. 또한, “상용 리튬이온전지에서 사용하는 수준의 높은 로딩의 리튬 코발트 산화물 양극을 사용하여 전지의 수명 특성을 극대화했기 때문에 산업에의 빠른 적용 및 향후 고에너지밀도 전지 시스템 설계에 있어 이정표로 작용할 수 있을 것이다”라고 전했다.
최남순 교수는 "개발된 전해액 기술은 상용 용매로 사용되고 있는 카보네이트 유기용매의 부족한 고전압 내구성을 에스테르 용매로 획기적으로 극복하였으며 이를 통해 배터리 충전과정에서 가스 발생을 최소화하는 고전압 전해액 시스템을 구축했다ˮ라고 말했다. 또한, "이러한 고전압 용매 조성과 전해액 첨가제 조합 기술은 리튬이온전지의 한계 에너지밀도를 끌어올리기 위한 전해액의 고전압화를 위한 돌파기술이라는 점에서 그 의미가 크다고 하겠다ˮ라고 연구의 의미를 강조했다.
이번 연구에서 생명화학공학과 최남순 교수와 김세훈, 이정아 연구원은 리튬이온전지의 고전압 구동을 위한 새로운 전해액 조성 기술을 개발하고 이에 대한 효과를 검증하였으며 작동 메커니즘을 규명하였다. 경상국립대학교 나노신소재융합공학과 (나노·신소재공학부 고분자공학 전공) 이태경 교수와 이동규, 손준수 연구원은 전해액 용매 및 첨가제의 작동 메커니즘을 계산화학을 통해 구체화하는 연구를 진행하였다. 이번 연구는 저명한 국제 학술지 `에이시에스 에너지 레터즈 (ACS Energy Letters)'에 1월 12일자로 발간되었으며 커버 논문으로 선정되었다 (논문명 : Designing Electrolytes for Stable Operation of High-Voltage LiCoO2 in Lithium-Ion Batteries).
이번 연구 수행은 삼성 에스디아이 (Samsung SDI)의 지원을 받아 수행됐다.
2024.02.06 조회수 9832 암, 루게릭병 등 난치성 질환 발병 기전 밝혀
단백질 정보를 가진 mRNA 유전자 조절 기전에서 알루 요소(Alu)의 중요성을 제시하고, 나아가 종양 형성, 퇴행성 뇌질환 등 mRNA가 변화하는 다양한 질환에서 역방향 알루 반복구조(IRAlus)라는 새로운 발병 원인을 최초로 제시함으로써 질병 치료에 획기적인 방안을 제시하였다.
우리 대학 생명화학공학과 김유식 교수와 바이오및뇌공학과 이영석 교수 공동 연구팀이 종양 형성과 퇴행성 뇌질환을 유발하는 새로운 유전자 조절 기전을 찾아냈다고 6일 밝혔다.
인간 유전체의 약 10%를 차지하는 반복서열인 알루 요소(Alu element, Alu)는 단백질 정보를 가지는 전령 RNA(messenger RNA, mRNA)의 단백질 생산 효율을 조절할 수 있다. 특히, mRNA가 2개의 알루 요소로 형성된 역방향 알루 반복 구조(Inverted Alu repeats, IRAlus)를 가지게 되면 mRNA의 세포 내 이동이 방해되어 단백질 생산이 감소한다.
연구팀은 질환 특이적으로 mRNA가 변화하는 과정에서 주요 mRNA가 역방향 알루 반복 구조(IRAlus)에 의해 조절받게 하고 이는 mRNA가 가지고 있는 유전자 발현 억제로 이어져 질환을 일으킨다는 새로운 발병 기전을 밝혔다.
알루(Alu)는 유전체의 단백질 정보를 가지고 있지만 유전체 상에서 본인의 서열만을 복제하는 성질이 있어 ‘이기적 서열’로 알려져 있었다. 최근 연구에 의하면 mRNA 내의 존재하는 역방향 알루 반복 구조(IRAlus)는 숙주 mRNA의 세포질로의 이동을 방해하여 해당 유전자의 단백질 번역을 억제한다. 그러나, 해당 유전자 발현 조절 기전의 생물학적 중요성에 대해서는 보고된 바가 없었다.
연구팀은 역방향 알루 반복 구조(IRAlus)를 인지할 수 있는 항체를 활용한 차세대 염기서열 분석법을 사용해 특정 세포 내 활성화된, 기능적인 역방향 알루 반복 구조(IRAlus)를 가지고 있어 역방향 알루 반복 구조(IRAlus)에 의해 단백질 합성이 억제될 수 있는 mRNA 유전자 목록을 완성했다.
종양 형성 과정에서 역방향 알루 반복 구조(IRAlus)의 유전자 조절 기전의 영향을 분석했다. 연구팀은 대표적인 종양억제유전자를 억제하는 종양 유전자 조절을 하고 이는 단백질 발현 증가로 이어지며 결과적으로 종양억제유전자 활성이 억제됨으로써 암 발달을 촉진할 수 있다.
나아가, 특정 mRNA 서열과 상보적으로 결합해 mRNA의 기능을 억제해 다양한 질병 치료 및 조절 도구로 현재 연구되고 있는 혁신 RNA 치료제인 안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, 이하 ASO)를 활용해 단백질 발현을 복구하는 암 치료 전략을 탐색했다.
연구팀은 신경계 세포에서 역방향 알루 반복 구조(IRAlus)로 인한 유전자 조절이 활발하다는 것을 확인했다. 또한, 해당 현상의 과도한 활성과 루게릭병으로 알려진 근위축성 측삭경화증을 비롯한 퇴행성 뇌질환 간의 연관성을 최초로 제시했다.
생명화학공학과 김유식 교수는 “이번 연구는 인간 유전체 내 반복서열인 역방향 알루 반복 구조(IRAlus)를 가지는 유전자를 목록화하는 것을 넘어서 해당 유전자 발현 조절이 인간 질환, 특히 종양 형성 및 퇴행성 뇌질환 발병과정에서 핵심적인 역할을 하는 것을 최초로 확인했다”면서 “이번 연구에서 제시한 역방향 알루 반복 구조(IRAlus)라는 새로운 타겟 물질을 활용하면 종양과 노화를 비롯해 다양한 퇴행성 질환의 발병 기전 분석에 근본적이고 효과적인 치료전략을 마련하는 데 유용할 것”이라고 말했다.
생명화학공학과 구자영 박사(현 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학 (Harvard Medical School) 박사후연구원)와 이건용 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 2월 2일 字에 온라인 게재됐다. (논문명 : Alternative Polyadenylation Determines the Functional Landscape of Inverted Alu Repeats).
우리 대학 생명과학과 임정훈 교수 연구팀과 의과학대학원 한진주 교수 연구팀이 참여한 이번 연구는 한국연구재단 기초연구실 지원사업과 KAIST 도약연구사업의 지원을 받아 수행됐다.
2024.02.06 조회수 6437
암, 루게릭병 등 난치성 질환 발병 기전 밝혀
단백질 정보를 가진 mRNA 유전자 조절 기전에서 알루 요소(Alu)의 중요성을 제시하고, 나아가 종양 형성, 퇴행성 뇌질환 등 mRNA가 변화하는 다양한 질환에서 역방향 알루 반복구조(IRAlus)라는 새로운 발병 원인을 최초로 제시함으로써 질병 치료에 획기적인 방안을 제시하였다.
우리 대학 생명화학공학과 김유식 교수와 바이오및뇌공학과 이영석 교수 공동 연구팀이 종양 형성과 퇴행성 뇌질환을 유발하는 새로운 유전자 조절 기전을 찾아냈다고 6일 밝혔다.
인간 유전체의 약 10%를 차지하는 반복서열인 알루 요소(Alu element, Alu)는 단백질 정보를 가지는 전령 RNA(messenger RNA, mRNA)의 단백질 생산 효율을 조절할 수 있다. 특히, mRNA가 2개의 알루 요소로 형성된 역방향 알루 반복 구조(Inverted Alu repeats, IRAlus)를 가지게 되면 mRNA의 세포 내 이동이 방해되어 단백질 생산이 감소한다.
연구팀은 질환 특이적으로 mRNA가 변화하는 과정에서 주요 mRNA가 역방향 알루 반복 구조(IRAlus)에 의해 조절받게 하고 이는 mRNA가 가지고 있는 유전자 발현 억제로 이어져 질환을 일으킨다는 새로운 발병 기전을 밝혔다.
알루(Alu)는 유전체의 단백질 정보를 가지고 있지만 유전체 상에서 본인의 서열만을 복제하는 성질이 있어 ‘이기적 서열’로 알려져 있었다. 최근 연구에 의하면 mRNA 내의 존재하는 역방향 알루 반복 구조(IRAlus)는 숙주 mRNA의 세포질로의 이동을 방해하여 해당 유전자의 단백질 번역을 억제한다. 그러나, 해당 유전자 발현 조절 기전의 생물학적 중요성에 대해서는 보고된 바가 없었다.
연구팀은 역방향 알루 반복 구조(IRAlus)를 인지할 수 있는 항체를 활용한 차세대 염기서열 분석법을 사용해 특정 세포 내 활성화된, 기능적인 역방향 알루 반복 구조(IRAlus)를 가지고 있어 역방향 알루 반복 구조(IRAlus)에 의해 단백질 합성이 억제될 수 있는 mRNA 유전자 목록을 완성했다.
종양 형성 과정에서 역방향 알루 반복 구조(IRAlus)의 유전자 조절 기전의 영향을 분석했다. 연구팀은 대표적인 종양억제유전자를 억제하는 종양 유전자 조절을 하고 이는 단백질 발현 증가로 이어지며 결과적으로 종양억제유전자 활성이 억제됨으로써 암 발달을 촉진할 수 있다.
나아가, 특정 mRNA 서열과 상보적으로 결합해 mRNA의 기능을 억제해 다양한 질병 치료 및 조절 도구로 현재 연구되고 있는 혁신 RNA 치료제인 안티센스 올리고뉴클레오타이드(Antisense oligonucleotide, 이하 ASO)를 활용해 단백질 발현을 복구하는 암 치료 전략을 탐색했다.
연구팀은 신경계 세포에서 역방향 알루 반복 구조(IRAlus)로 인한 유전자 조절이 활발하다는 것을 확인했다. 또한, 해당 현상의 과도한 활성과 루게릭병으로 알려진 근위축성 측삭경화증을 비롯한 퇴행성 뇌질환 간의 연관성을 최초로 제시했다.
생명화학공학과 김유식 교수는 “이번 연구는 인간 유전체 내 반복서열인 역방향 알루 반복 구조(IRAlus)를 가지는 유전자를 목록화하는 것을 넘어서 해당 유전자 발현 조절이 인간 질환, 특히 종양 형성 및 퇴행성 뇌질환 발병과정에서 핵심적인 역할을 하는 것을 최초로 확인했다”면서 “이번 연구에서 제시한 역방향 알루 반복 구조(IRAlus)라는 새로운 타겟 물질을 활용하면 종양과 노화를 비롯해 다양한 퇴행성 질환의 발병 기전 분석에 근본적이고 효과적인 치료전략을 마련하는 데 유용할 것”이라고 말했다.
생명화학공학과 구자영 박사(현 보스턴 아동병원 (Boston Children’s Hospital) 및 하버드 의과대학 (Harvard Medical School) 박사후연구원)와 이건용 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 셀(Cell) 자매지인 ‘몰레큘러 셀(Molecular Cell)’ 2월 2일 字에 온라인 게재됐다. (논문명 : Alternative Polyadenylation Determines the Functional Landscape of Inverted Alu Repeats).
우리 대학 생명과학과 임정훈 교수 연구팀과 의과학대학원 한진주 교수 연구팀이 참여한 이번 연구는 한국연구재단 기초연구실 지원사업과 KAIST 도약연구사업의 지원을 받아 수행됐다.
2024.02.06 조회수 6437 차세대 2차원 반도체 다기능 전자 소자 개발
공급 전압에 의한 2차원 반도체의 극성 전환을 이용해 새로운 전자 소자로의 응용이 보고된 바 있으나, 모두 누설 전류가 크거나 낮은 전류점멸비로 인해 실제 집적 회로(IC)칩에서 사용하기 어려웠다. 우리 대학 연구팀은 다기능 전자 소자를 통해 프로그램 및 기능성 변환이 가능한 회로 구현의 가능성을 제시하고 IC칩에서의 2차원 반도체의 활용성을 확장하는 기술을 개발하였다.
우리 대학 전기및전자공학부 이가영 교수 연구팀이 양극성 반도체 특성을 가진 2차원 나노 반도체 기반의 다기능 전자 소자를 개발했다고 2일 밝혔다. 다기능 전자 소자란 기존 트랜지스터와 달리 전압에 따라 기능을 변환할 수 있는 소자로, 연구팀의 소자는 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광 감지 소자로 변환 가능하여 폭 넓은 사용이 가능하다.
기존 실리콘 반도체보다 성능이 뛰어난 이황화 몰리브덴(MoS2)는 층상 구조의 2차원 반도체 나노 소재로, 전자가 흐르는 N형 반도체 특성을 가지면서 대기에서 안정적이다. 또한, 기존 실리콘 반도체가 미세화될수록 성능 저하에 취약함에 반해, 이황화 몰리브덴은 관련 문제가 적어 차세대 반도체로서 학계뿐만 아니라 삼성, TSMC, 인텔과 같은 산업계에서의 연구도 활발하다.
그러나 상보적 금속산화막 반도체(CMOS) 구현을 위해서는 음(N) 전하를 띄는 전자뿐만 아니라 양(P) 전하를 띄는 정공 유도도 필요한 데, 이황화 몰리브덴에서는 정공 유도가 어려웠다. 이 문제를 해결하기 위해 이황화 몰리브덴에 추가적인 공정을 도입하거나 다른 P형 물질을 사용하는 방법이 시도됐으나, 공정 난이도가 높다. 이러한 문제점은 현재까지도 이황화 몰리브덴을 상용화하기 위해 해결해야 할 중요한 과제로 남아 있다.
이가영 교수 연구팀은 채널 하부에 전극을 배치하고 금속/반도체 접합 특성을 개선해 전자와 정공 모두 선택적으로 흐를 수 있는 양극성 특성을 구현하는 데 성공했다. 이로써 전류의 점멸 비율을 대폭 높일 뿐만 아니라, 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광감지 소자로 다기능 변조 동작이 가능한 이황화 몰리브덴 전자 소자를 개발했다. 또한 이를 기반으로 집적도가 개선된 논리 연산이 가능함도 보였다.
이번 연구를 주도한 송준기, 이수연 학생은 “기존 실리콘 금속산화막 반도체(CMOS) 공정 호환성이 높은 공정 과정을 통해 차세대 2차원 반도체의 다양한 기능을 구현했다”며 “IC칩에서 이황화 몰리브덴의 전자소자로의 활용성 및 실용성을 넓히는 계기가 될 것이다”라고 덧붙였다.
이가영 교수는 “이번에 개발한 전자 소자는 주어진 전압 특성에 따라 다양한 기능을 수행하면서도 각 기능의 성능이 우수하다”며 “서로 다른 기능의 소자들은 대개 구조와 공정 방법들이 달라 함께 집적시 공정 난이도가 높고 회로 도면 변화에 따른 공정 전환이 까다롭다. 반면, 이번에 개발한 신개념 소자는 하나의 소자에서 다기능을 할 수 있어서 현재 수요가 급증하고 있는 맞춤형 반도체의 제작 및 공정 전환을 용이하게 할 것이다. 목적에 따라 회로 자체의 기능성을 변환할 수 있어 단일 칩 시스템의 소형화에도 기여할 것으로 기대한다”라고 말했다.
우리 대학 전기및전자공학부 송준기 석박통합과정 학생과 이수연 석사과정 학생이 공동 제1 저자로 참여한 이번 연구는 나노과학 분야 저명 국제 학술지 `ACS Nano'에 2024년 1월 26일 온라인판에 출판됐다. (논문명 : Drain-induced multifunctional ambipolar electronics based on junctionless MoS2)
한편 이번 연구는 한국연구재단의 기초연구사업 및 BK21, KAIST의 C2 사업, 그리고 LX 세미콘-KAIST 미래기술센터의 지원을 받아 수행됐다.
2024.02.05 조회수 7543
차세대 2차원 반도체 다기능 전자 소자 개발
공급 전압에 의한 2차원 반도체의 극성 전환을 이용해 새로운 전자 소자로의 응용이 보고된 바 있으나, 모두 누설 전류가 크거나 낮은 전류점멸비로 인해 실제 집적 회로(IC)칩에서 사용하기 어려웠다. 우리 대학 연구팀은 다기능 전자 소자를 통해 프로그램 및 기능성 변환이 가능한 회로 구현의 가능성을 제시하고 IC칩에서의 2차원 반도체의 활용성을 확장하는 기술을 개발하였다.
우리 대학 전기및전자공학부 이가영 교수 연구팀이 양극성 반도체 특성을 가진 2차원 나노 반도체 기반의 다기능 전자 소자를 개발했다고 2일 밝혔다. 다기능 전자 소자란 기존 트랜지스터와 달리 전압에 따라 기능을 변환할 수 있는 소자로, 연구팀의 소자는 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광 감지 소자로 변환 가능하여 폭 넓은 사용이 가능하다.
기존 실리콘 반도체보다 성능이 뛰어난 이황화 몰리브덴(MoS2)는 층상 구조의 2차원 반도체 나노 소재로, 전자가 흐르는 N형 반도체 특성을 가지면서 대기에서 안정적이다. 또한, 기존 실리콘 반도체가 미세화될수록 성능 저하에 취약함에 반해, 이황화 몰리브덴은 관련 문제가 적어 차세대 반도체로서 학계뿐만 아니라 삼성, TSMC, 인텔과 같은 산업계에서의 연구도 활발하다.
그러나 상보적 금속산화막 반도체(CMOS) 구현을 위해서는 음(N) 전하를 띄는 전자뿐만 아니라 양(P) 전하를 띄는 정공 유도도 필요한 데, 이황화 몰리브덴에서는 정공 유도가 어려웠다. 이 문제를 해결하기 위해 이황화 몰리브덴에 추가적인 공정을 도입하거나 다른 P형 물질을 사용하는 방법이 시도됐으나, 공정 난이도가 높다. 이러한 문제점은 현재까지도 이황화 몰리브덴을 상용화하기 위해 해결해야 할 중요한 과제로 남아 있다.
이가영 교수 연구팀은 채널 하부에 전극을 배치하고 금속/반도체 접합 특성을 개선해 전자와 정공 모두 선택적으로 흐를 수 있는 양극성 특성을 구현하는 데 성공했다. 이로써 전류의 점멸 비율을 대폭 높일 뿐만 아니라, 양극성 트랜지스터, N형 트랜지스터, 다이오드, 항복 다이오드 그리고 광감지 소자로 다기능 변조 동작이 가능한 이황화 몰리브덴 전자 소자를 개발했다. 또한 이를 기반으로 집적도가 개선된 논리 연산이 가능함도 보였다.
이번 연구를 주도한 송준기, 이수연 학생은 “기존 실리콘 금속산화막 반도체(CMOS) 공정 호환성이 높은 공정 과정을 통해 차세대 2차원 반도체의 다양한 기능을 구현했다”며 “IC칩에서 이황화 몰리브덴의 전자소자로의 활용성 및 실용성을 넓히는 계기가 될 것이다”라고 덧붙였다.
이가영 교수는 “이번에 개발한 전자 소자는 주어진 전압 특성에 따라 다양한 기능을 수행하면서도 각 기능의 성능이 우수하다”며 “서로 다른 기능의 소자들은 대개 구조와 공정 방법들이 달라 함께 집적시 공정 난이도가 높고 회로 도면 변화에 따른 공정 전환이 까다롭다. 반면, 이번에 개발한 신개념 소자는 하나의 소자에서 다기능을 할 수 있어서 현재 수요가 급증하고 있는 맞춤형 반도체의 제작 및 공정 전환을 용이하게 할 것이다. 목적에 따라 회로 자체의 기능성을 변환할 수 있어 단일 칩 시스템의 소형화에도 기여할 것으로 기대한다”라고 말했다.
우리 대학 전기및전자공학부 송준기 석박통합과정 학생과 이수연 석사과정 학생이 공동 제1 저자로 참여한 이번 연구는 나노과학 분야 저명 국제 학술지 `ACS Nano'에 2024년 1월 26일 온라인판에 출판됐다. (논문명 : Drain-induced multifunctional ambipolar electronics based on junctionless MoS2)
한편 이번 연구는 한국연구재단의 기초연구사업 및 BK21, KAIST의 C2 사업, 그리고 LX 세미콘-KAIST 미래기술센터의 지원을 받아 수행됐다.
2024.02.05 조회수 7543 입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
2024.02.01 조회수 6297
입찰자, 판매자 모두에게 이득되는 경매?
일반적인 경매는 참여자가 늘어나면 경쟁만 심해지기 때문에 ‘친구’를 함께 데리고 갈 이유가 없다. 하지만 판매자 입장에서는 가격을 올리기 위해 친구를 ‘추천’해서 참여시켜 주길 원한다. 이렇게 판매자와 추천할 친구가 있는 입찰자의 이해관계 상충을 어떻게 해결할 수 있을까?
우리 대학 기술경영학부 정승원 교수가 성균관대학교 이주성 교수와 공동연구를 통해, 참여자가 친구를 추천할 유인(Incentive)을 제공하며, 판매자 입장에서도 기존 경매 방식들보다 높은 수익을 얻을 수 있는 새로운 경매 메커니즘 지피알(GPR, Groupwise-Pivotal Referral)을 개발했다고 2월 1일 밝혔다.
이번에 새로 개발된 지피알 경매는 판매자도 기존 경매 방식 대비 많은 이익을 가져오며, 입찰자도 자신의 친구를 추천하여 함께 참여하는 것이 항상 이득이 된다. 만약 내가 추천을 안 하더라도 낙찰을 받을 수 있으며 추천을 해서 타인이 낙찰받게 될 경우, 오히려 직접 낙찰받는 것보다 더 큰 보너스를 받게 된다.
일반적으로 많이 사용하는 비공개 입찰방식은 최고가격(First-Price)경매 또는 차순위가격(Second-Price) 경매가 있다. 최고가격 경매는 참여자 모두가 입찰가를 비공개로 적어내고, 가장 높은 가격을 적어낸 사람이 해당 가격에 낙찰을 받는 경매 방식이다. 반면, 차순위가격 경매는 최고가를 적어낸 사람이 낙찰을 받되, 두 번째로 높은 금액만 내는 경매 방식이다.
최고가격 경매의 참여자 면에서 단점은 입찰가를 정하는 것이 매우 어렵다는 점이다. 두 번째로 높은 금액보다 아주 조금만 높게 적어내는 것이 최선이지만, 두 번째로 높은 금액을 알 수가 없기 때문이다. 2014년에 최고가 경매로 팔린 한전 부지의 경우 현대차가 10조 5,500억 원에 낙찰을 받았고, 두 번째 금액으로 추정되는 삼성전자의 입찰가가 4조 6,700억 원이라 언론을 통해 알려진 바가 있다. 이렇기 때문에 규모가 큰 최고가격경매의 경우, 경쟁자의 입찰가를 알아내기 위해, 또 역으로 거짓 정보를 흘린다든지, 많은 신경전이 일어나기도 한다.
차순위가격 경매의 경우, 경쟁자가 어떻게 입찰하든지 간에 상관없이 각 참여자가 자신의 실제 가치를 입찰하는 것이 본인한테도 최선이 되는, 유인합치성(incentive compatibility)이라고 불리는 좋은 성질이 있다. 차순위가격 경매는 이를 연구한 노벨경제학 수상자 월리엄 비크리(William Vickrey)의 이름을 따서, 비크리 경매라고도 부른다.
일반적인 환경의 비크리 경매에서는 각 참여자가 자신의 외부효과만큼 지불하는데 이를 통해 유인합치성이 만족되게 된다. 하지만 추천을 통해 비크리 경매에 참여하는 경우, 과도한 추천 보너스 지급으로 인해 정작 판매자의 수익이 마이너스가 되는 경우가 발생할 수 있는 결정적인 단점이 있다.
이번에 새로 개발된 지피알 경매의 경우, 외부효과를 추천 네트워크상의 그룹별로 계산함으로써, 여러 좋은 성질을 가지게 된다.
연구에 참여한 우리 대학 경영대학 기술경영학부 정승원 교수는 “이번 연구는 입찰자 입장에서도 손해 볼 걱정없이 다른 입찰자들을 추천해서 참여시킬 수 있고, 판매자 입장에서도 마이너스 수익이 발생하지 않음은 물론, 기존의 여러 경매 방식보다 수익이 항상 더 크게 나오는 경매 방식을 최초로 제시한다는 점에서 의미가 있다”며 “또한 모든 수익을 판매자와 직접 연결된 입찰자와 판매자 둘이서만 나눠 가지게 되는 GPR 메커니즘의 내쉬 균형(Nash Equilibrium)의 경우, 마치 원청업체가 하청업체보다 높은 수익을 얻는 상황의 극한값으로도 설명될 수 있다”고 말했다.
이번 연구 결과는 국제 학술지 `Games and Economic Behavior'에 지난 1월 게재됐다. (논문명: The groupwise-pivotal referral auction: Core-selecting referral strategy-proof mechanism)
논문링크:https://www.sciencedirect.com/science/article/pii/S0899825623001847
2024.02.01 조회수 6297 인공지능으로 인간 추론 능력 극대화시키다
최근 인공지능 기술이 인식, 생성, 제어, 대화와 같은 실제 문제를 빠르게 해결해 나감에 따라 인간의 역할과 일자리 생태계가 변화하고 있다. 인공지능의 발전 속도를 본다면 가까운 미래에는 인공지능이 인간보다 똑똑해질 수도 있다. 이와 반대로 인공지능을 이용해 인간의 사고력 자체를 향상시킬 순 없을까?
우리 대학 뇌인지과학과 이상완 교수(신경과학-인공지능 융합연구센터장) 연구팀이 인간의 빠른 추론 능력을 유도해 인과관계의 학습 효율을 향상할 수 있는 뇌 기반 인공지능 기술 개발에 성공했다고 31일 밝혔다.
우리는 일상생활에서 다양한 사건을 경험하며 세상의 다양한 요소에 대한 인과관계를 학습해 나가고, 공부할 때는 지식 조각들을 조합하며 통합적인 지식을 습득한다. 이러한 과정은 점진적으로 추론하는 베이시안 모델 또는 특정한 상황에서 한 번의 경험으로부터 빠르게 결론을 도출하는 고속추론 또는 원샷 추론이 있다.
연구팀은 이전 연구에서 인간의 원샷 추론 과정을 모델링하고 전두엽과 해마가 이러한 과정에 관여하고 있음을 규명한 바 있다. 이번 연구에서 이 모델에 인간의 원샷 추론 과정을 특정한 상태로 유도하기 위해 알파고에 사용된 바 있는 심층 강화학습 기술을 접목했다. 이는 강화학습 알고리즘이 인간의 원샷 추론 과정을 수없이 시뮬레이션하면서 전두엽과 해마가 가장 효율적으로 학습할 수 있는 최적의 조건을 탐색하는 과정으로 볼 수 있다.
연구팀은 126명의 인간 피험자를 대상으로 한 인과관계 학습 및 추론 실험에서 제안 기술을 사용해 학습했을 때 단순 반복 학습 대비 최대 약 40%까지 학습 효율이 향상됨을 보였다. 더 나아가 오랜 시간에 걸쳐 신중하게 학습하거나 몇 가지 단서만을 조합해 빠르게 결론을 도출하는 것 같은 개인별 학습 성향을 고려한 맞춤형 설계가 가능함을 보였다.
인간의 사고체계에 대한 뇌과학적인 이해를 바탕으로 원샷 추론과 같은 인간의 잠재적 능력을 극대화하는 이 기술은 차세대 인공지능의 중요한 도전과제 중 하나이며, 뇌 기반 인공지능 기술은 인간과 유사한 사고체계를 바탕으로 가치판단을 할 수 있으므로 장기적으로 인간과 인공지능이 협업하는 분야에서 인공지능의 신뢰성 및 윤리성을 높이는 데도 기여할 수 있을 것으로 기대된다.
개발 기술은 스마트 교육, 게임 콘텐츠 개발, 추론 능력 측정, 인지훈련 등 인간의 추론 학습과 관련된 모든 분야에 적용될 수 있다. 기존 기술은 단편적인 기억회상, 특정 인지기능, 정답률 증가와 같은 행동적 측면에 집중해 왔다면, 이번 기술은 인공지능을 이용해 과거의 경험을 일반화시키는 인간의 사고체계 자체를 높이는 가능성을 확인한 최초의 사례로 평가된다.
KAIST에서 연구를 주도한 제1 저자 이지항 교수(현 상명대 서울캠퍼스 조교수)는 "이번 연구를 통해 인간의 인지기능을 인공지능에 이식하여 뇌 기반 인공지능을 실현하는 사례를 보였고, 이를 통해 인간의 고위 수준 인지를 적절한 방향으로 유도할 수 있는 새로운 인간-인공지능 상호작용 패러다임을 제시했다ˮ라고 강조하며, 추후 "인간중심 인공지능 연구 개발뿐만 아니라 바이오메디컬 분야, 특히 정신 건강과 관련된 디지털 치료 분야에 적용했을 때 큰 파급력을 보일 것ˮ이라고 말했다.
연구 책임자인 이상완 교수는 "이번 기술의 잠재력은 인공지능의 방대한 지식을 인간이 빠르게 흡수할 수 있는 형태로 변환할 수 있다는 데 있다ˮ며, "챗 GPT, GPT-4와 같은 언어 인공지능에서 추출되는 다양한 정보를 인간이 빠르게 추론 학습할 수 있게 변환하거나, 게임이나 가상현실의 콘텐츠를 인간의 추론 과정에 맞게 최적화해 몰입도를 높일 수 있고, 반대로 몰입도를 적절한 수준에서 제어할 경우 중독을 완화하는 효과를 기대할 수 있다ˮ라고 말했다.
관련 기술은 국내 및 해외에 특허 출원된 상태이며, KAIST 기술설명회(테크페어)에 소개된 바 있다. 이상완 교수 연구팀은 이러한 뇌 기반 인공지능 원천기술의 파급력을 높이기 위해 2019년 KAIST 신경과학-인공지능 융합연구센터를 설립하고, 구글 딥마인드, 마이크로소프트 연구소, IBM 연구소, 옥스퍼드 대학 등 다양한 해외 연구팀들과 함께 국제공동연구를 수행해 오고 있다.
이번 연구는 `시뮬레이션 기반 실험 디자인을 이용한 인간의 인과관계 추론과정 제어'라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 1월 호 온라인판에 1월 30일 자 게재됐다. (논문명: Controlling human causal inference through in-silico task design)
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 SW스타랩 및 한국연구재단의 지원을 받아 수행됐다.
2024.01.31 조회수 7146
인공지능으로 인간 추론 능력 극대화시키다
최근 인공지능 기술이 인식, 생성, 제어, 대화와 같은 실제 문제를 빠르게 해결해 나감에 따라 인간의 역할과 일자리 생태계가 변화하고 있다. 인공지능의 발전 속도를 본다면 가까운 미래에는 인공지능이 인간보다 똑똑해질 수도 있다. 이와 반대로 인공지능을 이용해 인간의 사고력 자체를 향상시킬 순 없을까?
우리 대학 뇌인지과학과 이상완 교수(신경과학-인공지능 융합연구센터장) 연구팀이 인간의 빠른 추론 능력을 유도해 인과관계의 학습 효율을 향상할 수 있는 뇌 기반 인공지능 기술 개발에 성공했다고 31일 밝혔다.
우리는 일상생활에서 다양한 사건을 경험하며 세상의 다양한 요소에 대한 인과관계를 학습해 나가고, 공부할 때는 지식 조각들을 조합하며 통합적인 지식을 습득한다. 이러한 과정은 점진적으로 추론하는 베이시안 모델 또는 특정한 상황에서 한 번의 경험으로부터 빠르게 결론을 도출하는 고속추론 또는 원샷 추론이 있다.
연구팀은 이전 연구에서 인간의 원샷 추론 과정을 모델링하고 전두엽과 해마가 이러한 과정에 관여하고 있음을 규명한 바 있다. 이번 연구에서 이 모델에 인간의 원샷 추론 과정을 특정한 상태로 유도하기 위해 알파고에 사용된 바 있는 심층 강화학습 기술을 접목했다. 이는 강화학습 알고리즘이 인간의 원샷 추론 과정을 수없이 시뮬레이션하면서 전두엽과 해마가 가장 효율적으로 학습할 수 있는 최적의 조건을 탐색하는 과정으로 볼 수 있다.
연구팀은 126명의 인간 피험자를 대상으로 한 인과관계 학습 및 추론 실험에서 제안 기술을 사용해 학습했을 때 단순 반복 학습 대비 최대 약 40%까지 학습 효율이 향상됨을 보였다. 더 나아가 오랜 시간에 걸쳐 신중하게 학습하거나 몇 가지 단서만을 조합해 빠르게 결론을 도출하는 것 같은 개인별 학습 성향을 고려한 맞춤형 설계가 가능함을 보였다.
인간의 사고체계에 대한 뇌과학적인 이해를 바탕으로 원샷 추론과 같은 인간의 잠재적 능력을 극대화하는 이 기술은 차세대 인공지능의 중요한 도전과제 중 하나이며, 뇌 기반 인공지능 기술은 인간과 유사한 사고체계를 바탕으로 가치판단을 할 수 있으므로 장기적으로 인간과 인공지능이 협업하는 분야에서 인공지능의 신뢰성 및 윤리성을 높이는 데도 기여할 수 있을 것으로 기대된다.
개발 기술은 스마트 교육, 게임 콘텐츠 개발, 추론 능력 측정, 인지훈련 등 인간의 추론 학습과 관련된 모든 분야에 적용될 수 있다. 기존 기술은 단편적인 기억회상, 특정 인지기능, 정답률 증가와 같은 행동적 측면에 집중해 왔다면, 이번 기술은 인공지능을 이용해 과거의 경험을 일반화시키는 인간의 사고체계 자체를 높이는 가능성을 확인한 최초의 사례로 평가된다.
KAIST에서 연구를 주도한 제1 저자 이지항 교수(현 상명대 서울캠퍼스 조교수)는 "이번 연구를 통해 인간의 인지기능을 인공지능에 이식하여 뇌 기반 인공지능을 실현하는 사례를 보였고, 이를 통해 인간의 고위 수준 인지를 적절한 방향으로 유도할 수 있는 새로운 인간-인공지능 상호작용 패러다임을 제시했다ˮ라고 강조하며, 추후 "인간중심 인공지능 연구 개발뿐만 아니라 바이오메디컬 분야, 특히 정신 건강과 관련된 디지털 치료 분야에 적용했을 때 큰 파급력을 보일 것ˮ이라고 말했다.
연구 책임자인 이상완 교수는 "이번 기술의 잠재력은 인공지능의 방대한 지식을 인간이 빠르게 흡수할 수 있는 형태로 변환할 수 있다는 데 있다ˮ며, "챗 GPT, GPT-4와 같은 언어 인공지능에서 추출되는 다양한 정보를 인간이 빠르게 추론 학습할 수 있게 변환하거나, 게임이나 가상현실의 콘텐츠를 인간의 추론 과정에 맞게 최적화해 몰입도를 높일 수 있고, 반대로 몰입도를 적절한 수준에서 제어할 경우 중독을 완화하는 효과를 기대할 수 있다ˮ라고 말했다.
관련 기술은 국내 및 해외에 특허 출원된 상태이며, KAIST 기술설명회(테크페어)에 소개된 바 있다. 이상완 교수 연구팀은 이러한 뇌 기반 인공지능 원천기술의 파급력을 높이기 위해 2019년 KAIST 신경과학-인공지능 융합연구센터를 설립하고, 구글 딥마인드, 마이크로소프트 연구소, IBM 연구소, 옥스퍼드 대학 등 다양한 해외 연구팀들과 함께 국제공동연구를 수행해 오고 있다.
이번 연구는 `시뮬레이션 기반 실험 디자인을 이용한 인간의 인과관계 추론과정 제어'라는 제목으로 국제 학술지 셀(Cell)의 오픈 액세스 저널인 `셀 리포트(Cell Reports)'에 1월 호 온라인판에 1월 30일 자 게재됐다. (논문명: Controlling human causal inference through in-silico task design)
한편 이번 연구는 삼성전자 미래기술육성센터, 과학기술정보통신부 정보통신기획평가원 SW스타랩 및 한국연구재단의 지원을 받아 수행됐다.
2024.01.31 조회수 7146 지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
2024.01.30 조회수 9428
지방간 치료제 신약 물질 개발
국내 연구진이 말초조직에 작용하는 비알코올성 지방간질환(NAFLD, Nonalcoholic fatty liver disease) 치료를 위한 신약 후보 물질을 개발하는 데 성공했다. 현재까지 최적의 비알코올성 지방간염(NASH) 치료제가 없는 상황에서 지방간 축적과 간 섬유화를 동시에 억제하면서 안전성이 증명된 치료제 개발이 기대된다.
광주과학기술원(GIST)은 화학과 안진희 교수 연구팀과 우리 대학 의과학대학원 김하일 교수 연구팀이 다년간 기초연구를 통해 질환 특이 단백질(HTR2A)을 억제할 수 있는 신규 화합물을 개발했으며, 안진희 교수의 창업기업인 ㈜제이디바이오사이언스에서 전임상 시험(동물 시험)을 통해 효능과 안전성을 입증하는 데 성공했다고 밝혔다.
비알코올성 지방간 질환의 유병율은 20~30%에 이르고, 지방간염 질환은 전 세계 성인 인구의 5% 이상이 보유하고 있을 정도로 높은 유병률을 보임에도 불구하고 현재까지 제품화된 치료제가 전혀 없다.
비알코올성 지방간질환은 지방간에서 시작해 지방간염, 섬유화, 간경화, 간암으로 진행되는 만성질환이며, 심혈관질환 및 간 관련 합병증 등에 의해 사망률이 증가하므로 발병 초기에 적절한 치료가 필요하다.
GIST와 KAIST 공동 연구팀이 개발한 이 신규 화합물은 지방간염에 치료 효과를 보이는 혁신신약 후보 물질로서, 세로토닌 수용체 단백질(5HT2A)을 억제함으로써 간 내 지방 축적과 간 섬유화를 동시에 억제하는 이중 작용 기전을 갖고 있다.
연구팀은 이 물질이 지방간 동물 및 지방간염 동물 모델에서 간 내 지방 축적으로 발생하는 간 지방증과 간 섬유화*를 동시에 50~70% 가량 억제함으로써 치료 효과가 있는 것을 확인하였다.
* 섬유화(fibrosis): 간의 일부가 굳는 현상으로, 지방간염 개선의 주요 지표로 쓰임
이 물질은 혈액-뇌 장벽(Blood-Brain Barrier) 투과도가 최소화되도록 최적의 극성과 지질친화도를 갖춘 화합물로 설계되어 뇌에 영향을 주지 않아 우울증, 자살 충동 등 중추신경계(CNS) 부작용이 적으며, 뇌 이외의 조직에서는 질환 타겟에 대한 억제력이 우수(IC50*=14 nM)하다고 연구팀은 설명했다. 또한 임상 3상 단계의 경쟁 약물과 효능을 비교해 본 결과, 간섬유화 개선 효능이 월등히 우수한 것으로 나타났다.
* IC50(half maximal inhibitory concentration): 특정 생물학적 또는 생화학적 기능을 50% 억제하는 물질의 농도
전임상 시험에 의해 얻은 약리작용 데이터를 토대로 건강한 사람에게서 부작용 및 안전한 약물 용량을 확인하는 단계인 임상 1상 시험에서 건강한 성인 총 88명을 대상으로 평가한 결과, 심각한 부작용은 발생하지 않았으며 안전성 또한 양호한 것으로 확인했다.
또한 지방간염 소견을 보이는 성인 8명을 대상으로 한 예비 효능 평가는 현재 진행 중이다.
안진희 교수는 “이번 연구는 비알콜성 지방간염의 치료를 위한 새로운 타겟 발굴을 통해 부작용이 적고 안전성이 보장된 치료제 개발을 목적으로, 현재 혁신신약 개발 바이오 벤처인 ㈜제이디바이오사이언스를 통해 호주에서 글로벌 임상 1상을 진행 중”이라고 밝혔다.
안 교수는 또한 “연구팀이 개발하고 있는 신약 후보물질은 안전성이 높으면서 간 지방축적을 억제시키는 예방효과뿐만 아니라 간 섬유화에 직접적인 치료 효과를 보인다는 강점이 있어 다른 경쟁 약물과는 차별화된다”고 설명했다.
우리 대학 김하일 교수는 “현재까지 체중을 조절하는 방법 외에는 치료방법이 없는 이 질환에서 비만하지 않은 환자에게 사용할 수 있는 약은 개발이 시도된 적도 없다”면서 “이번 연구를 계기로 체중에 영향을 주지 않으면서 비알코올성 지방간염을 포함한 다양한 대사질환 치료기술의 개발이 가능해질 것으로 기대한다”고 말했다.
GIST 안진희 교수 연구팀과 KAIST 김하일 교수 연구팀, ㈜제이디바이오사이언스(JD BIOSCIENCE) 연구팀이 함께 수행한 이번 연구는 과학기술정보통신부, 국가신약개발사업에서 지원을 받아 수행됐으며, 국제 학술지인 ‘네이처 커뮤니케이션즈(Nature Communications)’에 2024년 1월 20일 게재됐다.
또한 지난 4일부터 3일간 미국 유타에서 개최된 ‘NASH 치료제 전문 콘퍼런스(NASH-TAG Conference 2024)’에서 대사이상 관련 지방간염(MASH)* 치료제 후보물질인 ‘GM-60106(개발코드명)’의 임상 연구 결과를 발표해 우수 초록으로 선정되기도 했다.
* 대사이상 관련 지방간염(MASH): 비알코올성 지방간염(NASH)의 새로운 명칭
2024.01.30 조회수 9428 알츠하이머 발병 과정을 관찰하다
퇴행성 질환을 유발하는 아밀로이드 섬유 단백질의 초기 불안정한 움직임과 같은 생명 현상을 분자 수준에서 실시간 관찰이 가능한 기술이 개발되었다. 이를 통해 알츠하이머나 파킨슨 병과 같은 퇴행성 질환의 발병 과정에 대한 실마리를 제공할 수 있을 것으로 기대된다.
우리 대학 신소재공학과 육종민 교수 연구팀이 한국기초과학지원연구원, 포항산업과학연구원, 성균관대학교 약학대학 연구팀과 함께 그래핀을 이용해 알츠하이머 질병을 유발한다고 알려진 아밀로이드 섬유 단백질의 실시간 거동을 관찰할 수 있는 새로운 단분자 관찰 기술(single-molecule technique)을 개발했다고 30일 밝혔다.
단분자 관찰 기술은 단일 분자 수준에서 발생하는 현상을 관찰할 수 있는 기법을 말한다. 생체 과정에서 수반되는 단백질 간의 상호작용, 접힘, 조립 과정 등을 이해하는 데 핵심적인 기술이다. 현재까지 단분자 관찰 기술로는 특정 분자를 식별하기 위한 형광 현미경을 이용해 관찰하거나, 단백질을 급속 냉동시켜 움직임을 고정해 분자 구조를 해석하는 초저온 전자현미경 기법이 활용 돼왔다.
하지만, 자연 그대로의 단백질을 특별한 전처리 없이 분자 단위에서 실시간으로 관찰할 수 있는 기술은 여전히 부재한 상황이었다.
최근 이에 대한 대안으로 물질을 얼리지 않고 상온 상태에서 관찰하는 액상 전자현미경 기술이 최근 주목을 받고 있다. 이 기술은 얇은 투과막을 이용해 액체를 감싸 전자현미경 내에서 물질의 변화를 관찰할 수 있는 기술이지만, 두꺼운 투과 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성은 해결해야 하는 숙제였다.
육종민 교수 연구팀은 차세대 소재로 주목받고 있는 그래핀을 이용해 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성 문제를 해결하며, 단백질의 거동을 실시간 관찰할 수 있는 단분자 그래핀 액상 셀 전자현미경 기술을 개발했다. [그림 1]
이번 연구에서 투과 막으로 이용한 그래핀은 원자 단위의 두께를 가지고 있어 분자 수준 관찰을 가능하게 할 뿐만 아니라, 전자빔에 의한 단백질의 산화를 방지하는 산화 방지 역할을 해 기존 대비 40배 가량 변성을 억제해 단백질의 거동을 실시간으로 관찰할 수 있게 했다.
연구팀은 개발한 전자현미경 기술을 활용해, 알츠하이머 질병을 유발한다고 알려진 아밀로이드 베타 섬유의 초기 성장 과정에서 발현되는 분자 불안정성을 세계 최초로 관찰했다. [그림 2]
이 전자현미경 기술은 온전한 단백질의 다양한 거동들을 분자 수준에서 관찰을 가능하게 하므로, 코로나19와 같은 바이러스성 단백질의 감염 과정, 퇴행성 질환을 일으키는 아밀로이드성 단백질의 섬유화/응집 거동 등과 같이 단백질의 상호작용에 의한 생명 현상을 이해하는 데 활용될 수 있을 것으로 기대된다.
육 교수는 "현미경 기술의 발전은 생명과학 및 공학 기술 발전의 토대가 되는 것으로, 분자 단위의 현상을 관찰할 수 있다면 단백질들의 상호작용을 이해하고 조절할 수 있는 실마리를 제공할 수 있으며, 이를 통해 알츠하이머와 같은 퇴행성 질환의 신약 개발에 도움을 줄 수 있을 것으로 기대한다ˮ 라고 말했다.
우리 대학 신소재공학과 졸업생 박정재 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 머티리얼스(Advanced Materials)' 지난 11월 온라인으로 발표됐다. (논문명 : Single-Molecule Graphene Liquid Cell Electron Microscopy for Instability of Intermediate Amyloid Fibrils).
이번 연구는 한국연구재단의 중견연구자지원사업(MIST) (NRF-2022R1A2C2008929)과 나노 및 소재 기술개발사업(MIST)(NRF-2021M3H4A6A02050365)의 지원을 받아 수행됐다.
2024.01.30 조회수 7682
알츠하이머 발병 과정을 관찰하다
퇴행성 질환을 유발하는 아밀로이드 섬유 단백질의 초기 불안정한 움직임과 같은 생명 현상을 분자 수준에서 실시간 관찰이 가능한 기술이 개발되었다. 이를 통해 알츠하이머나 파킨슨 병과 같은 퇴행성 질환의 발병 과정에 대한 실마리를 제공할 수 있을 것으로 기대된다.
우리 대학 신소재공학과 육종민 교수 연구팀이 한국기초과학지원연구원, 포항산업과학연구원, 성균관대학교 약학대학 연구팀과 함께 그래핀을 이용해 알츠하이머 질병을 유발한다고 알려진 아밀로이드 섬유 단백질의 실시간 거동을 관찰할 수 있는 새로운 단분자 관찰 기술(single-molecule technique)을 개발했다고 30일 밝혔다.
단분자 관찰 기술은 단일 분자 수준에서 발생하는 현상을 관찰할 수 있는 기법을 말한다. 생체 과정에서 수반되는 단백질 간의 상호작용, 접힘, 조립 과정 등을 이해하는 데 핵심적인 기술이다. 현재까지 단분자 관찰 기술로는 특정 분자를 식별하기 위한 형광 현미경을 이용해 관찰하거나, 단백질을 급속 냉동시켜 움직임을 고정해 분자 구조를 해석하는 초저온 전자현미경 기법이 활용 돼왔다.
하지만, 자연 그대로의 단백질을 특별한 전처리 없이 분자 단위에서 실시간으로 관찰할 수 있는 기술은 여전히 부재한 상황이었다.
최근 이에 대한 대안으로 물질을 얼리지 않고 상온 상태에서 관찰하는 액상 전자현미경 기술이 최근 주목을 받고 있다. 이 기술은 얇은 투과막을 이용해 액체를 감싸 전자현미경 내에서 물질의 변화를 관찰할 수 있는 기술이지만, 두꺼운 투과 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성은 해결해야 하는 숙제였다.
육종민 교수 연구팀은 차세대 소재로 주목받고 있는 그래핀을 이용해 막에 의한 분해능 저하와 전자빔에 의한 단백질 변성 문제를 해결하며, 단백질의 거동을 실시간 관찰할 수 있는 단분자 그래핀 액상 셀 전자현미경 기술을 개발했다. [그림 1]
이번 연구에서 투과 막으로 이용한 그래핀은 원자 단위의 두께를 가지고 있어 분자 수준 관찰을 가능하게 할 뿐만 아니라, 전자빔에 의한 단백질의 산화를 방지하는 산화 방지 역할을 해 기존 대비 40배 가량 변성을 억제해 단백질의 거동을 실시간으로 관찰할 수 있게 했다.
연구팀은 개발한 전자현미경 기술을 활용해, 알츠하이머 질병을 유발한다고 알려진 아밀로이드 베타 섬유의 초기 성장 과정에서 발현되는 분자 불안정성을 세계 최초로 관찰했다. [그림 2]
이 전자현미경 기술은 온전한 단백질의 다양한 거동들을 분자 수준에서 관찰을 가능하게 하므로, 코로나19와 같은 바이러스성 단백질의 감염 과정, 퇴행성 질환을 일으키는 아밀로이드성 단백질의 섬유화/응집 거동 등과 같이 단백질의 상호작용에 의한 생명 현상을 이해하는 데 활용될 수 있을 것으로 기대된다.
육 교수는 "현미경 기술의 발전은 생명과학 및 공학 기술 발전의 토대가 되는 것으로, 분자 단위의 현상을 관찰할 수 있다면 단백질들의 상호작용을 이해하고 조절할 수 있는 실마리를 제공할 수 있으며, 이를 통해 알츠하이머와 같은 퇴행성 질환의 신약 개발에 도움을 줄 수 있을 것으로 기대한다ˮ 라고 말했다.
우리 대학 신소재공학과 졸업생 박정재 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `어드밴스드 머티리얼스(Advanced Materials)' 지난 11월 온라인으로 발표됐다. (논문명 : Single-Molecule Graphene Liquid Cell Electron Microscopy for Instability of Intermediate Amyloid Fibrils).
이번 연구는 한국연구재단의 중견연구자지원사업(MIST) (NRF-2022R1A2C2008929)과 나노 및 소재 기술개발사업(MIST)(NRF-2021M3H4A6A02050365)의 지원을 받아 수행됐다.
2024.01.30 조회수 7682 양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.01.29 조회수 7288
양자 시뮬레이터로 양자얽힘 관측 도전
고온 초전도물질은 수십 년이 지난 지금도 어떠한 물리적인 기작으로 초전도가 형성되는지 명확하게 규명되지 않았다. 광격자 양자 시뮬레이터는 이러한 문제를 풀기 위한 새로운 접근 방식으로 이미 고전 컴퓨터가 연산할 수 없는 영역에 우위를 보여주었으며, 최근 고온 초전도체에서 관측된 반강자성을 관측하는 등 미래에 고온 초전도 문제를 풀 수 있는 강력한 후보다.
우리 대학 물리학과 최재윤 교수 연구팀이 포항공대 조길영 교수 연구팀과 공동연구를 통해 중성원자 양자 시뮬레이터의 오류 정정 기술을 개발해 최초로 2차원에서의 비국소 질서 변수를 측정함으로써 향후위상 물질과 고온 초전도체 물질 특성을 알아낼 수 있도록 하는 데 성공했다고 29일 밝혔다.
이러한 양자 시뮬레이터의 큰 단점은 관측 과정 및 양자 상태 준비 과정에서 발생하는 결함으로(예: 원자 손실), 이를 체계적으로 파악하고, 정정하는 것이 매우 어렵다. 이러한 결함은 특히 위상물질의 특성을 규정짓는 비국소 질서변수를 측정하는데 큰 걸림돌이 되며, 2차원에서는 그 효과가 더욱 커져 큰 시스템에서 비국소 질서 변수의 실험적 관측을 어렵게 만드는 주요 요소다.
일반적으로 우리가 관측하는 물리량은 국소성을 띄기 때문에, 이러한 양자역학적 특이성인 양자 얽힘(entanglement)이 물성을 지배하는 물질인 위상물질의 비국소 질서 변수를 측정하는 것은 간단하지 않다. 더욱이 2차원, 3차원 물질의 경우 실험적 노이즈에 의해 그 신호가 급격하게 약해지기 때문에 이를 실험적으로 관측하기는 매우 어렵다.
최 교수 연구팀은 양자 시뮬레이터에 비국소 질서 변수가 측정 가능하고 실험적인 결함도 함께 찾아내는 방법을 개발했다. 또한 연구팀은 2차원에서도 양자얽힘의 위상 물질의 물성을 규정짓는 것도 가능함을 보여주었다. 시뮬레이터 실시과정에서 발생한 결점까지 제거하는데 성공한 이후, 위상물질의 2차원 비국소 질서변수는 급격하게(100배 이상) 증가하는 양상을 보였으며, 원자 수에 무관하게 측정값이 일정하게 유지되는 것을 확인하는 등 이론적으로 예측된 경향을 모두 확인할 수 있었다.
해당 기술은 여러 가지 중성원자 양자 시뮬레이터에 활용이 가능하다. 원거리 상호작용이 주요한 양자 시뮬레이터의 경우, 양자 스핀 액상과 같은 2차원 위상 물질의 물성을 규정하는데 적용 가능하며, 고온 초전도체 물질을 흉내 내는 양자 시뮬레이터에도 해당 기법을 응용할 수 있을 것으로 기대된다.
최재윤 교수는 “이번 연구는 중성원자 양자 시뮬레이터에 존재하는 실험적 결함을 보정하는 것이 가능함을 보여준 최초의 연구이며, 향후 위상 양자 연산에 이용되는 양자 스핀 액상과 같은 고차원 위상 물질 발견 및 물성 규정에 주요하게 활용될 것”이라고 하였다.
우리 대학 허준혁 연구원과 포스텍 이원준 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `피지컬 리뷰 X (Physical Review X)' 14권 1호에 지난 1월 8일 출판됐다. (논문명 : Measuring nonlocal brane order with error-corrected quantum gas microscopes).
한편 이번 연구는 삼성미래기술재단과 한국연구재단의 지원으로 수행됐다.
2024.01.29 조회수 7288 금이 간 뼈에 ‘뼈 반창고’ 신소재 개발
뼈 재생은 복잡하며 기존의 골 이식 및 성장 인자 전달 등과 같은 재생을 할 경우 높은 단가 발생 등의 한계가 있었는데 뼈조직의 성장을 촉진하기 위한 압전 물질이 개발되었다.
우리 대학 신소재공학과 홍승범 교수 연구팀이 전남대학교 융합바이오시스템기계공학과 김장호 교수 연구팀과 협업을 통해 하이드록시아파타이트(HAp)의 고유한 골 형성 능력을 활용하여 압력을 가했을 때 전기적 신호가 발생하는 생체 모방 지지체를 개발했다고 25일 밝혔다.
하이드록시아파타이트(HAp)란 뼈나 치아에서 발견되는 염기성 인산칼슘으로 생체 친화적인 특징이 있으며, 충치를 예방하는 특성이 있어 치약에도 쓰이는 미네랄 물질이다.
이전의 압전 지지체 관련 연구들은 압전성이 뼈 재생을 촉진하고 골 융합을 향상하는 효과를 다양한 고분자 기반 소재에서 확인했지만, 최적의 골조직 재생에 필요한 복잡한 세포 환경을 모사하는 데 한계가 있었다. 그러나 이번 연구는 하이드록시아파타이트(HAp) 고유의 골 형성 능력을 활용해 생체의 골조직 환경을 모방하는 소재를 개발한 것으로, 연구팀은 새로운 방법을 제시했다.
연구팀은 하이드록시아파타이트(HAp)를 고분자 필름과 융합하는 제조 공정을 개발했다. 이 공정으로 제작된 유연하고 독립적인 지지체는 실험 쥐를 대상으로 한 체외 및 체내 실험에서 뼈 재생을 가속하는 놀라운 잠재력을 입증했다.
또한, 연구팀은 동 지지체의 골 재생 효과의 원인을 다각도로 밝혀냈다. 원자간력 현미경(AFM) 분석을 통해 지지체의 전기적 특성을 조사했으며, 세포 모양과 세포 골격 단백질 형성에 대한 상세한 표면 특성 평가를 진행했다. 또한, 압전 및 표면적 요소가 성장 인자 발현에 어떤 영향을 미치는지 조사했다.
신소재공학과 홍승범 교수는 "뼈의 재생 속도를 가속화시키는 효과를 통해 `뼈 반창고' 같은 역할을 하는 하이드록시아파타이트(HAp) 융합 압전성 복합소재를 개발했다ˮ며, "이번 연구는 생체 재료 설계에 새로운 방향성을 제시하는 데에 그치지 않고, 압전성과 표면적 특성이 뼈 재생에 미치는 영향을 탐구한 데에 의의가 있다ˮ 라고 강조했다.
홍승범 교수 연구팀 소속 주소연 박사과정 학생, 김소연 석사가 공동 제1 저자로 참여한 이번 연구는 2024년 1월 4일 국제학술지 `ACS Applied Materials & Interfaces'에 게재됐다. 또한, 김장호 교수팀의 권용현 박사과정 학생이 공동 제1 저자로, 김장호 교수가 공동교신저자로 기여했다. (논문 제목: Piezoelectrically and Topographically Engineered Scaffolds for Accelerating Bone Regeneration).
해당 연구는 KAIST 연구진흥팀, KUSTAR-KAIST 공동연구센터, KAIST의 글로벌 특이점 사업과 정부의 재원으로 한국연구재단 기초연구사업(NRF2022M3A9E4017151, NRF-2022K1A4A7A04095892, RS2023-00247245, NRF-2021R1A4A3025206)의 지원을 받아 수행됐다.
2024.01.25 조회수 8451
금이 간 뼈에 ‘뼈 반창고’ 신소재 개발
뼈 재생은 복잡하며 기존의 골 이식 및 성장 인자 전달 등과 같은 재생을 할 경우 높은 단가 발생 등의 한계가 있었는데 뼈조직의 성장을 촉진하기 위한 압전 물질이 개발되었다.
우리 대학 신소재공학과 홍승범 교수 연구팀이 전남대학교 융합바이오시스템기계공학과 김장호 교수 연구팀과 협업을 통해 하이드록시아파타이트(HAp)의 고유한 골 형성 능력을 활용하여 압력을 가했을 때 전기적 신호가 발생하는 생체 모방 지지체를 개발했다고 25일 밝혔다.
하이드록시아파타이트(HAp)란 뼈나 치아에서 발견되는 염기성 인산칼슘으로 생체 친화적인 특징이 있으며, 충치를 예방하는 특성이 있어 치약에도 쓰이는 미네랄 물질이다.
이전의 압전 지지체 관련 연구들은 압전성이 뼈 재생을 촉진하고 골 융합을 향상하는 효과를 다양한 고분자 기반 소재에서 확인했지만, 최적의 골조직 재생에 필요한 복잡한 세포 환경을 모사하는 데 한계가 있었다. 그러나 이번 연구는 하이드록시아파타이트(HAp) 고유의 골 형성 능력을 활용해 생체의 골조직 환경을 모방하는 소재를 개발한 것으로, 연구팀은 새로운 방법을 제시했다.
연구팀은 하이드록시아파타이트(HAp)를 고분자 필름과 융합하는 제조 공정을 개발했다. 이 공정으로 제작된 유연하고 독립적인 지지체는 실험 쥐를 대상으로 한 체외 및 체내 실험에서 뼈 재생을 가속하는 놀라운 잠재력을 입증했다.
또한, 연구팀은 동 지지체의 골 재생 효과의 원인을 다각도로 밝혀냈다. 원자간력 현미경(AFM) 분석을 통해 지지체의 전기적 특성을 조사했으며, 세포 모양과 세포 골격 단백질 형성에 대한 상세한 표면 특성 평가를 진행했다. 또한, 압전 및 표면적 요소가 성장 인자 발현에 어떤 영향을 미치는지 조사했다.
신소재공학과 홍승범 교수는 "뼈의 재생 속도를 가속화시키는 효과를 통해 `뼈 반창고' 같은 역할을 하는 하이드록시아파타이트(HAp) 융합 압전성 복합소재를 개발했다ˮ며, "이번 연구는 생체 재료 설계에 새로운 방향성을 제시하는 데에 그치지 않고, 압전성과 표면적 특성이 뼈 재생에 미치는 영향을 탐구한 데에 의의가 있다ˮ 라고 강조했다.
홍승범 교수 연구팀 소속 주소연 박사과정 학생, 김소연 석사가 공동 제1 저자로 참여한 이번 연구는 2024년 1월 4일 국제학술지 `ACS Applied Materials & Interfaces'에 게재됐다. 또한, 김장호 교수팀의 권용현 박사과정 학생이 공동 제1 저자로, 김장호 교수가 공동교신저자로 기여했다. (논문 제목: Piezoelectrically and Topographically Engineered Scaffolds for Accelerating Bone Regeneration).
해당 연구는 KAIST 연구진흥팀, KUSTAR-KAIST 공동연구센터, KAIST의 글로벌 특이점 사업과 정부의 재원으로 한국연구재단 기초연구사업(NRF2022M3A9E4017151, NRF-2022K1A4A7A04095892, RS2023-00247245, NRF-2021R1A4A3025206)의 지원을 받아 수행됐다.
2024.01.25 조회수 8451 땀에도 강한 웨어러블 로봇 제어 센서 선보이다
노인, 뇌졸중 환자, 외상 환자들의 다양한 재활치료에 활용되는 웨어러블 로봇이 착용자의 땀, 각질 등에도 끄떡없이 장기간 안정적으로 제어 가능하도록 도와주는 근전도 센서 기술이 개발되어 화제다.
우리 대학 전기및전자공학부 정재웅 교수와 기계공학과 김정 교수 연구팀이 공동 연구를 통해 피부 상태에 영향을 받지 않는 고품질의 전기 생리 신호 측정이 가능한 신축·접착성 마이크로니들 센서를 개발하는 데 성공했다고 23일 밝혔다.
다양한 재활치료에 활용되는 웨어러블 로봇이 사람의 움직임 의도를 인식하기 위해서는 몸에서 발생하는 근전도를 정확하게 측정하는 웨어러블 전기 생리 센서가 필요하다. 하지만 기존의 센서들은 시간에 따라 신호의 품질이 떨어지거나, 피부의 털, 각질, 땀 등의 영향을 많이 받고, 나아가 피부보다 단단한 물성으로 움직임 시 피부 변형을 따라갈 수 없어 노이즈(신호 잡음)를 발생시킬 수 있다. 이러한 단점들은 장시간의 신뢰성 높은 웨어러블 로봇 제어를 힘들게 한다.
이번에 개발된 기술은 잘 늘어나며 접착성이 있는 전도성 기판에 피부 각질층을 통과할 수 있는 마이크로니들 어레이를 집적해 불편함 없이 장기간 고품질의 근전도 측정을 가능하게 할 것으로 예상된다. 이와 같은 우수한 성능을 통해 땀, 각질 등을 제거하는 피부 준비 작업을 거치지 않아도 시간에 따른 착용자의 피부 상태 변화에 상관없이 웨어러블 로봇을 안정적으로 제어할 수 있을 것이라 기대된다.
연구팀은 부드러운 실리콘 중합체 기판을 활용해서 마이크로니들을 집적해 신축·접착성 마이크로니들 센서를 제작했다. 단단한 마이크로니들이 높은 저항을 가진 피부의 각질층을 투과해 피부 접촉 저항을 효과적으로 낮춰 털, 각질, 땀, 이물질로 피부가 오염돼도 고품질의 전기 생리 신호를 얻을 수 있다. 동시에 부드러운 전도성 접착 기판이 사람의 움직임으로 인한 피부의 늘어남에 순응해 편안한 착용감을 제공하고 움직임으로 인한 동작 잡음을 최소화할 수 있다.
연구팀은 개발된 신축·접착성 마이크로니들 센서 패치의 효용성을 검증하기 위해 웨어러블 로봇을 이용한 동작 보조 실험을 진행했다. 다리에 부착된 신축·접착성 마이크로니들 센서 패치는 근육에서 발생하는 전기신호를 감지하고 동작 의도를 웨어러블 로봇에 전송해 사람이 무거운 짐을 손쉽게 들어올릴 수 있도록 도와준다.
마이크로니들 센서 패치를 사용했을 때 피부 상태, 신체 움직임의 크기 및 종류와 상관없이 안정적인 근전도 센싱에 기반한 동작 의도 인식을 통해 웨어러블 로봇이 사용자의 동작을 효과적으로 보조할 수 있음을 연구팀은 확인했다.
이번 연구를 주도한 정재웅 교수는 “개발된 신축·접착성 마이크로니들 센서는 피부 상태에 영향받지 않는 안정적인 근전도 센싱을 통해 더욱 정확하고 안정적인 웨어러블 로봇 제어를 가능하게 하여 로봇을 활용하는 환자의 재활을 더 용이하게 할 수 있을 것이다”라고 말했다.
전기및전자공학부 김희수 박사과정과 이주현 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 1월 17일 字에 게재됐다.
(논문명 : Skin-preparation-free, stretchable microneedle adhesive patches for reliable electrophysiological sensing and exoskeleton robot control)
한편 이번 연구는 한국연구재단이 추진하는 생체신호센서융합기술개발사업, 전자약기술개발사업, 4단계 BK21 사업의 지원을 받아 수행됐다.
2024.01.23 조회수 7786
땀에도 강한 웨어러블 로봇 제어 센서 선보이다
노인, 뇌졸중 환자, 외상 환자들의 다양한 재활치료에 활용되는 웨어러블 로봇이 착용자의 땀, 각질 등에도 끄떡없이 장기간 안정적으로 제어 가능하도록 도와주는 근전도 센서 기술이 개발되어 화제다.
우리 대학 전기및전자공학부 정재웅 교수와 기계공학과 김정 교수 연구팀이 공동 연구를 통해 피부 상태에 영향을 받지 않는 고품질의 전기 생리 신호 측정이 가능한 신축·접착성 마이크로니들 센서를 개발하는 데 성공했다고 23일 밝혔다.
다양한 재활치료에 활용되는 웨어러블 로봇이 사람의 움직임 의도를 인식하기 위해서는 몸에서 발생하는 근전도를 정확하게 측정하는 웨어러블 전기 생리 센서가 필요하다. 하지만 기존의 센서들은 시간에 따라 신호의 품질이 떨어지거나, 피부의 털, 각질, 땀 등의 영향을 많이 받고, 나아가 피부보다 단단한 물성으로 움직임 시 피부 변형을 따라갈 수 없어 노이즈(신호 잡음)를 발생시킬 수 있다. 이러한 단점들은 장시간의 신뢰성 높은 웨어러블 로봇 제어를 힘들게 한다.
이번에 개발된 기술은 잘 늘어나며 접착성이 있는 전도성 기판에 피부 각질층을 통과할 수 있는 마이크로니들 어레이를 집적해 불편함 없이 장기간 고품질의 근전도 측정을 가능하게 할 것으로 예상된다. 이와 같은 우수한 성능을 통해 땀, 각질 등을 제거하는 피부 준비 작업을 거치지 않아도 시간에 따른 착용자의 피부 상태 변화에 상관없이 웨어러블 로봇을 안정적으로 제어할 수 있을 것이라 기대된다.
연구팀은 부드러운 실리콘 중합체 기판을 활용해서 마이크로니들을 집적해 신축·접착성 마이크로니들 센서를 제작했다. 단단한 마이크로니들이 높은 저항을 가진 피부의 각질층을 투과해 피부 접촉 저항을 효과적으로 낮춰 털, 각질, 땀, 이물질로 피부가 오염돼도 고품질의 전기 생리 신호를 얻을 수 있다. 동시에 부드러운 전도성 접착 기판이 사람의 움직임으로 인한 피부의 늘어남에 순응해 편안한 착용감을 제공하고 움직임으로 인한 동작 잡음을 최소화할 수 있다.
연구팀은 개발된 신축·접착성 마이크로니들 센서 패치의 효용성을 검증하기 위해 웨어러블 로봇을 이용한 동작 보조 실험을 진행했다. 다리에 부착된 신축·접착성 마이크로니들 센서 패치는 근육에서 발생하는 전기신호를 감지하고 동작 의도를 웨어러블 로봇에 전송해 사람이 무거운 짐을 손쉽게 들어올릴 수 있도록 도와준다.
마이크로니들 센서 패치를 사용했을 때 피부 상태, 신체 움직임의 크기 및 종류와 상관없이 안정적인 근전도 센싱에 기반한 동작 의도 인식을 통해 웨어러블 로봇이 사용자의 동작을 효과적으로 보조할 수 있음을 연구팀은 확인했다.
이번 연구를 주도한 정재웅 교수는 “개발된 신축·접착성 마이크로니들 센서는 피부 상태에 영향받지 않는 안정적인 근전도 센싱을 통해 더욱 정확하고 안정적인 웨어러블 로봇 제어를 가능하게 하여 로봇을 활용하는 환자의 재활을 더 용이하게 할 수 있을 것이다”라고 말했다.
전기및전자공학부 김희수 박사과정과 이주현 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 ‘사이언스 어드밴시스(Science Advances)’ 1월 17일 字에 게재됐다.
(논문명 : Skin-preparation-free, stretchable microneedle adhesive patches for reliable electrophysiological sensing and exoskeleton robot control)
한편 이번 연구는 한국연구재단이 추진하는 생체신호센서융합기술개발사업, 전자약기술개발사업, 4단계 BK21 사업의 지원을 받아 수행됐다.
2024.01.23 조회수 7786