-
 사람 3D 폐포 배양 기술로 코로나19 감염 기전을 규명하는 데 성공
우리 대학 연구진 포함 국내 연구진이 실험실에서 3차원으로 키운 사람의 폐포(허파꽈리)에 코로나19 바이러스를 배양해 감염 기전과 치료제 개발에 적용이 가능한 기술 개발에 성공했다.
국제 통계 사이트 월드오미터에 따르면 전 세계 누적 코로나바이러스감염증-19(이하 코로나19) 확진자 수는 25일 기준 4,331만 8,941명으로 지난 18일(4,030만 1,609명) 4,000만 명을 넘어선 후 일주일 만에 4,331만을 돌파하는 2차 대유행이 점차 현실화돼 가고 있다.
우리 대학 의과학대학원 주영석 교수 연구팀은 인간의 폐포 세포를 실험실에서 구현하는 3D 미니 장기기술을 개발하고 이를 활용해 코로나19 바이러스가 인간의 폐 세포를 파괴하는 과정을 정밀하게 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 영국 케임브리지대학 이주현 박사를 비롯해 국립보건연구원 국립감염병연구소 최병선 과장·기초과학연구원(IBS) 고규영 혈관연구단장(우리 대학 의과학대학원 교수)·서울대병원 김영태 교수와 우리 대학 교원창업기업인 ㈜지놈인사이트와 공동으로 진행됐다.
공동연구팀의 이번 연구 결과는 줄기세포 분야 세계적인 학술지 `Cell Stem Cell' 10월 22일 字 온라인판에 실렸다. (논문명: Three-dimensional human alveolar stem cell culture models reveal infection response to SARS-CoV-2)
정확한 질병 기전의 이해를 기반으로 치료제를 효과적으로 개발하기 위해서는 실험실에서 사용 가능한 인체를 모사한 모델 사용이 필수적이다. 코로나19 바이러스는 생쥐 모델에 감염시키기가 어렵고, 특히 실험실에서 사용할 수 있는 폐 세포 모델은 존재하지 않기 때문에 직접적인 감염 연구의 한계가 존재해왔다.
공동연구팀은 이런 문제를 해소하기 위해 지속적으로 배양이 가능한 3차원 인간 폐포 모델을 새롭게 정립했다. 이를 이용하면 실험실에서 사람의 폐 세포를 이용해 코로나19 바이러스 등 각종 호흡기 바이러스의 질병 기전을 연구할 수 있기 때문이다. 더 나가서 3차원 인간 폐포 모델은 약물 스크리닝 등 치료법 개발에도 직접적으로 응용할 수 있다는 장점이 있다.
공동연구팀은 폐암 등 사람의 수술 검사재료에서 확보되는 사람 폐 조직을 장기간 안정적으로 3차원 배양할 수 있는 조건을 알아내는 데 성공했다. 실험 결과, 3D 폐포는 코로나19 바이러스에 노출되면 6시간 내 급속한 바이러스 증식이 일어나 세포 감염이 완료됐으나, 이를 막기 위한 폐 세포의 선천 면역 반응 활성화에는 약 3일가량의 시간이 걸렸다.
이와 함께 하나의 코로나19 바이러스 입자는 하나의 세포를 감염시키는 데 충분하다는 사실을 알아냈다. 감염 3일째 공동연구팀은 세포 가운데 일부분이 고유의 기능을 급격히 상실한다는 사실도 확인했다.
공동 교신저자인 주영석 교수는 "이번에 개발한 3차원 인체 폐 배양 모델 규모를 확대한다면 코로나19 바이러스를 포함한 다양한 호흡기 바이러스의 감염 연구에 유용하게 사용될 것ˮ이라고 말했다.
주 교수는 이어 "동물이나 다른 장기 유래의 세포가 아닌 호흡기 바이러스의 표적 세포인 사람의 폐 세포를 직접적으로 질병 연구에 응용함으로써 효율적이고 정확한 기전 규명은 물론 치료제 개발에도 이용할 수 있다ˮ고 강조했다.
코로나19 바이러스 대응 기술개발을 위해서는 다양한 기관의 지원과 관련 연구자들의 협력 연구가 필수적이다. 공동연구팀의 이번 연구는 한국연구재단·질병관리청·기초과학연구원(IBS)·서울대학교 의과대학·유럽연구이사회(ERC)·서경배과학재단·휴먼프론티어과학재단의 지원을 받아 수행됐다.
사람 3D 폐포 배양 기술로 코로나19 감염 기전을 규명하는 데 성공
우리 대학 연구진 포함 국내 연구진이 실험실에서 3차원으로 키운 사람의 폐포(허파꽈리)에 코로나19 바이러스를 배양해 감염 기전과 치료제 개발에 적용이 가능한 기술 개발에 성공했다.
국제 통계 사이트 월드오미터에 따르면 전 세계 누적 코로나바이러스감염증-19(이하 코로나19) 확진자 수는 25일 기준 4,331만 8,941명으로 지난 18일(4,030만 1,609명) 4,000만 명을 넘어선 후 일주일 만에 4,331만을 돌파하는 2차 대유행이 점차 현실화돼 가고 있다.
우리 대학 의과학대학원 주영석 교수 연구팀은 인간의 폐포 세포를 실험실에서 구현하는 3D 미니 장기기술을 개발하고 이를 활용해 코로나19 바이러스가 인간의 폐 세포를 파괴하는 과정을 정밀하게 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 영국 케임브리지대학 이주현 박사를 비롯해 국립보건연구원 국립감염병연구소 최병선 과장·기초과학연구원(IBS) 고규영 혈관연구단장(우리 대학 의과학대학원 교수)·서울대병원 김영태 교수와 우리 대학 교원창업기업인 ㈜지놈인사이트와 공동으로 진행됐다.
공동연구팀의 이번 연구 결과는 줄기세포 분야 세계적인 학술지 `Cell Stem Cell' 10월 22일 字 온라인판에 실렸다. (논문명: Three-dimensional human alveolar stem cell culture models reveal infection response to SARS-CoV-2)
정확한 질병 기전의 이해를 기반으로 치료제를 효과적으로 개발하기 위해서는 실험실에서 사용 가능한 인체를 모사한 모델 사용이 필수적이다. 코로나19 바이러스는 생쥐 모델에 감염시키기가 어렵고, 특히 실험실에서 사용할 수 있는 폐 세포 모델은 존재하지 않기 때문에 직접적인 감염 연구의 한계가 존재해왔다.
공동연구팀은 이런 문제를 해소하기 위해 지속적으로 배양이 가능한 3차원 인간 폐포 모델을 새롭게 정립했다. 이를 이용하면 실험실에서 사람의 폐 세포를 이용해 코로나19 바이러스 등 각종 호흡기 바이러스의 질병 기전을 연구할 수 있기 때문이다. 더 나가서 3차원 인간 폐포 모델은 약물 스크리닝 등 치료법 개발에도 직접적으로 응용할 수 있다는 장점이 있다.
공동연구팀은 폐암 등 사람의 수술 검사재료에서 확보되는 사람 폐 조직을 장기간 안정적으로 3차원 배양할 수 있는 조건을 알아내는 데 성공했다. 실험 결과, 3D 폐포는 코로나19 바이러스에 노출되면 6시간 내 급속한 바이러스 증식이 일어나 세포 감염이 완료됐으나, 이를 막기 위한 폐 세포의 선천 면역 반응 활성화에는 약 3일가량의 시간이 걸렸다.
이와 함께 하나의 코로나19 바이러스 입자는 하나의 세포를 감염시키는 데 충분하다는 사실을 알아냈다. 감염 3일째 공동연구팀은 세포 가운데 일부분이 고유의 기능을 급격히 상실한다는 사실도 확인했다.
공동 교신저자인 주영석 교수는 "이번에 개발한 3차원 인체 폐 배양 모델 규모를 확대한다면 코로나19 바이러스를 포함한 다양한 호흡기 바이러스의 감염 연구에 유용하게 사용될 것ˮ이라고 말했다.
주 교수는 이어 "동물이나 다른 장기 유래의 세포가 아닌 호흡기 바이러스의 표적 세포인 사람의 폐 세포를 직접적으로 질병 연구에 응용함으로써 효율적이고 정확한 기전 규명은 물론 치료제 개발에도 이용할 수 있다ˮ고 강조했다.
코로나19 바이러스 대응 기술개발을 위해서는 다양한 기관의 지원과 관련 연구자들의 협력 연구가 필수적이다. 공동연구팀의 이번 연구는 한국연구재단·질병관리청·기초과학연구원(IBS)·서울대학교 의과대학·유럽연구이사회(ERC)·서경배과학재단·휴먼프론티어과학재단의 지원을 받아 수행됐다.
2020.10.26
조회수 33686
-
 포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2020.03.11
조회수 16493
-
 생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24
조회수 26309
-
 주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03
조회수 25694
-
 조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10
조회수 24573
-
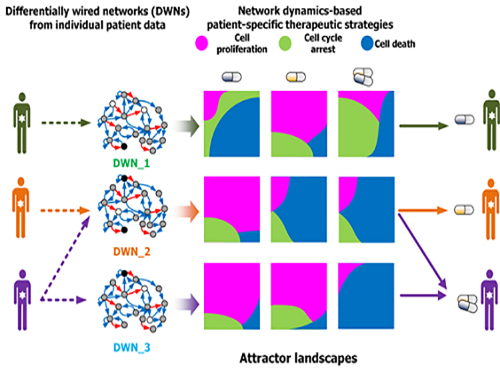 조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
2017.12.07
조회수 25176
-
 이현주 교수, 백금 사용량 10분의1로 줄인 단일원자 촉매 개발
〈 이 현 주 교수, 김 지 환 학생 〉
우리 대학 생명화학공학과 이현주 교수와 서울시립대 한정우 교수 공동 연구팀이 기존 촉매의 백금 사용량을 10분의 1로 줄일 수 있는 백금 단일원자 촉매를 개발했다.
이는 매우 안정적인 고함량의 백금 단일원자 촉매로 연구팀은 ‘직접 포름산 연료전지(Direct formic acid fuel cells)’에 적용하는 데 성공했다.
김지환 학생이 1저자로 참여한 이번 연구 결과는 재료 과학분야의 국제 학술지 ‘어드밴스드 에너지 머티리얼즈(Advanced Energy Materials)’ 9월 11일자 온라인 판에 게재됐다.
백금 기반의 축매는 활성과 안정성이 높아 다양한 촉매 반응에 적용되지만 가격이 비싸고 희귀하기 때문에 백금의 사용량을 최대한 줄이는 것이 중요하다.
그 중 단일원자 촉매는 백금 입자 크기를 원자 단위로 줄여 모든 원자가 반응에 참여하기 때문에 백금 촉매의 가격을 획기적으로 낮출 수 있다. 또한 두 개 이상의 원자들이 붙어 있는 앙상블 자리(ensemble site)가 없기 때문에 원하는 생성물을 선택적으로 얻을 수 있다.
이러한 장점에도 불구하고 단일원자 촉매는 낮은 배위수(coordination number)와 높은 표면자유에너지로 인해 쉽게 뭉치고 안정성이 떨어져 실제 장치에 적용이 어렵다는 한계를 갖는다.
연구팀은 백금 단일원자 촉매의 안정성을 높이기 위해 금속 원소인 안티몬이 첨가된 주석 산화물(Antimony-doped tin oxide, ATO) 위에 백금 단일원자가 주석과의 합금 형태로 존재하는 구조를 개발했다.
연구팀은 이러한 구조가 백금 단일원자가 안티몬-주석 합금 구조에서 안티몬의 자리를 대신해 열역학적으로 안정적인 형태로 존재함을 계산을 통해 증명했다.
연구팀이 개발한 촉매는 포름산 산화반응에서 일반적으로 사용되는 촉매인 상용백금촉매(Pt/C)보다 최대 50배 높은 활성을 보였고 장기안정성 또한 월등하게 높았다.
또한 연구팀은 이 촉매를 막과 전극으로 구성된 직접 포름산 연료전지에 적용했다. 단일원자 촉매를 완전지 형태의 연료전지에 적용한 것은 최초의 시도로, 기존 촉매에 비해 10분의 1 정도만의 백금을 사용해도 비슷한 출력을 얻을 수 있다.
이현주 교수는 “귀금속 단일원자 촉매의 가장 큰 문제점인 낮은 함량과 낮은 안정성을 높일 수 있었고 최초로 직접 포름산 연료전지에 적용했다”며 “연료전지에 적용 가능한 고함량 및 고안정성 귀금속 단일원자 촉매의 개발에 기여할 수 있을 것이다”고 말했다.
이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 백금 단일 원자 촉매의 개념도
그림2. 관찰한 촉매 및 백금 단일 원자 (흰색 원으로 표시된 밝은 점)
이현주 교수, 백금 사용량 10분의1로 줄인 단일원자 촉매 개발
〈 이 현 주 교수, 김 지 환 학생 〉
우리 대학 생명화학공학과 이현주 교수와 서울시립대 한정우 교수 공동 연구팀이 기존 촉매의 백금 사용량을 10분의 1로 줄일 수 있는 백금 단일원자 촉매를 개발했다.
이는 매우 안정적인 고함량의 백금 단일원자 촉매로 연구팀은 ‘직접 포름산 연료전지(Direct formic acid fuel cells)’에 적용하는 데 성공했다.
김지환 학생이 1저자로 참여한 이번 연구 결과는 재료 과학분야의 국제 학술지 ‘어드밴스드 에너지 머티리얼즈(Advanced Energy Materials)’ 9월 11일자 온라인 판에 게재됐다.
백금 기반의 축매는 활성과 안정성이 높아 다양한 촉매 반응에 적용되지만 가격이 비싸고 희귀하기 때문에 백금의 사용량을 최대한 줄이는 것이 중요하다.
그 중 단일원자 촉매는 백금 입자 크기를 원자 단위로 줄여 모든 원자가 반응에 참여하기 때문에 백금 촉매의 가격을 획기적으로 낮출 수 있다. 또한 두 개 이상의 원자들이 붙어 있는 앙상블 자리(ensemble site)가 없기 때문에 원하는 생성물을 선택적으로 얻을 수 있다.
이러한 장점에도 불구하고 단일원자 촉매는 낮은 배위수(coordination number)와 높은 표면자유에너지로 인해 쉽게 뭉치고 안정성이 떨어져 실제 장치에 적용이 어렵다는 한계를 갖는다.
연구팀은 백금 단일원자 촉매의 안정성을 높이기 위해 금속 원소인 안티몬이 첨가된 주석 산화물(Antimony-doped tin oxide, ATO) 위에 백금 단일원자가 주석과의 합금 형태로 존재하는 구조를 개발했다.
연구팀은 이러한 구조가 백금 단일원자가 안티몬-주석 합금 구조에서 안티몬의 자리를 대신해 열역학적으로 안정적인 형태로 존재함을 계산을 통해 증명했다.
연구팀이 개발한 촉매는 포름산 산화반응에서 일반적으로 사용되는 촉매인 상용백금촉매(Pt/C)보다 최대 50배 높은 활성을 보였고 장기안정성 또한 월등하게 높았다.
또한 연구팀은 이 촉매를 막과 전극으로 구성된 직접 포름산 연료전지에 적용했다. 단일원자 촉매를 완전지 형태의 연료전지에 적용한 것은 최초의 시도로, 기존 촉매에 비해 10분의 1 정도만의 백금을 사용해도 비슷한 출력을 얻을 수 있다.
이현주 교수는 “귀금속 단일원자 촉매의 가장 큰 문제점인 낮은 함량과 낮은 안정성을 높일 수 있었고 최초로 직접 포름산 연료전지에 적용했다”며 “연료전지에 적용 가능한 고함량 및 고안정성 귀금속 단일원자 촉매의 개발에 기여할 수 있을 것이다”고 말했다.
이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 백금 단일 원자 촉매의 개념도
그림2. 관찰한 촉매 및 백금 단일 원자 (흰색 원으로 표시된 밝은 점)
2017.10.24
조회수 21753
-
 김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27
조회수 22009
-
 최광욱 교수, 기관의 크기를 조절하는 유전자 발견
〈최 광 욱 교수〉
우리 대학 생명과학과 최광욱 교수 연구팀이 돌연변이 유전자의 세포분열이 증가하고 기관이 비정상적으로 커지는 현상의 원인을 밝혔다.
연구팀은 우리 몸의 각 기관이 정상적인 크기로 자라게 하는 히포네트워크(Hippo Network) 내에서 쉽원(Schip1)이라는 새로운 단백질을 발견하고 기능 원리를 규명했다.
이번 연구는 셀(Cell) 자매지인 ‘디벨롭멘탈 셀(Developmental Cell) 7일자 온라인 판에 게재됐다. (논문명: Drospohila Schip1 links Expanded to Tao-1 to regulate Hippo signaling)
생명체에는 각 기관들이 적절한 크기가 되도록 스스로 조절하는 능력이 있다. 이것을 가능하게 만드는 각 요소들은 서로 네트워크를 이뤄 작동하고, 그 네트워크를 히포 네트워크라 부른다.
이 히포네트워크에 유전적 혹은 후천적으로 문제가 발생하면 조절능력을 상실해 기관에서 종양을 만들게 되고 생명을 위협하는 요소가 된다. 따라서 네트워크를 구성하는 요소를 밝히고 완성시키는 것은 불확실한 종양의 발생원인 규명에 필수적이다.
과학계는 지속적 연구를 통해 히포네트워크의 구성요소들과 기능 및 역할을 발견했다. 하지만 이 네트워크에서 중심적으로 작동하는 두 요소인 ‘타오 원(Tao-1)’과 ‘익스팬디드(Expanded)’ 사이의 기작은 밝혀지지 않았다.
익스팬디드와 타오원이 네트워크 내에서 관련이 있다는 점은 밝혀졌지만 어떤 방식으로 연결됐는지, 직접적인 연관은 무엇인지에 대한 부분은 밝혀내야 할 숙제로 남아 있었다.
연구팀은 문제 해결을 위해 히포 네트워크 유전자가 처음 발견된 초파리를 이용했다. 히포 네트워크는 초파리부터 인간까지 거의 동일한 유전자에 의해 조절되고 있기 때문이다.
연구팀은 초파리 히포네트워크 내 쉽원(Schip1) 요소가 익스팬디드와 타오원 사이의 매개체라는 사실을 규명했다. 쉽원은 타오원을 세포막으로 끌어들이는 역할을 하고 익스팬디드는 쉽원이 적절한 위치를 잡게 해 준다.
이 쉽원 유전자에 돌연변이가 생길 경우 세포분열이 크게 증가하고 결과적으로 기관의 크기가 비정상적으로 커지는 등 암 조직에서 나타나는 여러 형질이 발생한다.
연구팀은 쉽원 유전자가 초파리 뿐 아니라 인체에도 잘 보존돼 있기 때문에 종양의 원인 규명 및 치료법 개발에도 중요한 역할을 할 것이라고 밝혔다. 향후 고등 생명체를 이용한 추가적 연구가 진행될 것으로 기대된다.
최 교수는 “지금까지 단절됐던 상류와 하류 요소를 이어주는 중요한 고리를 찾았다”며 “이는 매우 의미있는 발견이다”고 말했다.
정형록 박사과정이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
□ 그림 설명
그림1. 쉽원이 없을 때 초파리 눈 크기 변화
그림2. 이전의 완성되지 않았던 히포네트워크와 현재 본 논문을 통해 완성된 히포 네트워크
그림3. 쉽원 돌연변이에서 히포의 양이 급격하게 늘어나는 모습
최광욱 교수, 기관의 크기를 조절하는 유전자 발견
〈최 광 욱 교수〉
우리 대학 생명과학과 최광욱 교수 연구팀이 돌연변이 유전자의 세포분열이 증가하고 기관이 비정상적으로 커지는 현상의 원인을 밝혔다.
연구팀은 우리 몸의 각 기관이 정상적인 크기로 자라게 하는 히포네트워크(Hippo Network) 내에서 쉽원(Schip1)이라는 새로운 단백질을 발견하고 기능 원리를 규명했다.
이번 연구는 셀(Cell) 자매지인 ‘디벨롭멘탈 셀(Developmental Cell) 7일자 온라인 판에 게재됐다. (논문명: Drospohila Schip1 links Expanded to Tao-1 to regulate Hippo signaling)
생명체에는 각 기관들이 적절한 크기가 되도록 스스로 조절하는 능력이 있다. 이것을 가능하게 만드는 각 요소들은 서로 네트워크를 이뤄 작동하고, 그 네트워크를 히포 네트워크라 부른다.
이 히포네트워크에 유전적 혹은 후천적으로 문제가 발생하면 조절능력을 상실해 기관에서 종양을 만들게 되고 생명을 위협하는 요소가 된다. 따라서 네트워크를 구성하는 요소를 밝히고 완성시키는 것은 불확실한 종양의 발생원인 규명에 필수적이다.
과학계는 지속적 연구를 통해 히포네트워크의 구성요소들과 기능 및 역할을 발견했다. 하지만 이 네트워크에서 중심적으로 작동하는 두 요소인 ‘타오 원(Tao-1)’과 ‘익스팬디드(Expanded)’ 사이의 기작은 밝혀지지 않았다.
익스팬디드와 타오원이 네트워크 내에서 관련이 있다는 점은 밝혀졌지만 어떤 방식으로 연결됐는지, 직접적인 연관은 무엇인지에 대한 부분은 밝혀내야 할 숙제로 남아 있었다.
연구팀은 문제 해결을 위해 히포 네트워크 유전자가 처음 발견된 초파리를 이용했다. 히포 네트워크는 초파리부터 인간까지 거의 동일한 유전자에 의해 조절되고 있기 때문이다.
연구팀은 초파리 히포네트워크 내 쉽원(Schip1) 요소가 익스팬디드와 타오원 사이의 매개체라는 사실을 규명했다. 쉽원은 타오원을 세포막으로 끌어들이는 역할을 하고 익스팬디드는 쉽원이 적절한 위치를 잡게 해 준다.
이 쉽원 유전자에 돌연변이가 생길 경우 세포분열이 크게 증가하고 결과적으로 기관의 크기가 비정상적으로 커지는 등 암 조직에서 나타나는 여러 형질이 발생한다.
연구팀은 쉽원 유전자가 초파리 뿐 아니라 인체에도 잘 보존돼 있기 때문에 종양의 원인 규명 및 치료법 개발에도 중요한 역할을 할 것이라고 밝혔다. 향후 고등 생명체를 이용한 추가적 연구가 진행될 것으로 기대된다.
최 교수는 “지금까지 단절됐던 상류와 하류 요소를 이어주는 중요한 고리를 찾았다”며 “이는 매우 의미있는 발견이다”고 말했다.
정형록 박사과정이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
□ 그림 설명
그림1. 쉽원이 없을 때 초파리 눈 크기 변화
그림2. 이전의 완성되지 않았던 히포네트워크와 현재 본 논문을 통해 완성된 히포 네트워크
그림3. 쉽원 돌연변이에서 히포의 양이 급격하게 늘어나는 모습
2016.03.18
조회수 15199
-
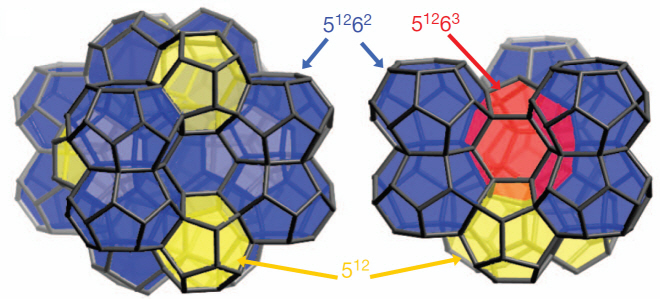 연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
2012.07.24
조회수 22821
-
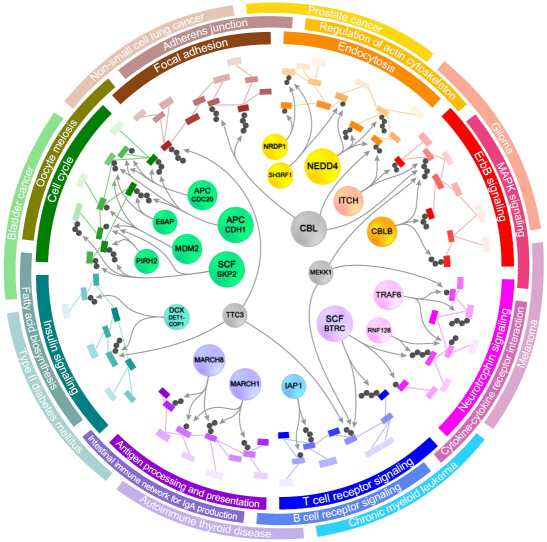 단백질 분해조절 효소 정보 담은 바이오마커 발굴 시스템 개발
- Mol Cell Proteomics지 게재, “바이오마커 개발의 새로운 패러다임 제시” -
단백질의 분해를 조절하는 효소와 기질에 대한 관계정보를 담은 바이오마커* 발굴 시스템(E3Net)이 국내 연구진에 의해 개발되어, 고부가가치의 새로운 바이오마커 개발에 가능성이 열렸다.
※ 바이오마커(Biomarker) : 유전자, 단백질 등에서 유래된 특이한 패턴의 분자적 정보로, 유전적․후천적 영향으로 발생한 신체의 변화를 감지할 수 있는 생물표지인자
우리학교 바이오및뇍 이관수 교수(49세)가 주도하고, 한영웅 박사과정생, 이호동 박사 및 박종철 교수가 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 선도연구센터지원사업(NCRC), 신기술융합형성장동력사업 및 교육과학기술부의 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원으로 수행되었고, 단백질체 연구 분야의 권위 있는 학술지인 ‘Molecular and Cellular Proteomics"지 4월호(4월 1일자)에 게재되었다. (논문명: A system for exploring E3-mediated regulatory networks of cellular functions)이관수 교수 연구팀은 전 세계 바이오 관련 DB(데이터베이스)와 논문(약 2만 편)으로부터 정보를 추출해 단백질 분해를 조절하는 효소(E3 효소)와 기질*들 간의 네트워크를 집대성하여, 이와 관련된 세포의 기능과 질병을 분석하는 ‘E3Net’ 시스템을 개발하였다.
※ 기질(substrate) : 효소와 특이적으로 결합하여 화학반응을 일으키는 분자로, 소화작용은 우리의 몸속에서 일어나는 효소와 기질간의 반응의 대표적인 사례
세포는 시시각각 변하는 환경에 대응하여 필요한 단백질들을 생산, 폐기 및 재활용하는 정교한 시스템을 가지고 있는데, 만일 이 과정에서 오류가 생기면 ‘질병’으로 이어질 수 있다.
따라서 단백질 분해를 조절하는 E3 효소와 기질 간의 관계를 파악하면 관련 질병을 치료하거나 예방할 수 있게 된다. 특히 E3 효소는 단백질 분해의 80%를 담당하는 것으로 알려져 수많은 질병이 관련되어 있을 것으로 예측되고 있다.
그러나 E3 효소와 기질 간의 정보들이 개별 논문과 DB에 흩어져 있어, 단백질 분해 조절과 관련된 세포의 기능과 질병의 특성을 종합적․체계적으로 분석할 수 없었다.
이 교수팀은 모든 E3 효소(2,201개)와 기질(4,896개) 및 그 조절관계(1,671개)에 대한 정보를 통합하여 E3 효소 조절 네트워크 내에 존재하는 관련된 세포의 기능과 질병을 시스템적으로 분석할 수 있는 E3Net을 구축하는데 성공하였다.
이 네트워크는 지금까지 구축된 조절정보를 모두 합친 것보다 무려 10배에 이르는 방대한 양으로, E3 효소가 독자적으로 또는 협력해서 조절하는 세포의 기능과 관련 질병을 정확히 파악할 수 있는 토대가 마련된 첫 사례로서 의미가 크다.
연구팀은 E3Net을 이용하면 각각의 질병과 관련된 단백질들의 분해조절을 담당하는 E3 효소들을 찾을 수 있고, 분해조절 원리와 세포기능 네트워크를 함께 파악하여 질병의 발생 원인이나 환자에 적합한 맞춤형 치료방법을 제공할 수 있는 바이오마커를 발굴할 수 있을 것으로 기대한다.
실제 연구팀은 E3Net을 활용해 암, 뇌심혈관 질환 및 당뇨병 등 현대인의 대표적 질환과 관련된 E3 바이오마커 후보 수십 개를 새롭게 발견하는 등 눈에 띄는 성과를 거두었고, 현재 이를 검증할 후속 연구를 계획하고 있다. 이관수 교수는 “이번 연구결과로 E3 효소와 관련된 단백질 분해조절의 네트워크가 구축되고, 이 네트워크에 존재하는 세포의 기능과 질병의 특이성을 시스템적으로 분석할 수 있게 됨에 따라, E3 효소와 관련된 세포의 기능 연구와 질병 연구에 새로운 전기가 마련되었다”고 연구의의를 밝혔다.
단백질 분해조절 효소 정보 담은 바이오마커 발굴 시스템 개발
- Mol Cell Proteomics지 게재, “바이오마커 개발의 새로운 패러다임 제시” -
단백질의 분해를 조절하는 효소와 기질에 대한 관계정보를 담은 바이오마커* 발굴 시스템(E3Net)이 국내 연구진에 의해 개발되어, 고부가가치의 새로운 바이오마커 개발에 가능성이 열렸다.
※ 바이오마커(Biomarker) : 유전자, 단백질 등에서 유래된 특이한 패턴의 분자적 정보로, 유전적․후천적 영향으로 발생한 신체의 변화를 감지할 수 있는 생물표지인자
우리학교 바이오및뇍 이관수 교수(49세)가 주도하고, 한영웅 박사과정생, 이호동 박사 및 박종철 교수가 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 선도연구센터지원사업(NCRC), 신기술융합형성장동력사업 및 교육과학기술부의 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원으로 수행되었고, 단백질체 연구 분야의 권위 있는 학술지인 ‘Molecular and Cellular Proteomics"지 4월호(4월 1일자)에 게재되었다. (논문명: A system for exploring E3-mediated regulatory networks of cellular functions)이관수 교수 연구팀은 전 세계 바이오 관련 DB(데이터베이스)와 논문(약 2만 편)으로부터 정보를 추출해 단백질 분해를 조절하는 효소(E3 효소)와 기질*들 간의 네트워크를 집대성하여, 이와 관련된 세포의 기능과 질병을 분석하는 ‘E3Net’ 시스템을 개발하였다.
※ 기질(substrate) : 효소와 특이적으로 결합하여 화학반응을 일으키는 분자로, 소화작용은 우리의 몸속에서 일어나는 효소와 기질간의 반응의 대표적인 사례
세포는 시시각각 변하는 환경에 대응하여 필요한 단백질들을 생산, 폐기 및 재활용하는 정교한 시스템을 가지고 있는데, 만일 이 과정에서 오류가 생기면 ‘질병’으로 이어질 수 있다.
따라서 단백질 분해를 조절하는 E3 효소와 기질 간의 관계를 파악하면 관련 질병을 치료하거나 예방할 수 있게 된다. 특히 E3 효소는 단백질 분해의 80%를 담당하는 것으로 알려져 수많은 질병이 관련되어 있을 것으로 예측되고 있다.
그러나 E3 효소와 기질 간의 정보들이 개별 논문과 DB에 흩어져 있어, 단백질 분해 조절과 관련된 세포의 기능과 질병의 특성을 종합적․체계적으로 분석할 수 없었다.
이 교수팀은 모든 E3 효소(2,201개)와 기질(4,896개) 및 그 조절관계(1,671개)에 대한 정보를 통합하여 E3 효소 조절 네트워크 내에 존재하는 관련된 세포의 기능과 질병을 시스템적으로 분석할 수 있는 E3Net을 구축하는데 성공하였다.
이 네트워크는 지금까지 구축된 조절정보를 모두 합친 것보다 무려 10배에 이르는 방대한 양으로, E3 효소가 독자적으로 또는 협력해서 조절하는 세포의 기능과 관련 질병을 정확히 파악할 수 있는 토대가 마련된 첫 사례로서 의미가 크다.
연구팀은 E3Net을 이용하면 각각의 질병과 관련된 단백질들의 분해조절을 담당하는 E3 효소들을 찾을 수 있고, 분해조절 원리와 세포기능 네트워크를 함께 파악하여 질병의 발생 원인이나 환자에 적합한 맞춤형 치료방법을 제공할 수 있는 바이오마커를 발굴할 수 있을 것으로 기대한다.
실제 연구팀은 E3Net을 활용해 암, 뇌심혈관 질환 및 당뇨병 등 현대인의 대표적 질환과 관련된 E3 바이오마커 후보 수십 개를 새롭게 발견하는 등 눈에 띄는 성과를 거두었고, 현재 이를 검증할 후속 연구를 계획하고 있다. 이관수 교수는 “이번 연구결과로 E3 효소와 관련된 단백질 분해조절의 네트워크가 구축되고, 이 네트워크에 존재하는 세포의 기능과 질병의 특이성을 시스템적으로 분석할 수 있게 됨에 따라, E3 효소와 관련된 세포의 기능 연구와 질병 연구에 새로운 전기가 마련되었다”고 연구의의를 밝혔다.
2012.05.01
조회수 25923
-
 매미와 개구리는 지휘자없이 어떻게 합창할까
나무위의 매미와 논두렁의 개구리는 지휘자 없이 어떻게 합창할까? 이와 관련해서, KAIST 바이오 및 뇌공학과의 조광현 교수는 생명체의 동기화된 주기적 진동신호의 생성원리를 최근 규명했다. 나무에 붙어있는 많은 반딧불들의 동시다발적인 깜빡임, 매미들의 조율된 울음소리, 뇌신경세포들간의 전기신호, 세포내 분자들의 농도변화에 이르기까지 생명체는 다양한 형태의 주기적 진동신호 교환을 통해 정보를 전달하는데, 이들은 놀랍게도 정확히 동일한 위상(phase)으로 동기화되곤 한다. 이는 마치 오케스트라에서 지휘자 없이도 모든 연주가 일정한 박자에 맞춰 이루어지는 것과 같다.
어떻게 생명체의 여러 주기적 진동신호들이 그러한 동기화를 이루는가?
우리학교 바이오및뇌공학과 조광현(曺光鉉) 교수 연구팀이 대규모 가상세포(virtual cell)실험을 통해 생명체의 다양한 주기적 진동(oscillation)신호들이 동기화(synchronization)되는 보편적인 원리를 규명했다.
曺교수팀은 이번 연구를 통해 여러 독립적인 주기적 진동신호들은 양성피드백(positive feedback)을 통해 서로의 위상에 영향을 줘 하나의 동일한 위상으로 수렴되는 현상을 밝혀냈다.
특히 양성피드백은 이중활성(double activation) 또는 이중억제(double inhibition)의 구조로 구현된다. 이중활성피드백은 연결시간지연이 짧을 때, 이중억제피드백은 연결시간지연이 길 때 보다 안정적인 신호동기화를 가능하게 했다.
또한, 노이즈(noise) 교란이 있을 때 이중활성피드백은 진동신호의 주기보다 진폭을 안정적으로 유지하는 반면 이중억제피드백은 연결강도에 불규칙한 변화가 주어졌을 때 일정한 주기와 진폭을 유지시켜줬다. 현존하는 대부분의 현상들이 이러한 원칙을 따르고 있었다.
이번에 규명된 원리는 생체내 주기적 진동신호의 동기화가 교란될 때 발생하는 뇌질환 등 여러 질병의 원인을 새롭게 조명하는 계기를 마련할 것으로 기대된다.
이번 연구는 기존 생명과학의 난제에 대해 IT융합기술인 시스템생물학(Systems Biology) 연구를 통해 해답을 제시할 수 있음을 보여줬으며, 향후 생명과학 연구에 있어서 가상세포실험의 무한한 가능성을 제시했다.
曺교수는 “생명체는 복잡하게 얽혀있는 것으로 보이는 네트워크속에 이와 같이 정교한 진화적 설계원리를 간직하고 있었다”며 “이러한 규칙들은 임의로 수많은 디지털 진동자들을 만들어 인공진화를 통해 신호의 동기화 현상을 관측하였을 때에도 마찬가지로 성립된다는 흥미로운 사실을 확인했다”고 말했다.
이 연구는 교육과학기술부가 지원하는 한국연구재단 연구사업의 일환으로 수행되었으며, 연구결과는 세포생물학 분야 권위지인 세포과학저널(Journal of Cell Science) 2010년 1월 26일자 온라인판에 게재됐다.
세포생물학 실험결과만을 출판하는 이 저널에 순수 컴퓨터시뮬레이션만으로 수행된 가상세포실험 연구결과가 게재된 것은 매우 이례적인 일이다.
인터넷주소: http://jcs.biologists.org/cgi/content/abstract/jcs.060061v1
<용어설명>◯ 양성피드백(positive feedback): 서로 연결되어 있는 두 요소 사이에 어느 하나의 변화가 결과적으로 스스로를 동일한 방향으로 더욱 변화시키는 형태의 연결구조.
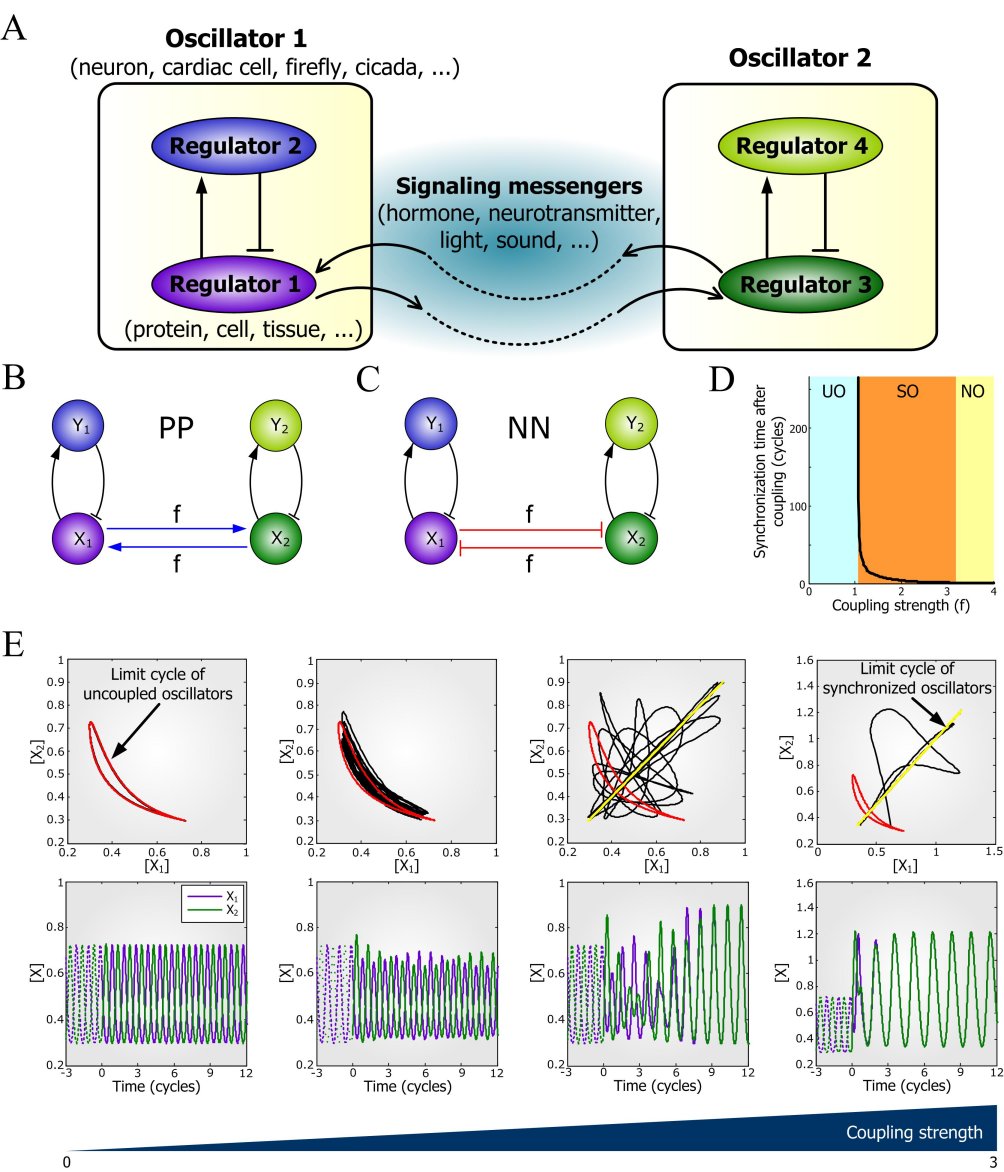
<사진설명>◯ 설명: A: 서로 상호작용하는 두 생체신호 진동자(oscillator)들의 예시. B: 이중활성 양성피드백으로 연결된 진동자들. C: 이중억제 양성피드백으로 연결된 진동자들. D: 연결강도에 따라 진동신호 동기화에 소요되는 시간. E: 연결강도 증가에 따라 점차 진동신호 동기화가 되어가는 모습의 예시 (좌측의 비동기화 진동신호들이 점차 우측의 동기화된 진동신호들로 변화되어 가는 과정을 나타냄).
매미와 개구리는 지휘자없이 어떻게 합창할까
나무위의 매미와 논두렁의 개구리는 지휘자 없이 어떻게 합창할까? 이와 관련해서, KAIST 바이오 및 뇌공학과의 조광현 교수는 생명체의 동기화된 주기적 진동신호의 생성원리를 최근 규명했다. 나무에 붙어있는 많은 반딧불들의 동시다발적인 깜빡임, 매미들의 조율된 울음소리, 뇌신경세포들간의 전기신호, 세포내 분자들의 농도변화에 이르기까지 생명체는 다양한 형태의 주기적 진동신호 교환을 통해 정보를 전달하는데, 이들은 놀랍게도 정확히 동일한 위상(phase)으로 동기화되곤 한다. 이는 마치 오케스트라에서 지휘자 없이도 모든 연주가 일정한 박자에 맞춰 이루어지는 것과 같다.
어떻게 생명체의 여러 주기적 진동신호들이 그러한 동기화를 이루는가?
우리학교 바이오및뇌공학과 조광현(曺光鉉) 교수 연구팀이 대규모 가상세포(virtual cell)실험을 통해 생명체의 다양한 주기적 진동(oscillation)신호들이 동기화(synchronization)되는 보편적인 원리를 규명했다.
曺교수팀은 이번 연구를 통해 여러 독립적인 주기적 진동신호들은 양성피드백(positive feedback)을 통해 서로의 위상에 영향을 줘 하나의 동일한 위상으로 수렴되는 현상을 밝혀냈다.
특히 양성피드백은 이중활성(double activation) 또는 이중억제(double inhibition)의 구조로 구현된다. 이중활성피드백은 연결시간지연이 짧을 때, 이중억제피드백은 연결시간지연이 길 때 보다 안정적인 신호동기화를 가능하게 했다.
또한, 노이즈(noise) 교란이 있을 때 이중활성피드백은 진동신호의 주기보다 진폭을 안정적으로 유지하는 반면 이중억제피드백은 연결강도에 불규칙한 변화가 주어졌을 때 일정한 주기와 진폭을 유지시켜줬다. 현존하는 대부분의 현상들이 이러한 원칙을 따르고 있었다.
이번에 규명된 원리는 생체내 주기적 진동신호의 동기화가 교란될 때 발생하는 뇌질환 등 여러 질병의 원인을 새롭게 조명하는 계기를 마련할 것으로 기대된다.
이번 연구는 기존 생명과학의 난제에 대해 IT융합기술인 시스템생물학(Systems Biology) 연구를 통해 해답을 제시할 수 있음을 보여줬으며, 향후 생명과학 연구에 있어서 가상세포실험의 무한한 가능성을 제시했다.
曺교수는 “생명체는 복잡하게 얽혀있는 것으로 보이는 네트워크속에 이와 같이 정교한 진화적 설계원리를 간직하고 있었다”며 “이러한 규칙들은 임의로 수많은 디지털 진동자들을 만들어 인공진화를 통해 신호의 동기화 현상을 관측하였을 때에도 마찬가지로 성립된다는 흥미로운 사실을 확인했다”고 말했다.
이 연구는 교육과학기술부가 지원하는 한국연구재단 연구사업의 일환으로 수행되었으며, 연구결과는 세포생물학 분야 권위지인 세포과학저널(Journal of Cell Science) 2010년 1월 26일자 온라인판에 게재됐다.
세포생물학 실험결과만을 출판하는 이 저널에 순수 컴퓨터시뮬레이션만으로 수행된 가상세포실험 연구결과가 게재된 것은 매우 이례적인 일이다.
인터넷주소: http://jcs.biologists.org/cgi/content/abstract/jcs.060061v1
<용어설명>◯ 양성피드백(positive feedback): 서로 연결되어 있는 두 요소 사이에 어느 하나의 변화가 결과적으로 스스로를 동일한 방향으로 더욱 변화시키는 형태의 연결구조.
<사진설명>◯ 설명: A: 서로 상호작용하는 두 생체신호 진동자(oscillator)들의 예시. B: 이중활성 양성피드백으로 연결된 진동자들. C: 이중억제 양성피드백으로 연결된 진동자들. D: 연결강도에 따라 진동신호 동기화에 소요되는 시간. E: 연결강도 증가에 따라 점차 진동신호 동기화가 되어가는 모습의 예시 (좌측의 비동기화 진동신호들이 점차 우측의 동기화된 진동신호들로 변화되어 가는 과정을 나타냄).
2010.02.02
조회수 25152
 사람 3D 폐포 배양 기술로 코로나19 감염 기전을 규명하는 데 성공
우리 대학 연구진 포함 국내 연구진이 실험실에서 3차원으로 키운 사람의 폐포(허파꽈리)에 코로나19 바이러스를 배양해 감염 기전과 치료제 개발에 적용이 가능한 기술 개발에 성공했다.
국제 통계 사이트 월드오미터에 따르면 전 세계 누적 코로나바이러스감염증-19(이하 코로나19) 확진자 수는 25일 기준 4,331만 8,941명으로 지난 18일(4,030만 1,609명) 4,000만 명을 넘어선 후 일주일 만에 4,331만을 돌파하는 2차 대유행이 점차 현실화돼 가고 있다.
우리 대학 의과학대학원 주영석 교수 연구팀은 인간의 폐포 세포를 실험실에서 구현하는 3D 미니 장기기술을 개발하고 이를 활용해 코로나19 바이러스가 인간의 폐 세포를 파괴하는 과정을 정밀하게 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 영국 케임브리지대학 이주현 박사를 비롯해 국립보건연구원 국립감염병연구소 최병선 과장·기초과학연구원(IBS) 고규영 혈관연구단장(우리 대학 의과학대학원 교수)·서울대병원 김영태 교수와 우리 대학 교원창업기업인 ㈜지놈인사이트와 공동으로 진행됐다.
공동연구팀의 이번 연구 결과는 줄기세포 분야 세계적인 학술지 `Cell Stem Cell' 10월 22일 字 온라인판에 실렸다. (논문명: Three-dimensional human alveolar stem cell culture models reveal infection response to SARS-CoV-2)
정확한 질병 기전의 이해를 기반으로 치료제를 효과적으로 개발하기 위해서는 실험실에서 사용 가능한 인체를 모사한 모델 사용이 필수적이다. 코로나19 바이러스는 생쥐 모델에 감염시키기가 어렵고, 특히 실험실에서 사용할 수 있는 폐 세포 모델은 존재하지 않기 때문에 직접적인 감염 연구의 한계가 존재해왔다.
공동연구팀은 이런 문제를 해소하기 위해 지속적으로 배양이 가능한 3차원 인간 폐포 모델을 새롭게 정립했다. 이를 이용하면 실험실에서 사람의 폐 세포를 이용해 코로나19 바이러스 등 각종 호흡기 바이러스의 질병 기전을 연구할 수 있기 때문이다. 더 나가서 3차원 인간 폐포 모델은 약물 스크리닝 등 치료법 개발에도 직접적으로 응용할 수 있다는 장점이 있다.
공동연구팀은 폐암 등 사람의 수술 검사재료에서 확보되는 사람 폐 조직을 장기간 안정적으로 3차원 배양할 수 있는 조건을 알아내는 데 성공했다. 실험 결과, 3D 폐포는 코로나19 바이러스에 노출되면 6시간 내 급속한 바이러스 증식이 일어나 세포 감염이 완료됐으나, 이를 막기 위한 폐 세포의 선천 면역 반응 활성화에는 약 3일가량의 시간이 걸렸다.
이와 함께 하나의 코로나19 바이러스 입자는 하나의 세포를 감염시키는 데 충분하다는 사실을 알아냈다. 감염 3일째 공동연구팀은 세포 가운데 일부분이 고유의 기능을 급격히 상실한다는 사실도 확인했다.
공동 교신저자인 주영석 교수는 "이번에 개발한 3차원 인체 폐 배양 모델 규모를 확대한다면 코로나19 바이러스를 포함한 다양한 호흡기 바이러스의 감염 연구에 유용하게 사용될 것ˮ이라고 말했다.
주 교수는 이어 "동물이나 다른 장기 유래의 세포가 아닌 호흡기 바이러스의 표적 세포인 사람의 폐 세포를 직접적으로 질병 연구에 응용함으로써 효율적이고 정확한 기전 규명은 물론 치료제 개발에도 이용할 수 있다ˮ고 강조했다.
코로나19 바이러스 대응 기술개발을 위해서는 다양한 기관의 지원과 관련 연구자들의 협력 연구가 필수적이다. 공동연구팀의 이번 연구는 한국연구재단·질병관리청·기초과학연구원(IBS)·서울대학교 의과대학·유럽연구이사회(ERC)·서경배과학재단·휴먼프론티어과학재단의 지원을 받아 수행됐다.
2020.10.26 조회수 33686
사람 3D 폐포 배양 기술로 코로나19 감염 기전을 규명하는 데 성공
우리 대학 연구진 포함 국내 연구진이 실험실에서 3차원으로 키운 사람의 폐포(허파꽈리)에 코로나19 바이러스를 배양해 감염 기전과 치료제 개발에 적용이 가능한 기술 개발에 성공했다.
국제 통계 사이트 월드오미터에 따르면 전 세계 누적 코로나바이러스감염증-19(이하 코로나19) 확진자 수는 25일 기준 4,331만 8,941명으로 지난 18일(4,030만 1,609명) 4,000만 명을 넘어선 후 일주일 만에 4,331만을 돌파하는 2차 대유행이 점차 현실화돼 가고 있다.
우리 대학 의과학대학원 주영석 교수 연구팀은 인간의 폐포 세포를 실험실에서 구현하는 3D 미니 장기기술을 개발하고 이를 활용해 코로나19 바이러스가 인간의 폐 세포를 파괴하는 과정을 정밀하게 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 영국 케임브리지대학 이주현 박사를 비롯해 국립보건연구원 국립감염병연구소 최병선 과장·기초과학연구원(IBS) 고규영 혈관연구단장(우리 대학 의과학대학원 교수)·서울대병원 김영태 교수와 우리 대학 교원창업기업인 ㈜지놈인사이트와 공동으로 진행됐다.
공동연구팀의 이번 연구 결과는 줄기세포 분야 세계적인 학술지 `Cell Stem Cell' 10월 22일 字 온라인판에 실렸다. (논문명: Three-dimensional human alveolar stem cell culture models reveal infection response to SARS-CoV-2)
정확한 질병 기전의 이해를 기반으로 치료제를 효과적으로 개발하기 위해서는 실험실에서 사용 가능한 인체를 모사한 모델 사용이 필수적이다. 코로나19 바이러스는 생쥐 모델에 감염시키기가 어렵고, 특히 실험실에서 사용할 수 있는 폐 세포 모델은 존재하지 않기 때문에 직접적인 감염 연구의 한계가 존재해왔다.
공동연구팀은 이런 문제를 해소하기 위해 지속적으로 배양이 가능한 3차원 인간 폐포 모델을 새롭게 정립했다. 이를 이용하면 실험실에서 사람의 폐 세포를 이용해 코로나19 바이러스 등 각종 호흡기 바이러스의 질병 기전을 연구할 수 있기 때문이다. 더 나가서 3차원 인간 폐포 모델은 약물 스크리닝 등 치료법 개발에도 직접적으로 응용할 수 있다는 장점이 있다.
공동연구팀은 폐암 등 사람의 수술 검사재료에서 확보되는 사람 폐 조직을 장기간 안정적으로 3차원 배양할 수 있는 조건을 알아내는 데 성공했다. 실험 결과, 3D 폐포는 코로나19 바이러스에 노출되면 6시간 내 급속한 바이러스 증식이 일어나 세포 감염이 완료됐으나, 이를 막기 위한 폐 세포의 선천 면역 반응 활성화에는 약 3일가량의 시간이 걸렸다.
이와 함께 하나의 코로나19 바이러스 입자는 하나의 세포를 감염시키는 데 충분하다는 사실을 알아냈다. 감염 3일째 공동연구팀은 세포 가운데 일부분이 고유의 기능을 급격히 상실한다는 사실도 확인했다.
공동 교신저자인 주영석 교수는 "이번에 개발한 3차원 인체 폐 배양 모델 규모를 확대한다면 코로나19 바이러스를 포함한 다양한 호흡기 바이러스의 감염 연구에 유용하게 사용될 것ˮ이라고 말했다.
주 교수는 이어 "동물이나 다른 장기 유래의 세포가 아닌 호흡기 바이러스의 표적 세포인 사람의 폐 세포를 직접적으로 질병 연구에 응용함으로써 효율적이고 정확한 기전 규명은 물론 치료제 개발에도 이용할 수 있다ˮ고 강조했다.
코로나19 바이러스 대응 기술개발을 위해서는 다양한 기관의 지원과 관련 연구자들의 협력 연구가 필수적이다. 공동연구팀의 이번 연구는 한국연구재단·질병관리청·기초과학연구원(IBS)·서울대학교 의과대학·유럽연구이사회(ERC)·서경배과학재단·휴먼프론티어과학재단의 지원을 받아 수행됐다.
2020.10.26 조회수 33686 포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2020.03.11 조회수 16493
포유류 종마다 시각 뇌신경망 구조 다른 원인 밝혀
바이오및뇌공학과 백세범 교수 연구팀이 포유류 종들의 시각피질에서 서로 다른 뇌신경망 구조가 형성되는 원리를 밝혔다.
이번 연구결과는 시스템 뇌신경과학 분야에서 수십 년간 설명되지 못했던 문제를 이론적 접근과 계산적 모델 시뮬레이션을 통해 해답을 제시한 계산뇌과학 연구의 성공적인 예시로 평가된다.
연구팀은 두뇌의 시각피질과 망막에 분포하는 신경세포들 간의 정보 추출 비율을 분석함으로써 특정 포유류 종이 갖는 시각피질의 기능적 구조를 예측할 수 있음을 밝혀냈다.
연구팀은 서로 다른 크기의 망막과 시각피질 사이의 신경망 연결 모델을 시뮬레이션 해 두 정보 처리 영역 사이에 대응되는 신경세포의 비율이 달라짐에 따라 완전히 다른 두 가지 구조의 기능성 뇌지도가 형성됨을 보이고, 이 결과가 실제 실험에서 관측되는 신경망 구조와 일치함을 증명했다.
장재선, 송민 박사과정이 공동 1저자로 참여한 이번 연구는 국제 학술지 ‘셀(cell)’의 온라인 자매지 ‘셀 리포츠(Cell Reports)’ 3월 10일 자에 게재됐다. (논문명 : Retino-cortical mapping ratio predicts columnar and salt-and-pepper organization in mammalian visual cortex)
포유류의 시각피질에서는 시각 자극의 방향에 따라 반응의 정도가 달라지는 성질인 방향 선택성(orientation selectivity)을 갖는 세포들이 관측된다. 원숭이, 고양이 등의 종에서는 이 세포들의 선호 방향이 연속적, 주기적인 형태로 변하는 방향성 지도(orientation map) 구조를 형성하는 반면, 생쥐 등의 설치류에서는 마치 소금과 후추를 뿌려 놓은 듯한 무작위에 가까운 형태로 분포해, 이를 소금-후추 구조(salt-and-pepper organization)라 한다.
동일한 역할을 수행하는 것으로 보이는 기능성 뇌신경망이 이렇게 종에 따라 다른 구조를 갖는 원인을 찾기 위해 지난 수십여 년 간 다양한 연구가 진행됐으나, 아직까지도 이를 결정하는 요인에 대해서는 명확하게 알려진 바가 없었다.
이러한 원리를 규명하기 위해 연구팀은 서로 다른 크기의 망막과 시각피질이 연결될 때 동일한 망막 신호를 샘플링하는 시각피질 세포의 비율이 달라지게 된다고 가정했다. 이러한 조건에서 망막-시각피질 신호의 샘플링 형태를 시뮬레이션 하여 샘플링 비율에 따라 시각피질에서 형성되는 기능성 지도의 구조가 완전히 다르게 결정될 수 있음을 발견했다.
이 결과를 기반으로 연구팀은 다양한 종들에 대한 망막 및 시각피질 데이터를 종합적으로 비교해 시각피질이 클수록, 또 망막이 작을수록 연속적인 방향성 지도가 형성되는 경향이 있음을 확인했다.
또한, 기존의 연구에서 확인된 포유류 여덟 종의 시각피질-망막 크기 비율을 기반으로 한 모델을 정량적으로 시뮬레이션하고, 이 결과가 실험에서 관측된 것과 같이 방향성 지도 존재 여부에 따라 두 그룹으로 명확히 나누어짐을 확인했다.
이러한 결과는 다른 종으로 진화가 이뤄질 때, 감각기관의 크기와 같은 지극히 단순한 물리적인 조건의 차이에 의해서도 뇌신경망의 구조가 완전히 다른 방향으로 변화될 수 있음을 뜻한다. 이는 다양한 생물학적 구조가 기존의 생각보다 훨씬 단순한 물리적 요소들의 차이에 의해 예측되거나 설명될 수 있음을 보여준다.
백세범 교수는 “이미 오랫동안 알려져 있었으나 그 의미를 찾아내지 못했던 데이터들과 이론적인 모델을 결합해 새로운 발견을 도출해낸 의미 있는 연구이다”라며 “뇌 과학뿐만 아니라 계통분류학, 진화생물학 등 생물의 기능적 구조와 관련된 다양한 생물학 분야에서 이론적 모델 연구의 역할에 대한 중요한 시각을 제공할 것이다”라고 언급했다.
이번 연구는 한국연구재단의 이공분야기초연구사업 및 원천기술개발사업의 지원을 받아 수행됐다.
2020.03.11 조회수 16493 생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24 조회수 26309
생명화학공학과 대학원생들, 시스템 대사공학 전략 발표
〈 양동수 박사과정, 박다현 석사과정, 최경록 박사과정, 조재성 박사과정, 장우대 박사과정 〉
우리 대학 생명화학공학과 대학원생 다섯 명이 대사공학과 시스템 생물학, 합성 생물학의 결합 시스템 등 대사공학 전반의 전략에 대한 논문을 발표했다.
생명화학공학과는 최근 박사학위를 마친 최경록 연구원과 장우대, 양동수, 조재성 박사과정, 박다현 석사과정이 친환경 화학물질 생산을 위해 필수적인 미생물 공장을 개발하는 전략을 총정리했다.
이 연구의 결과는 셀(Cell)지가 발행하는 생명공학 분야 권위 리뷰 저널인 ‘생명공학의 동향(Trends in Biotechnology)’ 8월호 표지논문 및 주 논문 (Feature review)에 게재됐다. (논문명 : Systems Metabolic Engineering Strategies: Integrating Systems and Synthetic Biology with Metabolic Engineering)
시스템 대사공학은 기존의 석유화학산업을 대체할 바이오산업의 핵심이 되는 미생물 균주를 보다 효과적으로 개발하기 위해 KAIST 생명화학공학과의 이상엽 특훈교수가 창시한 연구 분야다.
전통적 대사공학에 시스템 생물학, 합성 생물학 및 진화 공학 기법을 접목한 시스템 대사공학은 직관적 전략이나 무작위 돌연변이 유발에 의존하는 기존의 대사공학과 비교해 적은 비용과 인력, 짧은 시간 내에 산업에서 이용 가능한 고성능 균주 개발을 가능하게 만든다.
연구 기획 단계에서부터 실제 공장에서 균주의 발효 공정 및 발효를 통해 생산된 물질의 분리/정제 공정까지 고려함으로써 산업 균주 개발 도중 불필요한 시행착오를 최소화할 수 있다.
본 논문에서는 시스템 대사공학 전략을 연구의 흐름에 따라 ▲프로젝트 디자인 ▲균주 선정 ▲대사회로 재구성 ▲표적 화합물에 대한 내성 향상 ▲대사 흐름 최적화 ▲산업 수준으로의 생산 규모 확대 등 일곱 단계로 나누고, 각 단계에서 활용할 수 있는 최신 도구 및 전략들을 총망라했다.
더불어 바이오 기반 화합물 생산의 최신 동향과 함께 고성능 생산 균주를 보다 효과적으로 개발하기 위해 시스템 대사공학이 나아가야 할 방향도 함께 제시했다.
주저자인 최경록 연구원은 “기후 변화가 커지며 기존의 석유화학 산업을 친환경 바이오산업으로 대체하는 것이 불가피하다”라며 “시스템 대사공학은 산업에서 활용 가능한 고성능 생산 균주의 개발을 촉진해 바이오산업 시대의 도래를 앞당길 것이다”라고 말했다.
지도교수인 이상엽 특훈교수는 “그간 우리 연구실과 전 세계에서 수행한 수많은 대사공학연구를 우리가 제시한 시스템 대사공학 전략으로 통합해 체계적으로 분석 및 정리하고 앞으로의 전략을 제시했다는 점에서 큰 의미가 있다”라며 “권위 있는 학술지에 주 논문이자 표지논문으로 게재된 훌륭한 연구를 수행한 학생들이 자랑스럽다”라고 말했다.
이상엽 특훈교수 연구팀은 실제로 시스템 대사공학 전략을 이용해 천연물, 아미노산, 생분해성 플라스틱, 환경친화적 플라스틱 원료, 바이오 연료 등을 생산하는 고성능 균주들을 다수 개발한 바 있다.
이번 연구는 과학기술정보통신부가 지원하는 기후변화대응기술개발사업의 ‘바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제’ 및 한화케미칼이 지원하는 KAIST-한화 미래 기술 연구소의 지원을 받아 수행됐다.
2019.07.24 조회수 26309 주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03 조회수 25694
주영석 교수, 흡연과 무관한 폐암유발 돌연변이 유년기부터 발생 사실 밝혀
〈 주영석 교수 〉
우리 대학 의과학대학원 주영석 교수와 서울대학교 의과대학(학장 신찬수) 흉부외과 김영태 교수 공동 연구팀이 폐암을 일으키는 융합유전자 유전체 돌연변이의 생성 원리를 규명했다.
이번 연구는 흡연과 무관한 환경에서도 융합유전자로 인해 폐 선암이 발생할 수 있다는 사실을 밝힌 것으로, 비흡연자의 폐암 발생 원인 규명과 더불어 정밀치료 시스템을 구축하는 데 적용 가능할 것으로 기대된다.
우리 대학 출신 이준구 박사(現 하버드 의과대학 박사후연구원)와 박성열 박사과정이 공동 1 저자로 참여한 이번 연구는 국제 학술지 ‘셀(Cell)’ 5월 30일 자 온라인판에 게재됐다. (논문명 : Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma) 또한, 이번 연구에는 하버드 의과대학, 한국과학기술정보연구원, 국립암센터 연구자들도 함께 참여했다.
흡연은 폐 선암의 가장 큰 발병 인자로 잘 알려졌지만 암 융합유전자 돌연변이, 즉 ALK, RET, ROS1 등에 의한 암 발생은 대부분 비흡연자에게서 발견된다. 융합유전자로 인한 환자는 전체 폐 선암 환자의 10% 정도를 차지하고 있지만, 이 돌연변이의 생성과정에 대해서는 알려진 것이 거의 없었다.
이전까지의 폐 선암 유전체 연구는 주로 유전자 지역을 규명하는 ‘엑솜 서열분석 기법’이 사용됐으나 연구팀은 유전자 간 부분들을 총망라해 분석하는‘전장 유전체 서열분석 기법’을 대규모로 적용했다.
연구팀은 138개의 폐 선암(lung adenocarcinoma) 사례의 전장 유전체 서열 데이터(whole-genome sequencing)를 생성 및 분석해 암세포에 존재하는 다양한 양상의 유전체 돌연변이를 찾아냈다. 특히 흡연과 무관한 폐암의 직접적 원인인 융합유전자를 생성하는 유전체 구조 변이의 특성을 집중적으로 규명했다.
유전체에 발생하는 구조적 변이는 DNA의 두 부위가 절단된 후 서로 연결되는 단순 구조 변이와 DNA가 많은 조각으로 동시에 파쇄된 후 복잡하게 서로 재조합되는 복잡 구조 변이로 나눌 수 있다.
복잡 구조 변이는 암세포에서 많이 발견된다. DNA의 수백 부위 이상이 동시에 절단된 후 상당 부분 소실되고 일부가 다시 연결되는 ‘염색체 산산조각(chromothripsis)’ 현상이 대표적 사례이다. 연구팀은 70% 이상의 융합유전자가‘유전체 산산조각 (chromothripsis)’ 현상 등 복잡 구조 돌연변이에 의해 생성됨을 확인했다.
또한, 연구팀은 정밀 유전체 분석을 통해 복잡 구조 돌연변이가 폐암이 진단되기 수십 년 전의 어린 나이에도 이미 발생할 수 있다는 사실을 발견했다.
세포의 유전체는 노화에 따라 비교적 일정한 속도로 점돌연변이가 쌓이는데 연구팀은 이를 이용하여 마치 지질학의 연대측정과 비슷한 원리로 특정 구조 변이의 발생 시점을 통계적으로 추정할 수 있는 기술을 개발했다. 이 기술을 통해 융합유전자 발생은 폐암을 진단받기 수십 년 전, 심지어는 10대 이전의 유년기에도 발생할 수 있다는 사실을 확인했다.
이는 암을 일으키는 융합유전자 돌연변이가 흡연과 큰 관련 없이 정상 세포에서 발생할 수 있음을 명확히 보여주는 사례이며, 단일 세포가 암 발생 돌연변이를 획득한 후에도 실제 암세포로 발현되기 위해서는 추가적인 요인들이 오랜 기간 누적될 필요가 있음을 뜻한다.
연구팀의 이번 연구는 흡연과 무관한 폐암 발생 과정에 대한 지식을 한 단계 확장했다는 의의가 있다. 향후 폐암의 예방, 선별검사 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
연구팀은 한국과학기술정보연구원의 슈퍼컴퓨터 5호기 누리온 시스템을 통해 유전체 빅데이터의 신속한 정밀 분석을 수행했다. 슈퍼컴퓨터 5호기는 향후 타 유전체 빅데이터 연구자들에게도 활용 가능할 것으로 보인다.
주영석 교수는 “암유전체 전장서열 빅데이터를 통해 폐암을 발생시키는 첫 돌연변이의 양상을 규명했으며, 정상 폐 세포에서 흡연과 무관하게 이들 복잡 구조변이를 일으키는 분자 기전의 이해가 다음 연구의 핵심이 될 것이다”라고 말했다.
서울대학교 의과대학 김영태 교수는 “2012년 폐 선암의 KIF5B-RET 융합유전자 최초 발견으로 시작된 본 폐암 연구팀이 융합유전자의 생성과정부터 임상적 의미까지 집대성했다는 것이 이번 연구의 중요한 성과이다”라고 말했다.
이번 연구는 한국연구재단, 보건복지부 포스트게놈 다부처유전체사업/세계선도의과학자 육성사업, 서경배 과학재단 및 서울대학교 의과대학 교실지정기부금의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 흡연과 무관한 폐암에서 융합유전자에 의한 발암기전
그림2. 폐선암에서 관찰되는 다양한 복잡 구조 변이의 특성
그림3. 어린 나이에 생긴 융합유전자의 예시
2019.06.03 조회수 25694 조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 24573
조광현 교수, 뇌의 제어구조 규명
〈 조광현 교수 연구팀 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 뇌 영역 간 복잡한 연결 네트워크에 내재된 뇌의 제어구조를 규명했다.
이번 연구를 통해 뇌의 동작 원리에 대한 이해를 높이고, 뇌의 제어구조 분석을 통해 뇌 질환 연구 및 치료에 응용될 수 있을 것으로 기대된다. 또한 4차 산업혁명의 핵심기술로 주목받는 IT와 BT의 융합연구인 시스템생물학을 통해 규명했다는 의의가 있다.
이병욱 박사, 강의룡, 장홍준 박사과정이 참여한 이번 연구는 셀(Cell) 출판사가 펴내는 융합과학 국제학술지 ‘아이사이언스(iScience)’ 3월 29일 자에 게재됐다.
뇌의 다양한 인지기능은 뇌 영역들 사이의 복잡한 연결을 통한 영역 간 상호작용으로 이뤄진다. 최근 뇌의 연결성에 대한 정보가 뇌의 동작 원리를 파악하는 핵심이라는 의견이 대두되면서 세계적으로 뇌 연결성을 파악하기 위한 커넥톰(Connectome) 연구가 활발히 이뤄지고 있다.
이를 통해 뇌 영역 사이의 구체적 연결성이 파악되고 있지만 복잡한 연결성에 내재된 뇌의 동작 원리에 대한 이해는 아직 매우 부족한 상황이다. 특히 뇌의 강건하면서 효율적 정보처리 능력의 기반이 되는 뇌의 숨겨진 제어구조는 파악된 내용이 없다.
조 교수 연구팀은 뇌의 제어구조 분석을 위해 ‘미국국립보건원(NIH) 휴먼 커넥톰 프로젝트(Human Connectome Project)’에서 제공하는 정상인의 뇌 영상 이미지 데이터를 활용해 뇌 영영 간 네트워크를 구축했다.
이후 연구팀은 그래프 이론의 최소지배집합(minimum dominating set) 개념을 활용해 뇌 영역 간 복잡한 연결 네트워크의 제어구조를 분석했다.
최소지배집합이란 네트워크의 각 노드(뇌의 각 영역)가 링크(뇌의 서로 다른 영역간의 연결)로 연결된 이웃 노드에 직접적 영향을 줘 기능을 제어할 수 있다고 가정할 때, 네트워크를 구성하는 모든 노드를 제어하는 데 필요한 최소한의 노드 집합을 말한다.
기존 여러 연구를 통해 다양한 생체 네트워크 및 통신망, 전력망 등의 복잡계 네트워크를 제어하는 데 있어서 최소지배집합이 핵심적인 역할을 한다는 것이 보고된 바 있다.
연구팀은 최소지배집합을 기반으로 ‘제어영역의 분포(distribution of control)’와 ‘제어영역의 중첩(overlap in control area)’이라는 두 가지 지표를 정의한 뒤 이를 기준으로 총 네 종류의 제어구조를 정의했다.
이후 연구팀은 브레인 네트워크를 비롯해 도로망, 통신망, 소셜 네트워크 등 실존하는 다양한 복잡계 네트워크가 어떤 제어구조를 갖는지 분석했다. 분석 결과 뇌는 다른 대부분 네트워크와는 달리 제어영역이 분산된 동시에 서로 중첩된 특이한 구조로 이뤄짐을 밝혀냈다.
뇌의 이러한 제어구조는 외부 섭동에 의한 네트워크의 높은 강건성을 유지하면서 동시에 여러 인지기능을 효율적으로 수행하기 위한 영역들의 상호 활성화를 다양하게 하기 위한 것임을 밝혔다.
IT와 BT가 융합된 시스템생물학 접근을 통한 브레인 네트워크의 구조분석은 인공지능의 발전에도 기여할 것으로 보인다. 브레인 네트워크의 진화적 설계원리에 대한 이해를 높인다면 컴퓨터 과학자들이 이를 이용해 새로운 인공지능 기술을 개발할 수 있다.
조 교수는 “지금껏 뇌의 제어구조가 밝혀진 바가 없었다”라며 “복잡한 연결성에 숨겨진 브레인 네트워크의 진화적 설계원리를 시스템생물학 연구를 통해 찾아냄으로써 뇌의 동작 원리를 파악할 수 있는 새로운 가능성을 제시했다”라고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 뇌의 제어구조 규명
그림2. 뇌 영역 간 네트워크 구축
2019.04.10 조회수 24573 조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
2017.12.07 조회수 25176
조광현 교수, 암세포 유형별 최적 약물표적 발굴기술 개발
〈 최민수 박사, 조광현 교수 〉
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 암세포의 유형에 따라 최적의 약물 표적을 찾는 기술을 개발했다.
이는 시스템생물학을 이용해 암세포의 유전자변이가 반영된 분자네트워크의 다이나믹스(동역학)를 분석해 약물의 반응을 예측하는 기술로 향후 암 관련 신약 개발에 크게 기여할 것으로 기대된다.
최민수, 시 주 (Shi Jue), 주 양팅 (Zhu Yanting), 양 루젠 (Yang Ruizhen)이 참여한 이번 연구는 ‘네이처 커뮤니케이션즈(Nature Communications)’ 12월 5일자 온라인 판에 게재됐다.
인간의 암세포는 유전자 돌연변이, 유전체 단위의 반복적 변이 등 여러 형태의 유전자 변이가 있다. 이러한 변이는 같은 암종에서도 암세포에 따라 많은 차이를 보이기 때문에 약물에 대한 반응도 다양하다.
암 연구자들은 암 환자에게서 빈번하게 발견되는 유전자변이를 파악하고 이 중 특정 약물의 지표로 사용될 수 있는 유전자변이를 찾기 위해 노력해 왔다. 이러한 연구는 단일 유전자변이의 발견 또는 유전자네트워크의 구조적 특징 분석에 초점이 맞춰져 있다.
하지만 이러한 접근 방법은 암세포 내 다양한 유전자 및 단백질의 상호작용에 의해 유발되는 암의 생물학적 특성과 이로 인한 약물반응의 차이를 설명하지 못하는 한계가 있다.
암세포의 유전자변이는 해당 유전자 기능 뿐 아니라 이 유전자와 상호작용하는 다른 유전자, 단백질에 영향을 미치기 때문에 결과적으로 분자네트워크의 다이나믹스(동역학) 특성에 변화를 일으킨다.
이로 인해 항암제에 대한 암세포의 반응이 변화하게 된다. 따라서 분자네트워크의 다이나믹스(동역학) 특성을 무시하고 소수의 암 관련 유전자를 표적으로 하는 현재의 치료법은 일부 환자에게만 유용하고 약물저항성을 갖는 대다수 환자에게는 효과적으로 적용되지 못한다.
조 교수 연구팀은 문제 해결을 위해 슈퍼컴퓨팅을 이용한 대규모 컴퓨터시뮬레이션과 세포 실험을 융합해 암세포 분자네트워크의 다이나믹스(동역학) 변화를 분석했다.
이를 통해 약물반응을 예측해 유형별 암세포의 최적 약물 표적을 발굴하는 기술을 개발했다. 이 기술은 대다수 암 발생에 관여하는 것으로 알려진 암 억제 유전자 p53의 분자조절네트워크에 시범적으로 적용됐다.
연구팀은 국제 컨소시엄인 암 세포주 백과사전(CCLE : The Cancer Cell Line Encyclopedia)에 공개된 대규모 암세포 유전체 데이터를 분자네트워크에 반영해 구축했으며 유전변이의 특성에 따라 서로 다른 분자네트워크를 생성했다.
각 분자네트워크에 대해 약물반응을 모사한 섭동분석을 수행해 약물반응을 나타내는 암세포의 변화를 정량화하고 군집화했다. 그 후 컴퓨터시뮬레이션 분석을 통해 효능, 조합에 따른 시너지효과 등 약물반응정도를 예측했다.
이러한 컴퓨터시뮬레이션 결과를 토대로 폐암, 유방암, 골종양, 피부암, 신장암, 난소암 등 다양한 암세포주를 대상으로 약물반응 실험을 수행해 비교 검증했다.
이 기술은 임의의 분자네트워크에 대해서 동일한 방식으로 적용할 수 있고 최적의 약물 표적을 발굴해 개인 맞춤치료에 활용가능하다.
연구팀은 암세포의 이질성에 따른 다양한 약물반응의 원인을 특정 유전자나 단백질뿐만 아니라 상호조절작용을 종합적으로 고려해 분석할 수 있게 됐다고 밝혔다.
또한 약물저항성의 원인을 사전에 예측하고 이를 억제할 수 있는 최적의 약물 표적을 발굴할 수 있게 됐고 기존 약물의 새로운 적용대상을 찾는 약물재창출에 활용될 수 있는 핵심 원천기술을 확보하게 됐다고 말했다.
조 교수는 “암세포별 유전변이는 약물반응 다양성의 원인이지만 지금까지 이에 대한 총체적 분석이 이뤄지지 못했다”며 “시스템생물학을 통해 암세포 유형별 분자네트워크의 약물반응을 시뮬레이션으로 분석해 약물 반응의 근본적 원리를 파악하고 새로운 개념의 최적 약물 타겟을 발굴할 수 있게 됐다”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 바이오의료기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 컴퓨터시뮬레이션을 통한 암세포 유형별 약물반응 예측 및 세포실험 비교 검증
그림2. 암세포별 분자네트워크의 동역학 분석에 기반한 약물반응 예측 및 군집화
그림3. 세포 분자네트워크 분석에 따른 암세포 유형별 약물타겟 발굴 및 암환자별 맞춤치료 전략 수립
2017.12.07 조회수 25176 이현주 교수, 백금 사용량 10분의1로 줄인 단일원자 촉매 개발
〈 이 현 주 교수, 김 지 환 학생 〉
우리 대학 생명화학공학과 이현주 교수와 서울시립대 한정우 교수 공동 연구팀이 기존 촉매의 백금 사용량을 10분의 1로 줄일 수 있는 백금 단일원자 촉매를 개발했다.
이는 매우 안정적인 고함량의 백금 단일원자 촉매로 연구팀은 ‘직접 포름산 연료전지(Direct formic acid fuel cells)’에 적용하는 데 성공했다.
김지환 학생이 1저자로 참여한 이번 연구 결과는 재료 과학분야의 국제 학술지 ‘어드밴스드 에너지 머티리얼즈(Advanced Energy Materials)’ 9월 11일자 온라인 판에 게재됐다.
백금 기반의 축매는 활성과 안정성이 높아 다양한 촉매 반응에 적용되지만 가격이 비싸고 희귀하기 때문에 백금의 사용량을 최대한 줄이는 것이 중요하다.
그 중 단일원자 촉매는 백금 입자 크기를 원자 단위로 줄여 모든 원자가 반응에 참여하기 때문에 백금 촉매의 가격을 획기적으로 낮출 수 있다. 또한 두 개 이상의 원자들이 붙어 있는 앙상블 자리(ensemble site)가 없기 때문에 원하는 생성물을 선택적으로 얻을 수 있다.
이러한 장점에도 불구하고 단일원자 촉매는 낮은 배위수(coordination number)와 높은 표면자유에너지로 인해 쉽게 뭉치고 안정성이 떨어져 실제 장치에 적용이 어렵다는 한계를 갖는다.
연구팀은 백금 단일원자 촉매의 안정성을 높이기 위해 금속 원소인 안티몬이 첨가된 주석 산화물(Antimony-doped tin oxide, ATO) 위에 백금 단일원자가 주석과의 합금 형태로 존재하는 구조를 개발했다.
연구팀은 이러한 구조가 백금 단일원자가 안티몬-주석 합금 구조에서 안티몬의 자리를 대신해 열역학적으로 안정적인 형태로 존재함을 계산을 통해 증명했다.
연구팀이 개발한 촉매는 포름산 산화반응에서 일반적으로 사용되는 촉매인 상용백금촉매(Pt/C)보다 최대 50배 높은 활성을 보였고 장기안정성 또한 월등하게 높았다.
또한 연구팀은 이 촉매를 막과 전극으로 구성된 직접 포름산 연료전지에 적용했다. 단일원자 촉매를 완전지 형태의 연료전지에 적용한 것은 최초의 시도로, 기존 촉매에 비해 10분의 1 정도만의 백금을 사용해도 비슷한 출력을 얻을 수 있다.
이현주 교수는 “귀금속 단일원자 촉매의 가장 큰 문제점인 낮은 함량과 낮은 안정성을 높일 수 있었고 최초로 직접 포름산 연료전지에 적용했다”며 “연료전지에 적용 가능한 고함량 및 고안정성 귀금속 단일원자 촉매의 개발에 기여할 수 있을 것이다”고 말했다.
이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 백금 단일 원자 촉매의 개념도
그림2. 관찰한 촉매 및 백금 단일 원자 (흰색 원으로 표시된 밝은 점)
2017.10.24 조회수 21753
이현주 교수, 백금 사용량 10분의1로 줄인 단일원자 촉매 개발
〈 이 현 주 교수, 김 지 환 학생 〉
우리 대학 생명화학공학과 이현주 교수와 서울시립대 한정우 교수 공동 연구팀이 기존 촉매의 백금 사용량을 10분의 1로 줄일 수 있는 백금 단일원자 촉매를 개발했다.
이는 매우 안정적인 고함량의 백금 단일원자 촉매로 연구팀은 ‘직접 포름산 연료전지(Direct formic acid fuel cells)’에 적용하는 데 성공했다.
김지환 학생이 1저자로 참여한 이번 연구 결과는 재료 과학분야의 국제 학술지 ‘어드밴스드 에너지 머티리얼즈(Advanced Energy Materials)’ 9월 11일자 온라인 판에 게재됐다.
백금 기반의 축매는 활성과 안정성이 높아 다양한 촉매 반응에 적용되지만 가격이 비싸고 희귀하기 때문에 백금의 사용량을 최대한 줄이는 것이 중요하다.
그 중 단일원자 촉매는 백금 입자 크기를 원자 단위로 줄여 모든 원자가 반응에 참여하기 때문에 백금 촉매의 가격을 획기적으로 낮출 수 있다. 또한 두 개 이상의 원자들이 붙어 있는 앙상블 자리(ensemble site)가 없기 때문에 원하는 생성물을 선택적으로 얻을 수 있다.
이러한 장점에도 불구하고 단일원자 촉매는 낮은 배위수(coordination number)와 높은 표면자유에너지로 인해 쉽게 뭉치고 안정성이 떨어져 실제 장치에 적용이 어렵다는 한계를 갖는다.
연구팀은 백금 단일원자 촉매의 안정성을 높이기 위해 금속 원소인 안티몬이 첨가된 주석 산화물(Antimony-doped tin oxide, ATO) 위에 백금 단일원자가 주석과의 합금 형태로 존재하는 구조를 개발했다.
연구팀은 이러한 구조가 백금 단일원자가 안티몬-주석 합금 구조에서 안티몬의 자리를 대신해 열역학적으로 안정적인 형태로 존재함을 계산을 통해 증명했다.
연구팀이 개발한 촉매는 포름산 산화반응에서 일반적으로 사용되는 촉매인 상용백금촉매(Pt/C)보다 최대 50배 높은 활성을 보였고 장기안정성 또한 월등하게 높았다.
또한 연구팀은 이 촉매를 막과 전극으로 구성된 직접 포름산 연료전지에 적용했다. 단일원자 촉매를 완전지 형태의 연료전지에 적용한 것은 최초의 시도로, 기존 촉매에 비해 10분의 1 정도만의 백금을 사용해도 비슷한 출력을 얻을 수 있다.
이현주 교수는 “귀금속 단일원자 촉매의 가장 큰 문제점인 낮은 함량과 낮은 안정성을 높일 수 있었고 최초로 직접 포름산 연료전지에 적용했다”며 “연료전지에 적용 가능한 고함량 및 고안정성 귀금속 단일원자 촉매의 개발에 기여할 수 있을 것이다”고 말했다.
이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 백금 단일 원자 촉매의 개념도
그림2. 관찰한 촉매 및 백금 단일 원자 (흰색 원으로 표시된 밝은 점)
2017.10.24 조회수 21753 김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 22009
김호민 교수, 패혈증 원인 물질의 생체 내 메커니즘 최초 발견
우리 대학 의과학대학원 김호민 교수와 연세대학교 윤태영 교수 공동 연구팀이 우리 몸이 패혈증의 원인 물질인 박테리아 내독소를 어떻게 받아들이고 전달하는지 규명했다.
이를 통해 박테리아 내독소가 생체 내 단백질로 전달되는 분자 원리를 밝혀냄으로써 내독소가 전달되는 길목을 차단해 패혈증을 치료할 수 있는 새로운 가능성이 제시됐다.
패혈증은 감염에 의해서 과도하게 활성화된 면역반응에 따른 전신성 염증반응 증후군이다.
이 연구는 면역학 분야 국제 학술지이며, 셀(Cell) 자매지인‘이뮤니티 (Immunity)’12월 13일자에 게재되었다.
그람 음성균 세포외막에 존재하는 내독소는 생체 내 단백질을 통해 면역세포 표면의 세포수용체로 전달돼 선천성 면역 반응을 활성화시킨다.
감염에 의한 혈액 내 내독소 다량 유입은 고열, 혈압저하, 장기손상 등 과도한 염증반응의 결과인 패혈증으로 이어질 수 있지만, 내독소 인식 및 전달 관련 구체적인 분자 원리가 밝혀져 있지 않아 패혈증 치료제 개발에 한계가 있었다.
연구팀은 문제 해결을 위해 단분자 형광기법과 바이오 투과전자현미경을 활용했다. 마이셀(Micelle) 형태로 존재하는 내독소 표면에 막대 모양의 LBP가 결합하여 내독소를 인식하고, 여기에 CD14가 빠르게 결합해 내독소 한 분자를 가져간 후 면역세포 수용체인 TLR4-MD2와의 상호결합을 통해 건네주는 내독소 인식 및 전달 원리를 확인했다.
박테리아 내독소와 정제된 LBP 단백질을 혼합해 바이오투과전자현미경으로 사진을 찍은 후 각각의 분자의 모양을 컴퓨터를 활용한 이미지 프로세싱을 통해 분석함으로써 내독소와 결합한 LBP 단백질 구조를 최초로 규명했다.
특히 막대모양의 LBP 단백질이 그들의 N-도메인 끝을 통해 내독소 마이셀 표면에 결합함으로써 박테리아 내독소만을 특이적으로 인식하는 것을 발견했다.
연구팀은 박테리아 내독소에 형광을 부착시킨 후 내독소 항체를 활용해 유리슬라이드 표면에 코팅시키고, LBP, CD14, TLR4-MD2 단백질들을 흘려주면서 박테리아 내독소, LBP, CD14, TLR4-MD2 분자 하나하나의 동적인 움직임을 실시간으로 관찰하는 단분자 형광 시스템을 최초로 구축했다.
이를 통해 박테리아 내독소 표면에 결합한 LBP 단백질로부터 CD14 단백질이 내독소 한 분자만을 반복적으로 가져간 후 빠르게 TLR4-MD2로 전달함으로써 선천성 면역의 세포신호전달을 활성화 시키는 분자메커니즘을 최초로 규명했다.
또한 마우스 면역세포인 수지상세포를 활용하여 첨단 생물물리학적인 기법을 통해 제시한 분자메커니즘이 생체 내에서 내독소를 인식하여 면역반응을 유발하는 핵심 메커니즘을 검증했다.
기존의 실험방법으로 접근이 어려웠던 LBP, CD14, TLR4-MD2 단백질들 간의 동적인 상호작용을 최신 첨단 실험기법을 통하여 분자수준에서 규명함으로써 생체 내 내독소 인식 및 전달메커니즘을 규명했다.
연구 방법 및 결과는 박테리아 감염에 의한 선천성 면역 연구에 새로운 방향을 제시할 것이며 특히 이 연구에서 규명한 분자적, 구조적 지식들은 패혈증 발병메커니즘 연구 및 치료제 개발에 적극 활용될 수 있을 것으로 기대된다.
김호민 교수는“박테리아 내독소가 생체 내 단백질들의 동적인 상호작용에 의해 면역세포로 전달되는 일련의 과정들을 분자수준에서 최초로 밝힌 것이다”며 “박테리아 내독소 인식 및 전달메커니즘 이해를 통하여 선천성 면역 유발 메커니즘 이해뿐만 아니라 패혈증 예방 및 치료제 개발에 기여할 것으로 기대된다”라고 말했다.
이번 연구는 미래창조과학부, 한국연구재단 기초연구사업(개인연구, 집단연구), IBS 나노의학연구단의 지원으로 수행됐다.
□ 그림 설명
그림1. 생체 내 박테리아 내독소 전달 메커니즘
2016.12.27 조회수 22009 최광욱 교수, 기관의 크기를 조절하는 유전자 발견
〈최 광 욱 교수〉
우리 대학 생명과학과 최광욱 교수 연구팀이 돌연변이 유전자의 세포분열이 증가하고 기관이 비정상적으로 커지는 현상의 원인을 밝혔다.
연구팀은 우리 몸의 각 기관이 정상적인 크기로 자라게 하는 히포네트워크(Hippo Network) 내에서 쉽원(Schip1)이라는 새로운 단백질을 발견하고 기능 원리를 규명했다.
이번 연구는 셀(Cell) 자매지인 ‘디벨롭멘탈 셀(Developmental Cell) 7일자 온라인 판에 게재됐다. (논문명: Drospohila Schip1 links Expanded to Tao-1 to regulate Hippo signaling)
생명체에는 각 기관들이 적절한 크기가 되도록 스스로 조절하는 능력이 있다. 이것을 가능하게 만드는 각 요소들은 서로 네트워크를 이뤄 작동하고, 그 네트워크를 히포 네트워크라 부른다.
이 히포네트워크에 유전적 혹은 후천적으로 문제가 발생하면 조절능력을 상실해 기관에서 종양을 만들게 되고 생명을 위협하는 요소가 된다. 따라서 네트워크를 구성하는 요소를 밝히고 완성시키는 것은 불확실한 종양의 발생원인 규명에 필수적이다.
과학계는 지속적 연구를 통해 히포네트워크의 구성요소들과 기능 및 역할을 발견했다. 하지만 이 네트워크에서 중심적으로 작동하는 두 요소인 ‘타오 원(Tao-1)’과 ‘익스팬디드(Expanded)’ 사이의 기작은 밝혀지지 않았다.
익스팬디드와 타오원이 네트워크 내에서 관련이 있다는 점은 밝혀졌지만 어떤 방식으로 연결됐는지, 직접적인 연관은 무엇인지에 대한 부분은 밝혀내야 할 숙제로 남아 있었다.
연구팀은 문제 해결을 위해 히포 네트워크 유전자가 처음 발견된 초파리를 이용했다. 히포 네트워크는 초파리부터 인간까지 거의 동일한 유전자에 의해 조절되고 있기 때문이다.
연구팀은 초파리 히포네트워크 내 쉽원(Schip1) 요소가 익스팬디드와 타오원 사이의 매개체라는 사실을 규명했다. 쉽원은 타오원을 세포막으로 끌어들이는 역할을 하고 익스팬디드는 쉽원이 적절한 위치를 잡게 해 준다.
이 쉽원 유전자에 돌연변이가 생길 경우 세포분열이 크게 증가하고 결과적으로 기관의 크기가 비정상적으로 커지는 등 암 조직에서 나타나는 여러 형질이 발생한다.
연구팀은 쉽원 유전자가 초파리 뿐 아니라 인체에도 잘 보존돼 있기 때문에 종양의 원인 규명 및 치료법 개발에도 중요한 역할을 할 것이라고 밝혔다. 향후 고등 생명체를 이용한 추가적 연구가 진행될 것으로 기대된다.
최 교수는 “지금까지 단절됐던 상류와 하류 요소를 이어주는 중요한 고리를 찾았다”며 “이는 매우 의미있는 발견이다”고 말했다.
정형록 박사과정이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
□ 그림 설명
그림1. 쉽원이 없을 때 초파리 눈 크기 변화
그림2. 이전의 완성되지 않았던 히포네트워크와 현재 본 논문을 통해 완성된 히포 네트워크
그림3. 쉽원 돌연변이에서 히포의 양이 급격하게 늘어나는 모습
2016.03.18 조회수 15199
최광욱 교수, 기관의 크기를 조절하는 유전자 발견
〈최 광 욱 교수〉
우리 대학 생명과학과 최광욱 교수 연구팀이 돌연변이 유전자의 세포분열이 증가하고 기관이 비정상적으로 커지는 현상의 원인을 밝혔다.
연구팀은 우리 몸의 각 기관이 정상적인 크기로 자라게 하는 히포네트워크(Hippo Network) 내에서 쉽원(Schip1)이라는 새로운 단백질을 발견하고 기능 원리를 규명했다.
이번 연구는 셀(Cell) 자매지인 ‘디벨롭멘탈 셀(Developmental Cell) 7일자 온라인 판에 게재됐다. (논문명: Drospohila Schip1 links Expanded to Tao-1 to regulate Hippo signaling)
생명체에는 각 기관들이 적절한 크기가 되도록 스스로 조절하는 능력이 있다. 이것을 가능하게 만드는 각 요소들은 서로 네트워크를 이뤄 작동하고, 그 네트워크를 히포 네트워크라 부른다.
이 히포네트워크에 유전적 혹은 후천적으로 문제가 발생하면 조절능력을 상실해 기관에서 종양을 만들게 되고 생명을 위협하는 요소가 된다. 따라서 네트워크를 구성하는 요소를 밝히고 완성시키는 것은 불확실한 종양의 발생원인 규명에 필수적이다.
과학계는 지속적 연구를 통해 히포네트워크의 구성요소들과 기능 및 역할을 발견했다. 하지만 이 네트워크에서 중심적으로 작동하는 두 요소인 ‘타오 원(Tao-1)’과 ‘익스팬디드(Expanded)’ 사이의 기작은 밝혀지지 않았다.
익스팬디드와 타오원이 네트워크 내에서 관련이 있다는 점은 밝혀졌지만 어떤 방식으로 연결됐는지, 직접적인 연관은 무엇인지에 대한 부분은 밝혀내야 할 숙제로 남아 있었다.
연구팀은 문제 해결을 위해 히포 네트워크 유전자가 처음 발견된 초파리를 이용했다. 히포 네트워크는 초파리부터 인간까지 거의 동일한 유전자에 의해 조절되고 있기 때문이다.
연구팀은 초파리 히포네트워크 내 쉽원(Schip1) 요소가 익스팬디드와 타오원 사이의 매개체라는 사실을 규명했다. 쉽원은 타오원을 세포막으로 끌어들이는 역할을 하고 익스팬디드는 쉽원이 적절한 위치를 잡게 해 준다.
이 쉽원 유전자에 돌연변이가 생길 경우 세포분열이 크게 증가하고 결과적으로 기관의 크기가 비정상적으로 커지는 등 암 조직에서 나타나는 여러 형질이 발생한다.
연구팀은 쉽원 유전자가 초파리 뿐 아니라 인체에도 잘 보존돼 있기 때문에 종양의 원인 규명 및 치료법 개발에도 중요한 역할을 할 것이라고 밝혔다. 향후 고등 생명체를 이용한 추가적 연구가 진행될 것으로 기대된다.
최 교수는 “지금까지 단절됐던 상류와 하류 요소를 이어주는 중요한 고리를 찾았다”며 “이는 매우 의미있는 발견이다”고 말했다.
정형록 박사과정이 주도한 이번 연구는 교육부와 한국연구재단이 추진하는 중견연구자지원사업과 글로벌 연구실지원사업의 일환으로 수행됐다.
□ 그림 설명
그림1. 쉽원이 없을 때 초파리 눈 크기 변화
그림2. 이전의 완성되지 않았던 히포네트워크와 현재 본 논문을 통해 완성된 히포 네트워크
그림3. 쉽원 돌연변이에서 히포의 양이 급격하게 늘어나는 모습
2016.03.18 조회수 15199 연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
2012.07.24 조회수 22821
연성물질의 메조포러스 준결정 개발・분석 성공
오사무 테라사키 교수
- 네이처(Nature)지 7월 19일자 실려 -
메조포러스(mesoporous) 준결정(quaicrystal) 구조에 대한 의문이 우리 대학 연구진에 의해 보다 명확하게 풀렸다.
우리 학교 EEWS(책임교수 강정구) 대학원 소속 오사무 테라사키(Osamu Terasaki) 교수 연구팀이 불규칙적인 입자구조를 가지고 있는 준결정 메조포러스 실리카(quasicrystalline mesoporous silica) 합성에 성공하고 준결정 성장 과정을 분석하는 새로운 방법을 개발했다.
연구팀이 제시한 이론은 연성물질인 교질(micelles) 입자 형성 시 불규칙하게 나타나는 준결정 현상을 과학적으로 규명하는 토대를 만들었다. 세계적인 학술지 ‘네이처(Nature)’는 7월호(19일자)에 테라사키(Terasaki) 교수 연구팀의 논문을 게재했다.
과학자들은 그 동안 연성물질(solidified version of soft matter systems)에서 발견되는 메조포러스 준결정 구조를 체계적으로 설명하는데 많은 어려움을 겪어왔다. 하지만, 이번 연구를 통해 얻은 연성물질 내 준결정 성장에 대한 이론적인 근거는 앞으로 이 분야에 대한 연구를 촉진시켜 나노 구조를 가진 신소재 물질 개발에 박차를 가할 것으로 예측된다.
연성물질의 메조포러스 준결정은 높은 대칭균형(high symmetry)과 나노 스케일(nano scale)보다 더 큰 특성적 크기(large characteristic length scale)를 가지고 있어 광학적 특성을 자유자재로 조절할 수 있는 물질을 구현할 수 있다.
이를 활용하면 태양광을 사용하는 친환경적 에너지 저장 및 변환 기술 개발에 응용되어 지속가능한 에너지의 저장, 사용 및 재생산 기술 발전에 큰 도움을 줄 것으로 예상된다.
테라사키 교수 연구팀은 메조포러스 준결정 실리카 합성에 성공하고 투과전자현미경(Transmission Electron Microscopy)을 통해 실리카 입자 중앙에 12각형 기둥 모양의 순결정이 형성되어 있으며, 전자회절 무늬에서(electron diffraction pattern) 12각형의 회전대칭 무늬(rotational symmetry)가 순결정 주위에 형성되는 것을 증명하였다.
준결정(quasicrystal)은 준주기적 결정(quasiperiodic crystal)의 줄임말로서 금속 같은 일정한 규칙으로 배열된 결정 물질과 유리와 같은 비결정 물질의 중간 성질을 가지는 제 3의 고체(solid)로 최근 발견되었으며 2011년에는 노벨화학상이 이 분야 연구에 수여되기도 했다.
많은 양의 기공(porous)을 지닌 다공성 물질을 준결정으로 제조 하게 되면 기공들의 결정 구조를 ‘타일을 붙이듯(tiling)’ 원하는 방식대로 디자인 하고 성질을 조절하게 되어 다양한 분야에 필요한 새로운 소재를 개발하고 생산할 수 있게 된다.
테라사키 교수는 “높은 대칭성(high symmetry)을 가지는 준결정의 발견은 물질의 광학적 성질을 쉽게 조절해 가시광 영역대의 포토닉 크리스탈을 구현할 수 있다”며 “물질의 광학적 에너지 흡수를 조절 할 수 있는 이 기술은 향후 에너지 저장(energy harvesting)의 핵심기술이 될 수도 있을 것이다”라고 말했다.
이번 연구는 KAIST EEWS 대학원의 오사무 테라사키 교수와 스웨덴 스톡홀름(Stockholm University) 대학과 공동으로 수행되었다.(끝)
그림 1. 물질에서의 원자 배열 방법에 따라 구분되는 결정, 준결정과 비결정을 나타낸 모식도. 일반적으로는 원자가 일정한 패턴을 가지고 배열되어 있는 것을 결정, 그렇지 않은 것을 비결정이라고 하였으나, 준결정은 결정에서의 원자배열을 가지지는 않지만 정돈 되어 있는 구조이다. 투과전자현미경에서의 회절무늬를 보고 준결정을 판단할 수 있다.
그림 2. 메조포러스 실리카 준결정의 실제 모양과 원자 배열을 나타내는 투과전자현미경 이미지. 투과전자현미경으로부터 메조포러스 실리카가 12각형 기둥 모양을 하고 있음을 알 수 있으며(왼쪽 위의 이미지), 이는 투과전자현미경의 회절무늬에서도 나타난다(왼쪽 아래 이미지). 고배율의 투과전자현미경은 메조포러스 실리카의 실제 구조를 나타내고 있다(오른쪽).
그림 3. 메조포러스 실리카 준결정의 결정구조를 3차원 모델로 나타낸 모식도. 각각 다른 세 가지 다각형이 서로 정돈되어 결합해 메조포러스 준결정을 구성한다.
2012.07.24 조회수 22821 단백질 분해조절 효소 정보 담은 바이오마커 발굴 시스템 개발
- Mol Cell Proteomics지 게재, “바이오마커 개발의 새로운 패러다임 제시” -
단백질의 분해를 조절하는 효소와 기질에 대한 관계정보를 담은 바이오마커* 발굴 시스템(E3Net)이 국내 연구진에 의해 개발되어, 고부가가치의 새로운 바이오마커 개발에 가능성이 열렸다.
※ 바이오마커(Biomarker) : 유전자, 단백질 등에서 유래된 특이한 패턴의 분자적 정보로, 유전적․후천적 영향으로 발생한 신체의 변화를 감지할 수 있는 생물표지인자
우리학교 바이오및뇍 이관수 교수(49세)가 주도하고, 한영웅 박사과정생, 이호동 박사 및 박종철 교수가 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 선도연구센터지원사업(NCRC), 신기술융합형성장동력사업 및 교육과학기술부의 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원으로 수행되었고, 단백질체 연구 분야의 권위 있는 학술지인 ‘Molecular and Cellular Proteomics"지 4월호(4월 1일자)에 게재되었다. (논문명: A system for exploring E3-mediated regulatory networks of cellular functions)이관수 교수 연구팀은 전 세계 바이오 관련 DB(데이터베이스)와 논문(약 2만 편)으로부터 정보를 추출해 단백질 분해를 조절하는 효소(E3 효소)와 기질*들 간의 네트워크를 집대성하여, 이와 관련된 세포의 기능과 질병을 분석하는 ‘E3Net’ 시스템을 개발하였다.
※ 기질(substrate) : 효소와 특이적으로 결합하여 화학반응을 일으키는 분자로, 소화작용은 우리의 몸속에서 일어나는 효소와 기질간의 반응의 대표적인 사례
세포는 시시각각 변하는 환경에 대응하여 필요한 단백질들을 생산, 폐기 및 재활용하는 정교한 시스템을 가지고 있는데, 만일 이 과정에서 오류가 생기면 ‘질병’으로 이어질 수 있다.
따라서 단백질 분해를 조절하는 E3 효소와 기질 간의 관계를 파악하면 관련 질병을 치료하거나 예방할 수 있게 된다. 특히 E3 효소는 단백질 분해의 80%를 담당하는 것으로 알려져 수많은 질병이 관련되어 있을 것으로 예측되고 있다.
그러나 E3 효소와 기질 간의 정보들이 개별 논문과 DB에 흩어져 있어, 단백질 분해 조절과 관련된 세포의 기능과 질병의 특성을 종합적․체계적으로 분석할 수 없었다.
이 교수팀은 모든 E3 효소(2,201개)와 기질(4,896개) 및 그 조절관계(1,671개)에 대한 정보를 통합하여 E3 효소 조절 네트워크 내에 존재하는 관련된 세포의 기능과 질병을 시스템적으로 분석할 수 있는 E3Net을 구축하는데 성공하였다.
이 네트워크는 지금까지 구축된 조절정보를 모두 합친 것보다 무려 10배에 이르는 방대한 양으로, E3 효소가 독자적으로 또는 협력해서 조절하는 세포의 기능과 관련 질병을 정확히 파악할 수 있는 토대가 마련된 첫 사례로서 의미가 크다.
연구팀은 E3Net을 이용하면 각각의 질병과 관련된 단백질들의 분해조절을 담당하는 E3 효소들을 찾을 수 있고, 분해조절 원리와 세포기능 네트워크를 함께 파악하여 질병의 발생 원인이나 환자에 적합한 맞춤형 치료방법을 제공할 수 있는 바이오마커를 발굴할 수 있을 것으로 기대한다.
실제 연구팀은 E3Net을 활용해 암, 뇌심혈관 질환 및 당뇨병 등 현대인의 대표적 질환과 관련된 E3 바이오마커 후보 수십 개를 새롭게 발견하는 등 눈에 띄는 성과를 거두었고, 현재 이를 검증할 후속 연구를 계획하고 있다. 이관수 교수는 “이번 연구결과로 E3 효소와 관련된 단백질 분해조절의 네트워크가 구축되고, 이 네트워크에 존재하는 세포의 기능과 질병의 특이성을 시스템적으로 분석할 수 있게 됨에 따라, E3 효소와 관련된 세포의 기능 연구와 질병 연구에 새로운 전기가 마련되었다”고 연구의의를 밝혔다.
2012.05.01 조회수 25923
단백질 분해조절 효소 정보 담은 바이오마커 발굴 시스템 개발
- Mol Cell Proteomics지 게재, “바이오마커 개발의 새로운 패러다임 제시” -
단백질의 분해를 조절하는 효소와 기질에 대한 관계정보를 담은 바이오마커* 발굴 시스템(E3Net)이 국내 연구진에 의해 개발되어, 고부가가치의 새로운 바이오마커 개발에 가능성이 열렸다.
※ 바이오마커(Biomarker) : 유전자, 단백질 등에서 유래된 특이한 패턴의 분자적 정보로, 유전적․후천적 영향으로 발생한 신체의 변화를 감지할 수 있는 생물표지인자
우리학교 바이오및뇍 이관수 교수(49세)가 주도하고, 한영웅 박사과정생, 이호동 박사 및 박종철 교수가 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 선도연구센터지원사업(NCRC), 신기술융합형성장동력사업 및 교육과학기술부의 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원으로 수행되었고, 단백질체 연구 분야의 권위 있는 학술지인 ‘Molecular and Cellular Proteomics"지 4월호(4월 1일자)에 게재되었다. (논문명: A system for exploring E3-mediated regulatory networks of cellular functions)이관수 교수 연구팀은 전 세계 바이오 관련 DB(데이터베이스)와 논문(약 2만 편)으로부터 정보를 추출해 단백질 분해를 조절하는 효소(E3 효소)와 기질*들 간의 네트워크를 집대성하여, 이와 관련된 세포의 기능과 질병을 분석하는 ‘E3Net’ 시스템을 개발하였다.
※ 기질(substrate) : 효소와 특이적으로 결합하여 화학반응을 일으키는 분자로, 소화작용은 우리의 몸속에서 일어나는 효소와 기질간의 반응의 대표적인 사례
세포는 시시각각 변하는 환경에 대응하여 필요한 단백질들을 생산, 폐기 및 재활용하는 정교한 시스템을 가지고 있는데, 만일 이 과정에서 오류가 생기면 ‘질병’으로 이어질 수 있다.
따라서 단백질 분해를 조절하는 E3 효소와 기질 간의 관계를 파악하면 관련 질병을 치료하거나 예방할 수 있게 된다. 특히 E3 효소는 단백질 분해의 80%를 담당하는 것으로 알려져 수많은 질병이 관련되어 있을 것으로 예측되고 있다.
그러나 E3 효소와 기질 간의 정보들이 개별 논문과 DB에 흩어져 있어, 단백질 분해 조절과 관련된 세포의 기능과 질병의 특성을 종합적․체계적으로 분석할 수 없었다.
이 교수팀은 모든 E3 효소(2,201개)와 기질(4,896개) 및 그 조절관계(1,671개)에 대한 정보를 통합하여 E3 효소 조절 네트워크 내에 존재하는 관련된 세포의 기능과 질병을 시스템적으로 분석할 수 있는 E3Net을 구축하는데 성공하였다.
이 네트워크는 지금까지 구축된 조절정보를 모두 합친 것보다 무려 10배에 이르는 방대한 양으로, E3 효소가 독자적으로 또는 협력해서 조절하는 세포의 기능과 관련 질병을 정확히 파악할 수 있는 토대가 마련된 첫 사례로서 의미가 크다.
연구팀은 E3Net을 이용하면 각각의 질병과 관련된 단백질들의 분해조절을 담당하는 E3 효소들을 찾을 수 있고, 분해조절 원리와 세포기능 네트워크를 함께 파악하여 질병의 발생 원인이나 환자에 적합한 맞춤형 치료방법을 제공할 수 있는 바이오마커를 발굴할 수 있을 것으로 기대한다.
실제 연구팀은 E3Net을 활용해 암, 뇌심혈관 질환 및 당뇨병 등 현대인의 대표적 질환과 관련된 E3 바이오마커 후보 수십 개를 새롭게 발견하는 등 눈에 띄는 성과를 거두었고, 현재 이를 검증할 후속 연구를 계획하고 있다. 이관수 교수는 “이번 연구결과로 E3 효소와 관련된 단백질 분해조절의 네트워크가 구축되고, 이 네트워크에 존재하는 세포의 기능과 질병의 특이성을 시스템적으로 분석할 수 있게 됨에 따라, E3 효소와 관련된 세포의 기능 연구와 질병 연구에 새로운 전기가 마련되었다”고 연구의의를 밝혔다.
2012.05.01 조회수 25923 매미와 개구리는 지휘자없이 어떻게 합창할까
나무위의 매미와 논두렁의 개구리는 지휘자 없이 어떻게 합창할까? 이와 관련해서, KAIST 바이오 및 뇌공학과의 조광현 교수는 생명체의 동기화된 주기적 진동신호의 생성원리를 최근 규명했다. 나무에 붙어있는 많은 반딧불들의 동시다발적인 깜빡임, 매미들의 조율된 울음소리, 뇌신경세포들간의 전기신호, 세포내 분자들의 농도변화에 이르기까지 생명체는 다양한 형태의 주기적 진동신호 교환을 통해 정보를 전달하는데, 이들은 놀랍게도 정확히 동일한 위상(phase)으로 동기화되곤 한다. 이는 마치 오케스트라에서 지휘자 없이도 모든 연주가 일정한 박자에 맞춰 이루어지는 것과 같다.
어떻게 생명체의 여러 주기적 진동신호들이 그러한 동기화를 이루는가?
우리학교 바이오및뇌공학과 조광현(曺光鉉) 교수 연구팀이 대규모 가상세포(virtual cell)실험을 통해 생명체의 다양한 주기적 진동(oscillation)신호들이 동기화(synchronization)되는 보편적인 원리를 규명했다.
曺교수팀은 이번 연구를 통해 여러 독립적인 주기적 진동신호들은 양성피드백(positive feedback)을 통해 서로의 위상에 영향을 줘 하나의 동일한 위상으로 수렴되는 현상을 밝혀냈다.
특히 양성피드백은 이중활성(double activation) 또는 이중억제(double inhibition)의 구조로 구현된다. 이중활성피드백은 연결시간지연이 짧을 때, 이중억제피드백은 연결시간지연이 길 때 보다 안정적인 신호동기화를 가능하게 했다.
또한, 노이즈(noise) 교란이 있을 때 이중활성피드백은 진동신호의 주기보다 진폭을 안정적으로 유지하는 반면 이중억제피드백은 연결강도에 불규칙한 변화가 주어졌을 때 일정한 주기와 진폭을 유지시켜줬다. 현존하는 대부분의 현상들이 이러한 원칙을 따르고 있었다.
이번에 규명된 원리는 생체내 주기적 진동신호의 동기화가 교란될 때 발생하는 뇌질환 등 여러 질병의 원인을 새롭게 조명하는 계기를 마련할 것으로 기대된다.
이번 연구는 기존 생명과학의 난제에 대해 IT융합기술인 시스템생물학(Systems Biology) 연구를 통해 해답을 제시할 수 있음을 보여줬으며, 향후 생명과학 연구에 있어서 가상세포실험의 무한한 가능성을 제시했다.
曺교수는 “생명체는 복잡하게 얽혀있는 것으로 보이는 네트워크속에 이와 같이 정교한 진화적 설계원리를 간직하고 있었다”며 “이러한 규칙들은 임의로 수많은 디지털 진동자들을 만들어 인공진화를 통해 신호의 동기화 현상을 관측하였을 때에도 마찬가지로 성립된다는 흥미로운 사실을 확인했다”고 말했다.
이 연구는 교육과학기술부가 지원하는 한국연구재단 연구사업의 일환으로 수행되었으며, 연구결과는 세포생물학 분야 권위지인 세포과학저널(Journal of Cell Science) 2010년 1월 26일자 온라인판에 게재됐다.
세포생물학 실험결과만을 출판하는 이 저널에 순수 컴퓨터시뮬레이션만으로 수행된 가상세포실험 연구결과가 게재된 것은 매우 이례적인 일이다.
인터넷주소: http://jcs.biologists.org/cgi/content/abstract/jcs.060061v1
<용어설명>◯ 양성피드백(positive feedback): 서로 연결되어 있는 두 요소 사이에 어느 하나의 변화가 결과적으로 스스로를 동일한 방향으로 더욱 변화시키는 형태의 연결구조.
<사진설명>◯ 설명: A: 서로 상호작용하는 두 생체신호 진동자(oscillator)들의 예시. B: 이중활성 양성피드백으로 연결된 진동자들. C: 이중억제 양성피드백으로 연결된 진동자들. D: 연결강도에 따라 진동신호 동기화에 소요되는 시간. E: 연결강도 증가에 따라 점차 진동신호 동기화가 되어가는 모습의 예시 (좌측의 비동기화 진동신호들이 점차 우측의 동기화된 진동신호들로 변화되어 가는 과정을 나타냄).
2010.02.02 조회수 25152
매미와 개구리는 지휘자없이 어떻게 합창할까
나무위의 매미와 논두렁의 개구리는 지휘자 없이 어떻게 합창할까? 이와 관련해서, KAIST 바이오 및 뇌공학과의 조광현 교수는 생명체의 동기화된 주기적 진동신호의 생성원리를 최근 규명했다. 나무에 붙어있는 많은 반딧불들의 동시다발적인 깜빡임, 매미들의 조율된 울음소리, 뇌신경세포들간의 전기신호, 세포내 분자들의 농도변화에 이르기까지 생명체는 다양한 형태의 주기적 진동신호 교환을 통해 정보를 전달하는데, 이들은 놀랍게도 정확히 동일한 위상(phase)으로 동기화되곤 한다. 이는 마치 오케스트라에서 지휘자 없이도 모든 연주가 일정한 박자에 맞춰 이루어지는 것과 같다.
어떻게 생명체의 여러 주기적 진동신호들이 그러한 동기화를 이루는가?
우리학교 바이오및뇌공학과 조광현(曺光鉉) 교수 연구팀이 대규모 가상세포(virtual cell)실험을 통해 생명체의 다양한 주기적 진동(oscillation)신호들이 동기화(synchronization)되는 보편적인 원리를 규명했다.
曺교수팀은 이번 연구를 통해 여러 독립적인 주기적 진동신호들은 양성피드백(positive feedback)을 통해 서로의 위상에 영향을 줘 하나의 동일한 위상으로 수렴되는 현상을 밝혀냈다.
특히 양성피드백은 이중활성(double activation) 또는 이중억제(double inhibition)의 구조로 구현된다. 이중활성피드백은 연결시간지연이 짧을 때, 이중억제피드백은 연결시간지연이 길 때 보다 안정적인 신호동기화를 가능하게 했다.
또한, 노이즈(noise) 교란이 있을 때 이중활성피드백은 진동신호의 주기보다 진폭을 안정적으로 유지하는 반면 이중억제피드백은 연결강도에 불규칙한 변화가 주어졌을 때 일정한 주기와 진폭을 유지시켜줬다. 현존하는 대부분의 현상들이 이러한 원칙을 따르고 있었다.
이번에 규명된 원리는 생체내 주기적 진동신호의 동기화가 교란될 때 발생하는 뇌질환 등 여러 질병의 원인을 새롭게 조명하는 계기를 마련할 것으로 기대된다.
이번 연구는 기존 생명과학의 난제에 대해 IT융합기술인 시스템생물학(Systems Biology) 연구를 통해 해답을 제시할 수 있음을 보여줬으며, 향후 생명과학 연구에 있어서 가상세포실험의 무한한 가능성을 제시했다.
曺교수는 “생명체는 복잡하게 얽혀있는 것으로 보이는 네트워크속에 이와 같이 정교한 진화적 설계원리를 간직하고 있었다”며 “이러한 규칙들은 임의로 수많은 디지털 진동자들을 만들어 인공진화를 통해 신호의 동기화 현상을 관측하였을 때에도 마찬가지로 성립된다는 흥미로운 사실을 확인했다”고 말했다.
이 연구는 교육과학기술부가 지원하는 한국연구재단 연구사업의 일환으로 수행되었으며, 연구결과는 세포생물학 분야 권위지인 세포과학저널(Journal of Cell Science) 2010년 1월 26일자 온라인판에 게재됐다.
세포생물학 실험결과만을 출판하는 이 저널에 순수 컴퓨터시뮬레이션만으로 수행된 가상세포실험 연구결과가 게재된 것은 매우 이례적인 일이다.
인터넷주소: http://jcs.biologists.org/cgi/content/abstract/jcs.060061v1
<용어설명>◯ 양성피드백(positive feedback): 서로 연결되어 있는 두 요소 사이에 어느 하나의 변화가 결과적으로 스스로를 동일한 방향으로 더욱 변화시키는 형태의 연결구조.
<사진설명>◯ 설명: A: 서로 상호작용하는 두 생체신호 진동자(oscillator)들의 예시. B: 이중활성 양성피드백으로 연결된 진동자들. C: 이중억제 양성피드백으로 연결된 진동자들. D: 연결강도에 따라 진동신호 동기화에 소요되는 시간. E: 연결강도 증가에 따라 점차 진동신호 동기화가 되어가는 모습의 예시 (좌측의 비동기화 진동신호들이 점차 우측의 동기화된 진동신호들로 변화되어 가는 과정을 나타냄).
2010.02.02 조회수 25152