-
 물리학 난제였던 유전율 텐서 측정 구현
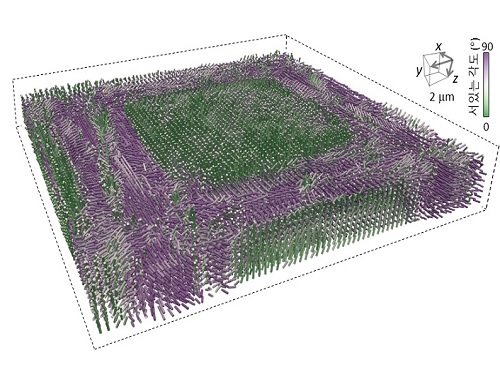
우리 대학 물리학과 박용근 교수 연구팀이 기존에는 이론조차 존재하지 않았던 물리학 난제 중 하나인 유전율 텐서의 3차원 단층 촬영 방법을 개발했다고 4일 밝혔다.
유전율 텐서는 빛과 물질의 상호작용을 근본적으로 기술하는, 물질의 광학적 이방성(異方性, 방향에 따라 달라 보이는 특성)을 정량적으로 표현할 수 있는 중요한 물리량이다. 유전율은 고등학교 물리학에서도 다루는 기본적인 개념이지만, 지금까지 3차원 유전율 텐서를 실험적으로 측정할 수 있는 방법이 존재하지 않았다. 병리학, 재료과학, 연성물질 과학, 또는 디스플레이 등 다양한 분야에서 갖는 중요성에도 불구하고, 직접적으로 측정할 방법이 없다는 한계가 있었다. 현재까지도 3차원 광학적 이방성은 2차원 편광현미경 측정 및 시뮬레이션을 통해 부정확하게 추정할 수밖에 없다.
3차원 유전율 텐서의 측정은 물리학, 광학 분야의 오래된 난제 중 하나였다. 1967년 광학적 이방성을 무시하고 유전율 텐서를 3차원 굴절률 수치로 단순화하여 측정하는 기술이 발명돼 지난 50여 년간 빠르게 성장하고 상용화까지 성공했지만, 여전히 3차원 유전율 텐서를 측정하는 방법은 개발되지 못했다.
여태껏 이 문제가 풀리지 못했던 까닭은, 3개의 고유치를 가지는 유전율 텐서를 측정하기에는 빛의 편광 방향 자유도가 2개로 제한되기 때문이다.
재료과학 분야 최고 권위지인 `네이처 머티리얼즈(Nature Materials, IF 43.84)'에 3일 발표된 이번 연구(논문명: Tomographic measurements of dielectric tensors at optical frequency)에서 연구팀은 이러한 한계를 극복하고 광학적 이방성 구조의 3차원 유전율 텐서 단층 촬영 이론을 개발해 구현하는 데 성공했다.
기존의 고정관념에서 벗어나, 빛의 방향을 살짝 틀어주어 중첩된 정보를 활용하면, 편광 방향 자유도를 3개로 늘려서 유전율 텐서의 3개 고유치를 모두 구할 수 있다는 점에 착안한 것이 연구진의 핵심 아이디어다. 이렇게 3개의 편광 자유도를 제어하는 것과 동시에, 병원에서 사용하는 엑스레이, 컴퓨터단층(CT) 촬영처럼, 여러 각도에서 광학적 이방성 구조를 홀로그래피 현미경을 개발하여 촬영함으로써 3차원 유전율 텐서를 직접적으로 측정했다.
연구팀은 개발된 방법을 이용해 뒤틀린 네마틱 (twisted nematic) 액정과 같은 잘 알려진 3차원 광학적 이방체의 3차원 유전율 텐서를 성공적으로 측정함으로써 기술의 구현을 입증했다. 더 나아가 열적 비평형 상태로 성장-소멸-융합하는 액정 동역학, 반복되는 위상학적 특이점 구조의 액정 네트워크 등 기존의 방법들로 추정하기 어려웠던 3차원 유전율 텐서를 실험적으로 최초 측정하는 성과를 거뒀다.
제1 저자인 물리학과 신승우 박사는 "지금까지 직접 볼 수 없던 유전율 텐서를 실제로 측정할 수 있는 방법론을 처음으로 개발한 것이 큰 의미ˮ라며 "액정, 카이랄 물질, 암조직과 같은 병리 조직 내부의 콜라겐 파이버 등과 같은 광학적 방향성을 보이는 다양한 물질들의 3차원 구조를 정량적이고 비침습적으로 직접 관측할 수 있기에 여러 분야에 범용적, 필수적으로 사용할 수 있는 도구로 기대한다ˮ라고 말했다.
이번 연구는 박용근 교수 연구팀의 기술 개발 이외에도 다학제적 접근을 통해 결실을 볼 수 있었다. UNIST 물리학과 정준우 교수, 우리 대학 생명화학공학과 김신현 교수, 우리 대학 화학과 윤동기 교수 연구팀들이 오랜 기간 발전시켜온 액정 구조체 제작 기술 덕분에, 다양한 액정 구조체를 통해 기술의 실험적 검증을 효과적으로 진행할 수 있었다.
한편 이번 연구는 과학기술정보통신부의 정보통신기획평가원, 한국연구재단 창의연구사업 및 G-CORE 사업의 지원을 받아 수행됐다.
물리학 난제였던 유전율 텐서 측정 구현
우리 대학 물리학과 박용근 교수 연구팀이 기존에는 이론조차 존재하지 않았던 물리학 난제 중 하나인 유전율 텐서의 3차원 단층 촬영 방법을 개발했다고 4일 밝혔다.
유전율 텐서는 빛과 물질의 상호작용을 근본적으로 기술하는, 물질의 광학적 이방성(異方性, 방향에 따라 달라 보이는 특성)을 정량적으로 표현할 수 있는 중요한 물리량이다. 유전율은 고등학교 물리학에서도 다루는 기본적인 개념이지만, 지금까지 3차원 유전율 텐서를 실험적으로 측정할 수 있는 방법이 존재하지 않았다. 병리학, 재료과학, 연성물질 과학, 또는 디스플레이 등 다양한 분야에서 갖는 중요성에도 불구하고, 직접적으로 측정할 방법이 없다는 한계가 있었다. 현재까지도 3차원 광학적 이방성은 2차원 편광현미경 측정 및 시뮬레이션을 통해 부정확하게 추정할 수밖에 없다.
3차원 유전율 텐서의 측정은 물리학, 광학 분야의 오래된 난제 중 하나였다. 1967년 광학적 이방성을 무시하고 유전율 텐서를 3차원 굴절률 수치로 단순화하여 측정하는 기술이 발명돼 지난 50여 년간 빠르게 성장하고 상용화까지 성공했지만, 여전히 3차원 유전율 텐서를 측정하는 방법은 개발되지 못했다.
여태껏 이 문제가 풀리지 못했던 까닭은, 3개의 고유치를 가지는 유전율 텐서를 측정하기에는 빛의 편광 방향 자유도가 2개로 제한되기 때문이다.
재료과학 분야 최고 권위지인 `네이처 머티리얼즈(Nature Materials, IF 43.84)'에 3일 발표된 이번 연구(논문명: Tomographic measurements of dielectric tensors at optical frequency)에서 연구팀은 이러한 한계를 극복하고 광학적 이방성 구조의 3차원 유전율 텐서 단층 촬영 이론을 개발해 구현하는 데 성공했다.
기존의 고정관념에서 벗어나, 빛의 방향을 살짝 틀어주어 중첩된 정보를 활용하면, 편광 방향 자유도를 3개로 늘려서 유전율 텐서의 3개 고유치를 모두 구할 수 있다는 점에 착안한 것이 연구진의 핵심 아이디어다. 이렇게 3개의 편광 자유도를 제어하는 것과 동시에, 병원에서 사용하는 엑스레이, 컴퓨터단층(CT) 촬영처럼, 여러 각도에서 광학적 이방성 구조를 홀로그래피 현미경을 개발하여 촬영함으로써 3차원 유전율 텐서를 직접적으로 측정했다.
연구팀은 개발된 방법을 이용해 뒤틀린 네마틱 (twisted nematic) 액정과 같은 잘 알려진 3차원 광학적 이방체의 3차원 유전율 텐서를 성공적으로 측정함으로써 기술의 구현을 입증했다. 더 나아가 열적 비평형 상태로 성장-소멸-융합하는 액정 동역학, 반복되는 위상학적 특이점 구조의 액정 네트워크 등 기존의 방법들로 추정하기 어려웠던 3차원 유전율 텐서를 실험적으로 최초 측정하는 성과를 거뒀다.
제1 저자인 물리학과 신승우 박사는 "지금까지 직접 볼 수 없던 유전율 텐서를 실제로 측정할 수 있는 방법론을 처음으로 개발한 것이 큰 의미ˮ라며 "액정, 카이랄 물질, 암조직과 같은 병리 조직 내부의 콜라겐 파이버 등과 같은 광학적 방향성을 보이는 다양한 물질들의 3차원 구조를 정량적이고 비침습적으로 직접 관측할 수 있기에 여러 분야에 범용적, 필수적으로 사용할 수 있는 도구로 기대한다ˮ라고 말했다.
이번 연구는 박용근 교수 연구팀의 기술 개발 이외에도 다학제적 접근을 통해 결실을 볼 수 있었다. UNIST 물리학과 정준우 교수, 우리 대학 생명화학공학과 김신현 교수, 우리 대학 화학과 윤동기 교수 연구팀들이 오랜 기간 발전시켜온 액정 구조체 제작 기술 덕분에, 다양한 액정 구조체를 통해 기술의 실험적 검증을 효과적으로 진행할 수 있었다.
한편 이번 연구는 과학기술정보통신부의 정보통신기획평가원, 한국연구재단 창의연구사업 및 G-CORE 사업의 지원을 받아 수행됐다.
2022.03.04
조회수 11923
-
 생각만으로 정확하게 로봇팔 조종이 가능한 뇌-기계 인터페이스 개발
우리 대학 바이오및뇌공학과 정재승 교수 연구팀이 3차원 공간상에서 생각만으로 로봇팔을 높은 정확도 (90.9~92.6%)로 조종하는 `뇌-기계 인터페이스 시스템'을 개발했다고 23일 밝혔다.
정 교수 연구팀은 인공지능과 유전자 알고리즘을 사용해 인간의 대뇌 심부에서 측정한 뇌파만으로 팔 움직임의 의도를 파악해 로봇팔을 제어하는 새로운 형태의 뇌-기계 인터페이스 시스템을 개발했다. 뇌 활동만으로 사람의 의도를 파악해 로봇이나 기계가 대신 행동에 옮기는 `뇌-기계 인터페이스' 기술은 최근 급속도로 발전하고 있다. 하지만 손을 움직이는 정도의 의도 파악을 넘어, 팔 움직임의 방향에 대한 의도를 섬세하게 파악해 정교하게 로봇팔을 움직이는 기술은 아직 정확도가 높지 않았다.
하지만 연구팀은 이번 연구에서 조종 `방향'에 대한 의도를 뇌 활동만으로 인식하는 인공지능 모델을 개발했고, 그 결과 3차원 공간상에서 24개의 방향을 90% 이상의 정확도로 정교하게 해석하는 시스템을 개발했다.
게다가 딥러닝 등 기존 기계학습 기술은 높은 사양의 GPU 하드웨어가 필요했지만, 이번 연구에서는 축적 컴퓨팅(Reservoir Computing) 기법을 이용해 낮은 사양의 하드웨어에서도 인공지능 학습이 가능하여 스마트 모바일 기기에서도 폭넓게 응용될 수 있도록 개발해, 향후 메타버스와 스마트 기기에도 폭넓게 적용이 가능할 것으로 기대된다.
우리 대학 김훈희 박사(現 강남대 조교수)가 제1 저자로 참여한 이번 연구는 국제학술지 `어플라이드 소프트 컴퓨팅(Applied Soft Computing)' 2022년 117권 3월호에 출판됐다. (논문명 : An electrocorticographic decoder for arm movement for brain-machine interface using an echo state network and Gaussian readout).
뇌-기계 인터페이스는 사용자의 뇌 활동을 통해 의도를 읽고 로봇이나 기계에 전달하는 기술로서 로봇, 드론, 컴퓨터뿐만 아니라 스마트 모바일 기기, 메타버스 등에서의 이용될 차세대 인터페이스 기술로 각광받고 있다.
특히 기존의 인터페이스가 외부 신체 기관을 통해 명령을 간접 전달(버튼, 터치, 제스처 등)해야 하지만 뇌-기계 인터페이스는 명령을 뇌로부터 직접적 전달한다는 점에서 가장 진보된 인터페이스 기술로 여겨진다.
그러나 뇌파는 개개인의 차이가 매우 크고, 단일 신경 세포로부터 정확한 신호를 읽는 것이 아니라 넓은 영역에 있는 신경 세포 집단의 전기적 신호 특성을 해석해야 하므로 잡음이 크다는 한계점을 가지고 있다.
연구팀은 이러한 문제 해결을 위해 최첨단 인공지능 기법의 하나인 `축적 컴퓨팅 기법'을 이용해 뇌-기계 인터페이스에서 필요한 개개인의 뇌파 신호의 중요 특성을 인공신경망이 자동으로 학습해 찾을 수 있도록 구현했다.
또한 유전자 알고리즘(Genetic Algorithm)을 이용해 인공지능 신경망이 최적의 뇌파 특성을 효율적으로 찾을 수 있게 시스템을 설계했다. 연구팀은 심부 뇌파를 최종 해석하는 리드아웃(Readout)을 가우시안(Gaussian) 모델로 설계해 시각피질 신경 세포가 방향을 표현하는 방법을 모방하는 인공신경망을 개발했다. 이런 리드아웃 방식은 축적 컴퓨팅의 선형 학습 알고리즘을 이용해 일반적 사양의 간단한 하드웨어에서도 빠르게 학습할 수 있어 메타버스, 스마트기기 등 일상생활에서 응용이 가능해진다.
특히, 이번 연구에서 만들어진 뇌-기계 인터페이스 인공지능 모델은 3차원상에서 24가지 방향 즉, 각 차원에서 8가지 방향을 디코딩할 수 있으며 모든 방향에서 평균 90% 이상의 정확도 (90.9%~92.6% 범위)를 보였다. 또한 연구된 뇌-기계 인터페이스는 3차원 공간상에서 로봇팔을 움직이는 상상을 할 때의 뇌파를 해석해 성공적으로 로봇팔을 움직이는 시뮬레이션 결과를 보였다.
인공지능 시스템을 만든 제1 저자인 김훈희 박사는 "공학적인 신호처리 기법에 의존해 온 기존 뇌파 디코딩 방법과는 달리, 인간 뇌의 실제 작동 구조를 모방한 인공신경망을 개발해 좀더 발전된 형태의 뇌-기계 인터페이스 시스템을 개발해 기쁘다ˮ면서 "향후 뇌의 특성을 좀 더 구체적으로 이용한 `뇌 모방 인공지능(Brain-inspired A.I.)'을 이용한 다양한 뇌-기계 인터페이스를 개발할 계획이다ˮ라고 말했다.
이번 연구를 주도한 연구책임자 정재승 교수는 "뇌파를 통해 생각만으로 로봇팔을 구동하는 `뇌-기계 인터페이스 시스템'들이 대부분 고사양 하드웨어가 필요해 실시간 응용으로 나아가기 어렵고 스마트기기 등으로 적용이 어려웠다. 그러나 이번 시스템은 90%~92%의 높은 정확도를 가진 의도 인식 인공지능 시스템을 만들어 메타버스 안에서 아바타를 생각대로 움직이게 하거나 앱을 생각만으로 컨트롤하는 스마트기기 등에 광범위하게 사용될 수 있다ˮ고 말했다.
이번 연구 결과는 사지마비 환자나 사고로 팔을 잃은 환자들을 위한 로봇팔 장착 및 제어 기술부터, 메타버스, 스마트기기, 게임, 엔터테인먼트 애플리케이션 등 다양한 시스템에 뇌-기계 인터페이스를 적용할 가능성을 열어 줄 것으로 기대된다.
이번 연구는 한국연구재단 뇌 원천기술개발사업의 지원을 받아 수행됐다.
생각만으로 정확하게 로봇팔 조종이 가능한 뇌-기계 인터페이스 개발
우리 대학 바이오및뇌공학과 정재승 교수 연구팀이 3차원 공간상에서 생각만으로 로봇팔을 높은 정확도 (90.9~92.6%)로 조종하는 `뇌-기계 인터페이스 시스템'을 개발했다고 23일 밝혔다.
정 교수 연구팀은 인공지능과 유전자 알고리즘을 사용해 인간의 대뇌 심부에서 측정한 뇌파만으로 팔 움직임의 의도를 파악해 로봇팔을 제어하는 새로운 형태의 뇌-기계 인터페이스 시스템을 개발했다. 뇌 활동만으로 사람의 의도를 파악해 로봇이나 기계가 대신 행동에 옮기는 `뇌-기계 인터페이스' 기술은 최근 급속도로 발전하고 있다. 하지만 손을 움직이는 정도의 의도 파악을 넘어, 팔 움직임의 방향에 대한 의도를 섬세하게 파악해 정교하게 로봇팔을 움직이는 기술은 아직 정확도가 높지 않았다.
하지만 연구팀은 이번 연구에서 조종 `방향'에 대한 의도를 뇌 활동만으로 인식하는 인공지능 모델을 개발했고, 그 결과 3차원 공간상에서 24개의 방향을 90% 이상의 정확도로 정교하게 해석하는 시스템을 개발했다.
게다가 딥러닝 등 기존 기계학습 기술은 높은 사양의 GPU 하드웨어가 필요했지만, 이번 연구에서는 축적 컴퓨팅(Reservoir Computing) 기법을 이용해 낮은 사양의 하드웨어에서도 인공지능 학습이 가능하여 스마트 모바일 기기에서도 폭넓게 응용될 수 있도록 개발해, 향후 메타버스와 스마트 기기에도 폭넓게 적용이 가능할 것으로 기대된다.
우리 대학 김훈희 박사(現 강남대 조교수)가 제1 저자로 참여한 이번 연구는 국제학술지 `어플라이드 소프트 컴퓨팅(Applied Soft Computing)' 2022년 117권 3월호에 출판됐다. (논문명 : An electrocorticographic decoder for arm movement for brain-machine interface using an echo state network and Gaussian readout).
뇌-기계 인터페이스는 사용자의 뇌 활동을 통해 의도를 읽고 로봇이나 기계에 전달하는 기술로서 로봇, 드론, 컴퓨터뿐만 아니라 스마트 모바일 기기, 메타버스 등에서의 이용될 차세대 인터페이스 기술로 각광받고 있다.
특히 기존의 인터페이스가 외부 신체 기관을 통해 명령을 간접 전달(버튼, 터치, 제스처 등)해야 하지만 뇌-기계 인터페이스는 명령을 뇌로부터 직접적 전달한다는 점에서 가장 진보된 인터페이스 기술로 여겨진다.
그러나 뇌파는 개개인의 차이가 매우 크고, 단일 신경 세포로부터 정확한 신호를 읽는 것이 아니라 넓은 영역에 있는 신경 세포 집단의 전기적 신호 특성을 해석해야 하므로 잡음이 크다는 한계점을 가지고 있다.
연구팀은 이러한 문제 해결을 위해 최첨단 인공지능 기법의 하나인 `축적 컴퓨팅 기법'을 이용해 뇌-기계 인터페이스에서 필요한 개개인의 뇌파 신호의 중요 특성을 인공신경망이 자동으로 학습해 찾을 수 있도록 구현했다.
또한 유전자 알고리즘(Genetic Algorithm)을 이용해 인공지능 신경망이 최적의 뇌파 특성을 효율적으로 찾을 수 있게 시스템을 설계했다. 연구팀은 심부 뇌파를 최종 해석하는 리드아웃(Readout)을 가우시안(Gaussian) 모델로 설계해 시각피질 신경 세포가 방향을 표현하는 방법을 모방하는 인공신경망을 개발했다. 이런 리드아웃 방식은 축적 컴퓨팅의 선형 학습 알고리즘을 이용해 일반적 사양의 간단한 하드웨어에서도 빠르게 학습할 수 있어 메타버스, 스마트기기 등 일상생활에서 응용이 가능해진다.
특히, 이번 연구에서 만들어진 뇌-기계 인터페이스 인공지능 모델은 3차원상에서 24가지 방향 즉, 각 차원에서 8가지 방향을 디코딩할 수 있으며 모든 방향에서 평균 90% 이상의 정확도 (90.9%~92.6% 범위)를 보였다. 또한 연구된 뇌-기계 인터페이스는 3차원 공간상에서 로봇팔을 움직이는 상상을 할 때의 뇌파를 해석해 성공적으로 로봇팔을 움직이는 시뮬레이션 결과를 보였다.
인공지능 시스템을 만든 제1 저자인 김훈희 박사는 "공학적인 신호처리 기법에 의존해 온 기존 뇌파 디코딩 방법과는 달리, 인간 뇌의 실제 작동 구조를 모방한 인공신경망을 개발해 좀더 발전된 형태의 뇌-기계 인터페이스 시스템을 개발해 기쁘다ˮ면서 "향후 뇌의 특성을 좀 더 구체적으로 이용한 `뇌 모방 인공지능(Brain-inspired A.I.)'을 이용한 다양한 뇌-기계 인터페이스를 개발할 계획이다ˮ라고 말했다.
이번 연구를 주도한 연구책임자 정재승 교수는 "뇌파를 통해 생각만으로 로봇팔을 구동하는 `뇌-기계 인터페이스 시스템'들이 대부분 고사양 하드웨어가 필요해 실시간 응용으로 나아가기 어렵고 스마트기기 등으로 적용이 어려웠다. 그러나 이번 시스템은 90%~92%의 높은 정확도를 가진 의도 인식 인공지능 시스템을 만들어 메타버스 안에서 아바타를 생각대로 움직이게 하거나 앱을 생각만으로 컨트롤하는 스마트기기 등에 광범위하게 사용될 수 있다ˮ고 말했다.
이번 연구 결과는 사지마비 환자나 사고로 팔을 잃은 환자들을 위한 로봇팔 장착 및 제어 기술부터, 메타버스, 스마트기기, 게임, 엔터테인먼트 애플리케이션 등 다양한 시스템에 뇌-기계 인터페이스를 적용할 가능성을 열어 줄 것으로 기대된다.
이번 연구는 한국연구재단 뇌 원천기술개발사업의 지원을 받아 수행됐다.
2022.02.24
조회수 16000
-
 단일세포 RNA 시퀀싱을 통한 꽃향기 합성 유전자 발굴
우리 대학 생명과학과 김상규 교수 연구팀이 꽃향기 합성 유전자를 발굴하기 위해 꽃잎 단일세포 RNA 시퀀싱 기술을 개발하고 벤질아세톤(benzylacetone) 꽃향기 합성 경로를 밝혔다.
벤질아세톤은 코요테담배(Nicotiana attenuata) 꽃에서 합성되고 밤에 분비가 되는 향기 물질이다. 이 향기물질은 밤에 활동하는 박각시나방을 유인한다. 그리고 꽃은 꿀을 제공하고 그 대가로 나방은 화분pollen을 멀리 날라준다. 또한 벤질아세톤은 코요테담배 꽃을 먹는 해충을 쫓아내는 기능을 하고 있다. 생태적으로 재미있는 기능을 하고 있는 물질이지만 생합성 경로에 대해서는 완전히 알려진 상태가 아니었다.
일반적으로 식물이 만들어내는 대사물질의 생합성 유전자를 밝히기 위해 사용하는 방법의 단점을 극복하기 위해서 꽃잎 단일세포에서 발현되는 유전자의 연관도를 이용하여 물질대사 경로를 밝힐 수 있다는 것을 이번 연구를 통해서 증명하였다. 특히 유전정보가 제한적으로 알려져 있고 다양한 생태형 ecotype을 가진 식물 집단이 없어도 비모델 식물에서 물질합성 경로에 있는 효소와 그 효소의 발현을 조절하는 전사인자 등도 찾을 수 있는 가능성을 제시하였다.
단일세포 RNA 시퀀싱의 장점을 활용하여 향기합성 유전자가 만들어지는 세포를 구별하고 꽃잎에서 향기가 합성되는 위치도 밝힐 수 있었다.
우리 대학 생명과학과 강문영 석박사통합과정 학생이 제1 저자로 참여한 이번 연구 결과는 'New Phytologist' 학술지에 게재됐다. (관련 논문명: Single-cell RNA-sequencing of Nicotiana attenuata corolla cells reveals the biosynthetic pathway of a floral scent)
한편 이번 연구는 삼성미래기술육성사업과 포스코사이언스펠로십 지원을 받아 수행됐다.
단일세포 RNA 시퀀싱을 통한 꽃향기 합성 유전자 발굴
우리 대학 생명과학과 김상규 교수 연구팀이 꽃향기 합성 유전자를 발굴하기 위해 꽃잎 단일세포 RNA 시퀀싱 기술을 개발하고 벤질아세톤(benzylacetone) 꽃향기 합성 경로를 밝혔다.
벤질아세톤은 코요테담배(Nicotiana attenuata) 꽃에서 합성되고 밤에 분비가 되는 향기 물질이다. 이 향기물질은 밤에 활동하는 박각시나방을 유인한다. 그리고 꽃은 꿀을 제공하고 그 대가로 나방은 화분pollen을 멀리 날라준다. 또한 벤질아세톤은 코요테담배 꽃을 먹는 해충을 쫓아내는 기능을 하고 있다. 생태적으로 재미있는 기능을 하고 있는 물질이지만 생합성 경로에 대해서는 완전히 알려진 상태가 아니었다.
일반적으로 식물이 만들어내는 대사물질의 생합성 유전자를 밝히기 위해 사용하는 방법의 단점을 극복하기 위해서 꽃잎 단일세포에서 발현되는 유전자의 연관도를 이용하여 물질대사 경로를 밝힐 수 있다는 것을 이번 연구를 통해서 증명하였다. 특히 유전정보가 제한적으로 알려져 있고 다양한 생태형 ecotype을 가진 식물 집단이 없어도 비모델 식물에서 물질합성 경로에 있는 효소와 그 효소의 발현을 조절하는 전사인자 등도 찾을 수 있는 가능성을 제시하였다.
단일세포 RNA 시퀀싱의 장점을 활용하여 향기합성 유전자가 만들어지는 세포를 구별하고 꽃잎에서 향기가 합성되는 위치도 밝힐 수 있었다.
우리 대학 생명과학과 강문영 석박사통합과정 학생이 제1 저자로 참여한 이번 연구 결과는 'New Phytologist' 학술지에 게재됐다. (관련 논문명: Single-cell RNA-sequencing of Nicotiana attenuata corolla cells reveals the biosynthetic pathway of a floral scent)
한편 이번 연구는 삼성미래기술육성사업과 포스코사이언스펠로십 지원을 받아 수행됐다.
2022.02.14
조회수 8659
-
 유전자 가위로 생체 내 정밀한 유전자 교정에 의한 면역 항암 치료
CRISPR/Cas9 시스템을 이용하여 유전자교정을 일으킴으로써 암의 면역 치료를 유도하는 기술이 우리 대학 연구진에 의해 개발됐다.
우리 대학 생명과학과 정현정 교수, 서울대학교 의과학과 정기훈 교수 공동연구팀이 CRISPR/Cas9 리보핵산단백질을 생체 내에 효과적으로 전달하는 나노복합체를 개발하여 면역 관문 유전자를 교정함으로써 항암 효과를 보이는데 성공했다고 밝혔다.
암은 현대인의 건강을 위협하는 대표적인 요인으로 꼽히고 있다. 암의 치료 방법 중 면역 항암 요법은 부작용이 적고 높은 치료 성적을 보여 다양한 암 유형에 적용할 수 있다. 기존에는 항체 기반 치료법이 주로 임상에서 사용되고 있으며 다양한 고형암의 치료에 승인되었으나, 일시적인 효과로 반복 투여가 필요하다.
CRISPR/Cas9 시스템은 유전체의 서열을 직접 정밀하게 교정할 수 있으며, DNA 이중가닥을 절단하는 Cas9 제한효소와 특정 서열을 표적하는 단일 가이드 RNA로 이루어진다. 유전자교정 치료제의 경우 일반적으로 바이러스 기반 치료 방법을 이용했으나 돌연변이 유발, 비특이적 표적 효과 등으로 인해 한계가 있다. 비바이러스 치료제로 Cas9 단백질 및 단일가닥 RNA를 이용하면 바이러스 치료보다 안전성을 높일 수 있으나 낮은 세포내 전달 효과로 치료 효능이 떨어진다. 전달 효율을 높이기 위해 기존에 다양한 방법이 개발되고 연구됐으나, 일반적으로 과량의 전달체물질을 사용함으로써 생체 내 독성 문제가 나타나는 한계점이 있다. 이러한 문제점을 개선하기 위해 연구팀은 Cas9 단백질에 세포내 유입을 촉진하는 고분자를 접합시켜 극미량의 전달체물질로 고효율 전달이 가능한 Cas9 컨쥬게이트를 제작하여 활용했다.
연구팀은 이러한 Cas9 컨쥬게이트, 단일 가이드 RNA 및 변형된 데옥시뉴클레오타이드(DNA)를 추가해 나노조립된 리보핵단백질 복합체(이하 NanoRNP)를 개발했다. 이 복합체는 Cas9 컨쥬게이트, RNA 및 DNA의 상호작용으로 쉽게 제작할 수 있고, 유전자 교정 치료제로써 단일 요법에 의해 항암 치료가 가능하다는 점이 장점이다.
우리 대학 생명과학과 석박사통합과정 이주희 학생이 제1 저자로 참여한 이번 연구 결과는 재료화학 분야 국제학술지 `케미스트리 오브 머티리얼즈(Chemistry of Materials)'에 12월 20일 字 온라인 게재됐다. (논문명 : Nano-assembly of a Chemically Tailored Cas9 Ribonucleoprotein for In Vivo Gene Editing and Cancer Immunotherapy)
NanoRNP의 경우 Cas9에 부착된 고분자가 강한 양이온성을 지녀 단일 가이드 RNA와 안정적으로 복합체를 형성시키며, 생체내 분해효소로부터 보호하여 활성을 향상시킨다. 본 연구팀은 NanoRNP를 피부암에서 많이 발현되는 프로그램된 세포사멸 리간드-1 (PD-L1) 유전자를 표적하는데 응용하였다. PD-L1은 면역 세포의 표면 수용체에 존재하는 프로그램된 세포사멸 수용체-1 (PD-1)과 상호작용하여 면역 세포의 반응을 억제해 암세포의 세포사멸 회피를 유도한다.
연구팀은 NanoRNP를 이용하여 PD-L1 유전자의 교정으로 유전자결손을 유도하여, 면역 세포들이 활성화되고 종양미세환경의 변화로 면역 세포에 의한 암세포 사멸이 유도됨을 확인했다.
연구팀은 이번 연구 결과를 응용해 향후 암 뿐만 아니라 유전 질환 등 다양한 질병에 적용함으로써 연구를 확대 및 발전시켜 나갈 수 있을 것으로 기대하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 범부처전주기의료기기연구개발사업 및 KAIST End Run 사업의 지원을 통해 이뤄졌다.
유전자 가위로 생체 내 정밀한 유전자 교정에 의한 면역 항암 치료
CRISPR/Cas9 시스템을 이용하여 유전자교정을 일으킴으로써 암의 면역 치료를 유도하는 기술이 우리 대학 연구진에 의해 개발됐다.
우리 대학 생명과학과 정현정 교수, 서울대학교 의과학과 정기훈 교수 공동연구팀이 CRISPR/Cas9 리보핵산단백질을 생체 내에 효과적으로 전달하는 나노복합체를 개발하여 면역 관문 유전자를 교정함으로써 항암 효과를 보이는데 성공했다고 밝혔다.
암은 현대인의 건강을 위협하는 대표적인 요인으로 꼽히고 있다. 암의 치료 방법 중 면역 항암 요법은 부작용이 적고 높은 치료 성적을 보여 다양한 암 유형에 적용할 수 있다. 기존에는 항체 기반 치료법이 주로 임상에서 사용되고 있으며 다양한 고형암의 치료에 승인되었으나, 일시적인 효과로 반복 투여가 필요하다.
CRISPR/Cas9 시스템은 유전체의 서열을 직접 정밀하게 교정할 수 있으며, DNA 이중가닥을 절단하는 Cas9 제한효소와 특정 서열을 표적하는 단일 가이드 RNA로 이루어진다. 유전자교정 치료제의 경우 일반적으로 바이러스 기반 치료 방법을 이용했으나 돌연변이 유발, 비특이적 표적 효과 등으로 인해 한계가 있다. 비바이러스 치료제로 Cas9 단백질 및 단일가닥 RNA를 이용하면 바이러스 치료보다 안전성을 높일 수 있으나 낮은 세포내 전달 효과로 치료 효능이 떨어진다. 전달 효율을 높이기 위해 기존에 다양한 방법이 개발되고 연구됐으나, 일반적으로 과량의 전달체물질을 사용함으로써 생체 내 독성 문제가 나타나는 한계점이 있다. 이러한 문제점을 개선하기 위해 연구팀은 Cas9 단백질에 세포내 유입을 촉진하는 고분자를 접합시켜 극미량의 전달체물질로 고효율 전달이 가능한 Cas9 컨쥬게이트를 제작하여 활용했다.
연구팀은 이러한 Cas9 컨쥬게이트, 단일 가이드 RNA 및 변형된 데옥시뉴클레오타이드(DNA)를 추가해 나노조립된 리보핵단백질 복합체(이하 NanoRNP)를 개발했다. 이 복합체는 Cas9 컨쥬게이트, RNA 및 DNA의 상호작용으로 쉽게 제작할 수 있고, 유전자 교정 치료제로써 단일 요법에 의해 항암 치료가 가능하다는 점이 장점이다.
우리 대학 생명과학과 석박사통합과정 이주희 학생이 제1 저자로 참여한 이번 연구 결과는 재료화학 분야 국제학술지 `케미스트리 오브 머티리얼즈(Chemistry of Materials)'에 12월 20일 字 온라인 게재됐다. (논문명 : Nano-assembly of a Chemically Tailored Cas9 Ribonucleoprotein for In Vivo Gene Editing and Cancer Immunotherapy)
NanoRNP의 경우 Cas9에 부착된 고분자가 강한 양이온성을 지녀 단일 가이드 RNA와 안정적으로 복합체를 형성시키며, 생체내 분해효소로부터 보호하여 활성을 향상시킨다. 본 연구팀은 NanoRNP를 피부암에서 많이 발현되는 프로그램된 세포사멸 리간드-1 (PD-L1) 유전자를 표적하는데 응용하였다. PD-L1은 면역 세포의 표면 수용체에 존재하는 프로그램된 세포사멸 수용체-1 (PD-1)과 상호작용하여 면역 세포의 반응을 억제해 암세포의 세포사멸 회피를 유도한다.
연구팀은 NanoRNP를 이용하여 PD-L1 유전자의 교정으로 유전자결손을 유도하여, 면역 세포들이 활성화되고 종양미세환경의 변화로 면역 세포에 의한 암세포 사멸이 유도됨을 확인했다.
연구팀은 이번 연구 결과를 응용해 향후 암 뿐만 아니라 유전 질환 등 다양한 질병에 적용함으로써 연구를 확대 및 발전시켜 나갈 수 있을 것으로 기대하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 범부처전주기의료기기연구개발사업 및 KAIST End Run 사업의 지원을 통해 이뤄졌다.
2021.12.24
조회수 12346
-
 사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
2021.12.08
조회수 12561
-
 빛으로 뇌 기능, 행동, 감정을 자유롭게 조절한다
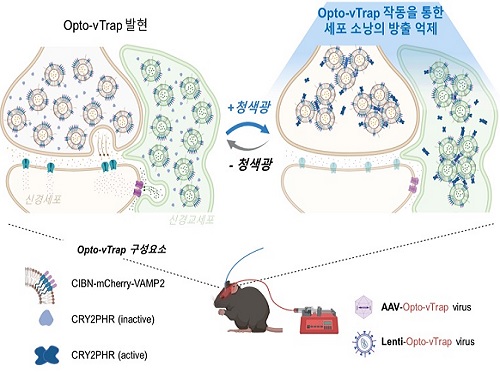
우리 대학 생명과학과 허원도 교수 연구팀은 빛으로 뇌 기능 및 행동을 자유자재로 조절하는 광유전학 기술인 ‘Opto-vTrap(옵토-브이트랩)’을 개발했다. 나아가 동물실험을 통해 뇌 활성 뿐 아니라 활동과 감정까지 조절할 수 있음을 확인했다.
뇌 활성은 신경세포와 신경교세포와 같은 뇌세포들이 서로 신호를 주고받으며 조절된다. 이 같은 상호작용은 뇌 세포 내 ‘소낭’안에 담긴 신경전달물질 분비를 통해 이루어진다. 소낭이 뇌 활성을 조절하는 사령관인 셈이다. 뇌 활성 조절은 뇌 연구를 위한 필수 기술이다. 뇌의 특정 부위나 세포의 활성을 촉진 및 억제해보면 특정 뇌 부위가 담당하는 기능, 여러 뇌 부위 간 상호작용의 역할, 특정 상황에서 다양한 뇌세포의 기능 등 특정 상황에서 뇌 작동이 어떠한 원리로 일어나는지 밝힐 수 있기 때문이다.
그러나 기존 뇌 활성 조절 기술은 원하는 시점에 특정 뇌세포의 활성을 자유롭게 조절하기 어려웠다. 지금까지는 세포 전위차 조절 방식을 사용하였는데, 이는 주변 환경의 산성도를 변화시키거나 원하지 않는 다른 자극을 유발할 뿐만 아니라 전위차에 반응하지 않는 세포에는 사용하지 못하는 한계가 있었다. 이번에 개발한 Opto-vTrap 기술은 세포 소낭을 직접 특이적으로 조절할 수 있어 원하는 시점에 다양한 종류의 뇌세포에서 이용이 가능하다.
연구진은 신경전달물질 분비를 직접 조절하고자 세포에 빛을 쪼이면 순간적으로 내부에 올가미처럼 트랩을 만드는 자체 개발 원천기술을 응용, 소낭에 적용했다. Opto-vTrap을 발현하는 세포나 조직에 빛(청색광)을 가하면 소낭 내 광수용체 단백질들이 엉겨 붙으며 소낭이 트랩 안에 포획되고 신경전달물질 분비가 억제된다. 요컨대 Opto-vTrap으로 소낭의 신호전달물질 분비를 직접 제어하여 뇌 활성을 자유롭게 조절하는 것이다. 연구진은 세포와 조직실험에서 나아가 Opto-vTrap 바이러스를 이용한 동물실험을 통해 뇌세포 신호전달 뿐만 아니라 기억·감정·행동도 조절 가능함을 확인하였다.
Opto-vTrap을 이용하면 뇌의 여러 부위간 복합적 상호작용 원리를 밝히고, 뇌세포 형태별 뇌 기능에 미치는 영향을 연구하는 데 유용하게 활용될 것으로 기대된다.
허원도 교수는 “Opto-vTrap은 신경세포와 신경교세포 모두에 잘 작동되기에 향후 다양한 뇌과학 연구 분야에 이용되리라 기대한다” 며 “앞으로 본 기술을 활용하여 특정 뇌세포의 시공간적 기능 연구를 진행하고자 한다.”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 중견연구과제 및 KAIST 글로벌 특이점 연구사업의 지원을 받아 수행됐다.
이번 연구 결과는 뇌 과학 학술지 뉴런 (Neuron, IF:17.173) 에 12월 1일(수) 1시(한국시간) 게재됐다.
빛으로 뇌 기능, 행동, 감정을 자유롭게 조절한다
우리 대학 생명과학과 허원도 교수 연구팀은 빛으로 뇌 기능 및 행동을 자유자재로 조절하는 광유전학 기술인 ‘Opto-vTrap(옵토-브이트랩)’을 개발했다. 나아가 동물실험을 통해 뇌 활성 뿐 아니라 활동과 감정까지 조절할 수 있음을 확인했다.
뇌 활성은 신경세포와 신경교세포와 같은 뇌세포들이 서로 신호를 주고받으며 조절된다. 이 같은 상호작용은 뇌 세포 내 ‘소낭’안에 담긴 신경전달물질 분비를 통해 이루어진다. 소낭이 뇌 활성을 조절하는 사령관인 셈이다. 뇌 활성 조절은 뇌 연구를 위한 필수 기술이다. 뇌의 특정 부위나 세포의 활성을 촉진 및 억제해보면 특정 뇌 부위가 담당하는 기능, 여러 뇌 부위 간 상호작용의 역할, 특정 상황에서 다양한 뇌세포의 기능 등 특정 상황에서 뇌 작동이 어떠한 원리로 일어나는지 밝힐 수 있기 때문이다.
그러나 기존 뇌 활성 조절 기술은 원하는 시점에 특정 뇌세포의 활성을 자유롭게 조절하기 어려웠다. 지금까지는 세포 전위차 조절 방식을 사용하였는데, 이는 주변 환경의 산성도를 변화시키거나 원하지 않는 다른 자극을 유발할 뿐만 아니라 전위차에 반응하지 않는 세포에는 사용하지 못하는 한계가 있었다. 이번에 개발한 Opto-vTrap 기술은 세포 소낭을 직접 특이적으로 조절할 수 있어 원하는 시점에 다양한 종류의 뇌세포에서 이용이 가능하다.
연구진은 신경전달물질 분비를 직접 조절하고자 세포에 빛을 쪼이면 순간적으로 내부에 올가미처럼 트랩을 만드는 자체 개발 원천기술을 응용, 소낭에 적용했다. Opto-vTrap을 발현하는 세포나 조직에 빛(청색광)을 가하면 소낭 내 광수용체 단백질들이 엉겨 붙으며 소낭이 트랩 안에 포획되고 신경전달물질 분비가 억제된다. 요컨대 Opto-vTrap으로 소낭의 신호전달물질 분비를 직접 제어하여 뇌 활성을 자유롭게 조절하는 것이다. 연구진은 세포와 조직실험에서 나아가 Opto-vTrap 바이러스를 이용한 동물실험을 통해 뇌세포 신호전달 뿐만 아니라 기억·감정·행동도 조절 가능함을 확인하였다.
Opto-vTrap을 이용하면 뇌의 여러 부위간 복합적 상호작용 원리를 밝히고, 뇌세포 형태별 뇌 기능에 미치는 영향을 연구하는 데 유용하게 활용될 것으로 기대된다.
허원도 교수는 “Opto-vTrap은 신경세포와 신경교세포 모두에 잘 작동되기에 향후 다양한 뇌과학 연구 분야에 이용되리라 기대한다” 며 “앞으로 본 기술을 활용하여 특정 뇌세포의 시공간적 기능 연구를 진행하고자 한다.”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 중견연구과제 및 KAIST 글로벌 특이점 연구사업의 지원을 받아 수행됐다.
이번 연구 결과는 뇌 과학 학술지 뉴런 (Neuron, IF:17.173) 에 12월 1일(수) 1시(한국시간) 게재됐다.
2021.12.03
조회수 10237
-
 악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
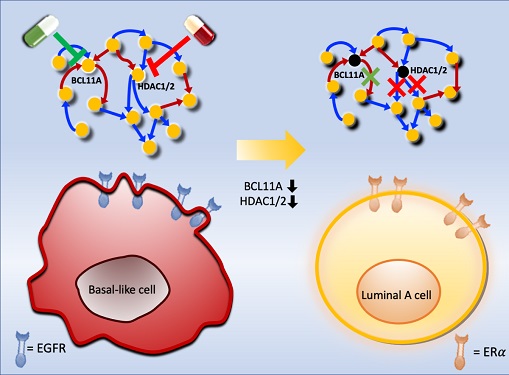
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30
조회수 12588
-
 건강한 장수를 유도하는 돌연변이 유전자 발굴
우리 대학 생명과학과 노화분자유전학 실험실 이승재 교수 연구팀이 가늘고 길게 사는 돌연변이체에 종양 억제 유전자 `PTEN'의 특정 돌연변이를 도입해 건강한 장수를 유도할 수 있다는 연구결과를 발표했다고 6일 밝혔다.
초고령화 사회에 도입한 우리나라의 가장 시급한 문제 중 하나는 단순히 수명을 늘리는 것이 아닌 건강하게 장수하는 방법을 개발하는 것이다. 노화가 건강에 부정적인 영향을 미치기 시작하기 전 시기를 건강 수명이라고 하며, 최근 노화 연구의 주요 목표 중 하나는 건강 수명을 늘리는 것이다.
인슐린 및 인슐린 유사 성장인자는 진화적으로 잘 보존이 된 수명 조절 호르몬인데, 이의 적절한 감소는 수명을 늘리지만 건강 수명(운동성, 성장, 생식능력, 발달 등)은 오히려 악화시킨다.
이승재 교수 연구팀은 노화 연구에서 많이 사용되고 수명이 3주 정도로 짧은 예쁜꼬마선충을 이용해 인슐린과 인슐린 유사 성장인자가 감소된 상황에서 종양 억제 유전자인 PTEN의 유전자 서열 하나만 바꾸면 장수와 건강을 모두 얻을 수 있음을 발견했다.
연구진이 발굴한 변이는 탈인산화 효소인 PTEN 단백질의 기능 중 지질 탈인산화 효소 활성은 감소시키지만, 단백질 탈인산화 효소 활성은 일부를 유지하는 방식으로 장수는 감소시키지 않으면서 건강은 유지하도록 생명체의 기능을 재조정했다.
그 결과, 장수 조절 유도인자인 FOXO의 활성은 유지하지만 과자극 시 건강에 해로운 전사인자인 NRF2의 활성을 적절히 억제해 긴 수명과 노화된 개체에서의 건강을 모두 획득했다.
연구팀은 이번 연구를 통해 장수 유도 신호전달 경로에서 효소 하나의 활성을 세심하게 조정해 장수 유지뿐 아니라 건강 수명을 늘릴 수 있다는 매우 획기적인 가능성을 제시했다.
특히, 인간을 비롯한 포유류에도 보존이 잘 돼 있는 종양 억제 유전자 PTEN이 건강한 장수유도에 중요하다는 것을 보여줬기에, PTEN 활성의 적절한 조절을 통해 인간의 건강 장수를 유도해 초고령화 사회의 문제 해소 가능성을 제시한 것에 의의가 있다.
생명과학과 박혜은 학생, 함석진 박사, 김은아 박사와 POSTECH 황우선 박사가 공동 제1 저자로 참여한 이번 연구는 한국연구재단 리더연구과제의 지원을 받아 수행됐으며 세계적인 과학 국제학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 2021년 9월 24일 날짜로 게재됐다.
(논문명: A PTEN variant uncouples longevity from impaired fitness in Caenorhabditis elegans with reduced insulin/IGF-1 signaling)
건강한 장수를 유도하는 돌연변이 유전자 발굴
우리 대학 생명과학과 노화분자유전학 실험실 이승재 교수 연구팀이 가늘고 길게 사는 돌연변이체에 종양 억제 유전자 `PTEN'의 특정 돌연변이를 도입해 건강한 장수를 유도할 수 있다는 연구결과를 발표했다고 6일 밝혔다.
초고령화 사회에 도입한 우리나라의 가장 시급한 문제 중 하나는 단순히 수명을 늘리는 것이 아닌 건강하게 장수하는 방법을 개발하는 것이다. 노화가 건강에 부정적인 영향을 미치기 시작하기 전 시기를 건강 수명이라고 하며, 최근 노화 연구의 주요 목표 중 하나는 건강 수명을 늘리는 것이다.
인슐린 및 인슐린 유사 성장인자는 진화적으로 잘 보존이 된 수명 조절 호르몬인데, 이의 적절한 감소는 수명을 늘리지만 건강 수명(운동성, 성장, 생식능력, 발달 등)은 오히려 악화시킨다.
이승재 교수 연구팀은 노화 연구에서 많이 사용되고 수명이 3주 정도로 짧은 예쁜꼬마선충을 이용해 인슐린과 인슐린 유사 성장인자가 감소된 상황에서 종양 억제 유전자인 PTEN의 유전자 서열 하나만 바꾸면 장수와 건강을 모두 얻을 수 있음을 발견했다.
연구진이 발굴한 변이는 탈인산화 효소인 PTEN 단백질의 기능 중 지질 탈인산화 효소 활성은 감소시키지만, 단백질 탈인산화 효소 활성은 일부를 유지하는 방식으로 장수는 감소시키지 않으면서 건강은 유지하도록 생명체의 기능을 재조정했다.
그 결과, 장수 조절 유도인자인 FOXO의 활성은 유지하지만 과자극 시 건강에 해로운 전사인자인 NRF2의 활성을 적절히 억제해 긴 수명과 노화된 개체에서의 건강을 모두 획득했다.
연구팀은 이번 연구를 통해 장수 유도 신호전달 경로에서 효소 하나의 활성을 세심하게 조정해 장수 유지뿐 아니라 건강 수명을 늘릴 수 있다는 매우 획기적인 가능성을 제시했다.
특히, 인간을 비롯한 포유류에도 보존이 잘 돼 있는 종양 억제 유전자 PTEN이 건강한 장수유도에 중요하다는 것을 보여줬기에, PTEN 활성의 적절한 조절을 통해 인간의 건강 장수를 유도해 초고령화 사회의 문제 해소 가능성을 제시한 것에 의의가 있다.
생명과학과 박혜은 학생, 함석진 박사, 김은아 박사와 POSTECH 황우선 박사가 공동 제1 저자로 참여한 이번 연구는 한국연구재단 리더연구과제의 지원을 받아 수행됐으며 세계적인 과학 국제학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 2021년 9월 24일 날짜로 게재됐다.
(논문명: A PTEN variant uncouples longevity from impaired fitness in Caenorhabditis elegans with reduced insulin/IGF-1 signaling)
2021.10.06
조회수 11926
-
 우수한 소재를 설계하는 딥러닝 방법론 개발
우리 대학 기계공학과 유승화 교수 연구팀이 능동-전이 학습 (active-transfer learning)과 데이터 증강기법(Data augmentation)에 기반해, 심층신경망 초기 훈련에 쓰인 소재들과 형태와 조합이 매우 다른 우수한 특성을 지닌 소재를 효율적으로 탐색하고 설계하는 방법론을 개발했다고 16일 밝혔다.
인공신경망에 기반해 방대한 설계 공간에서 새로운 소재를 찾기 위한 역설계 연구는 최근 매우 활발하게 진행되고 있다. 하지만 이러한 기존 설계 방식은 목표로 하는 소재의 형태와 조합이 심층신경망 훈련에 활용된 소재들과 매우 다를 때 인공신경망이 가지는 낮은 예측능력으로 인해 극히 많은 수의 소재 데이터 검증이 요구되며, 이에 따라 제한적으로만 활용이 가능하다.
연구팀은 이번 연구에서 이를 극복하기 위해 초기 훈련 데이터 영역에서 벗어나 우수한 소재를 효율적으로 탐색할 수 있는 인공신경망 기반 전진 설계 (Forward design) 방법론을 제안했다. 이 방법론은, <그림 1>에 도시된 바와 같이 유전 알고리즘과 결합된 능동-전이 학습 및 데이터 증강기법을 통해 심층신경망을 점진적으로 업데이트함으로써, 초기 훈련데이터를 벗어난 영역에서 심층신경망의 낮은 예측능력을 적은 숫자의 데이터 검증 및 추가로 보완한다.
유전 알고리즘에 의해 제안되는 우수 소재 후보군은 기보유한 소재 데이터를 조합해 도출하기 때문에 심층신경망의 신뢰할 수 있는 예측 영역과 설계 공간 측면에서 상대적으로 가까워 예측정확도가 유지된다. 이 후보군과 능동-전이 학습을 활용해 점진적으로 심층신경망의 신뢰성 있는 예측 범위를 확장하면, 초기 훈련데이터 영역 밖에서도 적은 데이터를 생성해 효율적인 설계 과정이 가능하다.
이번 방법은 천문학적인 수의 설계 구성을 가지는 그리드 복합소재 최적화 문제에 적용해 검증했으며, 이를 통해 전체 가능한 복합재 구조의 1029분의 1 가량인 10만 개의 복합재들만 초기 훈련 데이터로 활용해 심층신경망을 학습한 후, 이후 약 500개에 미치지 못하는 데이터 검증을 통해 초기 훈련에 쓰인 복합재와 매우 다른 구조를 가지고 우수한 특성을 지닌 복합재 구조를 설계할 수 있음을 보였다.
연구진이 개발한 방법론은 국소 최적점(Local optima)에 수렴하는 문제를 완화하면서도 인공신경망의 신뢰할 수 있는 예측 영역을 점진적으로 확장하는 효율적인 방법을 제공하기 때문에, 큰 설계 공간을 다루는 다양한 분야의 최적화 문제에 적용할 수 있을 것으로 기대되며, 특히 설계에 요구되는 데이터 검증의 숫자가 적기 때문에 데이터 생성에 시간이 오래 걸리고 비용이 많이 드는 설계 문제에서 이 방법론이 크게 활용될 수 있을 것으로 기대된다.
이번 연구는 공동 제 1저자 김용태 박사과정, 김영수 박사(한국기계연구원) 주도하에 진행됐으며, 유승화 교수(우리 대학 기계공학과)가 교신저자로 참여해, 국제학술지인 `npj 컴퓨테이셔널 머터리얼(Computational Material, IF:12.241)'에 `Deep Learning Framework for Material Design Space Exploration using Active Transfer Learning and Data Augmentation' 라는 제목으로 게재됐다.
이번 연구는 한국연구재단의 중견 연구자지원사업(3D 프린팅 복합재의 최적설계기법 및 피로수명 예측기법 개발)과 미래소재 디스커버리 사업 (레이저-물질 상호작용 멀티스케일 모델링을 통한 분자디자인), KAIST 글로벌 특이점 프렙 사업의 지원을 통해 수행됐다.
우수한 소재를 설계하는 딥러닝 방법론 개발
우리 대학 기계공학과 유승화 교수 연구팀이 능동-전이 학습 (active-transfer learning)과 데이터 증강기법(Data augmentation)에 기반해, 심층신경망 초기 훈련에 쓰인 소재들과 형태와 조합이 매우 다른 우수한 특성을 지닌 소재를 효율적으로 탐색하고 설계하는 방법론을 개발했다고 16일 밝혔다.
인공신경망에 기반해 방대한 설계 공간에서 새로운 소재를 찾기 위한 역설계 연구는 최근 매우 활발하게 진행되고 있다. 하지만 이러한 기존 설계 방식은 목표로 하는 소재의 형태와 조합이 심층신경망 훈련에 활용된 소재들과 매우 다를 때 인공신경망이 가지는 낮은 예측능력으로 인해 극히 많은 수의 소재 데이터 검증이 요구되며, 이에 따라 제한적으로만 활용이 가능하다.
연구팀은 이번 연구에서 이를 극복하기 위해 초기 훈련 데이터 영역에서 벗어나 우수한 소재를 효율적으로 탐색할 수 있는 인공신경망 기반 전진 설계 (Forward design) 방법론을 제안했다. 이 방법론은, <그림 1>에 도시된 바와 같이 유전 알고리즘과 결합된 능동-전이 학습 및 데이터 증강기법을 통해 심층신경망을 점진적으로 업데이트함으로써, 초기 훈련데이터를 벗어난 영역에서 심층신경망의 낮은 예측능력을 적은 숫자의 데이터 검증 및 추가로 보완한다.
유전 알고리즘에 의해 제안되는 우수 소재 후보군은 기보유한 소재 데이터를 조합해 도출하기 때문에 심층신경망의 신뢰할 수 있는 예측 영역과 설계 공간 측면에서 상대적으로 가까워 예측정확도가 유지된다. 이 후보군과 능동-전이 학습을 활용해 점진적으로 심층신경망의 신뢰성 있는 예측 범위를 확장하면, 초기 훈련데이터 영역 밖에서도 적은 데이터를 생성해 효율적인 설계 과정이 가능하다.
이번 방법은 천문학적인 수의 설계 구성을 가지는 그리드 복합소재 최적화 문제에 적용해 검증했으며, 이를 통해 전체 가능한 복합재 구조의 1029분의 1 가량인 10만 개의 복합재들만 초기 훈련 데이터로 활용해 심층신경망을 학습한 후, 이후 약 500개에 미치지 못하는 데이터 검증을 통해 초기 훈련에 쓰인 복합재와 매우 다른 구조를 가지고 우수한 특성을 지닌 복합재 구조를 설계할 수 있음을 보였다.
연구진이 개발한 방법론은 국소 최적점(Local optima)에 수렴하는 문제를 완화하면서도 인공신경망의 신뢰할 수 있는 예측 영역을 점진적으로 확장하는 효율적인 방법을 제공하기 때문에, 큰 설계 공간을 다루는 다양한 분야의 최적화 문제에 적용할 수 있을 것으로 기대되며, 특히 설계에 요구되는 데이터 검증의 숫자가 적기 때문에 데이터 생성에 시간이 오래 걸리고 비용이 많이 드는 설계 문제에서 이 방법론이 크게 활용될 수 있을 것으로 기대된다.
이번 연구는 공동 제 1저자 김용태 박사과정, 김영수 박사(한국기계연구원) 주도하에 진행됐으며, 유승화 교수(우리 대학 기계공학과)가 교신저자로 참여해, 국제학술지인 `npj 컴퓨테이셔널 머터리얼(Computational Material, IF:12.241)'에 `Deep Learning Framework for Material Design Space Exploration using Active Transfer Learning and Data Augmentation' 라는 제목으로 게재됐다.
이번 연구는 한국연구재단의 중견 연구자지원사업(3D 프린팅 복합재의 최적설계기법 및 피로수명 예측기법 개발)과 미래소재 디스커버리 사업 (레이저-물질 상호작용 멀티스케일 모델링을 통한 분자디자인), KAIST 글로벌 특이점 프렙 사업의 지원을 통해 수행됐다.
2021.09.16
조회수 12820
-
 유전체 기술 기반 인간 배아 발생과정 추적 성공
우리 대학 의과학대학원 주영석 교수 연구팀이 경북대학교 의과대학 해부학 교실 오지원 교수팀과 공동연구를 통해 전장 유전체 기술을 이용해 인간 발생과정을 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 인간 배아에 존재하는 소수의 세포들이 인체에 존재하는 총 40조 개의 세포를 어떻게 구성하고 각각의 장기로 언제 분화하는지 체계적으로 이해하기 위한 것으로 현존하는 세계 최대 규모의 결과다.
이번 연구는 초기 발생과정에서 각각의 세포에 자발적으로 발생하는 DNA 돌연변이를 대규모로 추적함으로써 배아의 파괴 없이 발생 과정 추적이 이뤄졌다. 연구팀은 단 하나의 세포(수정란)으로부터 복잡한 인체가 만들어지는 과정 동안 발생하는 돌연변이들과 세포들의 움직임을 고해상도로 재구성했으며, 이는 향후 발생과정의 이상으로 발병하는 희귀난치병을 이해하는데 기여할 것으로 기대된다.
우리 대학 박성열 박사(現 ㈜ 지놈인사이트 수석과학자), 경북대 의과대학 난다 말리(Nanda Mali) 박사, 우리 대학 김률 박사(現 삼성서울병원 내과 전임의)가 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처(Nature)' 8월 25일 字 온라인판에 게재됐다. (논문명 : Clonal dynamics in early human embryogenesis inferred from somatic mutation) 또한, 한국과학기술정보연구원(KISTI), 가톨릭의대, ㈜ 지놈인사이트, 이뮨스퀘어㈜ 의 연구자들도 함께 참여했다.
단 하나의 수정란이 인체의 다양한 장기를 만들어내는 인간 발생과정의 원리를 밝히는 것은 의생명과학의 근본적 물음이었다. 하지만 직접적인 연구를 위해서는 필연적으로 배아의 파괴를 동반하기 때문에 그동안 대부분의 배아발생 연구는 예쁜꼬마선충 (C. elegans), 초파리, 생쥐 등 모델 동물을 이용해 이뤄졌다. 특히 예쁜꼬마선충의 배아 발생과정 연구는 2002년 노벨생리의학상의 영예를 안겨주기도 하였다. 하지만 종 간의 차이로 이들로부터 인간의 발생과정을 근본적으로 이해하는 데는 한계가 있었다.
이를 극복하기 위해 공동연구팀은 DNA 돌연변이에 주목했다. 수정란이 세포 분열을 하는 과정에서 무작위적 돌연변이가 매 세포에 누적되는 것을 발견했다. 이렇게 발생한 돌연변이는 성체의 자손 세포에게도 전달되기 때문에, 전신에 분포한 단일세포의 DNA 돌연변이를 체계적으로 분석한다면 이들을 세포의 바코드로 삼아 배아 세포들의 움직임을 재구성해낼 수 있다는 결론을 얻었다. 이를 바탕으로, 7명의 시신 기증자에서 총 334개의 단일세포 및 379개의 조직을 기증받아 세계 최대 규모의 단일세포 전장유전체 분석을 수행했다.
이번 연구로부터 연구팀은 인간 배아 발생과정에 발생하는 현상들을 규명하는 데 성공했다. 그리고 배아 내 세포들이 발생 초기부터 서로 동등하지 않다는 것을 발견했다. 예를 들어 2세포기의 두 세포 중 한 세포가 다른 세포에 비해 더 항상 더 많은 자손 세포를 남기는 것으로 나타났다. 하지만 그 비율은 사람마다 달라서 사람의 발생과정이 개인 간 변동성이 높다는 사실을 확인했다.
또한 초기 배아 세포들이 각각의 장기 특이적인 세포로 분화하기 시작하는 시점도 특정할 수 있었다. 수정 후 3일 내, 매우 이른 시기의 배아에서도 (2세포-16세포기) 인체의 좌-우 조직에 대한 배아 세포의 비대칭적 분포가 나타나기 시작했으며, 이어서 3배엽 분화에 대한 비대칭성, 각 조직 및 장기에 대한 비대칭성이 차례로 형성되는 것을 확인했다.
연구팀의 이번 연구는 전장 유전체 빅데이터를 이용하여 윤리적인 문제 없이 인간의 초기 배아 발생 과정 추적이 가능하다는 것을 명쾌하게 증명해냈다는 데 의의가 있다. 이를 응용하면 개개인마다 발생과정 중 나타나는 세포들의 움직임을 재구성할 수 있게 된다. 이번 기술은 향후 발생 과정에서 생기는 희귀질환의 예방, 선별검사 및 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
경북대학교 의과대학 오지원 교수는 "죽음에 이른 신체로부터 인간 생명의 첫 순간을 규명할 수 있다는 것을 보여준 놀라운 연구ˮ라며 "숭고한 희생정신으로 본인의 신체를 기증한 분들이 없었다면 이번 연구는 불가능하였을 것ˮ이라고 말했다.
우리 대학 의과학대학원 주영석 교수는 "인간 게놈 프로젝트 완성 20년 만에 단일세포 유전체에 존재하는 돌연변이를 정확히 규명할 수 있을 만큼 발전한 유전체 기술의 쾌거ˮ라며 "기술 혁신을 기반으로 향후 지속적으로 더 높은 해상도의 인간 배아 발생과정 추적이 가능할 것ˮ이라고 말했다.
한편 이번 연구는 보건복지부 세계선도의과학자 육성사업, 서경배 과학재단 및 한국연구재단(리더과제, 우수신진연구, 지역대학우수과학자, 선도연구센터)의 지원을 받아 수행됐다.
유전체 기술 기반 인간 배아 발생과정 추적 성공
우리 대학 의과학대학원 주영석 교수 연구팀이 경북대학교 의과대학 해부학 교실 오지원 교수팀과 공동연구를 통해 전장 유전체 기술을 이용해 인간 발생과정을 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 인간 배아에 존재하는 소수의 세포들이 인체에 존재하는 총 40조 개의 세포를 어떻게 구성하고 각각의 장기로 언제 분화하는지 체계적으로 이해하기 위한 것으로 현존하는 세계 최대 규모의 결과다.
이번 연구는 초기 발생과정에서 각각의 세포에 자발적으로 발생하는 DNA 돌연변이를 대규모로 추적함으로써 배아의 파괴 없이 발생 과정 추적이 이뤄졌다. 연구팀은 단 하나의 세포(수정란)으로부터 복잡한 인체가 만들어지는 과정 동안 발생하는 돌연변이들과 세포들의 움직임을 고해상도로 재구성했으며, 이는 향후 발생과정의 이상으로 발병하는 희귀난치병을 이해하는데 기여할 것으로 기대된다.
우리 대학 박성열 박사(現 ㈜ 지놈인사이트 수석과학자), 경북대 의과대학 난다 말리(Nanda Mali) 박사, 우리 대학 김률 박사(現 삼성서울병원 내과 전임의)가 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처(Nature)' 8월 25일 字 온라인판에 게재됐다. (논문명 : Clonal dynamics in early human embryogenesis inferred from somatic mutation) 또한, 한국과학기술정보연구원(KISTI), 가톨릭의대, ㈜ 지놈인사이트, 이뮨스퀘어㈜ 의 연구자들도 함께 참여했다.
단 하나의 수정란이 인체의 다양한 장기를 만들어내는 인간 발생과정의 원리를 밝히는 것은 의생명과학의 근본적 물음이었다. 하지만 직접적인 연구를 위해서는 필연적으로 배아의 파괴를 동반하기 때문에 그동안 대부분의 배아발생 연구는 예쁜꼬마선충 (C. elegans), 초파리, 생쥐 등 모델 동물을 이용해 이뤄졌다. 특히 예쁜꼬마선충의 배아 발생과정 연구는 2002년 노벨생리의학상의 영예를 안겨주기도 하였다. 하지만 종 간의 차이로 이들로부터 인간의 발생과정을 근본적으로 이해하는 데는 한계가 있었다.
이를 극복하기 위해 공동연구팀은 DNA 돌연변이에 주목했다. 수정란이 세포 분열을 하는 과정에서 무작위적 돌연변이가 매 세포에 누적되는 것을 발견했다. 이렇게 발생한 돌연변이는 성체의 자손 세포에게도 전달되기 때문에, 전신에 분포한 단일세포의 DNA 돌연변이를 체계적으로 분석한다면 이들을 세포의 바코드로 삼아 배아 세포들의 움직임을 재구성해낼 수 있다는 결론을 얻었다. 이를 바탕으로, 7명의 시신 기증자에서 총 334개의 단일세포 및 379개의 조직을 기증받아 세계 최대 규모의 단일세포 전장유전체 분석을 수행했다.
이번 연구로부터 연구팀은 인간 배아 발생과정에 발생하는 현상들을 규명하는 데 성공했다. 그리고 배아 내 세포들이 발생 초기부터 서로 동등하지 않다는 것을 발견했다. 예를 들어 2세포기의 두 세포 중 한 세포가 다른 세포에 비해 더 항상 더 많은 자손 세포를 남기는 것으로 나타났다. 하지만 그 비율은 사람마다 달라서 사람의 발생과정이 개인 간 변동성이 높다는 사실을 확인했다.
또한 초기 배아 세포들이 각각의 장기 특이적인 세포로 분화하기 시작하는 시점도 특정할 수 있었다. 수정 후 3일 내, 매우 이른 시기의 배아에서도 (2세포-16세포기) 인체의 좌-우 조직에 대한 배아 세포의 비대칭적 분포가 나타나기 시작했으며, 이어서 3배엽 분화에 대한 비대칭성, 각 조직 및 장기에 대한 비대칭성이 차례로 형성되는 것을 확인했다.
연구팀의 이번 연구는 전장 유전체 빅데이터를 이용하여 윤리적인 문제 없이 인간의 초기 배아 발생 과정 추적이 가능하다는 것을 명쾌하게 증명해냈다는 데 의의가 있다. 이를 응용하면 개개인마다 발생과정 중 나타나는 세포들의 움직임을 재구성할 수 있게 된다. 이번 기술은 향후 발생 과정에서 생기는 희귀질환의 예방, 선별검사 및 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
경북대학교 의과대학 오지원 교수는 "죽음에 이른 신체로부터 인간 생명의 첫 순간을 규명할 수 있다는 것을 보여준 놀라운 연구ˮ라며 "숭고한 희생정신으로 본인의 신체를 기증한 분들이 없었다면 이번 연구는 불가능하였을 것ˮ이라고 말했다.
우리 대학 의과학대학원 주영석 교수는 "인간 게놈 프로젝트 완성 20년 만에 단일세포 유전체에 존재하는 돌연변이를 정확히 규명할 수 있을 만큼 발전한 유전체 기술의 쾌거ˮ라며 "기술 혁신을 기반으로 향후 지속적으로 더 높은 해상도의 인간 배아 발생과정 추적이 가능할 것ˮ이라고 말했다.
한편 이번 연구는 보건복지부 세계선도의과학자 육성사업, 서경배 과학재단 및 한국연구재단(리더과제, 우수신진연구, 지역대학우수과학자, 선도연구센터)의 지원을 받아 수행됐다.
2021.08.26
조회수 12839
-
 시각 정보가 행동으로 변환되는 신경회로 규명
우리 대학 생명과학과 이승희 교수 연구팀이 시각 정보를 인식해 목표 지향적 행동을 결정하는 대뇌 전두엽의 신경회로 기전을 새롭게 규명했다고 26일 밝혔다.
이 교수 연구팀은 시각 피질과 상호 작용하는 전측 대상회(전대상) 피질(Anterior cingulate cortex, ACC)의 억제성 신경회로가 동물이 시각 정보를 인식하고 이에 맞는 정확한 행동을 개시하는 데 중요한 역할을 함을 밝혔다. 연구 결과는 포유류 전두엽 전대상 피질의 신경회로가 어떻게 시각 인지 행동 및 충동적 행동을 제어할 수 있는지를 새롭게 규명해, 주의력결핍과잉행동장애(ADHD)와 같은 인지장애 및 충동성을 주 증상으로 하는 뇌질환 치료에 적용될 수 있을 것으로 기대된다.
생명과학과 김재현 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 뉴로사이언스 (Nature Neuroscience, IF 20.071)' 8월 19일 字 온라인판에 게재됐다. (논문명 : Gated feedforward inhibition in the frontal cortex releases goal-directed action)
우리는 외부 환경에서 유입되는 다양한 감각 정보를 인지해 상황에 맞는 행동을 수행한다. 한 예로, 운전할 때 신호등 앞에서 빨간색 신호를 보면 출발하지 않고 멈춰야 하며, 초록색 신호로 바뀌면 출발하게 된다. 이처럼 시각 정보를 인식하고 이에 맞는 운동 행동을 결정하기 위해 우리 뇌는 받아들인 감각 정보를 적절한 운동 정보로 변환해야 하는데, 이 교수 연구팀은 이것이 전대상 피질의 억제성 회로에 의해 이루어짐을 밝혔다.
연구팀은 뇌가 받아들인 시각 정보를 어떻게 운동 정보로 전달하는지 규명하기 위해, 시각 자극을 보면 물을 핥고 그렇지 않으면 물 핥기를 멈추는 목표 지향적 행동을 학습시킨 생쥐의 전대상 피질에 고밀도 실리콘 전극을 삽입해 생체 내 신경 신호를 측정 및 분석했다. 그 결과, 전두엽 전대상 피질 내에서 시각 피질로부터 정보를 받는 시각 반응성 신경세포들이 주변의 세포들을 억제할 경우 생쥐가 운동을 개시할 수 있음을 밝혔다.
또한, 약물적 방법을 이용해 전대상 피질의 활성 정도를 낮추게 되면 생쥐는 시각 자극이 주어지지 않았음에도 불구하고 충동적으로 목표 지향적 행위를 지속하는 비정상적인 행동 양상을 보였다. 이를 통해 전대상 피질은 정상적인 감각-운동 변환 과정에서도 핵심적인 기능을 수행할 뿐 아니라, 시각 정보가 없을 때 운동 개시를 멈추고 기다려야 하는 충동 조절에도 중요한 역할을 하고 있음을 밝혔다.
이 교수 연구팀은 바이러스 추적자, 광유전학, 다채널 전극 레코딩과 같은 신경과학 최첨단 실험 기법을 활용해 전대상 피질 내의 신경세포 타입과 회로가 어떠한 방식으로 시각 정보를 목표 지향적 운동 행위로 변환하는지에 대한 신경 메커니즘 원리를 최초로 규명했다.
전대상 피질에는 시각 정보에 반응하는 시각 반응성 신경세포, 운동 개시를 억제하는 운동 억제성 신경세포, 그리고 시각 정보와 운동 개시에 반응하지 않는 나머지 신경세포들이 존재함을 확인했다. 그리고 이와 같은 세 종류의 뉴런들의 신경 활성도는 생쥐가 시각 정보를 인지하여 행동을 개시하는 반응 속도와 유의미한 상관관계가 있음을 규명했다.
특히, 광유전학적(optognetics) 방법을 이용한 실험에서, 전대상 피질의 시각 반응성 뉴런들은 시각 피질로부터 신경 정보를 직접 전달받음을 확인했고, 광 자극으로 해당 신경 회로를 활성화할 때 시각 자극이 없어도 생쥐의 목표 지향적 행동을 유발할 수 있음을 증명했다.
이승희 교수는 "이번 연구 결과는 주의력결핍과잉행동장애 및 조현병과 같은 질병에서 전대상 피질이 정상적으로 작동하지 못할 때 나타나는 행동 장애를 치료하기 위한 정밀한 신경회로 타겟을 제시했다ˮ라고 말했다.
한편, 이번 연구는 한국 연구재단 및 KAIST 글로벌 특이점 프로그램의 지원을 통해 수행됐다.
시각 정보가 행동으로 변환되는 신경회로 규명
우리 대학 생명과학과 이승희 교수 연구팀이 시각 정보를 인식해 목표 지향적 행동을 결정하는 대뇌 전두엽의 신경회로 기전을 새롭게 규명했다고 26일 밝혔다.
이 교수 연구팀은 시각 피질과 상호 작용하는 전측 대상회(전대상) 피질(Anterior cingulate cortex, ACC)의 억제성 신경회로가 동물이 시각 정보를 인식하고 이에 맞는 정확한 행동을 개시하는 데 중요한 역할을 함을 밝혔다. 연구 결과는 포유류 전두엽 전대상 피질의 신경회로가 어떻게 시각 인지 행동 및 충동적 행동을 제어할 수 있는지를 새롭게 규명해, 주의력결핍과잉행동장애(ADHD)와 같은 인지장애 및 충동성을 주 증상으로 하는 뇌질환 치료에 적용될 수 있을 것으로 기대된다.
생명과학과 김재현 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 뉴로사이언스 (Nature Neuroscience, IF 20.071)' 8월 19일 字 온라인판에 게재됐다. (논문명 : Gated feedforward inhibition in the frontal cortex releases goal-directed action)
우리는 외부 환경에서 유입되는 다양한 감각 정보를 인지해 상황에 맞는 행동을 수행한다. 한 예로, 운전할 때 신호등 앞에서 빨간색 신호를 보면 출발하지 않고 멈춰야 하며, 초록색 신호로 바뀌면 출발하게 된다. 이처럼 시각 정보를 인식하고 이에 맞는 운동 행동을 결정하기 위해 우리 뇌는 받아들인 감각 정보를 적절한 운동 정보로 변환해야 하는데, 이 교수 연구팀은 이것이 전대상 피질의 억제성 회로에 의해 이루어짐을 밝혔다.
연구팀은 뇌가 받아들인 시각 정보를 어떻게 운동 정보로 전달하는지 규명하기 위해, 시각 자극을 보면 물을 핥고 그렇지 않으면 물 핥기를 멈추는 목표 지향적 행동을 학습시킨 생쥐의 전대상 피질에 고밀도 실리콘 전극을 삽입해 생체 내 신경 신호를 측정 및 분석했다. 그 결과, 전두엽 전대상 피질 내에서 시각 피질로부터 정보를 받는 시각 반응성 신경세포들이 주변의 세포들을 억제할 경우 생쥐가 운동을 개시할 수 있음을 밝혔다.
또한, 약물적 방법을 이용해 전대상 피질의 활성 정도를 낮추게 되면 생쥐는 시각 자극이 주어지지 않았음에도 불구하고 충동적으로 목표 지향적 행위를 지속하는 비정상적인 행동 양상을 보였다. 이를 통해 전대상 피질은 정상적인 감각-운동 변환 과정에서도 핵심적인 기능을 수행할 뿐 아니라, 시각 정보가 없을 때 운동 개시를 멈추고 기다려야 하는 충동 조절에도 중요한 역할을 하고 있음을 밝혔다.
이 교수 연구팀은 바이러스 추적자, 광유전학, 다채널 전극 레코딩과 같은 신경과학 최첨단 실험 기법을 활용해 전대상 피질 내의 신경세포 타입과 회로가 어떠한 방식으로 시각 정보를 목표 지향적 운동 행위로 변환하는지에 대한 신경 메커니즘 원리를 최초로 규명했다.
전대상 피질에는 시각 정보에 반응하는 시각 반응성 신경세포, 운동 개시를 억제하는 운동 억제성 신경세포, 그리고 시각 정보와 운동 개시에 반응하지 않는 나머지 신경세포들이 존재함을 확인했다. 그리고 이와 같은 세 종류의 뉴런들의 신경 활성도는 생쥐가 시각 정보를 인지하여 행동을 개시하는 반응 속도와 유의미한 상관관계가 있음을 규명했다.
특히, 광유전학적(optognetics) 방법을 이용한 실험에서, 전대상 피질의 시각 반응성 뉴런들은 시각 피질로부터 신경 정보를 직접 전달받음을 확인했고, 광 자극으로 해당 신경 회로를 활성화할 때 시각 자극이 없어도 생쥐의 목표 지향적 행동을 유발할 수 있음을 증명했다.
이승희 교수는 "이번 연구 결과는 주의력결핍과잉행동장애 및 조현병과 같은 질병에서 전대상 피질이 정상적으로 작동하지 못할 때 나타나는 행동 장애를 치료하기 위한 정밀한 신경회로 타겟을 제시했다ˮ라고 말했다.
한편, 이번 연구는 한국 연구재단 및 KAIST 글로벌 특이점 프로그램의 지원을 통해 수행됐다.
2021.08.26
조회수 13732
-
 3개 학과 공동연구팀, 다학제적 접근 통해 뇌전증 발병 기전 규명
우리 대학 의과학대학원 이정호 교수, 바이오및뇌공학과 백세범 교수, 생명과학과 손종우 교수 공동 연구팀이 MTOR 유전자 돌연변이에 의해 약물 저항성이 높은 뇌전증이 발병하는 메커니즘을 규명했다고 25일 밝혔다.
이번 연구 결과는 극소수의 신경세포에 발생한 돌연변이가 신경망의 과다 활동(hyperactivity) 상태로 이어지는 구체적인 메커니즘을 밝혀, 뇌전증의 발병 원인 및 치료법 개발에 대한 새로운 시각을 제공한다.
특히 3개 학과간 공동 연구팀의 다학제적인 접근을 통해 세포 내 유전학적인 관점에서부터 단일 신경세포의 전기생리학, 이로부터 근접한 거리에 있는 뇌조직의 네트워크, 그리고 뇌 전체 수준에서의 신경망 수준으로 이어지는 다양한 실험 및 시뮬레이션 연구가 이루어져, 뇌전증의 복잡한 발병 메커니즘을 전반적으로 설명하는 성과를 얻었다.
국소피질 이형성증은 대뇌발달 과정에서 일부 신경줄기세포의 mTOR 경로상의 체성유전변이(MTOR, TSC, DEPDC5) 로 발생하는 질환으로, 흔한 뇌전증의 원인 중 하나이며 항뇌전증제 약물 치료에 잘 반응하지 않아 치료가 어렵다. 이에 연구팀은 국소피질 이형성증 환자의 실제 조직과 같은 질환을 가진 동물 모델을 이용한 실험을 통해, 개별 신경세포의 체성유전변이가 신경망 수준의 발작도로 이어지는 구체적인 원리를 규명했다.
먼저 연구팀은 이러한 체성유전변이는 뇌 조직의 5% 이하인 적은 수의 신경세포에서 발생하며, 해당 신경세포들의 전기적 성질이 정상 세포와는 다르게 변화하는 것을 발견했다. 하지만 대다수 정상 세포를 포함한 전반적인 신경망 활동의 시뮬레이션 결과, 이러한 돌연변이는 매우 적은 비율의 신경세포에만 국한돼 있어, 이 세포들 자체의 전기적 성질 변화만으로는 전체 신경망의 비정상적인 활동으로 이어지지 않았고, 이로 인해 뇌전증에서 보이는 신경망 수준의 발작 활성도가 발생하는 이유를 설명할 수 없었다.
이에 연구팀은 후속 실험을 통해, 뇌전증 발작을 유도할 수 있는 활성도가 MTOR 체성 유전변이를 가진 신경세포가 아니라 그 세포들 주변의 변이가 없는 신경세포에 의해 발생하는 것을 발견했다. 이는 유전자 변이를 가진 신경세포의 활성도가 뇌전증의 직접적인 원인이 되는 것이 아니라, 이들 세포가 주변 대다수 비변이 신경세포에 특정 변화를 유도하고 이로 인해 전체 신경망 수준의 발작 활성도가 발생한다는 뜻으로, 뇌 체성유전변이로 인한 비세포 자율성 활성도(non-cell autonomous hyperexcitability)를 보여주는 한 예가 된다.
이에 착안해 추가적인 동물실험과 수술 후 환자 뇌 조직을 이용한 연구를 통해 MTOR 체성유전변이를 가진 세포에서는 ADK(adenosine kinase, 아데노신 키나제) 유전자가 과발현되는 것을 발견했다. 또한, 이로부터 주변 대다수 비변이 신경세포의 네트워크 체계가 교란돼 과활성도가 유도되고, 더 나아가 전체 신경망 수준의 과다 활동으로까지 이어지는 것을 확인했다.
의과학대학원 고현용 박사, 바이오및뇌공학과 장재선 박사, 생명과학과 주상현 학생이 공동 제1 저자로 참여한 이번 연구는 신경학 분야의 국제 학술지 `애널스 오브 뉴롤로지 (Annals of Neurology)' 7월 29일 字에 게재됐다. (논문명: Non-cell autonomous epileptogenesis in focal cortical dysplasia)
이정호, 백세범, 손종우 교수는 "약물 저항성이 높아 기존에 효과적으로 대처할 수 없었던 뇌전증의 발병 원인에 대해 한층 더 깊은 통찰을 제공하는 연구ˮ라며 "한 분야의 실험이나 연구 기법만으로는 해결하기 어려운 문제에 대해, 유전체학, 신경생물학, 계산뇌과학에 걸친 다학제적 접근으로 해결책을 제시한 효과적인 공동연구의 좋은 예시였다ˮ라고 언급했다.
한편 이번 연구는 한국연구재단 이공분야기초연구사업의 리더연구자지원사업 및 중견연구자지원사업, 보건복지부의 질환극복기술개발사업, 서경배 과학재단, 그리고 소바젠의 지원을 받아 수행됐다.
3개 학과 공동연구팀, 다학제적 접근 통해 뇌전증 발병 기전 규명
우리 대학 의과학대학원 이정호 교수, 바이오및뇌공학과 백세범 교수, 생명과학과 손종우 교수 공동 연구팀이 MTOR 유전자 돌연변이에 의해 약물 저항성이 높은 뇌전증이 발병하는 메커니즘을 규명했다고 25일 밝혔다.
이번 연구 결과는 극소수의 신경세포에 발생한 돌연변이가 신경망의 과다 활동(hyperactivity) 상태로 이어지는 구체적인 메커니즘을 밝혀, 뇌전증의 발병 원인 및 치료법 개발에 대한 새로운 시각을 제공한다.
특히 3개 학과간 공동 연구팀의 다학제적인 접근을 통해 세포 내 유전학적인 관점에서부터 단일 신경세포의 전기생리학, 이로부터 근접한 거리에 있는 뇌조직의 네트워크, 그리고 뇌 전체 수준에서의 신경망 수준으로 이어지는 다양한 실험 및 시뮬레이션 연구가 이루어져, 뇌전증의 복잡한 발병 메커니즘을 전반적으로 설명하는 성과를 얻었다.
국소피질 이형성증은 대뇌발달 과정에서 일부 신경줄기세포의 mTOR 경로상의 체성유전변이(MTOR, TSC, DEPDC5) 로 발생하는 질환으로, 흔한 뇌전증의 원인 중 하나이며 항뇌전증제 약물 치료에 잘 반응하지 않아 치료가 어렵다. 이에 연구팀은 국소피질 이형성증 환자의 실제 조직과 같은 질환을 가진 동물 모델을 이용한 실험을 통해, 개별 신경세포의 체성유전변이가 신경망 수준의 발작도로 이어지는 구체적인 원리를 규명했다.
먼저 연구팀은 이러한 체성유전변이는 뇌 조직의 5% 이하인 적은 수의 신경세포에서 발생하며, 해당 신경세포들의 전기적 성질이 정상 세포와는 다르게 변화하는 것을 발견했다. 하지만 대다수 정상 세포를 포함한 전반적인 신경망 활동의 시뮬레이션 결과, 이러한 돌연변이는 매우 적은 비율의 신경세포에만 국한돼 있어, 이 세포들 자체의 전기적 성질 변화만으로는 전체 신경망의 비정상적인 활동으로 이어지지 않았고, 이로 인해 뇌전증에서 보이는 신경망 수준의 발작 활성도가 발생하는 이유를 설명할 수 없었다.
이에 연구팀은 후속 실험을 통해, 뇌전증 발작을 유도할 수 있는 활성도가 MTOR 체성 유전변이를 가진 신경세포가 아니라 그 세포들 주변의 변이가 없는 신경세포에 의해 발생하는 것을 발견했다. 이는 유전자 변이를 가진 신경세포의 활성도가 뇌전증의 직접적인 원인이 되는 것이 아니라, 이들 세포가 주변 대다수 비변이 신경세포에 특정 변화를 유도하고 이로 인해 전체 신경망 수준의 발작 활성도가 발생한다는 뜻으로, 뇌 체성유전변이로 인한 비세포 자율성 활성도(non-cell autonomous hyperexcitability)를 보여주는 한 예가 된다.
이에 착안해 추가적인 동물실험과 수술 후 환자 뇌 조직을 이용한 연구를 통해 MTOR 체성유전변이를 가진 세포에서는 ADK(adenosine kinase, 아데노신 키나제) 유전자가 과발현되는 것을 발견했다. 또한, 이로부터 주변 대다수 비변이 신경세포의 네트워크 체계가 교란돼 과활성도가 유도되고, 더 나아가 전체 신경망 수준의 과다 활동으로까지 이어지는 것을 확인했다.
의과학대학원 고현용 박사, 바이오및뇌공학과 장재선 박사, 생명과학과 주상현 학생이 공동 제1 저자로 참여한 이번 연구는 신경학 분야의 국제 학술지 `애널스 오브 뉴롤로지 (Annals of Neurology)' 7월 29일 字에 게재됐다. (논문명: Non-cell autonomous epileptogenesis in focal cortical dysplasia)
이정호, 백세범, 손종우 교수는 "약물 저항성이 높아 기존에 효과적으로 대처할 수 없었던 뇌전증의 발병 원인에 대해 한층 더 깊은 통찰을 제공하는 연구ˮ라며 "한 분야의 실험이나 연구 기법만으로는 해결하기 어려운 문제에 대해, 유전체학, 신경생물학, 계산뇌과학에 걸친 다학제적 접근으로 해결책을 제시한 효과적인 공동연구의 좋은 예시였다ˮ라고 언급했다.
한편 이번 연구는 한국연구재단 이공분야기초연구사업의 리더연구자지원사업 및 중견연구자지원사업, 보건복지부의 질환극복기술개발사업, 서경배 과학재단, 그리고 소바젠의 지원을 받아 수행됐다.
2021.08.26
조회수 13348
 물리학 난제였던 유전율 텐서 측정 구현
우리 대학 물리학과 박용근 교수 연구팀이 기존에는 이론조차 존재하지 않았던 물리학 난제 중 하나인 유전율 텐서의 3차원 단층 촬영 방법을 개발했다고 4일 밝혔다.
유전율 텐서는 빛과 물질의 상호작용을 근본적으로 기술하는, 물질의 광학적 이방성(異方性, 방향에 따라 달라 보이는 특성)을 정량적으로 표현할 수 있는 중요한 물리량이다. 유전율은 고등학교 물리학에서도 다루는 기본적인 개념이지만, 지금까지 3차원 유전율 텐서를 실험적으로 측정할 수 있는 방법이 존재하지 않았다. 병리학, 재료과학, 연성물질 과학, 또는 디스플레이 등 다양한 분야에서 갖는 중요성에도 불구하고, 직접적으로 측정할 방법이 없다는 한계가 있었다. 현재까지도 3차원 광학적 이방성은 2차원 편광현미경 측정 및 시뮬레이션을 통해 부정확하게 추정할 수밖에 없다.
3차원 유전율 텐서의 측정은 물리학, 광학 분야의 오래된 난제 중 하나였다. 1967년 광학적 이방성을 무시하고 유전율 텐서를 3차원 굴절률 수치로 단순화하여 측정하는 기술이 발명돼 지난 50여 년간 빠르게 성장하고 상용화까지 성공했지만, 여전히 3차원 유전율 텐서를 측정하는 방법은 개발되지 못했다.
여태껏 이 문제가 풀리지 못했던 까닭은, 3개의 고유치를 가지는 유전율 텐서를 측정하기에는 빛의 편광 방향 자유도가 2개로 제한되기 때문이다.
재료과학 분야 최고 권위지인 `네이처 머티리얼즈(Nature Materials, IF 43.84)'에 3일 발표된 이번 연구(논문명: Tomographic measurements of dielectric tensors at optical frequency)에서 연구팀은 이러한 한계를 극복하고 광학적 이방성 구조의 3차원 유전율 텐서 단층 촬영 이론을 개발해 구현하는 데 성공했다.
기존의 고정관념에서 벗어나, 빛의 방향을 살짝 틀어주어 중첩된 정보를 활용하면, 편광 방향 자유도를 3개로 늘려서 유전율 텐서의 3개 고유치를 모두 구할 수 있다는 점에 착안한 것이 연구진의 핵심 아이디어다. 이렇게 3개의 편광 자유도를 제어하는 것과 동시에, 병원에서 사용하는 엑스레이, 컴퓨터단층(CT) 촬영처럼, 여러 각도에서 광학적 이방성 구조를 홀로그래피 현미경을 개발하여 촬영함으로써 3차원 유전율 텐서를 직접적으로 측정했다.
연구팀은 개발된 방법을 이용해 뒤틀린 네마틱 (twisted nematic) 액정과 같은 잘 알려진 3차원 광학적 이방체의 3차원 유전율 텐서를 성공적으로 측정함으로써 기술의 구현을 입증했다. 더 나아가 열적 비평형 상태로 성장-소멸-융합하는 액정 동역학, 반복되는 위상학적 특이점 구조의 액정 네트워크 등 기존의 방법들로 추정하기 어려웠던 3차원 유전율 텐서를 실험적으로 최초 측정하는 성과를 거뒀다.
제1 저자인 물리학과 신승우 박사는 "지금까지 직접 볼 수 없던 유전율 텐서를 실제로 측정할 수 있는 방법론을 처음으로 개발한 것이 큰 의미ˮ라며 "액정, 카이랄 물질, 암조직과 같은 병리 조직 내부의 콜라겐 파이버 등과 같은 광학적 방향성을 보이는 다양한 물질들의 3차원 구조를 정량적이고 비침습적으로 직접 관측할 수 있기에 여러 분야에 범용적, 필수적으로 사용할 수 있는 도구로 기대한다ˮ라고 말했다.
이번 연구는 박용근 교수 연구팀의 기술 개발 이외에도 다학제적 접근을 통해 결실을 볼 수 있었다. UNIST 물리학과 정준우 교수, 우리 대학 생명화학공학과 김신현 교수, 우리 대학 화학과 윤동기 교수 연구팀들이 오랜 기간 발전시켜온 액정 구조체 제작 기술 덕분에, 다양한 액정 구조체를 통해 기술의 실험적 검증을 효과적으로 진행할 수 있었다.
한편 이번 연구는 과학기술정보통신부의 정보통신기획평가원, 한국연구재단 창의연구사업 및 G-CORE 사업의 지원을 받아 수행됐다.
2022.03.04 조회수 11923
물리학 난제였던 유전율 텐서 측정 구현
우리 대학 물리학과 박용근 교수 연구팀이 기존에는 이론조차 존재하지 않았던 물리학 난제 중 하나인 유전율 텐서의 3차원 단층 촬영 방법을 개발했다고 4일 밝혔다.
유전율 텐서는 빛과 물질의 상호작용을 근본적으로 기술하는, 물질의 광학적 이방성(異方性, 방향에 따라 달라 보이는 특성)을 정량적으로 표현할 수 있는 중요한 물리량이다. 유전율은 고등학교 물리학에서도 다루는 기본적인 개념이지만, 지금까지 3차원 유전율 텐서를 실험적으로 측정할 수 있는 방법이 존재하지 않았다. 병리학, 재료과학, 연성물질 과학, 또는 디스플레이 등 다양한 분야에서 갖는 중요성에도 불구하고, 직접적으로 측정할 방법이 없다는 한계가 있었다. 현재까지도 3차원 광학적 이방성은 2차원 편광현미경 측정 및 시뮬레이션을 통해 부정확하게 추정할 수밖에 없다.
3차원 유전율 텐서의 측정은 물리학, 광학 분야의 오래된 난제 중 하나였다. 1967년 광학적 이방성을 무시하고 유전율 텐서를 3차원 굴절률 수치로 단순화하여 측정하는 기술이 발명돼 지난 50여 년간 빠르게 성장하고 상용화까지 성공했지만, 여전히 3차원 유전율 텐서를 측정하는 방법은 개발되지 못했다.
여태껏 이 문제가 풀리지 못했던 까닭은, 3개의 고유치를 가지는 유전율 텐서를 측정하기에는 빛의 편광 방향 자유도가 2개로 제한되기 때문이다.
재료과학 분야 최고 권위지인 `네이처 머티리얼즈(Nature Materials, IF 43.84)'에 3일 발표된 이번 연구(논문명: Tomographic measurements of dielectric tensors at optical frequency)에서 연구팀은 이러한 한계를 극복하고 광학적 이방성 구조의 3차원 유전율 텐서 단층 촬영 이론을 개발해 구현하는 데 성공했다.
기존의 고정관념에서 벗어나, 빛의 방향을 살짝 틀어주어 중첩된 정보를 활용하면, 편광 방향 자유도를 3개로 늘려서 유전율 텐서의 3개 고유치를 모두 구할 수 있다는 점에 착안한 것이 연구진의 핵심 아이디어다. 이렇게 3개의 편광 자유도를 제어하는 것과 동시에, 병원에서 사용하는 엑스레이, 컴퓨터단층(CT) 촬영처럼, 여러 각도에서 광학적 이방성 구조를 홀로그래피 현미경을 개발하여 촬영함으로써 3차원 유전율 텐서를 직접적으로 측정했다.
연구팀은 개발된 방법을 이용해 뒤틀린 네마틱 (twisted nematic) 액정과 같은 잘 알려진 3차원 광학적 이방체의 3차원 유전율 텐서를 성공적으로 측정함으로써 기술의 구현을 입증했다. 더 나아가 열적 비평형 상태로 성장-소멸-융합하는 액정 동역학, 반복되는 위상학적 특이점 구조의 액정 네트워크 등 기존의 방법들로 추정하기 어려웠던 3차원 유전율 텐서를 실험적으로 최초 측정하는 성과를 거뒀다.
제1 저자인 물리학과 신승우 박사는 "지금까지 직접 볼 수 없던 유전율 텐서를 실제로 측정할 수 있는 방법론을 처음으로 개발한 것이 큰 의미ˮ라며 "액정, 카이랄 물질, 암조직과 같은 병리 조직 내부의 콜라겐 파이버 등과 같은 광학적 방향성을 보이는 다양한 물질들의 3차원 구조를 정량적이고 비침습적으로 직접 관측할 수 있기에 여러 분야에 범용적, 필수적으로 사용할 수 있는 도구로 기대한다ˮ라고 말했다.
이번 연구는 박용근 교수 연구팀의 기술 개발 이외에도 다학제적 접근을 통해 결실을 볼 수 있었다. UNIST 물리학과 정준우 교수, 우리 대학 생명화학공학과 김신현 교수, 우리 대학 화학과 윤동기 교수 연구팀들이 오랜 기간 발전시켜온 액정 구조체 제작 기술 덕분에, 다양한 액정 구조체를 통해 기술의 실험적 검증을 효과적으로 진행할 수 있었다.
한편 이번 연구는 과학기술정보통신부의 정보통신기획평가원, 한국연구재단 창의연구사업 및 G-CORE 사업의 지원을 받아 수행됐다.
2022.03.04 조회수 11923 생각만으로 정확하게 로봇팔 조종이 가능한 뇌-기계 인터페이스 개발
우리 대학 바이오및뇌공학과 정재승 교수 연구팀이 3차원 공간상에서 생각만으로 로봇팔을 높은 정확도 (90.9~92.6%)로 조종하는 `뇌-기계 인터페이스 시스템'을 개발했다고 23일 밝혔다.
정 교수 연구팀은 인공지능과 유전자 알고리즘을 사용해 인간의 대뇌 심부에서 측정한 뇌파만으로 팔 움직임의 의도를 파악해 로봇팔을 제어하는 새로운 형태의 뇌-기계 인터페이스 시스템을 개발했다. 뇌 활동만으로 사람의 의도를 파악해 로봇이나 기계가 대신 행동에 옮기는 `뇌-기계 인터페이스' 기술은 최근 급속도로 발전하고 있다. 하지만 손을 움직이는 정도의 의도 파악을 넘어, 팔 움직임의 방향에 대한 의도를 섬세하게 파악해 정교하게 로봇팔을 움직이는 기술은 아직 정확도가 높지 않았다.
하지만 연구팀은 이번 연구에서 조종 `방향'에 대한 의도를 뇌 활동만으로 인식하는 인공지능 모델을 개발했고, 그 결과 3차원 공간상에서 24개의 방향을 90% 이상의 정확도로 정교하게 해석하는 시스템을 개발했다.
게다가 딥러닝 등 기존 기계학습 기술은 높은 사양의 GPU 하드웨어가 필요했지만, 이번 연구에서는 축적 컴퓨팅(Reservoir Computing) 기법을 이용해 낮은 사양의 하드웨어에서도 인공지능 학습이 가능하여 스마트 모바일 기기에서도 폭넓게 응용될 수 있도록 개발해, 향후 메타버스와 스마트 기기에도 폭넓게 적용이 가능할 것으로 기대된다.
우리 대학 김훈희 박사(現 강남대 조교수)가 제1 저자로 참여한 이번 연구는 국제학술지 `어플라이드 소프트 컴퓨팅(Applied Soft Computing)' 2022년 117권 3월호에 출판됐다. (논문명 : An electrocorticographic decoder for arm movement for brain-machine interface using an echo state network and Gaussian readout).
뇌-기계 인터페이스는 사용자의 뇌 활동을 통해 의도를 읽고 로봇이나 기계에 전달하는 기술로서 로봇, 드론, 컴퓨터뿐만 아니라 스마트 모바일 기기, 메타버스 등에서의 이용될 차세대 인터페이스 기술로 각광받고 있다.
특히 기존의 인터페이스가 외부 신체 기관을 통해 명령을 간접 전달(버튼, 터치, 제스처 등)해야 하지만 뇌-기계 인터페이스는 명령을 뇌로부터 직접적 전달한다는 점에서 가장 진보된 인터페이스 기술로 여겨진다.
그러나 뇌파는 개개인의 차이가 매우 크고, 단일 신경 세포로부터 정확한 신호를 읽는 것이 아니라 넓은 영역에 있는 신경 세포 집단의 전기적 신호 특성을 해석해야 하므로 잡음이 크다는 한계점을 가지고 있다.
연구팀은 이러한 문제 해결을 위해 최첨단 인공지능 기법의 하나인 `축적 컴퓨팅 기법'을 이용해 뇌-기계 인터페이스에서 필요한 개개인의 뇌파 신호의 중요 특성을 인공신경망이 자동으로 학습해 찾을 수 있도록 구현했다.
또한 유전자 알고리즘(Genetic Algorithm)을 이용해 인공지능 신경망이 최적의 뇌파 특성을 효율적으로 찾을 수 있게 시스템을 설계했다. 연구팀은 심부 뇌파를 최종 해석하는 리드아웃(Readout)을 가우시안(Gaussian) 모델로 설계해 시각피질 신경 세포가 방향을 표현하는 방법을 모방하는 인공신경망을 개발했다. 이런 리드아웃 방식은 축적 컴퓨팅의 선형 학습 알고리즘을 이용해 일반적 사양의 간단한 하드웨어에서도 빠르게 학습할 수 있어 메타버스, 스마트기기 등 일상생활에서 응용이 가능해진다.
특히, 이번 연구에서 만들어진 뇌-기계 인터페이스 인공지능 모델은 3차원상에서 24가지 방향 즉, 각 차원에서 8가지 방향을 디코딩할 수 있으며 모든 방향에서 평균 90% 이상의 정확도 (90.9%~92.6% 범위)를 보였다. 또한 연구된 뇌-기계 인터페이스는 3차원 공간상에서 로봇팔을 움직이는 상상을 할 때의 뇌파를 해석해 성공적으로 로봇팔을 움직이는 시뮬레이션 결과를 보였다.
인공지능 시스템을 만든 제1 저자인 김훈희 박사는 "공학적인 신호처리 기법에 의존해 온 기존 뇌파 디코딩 방법과는 달리, 인간 뇌의 실제 작동 구조를 모방한 인공신경망을 개발해 좀더 발전된 형태의 뇌-기계 인터페이스 시스템을 개발해 기쁘다ˮ면서 "향후 뇌의 특성을 좀 더 구체적으로 이용한 `뇌 모방 인공지능(Brain-inspired A.I.)'을 이용한 다양한 뇌-기계 인터페이스를 개발할 계획이다ˮ라고 말했다.
이번 연구를 주도한 연구책임자 정재승 교수는 "뇌파를 통해 생각만으로 로봇팔을 구동하는 `뇌-기계 인터페이스 시스템'들이 대부분 고사양 하드웨어가 필요해 실시간 응용으로 나아가기 어렵고 스마트기기 등으로 적용이 어려웠다. 그러나 이번 시스템은 90%~92%의 높은 정확도를 가진 의도 인식 인공지능 시스템을 만들어 메타버스 안에서 아바타를 생각대로 움직이게 하거나 앱을 생각만으로 컨트롤하는 스마트기기 등에 광범위하게 사용될 수 있다ˮ고 말했다.
이번 연구 결과는 사지마비 환자나 사고로 팔을 잃은 환자들을 위한 로봇팔 장착 및 제어 기술부터, 메타버스, 스마트기기, 게임, 엔터테인먼트 애플리케이션 등 다양한 시스템에 뇌-기계 인터페이스를 적용할 가능성을 열어 줄 것으로 기대된다.
이번 연구는 한국연구재단 뇌 원천기술개발사업의 지원을 받아 수행됐다.
2022.02.24 조회수 16000
생각만으로 정확하게 로봇팔 조종이 가능한 뇌-기계 인터페이스 개발
우리 대학 바이오및뇌공학과 정재승 교수 연구팀이 3차원 공간상에서 생각만으로 로봇팔을 높은 정확도 (90.9~92.6%)로 조종하는 `뇌-기계 인터페이스 시스템'을 개발했다고 23일 밝혔다.
정 교수 연구팀은 인공지능과 유전자 알고리즘을 사용해 인간의 대뇌 심부에서 측정한 뇌파만으로 팔 움직임의 의도를 파악해 로봇팔을 제어하는 새로운 형태의 뇌-기계 인터페이스 시스템을 개발했다. 뇌 활동만으로 사람의 의도를 파악해 로봇이나 기계가 대신 행동에 옮기는 `뇌-기계 인터페이스' 기술은 최근 급속도로 발전하고 있다. 하지만 손을 움직이는 정도의 의도 파악을 넘어, 팔 움직임의 방향에 대한 의도를 섬세하게 파악해 정교하게 로봇팔을 움직이는 기술은 아직 정확도가 높지 않았다.
하지만 연구팀은 이번 연구에서 조종 `방향'에 대한 의도를 뇌 활동만으로 인식하는 인공지능 모델을 개발했고, 그 결과 3차원 공간상에서 24개의 방향을 90% 이상의 정확도로 정교하게 해석하는 시스템을 개발했다.
게다가 딥러닝 등 기존 기계학습 기술은 높은 사양의 GPU 하드웨어가 필요했지만, 이번 연구에서는 축적 컴퓨팅(Reservoir Computing) 기법을 이용해 낮은 사양의 하드웨어에서도 인공지능 학습이 가능하여 스마트 모바일 기기에서도 폭넓게 응용될 수 있도록 개발해, 향후 메타버스와 스마트 기기에도 폭넓게 적용이 가능할 것으로 기대된다.
우리 대학 김훈희 박사(現 강남대 조교수)가 제1 저자로 참여한 이번 연구는 국제학술지 `어플라이드 소프트 컴퓨팅(Applied Soft Computing)' 2022년 117권 3월호에 출판됐다. (논문명 : An electrocorticographic decoder for arm movement for brain-machine interface using an echo state network and Gaussian readout).
뇌-기계 인터페이스는 사용자의 뇌 활동을 통해 의도를 읽고 로봇이나 기계에 전달하는 기술로서 로봇, 드론, 컴퓨터뿐만 아니라 스마트 모바일 기기, 메타버스 등에서의 이용될 차세대 인터페이스 기술로 각광받고 있다.
특히 기존의 인터페이스가 외부 신체 기관을 통해 명령을 간접 전달(버튼, 터치, 제스처 등)해야 하지만 뇌-기계 인터페이스는 명령을 뇌로부터 직접적 전달한다는 점에서 가장 진보된 인터페이스 기술로 여겨진다.
그러나 뇌파는 개개인의 차이가 매우 크고, 단일 신경 세포로부터 정확한 신호를 읽는 것이 아니라 넓은 영역에 있는 신경 세포 집단의 전기적 신호 특성을 해석해야 하므로 잡음이 크다는 한계점을 가지고 있다.
연구팀은 이러한 문제 해결을 위해 최첨단 인공지능 기법의 하나인 `축적 컴퓨팅 기법'을 이용해 뇌-기계 인터페이스에서 필요한 개개인의 뇌파 신호의 중요 특성을 인공신경망이 자동으로 학습해 찾을 수 있도록 구현했다.
또한 유전자 알고리즘(Genetic Algorithm)을 이용해 인공지능 신경망이 최적의 뇌파 특성을 효율적으로 찾을 수 있게 시스템을 설계했다. 연구팀은 심부 뇌파를 최종 해석하는 리드아웃(Readout)을 가우시안(Gaussian) 모델로 설계해 시각피질 신경 세포가 방향을 표현하는 방법을 모방하는 인공신경망을 개발했다. 이런 리드아웃 방식은 축적 컴퓨팅의 선형 학습 알고리즘을 이용해 일반적 사양의 간단한 하드웨어에서도 빠르게 학습할 수 있어 메타버스, 스마트기기 등 일상생활에서 응용이 가능해진다.
특히, 이번 연구에서 만들어진 뇌-기계 인터페이스 인공지능 모델은 3차원상에서 24가지 방향 즉, 각 차원에서 8가지 방향을 디코딩할 수 있으며 모든 방향에서 평균 90% 이상의 정확도 (90.9%~92.6% 범위)를 보였다. 또한 연구된 뇌-기계 인터페이스는 3차원 공간상에서 로봇팔을 움직이는 상상을 할 때의 뇌파를 해석해 성공적으로 로봇팔을 움직이는 시뮬레이션 결과를 보였다.
인공지능 시스템을 만든 제1 저자인 김훈희 박사는 "공학적인 신호처리 기법에 의존해 온 기존 뇌파 디코딩 방법과는 달리, 인간 뇌의 실제 작동 구조를 모방한 인공신경망을 개발해 좀더 발전된 형태의 뇌-기계 인터페이스 시스템을 개발해 기쁘다ˮ면서 "향후 뇌의 특성을 좀 더 구체적으로 이용한 `뇌 모방 인공지능(Brain-inspired A.I.)'을 이용한 다양한 뇌-기계 인터페이스를 개발할 계획이다ˮ라고 말했다.
이번 연구를 주도한 연구책임자 정재승 교수는 "뇌파를 통해 생각만으로 로봇팔을 구동하는 `뇌-기계 인터페이스 시스템'들이 대부분 고사양 하드웨어가 필요해 실시간 응용으로 나아가기 어렵고 스마트기기 등으로 적용이 어려웠다. 그러나 이번 시스템은 90%~92%의 높은 정확도를 가진 의도 인식 인공지능 시스템을 만들어 메타버스 안에서 아바타를 생각대로 움직이게 하거나 앱을 생각만으로 컨트롤하는 스마트기기 등에 광범위하게 사용될 수 있다ˮ고 말했다.
이번 연구 결과는 사지마비 환자나 사고로 팔을 잃은 환자들을 위한 로봇팔 장착 및 제어 기술부터, 메타버스, 스마트기기, 게임, 엔터테인먼트 애플리케이션 등 다양한 시스템에 뇌-기계 인터페이스를 적용할 가능성을 열어 줄 것으로 기대된다.
이번 연구는 한국연구재단 뇌 원천기술개발사업의 지원을 받아 수행됐다.
2022.02.24 조회수 16000 단일세포 RNA 시퀀싱을 통한 꽃향기 합성 유전자 발굴
우리 대학 생명과학과 김상규 교수 연구팀이 꽃향기 합성 유전자를 발굴하기 위해 꽃잎 단일세포 RNA 시퀀싱 기술을 개발하고 벤질아세톤(benzylacetone) 꽃향기 합성 경로를 밝혔다.
벤질아세톤은 코요테담배(Nicotiana attenuata) 꽃에서 합성되고 밤에 분비가 되는 향기 물질이다. 이 향기물질은 밤에 활동하는 박각시나방을 유인한다. 그리고 꽃은 꿀을 제공하고 그 대가로 나방은 화분pollen을 멀리 날라준다. 또한 벤질아세톤은 코요테담배 꽃을 먹는 해충을 쫓아내는 기능을 하고 있다. 생태적으로 재미있는 기능을 하고 있는 물질이지만 생합성 경로에 대해서는 완전히 알려진 상태가 아니었다.
일반적으로 식물이 만들어내는 대사물질의 생합성 유전자를 밝히기 위해 사용하는 방법의 단점을 극복하기 위해서 꽃잎 단일세포에서 발현되는 유전자의 연관도를 이용하여 물질대사 경로를 밝힐 수 있다는 것을 이번 연구를 통해서 증명하였다. 특히 유전정보가 제한적으로 알려져 있고 다양한 생태형 ecotype을 가진 식물 집단이 없어도 비모델 식물에서 물질합성 경로에 있는 효소와 그 효소의 발현을 조절하는 전사인자 등도 찾을 수 있는 가능성을 제시하였다.
단일세포 RNA 시퀀싱의 장점을 활용하여 향기합성 유전자가 만들어지는 세포를 구별하고 꽃잎에서 향기가 합성되는 위치도 밝힐 수 있었다.
우리 대학 생명과학과 강문영 석박사통합과정 학생이 제1 저자로 참여한 이번 연구 결과는 'New Phytologist' 학술지에 게재됐다. (관련 논문명: Single-cell RNA-sequencing of Nicotiana attenuata corolla cells reveals the biosynthetic pathway of a floral scent)
한편 이번 연구는 삼성미래기술육성사업과 포스코사이언스펠로십 지원을 받아 수행됐다.
2022.02.14 조회수 8659
단일세포 RNA 시퀀싱을 통한 꽃향기 합성 유전자 발굴
우리 대학 생명과학과 김상규 교수 연구팀이 꽃향기 합성 유전자를 발굴하기 위해 꽃잎 단일세포 RNA 시퀀싱 기술을 개발하고 벤질아세톤(benzylacetone) 꽃향기 합성 경로를 밝혔다.
벤질아세톤은 코요테담배(Nicotiana attenuata) 꽃에서 합성되고 밤에 분비가 되는 향기 물질이다. 이 향기물질은 밤에 활동하는 박각시나방을 유인한다. 그리고 꽃은 꿀을 제공하고 그 대가로 나방은 화분pollen을 멀리 날라준다. 또한 벤질아세톤은 코요테담배 꽃을 먹는 해충을 쫓아내는 기능을 하고 있다. 생태적으로 재미있는 기능을 하고 있는 물질이지만 생합성 경로에 대해서는 완전히 알려진 상태가 아니었다.
일반적으로 식물이 만들어내는 대사물질의 생합성 유전자를 밝히기 위해 사용하는 방법의 단점을 극복하기 위해서 꽃잎 단일세포에서 발현되는 유전자의 연관도를 이용하여 물질대사 경로를 밝힐 수 있다는 것을 이번 연구를 통해서 증명하였다. 특히 유전정보가 제한적으로 알려져 있고 다양한 생태형 ecotype을 가진 식물 집단이 없어도 비모델 식물에서 물질합성 경로에 있는 효소와 그 효소의 발현을 조절하는 전사인자 등도 찾을 수 있는 가능성을 제시하였다.
단일세포 RNA 시퀀싱의 장점을 활용하여 향기합성 유전자가 만들어지는 세포를 구별하고 꽃잎에서 향기가 합성되는 위치도 밝힐 수 있었다.
우리 대학 생명과학과 강문영 석박사통합과정 학생이 제1 저자로 참여한 이번 연구 결과는 'New Phytologist' 학술지에 게재됐다. (관련 논문명: Single-cell RNA-sequencing of Nicotiana attenuata corolla cells reveals the biosynthetic pathway of a floral scent)
한편 이번 연구는 삼성미래기술육성사업과 포스코사이언스펠로십 지원을 받아 수행됐다.
2022.02.14 조회수 8659 유전자 가위로 생체 내 정밀한 유전자 교정에 의한 면역 항암 치료
CRISPR/Cas9 시스템을 이용하여 유전자교정을 일으킴으로써 암의 면역 치료를 유도하는 기술이 우리 대학 연구진에 의해 개발됐다.
우리 대학 생명과학과 정현정 교수, 서울대학교 의과학과 정기훈 교수 공동연구팀이 CRISPR/Cas9 리보핵산단백질을 생체 내에 효과적으로 전달하는 나노복합체를 개발하여 면역 관문 유전자를 교정함으로써 항암 효과를 보이는데 성공했다고 밝혔다.
암은 현대인의 건강을 위협하는 대표적인 요인으로 꼽히고 있다. 암의 치료 방법 중 면역 항암 요법은 부작용이 적고 높은 치료 성적을 보여 다양한 암 유형에 적용할 수 있다. 기존에는 항체 기반 치료법이 주로 임상에서 사용되고 있으며 다양한 고형암의 치료에 승인되었으나, 일시적인 효과로 반복 투여가 필요하다.
CRISPR/Cas9 시스템은 유전체의 서열을 직접 정밀하게 교정할 수 있으며, DNA 이중가닥을 절단하는 Cas9 제한효소와 특정 서열을 표적하는 단일 가이드 RNA로 이루어진다. 유전자교정 치료제의 경우 일반적으로 바이러스 기반 치료 방법을 이용했으나 돌연변이 유발, 비특이적 표적 효과 등으로 인해 한계가 있다. 비바이러스 치료제로 Cas9 단백질 및 단일가닥 RNA를 이용하면 바이러스 치료보다 안전성을 높일 수 있으나 낮은 세포내 전달 효과로 치료 효능이 떨어진다. 전달 효율을 높이기 위해 기존에 다양한 방법이 개발되고 연구됐으나, 일반적으로 과량의 전달체물질을 사용함으로써 생체 내 독성 문제가 나타나는 한계점이 있다. 이러한 문제점을 개선하기 위해 연구팀은 Cas9 단백질에 세포내 유입을 촉진하는 고분자를 접합시켜 극미량의 전달체물질로 고효율 전달이 가능한 Cas9 컨쥬게이트를 제작하여 활용했다.
연구팀은 이러한 Cas9 컨쥬게이트, 단일 가이드 RNA 및 변형된 데옥시뉴클레오타이드(DNA)를 추가해 나노조립된 리보핵단백질 복합체(이하 NanoRNP)를 개발했다. 이 복합체는 Cas9 컨쥬게이트, RNA 및 DNA의 상호작용으로 쉽게 제작할 수 있고, 유전자 교정 치료제로써 단일 요법에 의해 항암 치료가 가능하다는 점이 장점이다.
우리 대학 생명과학과 석박사통합과정 이주희 학생이 제1 저자로 참여한 이번 연구 결과는 재료화학 분야 국제학술지 `케미스트리 오브 머티리얼즈(Chemistry of Materials)'에 12월 20일 字 온라인 게재됐다. (논문명 : Nano-assembly of a Chemically Tailored Cas9 Ribonucleoprotein for In Vivo Gene Editing and Cancer Immunotherapy)
NanoRNP의 경우 Cas9에 부착된 고분자가 강한 양이온성을 지녀 단일 가이드 RNA와 안정적으로 복합체를 형성시키며, 생체내 분해효소로부터 보호하여 활성을 향상시킨다. 본 연구팀은 NanoRNP를 피부암에서 많이 발현되는 프로그램된 세포사멸 리간드-1 (PD-L1) 유전자를 표적하는데 응용하였다. PD-L1은 면역 세포의 표면 수용체에 존재하는 프로그램된 세포사멸 수용체-1 (PD-1)과 상호작용하여 면역 세포의 반응을 억제해 암세포의 세포사멸 회피를 유도한다.
연구팀은 NanoRNP를 이용하여 PD-L1 유전자의 교정으로 유전자결손을 유도하여, 면역 세포들이 활성화되고 종양미세환경의 변화로 면역 세포에 의한 암세포 사멸이 유도됨을 확인했다.
연구팀은 이번 연구 결과를 응용해 향후 암 뿐만 아니라 유전 질환 등 다양한 질병에 적용함으로써 연구를 확대 및 발전시켜 나갈 수 있을 것으로 기대하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 범부처전주기의료기기연구개발사업 및 KAIST End Run 사업의 지원을 통해 이뤄졌다.
2021.12.24 조회수 12346
유전자 가위로 생체 내 정밀한 유전자 교정에 의한 면역 항암 치료
CRISPR/Cas9 시스템을 이용하여 유전자교정을 일으킴으로써 암의 면역 치료를 유도하는 기술이 우리 대학 연구진에 의해 개발됐다.
우리 대학 생명과학과 정현정 교수, 서울대학교 의과학과 정기훈 교수 공동연구팀이 CRISPR/Cas9 리보핵산단백질을 생체 내에 효과적으로 전달하는 나노복합체를 개발하여 면역 관문 유전자를 교정함으로써 항암 효과를 보이는데 성공했다고 밝혔다.
암은 현대인의 건강을 위협하는 대표적인 요인으로 꼽히고 있다. 암의 치료 방법 중 면역 항암 요법은 부작용이 적고 높은 치료 성적을 보여 다양한 암 유형에 적용할 수 있다. 기존에는 항체 기반 치료법이 주로 임상에서 사용되고 있으며 다양한 고형암의 치료에 승인되었으나, 일시적인 효과로 반복 투여가 필요하다.
CRISPR/Cas9 시스템은 유전체의 서열을 직접 정밀하게 교정할 수 있으며, DNA 이중가닥을 절단하는 Cas9 제한효소와 특정 서열을 표적하는 단일 가이드 RNA로 이루어진다. 유전자교정 치료제의 경우 일반적으로 바이러스 기반 치료 방법을 이용했으나 돌연변이 유발, 비특이적 표적 효과 등으로 인해 한계가 있다. 비바이러스 치료제로 Cas9 단백질 및 단일가닥 RNA를 이용하면 바이러스 치료보다 안전성을 높일 수 있으나 낮은 세포내 전달 효과로 치료 효능이 떨어진다. 전달 효율을 높이기 위해 기존에 다양한 방법이 개발되고 연구됐으나, 일반적으로 과량의 전달체물질을 사용함으로써 생체 내 독성 문제가 나타나는 한계점이 있다. 이러한 문제점을 개선하기 위해 연구팀은 Cas9 단백질에 세포내 유입을 촉진하는 고분자를 접합시켜 극미량의 전달체물질로 고효율 전달이 가능한 Cas9 컨쥬게이트를 제작하여 활용했다.
연구팀은 이러한 Cas9 컨쥬게이트, 단일 가이드 RNA 및 변형된 데옥시뉴클레오타이드(DNA)를 추가해 나노조립된 리보핵단백질 복합체(이하 NanoRNP)를 개발했다. 이 복합체는 Cas9 컨쥬게이트, RNA 및 DNA의 상호작용으로 쉽게 제작할 수 있고, 유전자 교정 치료제로써 단일 요법에 의해 항암 치료가 가능하다는 점이 장점이다.
우리 대학 생명과학과 석박사통합과정 이주희 학생이 제1 저자로 참여한 이번 연구 결과는 재료화학 분야 국제학술지 `케미스트리 오브 머티리얼즈(Chemistry of Materials)'에 12월 20일 字 온라인 게재됐다. (논문명 : Nano-assembly of a Chemically Tailored Cas9 Ribonucleoprotein for In Vivo Gene Editing and Cancer Immunotherapy)
NanoRNP의 경우 Cas9에 부착된 고분자가 강한 양이온성을 지녀 단일 가이드 RNA와 안정적으로 복합체를 형성시키며, 생체내 분해효소로부터 보호하여 활성을 향상시킨다. 본 연구팀은 NanoRNP를 피부암에서 많이 발현되는 프로그램된 세포사멸 리간드-1 (PD-L1) 유전자를 표적하는데 응용하였다. PD-L1은 면역 세포의 표면 수용체에 존재하는 프로그램된 세포사멸 수용체-1 (PD-1)과 상호작용하여 면역 세포의 반응을 억제해 암세포의 세포사멸 회피를 유도한다.
연구팀은 NanoRNP를 이용하여 PD-L1 유전자의 교정으로 유전자결손을 유도하여, 면역 세포들이 활성화되고 종양미세환경의 변화로 면역 세포에 의한 암세포 사멸이 유도됨을 확인했다.
연구팀은 이번 연구 결과를 응용해 향후 암 뿐만 아니라 유전 질환 등 다양한 질병에 적용함으로써 연구를 확대 및 발전시켜 나갈 수 있을 것으로 기대하고 있다.
한편 이번 연구는 한국연구재단 중견연구자지원사업, 범부처전주기의료기기연구개발사업 및 KAIST End Run 사업의 지원을 통해 이뤄졌다.
2021.12.24 조회수 12346 사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
2021.12.08 조회수 12561
사물인터넷 기반 다수의 뇌 신경회로 동시 원격제어 시스템 개발
우리 연구진이 인터넷을 이용해 뇌 신경회로를 원격 제어할 수 있는 무선 네트워크 기술을 개발했다. 이 기술을 활용하면 시간과 장소에 구애받지 않고 목표 동물의 뇌 신경회로를 정교하게 제어할 수 있다.
우리 대학 전기및전자공학부 정재웅 교수 연구팀이 미국 워싱턴 대학교(Washington University in St. Louis), 미국 콜로라도 대학교(University of Colorado Boulder) 연구팀과의 공동 연구를 통해 사물인터넷 기반의 뇌 신경회로 원격제어 시스템을 개발했다고 8일 밝혔다.
이번 개발 기술은 많은 시간과 인력이 있어야 하는 뇌 연구 및 다양한 신경과학 연구를 자동화시켜 다양한 퇴행성 뇌 질환과 정신질환의 발병 기전 규명과 치료법 개발의 가속화에 크게 기여할 것으로 기대된다. 또한, 먼 거리에 있는 환자의 질환을 원격으로 치료하는 원격 의료 구현에도 활용될 수 있을 것으로 예상된다.
우리 대학 전기및전자공학부 라자 콰지(Raza Qazi) 연구원과 김충연 박사과정, 그리고 워싱턴대 카일 파커(Kyle E. Parker) 연구원이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)' 11월 25일 字에 게재됐다. (논문명 : Scalable and modular wireless-network infrastructure for large-scale behavioural neuroscience)
전 세계적으로 고령화 시대에 접어드는 현 상황에서 알츠하이머병, 파킨슨병과 같은 뇌 질환들로 고통받는 환자 수가 급증하고 있다. 이에 따라 근본적인 뇌 질환 치료법을 개발하기 위해 뇌 기능 및 뇌 질환 발병기전을 규명하기 위한 뇌 연구가 매우 시급하지만, 뇌 연구의 진행 속도가 뇌 질환 환자의 증가 속도를 따라잡지 못하고 있어서 뇌 연구의 효율성을 극대화하기 위한 새로운 기술 개발이 절실히 요구된다.
기존 뇌 연구에 사용되던 대부분의 신경과학 장치들은 외부 장비와 선으로 연결된 유선 방식으로 구동됐지만, 이러한 방식은 피실험 동물들을 물리적으로 제약할 뿐 아니라 실험 진행자의 직접적인 개입이 불가피해 피실험 동물의 행동에 영향을 주는 `관찰자 효과'를 발생시켜서 정확한 뇌 연구 결과 도출을 어렵게 만든다. 아울러 모든 과정에서 실험자의 직접적인 조작이 요구돼 연구에 많은 시간과 인력, 비용이 발생하게 한다.
연구팀은 사물인터넷(Internet of Things; IoT) 기술을 접목해 다양한 다수의 뇌 이식용 기기들을 인터넷 원격으로 동시 제어하거나 예약된 스케줄에 따라 기기들이 자동으로 구동되도록 하는 무선 네트워크 시스템을 개발했다. 이를 통해 시간과 장소에 상관없이 목표 동물들의 특정 뇌 회로를 원격 제어하는 것을 가능하게 했다. 이 시스템은 사용자가 인터넷 웹사이트 기반의 무선 네트워크 플랫폼을 통해 뇌 이식용 장치의 원격제어, 자동화된 데이터 수집, 뇌 회로 제어 스케줄링 등의 다양한 기능을 손쉽게 구현할 수 있도록 설계됐다.
연구팀은 이 시스템의 뇌 신경회로 자동 원격제어 기능을 사용해 자체 제작한 무선 장치(뉴럴 임플란트)가 이식된 수십 마리의 쥐의 뇌 신경회로를 광유전학적 방법으로 사람의 개입 없이 정교하게 원격 자동 제어함으로써, 완전 자동화된 뇌 연구 실험에 적용 가능함을 입증했다. 이 실험을 통해 쥐의 먹이 섭취량, 활동량, 그리고 다른 쥐들과의 사회적 상호작용 빈도를 성공적으로 조절함으로써, 예약이 설정된 대로 다수 동물의 뇌 신경회로를 동시에 독립적으로 원격 제어할 수 있음을 보였다.
정 교수는 "개발된 원격제어 기술은 동물을 활용한 뇌 연구에 필요한 인간개입을 최소화함으로써 뇌 연구의 효율을 높이고 실험의 불확실성을 크게 줄일 수 있을 것ˮ이라며 "이 기술은 뇌 연구를 넘어, 많은 동물 실험을 필요로 하는 신약 개발, 병원 방문 없이 뇌 질환 및 다양한 질병을 치료하기 위한 원격 의료 구현에도 적용될 수 있을 것이다ˮ라고 말했다.
연구팀은 이 기술이 더욱 광범위하게 뇌 과학 연구 및 치료에 사용될 수 있게 하도록, 인공지능 기반의 실시간 뇌파 원격 모니터링 기술을 개발해 본 시스템과 접목하기 위한 연구를 계획하고 있다.
한편 이번 연구는 KAIST 글로벌 특이점 연구사업, 한국연구재단이 추진하는 중견연구자지원사업 및 바이오의료기술개발사업, 미국 국립보건원의 지원을 받아 수행됐다.
2021.12.08 조회수 12561 빛으로 뇌 기능, 행동, 감정을 자유롭게 조절한다
우리 대학 생명과학과 허원도 교수 연구팀은 빛으로 뇌 기능 및 행동을 자유자재로 조절하는 광유전학 기술인 ‘Opto-vTrap(옵토-브이트랩)’을 개발했다. 나아가 동물실험을 통해 뇌 활성 뿐 아니라 활동과 감정까지 조절할 수 있음을 확인했다.
뇌 활성은 신경세포와 신경교세포와 같은 뇌세포들이 서로 신호를 주고받으며 조절된다. 이 같은 상호작용은 뇌 세포 내 ‘소낭’안에 담긴 신경전달물질 분비를 통해 이루어진다. 소낭이 뇌 활성을 조절하는 사령관인 셈이다. 뇌 활성 조절은 뇌 연구를 위한 필수 기술이다. 뇌의 특정 부위나 세포의 활성을 촉진 및 억제해보면 특정 뇌 부위가 담당하는 기능, 여러 뇌 부위 간 상호작용의 역할, 특정 상황에서 다양한 뇌세포의 기능 등 특정 상황에서 뇌 작동이 어떠한 원리로 일어나는지 밝힐 수 있기 때문이다.
그러나 기존 뇌 활성 조절 기술은 원하는 시점에 특정 뇌세포의 활성을 자유롭게 조절하기 어려웠다. 지금까지는 세포 전위차 조절 방식을 사용하였는데, 이는 주변 환경의 산성도를 변화시키거나 원하지 않는 다른 자극을 유발할 뿐만 아니라 전위차에 반응하지 않는 세포에는 사용하지 못하는 한계가 있었다. 이번에 개발한 Opto-vTrap 기술은 세포 소낭을 직접 특이적으로 조절할 수 있어 원하는 시점에 다양한 종류의 뇌세포에서 이용이 가능하다.
연구진은 신경전달물질 분비를 직접 조절하고자 세포에 빛을 쪼이면 순간적으로 내부에 올가미처럼 트랩을 만드는 자체 개발 원천기술을 응용, 소낭에 적용했다. Opto-vTrap을 발현하는 세포나 조직에 빛(청색광)을 가하면 소낭 내 광수용체 단백질들이 엉겨 붙으며 소낭이 트랩 안에 포획되고 신경전달물질 분비가 억제된다. 요컨대 Opto-vTrap으로 소낭의 신호전달물질 분비를 직접 제어하여 뇌 활성을 자유롭게 조절하는 것이다. 연구진은 세포와 조직실험에서 나아가 Opto-vTrap 바이러스를 이용한 동물실험을 통해 뇌세포 신호전달 뿐만 아니라 기억·감정·행동도 조절 가능함을 확인하였다.
Opto-vTrap을 이용하면 뇌의 여러 부위간 복합적 상호작용 원리를 밝히고, 뇌세포 형태별 뇌 기능에 미치는 영향을 연구하는 데 유용하게 활용될 것으로 기대된다.
허원도 교수는 “Opto-vTrap은 신경세포와 신경교세포 모두에 잘 작동되기에 향후 다양한 뇌과학 연구 분야에 이용되리라 기대한다” 며 “앞으로 본 기술을 활용하여 특정 뇌세포의 시공간적 기능 연구를 진행하고자 한다.”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 중견연구과제 및 KAIST 글로벌 특이점 연구사업의 지원을 받아 수행됐다.
이번 연구 결과는 뇌 과학 학술지 뉴런 (Neuron, IF:17.173) 에 12월 1일(수) 1시(한국시간) 게재됐다.
2021.12.03 조회수 10237
빛으로 뇌 기능, 행동, 감정을 자유롭게 조절한다
우리 대학 생명과학과 허원도 교수 연구팀은 빛으로 뇌 기능 및 행동을 자유자재로 조절하는 광유전학 기술인 ‘Opto-vTrap(옵토-브이트랩)’을 개발했다. 나아가 동물실험을 통해 뇌 활성 뿐 아니라 활동과 감정까지 조절할 수 있음을 확인했다.
뇌 활성은 신경세포와 신경교세포와 같은 뇌세포들이 서로 신호를 주고받으며 조절된다. 이 같은 상호작용은 뇌 세포 내 ‘소낭’안에 담긴 신경전달물질 분비를 통해 이루어진다. 소낭이 뇌 활성을 조절하는 사령관인 셈이다. 뇌 활성 조절은 뇌 연구를 위한 필수 기술이다. 뇌의 특정 부위나 세포의 활성을 촉진 및 억제해보면 특정 뇌 부위가 담당하는 기능, 여러 뇌 부위 간 상호작용의 역할, 특정 상황에서 다양한 뇌세포의 기능 등 특정 상황에서 뇌 작동이 어떠한 원리로 일어나는지 밝힐 수 있기 때문이다.
그러나 기존 뇌 활성 조절 기술은 원하는 시점에 특정 뇌세포의 활성을 자유롭게 조절하기 어려웠다. 지금까지는 세포 전위차 조절 방식을 사용하였는데, 이는 주변 환경의 산성도를 변화시키거나 원하지 않는 다른 자극을 유발할 뿐만 아니라 전위차에 반응하지 않는 세포에는 사용하지 못하는 한계가 있었다. 이번에 개발한 Opto-vTrap 기술은 세포 소낭을 직접 특이적으로 조절할 수 있어 원하는 시점에 다양한 종류의 뇌세포에서 이용이 가능하다.
연구진은 신경전달물질 분비를 직접 조절하고자 세포에 빛을 쪼이면 순간적으로 내부에 올가미처럼 트랩을 만드는 자체 개발 원천기술을 응용, 소낭에 적용했다. Opto-vTrap을 발현하는 세포나 조직에 빛(청색광)을 가하면 소낭 내 광수용체 단백질들이 엉겨 붙으며 소낭이 트랩 안에 포획되고 신경전달물질 분비가 억제된다. 요컨대 Opto-vTrap으로 소낭의 신호전달물질 분비를 직접 제어하여 뇌 활성을 자유롭게 조절하는 것이다. 연구진은 세포와 조직실험에서 나아가 Opto-vTrap 바이러스를 이용한 동물실험을 통해 뇌세포 신호전달 뿐만 아니라 기억·감정·행동도 조절 가능함을 확인하였다.
Opto-vTrap을 이용하면 뇌의 여러 부위간 복합적 상호작용 원리를 밝히고, 뇌세포 형태별 뇌 기능에 미치는 영향을 연구하는 데 유용하게 활용될 것으로 기대된다.
허원도 교수는 “Opto-vTrap은 신경세포와 신경교세포 모두에 잘 작동되기에 향후 다양한 뇌과학 연구 분야에 이용되리라 기대한다” 며 “앞으로 본 기술을 활용하여 특정 뇌세포의 시공간적 기능 연구를 진행하고자 한다.”고 말했다.
이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 중견연구과제 및 KAIST 글로벌 특이점 연구사업의 지원을 받아 수행됐다.
이번 연구 결과는 뇌 과학 학술지 뉴런 (Neuron, IF:17.173) 에 12월 1일(수) 1시(한국시간) 게재됐다.
2021.12.03 조회수 10237 악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30 조회수 12588
악성 유방암 세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술 개발
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 악성 유방암세포를 치료 가능한 상태로 되돌리는 암세포 리프로그래밍 기술을 개발하는 데 성공했다고 30일 밝혔다.
연구팀은 유방암 아류 중에서 가장 악성으로 알려진 삼중음성 유방암(basal-like 혹은 triple negative) 환자들과 호르몬 치료가 가능한 루미날-A 유방암(luminal-A) 환자들의 유전자 네트워크를 컴퓨터시뮬레이션을 통해 분석함으로써 삼중음성 유방암세포를 루미날-A 유방암세포로 변환하는데 필요한 핵심 인자를 규명했다. 그리고 이를 조절해 삼중음성 유방암세포를 루미날-A 유방암세포로 리프로그래밍한 뒤 호르몬 치료를 시행하는 새로운 치료 원리를 개발했다.
우리 대학 최새롬 박사과정, 황채영 박사, 이종훈 박사과정 등이 참여한 이번 연구결과는 미국암학회(AACR)에서 출간하는 국제저널 `캔서 리서치 (Cancer Research)' 11월 30일 字 논문으로 출판됐다. (논문명: Network analysis identifies regulators of basal-like breast cancer reprogramming and endocrine therapy vulnerability)
현재 삼중음성 유방암 환자들에게 적용되는 항암 화학요법은 빠르게 분열해 전이를 일으키는 암세포를 공격해 죽임으로써 암세포의 증식을 억제하는 방식이다. 하지만 이러한 치료는 신체 내 정상적으로 분열하고 있는 세포들까지도 함께 사멸시켜 구토, 설사, 탈모, 골수 기능장애, 무기력 등의 심각한 부작용을 일으킨다. 또한 삼중음성 유방암세포들은 이와 같은 독성항암제에 처음부터 내성을 갖거나 새로운 내성을 획득하면서 결국 약물에 높은 저항성을 가지는 암세포로 진화하게 된다. 따라서 삼중음성 유방암에 대한 현재의 항암치료는 내성을 갖는 암세포를 없애기 위해 더 많은 정상세포의 사멸을 감수해야만 하는 큰 한계를 지니고 있다.
이를 극복하기 위해 암세포만을 특이적으로 공격하는 표적 항암요법과 우리 몸의 면역시스템을 활용한 면역 항암요법이 주목을 받고 있으나 각각 효과와 적용대상이 매우 제한적이며 장기치료 시 여전히 내성 발생의 문제가 보고되고 있다. 이처럼 현재 개발된 항암요법들은 암세포를 죽이려는 공통적인 원리 때문에 근본적인 한계를 가진다.
조 교수 연구팀은 시스템생물학 연구기법을 통해 악성 유방암세포인 삼중음성 유방암세포를 호르몬 치료가 가능한 루미날-A 유방암세포로 변환시킨 뒤 치료하는 새로운 개념의 치료전략을 개발했다. 이를 위해 유전자 네트워크의 수학모델을 개발하고 대규모 컴퓨터시뮬레이션 분석과 복잡계 네트워크 제어기술을 적용한 결과 두 개의 핵심 분자 타겟인 `BCL11A'와 `HDAC1/2'를 발굴했다.
조 교수 연구팀은 BCL11A와 HDAC1/2를 억제함으로써 삼중음성 유방암세포를 효과적으로 루미날-A 유방암세포로 변환시킬 수 있음을 분자 세포실험을 통해 증명했다. 삼중음성 유방암세포에서 이 핵심 인자들을 억제했을 때 세포의 분열이 감소하고, 삼중음성 유방암세포의 주요 세포성장 신호 흐름 경로인 `EGFR'과 관련된 인자들의 활동이 감소했으며, 루미날-A 유방암세포의 주요 세포성장 신호흐름 경로인 `ERa' 신호전달 경로 인자들의 활성이 회복되는 것을 확인했다.
이번 연구에서 발굴된 분자 타겟 중 BCL11A 단백질의 활성을 억제할 수 있는 저분자화합물은 아직 개발된 바 없으며 추후 신약개발과 임상실험을 통해 악성 유방암세포를 치료 가능한 세포상태로 리프로그래밍 함으로써 안전하고 효과적으로 치료하는 새로운 치료기술이 실현될 수 있을 것으로 보인다. 특히 이처럼 암세포의 성질을 되돌리거나 변환하는 암세포 리프로그래밍 기반의 새로운 치료전략이 임상에서 실현된다면 현재 항암치료의 많은 부작용과 내성 발생을 근본적으로 해결함으로써 암 환자의 고통을 최소화하고 삶의 질을 크게 향상시킬 수 있을 것으로 기대된다.
조 교수는 "그동안 유방암 중에서도 가장 악성인 삼중음성 유방암은 독성이 강해 큰 부작용을 일으키는 화학 항암치료 외에는 방법이 없었으나 이를 호르몬 치료가 가능하며 덜 악성인 루미날-A 유방암세포로 리프로그래밍해 효과적으로 치료할 수 있는 새로운 가능성을 열었다ˮ라며 "이번 연구는 악성 암세포를 직접 없애려고 하기보다 치료가 수월한 세포 상태로 되돌린 뒤 치료하는 새로운 방식의 항암 치료전략을 제시했다ˮ라고 말했다.
조 교수 연구팀은 2020년 1월에 대장암세포를 정상 대장 세포로 되돌리는 연구에 성공한 바 있으며, 이번 연구 결과는 암세포 리프로그래밍을 통한 가역화 기술 개발의 두 번째 성과다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업과 한국전자통신연구소 공동연구사업, KAIST Grand Challenge 30의 지원으로 수행됐다.
2021.11.30 조회수 12588 건강한 장수를 유도하는 돌연변이 유전자 발굴
우리 대학 생명과학과 노화분자유전학 실험실 이승재 교수 연구팀이 가늘고 길게 사는 돌연변이체에 종양 억제 유전자 `PTEN'의 특정 돌연변이를 도입해 건강한 장수를 유도할 수 있다는 연구결과를 발표했다고 6일 밝혔다.
초고령화 사회에 도입한 우리나라의 가장 시급한 문제 중 하나는 단순히 수명을 늘리는 것이 아닌 건강하게 장수하는 방법을 개발하는 것이다. 노화가 건강에 부정적인 영향을 미치기 시작하기 전 시기를 건강 수명이라고 하며, 최근 노화 연구의 주요 목표 중 하나는 건강 수명을 늘리는 것이다.
인슐린 및 인슐린 유사 성장인자는 진화적으로 잘 보존이 된 수명 조절 호르몬인데, 이의 적절한 감소는 수명을 늘리지만 건강 수명(운동성, 성장, 생식능력, 발달 등)은 오히려 악화시킨다.
이승재 교수 연구팀은 노화 연구에서 많이 사용되고 수명이 3주 정도로 짧은 예쁜꼬마선충을 이용해 인슐린과 인슐린 유사 성장인자가 감소된 상황에서 종양 억제 유전자인 PTEN의 유전자 서열 하나만 바꾸면 장수와 건강을 모두 얻을 수 있음을 발견했다.
연구진이 발굴한 변이는 탈인산화 효소인 PTEN 단백질의 기능 중 지질 탈인산화 효소 활성은 감소시키지만, 단백질 탈인산화 효소 활성은 일부를 유지하는 방식으로 장수는 감소시키지 않으면서 건강은 유지하도록 생명체의 기능을 재조정했다.
그 결과, 장수 조절 유도인자인 FOXO의 활성은 유지하지만 과자극 시 건강에 해로운 전사인자인 NRF2의 활성을 적절히 억제해 긴 수명과 노화된 개체에서의 건강을 모두 획득했다.
연구팀은 이번 연구를 통해 장수 유도 신호전달 경로에서 효소 하나의 활성을 세심하게 조정해 장수 유지뿐 아니라 건강 수명을 늘릴 수 있다는 매우 획기적인 가능성을 제시했다.
특히, 인간을 비롯한 포유류에도 보존이 잘 돼 있는 종양 억제 유전자 PTEN이 건강한 장수유도에 중요하다는 것을 보여줬기에, PTEN 활성의 적절한 조절을 통해 인간의 건강 장수를 유도해 초고령화 사회의 문제 해소 가능성을 제시한 것에 의의가 있다.
생명과학과 박혜은 학생, 함석진 박사, 김은아 박사와 POSTECH 황우선 박사가 공동 제1 저자로 참여한 이번 연구는 한국연구재단 리더연구과제의 지원을 받아 수행됐으며 세계적인 과학 국제학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 2021년 9월 24일 날짜로 게재됐다.
(논문명: A PTEN variant uncouples longevity from impaired fitness in Caenorhabditis elegans with reduced insulin/IGF-1 signaling)
2021.10.06 조회수 11926
건강한 장수를 유도하는 돌연변이 유전자 발굴
우리 대학 생명과학과 노화분자유전학 실험실 이승재 교수 연구팀이 가늘고 길게 사는 돌연변이체에 종양 억제 유전자 `PTEN'의 특정 돌연변이를 도입해 건강한 장수를 유도할 수 있다는 연구결과를 발표했다고 6일 밝혔다.
초고령화 사회에 도입한 우리나라의 가장 시급한 문제 중 하나는 단순히 수명을 늘리는 것이 아닌 건강하게 장수하는 방법을 개발하는 것이다. 노화가 건강에 부정적인 영향을 미치기 시작하기 전 시기를 건강 수명이라고 하며, 최근 노화 연구의 주요 목표 중 하나는 건강 수명을 늘리는 것이다.
인슐린 및 인슐린 유사 성장인자는 진화적으로 잘 보존이 된 수명 조절 호르몬인데, 이의 적절한 감소는 수명을 늘리지만 건강 수명(운동성, 성장, 생식능력, 발달 등)은 오히려 악화시킨다.
이승재 교수 연구팀은 노화 연구에서 많이 사용되고 수명이 3주 정도로 짧은 예쁜꼬마선충을 이용해 인슐린과 인슐린 유사 성장인자가 감소된 상황에서 종양 억제 유전자인 PTEN의 유전자 서열 하나만 바꾸면 장수와 건강을 모두 얻을 수 있음을 발견했다.
연구진이 발굴한 변이는 탈인산화 효소인 PTEN 단백질의 기능 중 지질 탈인산화 효소 활성은 감소시키지만, 단백질 탈인산화 효소 활성은 일부를 유지하는 방식으로 장수는 감소시키지 않으면서 건강은 유지하도록 생명체의 기능을 재조정했다.
그 결과, 장수 조절 유도인자인 FOXO의 활성은 유지하지만 과자극 시 건강에 해로운 전사인자인 NRF2의 활성을 적절히 억제해 긴 수명과 노화된 개체에서의 건강을 모두 획득했다.
연구팀은 이번 연구를 통해 장수 유도 신호전달 경로에서 효소 하나의 활성을 세심하게 조정해 장수 유지뿐 아니라 건강 수명을 늘릴 수 있다는 매우 획기적인 가능성을 제시했다.
특히, 인간을 비롯한 포유류에도 보존이 잘 돼 있는 종양 억제 유전자 PTEN이 건강한 장수유도에 중요하다는 것을 보여줬기에, PTEN 활성의 적절한 조절을 통해 인간의 건강 장수를 유도해 초고령화 사회의 문제 해소 가능성을 제시한 것에 의의가 있다.
생명과학과 박혜은 학생, 함석진 박사, 김은아 박사와 POSTECH 황우선 박사가 공동 제1 저자로 참여한 이번 연구는 한국연구재단 리더연구과제의 지원을 받아 수행됐으며 세계적인 과학 국제학술지 `네이처 커뮤니케이션즈 (Nature Communications)'에 2021년 9월 24일 날짜로 게재됐다.
(논문명: A PTEN variant uncouples longevity from impaired fitness in Caenorhabditis elegans with reduced insulin/IGF-1 signaling)
2021.10.06 조회수 11926 우수한 소재를 설계하는 딥러닝 방법론 개발
우리 대학 기계공학과 유승화 교수 연구팀이 능동-전이 학습 (active-transfer learning)과 데이터 증강기법(Data augmentation)에 기반해, 심층신경망 초기 훈련에 쓰인 소재들과 형태와 조합이 매우 다른 우수한 특성을 지닌 소재를 효율적으로 탐색하고 설계하는 방법론을 개발했다고 16일 밝혔다.
인공신경망에 기반해 방대한 설계 공간에서 새로운 소재를 찾기 위한 역설계 연구는 최근 매우 활발하게 진행되고 있다. 하지만 이러한 기존 설계 방식은 목표로 하는 소재의 형태와 조합이 심층신경망 훈련에 활용된 소재들과 매우 다를 때 인공신경망이 가지는 낮은 예측능력으로 인해 극히 많은 수의 소재 데이터 검증이 요구되며, 이에 따라 제한적으로만 활용이 가능하다.
연구팀은 이번 연구에서 이를 극복하기 위해 초기 훈련 데이터 영역에서 벗어나 우수한 소재를 효율적으로 탐색할 수 있는 인공신경망 기반 전진 설계 (Forward design) 방법론을 제안했다. 이 방법론은, <그림 1>에 도시된 바와 같이 유전 알고리즘과 결합된 능동-전이 학습 및 데이터 증강기법을 통해 심층신경망을 점진적으로 업데이트함으로써, 초기 훈련데이터를 벗어난 영역에서 심층신경망의 낮은 예측능력을 적은 숫자의 데이터 검증 및 추가로 보완한다.
유전 알고리즘에 의해 제안되는 우수 소재 후보군은 기보유한 소재 데이터를 조합해 도출하기 때문에 심층신경망의 신뢰할 수 있는 예측 영역과 설계 공간 측면에서 상대적으로 가까워 예측정확도가 유지된다. 이 후보군과 능동-전이 학습을 활용해 점진적으로 심층신경망의 신뢰성 있는 예측 범위를 확장하면, 초기 훈련데이터 영역 밖에서도 적은 데이터를 생성해 효율적인 설계 과정이 가능하다.
이번 방법은 천문학적인 수의 설계 구성을 가지는 그리드 복합소재 최적화 문제에 적용해 검증했으며, 이를 통해 전체 가능한 복합재 구조의 1029분의 1 가량인 10만 개의 복합재들만 초기 훈련 데이터로 활용해 심층신경망을 학습한 후, 이후 약 500개에 미치지 못하는 데이터 검증을 통해 초기 훈련에 쓰인 복합재와 매우 다른 구조를 가지고 우수한 특성을 지닌 복합재 구조를 설계할 수 있음을 보였다.
연구진이 개발한 방법론은 국소 최적점(Local optima)에 수렴하는 문제를 완화하면서도 인공신경망의 신뢰할 수 있는 예측 영역을 점진적으로 확장하는 효율적인 방법을 제공하기 때문에, 큰 설계 공간을 다루는 다양한 분야의 최적화 문제에 적용할 수 있을 것으로 기대되며, 특히 설계에 요구되는 데이터 검증의 숫자가 적기 때문에 데이터 생성에 시간이 오래 걸리고 비용이 많이 드는 설계 문제에서 이 방법론이 크게 활용될 수 있을 것으로 기대된다.
이번 연구는 공동 제 1저자 김용태 박사과정, 김영수 박사(한국기계연구원) 주도하에 진행됐으며, 유승화 교수(우리 대학 기계공학과)가 교신저자로 참여해, 국제학술지인 `npj 컴퓨테이셔널 머터리얼(Computational Material, IF:12.241)'에 `Deep Learning Framework for Material Design Space Exploration using Active Transfer Learning and Data Augmentation' 라는 제목으로 게재됐다.
이번 연구는 한국연구재단의 중견 연구자지원사업(3D 프린팅 복합재의 최적설계기법 및 피로수명 예측기법 개발)과 미래소재 디스커버리 사업 (레이저-물질 상호작용 멀티스케일 모델링을 통한 분자디자인), KAIST 글로벌 특이점 프렙 사업의 지원을 통해 수행됐다.
2021.09.16 조회수 12820
우수한 소재를 설계하는 딥러닝 방법론 개발
우리 대학 기계공학과 유승화 교수 연구팀이 능동-전이 학습 (active-transfer learning)과 데이터 증강기법(Data augmentation)에 기반해, 심층신경망 초기 훈련에 쓰인 소재들과 형태와 조합이 매우 다른 우수한 특성을 지닌 소재를 효율적으로 탐색하고 설계하는 방법론을 개발했다고 16일 밝혔다.
인공신경망에 기반해 방대한 설계 공간에서 새로운 소재를 찾기 위한 역설계 연구는 최근 매우 활발하게 진행되고 있다. 하지만 이러한 기존 설계 방식은 목표로 하는 소재의 형태와 조합이 심층신경망 훈련에 활용된 소재들과 매우 다를 때 인공신경망이 가지는 낮은 예측능력으로 인해 극히 많은 수의 소재 데이터 검증이 요구되며, 이에 따라 제한적으로만 활용이 가능하다.
연구팀은 이번 연구에서 이를 극복하기 위해 초기 훈련 데이터 영역에서 벗어나 우수한 소재를 효율적으로 탐색할 수 있는 인공신경망 기반 전진 설계 (Forward design) 방법론을 제안했다. 이 방법론은, <그림 1>에 도시된 바와 같이 유전 알고리즘과 결합된 능동-전이 학습 및 데이터 증강기법을 통해 심층신경망을 점진적으로 업데이트함으로써, 초기 훈련데이터를 벗어난 영역에서 심층신경망의 낮은 예측능력을 적은 숫자의 데이터 검증 및 추가로 보완한다.
유전 알고리즘에 의해 제안되는 우수 소재 후보군은 기보유한 소재 데이터를 조합해 도출하기 때문에 심층신경망의 신뢰할 수 있는 예측 영역과 설계 공간 측면에서 상대적으로 가까워 예측정확도가 유지된다. 이 후보군과 능동-전이 학습을 활용해 점진적으로 심층신경망의 신뢰성 있는 예측 범위를 확장하면, 초기 훈련데이터 영역 밖에서도 적은 데이터를 생성해 효율적인 설계 과정이 가능하다.
이번 방법은 천문학적인 수의 설계 구성을 가지는 그리드 복합소재 최적화 문제에 적용해 검증했으며, 이를 통해 전체 가능한 복합재 구조의 1029분의 1 가량인 10만 개의 복합재들만 초기 훈련 데이터로 활용해 심층신경망을 학습한 후, 이후 약 500개에 미치지 못하는 데이터 검증을 통해 초기 훈련에 쓰인 복합재와 매우 다른 구조를 가지고 우수한 특성을 지닌 복합재 구조를 설계할 수 있음을 보였다.
연구진이 개발한 방법론은 국소 최적점(Local optima)에 수렴하는 문제를 완화하면서도 인공신경망의 신뢰할 수 있는 예측 영역을 점진적으로 확장하는 효율적인 방법을 제공하기 때문에, 큰 설계 공간을 다루는 다양한 분야의 최적화 문제에 적용할 수 있을 것으로 기대되며, 특히 설계에 요구되는 데이터 검증의 숫자가 적기 때문에 데이터 생성에 시간이 오래 걸리고 비용이 많이 드는 설계 문제에서 이 방법론이 크게 활용될 수 있을 것으로 기대된다.
이번 연구는 공동 제 1저자 김용태 박사과정, 김영수 박사(한국기계연구원) 주도하에 진행됐으며, 유승화 교수(우리 대학 기계공학과)가 교신저자로 참여해, 국제학술지인 `npj 컴퓨테이셔널 머터리얼(Computational Material, IF:12.241)'에 `Deep Learning Framework for Material Design Space Exploration using Active Transfer Learning and Data Augmentation' 라는 제목으로 게재됐다.
이번 연구는 한국연구재단의 중견 연구자지원사업(3D 프린팅 복합재의 최적설계기법 및 피로수명 예측기법 개발)과 미래소재 디스커버리 사업 (레이저-물질 상호작용 멀티스케일 모델링을 통한 분자디자인), KAIST 글로벌 특이점 프렙 사업의 지원을 통해 수행됐다.
2021.09.16 조회수 12820 유전체 기술 기반 인간 배아 발생과정 추적 성공
우리 대학 의과학대학원 주영석 교수 연구팀이 경북대학교 의과대학 해부학 교실 오지원 교수팀과 공동연구를 통해 전장 유전체 기술을 이용해 인간 발생과정을 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 인간 배아에 존재하는 소수의 세포들이 인체에 존재하는 총 40조 개의 세포를 어떻게 구성하고 각각의 장기로 언제 분화하는지 체계적으로 이해하기 위한 것으로 현존하는 세계 최대 규모의 결과다.
이번 연구는 초기 발생과정에서 각각의 세포에 자발적으로 발생하는 DNA 돌연변이를 대규모로 추적함으로써 배아의 파괴 없이 발생 과정 추적이 이뤄졌다. 연구팀은 단 하나의 세포(수정란)으로부터 복잡한 인체가 만들어지는 과정 동안 발생하는 돌연변이들과 세포들의 움직임을 고해상도로 재구성했으며, 이는 향후 발생과정의 이상으로 발병하는 희귀난치병을 이해하는데 기여할 것으로 기대된다.
우리 대학 박성열 박사(現 ㈜ 지놈인사이트 수석과학자), 경북대 의과대학 난다 말리(Nanda Mali) 박사, 우리 대학 김률 박사(現 삼성서울병원 내과 전임의)가 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처(Nature)' 8월 25일 字 온라인판에 게재됐다. (논문명 : Clonal dynamics in early human embryogenesis inferred from somatic mutation) 또한, 한국과학기술정보연구원(KISTI), 가톨릭의대, ㈜ 지놈인사이트, 이뮨스퀘어㈜ 의 연구자들도 함께 참여했다.
단 하나의 수정란이 인체의 다양한 장기를 만들어내는 인간 발생과정의 원리를 밝히는 것은 의생명과학의 근본적 물음이었다. 하지만 직접적인 연구를 위해서는 필연적으로 배아의 파괴를 동반하기 때문에 그동안 대부분의 배아발생 연구는 예쁜꼬마선충 (C. elegans), 초파리, 생쥐 등 모델 동물을 이용해 이뤄졌다. 특히 예쁜꼬마선충의 배아 발생과정 연구는 2002년 노벨생리의학상의 영예를 안겨주기도 하였다. 하지만 종 간의 차이로 이들로부터 인간의 발생과정을 근본적으로 이해하는 데는 한계가 있었다.
이를 극복하기 위해 공동연구팀은 DNA 돌연변이에 주목했다. 수정란이 세포 분열을 하는 과정에서 무작위적 돌연변이가 매 세포에 누적되는 것을 발견했다. 이렇게 발생한 돌연변이는 성체의 자손 세포에게도 전달되기 때문에, 전신에 분포한 단일세포의 DNA 돌연변이를 체계적으로 분석한다면 이들을 세포의 바코드로 삼아 배아 세포들의 움직임을 재구성해낼 수 있다는 결론을 얻었다. 이를 바탕으로, 7명의 시신 기증자에서 총 334개의 단일세포 및 379개의 조직을 기증받아 세계 최대 규모의 단일세포 전장유전체 분석을 수행했다.
이번 연구로부터 연구팀은 인간 배아 발생과정에 발생하는 현상들을 규명하는 데 성공했다. 그리고 배아 내 세포들이 발생 초기부터 서로 동등하지 않다는 것을 발견했다. 예를 들어 2세포기의 두 세포 중 한 세포가 다른 세포에 비해 더 항상 더 많은 자손 세포를 남기는 것으로 나타났다. 하지만 그 비율은 사람마다 달라서 사람의 발생과정이 개인 간 변동성이 높다는 사실을 확인했다.
또한 초기 배아 세포들이 각각의 장기 특이적인 세포로 분화하기 시작하는 시점도 특정할 수 있었다. 수정 후 3일 내, 매우 이른 시기의 배아에서도 (2세포-16세포기) 인체의 좌-우 조직에 대한 배아 세포의 비대칭적 분포가 나타나기 시작했으며, 이어서 3배엽 분화에 대한 비대칭성, 각 조직 및 장기에 대한 비대칭성이 차례로 형성되는 것을 확인했다.
연구팀의 이번 연구는 전장 유전체 빅데이터를 이용하여 윤리적인 문제 없이 인간의 초기 배아 발생 과정 추적이 가능하다는 것을 명쾌하게 증명해냈다는 데 의의가 있다. 이를 응용하면 개개인마다 발생과정 중 나타나는 세포들의 움직임을 재구성할 수 있게 된다. 이번 기술은 향후 발생 과정에서 생기는 희귀질환의 예방, 선별검사 및 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
경북대학교 의과대학 오지원 교수는 "죽음에 이른 신체로부터 인간 생명의 첫 순간을 규명할 수 있다는 것을 보여준 놀라운 연구ˮ라며 "숭고한 희생정신으로 본인의 신체를 기증한 분들이 없었다면 이번 연구는 불가능하였을 것ˮ이라고 말했다.
우리 대학 의과학대학원 주영석 교수는 "인간 게놈 프로젝트 완성 20년 만에 단일세포 유전체에 존재하는 돌연변이를 정확히 규명할 수 있을 만큼 발전한 유전체 기술의 쾌거ˮ라며 "기술 혁신을 기반으로 향후 지속적으로 더 높은 해상도의 인간 배아 발생과정 추적이 가능할 것ˮ이라고 말했다.
한편 이번 연구는 보건복지부 세계선도의과학자 육성사업, 서경배 과학재단 및 한국연구재단(리더과제, 우수신진연구, 지역대학우수과학자, 선도연구센터)의 지원을 받아 수행됐다.
2021.08.26 조회수 12839
유전체 기술 기반 인간 배아 발생과정 추적 성공
우리 대학 의과학대학원 주영석 교수 연구팀이 경북대학교 의과대학 해부학 교실 오지원 교수팀과 공동연구를 통해 전장 유전체 기술을 이용해 인간 발생과정을 규명하는 데 성공했다고 26일 밝혔다.
이번 연구는 인간 배아에 존재하는 소수의 세포들이 인체에 존재하는 총 40조 개의 세포를 어떻게 구성하고 각각의 장기로 언제 분화하는지 체계적으로 이해하기 위한 것으로 현존하는 세계 최대 규모의 결과다.
이번 연구는 초기 발생과정에서 각각의 세포에 자발적으로 발생하는 DNA 돌연변이를 대규모로 추적함으로써 배아의 파괴 없이 발생 과정 추적이 이뤄졌다. 연구팀은 단 하나의 세포(수정란)으로부터 복잡한 인체가 만들어지는 과정 동안 발생하는 돌연변이들과 세포들의 움직임을 고해상도로 재구성했으며, 이는 향후 발생과정의 이상으로 발병하는 희귀난치병을 이해하는데 기여할 것으로 기대된다.
우리 대학 박성열 박사(現 ㈜ 지놈인사이트 수석과학자), 경북대 의과대학 난다 말리(Nanda Mali) 박사, 우리 대학 김률 박사(現 삼성서울병원 내과 전임의)가 공동 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처(Nature)' 8월 25일 字 온라인판에 게재됐다. (논문명 : Clonal dynamics in early human embryogenesis inferred from somatic mutation) 또한, 한국과학기술정보연구원(KISTI), 가톨릭의대, ㈜ 지놈인사이트, 이뮨스퀘어㈜ 의 연구자들도 함께 참여했다.
단 하나의 수정란이 인체의 다양한 장기를 만들어내는 인간 발생과정의 원리를 밝히는 것은 의생명과학의 근본적 물음이었다. 하지만 직접적인 연구를 위해서는 필연적으로 배아의 파괴를 동반하기 때문에 그동안 대부분의 배아발생 연구는 예쁜꼬마선충 (C. elegans), 초파리, 생쥐 등 모델 동물을 이용해 이뤄졌다. 특히 예쁜꼬마선충의 배아 발생과정 연구는 2002년 노벨생리의학상의 영예를 안겨주기도 하였다. 하지만 종 간의 차이로 이들로부터 인간의 발생과정을 근본적으로 이해하는 데는 한계가 있었다.
이를 극복하기 위해 공동연구팀은 DNA 돌연변이에 주목했다. 수정란이 세포 분열을 하는 과정에서 무작위적 돌연변이가 매 세포에 누적되는 것을 발견했다. 이렇게 발생한 돌연변이는 성체의 자손 세포에게도 전달되기 때문에, 전신에 분포한 단일세포의 DNA 돌연변이를 체계적으로 분석한다면 이들을 세포의 바코드로 삼아 배아 세포들의 움직임을 재구성해낼 수 있다는 결론을 얻었다. 이를 바탕으로, 7명의 시신 기증자에서 총 334개의 단일세포 및 379개의 조직을 기증받아 세계 최대 규모의 단일세포 전장유전체 분석을 수행했다.
이번 연구로부터 연구팀은 인간 배아 발생과정에 발생하는 현상들을 규명하는 데 성공했다. 그리고 배아 내 세포들이 발생 초기부터 서로 동등하지 않다는 것을 발견했다. 예를 들어 2세포기의 두 세포 중 한 세포가 다른 세포에 비해 더 항상 더 많은 자손 세포를 남기는 것으로 나타났다. 하지만 그 비율은 사람마다 달라서 사람의 발생과정이 개인 간 변동성이 높다는 사실을 확인했다.
또한 초기 배아 세포들이 각각의 장기 특이적인 세포로 분화하기 시작하는 시점도 특정할 수 있었다. 수정 후 3일 내, 매우 이른 시기의 배아에서도 (2세포-16세포기) 인체의 좌-우 조직에 대한 배아 세포의 비대칭적 분포가 나타나기 시작했으며, 이어서 3배엽 분화에 대한 비대칭성, 각 조직 및 장기에 대한 비대칭성이 차례로 형성되는 것을 확인했다.
연구팀의 이번 연구는 전장 유전체 빅데이터를 이용하여 윤리적인 문제 없이 인간의 초기 배아 발생 과정 추적이 가능하다는 것을 명쾌하게 증명해냈다는 데 의의가 있다. 이를 응용하면 개개인마다 발생과정 중 나타나는 세포들의 움직임을 재구성할 수 있게 된다. 이번 기술은 향후 발생 과정에서 생기는 희귀질환의 예방, 선별검사 및 정밀치료 시스템 구축에 이바지할 수 있을 것으로 기대된다.
경북대학교 의과대학 오지원 교수는 "죽음에 이른 신체로부터 인간 생명의 첫 순간을 규명할 수 있다는 것을 보여준 놀라운 연구ˮ라며 "숭고한 희생정신으로 본인의 신체를 기증한 분들이 없었다면 이번 연구는 불가능하였을 것ˮ이라고 말했다.
우리 대학 의과학대학원 주영석 교수는 "인간 게놈 프로젝트 완성 20년 만에 단일세포 유전체에 존재하는 돌연변이를 정확히 규명할 수 있을 만큼 발전한 유전체 기술의 쾌거ˮ라며 "기술 혁신을 기반으로 향후 지속적으로 더 높은 해상도의 인간 배아 발생과정 추적이 가능할 것ˮ이라고 말했다.
한편 이번 연구는 보건복지부 세계선도의과학자 육성사업, 서경배 과학재단 및 한국연구재단(리더과제, 우수신진연구, 지역대학우수과학자, 선도연구센터)의 지원을 받아 수행됐다.
2021.08.26 조회수 12839 시각 정보가 행동으로 변환되는 신경회로 규명
우리 대학 생명과학과 이승희 교수 연구팀이 시각 정보를 인식해 목표 지향적 행동을 결정하는 대뇌 전두엽의 신경회로 기전을 새롭게 규명했다고 26일 밝혔다.
이 교수 연구팀은 시각 피질과 상호 작용하는 전측 대상회(전대상) 피질(Anterior cingulate cortex, ACC)의 억제성 신경회로가 동물이 시각 정보를 인식하고 이에 맞는 정확한 행동을 개시하는 데 중요한 역할을 함을 밝혔다. 연구 결과는 포유류 전두엽 전대상 피질의 신경회로가 어떻게 시각 인지 행동 및 충동적 행동을 제어할 수 있는지를 새롭게 규명해, 주의력결핍과잉행동장애(ADHD)와 같은 인지장애 및 충동성을 주 증상으로 하는 뇌질환 치료에 적용될 수 있을 것으로 기대된다.
생명과학과 김재현 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 뉴로사이언스 (Nature Neuroscience, IF 20.071)' 8월 19일 字 온라인판에 게재됐다. (논문명 : Gated feedforward inhibition in the frontal cortex releases goal-directed action)
우리는 외부 환경에서 유입되는 다양한 감각 정보를 인지해 상황에 맞는 행동을 수행한다. 한 예로, 운전할 때 신호등 앞에서 빨간색 신호를 보면 출발하지 않고 멈춰야 하며, 초록색 신호로 바뀌면 출발하게 된다. 이처럼 시각 정보를 인식하고 이에 맞는 운동 행동을 결정하기 위해 우리 뇌는 받아들인 감각 정보를 적절한 운동 정보로 변환해야 하는데, 이 교수 연구팀은 이것이 전대상 피질의 억제성 회로에 의해 이루어짐을 밝혔다.
연구팀은 뇌가 받아들인 시각 정보를 어떻게 운동 정보로 전달하는지 규명하기 위해, 시각 자극을 보면 물을 핥고 그렇지 않으면 물 핥기를 멈추는 목표 지향적 행동을 학습시킨 생쥐의 전대상 피질에 고밀도 실리콘 전극을 삽입해 생체 내 신경 신호를 측정 및 분석했다. 그 결과, 전두엽 전대상 피질 내에서 시각 피질로부터 정보를 받는 시각 반응성 신경세포들이 주변의 세포들을 억제할 경우 생쥐가 운동을 개시할 수 있음을 밝혔다.
또한, 약물적 방법을 이용해 전대상 피질의 활성 정도를 낮추게 되면 생쥐는 시각 자극이 주어지지 않았음에도 불구하고 충동적으로 목표 지향적 행위를 지속하는 비정상적인 행동 양상을 보였다. 이를 통해 전대상 피질은 정상적인 감각-운동 변환 과정에서도 핵심적인 기능을 수행할 뿐 아니라, 시각 정보가 없을 때 운동 개시를 멈추고 기다려야 하는 충동 조절에도 중요한 역할을 하고 있음을 밝혔다.
이 교수 연구팀은 바이러스 추적자, 광유전학, 다채널 전극 레코딩과 같은 신경과학 최첨단 실험 기법을 활용해 전대상 피질 내의 신경세포 타입과 회로가 어떠한 방식으로 시각 정보를 목표 지향적 운동 행위로 변환하는지에 대한 신경 메커니즘 원리를 최초로 규명했다.
전대상 피질에는 시각 정보에 반응하는 시각 반응성 신경세포, 운동 개시를 억제하는 운동 억제성 신경세포, 그리고 시각 정보와 운동 개시에 반응하지 않는 나머지 신경세포들이 존재함을 확인했다. 그리고 이와 같은 세 종류의 뉴런들의 신경 활성도는 생쥐가 시각 정보를 인지하여 행동을 개시하는 반응 속도와 유의미한 상관관계가 있음을 규명했다.
특히, 광유전학적(optognetics) 방법을 이용한 실험에서, 전대상 피질의 시각 반응성 뉴런들은 시각 피질로부터 신경 정보를 직접 전달받음을 확인했고, 광 자극으로 해당 신경 회로를 활성화할 때 시각 자극이 없어도 생쥐의 목표 지향적 행동을 유발할 수 있음을 증명했다.
이승희 교수는 "이번 연구 결과는 주의력결핍과잉행동장애 및 조현병과 같은 질병에서 전대상 피질이 정상적으로 작동하지 못할 때 나타나는 행동 장애를 치료하기 위한 정밀한 신경회로 타겟을 제시했다ˮ라고 말했다.
한편, 이번 연구는 한국 연구재단 및 KAIST 글로벌 특이점 프로그램의 지원을 통해 수행됐다.
2021.08.26 조회수 13732
시각 정보가 행동으로 변환되는 신경회로 규명
우리 대학 생명과학과 이승희 교수 연구팀이 시각 정보를 인식해 목표 지향적 행동을 결정하는 대뇌 전두엽의 신경회로 기전을 새롭게 규명했다고 26일 밝혔다.
이 교수 연구팀은 시각 피질과 상호 작용하는 전측 대상회(전대상) 피질(Anterior cingulate cortex, ACC)의 억제성 신경회로가 동물이 시각 정보를 인식하고 이에 맞는 정확한 행동을 개시하는 데 중요한 역할을 함을 밝혔다. 연구 결과는 포유류 전두엽 전대상 피질의 신경회로가 어떻게 시각 인지 행동 및 충동적 행동을 제어할 수 있는지를 새롭게 규명해, 주의력결핍과잉행동장애(ADHD)와 같은 인지장애 및 충동성을 주 증상으로 하는 뇌질환 치료에 적용될 수 있을 것으로 기대된다.
생명과학과 김재현 박사가 제1 저자로 참여한 이번 연구는 국제 학술지 `네이처 뉴로사이언스 (Nature Neuroscience, IF 20.071)' 8월 19일 字 온라인판에 게재됐다. (논문명 : Gated feedforward inhibition in the frontal cortex releases goal-directed action)
우리는 외부 환경에서 유입되는 다양한 감각 정보를 인지해 상황에 맞는 행동을 수행한다. 한 예로, 운전할 때 신호등 앞에서 빨간색 신호를 보면 출발하지 않고 멈춰야 하며, 초록색 신호로 바뀌면 출발하게 된다. 이처럼 시각 정보를 인식하고 이에 맞는 운동 행동을 결정하기 위해 우리 뇌는 받아들인 감각 정보를 적절한 운동 정보로 변환해야 하는데, 이 교수 연구팀은 이것이 전대상 피질의 억제성 회로에 의해 이루어짐을 밝혔다.
연구팀은 뇌가 받아들인 시각 정보를 어떻게 운동 정보로 전달하는지 규명하기 위해, 시각 자극을 보면 물을 핥고 그렇지 않으면 물 핥기를 멈추는 목표 지향적 행동을 학습시킨 생쥐의 전대상 피질에 고밀도 실리콘 전극을 삽입해 생체 내 신경 신호를 측정 및 분석했다. 그 결과, 전두엽 전대상 피질 내에서 시각 피질로부터 정보를 받는 시각 반응성 신경세포들이 주변의 세포들을 억제할 경우 생쥐가 운동을 개시할 수 있음을 밝혔다.
또한, 약물적 방법을 이용해 전대상 피질의 활성 정도를 낮추게 되면 생쥐는 시각 자극이 주어지지 않았음에도 불구하고 충동적으로 목표 지향적 행위를 지속하는 비정상적인 행동 양상을 보였다. 이를 통해 전대상 피질은 정상적인 감각-운동 변환 과정에서도 핵심적인 기능을 수행할 뿐 아니라, 시각 정보가 없을 때 운동 개시를 멈추고 기다려야 하는 충동 조절에도 중요한 역할을 하고 있음을 밝혔다.
이 교수 연구팀은 바이러스 추적자, 광유전학, 다채널 전극 레코딩과 같은 신경과학 최첨단 실험 기법을 활용해 전대상 피질 내의 신경세포 타입과 회로가 어떠한 방식으로 시각 정보를 목표 지향적 운동 행위로 변환하는지에 대한 신경 메커니즘 원리를 최초로 규명했다.
전대상 피질에는 시각 정보에 반응하는 시각 반응성 신경세포, 운동 개시를 억제하는 운동 억제성 신경세포, 그리고 시각 정보와 운동 개시에 반응하지 않는 나머지 신경세포들이 존재함을 확인했다. 그리고 이와 같은 세 종류의 뉴런들의 신경 활성도는 생쥐가 시각 정보를 인지하여 행동을 개시하는 반응 속도와 유의미한 상관관계가 있음을 규명했다.
특히, 광유전학적(optognetics) 방법을 이용한 실험에서, 전대상 피질의 시각 반응성 뉴런들은 시각 피질로부터 신경 정보를 직접 전달받음을 확인했고, 광 자극으로 해당 신경 회로를 활성화할 때 시각 자극이 없어도 생쥐의 목표 지향적 행동을 유발할 수 있음을 증명했다.
이승희 교수는 "이번 연구 결과는 주의력결핍과잉행동장애 및 조현병과 같은 질병에서 전대상 피질이 정상적으로 작동하지 못할 때 나타나는 행동 장애를 치료하기 위한 정밀한 신경회로 타겟을 제시했다ˮ라고 말했다.
한편, 이번 연구는 한국 연구재단 및 KAIST 글로벌 특이점 프로그램의 지원을 통해 수행됐다.
2021.08.26 조회수 13732 3개 학과 공동연구팀, 다학제적 접근 통해 뇌전증 발병 기전 규명
우리 대학 의과학대학원 이정호 교수, 바이오및뇌공학과 백세범 교수, 생명과학과 손종우 교수 공동 연구팀이 MTOR 유전자 돌연변이에 의해 약물 저항성이 높은 뇌전증이 발병하는 메커니즘을 규명했다고 25일 밝혔다.
이번 연구 결과는 극소수의 신경세포에 발생한 돌연변이가 신경망의 과다 활동(hyperactivity) 상태로 이어지는 구체적인 메커니즘을 밝혀, 뇌전증의 발병 원인 및 치료법 개발에 대한 새로운 시각을 제공한다.
특히 3개 학과간 공동 연구팀의 다학제적인 접근을 통해 세포 내 유전학적인 관점에서부터 단일 신경세포의 전기생리학, 이로부터 근접한 거리에 있는 뇌조직의 네트워크, 그리고 뇌 전체 수준에서의 신경망 수준으로 이어지는 다양한 실험 및 시뮬레이션 연구가 이루어져, 뇌전증의 복잡한 발병 메커니즘을 전반적으로 설명하는 성과를 얻었다.
국소피질 이형성증은 대뇌발달 과정에서 일부 신경줄기세포의 mTOR 경로상의 체성유전변이(MTOR, TSC, DEPDC5) 로 발생하는 질환으로, 흔한 뇌전증의 원인 중 하나이며 항뇌전증제 약물 치료에 잘 반응하지 않아 치료가 어렵다. 이에 연구팀은 국소피질 이형성증 환자의 실제 조직과 같은 질환을 가진 동물 모델을 이용한 실험을 통해, 개별 신경세포의 체성유전변이가 신경망 수준의 발작도로 이어지는 구체적인 원리를 규명했다.
먼저 연구팀은 이러한 체성유전변이는 뇌 조직의 5% 이하인 적은 수의 신경세포에서 발생하며, 해당 신경세포들의 전기적 성질이 정상 세포와는 다르게 변화하는 것을 발견했다. 하지만 대다수 정상 세포를 포함한 전반적인 신경망 활동의 시뮬레이션 결과, 이러한 돌연변이는 매우 적은 비율의 신경세포에만 국한돼 있어, 이 세포들 자체의 전기적 성질 변화만으로는 전체 신경망의 비정상적인 활동으로 이어지지 않았고, 이로 인해 뇌전증에서 보이는 신경망 수준의 발작 활성도가 발생하는 이유를 설명할 수 없었다.
이에 연구팀은 후속 실험을 통해, 뇌전증 발작을 유도할 수 있는 활성도가 MTOR 체성 유전변이를 가진 신경세포가 아니라 그 세포들 주변의 변이가 없는 신경세포에 의해 발생하는 것을 발견했다. 이는 유전자 변이를 가진 신경세포의 활성도가 뇌전증의 직접적인 원인이 되는 것이 아니라, 이들 세포가 주변 대다수 비변이 신경세포에 특정 변화를 유도하고 이로 인해 전체 신경망 수준의 발작 활성도가 발생한다는 뜻으로, 뇌 체성유전변이로 인한 비세포 자율성 활성도(non-cell autonomous hyperexcitability)를 보여주는 한 예가 된다.
이에 착안해 추가적인 동물실험과 수술 후 환자 뇌 조직을 이용한 연구를 통해 MTOR 체성유전변이를 가진 세포에서는 ADK(adenosine kinase, 아데노신 키나제) 유전자가 과발현되는 것을 발견했다. 또한, 이로부터 주변 대다수 비변이 신경세포의 네트워크 체계가 교란돼 과활성도가 유도되고, 더 나아가 전체 신경망 수준의 과다 활동으로까지 이어지는 것을 확인했다.
의과학대학원 고현용 박사, 바이오및뇌공학과 장재선 박사, 생명과학과 주상현 학생이 공동 제1 저자로 참여한 이번 연구는 신경학 분야의 국제 학술지 `애널스 오브 뉴롤로지 (Annals of Neurology)' 7월 29일 字에 게재됐다. (논문명: Non-cell autonomous epileptogenesis in focal cortical dysplasia)
이정호, 백세범, 손종우 교수는 "약물 저항성이 높아 기존에 효과적으로 대처할 수 없었던 뇌전증의 발병 원인에 대해 한층 더 깊은 통찰을 제공하는 연구ˮ라며 "한 분야의 실험이나 연구 기법만으로는 해결하기 어려운 문제에 대해, 유전체학, 신경생물학, 계산뇌과학에 걸친 다학제적 접근으로 해결책을 제시한 효과적인 공동연구의 좋은 예시였다ˮ라고 언급했다.
한편 이번 연구는 한국연구재단 이공분야기초연구사업의 리더연구자지원사업 및 중견연구자지원사업, 보건복지부의 질환극복기술개발사업, 서경배 과학재단, 그리고 소바젠의 지원을 받아 수행됐다.
2021.08.26 조회수 13348
3개 학과 공동연구팀, 다학제적 접근 통해 뇌전증 발병 기전 규명
우리 대학 의과학대학원 이정호 교수, 바이오및뇌공학과 백세범 교수, 생명과학과 손종우 교수 공동 연구팀이 MTOR 유전자 돌연변이에 의해 약물 저항성이 높은 뇌전증이 발병하는 메커니즘을 규명했다고 25일 밝혔다.
이번 연구 결과는 극소수의 신경세포에 발생한 돌연변이가 신경망의 과다 활동(hyperactivity) 상태로 이어지는 구체적인 메커니즘을 밝혀, 뇌전증의 발병 원인 및 치료법 개발에 대한 새로운 시각을 제공한다.
특히 3개 학과간 공동 연구팀의 다학제적인 접근을 통해 세포 내 유전학적인 관점에서부터 단일 신경세포의 전기생리학, 이로부터 근접한 거리에 있는 뇌조직의 네트워크, 그리고 뇌 전체 수준에서의 신경망 수준으로 이어지는 다양한 실험 및 시뮬레이션 연구가 이루어져, 뇌전증의 복잡한 발병 메커니즘을 전반적으로 설명하는 성과를 얻었다.
국소피질 이형성증은 대뇌발달 과정에서 일부 신경줄기세포의 mTOR 경로상의 체성유전변이(MTOR, TSC, DEPDC5) 로 발생하는 질환으로, 흔한 뇌전증의 원인 중 하나이며 항뇌전증제 약물 치료에 잘 반응하지 않아 치료가 어렵다. 이에 연구팀은 국소피질 이형성증 환자의 실제 조직과 같은 질환을 가진 동물 모델을 이용한 실험을 통해, 개별 신경세포의 체성유전변이가 신경망 수준의 발작도로 이어지는 구체적인 원리를 규명했다.
먼저 연구팀은 이러한 체성유전변이는 뇌 조직의 5% 이하인 적은 수의 신경세포에서 발생하며, 해당 신경세포들의 전기적 성질이 정상 세포와는 다르게 변화하는 것을 발견했다. 하지만 대다수 정상 세포를 포함한 전반적인 신경망 활동의 시뮬레이션 결과, 이러한 돌연변이는 매우 적은 비율의 신경세포에만 국한돼 있어, 이 세포들 자체의 전기적 성질 변화만으로는 전체 신경망의 비정상적인 활동으로 이어지지 않았고, 이로 인해 뇌전증에서 보이는 신경망 수준의 발작 활성도가 발생하는 이유를 설명할 수 없었다.
이에 연구팀은 후속 실험을 통해, 뇌전증 발작을 유도할 수 있는 활성도가 MTOR 체성 유전변이를 가진 신경세포가 아니라 그 세포들 주변의 변이가 없는 신경세포에 의해 발생하는 것을 발견했다. 이는 유전자 변이를 가진 신경세포의 활성도가 뇌전증의 직접적인 원인이 되는 것이 아니라, 이들 세포가 주변 대다수 비변이 신경세포에 특정 변화를 유도하고 이로 인해 전체 신경망 수준의 발작 활성도가 발생한다는 뜻으로, 뇌 체성유전변이로 인한 비세포 자율성 활성도(non-cell autonomous hyperexcitability)를 보여주는 한 예가 된다.
이에 착안해 추가적인 동물실험과 수술 후 환자 뇌 조직을 이용한 연구를 통해 MTOR 체성유전변이를 가진 세포에서는 ADK(adenosine kinase, 아데노신 키나제) 유전자가 과발현되는 것을 발견했다. 또한, 이로부터 주변 대다수 비변이 신경세포의 네트워크 체계가 교란돼 과활성도가 유도되고, 더 나아가 전체 신경망 수준의 과다 활동으로까지 이어지는 것을 확인했다.
의과학대학원 고현용 박사, 바이오및뇌공학과 장재선 박사, 생명과학과 주상현 학생이 공동 제1 저자로 참여한 이번 연구는 신경학 분야의 국제 학술지 `애널스 오브 뉴롤로지 (Annals of Neurology)' 7월 29일 字에 게재됐다. (논문명: Non-cell autonomous epileptogenesis in focal cortical dysplasia)
이정호, 백세범, 손종우 교수는 "약물 저항성이 높아 기존에 효과적으로 대처할 수 없었던 뇌전증의 발병 원인에 대해 한층 더 깊은 통찰을 제공하는 연구ˮ라며 "한 분야의 실험이나 연구 기법만으로는 해결하기 어려운 문제에 대해, 유전체학, 신경생물학, 계산뇌과학에 걸친 다학제적 접근으로 해결책을 제시한 효과적인 공동연구의 좋은 예시였다ˮ라고 언급했다.
한편 이번 연구는 한국연구재단 이공분야기초연구사업의 리더연구자지원사업 및 중견연구자지원사업, 보건복지부의 질환극복기술개발사업, 서경배 과학재단, 그리고 소바젠의 지원을 받아 수행됐다.
2021.08.26 조회수 13348