-
 달걀 모방한 세포보호 및 분해기술 개발
특정 미생물은 영양분이 부족한 환경에서 생존이 불리해지면 DNA 보존을 위해 세포외벽에 단단한 보호막인 내생포자를 형성한다. 이렇게 만들어진 내생포자가 생존에 적합한 환경을 만나면 다시 세포증식이 가능한 원래 상태로 돌아간다.
이 현상을 인공적으로 조절하는 기술이 국제 공동연구진에 의해 개발됐다. 달걀껍질처럼 하나의 세포를 감싸서 보존했다가 원하는 시기에 분해할 수 있어 세포기반 바이오센서·세포 치료제·바이오촉매 등에 활용될 것으로 기대된다.
우리 학교 화학과 최인성·이영훈 교수는 호주 멜버른대학교 화학공학과 프랭크 카루소(Frank Caruso) 교수와 공동으로 나노미터 스케일의 필름으로 단일 세포를 코팅해 세포의 생존을 유지하다가 원하는 시간에 분해할 수 있는 기술을 개발했다.
연구결과는 화학분야 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition) 11월 10일자 속표지(frontispiece) 논문으로 소개됐다.
세포피포화(細胞被包化)는 세포의 생존을 최대한 유지하면서 각각의 세포를 단단한 캡슐로 포획하는 기술이다. 세포를 기반으로 한 응용 분야에서 당면한 문제인 세포 안정도 유지와 세포분열제어를 위해 중요성이 높아지고 있다.
기존 세포피포화 방법은 유기박막 혹은 유기박막을 주형으로 만들어진 무기물 캡슐을 이용했다. 이들은 세포표면에 단단하게 형성됐으나 잘 분해되지 않아 활용하기가 어려웠다.
연구팀은 효모세포를 가지고 탄닌산 수용액과 철이온 수용액을 섞어 세포를 하나씩 금속-폴리페놀박막으로 감싸는 데 세계 최초로 성공했다.
탄닌산은 참나무껍질이나 포도껍질에서 추출한 천연물질로 세포친화도가 높아 철이온과 만나면 10초 이내로 금속-폴리페놀박막이 만들어진다. 이 박막으로 피포화된 세포들은 높은 생존율을 보였으며 박막 형성시간이 짧고 간단해 효율적으로 많은 양의 피포화 세포를 얻을 수 있었다.
이와 함께 연구팀은 금속-폴리페놀박막이 중성 pH(수소이온지수)에서는 안정하지만 약한 산성조건에서 빠르게 분해되는 특성을 이용해 원하는 시간에 세포를 피포화 전 상태로 복구해 세포분열을 조절할 수 있음을 밝혔다.
달걀껍질처럼 외부환경으로부터 내부 세포를 보호해주는 금속-폴리페놀박막은 △세포에 손상을 줄 수 있는 분해효소 △장시간의 자외선 처리 △은나노입자에 대한 방어기작을 가져 세포가 극한의 외부환경에 노출되더라도 높은 세포 생존도를 유지하는 결과를 나타냈다.
이영훈 교수는 이번 연구에 대해 “이 기술을 통해 피포화과정에서의 세포생존도를 유지함은 물론 극한의 외부환경에 대항하여 세포를 보호할 수 있다”며 “나아가 응답형 분해기작으로 원하는 때에 피포화된 세포의 분열시기를 조절할 수 있는 차세대 세포피포화기술”이라고 말했다.
최인성 교수는 “세포피포화기술은 아직 걸음마 단계지만 기술이 성숙함에 따라 세포조작기술의 응용가능성이 현실화될 것”이라며 “세포기반 응용분야에서 현실적으로 당면한 문제들을 해결할 맞춤형 대안이 될 것”이라고 덧붙였다.
미래창조과학부와 한국연구재단이 추진하는 리더연구자지원사업과 글로벌연구실지원사업의 지원으로 수행된 이번 연구는 KAIST와 호주 멜버른대학교 국제 공동 교수진의 지도아래 KAIST 화학과 박지훈·김경환 석사과정 학생이 주도했다.
그림 1. 앙게반테 케미 속표지
배경 : 금속-폴리페놀박막(붉은색으로 염색)이 형성된 효모세포가 생존을 유지하고 있음(초록색으로 염색-생존도를 가지고 효소활성을 나타냄)을 보여줌.
앞쪽그림 : 각 피포화 단계의 효모세포 왼쪽아래 : 세포는 피포화하기전 상태, 붉은색 화살표를 따라가면 보라색 금속-폴리페놀박막이 형성되어 보라색으로 나타나는 효모세포, 초록색 화살표를 따라가면 약 산성 pH에서 금속-폴리페놀박막이 표면에서 분해되는 것을 형상화했다.
그림 2. 금속-폴리페놀박막을 이용한 세포피포화(細胞被包化) 모식도
(위)피포화하기전 효모세포
(중간) 금속-폴리페놀 나노캡슐(Tannic Acid-Fe(III) Nanoshell)으로 피포화된 효모세포-피포화된 효모세포는 세포분열이 pH에 따라 조절(Cell-Division Control)되고, UV-C, 분해효소와 은나노입자에 대한 저항성을 가진다. (아래) 원하는 시간에 pH 조절로 금속-폴리페놀박막이 분해되는 것을 형상화
달걀 모방한 세포보호 및 분해기술 개발
특정 미생물은 영양분이 부족한 환경에서 생존이 불리해지면 DNA 보존을 위해 세포외벽에 단단한 보호막인 내생포자를 형성한다. 이렇게 만들어진 내생포자가 생존에 적합한 환경을 만나면 다시 세포증식이 가능한 원래 상태로 돌아간다.
이 현상을 인공적으로 조절하는 기술이 국제 공동연구진에 의해 개발됐다. 달걀껍질처럼 하나의 세포를 감싸서 보존했다가 원하는 시기에 분해할 수 있어 세포기반 바이오센서·세포 치료제·바이오촉매 등에 활용될 것으로 기대된다.
우리 학교 화학과 최인성·이영훈 교수는 호주 멜버른대학교 화학공학과 프랭크 카루소(Frank Caruso) 교수와 공동으로 나노미터 스케일의 필름으로 단일 세포를 코팅해 세포의 생존을 유지하다가 원하는 시간에 분해할 수 있는 기술을 개발했다.
연구결과는 화학분야 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition) 11월 10일자 속표지(frontispiece) 논문으로 소개됐다.
세포피포화(細胞被包化)는 세포의 생존을 최대한 유지하면서 각각의 세포를 단단한 캡슐로 포획하는 기술이다. 세포를 기반으로 한 응용 분야에서 당면한 문제인 세포 안정도 유지와 세포분열제어를 위해 중요성이 높아지고 있다.
기존 세포피포화 방법은 유기박막 혹은 유기박막을 주형으로 만들어진 무기물 캡슐을 이용했다. 이들은 세포표면에 단단하게 형성됐으나 잘 분해되지 않아 활용하기가 어려웠다.
연구팀은 효모세포를 가지고 탄닌산 수용액과 철이온 수용액을 섞어 세포를 하나씩 금속-폴리페놀박막으로 감싸는 데 세계 최초로 성공했다.
탄닌산은 참나무껍질이나 포도껍질에서 추출한 천연물질로 세포친화도가 높아 철이온과 만나면 10초 이내로 금속-폴리페놀박막이 만들어진다. 이 박막으로 피포화된 세포들은 높은 생존율을 보였으며 박막 형성시간이 짧고 간단해 효율적으로 많은 양의 피포화 세포를 얻을 수 있었다.
이와 함께 연구팀은 금속-폴리페놀박막이 중성 pH(수소이온지수)에서는 안정하지만 약한 산성조건에서 빠르게 분해되는 특성을 이용해 원하는 시간에 세포를 피포화 전 상태로 복구해 세포분열을 조절할 수 있음을 밝혔다.
달걀껍질처럼 외부환경으로부터 내부 세포를 보호해주는 금속-폴리페놀박막은 △세포에 손상을 줄 수 있는 분해효소 △장시간의 자외선 처리 △은나노입자에 대한 방어기작을 가져 세포가 극한의 외부환경에 노출되더라도 높은 세포 생존도를 유지하는 결과를 나타냈다.
이영훈 교수는 이번 연구에 대해 “이 기술을 통해 피포화과정에서의 세포생존도를 유지함은 물론 극한의 외부환경에 대항하여 세포를 보호할 수 있다”며 “나아가 응답형 분해기작으로 원하는 때에 피포화된 세포의 분열시기를 조절할 수 있는 차세대 세포피포화기술”이라고 말했다.
최인성 교수는 “세포피포화기술은 아직 걸음마 단계지만 기술이 성숙함에 따라 세포조작기술의 응용가능성이 현실화될 것”이라며 “세포기반 응용분야에서 현실적으로 당면한 문제들을 해결할 맞춤형 대안이 될 것”이라고 덧붙였다.
미래창조과학부와 한국연구재단이 추진하는 리더연구자지원사업과 글로벌연구실지원사업의 지원으로 수행된 이번 연구는 KAIST와 호주 멜버른대학교 국제 공동 교수진의 지도아래 KAIST 화학과 박지훈·김경환 석사과정 학생이 주도했다.
그림 1. 앙게반테 케미 속표지
배경 : 금속-폴리페놀박막(붉은색으로 염색)이 형성된 효모세포가 생존을 유지하고 있음(초록색으로 염색-생존도를 가지고 효소활성을 나타냄)을 보여줌.
앞쪽그림 : 각 피포화 단계의 효모세포 왼쪽아래 : 세포는 피포화하기전 상태, 붉은색 화살표를 따라가면 보라색 금속-폴리페놀박막이 형성되어 보라색으로 나타나는 효모세포, 초록색 화살표를 따라가면 약 산성 pH에서 금속-폴리페놀박막이 표면에서 분해되는 것을 형상화했다.
그림 2. 금속-폴리페놀박막을 이용한 세포피포화(細胞被包化) 모식도
(위)피포화하기전 효모세포
(중간) 금속-폴리페놀 나노캡슐(Tannic Acid-Fe(III) Nanoshell)으로 피포화된 효모세포-피포화된 효모세포는 세포분열이 pH에 따라 조절(Cell-Division Control)되고, UV-C, 분해효소와 은나노입자에 대한 저항성을 가진다. (아래) 원하는 시간에 pH 조절로 금속-폴리페놀박막이 분해되는 것을 형상화
2014.11.18
조회수 17511
-
 신기루 현상 착안해 테라헤르츠파 광학렌즈 개발
무더운 여름, 아스팔트 도로에 물웅덩이가 보이다가 가까이 다가가면 사라지고 좀 가다보면 또 물웅덩이가 나타난다. ‘신기루’라고 불리는 이 현상은 지표면 가까운 공기층의 큰 온도차로 인한 공기밀도 변화로 빛이 굴절되기 때문이다.
우리 학교 바이오및뇌공학과 정기훈 교수는 물리학과 안재욱 교수와 신기루 현상에서 착안한 물리적 효과를 이용해 테라헤르츠파 굴절률 분포형 렌즈를 세계 최초로 개발했다.
실리콘 소재를 곡면으로 가공해 만드는 카메라렌즈에 사용되는 기존방식과는 달리 이번에 개발된 렌즈는 평평한 실리콘 웨이퍼를 소재로 반도체 양산공정으로 제작해 비용을 최대 1/100 수준으로 낮출 수 있으며 제작시간도 훨씬 단축시킬 수 있다. 광원 추출효율은 4배 이상 향상시켰다.
테라헤르츠파는 0.1THz~30THz(테라헤르츠, 1조헤르츠) 대역의 전자기파로 가시광선이나 적외선보다 파장이 길어 X선처럼 물체의 내부를 높은 해상도로 정확히 식별할 수 있어 보안검색, 의료영상기술 등 비파괴 검사 도구나 의료용 진단기구의 성능을 획기적으로 향상시킬 수 있을 것으로 전망된다.
그러나 넓은 대역의 주파수 특성으로 인해 손실되는 전자기파의 비율이 높아 테라헤르츠파를 높은 효율로 집중시킬 수 있는 광학소자 개발이 요구됐다.
정 교수 연구팀은 평평한 실리콘에 테라헤르츠파 파장(약 300㎛) 보다 작은 80~120㎛ 크기의 구멍을 반도체 양산방법인 광식각공정으로 만들었다. 렌즈 가장자리로 갈수록 홀 사이즈는 크게 만들었다.
테라헤르츠파를 쪼이자 공기와 실리콘 중 공기 비율이 높은 가장자리는 굴절률이 낮았으며, 상대적으로 공기의 비율이 낮은 가운데는 굴절률이 높았다. 평평한 소재를 광학특성을 공학적으로 설계해 빛을 모으는 볼록렌즈와 같은 기능을 한 것으로 신기루 현상과 같은 물리적 효과와 같다.
이번 연구를 주도한 정기훈 교수는 “자연현상에서 착안해 자연계에 존재하지 않는 다양한 광학특성을 띄는 메타물질을 인공적으로 만든 것”이라며 “물질적 제약으로 인해 다양한 광학소자개발이 더딘 테라헤르츠파 기술 진보에 상당한 도움이 될 것”이라고 연구의의를 밝혔다.
미래창조과학부가 지원하는 한국연구재단의 도약연구자지원사업, 그린나노기술개발사업, 글로벌프론티어사업의 일환으로 수행된 이번 연구는 미국물리협회에서 발간하는 귄위 있는 국제학술지인 ‘어플라이드 피직스 레터(Applied Physics Letter)’에 9월자 특집논문 및 표지논문(제1저자 박상길 박사과정)으로 게재됐다.
그림1. 유전체 메타물질을 이용한 실리콘 굴절률 분포형 렌즈. 머리카락 굵기(80~120µm) 수준의 구멍이 실리콘 기판에 서로 다른 크기로 형성돼 있다.
그림2. 굴절률 분포형 렌즈 원리
그림3. 신기루 현상신기루는 아스팔트 도로 위에서 흔하게 나타나는 대기 굴절 현상이다. 이 현상은 도로면이 물체를 반사하는 것처럼 보이게 하는데 이 때문에 도로면에 물웅덩이가 있는 것처럼 착각하게 된다. 아래 사진에는 멀리서 다가오는 차의 상이 도로면을 통해 보인다. <사진 : 경기북과학고등학교 조영우 선생님 제공>
그림4. 논문표지
신기루 현상 착안해 테라헤르츠파 광학렌즈 개발
무더운 여름, 아스팔트 도로에 물웅덩이가 보이다가 가까이 다가가면 사라지고 좀 가다보면 또 물웅덩이가 나타난다. ‘신기루’라고 불리는 이 현상은 지표면 가까운 공기층의 큰 온도차로 인한 공기밀도 변화로 빛이 굴절되기 때문이다.
우리 학교 바이오및뇌공학과 정기훈 교수는 물리학과 안재욱 교수와 신기루 현상에서 착안한 물리적 효과를 이용해 테라헤르츠파 굴절률 분포형 렌즈를 세계 최초로 개발했다.
실리콘 소재를 곡면으로 가공해 만드는 카메라렌즈에 사용되는 기존방식과는 달리 이번에 개발된 렌즈는 평평한 실리콘 웨이퍼를 소재로 반도체 양산공정으로 제작해 비용을 최대 1/100 수준으로 낮출 수 있으며 제작시간도 훨씬 단축시킬 수 있다. 광원 추출효율은 4배 이상 향상시켰다.
테라헤르츠파는 0.1THz~30THz(테라헤르츠, 1조헤르츠) 대역의 전자기파로 가시광선이나 적외선보다 파장이 길어 X선처럼 물체의 내부를 높은 해상도로 정확히 식별할 수 있어 보안검색, 의료영상기술 등 비파괴 검사 도구나 의료용 진단기구의 성능을 획기적으로 향상시킬 수 있을 것으로 전망된다.
그러나 넓은 대역의 주파수 특성으로 인해 손실되는 전자기파의 비율이 높아 테라헤르츠파를 높은 효율로 집중시킬 수 있는 광학소자 개발이 요구됐다.
정 교수 연구팀은 평평한 실리콘에 테라헤르츠파 파장(약 300㎛) 보다 작은 80~120㎛ 크기의 구멍을 반도체 양산방법인 광식각공정으로 만들었다. 렌즈 가장자리로 갈수록 홀 사이즈는 크게 만들었다.
테라헤르츠파를 쪼이자 공기와 실리콘 중 공기 비율이 높은 가장자리는 굴절률이 낮았으며, 상대적으로 공기의 비율이 낮은 가운데는 굴절률이 높았다. 평평한 소재를 광학특성을 공학적으로 설계해 빛을 모으는 볼록렌즈와 같은 기능을 한 것으로 신기루 현상과 같은 물리적 효과와 같다.
이번 연구를 주도한 정기훈 교수는 “자연현상에서 착안해 자연계에 존재하지 않는 다양한 광학특성을 띄는 메타물질을 인공적으로 만든 것”이라며 “물질적 제약으로 인해 다양한 광학소자개발이 더딘 테라헤르츠파 기술 진보에 상당한 도움이 될 것”이라고 연구의의를 밝혔다.
미래창조과학부가 지원하는 한국연구재단의 도약연구자지원사업, 그린나노기술개발사업, 글로벌프론티어사업의 일환으로 수행된 이번 연구는 미국물리협회에서 발간하는 귄위 있는 국제학술지인 ‘어플라이드 피직스 레터(Applied Physics Letter)’에 9월자 특집논문 및 표지논문(제1저자 박상길 박사과정)으로 게재됐다.
그림1. 유전체 메타물질을 이용한 실리콘 굴절률 분포형 렌즈. 머리카락 굵기(80~120µm) 수준의 구멍이 실리콘 기판에 서로 다른 크기로 형성돼 있다.
그림2. 굴절률 분포형 렌즈 원리
그림3. 신기루 현상신기루는 아스팔트 도로 위에서 흔하게 나타나는 대기 굴절 현상이다. 이 현상은 도로면이 물체를 반사하는 것처럼 보이게 하는데 이 때문에 도로면에 물웅덩이가 있는 것처럼 착각하게 된다. 아래 사진에는 멀리서 다가오는 차의 상이 도로면을 통해 보인다. <사진 : 경기북과학고등학교 조영우 선생님 제공>
그림4. 논문표지
2014.09.24
조회수 24747
-
 종이 한 장으로 구제역 조기 진단 가능해진다
지난 2010년 11월 말 경북 안동에서 시작돼 이듬해 4월 초까지 전국으로 퍼졌던 구제역파동은 직접적인 피해액만 3조원으로 추산되며 경제 전반에 미친 파급효과는 5조원 이상이라는 분석도 있다.
구제역과 같은 전염성 강한 질병을 현장에서 즉시 진단할 수 없기 때문에 피해가 확산될 가능성이 높다. 의심신고가 들어오면 시료를 채취해 전문기관에서 분석하는 데만 2~3일 걸린다. 그 사이 바이러스는 걷잡을 수 없이 퍼진다.
구제역, 조류독감, 신종플루 등 전염성이 강한 질병 진단을 위한 바이오센서를 저렴한 가격에 만들 수 있게 됐다.
우리 학교 생명화학공학과 정기준·임성갑(41) 교수 공동연구팀은 종이나 비닐 등 다양한 물질에 항체를 고정하는데 성공해 보급형 바이오센서개발에 필요한 원천기술을 확보했다.
연구결과는 세계적 학술지 ‘폴리머 케미스트리(Polymer Chemistry)’ 후면 표지논문(7월 7일자)으로 게재됐다.
바이오센서의 기판은 안정성이 높은 금이나 유리를 주로 사용한다. 그러나 가격이 비싸고 휴대성이 떨어지기 때문에 현장에서 쓰기 어렵다.
게다가 항원 진단을 위해 사용되는 항체의 높은 생산 단가로 인해 진단시스템의 가격이 비싸 축산농가 등에 보급이 어려웠다.
연구팀은 기존에 있던 두 가지 핵심기술을 보급형 바이오센서 개발에 활용했다.
연구팀은 바이오센서의 제조단가를 획기적으로 줄이는 동시에 휴대성을 높이기 위해 초기 화학적 진공증착법(iCVD, Initiated chemical vapour deposition)으로 종이나 비닐에 고분자 박막을 증착했다. 또 박막과의 화학적 반응을 통해 항체 단백질을 안정적으로 고정하는데도 성공했다.
이와 함께 가격이 비싸고 고온에 견디지 못했던 기존의 항체 대신, 미생물을 기반으로 만들어 저렴하면서도 70℃의 높은 온도에서도 뛰어난 안정성을 보여주는 ‘크링글도메인’이라는 유사항체를 활용했다.
그 결과 연구팀은 기존 진단시스템의 고비용·불안정성 문제를 동시에 해결했다.
이번 연구를 주도한 정기준 교수는 “기판을 종이나 비닐로 대체하고 유사항체를 활용해 지금보다 훨씬 저렴하면서도 안정성 높은 바이오센서를 만드는 것이 핵심기술”이라고 설명했다.
이와 함께 “최근 국내에서 발병해 국민경제에 커다란 피해를 유발했던 구제역처럼 급속한 전파력을 갖는 바이러스성 질병을 현장에서 신속하게 진단할 수 있을 것”이라며 “향후 포스트잇 또는 책자 형태로 바이오센서를 만들어 축산농가에 보급되면 전수조사가 가능해져 무조건적인 살처분을 막고 샘플링검사로 인한 부정확성을 줄일 수 있을 것”이라고 말했다.
한편, 이번 연구는 미래창조과학부 신기술융합형 성장동력사업(바이오제약) 및 글로벌프론티어사업(차세대바이오매스연구단)의 지원을 받아 수행됐다.
그림1. 종이 비닐 등 다양한 표면 물질 위에 단백질을 고정화하는 기술의 모식도
그림2. 비닐(a)과 종이(b)에 고정화된 비항체 단백질 골격을 이용한 바이오센서
그림3. 고분자 박막 증착 기술에 기반한 단백질 고정화 시스템 이미지
종이 한 장으로 구제역 조기 진단 가능해진다
지난 2010년 11월 말 경북 안동에서 시작돼 이듬해 4월 초까지 전국으로 퍼졌던 구제역파동은 직접적인 피해액만 3조원으로 추산되며 경제 전반에 미친 파급효과는 5조원 이상이라는 분석도 있다.
구제역과 같은 전염성 강한 질병을 현장에서 즉시 진단할 수 없기 때문에 피해가 확산될 가능성이 높다. 의심신고가 들어오면 시료를 채취해 전문기관에서 분석하는 데만 2~3일 걸린다. 그 사이 바이러스는 걷잡을 수 없이 퍼진다.
구제역, 조류독감, 신종플루 등 전염성이 강한 질병 진단을 위한 바이오센서를 저렴한 가격에 만들 수 있게 됐다.
우리 학교 생명화학공학과 정기준·임성갑(41) 교수 공동연구팀은 종이나 비닐 등 다양한 물질에 항체를 고정하는데 성공해 보급형 바이오센서개발에 필요한 원천기술을 확보했다.
연구결과는 세계적 학술지 ‘폴리머 케미스트리(Polymer Chemistry)’ 후면 표지논문(7월 7일자)으로 게재됐다.
바이오센서의 기판은 안정성이 높은 금이나 유리를 주로 사용한다. 그러나 가격이 비싸고 휴대성이 떨어지기 때문에 현장에서 쓰기 어렵다.
게다가 항원 진단을 위해 사용되는 항체의 높은 생산 단가로 인해 진단시스템의 가격이 비싸 축산농가 등에 보급이 어려웠다.
연구팀은 기존에 있던 두 가지 핵심기술을 보급형 바이오센서 개발에 활용했다.
연구팀은 바이오센서의 제조단가를 획기적으로 줄이는 동시에 휴대성을 높이기 위해 초기 화학적 진공증착법(iCVD, Initiated chemical vapour deposition)으로 종이나 비닐에 고분자 박막을 증착했다. 또 박막과의 화학적 반응을 통해 항체 단백질을 안정적으로 고정하는데도 성공했다.
이와 함께 가격이 비싸고 고온에 견디지 못했던 기존의 항체 대신, 미생물을 기반으로 만들어 저렴하면서도 70℃의 높은 온도에서도 뛰어난 안정성을 보여주는 ‘크링글도메인’이라는 유사항체를 활용했다.
그 결과 연구팀은 기존 진단시스템의 고비용·불안정성 문제를 동시에 해결했다.
이번 연구를 주도한 정기준 교수는 “기판을 종이나 비닐로 대체하고 유사항체를 활용해 지금보다 훨씬 저렴하면서도 안정성 높은 바이오센서를 만드는 것이 핵심기술”이라고 설명했다.
이와 함께 “최근 국내에서 발병해 국민경제에 커다란 피해를 유발했던 구제역처럼 급속한 전파력을 갖는 바이러스성 질병을 현장에서 신속하게 진단할 수 있을 것”이라며 “향후 포스트잇 또는 책자 형태로 바이오센서를 만들어 축산농가에 보급되면 전수조사가 가능해져 무조건적인 살처분을 막고 샘플링검사로 인한 부정확성을 줄일 수 있을 것”이라고 말했다.
한편, 이번 연구는 미래창조과학부 신기술융합형 성장동력사업(바이오제약) 및 글로벌프론티어사업(차세대바이오매스연구단)의 지원을 받아 수행됐다.
그림1. 종이 비닐 등 다양한 표면 물질 위에 단백질을 고정화하는 기술의 모식도
그림2. 비닐(a)과 종이(b)에 고정화된 비항체 단백질 골격을 이용한 바이오센서
그림3. 고분자 박막 증착 기술에 기반한 단백질 고정화 시스템 이미지
2014.07.16
조회수 17083
-
 고효율 나노발전기 상용화길 열어
아주 작은 움직임으로도 전기를 생산하는 나노발전기가 개발됐다. 몸에 붙이고 다니면 충전되는 웨어러블 전자기기 전력원 등 다양한 활용이 기대된다.
우리 학교 신소재공학과 이건재 교수팀은 레이저 박리 전사기술과 유연한 압전박막 소재를 활용해 기존보다 약 40배 높은 효율을 갖는 나노발전기 개발에 성공했다.
연구결과는 세계적 학술지 ‘어드밴스드 머티리얼스(Advanced Materials)’ 4월 23일자 표지논문으로 게재됐다.
나노발전기는 유연한 나노소재에 미세한 압력이나 구부러짐이 가해질 때 전기 에너지가 생성되는 기술이다. 전선과 배터리 없이도 에너지공급이 가능하기 때문에 휘어지는 전자제품은 물론 심장 박동기와 같이 몸속에 집어넣는 기기나 로봇의 에너지원으로도 활용 가능하다. 그러나 지금까지는 에너지 효율이 낮고 제작공정이 복잡해 상용화가 어려웠다.
이 교수 연구팀은 고온에서 결정화된 고효율 압전박막물질을 현재 상용화된 레이저 박리기술을 이용해 딱딱한 기판에서 플라스틱 기판으로 전사, 효율을 크게 향상시키면서도 대면적으로 양산 가능성을 높였다.
이번에 개발된 유연한 기판(2cm × 2cm)에 만들어진 나노발전기는 미세한 구부림에 의해 생성된 에너지(250V, 8㎂)로 105개의 LED를 작동시키는데 성공했다.
이 교수는 “이번에 개발된 고효율의 나노발전기술은 자연에서 발생하는 바람, 진동, 소리와 같은 미세한 에너지는 물론 심장박동, 혈액흐름, 근육수축·이완 등 사람 몸에서 발생되는 생체역학적 힘을 이용해 전기를 생산할 수 있는 무한 에너지원으로 사용될 수 있다”고 응용가능성에 대해 설명했다.
이와 함께 “발전효율이 세계최고기록보다 40여배 높고 대량 양산이 가능한 레이저 박리기술을 활용해 그동안 상용화를 가로막았던 저효율과 복잡한 제조공정의 문제점을 해결했다는데 큰 의의가 있다”고 말했다.
이 교수팀은 향후 압전박막물질을 삼차원으로 적층해 생성전력을 더욱 높이고 이를 동물에 이식하는 생체실험을 수행할 계획이다.
이번 연구결과는 미래창조과학부 도약연구사업과 ‘코오롱-카이스트 라이프스타일 이노베이션센터(KOLON-KAIST LifeStyle Innovation Center)’의 지원으로 수행됐다.
그림1. 레이저 박리 기술로 제작된 대면적 형태의 나노발전기 이미지(논문표지)
그림2. 플라스틱에 제작된 나노발전기에서 생성된 전력을 이용해 105개의 LED를 작동하는 모습
고효율 나노발전기 상용화길 열어
아주 작은 움직임으로도 전기를 생산하는 나노발전기가 개발됐다. 몸에 붙이고 다니면 충전되는 웨어러블 전자기기 전력원 등 다양한 활용이 기대된다.
우리 학교 신소재공학과 이건재 교수팀은 레이저 박리 전사기술과 유연한 압전박막 소재를 활용해 기존보다 약 40배 높은 효율을 갖는 나노발전기 개발에 성공했다.
연구결과는 세계적 학술지 ‘어드밴스드 머티리얼스(Advanced Materials)’ 4월 23일자 표지논문으로 게재됐다.
나노발전기는 유연한 나노소재에 미세한 압력이나 구부러짐이 가해질 때 전기 에너지가 생성되는 기술이다. 전선과 배터리 없이도 에너지공급이 가능하기 때문에 휘어지는 전자제품은 물론 심장 박동기와 같이 몸속에 집어넣는 기기나 로봇의 에너지원으로도 활용 가능하다. 그러나 지금까지는 에너지 효율이 낮고 제작공정이 복잡해 상용화가 어려웠다.
이 교수 연구팀은 고온에서 결정화된 고효율 압전박막물질을 현재 상용화된 레이저 박리기술을 이용해 딱딱한 기판에서 플라스틱 기판으로 전사, 효율을 크게 향상시키면서도 대면적으로 양산 가능성을 높였다.
이번에 개발된 유연한 기판(2cm × 2cm)에 만들어진 나노발전기는 미세한 구부림에 의해 생성된 에너지(250V, 8㎂)로 105개의 LED를 작동시키는데 성공했다.
이 교수는 “이번에 개발된 고효율의 나노발전기술은 자연에서 발생하는 바람, 진동, 소리와 같은 미세한 에너지는 물론 심장박동, 혈액흐름, 근육수축·이완 등 사람 몸에서 발생되는 생체역학적 힘을 이용해 전기를 생산할 수 있는 무한 에너지원으로 사용될 수 있다”고 응용가능성에 대해 설명했다.
이와 함께 “발전효율이 세계최고기록보다 40여배 높고 대량 양산이 가능한 레이저 박리기술을 활용해 그동안 상용화를 가로막았던 저효율과 복잡한 제조공정의 문제점을 해결했다는데 큰 의의가 있다”고 말했다.
이 교수팀은 향후 압전박막물질을 삼차원으로 적층해 생성전력을 더욱 높이고 이를 동물에 이식하는 생체실험을 수행할 계획이다.
이번 연구결과는 미래창조과학부 도약연구사업과 ‘코오롱-카이스트 라이프스타일 이노베이션센터(KOLON-KAIST LifeStyle Innovation Center)’의 지원으로 수행됐다.
그림1. 레이저 박리 기술로 제작된 대면적 형태의 나노발전기 이미지(논문표지)
그림2. 플라스틱에 제작된 나노발전기에서 생성된 전력을 이용해 105개의 LED를 작동하는 모습
2014.05.15
조회수 21469
-
 건강한 망막혈관 생성을 유도하는 치료방법 개발
- 향후 당뇨망막병증 치료방법으로 적용 기대
우리 학교 연구진이 실명으로 이어질 수 있는 망막혈관 질환치료의 실마리를 찾아냈다. 혈액공급이 잘되지 않는 망막 부위로 건강한 망막혈관이 생성되도록 하여 망막신경을 보호하는 혈관생성단백질을 찾아낸 것. 향후 당뇨망막병증*과 미숙아망막병증**의 치료방법 개선을 위한 연구의 단초가 될 것으로 기대된다.
이번 연구결과는 국내에서 전문적인 기초과학 교육을 받고 있는 안과 전문의 연구원에 의해 이루어진 대표적인 중개연구의 결과여서 더욱 주목받고 있다.
* 미숙아망막병증 : 망막 혈관의 발달이 완성되지 않은 시기에 출생한 미숙아에서 발생하는 망막 혈관질환으로 소아실명의 가장 흔한 원인 질환이다.
* 당뇨망막병증 : 당뇨병의 합병증으로 망막조직으로의 불충분한 혈액공급으로 생기는 망막 혈관질환으로 성인실명의 중요한 원인 질환이다.
우리 학교 의과학대학원 이준엽 연구원이(안과 전문의, 지도교수: 고규영,유욱준) 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)의 지원으로 수행되었고, 연구결과는 사이언스 중개의학(Science Translational Medicine) 표지논문(9월 18일자)으로 소개되었다. 이 학술지는 임상의학과 기초과학을 연계하는 중개의학 분야 권위지로 사이언스지 자매지이다.
(논문명 : Angiopoietin-1 Guides Directional Angiogenesis Through Integrin αvβ5 Signaling for Recovery of Ischemic Retinopathy)
당뇨망막병증의 치료에는 망막조직을 파괴하는 레이저광응고술이나혈관증식과 혈액누출을 억제하는 항체치료제*가 적용되고 있다.
항체치료제는 망막신경을 파괴하지 않는 장점이 있지만 한시적으로 혈관증식을 억제할 뿐, 근본적인 해결이 아니어서 반복적인 치료가 필요하다는 한계가 있었다.
* 항체치료제 : 비정상적인 혈관증식과 혈액누출을 선택적으로 억제하기 위하여 개발된 항체로서, 현재 혈관내피세포성장인자 (VEGF)를 저해하는 아바스틴 (Avastin) 과 루센티스 (Lucentis) 가 대표적인 항체치료제이다.
연구팀은 개체의 발달과정에서 혈관의 생성과 안정화에 필수적이라고 알려진 안지오포이에틴-1* 단백질이 망막혈관의 생성과정에도 중요한 역할을 함을 동물실험을 통해 규명해냈다.
망막출혈에 의한 시력상실의 근본 원인이 되는 망막허혈**을 개선하고 망막신경을 보호하는 단백질을 알아낸 것이다.
망막조직으로 충분한 혈액을 공급해 망막신경의 기능을 보존하는 방식의 근본적인 치료방법 개발의 실마리가 될 것으로 기대된다.
* 망막허혈 : 망막 조직에 충분한 혈액 공급이 되지 않는 상태
* 안지오포이에틴-1(Angiopoietin-1) : 건강한 혈관의 생성을 유도하고 생성된 혈관의 안정화를 유지하는 데 중요한 성장인자.
실제 안지오포이에틴-1을 망막병증 생쥐모델의 안구에 투약한 결과 건강한 망막혈관의 생성이 촉진되어, 망막허혈에 따르는 비정상적인 혈관증식이나 망막출혈, 시력상실이 예방되었다.
이준엽 연구원은 “이번 연구는 안지오포이에틴-1이 망막혈관의 생성과 안정화에 중요한 인자라는 사실을 새롭게 규명함으로써 혈관생성을 억제하는 현재의 치료법에서 건강한 혈관을 생성하고 혈관의 기능을 강화하는 방식의 치료법으로 패러다임이 전환될 것을 기대한다”고 연구 의의를 밝혔다.
그림 1. 망막병증 생쥐모델에서의 안구 내 투여한 Angiopoietin-1의 역할 대조군에 비해 VEGF-Trap 치료군과 Angiopoietin-1 (Ang1) 치료군은 병적인 혈관의 증식을 유의하게 억제함 (아래), 추가적으로 Ang1 치료군은 망막 중심부의 무혈관부위(망막허혈)를 향하여 혈관이 생성되었고, 이러한 현상은 VEGF-Trap 치료군에서는 관찰되지 않음 (위).
그림 2. Angiopoietin-1에 의한 망막허혈과 망막 출혈의 감소 및 혈관의 정상화 (좌) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막허혈부위 면적(화살표)을 유의하게 감소시켰으며, 망막 출혈의 양도 Ang1 치료에 의해 감소함. (우) Ang1 에 의해 새롭게 형성된 혈관은 정상 망막 혈관과 같이 혈관주위세포에 의한 지지를 받는 구조적으로 안정된 혈관임.
그림 3. Angiopoietin-1에 의한 망막 신경 보호 효과 (위) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막 중앙부 와 주변부의 신경세포의 세포자멸사를 유의하게 억제함. (아래) 이러한 Ang1에 의한 망막 신경 보호 효과는 전기 생리학적 검사인 망막전위도 검사를 통해 확인됨.
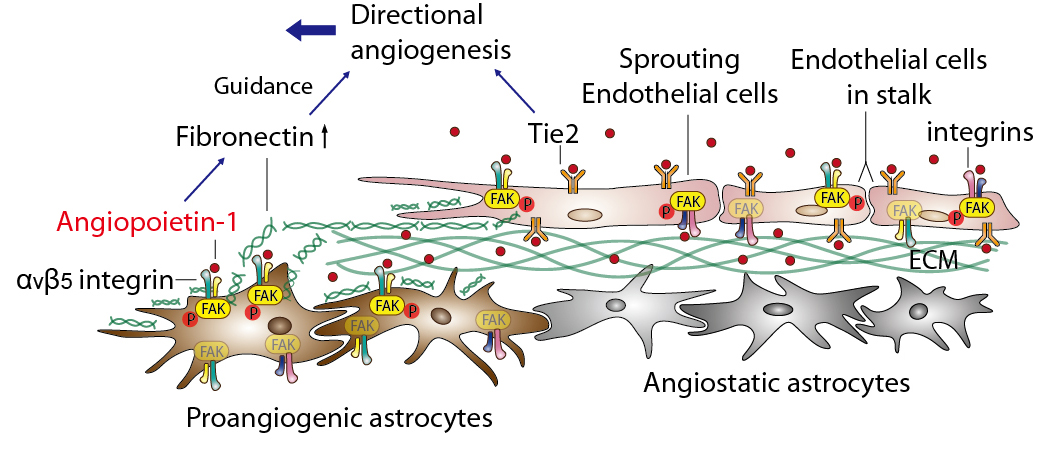
그림 4. Angiopoietin-1 이 망막 혈관 생성을 유도하는 기전 Angiopoietin-1은 망막 혈관의 내피세포 (Endothelial cell) 에 작용하여 혈관의 안정성 유지에 중요한 역할을 할 뿐만 아니라 망막의 별아교세포 (Astrocyte) 의 integrin 수용체를 통하여 fibronectin 이라는 세포외기질의 생성을 증가시켜 망막 조직 내로의 혈관 생성의 경로를 안내하는 역할을 함.
건강한 망막혈관 생성을 유도하는 치료방법 개발
- 향후 당뇨망막병증 치료방법으로 적용 기대
우리 학교 연구진이 실명으로 이어질 수 있는 망막혈관 질환치료의 실마리를 찾아냈다. 혈액공급이 잘되지 않는 망막 부위로 건강한 망막혈관이 생성되도록 하여 망막신경을 보호하는 혈관생성단백질을 찾아낸 것. 향후 당뇨망막병증*과 미숙아망막병증**의 치료방법 개선을 위한 연구의 단초가 될 것으로 기대된다.
이번 연구결과는 국내에서 전문적인 기초과학 교육을 받고 있는 안과 전문의 연구원에 의해 이루어진 대표적인 중개연구의 결과여서 더욱 주목받고 있다.
* 미숙아망막병증 : 망막 혈관의 발달이 완성되지 않은 시기에 출생한 미숙아에서 발생하는 망막 혈관질환으로 소아실명의 가장 흔한 원인 질환이다.
* 당뇨망막병증 : 당뇨병의 합병증으로 망막조직으로의 불충분한 혈액공급으로 생기는 망막 혈관질환으로 성인실명의 중요한 원인 질환이다.
우리 학교 의과학대학원 이준엽 연구원이(안과 전문의, 지도교수: 고규영,유욱준) 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)의 지원으로 수행되었고, 연구결과는 사이언스 중개의학(Science Translational Medicine) 표지논문(9월 18일자)으로 소개되었다. 이 학술지는 임상의학과 기초과학을 연계하는 중개의학 분야 권위지로 사이언스지 자매지이다.
(논문명 : Angiopoietin-1 Guides Directional Angiogenesis Through Integrin αvβ5 Signaling for Recovery of Ischemic Retinopathy)
당뇨망막병증의 치료에는 망막조직을 파괴하는 레이저광응고술이나혈관증식과 혈액누출을 억제하는 항체치료제*가 적용되고 있다.
항체치료제는 망막신경을 파괴하지 않는 장점이 있지만 한시적으로 혈관증식을 억제할 뿐, 근본적인 해결이 아니어서 반복적인 치료가 필요하다는 한계가 있었다.
* 항체치료제 : 비정상적인 혈관증식과 혈액누출을 선택적으로 억제하기 위하여 개발된 항체로서, 현재 혈관내피세포성장인자 (VEGF)를 저해하는 아바스틴 (Avastin) 과 루센티스 (Lucentis) 가 대표적인 항체치료제이다.
연구팀은 개체의 발달과정에서 혈관의 생성과 안정화에 필수적이라고 알려진 안지오포이에틴-1* 단백질이 망막혈관의 생성과정에도 중요한 역할을 함을 동물실험을 통해 규명해냈다.
망막출혈에 의한 시력상실의 근본 원인이 되는 망막허혈**을 개선하고 망막신경을 보호하는 단백질을 알아낸 것이다.
망막조직으로 충분한 혈액을 공급해 망막신경의 기능을 보존하는 방식의 근본적인 치료방법 개발의 실마리가 될 것으로 기대된다.
* 망막허혈 : 망막 조직에 충분한 혈액 공급이 되지 않는 상태
* 안지오포이에틴-1(Angiopoietin-1) : 건강한 혈관의 생성을 유도하고 생성된 혈관의 안정화를 유지하는 데 중요한 성장인자.
실제 안지오포이에틴-1을 망막병증 생쥐모델의 안구에 투약한 결과 건강한 망막혈관의 생성이 촉진되어, 망막허혈에 따르는 비정상적인 혈관증식이나 망막출혈, 시력상실이 예방되었다.
이준엽 연구원은 “이번 연구는 안지오포이에틴-1이 망막혈관의 생성과 안정화에 중요한 인자라는 사실을 새롭게 규명함으로써 혈관생성을 억제하는 현재의 치료법에서 건강한 혈관을 생성하고 혈관의 기능을 강화하는 방식의 치료법으로 패러다임이 전환될 것을 기대한다”고 연구 의의를 밝혔다.
그림 1. 망막병증 생쥐모델에서의 안구 내 투여한 Angiopoietin-1의 역할 대조군에 비해 VEGF-Trap 치료군과 Angiopoietin-1 (Ang1) 치료군은 병적인 혈관의 증식을 유의하게 억제함 (아래), 추가적으로 Ang1 치료군은 망막 중심부의 무혈관부위(망막허혈)를 향하여 혈관이 생성되었고, 이러한 현상은 VEGF-Trap 치료군에서는 관찰되지 않음 (위).
그림 2. Angiopoietin-1에 의한 망막허혈과 망막 출혈의 감소 및 혈관의 정상화 (좌) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막허혈부위 면적(화살표)을 유의하게 감소시켰으며, 망막 출혈의 양도 Ang1 치료에 의해 감소함. (우) Ang1 에 의해 새롭게 형성된 혈관은 정상 망막 혈관과 같이 혈관주위세포에 의한 지지를 받는 구조적으로 안정된 혈관임.
그림 3. Angiopoietin-1에 의한 망막 신경 보호 효과 (위) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막 중앙부 와 주변부의 신경세포의 세포자멸사를 유의하게 억제함. (아래) 이러한 Ang1에 의한 망막 신경 보호 효과는 전기 생리학적 검사인 망막전위도 검사를 통해 확인됨.
그림 4. Angiopoietin-1 이 망막 혈관 생성을 유도하는 기전 Angiopoietin-1은 망막 혈관의 내피세포 (Endothelial cell) 에 작용하여 혈관의 안정성 유지에 중요한 역할을 할 뿐만 아니라 망막의 별아교세포 (Astrocyte) 의 integrin 수용체를 통하여 fibronectin 이라는 세포외기질의 생성을 증가시켜 망막 조직 내로의 혈관 생성의 경로를 안내하는 역할을 함.
2013.09.22
조회수 22612
-
 순수한 그래핀의 양자점 개발 성공
- 수 나노미터 직경의 완전히 순수한 그래핀 양자점 개발 -- “바이오센서, 광센서, 바이오 이미징 등 다양한 분야로 응용 가능” -
우리 학교 생명화학공학과 서태석(42) 교수와 물리학과 조용훈(48) 교수 공동 연구팀은 흑연 나노입자를 이용해 순수한 그래핀 양자점을 개발하는데 성공하고 그래핀 양자점에서의 방출되는 형광 빛의 원인을 밝혔다.
연구결과는 나노분야의 권위 있는 학술지 ‘어드밴스드 머티리얼스(Advanced Materials)’ 7월 19일자 표지논문(Back Cover)으로 게재됐다.
이번에 개발된 그래핀 양자점은 흑연으로 제작돼 인체에 무해한 친환경 소재라는 점에서 바이오센서, 광센서, 바이오 이미징 등 다양한 응용 분야에 적용할 수 있을 것으로 기대된다.
그래핀 양자점은 수 나노미터 이하의 직경을 갖고 있으며, 가시광 영역의 형광을 방출하는 특징이 있다.
기존 그래핀 양자점은 대부분 산화된 그래핀 양자점을 다시 환원하는 방식으로 제작했다. 따라서 그래핀 양자점 구조에 존재하는 순수한 탄소 결합과 산소 결합에 의한 형광 특성이 혼합돼 있어 발광의 근원을 정확하게 구분하기 어려웠다. 또 복잡한 화학적 방법으로 제작해 생산성이 떨어졌다.
연구팀은 그래핀 양자점의 정확한 발광 원인을 규명하기 위해 수 나노미터 크기의 흑연 나노입자를 이용해 순수한 그래핀 양자점을 산화반응 과정 없이 제작했다. 또 일반적으로 사용되고 있는 산화 과정을 흑연 나노입자에 적용해 산화 그래핀 양자점을 간단하게 제작하는 방법도 개발했다.
연구팀은 개발된 순수한 그래핀 양자점과 산화 그래핀 양자점으로부터 각각 파란색과 녹색 형광의 빛을 방출하는 것을 확인했는데, 이 두 종류의 양자점들은 산소 결합의 유무에 근본적 차이가 있다는 것을 밝혔다.
이와 함께 다양한 광분석 기법을 이용해 순수한 그래핀 양자점의 파란색 형광 현상이 벤젠 형태의 탄소 결합에 의한 것임을 규명하고, 산화 그래핀 양자점의 녹색 발광이 그래핀에 결합된 다양한 산소 기능기에 의한 것임을 규명했다.
서태석 교수는 “순수한 그래핀 양자점의 개발과 발광 특성 분석을 통해 기존에 뚜렷하게 설명되지 않았던 그래핀 양자점에서의 파란색 형광 빛의 원인을 밝혀냈다”고 이번 연구의 의의를 밝혔다.
KAIST 생명화학공학과 페이 리우(Fei Liu), 물리학과 장민호(제1저자) 박사과정 학생이 서태석, 조용훈 교수의 지도를 받아 수행한 이번 연구는 환경융합 신기술개발사업과 KAIST 나노융합연구소의 그래핀 연구센터 지원으로 수행됐다.
서태석 교수(왼쪽), 조용훈 교수(오른쪽)
순수한 그래핀의 양자점 개발 성공
- 수 나노미터 직경의 완전히 순수한 그래핀 양자점 개발 -- “바이오센서, 광센서, 바이오 이미징 등 다양한 분야로 응용 가능” -
우리 학교 생명화학공학과 서태석(42) 교수와 물리학과 조용훈(48) 교수 공동 연구팀은 흑연 나노입자를 이용해 순수한 그래핀 양자점을 개발하는데 성공하고 그래핀 양자점에서의 방출되는 형광 빛의 원인을 밝혔다.
연구결과는 나노분야의 권위 있는 학술지 ‘어드밴스드 머티리얼스(Advanced Materials)’ 7월 19일자 표지논문(Back Cover)으로 게재됐다.
이번에 개발된 그래핀 양자점은 흑연으로 제작돼 인체에 무해한 친환경 소재라는 점에서 바이오센서, 광센서, 바이오 이미징 등 다양한 응용 분야에 적용할 수 있을 것으로 기대된다.
그래핀 양자점은 수 나노미터 이하의 직경을 갖고 있으며, 가시광 영역의 형광을 방출하는 특징이 있다.
기존 그래핀 양자점은 대부분 산화된 그래핀 양자점을 다시 환원하는 방식으로 제작했다. 따라서 그래핀 양자점 구조에 존재하는 순수한 탄소 결합과 산소 결합에 의한 형광 특성이 혼합돼 있어 발광의 근원을 정확하게 구분하기 어려웠다. 또 복잡한 화학적 방법으로 제작해 생산성이 떨어졌다.
연구팀은 그래핀 양자점의 정확한 발광 원인을 규명하기 위해 수 나노미터 크기의 흑연 나노입자를 이용해 순수한 그래핀 양자점을 산화반응 과정 없이 제작했다. 또 일반적으로 사용되고 있는 산화 과정을 흑연 나노입자에 적용해 산화 그래핀 양자점을 간단하게 제작하는 방법도 개발했다.
연구팀은 개발된 순수한 그래핀 양자점과 산화 그래핀 양자점으로부터 각각 파란색과 녹색 형광의 빛을 방출하는 것을 확인했는데, 이 두 종류의 양자점들은 산소 결합의 유무에 근본적 차이가 있다는 것을 밝혔다.
이와 함께 다양한 광분석 기법을 이용해 순수한 그래핀 양자점의 파란색 형광 현상이 벤젠 형태의 탄소 결합에 의한 것임을 규명하고, 산화 그래핀 양자점의 녹색 발광이 그래핀에 결합된 다양한 산소 기능기에 의한 것임을 규명했다.
서태석 교수는 “순수한 그래핀 양자점의 개발과 발광 특성 분석을 통해 기존에 뚜렷하게 설명되지 않았던 그래핀 양자점에서의 파란색 형광 빛의 원인을 밝혀냈다”고 이번 연구의 의의를 밝혔다.
KAIST 생명화학공학과 페이 리우(Fei Liu), 물리학과 장민호(제1저자) 박사과정 학생이 서태석, 조용훈 교수의 지도를 받아 수행한 이번 연구는 환경융합 신기술개발사업과 KAIST 나노융합연구소의 그래핀 연구센터 지원으로 수행됐다.
서태석 교수(왼쪽), 조용훈 교수(오른쪽)
2013.08.07
조회수 18152
-
 유방암 세포의 자살을 유도하는 최적의 약물조합 발견
조광현 교수
- Science 자매지 표지논문 발표,“IT와 BT의 융합연구로 세포내 분자조절네트워크 제어를 통해 가능”-
국내 연구진이 대다수 암 발생에 직접 관여하는 것으로 알려진 암억제 유전자(p53)의 분자조절네트워크를 제어하여 유방암 세포의 사멸을 유도하는 최적의 약물조합을 찾아내, 향후 신개념 암치료제 개발에 새로운 단초를 열었다. 특히 이번 연구는 IT와 BT의 융합연구인 시스템 생물학 연구로 가능했다는 점에서 의미가 크다.
우리 학교 바이오및뇌공학과 조광현 석좌교수가 주도하고 최민수 박사과정생, 주시 박사, 정성훈 교수 및 시첸 박사과정생이 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약/도전연구)과 기초연구실사업의 지원으로 수행되었다.
연구결과는 세계 최고 과학전문지인 ‘사이언스’의 첫 번째 자매지로서 세포신호전달분야의 권위지인 ‘Science Signaling’지 최신호(11월 20일자) 표지논문으로 선정되었고, 사이언스지의 ‘편집자의 선택(Editor"s Choice)’에 하이라이트 특집기사로 소개되는 영예를 얻었다. (논문명: Attractor Landscape Analysis Reveals Feedback Loops in the p53 Network That Control the Cellular Response to DNA Damage)
유방암은 미국이나 유럽 등 선진국에서 발병하는 여성암 중 가장 흔한 암으로, 40~55세 미국 여성의 사망원인 1위를 차지한다.
지난 10월 15일에는 영국 일간지 ‘데일리메일’이 2040년까지 유방암 환자 수가 현재의 3배가 넘는 168만 명으로 늘어나 일명 “유방암 대란”이 일어날 수도 있다는 충격적인 연구결과를 보도하기도 하였다.
우리나라 보건복지부 자료에 따르면, 국내에서도 미국 등과 같이 유방암 발병빈도가 매년 증가하는 추세인데, 이것은 서구식 식습관과 저출산, 모유수유 기피 등 생활패턴의 변화에 기인한 것으로 알려져 있다.
p53은 ‘유전자의 수호자’로도 잘 알려진 암 억제 단백질로서 33년 전 처음 발견된 후 지금까지 암 치료를 위해 집중적으로 연구되는 분자이다.
p53은 세포의 증식 조절과 사멸 촉진 등 세포의 운명을 결정하는데 중요한 역할을 한다. 우리 몸의 세포가 손상되거나 오작동하면, p53은 세포주기의 진행을 중단시켜 손상된 DNA의 복제를 억제하고, 손상된 세포의 복구를 시도한다. 이 때 만일 세포가 복구될 수 없다고 판단되면, p53은 세포가 스스로 자살하도록 유도한다.
그러나 암세포는 이러한 p53의 기능이 정상적으로 작동되지 않아 이를 인위적으로 조절하여 암 치료에 응용하려는 시도가 꾸준히 이어져왔다. 그러나 지금까지 임상실험에서는 기대와는 달리 효과가 미미하거나 부작용이 발생하는 등 여러 문제점들이 나타났다.
이는 p53이 단독으로 작동하는 것이 아니라 복잡한 신호전달 네트워크 속에서 다수의 양성과 음성 피드백(positive and negative feedbacks)에 의해 조절되고 있었으나, 지금까지 p53만을 단독으로 집중 연구했기 때문이다. 즉, 다양한 피드백 조절에 의해 p53의 동역학적(dynamics) 변화와 기능이 결정되므로, 네트워크 전체를 이해하고 제어하는 시스템 생물학적 접근이 반드시 필요하다.
조광현 교수가 이끈 융합 연구팀은 p53을 중심으로 관련된 모든 실험 데이터를 집대성하여 p53의 조절 네트워크에 대한 수학모형을 구축하였다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 p53의 동역학적 변화 특성에 따른 세포의 운명(증식 또는 사멸) 조절과정을 밝혀내고 이를 효과적으로 제어할 수 있는 방법을 찾아냈다. 그리고 이 방법을 적용한 시뮬레이션 결과를 단일세포실험으로 검증하였다.
조광현 교수팀은 수많은 피드백으로 복잡하게 얽혀 있는 p53 조절 네트워크의 다양한 변이조건에 따른 컴퓨터 시뮬레이션 분석과 세포생물학실험으로, p53의 동역학적 특성과 기능을 결정하는 핵심 조절회로를 발견하고, 이와 같은 p53의 동역학적 특성 변화에 따라 세포의 운명이 달라질 수 있음을 규명하였다.
또한 유방암 세포의 네트워크 모형에서, 위의 분석결과로부터 찾아낸 핵심회로를 억제하는 표적약물(Wip1 억제제)과 기존의 표적항암약물(뉴트린, nutlin-3)을 조합하면 유방암 세포의 사멸을 매우 효율적으로 유도할 수 있음을 발견하였다. 그리고 실제 유방암 세포(MCF7)를 이용한 세포실험을 통해 직접 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 시스템 생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암세포의 조절과정을 네트워크 차원에서 분석하여 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 연구의의를 밝혔다.
한편, 조 교수의 이번 연구 논문은 23일자 사이언스 편집자의 선택(Editors" Choice)으로 선정되는 영예를 얻기도 했다.
여러 양성 및 음성 피드백으로 복잡하게 구성된 p53 조절네트워크
유방암 세포의 자살을 유도하는 최적의 약물조합 발견
조광현 교수
- Science 자매지 표지논문 발표,“IT와 BT의 융합연구로 세포내 분자조절네트워크 제어를 통해 가능”-
국내 연구진이 대다수 암 발생에 직접 관여하는 것으로 알려진 암억제 유전자(p53)의 분자조절네트워크를 제어하여 유방암 세포의 사멸을 유도하는 최적의 약물조합을 찾아내, 향후 신개념 암치료제 개발에 새로운 단초를 열었다. 특히 이번 연구는 IT와 BT의 융합연구인 시스템 생물학 연구로 가능했다는 점에서 의미가 크다.
우리 학교 바이오및뇌공학과 조광현 석좌교수가 주도하고 최민수 박사과정생, 주시 박사, 정성훈 교수 및 시첸 박사과정생이 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약/도전연구)과 기초연구실사업의 지원으로 수행되었다.
연구결과는 세계 최고 과학전문지인 ‘사이언스’의 첫 번째 자매지로서 세포신호전달분야의 권위지인 ‘Science Signaling’지 최신호(11월 20일자) 표지논문으로 선정되었고, 사이언스지의 ‘편집자의 선택(Editor"s Choice)’에 하이라이트 특집기사로 소개되는 영예를 얻었다. (논문명: Attractor Landscape Analysis Reveals Feedback Loops in the p53 Network That Control the Cellular Response to DNA Damage)
유방암은 미국이나 유럽 등 선진국에서 발병하는 여성암 중 가장 흔한 암으로, 40~55세 미국 여성의 사망원인 1위를 차지한다.
지난 10월 15일에는 영국 일간지 ‘데일리메일’이 2040년까지 유방암 환자 수가 현재의 3배가 넘는 168만 명으로 늘어나 일명 “유방암 대란”이 일어날 수도 있다는 충격적인 연구결과를 보도하기도 하였다.
우리나라 보건복지부 자료에 따르면, 국내에서도 미국 등과 같이 유방암 발병빈도가 매년 증가하는 추세인데, 이것은 서구식 식습관과 저출산, 모유수유 기피 등 생활패턴의 변화에 기인한 것으로 알려져 있다.
p53은 ‘유전자의 수호자’로도 잘 알려진 암 억제 단백질로서 33년 전 처음 발견된 후 지금까지 암 치료를 위해 집중적으로 연구되는 분자이다.
p53은 세포의 증식 조절과 사멸 촉진 등 세포의 운명을 결정하는데 중요한 역할을 한다. 우리 몸의 세포가 손상되거나 오작동하면, p53은 세포주기의 진행을 중단시켜 손상된 DNA의 복제를 억제하고, 손상된 세포의 복구를 시도한다. 이 때 만일 세포가 복구될 수 없다고 판단되면, p53은 세포가 스스로 자살하도록 유도한다.
그러나 암세포는 이러한 p53의 기능이 정상적으로 작동되지 않아 이를 인위적으로 조절하여 암 치료에 응용하려는 시도가 꾸준히 이어져왔다. 그러나 지금까지 임상실험에서는 기대와는 달리 효과가 미미하거나 부작용이 발생하는 등 여러 문제점들이 나타났다.
이는 p53이 단독으로 작동하는 것이 아니라 복잡한 신호전달 네트워크 속에서 다수의 양성과 음성 피드백(positive and negative feedbacks)에 의해 조절되고 있었으나, 지금까지 p53만을 단독으로 집중 연구했기 때문이다. 즉, 다양한 피드백 조절에 의해 p53의 동역학적(dynamics) 변화와 기능이 결정되므로, 네트워크 전체를 이해하고 제어하는 시스템 생물학적 접근이 반드시 필요하다.
조광현 교수가 이끈 융합 연구팀은 p53을 중심으로 관련된 모든 실험 데이터를 집대성하여 p53의 조절 네트워크에 대한 수학모형을 구축하였다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 p53의 동역학적 변화 특성에 따른 세포의 운명(증식 또는 사멸) 조절과정을 밝혀내고 이를 효과적으로 제어할 수 있는 방법을 찾아냈다. 그리고 이 방법을 적용한 시뮬레이션 결과를 단일세포실험으로 검증하였다.
조광현 교수팀은 수많은 피드백으로 복잡하게 얽혀 있는 p53 조절 네트워크의 다양한 변이조건에 따른 컴퓨터 시뮬레이션 분석과 세포생물학실험으로, p53의 동역학적 특성과 기능을 결정하는 핵심 조절회로를 발견하고, 이와 같은 p53의 동역학적 특성 변화에 따라 세포의 운명이 달라질 수 있음을 규명하였다.
또한 유방암 세포의 네트워크 모형에서, 위의 분석결과로부터 찾아낸 핵심회로를 억제하는 표적약물(Wip1 억제제)과 기존의 표적항암약물(뉴트린, nutlin-3)을 조합하면 유방암 세포의 사멸을 매우 효율적으로 유도할 수 있음을 발견하였다. 그리고 실제 유방암 세포(MCF7)를 이용한 세포실험을 통해 직접 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 시스템 생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암세포의 조절과정을 네트워크 차원에서 분석하여 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 연구의의를 밝혔다.
한편, 조 교수의 이번 연구 논문은 23일자 사이언스 편집자의 선택(Editors" Choice)으로 선정되는 영예를 얻기도 했다.
여러 양성 및 음성 피드백으로 복잡하게 구성된 p53 조절네트워크
2012.11.23
조회수 18740
-
 곤충 눈을 모사한 무반사 미세렌즈 개발
정기훈 교수
- KAIST 정기훈 교수 연구팀, 세계적 물리학회지에 표지논문으로 게재돼, 국내외 특허출원 중 -
- 반도체 양산공정 그대로 활용할 수 있어 상용화 기대 커 -- 빛 반사율 1%이하로 낮춰 값비싼 무반사 코팅 대체 가능 -
국내 연구진이 곤충의 눈을 모사해 빛의 반사를 최소화한 무반사 미세렌즈를 개발하는데 성공했다. 이 렌즈는 특히 휴대폰, 디지털카메라 등에 적용된 이미지센서에 활용할 수 있는 데다, 기존 반도체 양산 공정을 그대로 활용할 수 있다는 점에서 상용화에 대한 기대가 크다.
우리 학교 바이오및뇌공학과 정기훈 교수 연구팀이 곤충의 눈 표면에 형성된 나노구조를 모사해 저렴하면서도 빛 반사율을 1%이하로 낮춘 무반사 미세렌즈 양산기술을 개발하는 데 성공했다.
KAIST는 정 교수 연구팀이 개발한 이번 기술을 카메라 이미지센서용 미세렌즈에 적용할 경우 집광효율이 높기 때문에 대조 효과와 밝기에 대한 특성이 우수한 고감도 카메라를 만들 수 있다는 점에서 국내외로부터 많은 관심을 받을 것으로 예상된다고 설명했다.
특히 정 교수팀이 개발한 공정은 이미 상용화 중에 있는 기존의 반도체공정을 그대로 활용할 수 있다. 따라서 렌즈 표면에 굴절률이 낮은 막을 여러 번 입히는 기존의 무반사 코팅보다 제품 제작비용이 훨씬 줄어들 것으로 기대된다고 강조했다.
나비, 잠자리 등 곤충의 눈은 대부분 겹눈 2개로 구성돼 있다. 이들 곤충은 겹눈을 형성하는 벌집모양의 낱눈을 약 1만~3만 개를 가지고 있는데, 낱눈에는 수많은 나노 돌기가 빛의 투과를 돕는 역할을 한다.
연구팀은 이 같은 특성을 갖는 곤충의 눈이 오랜 진화를 통해 최적의 조건을 만들어 온 것으로 판단해, 컴퓨터 시뮬레이션을 거쳐 빛이 가장 잘 투과되는 나노 구조라는 것을 알아냈다.
이후 이 구조를 모사해 수십 마이크로미터(㎛) 크기의 카메라 미세렌즈에 적용한 결과 반사율이 기존 10%에서 1%이하로 현격히 감소하는 특성을 확인했다.
정 교수 연구팀은 곤충에서 착안한 무반사 구조를 만들기 위해 기존 반도체 생산에 쓰이는 식각공정을 활용했다.
미세렌즈에 은 박막 코팅을 한 후 저온열처리를 통해 은나노 입자를 미세렌즈 표면에 형성시켰다. 이를 마스크로 삼아 렌즈표면을 건식 식각해 무반사 특성을 갖는 나노구조를 렌즈 곡면에 구현하는 데 성공했다.
정기훈 교수는 “곡면 구조의 카메라 미세렌즈 표면에서 빛의 반사가 심해 집광효율이 감소하는 문제가 있었는데, 몰포나비의 눈에 형성된 나노 구조에 착안해 기술개발에 성공했다”며 “기존 반도체공정을 그대로 이용할 수 있기 때문에 고가의 무 반사 코팅보다 훨씬 저렴한 단가로 카메라 이미지센서용 무반사 미세렌즈에 즉시 적용할 수 있다”고 말했다.
한편, 정기훈 교수가 주도하고 정혁진 박사과정 학생이 참여한 이번 연구는 세계적인 물리학회지 ‘어플라이드 피직스 레터스(Applied Physics Letters)’ 최신호(11월 12일자)에 표지논문으로 게재됐으며 현재 국내외 특허 출원중이다.
그림1. 곤충 겹눈(좌), 곤충의 낱눈(우)을 확대한 현미경 사진
그림2. 곤충 겹눈의 나노돌기 구조를 모사한 고효율 미세렌즈 배열. 무반사 렌즈는 일반 렌즈에 비해 표면 반사를 현격히 감소시켜 무반사 렌즈를 통해 맺힌 이미지의 선명도를 증가시킨다.
그림3. 카메라 이미지센서용 미세렌즈 개발 공정
1) 고분자 미세렌즈 배열 전면에 은 박막을 코팅
2) 가열을 통해 은 박막을 은 나노입자로 변형
3) 은 나노입자를 마스크로 삼아 렌즈 식각
4) 은 나노입자 제거하여 무반사 미세렌즈 배열 완성
그림4. 논문표지
곤충 눈을 모사한 무반사 미세렌즈 개발
정기훈 교수
- KAIST 정기훈 교수 연구팀, 세계적 물리학회지에 표지논문으로 게재돼, 국내외 특허출원 중 -
- 반도체 양산공정 그대로 활용할 수 있어 상용화 기대 커 -- 빛 반사율 1%이하로 낮춰 값비싼 무반사 코팅 대체 가능 -
국내 연구진이 곤충의 눈을 모사해 빛의 반사를 최소화한 무반사 미세렌즈를 개발하는데 성공했다. 이 렌즈는 특히 휴대폰, 디지털카메라 등에 적용된 이미지센서에 활용할 수 있는 데다, 기존 반도체 양산 공정을 그대로 활용할 수 있다는 점에서 상용화에 대한 기대가 크다.
우리 학교 바이오및뇌공학과 정기훈 교수 연구팀이 곤충의 눈 표면에 형성된 나노구조를 모사해 저렴하면서도 빛 반사율을 1%이하로 낮춘 무반사 미세렌즈 양산기술을 개발하는 데 성공했다.
KAIST는 정 교수 연구팀이 개발한 이번 기술을 카메라 이미지센서용 미세렌즈에 적용할 경우 집광효율이 높기 때문에 대조 효과와 밝기에 대한 특성이 우수한 고감도 카메라를 만들 수 있다는 점에서 국내외로부터 많은 관심을 받을 것으로 예상된다고 설명했다.
특히 정 교수팀이 개발한 공정은 이미 상용화 중에 있는 기존의 반도체공정을 그대로 활용할 수 있다. 따라서 렌즈 표면에 굴절률이 낮은 막을 여러 번 입히는 기존의 무반사 코팅보다 제품 제작비용이 훨씬 줄어들 것으로 기대된다고 강조했다.
나비, 잠자리 등 곤충의 눈은 대부분 겹눈 2개로 구성돼 있다. 이들 곤충은 겹눈을 형성하는 벌집모양의 낱눈을 약 1만~3만 개를 가지고 있는데, 낱눈에는 수많은 나노 돌기가 빛의 투과를 돕는 역할을 한다.
연구팀은 이 같은 특성을 갖는 곤충의 눈이 오랜 진화를 통해 최적의 조건을 만들어 온 것으로 판단해, 컴퓨터 시뮬레이션을 거쳐 빛이 가장 잘 투과되는 나노 구조라는 것을 알아냈다.
이후 이 구조를 모사해 수십 마이크로미터(㎛) 크기의 카메라 미세렌즈에 적용한 결과 반사율이 기존 10%에서 1%이하로 현격히 감소하는 특성을 확인했다.
정 교수 연구팀은 곤충에서 착안한 무반사 구조를 만들기 위해 기존 반도체 생산에 쓰이는 식각공정을 활용했다.
미세렌즈에 은 박막 코팅을 한 후 저온열처리를 통해 은나노 입자를 미세렌즈 표면에 형성시켰다. 이를 마스크로 삼아 렌즈표면을 건식 식각해 무반사 특성을 갖는 나노구조를 렌즈 곡면에 구현하는 데 성공했다.
정기훈 교수는 “곡면 구조의 카메라 미세렌즈 표면에서 빛의 반사가 심해 집광효율이 감소하는 문제가 있었는데, 몰포나비의 눈에 형성된 나노 구조에 착안해 기술개발에 성공했다”며 “기존 반도체공정을 그대로 이용할 수 있기 때문에 고가의 무 반사 코팅보다 훨씬 저렴한 단가로 카메라 이미지센서용 무반사 미세렌즈에 즉시 적용할 수 있다”고 말했다.
한편, 정기훈 교수가 주도하고 정혁진 박사과정 학생이 참여한 이번 연구는 세계적인 물리학회지 ‘어플라이드 피직스 레터스(Applied Physics Letters)’ 최신호(11월 12일자)에 표지논문으로 게재됐으며 현재 국내외 특허 출원중이다.
그림1. 곤충 겹눈(좌), 곤충의 낱눈(우)을 확대한 현미경 사진
그림2. 곤충 겹눈의 나노돌기 구조를 모사한 고효율 미세렌즈 배열. 무반사 렌즈는 일반 렌즈에 비해 표면 반사를 현격히 감소시켜 무반사 렌즈를 통해 맺힌 이미지의 선명도를 증가시킨다.
그림3. 카메라 이미지센서용 미세렌즈 개발 공정
1) 고분자 미세렌즈 배열 전면에 은 박막을 코팅
2) 가열을 통해 은 박막을 은 나노입자로 변형
3) 은 나노입자를 마스크로 삼아 렌즈 식각
4) 은 나노입자 제거하여 무반사 미세렌즈 배열 완성
그림4. 논문표지
2012.11.21
조회수 17097
-
 DNA 기반 반도체 핵심 원천기술 개발
박현규 교수
- 분자 비콘을 이용해 모든(8가지) 논리게이트 구현하는 데 성공 -- 스몰(Small)誌 7월호 표지논문으로 실려 -
초소형 미래 바이오전자기기를 구현하기 위한 핵심기술 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 DNA를 이용해 모든 논리게이트를 구현하는 데 성공, 나노분야의 세계적 학술지 ‘스몰(Small)’ 7월호(23일자) 표지논문으로 실렸다.
현재 최첨단 기술로도 10nm(나노미터) 이하의 실리콘 기반 반도체 제작은 불가능한 것으로 알려져 있지만, DNA는 굵기가 2nm 정도로 가늘기 때문에 보다 저렴하면서도 획기적인 집적도를 가진 반도체를 만들 수 있을 것으로 기대된다.
2나노급 반도체가 개발되면 우표 크기의 메모리 반도체에 고화질 영화 10000편을 저장하는 등 현재 상용화중인 20나노급 반도체보다 약 100배의 용량을 담을 수 있게 된다.
DNA는 네 종류의 염기인 아데닌(adenine, A), 시토신(cytosine, C), 구아닌(guanin, G), 티민(thymine, T)이 연속적으로 연결돼 있는데 A는 T와, G는 C와 각각 특이적으로 결합하는 특성을 갖고 있다.
특정 DNA는 특이적으로 결합하는 염기서열을 지닌 또 다른 DNA와 결합해 이중나선 구조를 형성하는 데, 연구팀은 이러한 DNA의 특이적 결합 특성과 구조 변화에 따른 형광신호 특성이 있는 고리모양의 분자 비콘을 이용했다.
연구팀은 생체 DNA물질을 디지털 회로에서 사용되는 논리게이트와 같은 역할을 담당하도록 입력신호로 사용해 고리모양의 DNA가 열리거나 닫히도록 했다.
고리모양 DNA가 열린 형태에서는 형광신호가 증가하고 닫힌 상태에서는 형광 신호가 감소하며 이로 인해 발생하는 형광신호의 변화를 출력신호로 사용했다.
연구팀은 제한적인 시스템만을 구현하는 기존의 논리게이트의 문제점을 극복, 8가지 모든 논리게이트(AND, OR, XOR, INHIBIT, NAND, NOR, XNOR, IMPlCATION)를 구현하는 데 성공해 반도체 기술로써의 적용 가능성을 높였다.
이와 함께, 각각의 논리게이트의 연결을 통한 다중 논리게이트(Multilevel circuits)와 논리게이트의 재생성을 보여주는 데도 성공했다.
박현규 교수는 “하나의 분자 비콘을 모든 게이트 구성을 위한 보편적인 요소로 사용해 저렴하면서도 초고집적 바이오 전자기기의 가능성을 높였다”며 “앞으로 분자 수준의 전자 소자 연구에 큰 변화가 있을 것으로 예상된다”고 말했다.
이번 연구를 주도한 박기수 박사과정 학생(제1저자)은 “DNA는 10개의 염기서열 길이가 3.4nm이고 굵기가 2nm밖에 되지 않는 매우 작은 물질이기 때문에 이를 이용해 전자 소자를 구현하면 획기적인 집적도 향상을 이룰 수 있다”며 “간단한 시스템 디자인을 통해 정확한 논리게이트를 구현해 내 DNA 반도체를 탑재한 바이오컴퓨터가 곧 현실로 다가올 것”이라고 말했다.XOR 게이트 : 입력 DNA A(input A)와 입력 DNA B(input B) 둘 중 하나만 있을 때는 고리모양 DNA가 열려서 형광 신호가 나오고(출력신호 1), DNA A와 B가 모두 없을 경우와 모두 있는 경우에는 고리모양 DNA가 고리모양을 유지하여 형광을 발생하지 않게 함으로써 XOR 논리게이트를 정확하게 구현했다.
DNA 기반 반도체 핵심 원천기술 개발
박현규 교수
- 분자 비콘을 이용해 모든(8가지) 논리게이트 구현하는 데 성공 -- 스몰(Small)誌 7월호 표지논문으로 실려 -
초소형 미래 바이오전자기기를 구현하기 위한 핵심기술 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 DNA를 이용해 모든 논리게이트를 구현하는 데 성공, 나노분야의 세계적 학술지 ‘스몰(Small)’ 7월호(23일자) 표지논문으로 실렸다.
현재 최첨단 기술로도 10nm(나노미터) 이하의 실리콘 기반 반도체 제작은 불가능한 것으로 알려져 있지만, DNA는 굵기가 2nm 정도로 가늘기 때문에 보다 저렴하면서도 획기적인 집적도를 가진 반도체를 만들 수 있을 것으로 기대된다.
2나노급 반도체가 개발되면 우표 크기의 메모리 반도체에 고화질 영화 10000편을 저장하는 등 현재 상용화중인 20나노급 반도체보다 약 100배의 용량을 담을 수 있게 된다.
DNA는 네 종류의 염기인 아데닌(adenine, A), 시토신(cytosine, C), 구아닌(guanin, G), 티민(thymine, T)이 연속적으로 연결돼 있는데 A는 T와, G는 C와 각각 특이적으로 결합하는 특성을 갖고 있다.
특정 DNA는 특이적으로 결합하는 염기서열을 지닌 또 다른 DNA와 결합해 이중나선 구조를 형성하는 데, 연구팀은 이러한 DNA의 특이적 결합 특성과 구조 변화에 따른 형광신호 특성이 있는 고리모양의 분자 비콘을 이용했다.
연구팀은 생체 DNA물질을 디지털 회로에서 사용되는 논리게이트와 같은 역할을 담당하도록 입력신호로 사용해 고리모양의 DNA가 열리거나 닫히도록 했다.
고리모양 DNA가 열린 형태에서는 형광신호가 증가하고 닫힌 상태에서는 형광 신호가 감소하며 이로 인해 발생하는 형광신호의 변화를 출력신호로 사용했다.
연구팀은 제한적인 시스템만을 구현하는 기존의 논리게이트의 문제점을 극복, 8가지 모든 논리게이트(AND, OR, XOR, INHIBIT, NAND, NOR, XNOR, IMPlCATION)를 구현하는 데 성공해 반도체 기술로써의 적용 가능성을 높였다.
이와 함께, 각각의 논리게이트의 연결을 통한 다중 논리게이트(Multilevel circuits)와 논리게이트의 재생성을 보여주는 데도 성공했다.
박현규 교수는 “하나의 분자 비콘을 모든 게이트 구성을 위한 보편적인 요소로 사용해 저렴하면서도 초고집적 바이오 전자기기의 가능성을 높였다”며 “앞으로 분자 수준의 전자 소자 연구에 큰 변화가 있을 것으로 예상된다”고 말했다.
이번 연구를 주도한 박기수 박사과정 학생(제1저자)은 “DNA는 10개의 염기서열 길이가 3.4nm이고 굵기가 2nm밖에 되지 않는 매우 작은 물질이기 때문에 이를 이용해 전자 소자를 구현하면 획기적인 집적도 향상을 이룰 수 있다”며 “간단한 시스템 디자인을 통해 정확한 논리게이트를 구현해 내 DNA 반도체를 탑재한 바이오컴퓨터가 곧 현실로 다가올 것”이라고 말했다.XOR 게이트 : 입력 DNA A(input A)와 입력 DNA B(input B) 둘 중 하나만 있을 때는 고리모양 DNA가 열려서 형광 신호가 나오고(출력신호 1), DNA A와 B가 모두 없을 경우와 모두 있는 경우에는 고리모양 DNA가 고리모양을 유지하여 형광을 발생하지 않게 함으로써 XOR 논리게이트를 정확하게 구현했다.
2012.09.18
조회수 16893
-
 C형 간염 바이러스의 간 손상 메카니즘 규명
- 부작용 없이 간세포 손상 억제하는 치료제 개발 길 열어 -- 의학분야 세계 최고수준 학술지 ‘헤파톨로지’ 9월호 표지논문 장식 -
의사출신으로 구성된 KAIST 연구진이 C형 간염 바이러스 기전을 밝혀내 치료제 개발에 탄력을 받게 됐다.
우리 학교 바이오및뇌공학과 최철희 교수와 의과학대학원 신의철 교수팀이 공동으로 C형 간염 바이러스에 감염된 환자의 간 손상에 대한 메카니즘을 세계 최초로 규명했다.
이번 연구결과로 앞으로 부작용이 없으면서도 간세포 손상이 적은 C형 간염 바이러스 치료제가 개발될 수 있을 것으로 기대된다.
C형 간염은 C형 간염 바이러스(HCV, Hepatitis C virus)에 감염되었을 때 이에 대응하기 위한 신체의 면역반응으로 인해 간에 염증이 생기는 질환이다.
C형 간염 바이러스는 전 세계적으로 약 1억 7천만 명, 그리고 우리나라에서도 1%정도가 감염되어 있는 것으로 추정된다. 감염되면 대부분 만성으로 변하며, 간경변증이나 간암을 유발해 사망할 수 있는 무서운 질병이다.
하지만 2005년 시험관 내 세포에서 C형 간염 바이러스의 감염이 성공하기 전까지는 세포실험이 불가능했고, 침팬지 이외에는 감염시키는 동물이 없어 동물실험이 어려워 연구에 한계가 있었다.
연구팀은 C형 간염 바이러스에 감염시킨 세포주를 이용해 바이러스가 면역을 담당하는 세포에 의해 분비되는 단백질인 종양괴사인자(TNF-α)에 의한 세포의 사멸이 크게 증가하는 메카니즘을 세계 최초로 밝혀냈다.
이와 함께 이러한 작용을 일으키는 바이러스 구성 단백질도 규명에도 성공했다.
기존에는 C형 간염 바이러스가 간 손상을 일으키는 기전을 밝혀내지 못해 주로 바이러스의 증식을 억제하는 데 초점을 맞춰 신약이 개발돼 부작용이 많았다.
이번 연구결과를 통해 바이러스에 의한 간세포 손상을 억제하는 부작용 없는 신약개발이 가능하게 될 것으로 전망된다.
최철희 교수는 “이번 연구를 통해 C형 간염 바이러스가 숙주의 간세포와 어떤 상호 작용을 하는지 밝혀내 감염 환자의 치료법을 획기적으로 개선할 수 있을 것”이라고 말했다.
신의철 교수는 “이번 연구는 기초의학과 응용의학의 융합연구가 성공한 대표적 사례”라며 “앞으로도 다학제간 융합연구를 실시하면 그동안 풀지 못했던 난제들을 효율적으로 해결할 수 있을 것”이라고 강조했다.
한편, 교육과학기술부 미래기반기술개발사업(신약타겟검증연구사업)의 지원을 받아 수행된 이번 연구 결과는 의학 분야의 세계적 학술지인 헤파톨로지(Hepatolog, Impact Factor=11.665) 9월호 표지 논문으로 선정됐다.
□ 연구 세부사항 설명
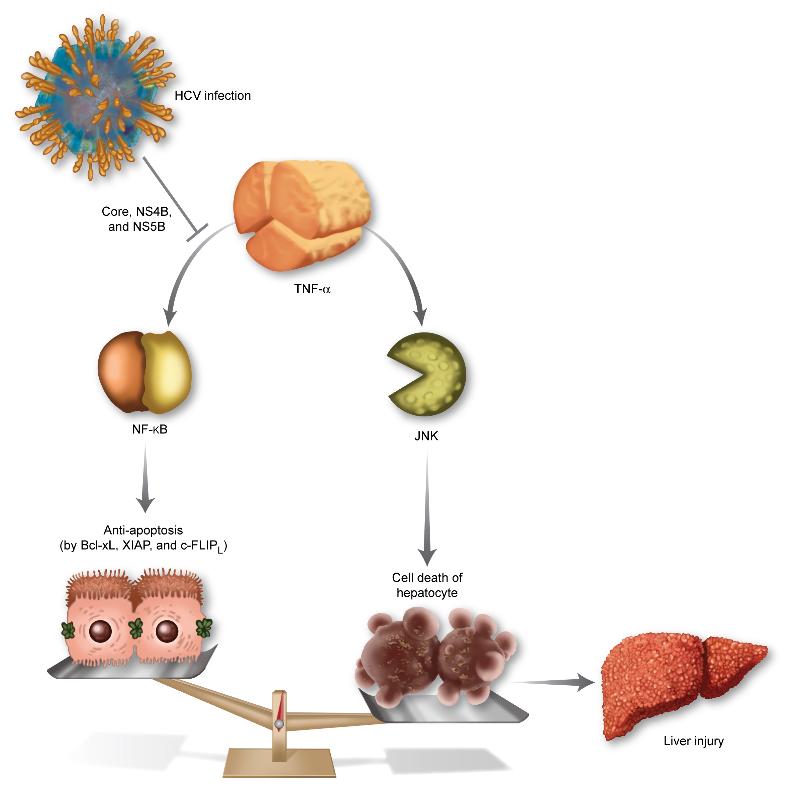
TNF-α(종양괴사인자)는 면역을 담당하는 세포에 의해 분비되는 단백질이다. HCV에 감염되면 바이러스의 증식을 억제하기 위해 체내의 면역작용이 활발해지고 TNF-α의 분비도 늘어난다.
TNF-α는 세포의 생존을 담당하는 NF-κB 신호전달과 세포의 죽음을 담당하는 JNK 신호 전달을 동시에 활성화시킨다. HCV에 감염되면, 세포의 생존을 담당하는 NF-κB 쪽 신호전달 경로만 선택적으로 활성을 억제하게 되고, TNF-α의 역할은 세포의 죽음 쪽으로 균형이 기울게 된다.
바이러스의 증식을 억제하기 위해 분비된 TNF-α가 오히려 간세포를 죽이게 되는 것이다. 이는 곧 간 손상을 뜻하며, HCV를 구성하는 10가지의 단백질 중 core, NF4B, NS5B 라는 단백질이 이러한 작용을 한다고 규명해냈다.
C형 간염 바이러스의 간 손상 메카니즘 규명
- 부작용 없이 간세포 손상 억제하는 치료제 개발 길 열어 -- 의학분야 세계 최고수준 학술지 ‘헤파톨로지’ 9월호 표지논문 장식 -
의사출신으로 구성된 KAIST 연구진이 C형 간염 바이러스 기전을 밝혀내 치료제 개발에 탄력을 받게 됐다.
우리 학교 바이오및뇌공학과 최철희 교수와 의과학대학원 신의철 교수팀이 공동으로 C형 간염 바이러스에 감염된 환자의 간 손상에 대한 메카니즘을 세계 최초로 규명했다.
이번 연구결과로 앞으로 부작용이 없으면서도 간세포 손상이 적은 C형 간염 바이러스 치료제가 개발될 수 있을 것으로 기대된다.
C형 간염은 C형 간염 바이러스(HCV, Hepatitis C virus)에 감염되었을 때 이에 대응하기 위한 신체의 면역반응으로 인해 간에 염증이 생기는 질환이다.
C형 간염 바이러스는 전 세계적으로 약 1억 7천만 명, 그리고 우리나라에서도 1%정도가 감염되어 있는 것으로 추정된다. 감염되면 대부분 만성으로 변하며, 간경변증이나 간암을 유발해 사망할 수 있는 무서운 질병이다.
하지만 2005년 시험관 내 세포에서 C형 간염 바이러스의 감염이 성공하기 전까지는 세포실험이 불가능했고, 침팬지 이외에는 감염시키는 동물이 없어 동물실험이 어려워 연구에 한계가 있었다.
연구팀은 C형 간염 바이러스에 감염시킨 세포주를 이용해 바이러스가 면역을 담당하는 세포에 의해 분비되는 단백질인 종양괴사인자(TNF-α)에 의한 세포의 사멸이 크게 증가하는 메카니즘을 세계 최초로 밝혀냈다.
이와 함께 이러한 작용을 일으키는 바이러스 구성 단백질도 규명에도 성공했다.
기존에는 C형 간염 바이러스가 간 손상을 일으키는 기전을 밝혀내지 못해 주로 바이러스의 증식을 억제하는 데 초점을 맞춰 신약이 개발돼 부작용이 많았다.
이번 연구결과를 통해 바이러스에 의한 간세포 손상을 억제하는 부작용 없는 신약개발이 가능하게 될 것으로 전망된다.
최철희 교수는 “이번 연구를 통해 C형 간염 바이러스가 숙주의 간세포와 어떤 상호 작용을 하는지 밝혀내 감염 환자의 치료법을 획기적으로 개선할 수 있을 것”이라고 말했다.
신의철 교수는 “이번 연구는 기초의학과 응용의학의 융합연구가 성공한 대표적 사례”라며 “앞으로도 다학제간 융합연구를 실시하면 그동안 풀지 못했던 난제들을 효율적으로 해결할 수 있을 것”이라고 강조했다.
한편, 교육과학기술부 미래기반기술개발사업(신약타겟검증연구사업)의 지원을 받아 수행된 이번 연구 결과는 의학 분야의 세계적 학술지인 헤파톨로지(Hepatolog, Impact Factor=11.665) 9월호 표지 논문으로 선정됐다.
□ 연구 세부사항 설명
TNF-α(종양괴사인자)는 면역을 담당하는 세포에 의해 분비되는 단백질이다. HCV에 감염되면 바이러스의 증식을 억제하기 위해 체내의 면역작용이 활발해지고 TNF-α의 분비도 늘어난다.
TNF-α는 세포의 생존을 담당하는 NF-κB 신호전달과 세포의 죽음을 담당하는 JNK 신호 전달을 동시에 활성화시킨다. HCV에 감염되면, 세포의 생존을 담당하는 NF-κB 쪽 신호전달 경로만 선택적으로 활성을 억제하게 되고, TNF-α의 역할은 세포의 죽음 쪽으로 균형이 기울게 된다.
바이러스의 증식을 억제하기 위해 분비된 TNF-α가 오히려 간세포를 죽이게 되는 것이다. 이는 곧 간 손상을 뜻하며, HCV를 구성하는 10가지의 단백질 중 core, NF4B, NS5B 라는 단백질이 이러한 작용을 한다고 규명해냈다.
2012.09.04
조회수 18913
-
 화학과 학부생, 세계적 저널에 표지논문 게재
- 화학과 4학년 조상연, 물리학과 4년 김수민 학생, 말라리아 연구를 위한 광학영상 기술을 분석해 셀(Cell) 자매지 표지논문에 게재 -- 국내최초 소방관인 故 조용완씨 손자, 3월 의무소방요원으로 입대예정 -
“교수님, 하이젠 베르크(Werner Heisenberg) 같은 역사 속 과학자들은 20대 초반에 세계적인 연구 성과를 냈는데 저는 이대로 가다간 늦어버릴 것 같습니다. 교수님 연구실에서 융합연구를 할 수 있게 도와주세요”
우리 학교 화학과 4학년에 재학 중인 조상연(22) 君이 1학년 때 이 대학에서 물리화학 분야 융합연구의 세계적인 석학인 이효철 화학과 교수를 찾아 와 당차게 부탁한 한 마디다.
조상연 학생이 말라리아 연구와 관련해 제1저자로 발표한 논문이 셀(Cell)지가 발행하는 생명공학분야 최고 권위 학술지인 ‘생명공학의 동향(Trends in Biotechnology, IF=9.644)’ 2월호 표지논문으로 선정됐다.
근래 들어 학부생의 연구 참여가 활발해진 까닭에 과학기술논문인용색인(SCI)급 국제학술지에 논문이 실리는 경우가 가끔씩은 있었지만, 셀 자매지와 같은 세계적인 학술지에, 그것도 표지논문으로 실리는 경우는 거의 없었다. 하지만 오랜만에 KAIST 학부재학생인 조상연 君이 큰일을 이뤄내 학교 안팎으로부터 많은 화제를 모으고 있다.
광주과학고를 2년 만에 조기 졸업하고 2008년 KAIST에 입학한 조 군은 평소 연구에 대한 높은 관심으로 신입생 때부터 KAIST내 다양한 학과를 넘나들며 연구거리를 찾아다녔다.
2학년 때는 화학과 이효철 교수의 지도아래 학부생 연구지원 프로그램인 URP에 참여, ‘시간분해회절에 의한 용액 상 구조 동력학 분석’에 관한 탁월한 연구 성과를 거뒀다. 이 연구로 조 君은 2학년 학생으로는 이례적으로 최우수상을 수상하는 한편 후속연구비 1000만원과 해외학회 참가라는 특전을 받으며 두각을 보이기 시작했다.
바이오 및 뇌 공학과 김동섭 교수와 ‘알카인 수화반응을 촉매하는 단백질의 컴퓨터 디자인’에 대한 연구를 진행하는 한편 EEWS대학원 정유성 교수와는 ‘전산모사를 통한 이산화탄소 흡착 촉매 디자인’ 등에 대한 연구를 수행하기도 했었다.
이후 조상연 君은 2011년 2월부터 약 1년간 바이오광학분야 융합 연구에 대한 세계적 학자인 물리학과 및 광기술연구소 박용근(32) 교수의 지도를 받아 왔다. 이번 셀 자매지에 게재한 논문은 박용근 교수의 지도를 받으며 수행한 연구과제 중 하나다. 같은 공동저자 중 한명인 김수민 학생(24, 제2저자) 역시 물리학과 학부생으로 ‘개별연구제도’를 통해 연구에 참여했다.
조상연 학생은 ‘말라리아 연구를 위한 광학 영상기술’이라는 제목의 이번 논문을 통해 “학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 또 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다”며 문제를 제기했다.
이와 함께 첨단 광학기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 말라리아 연구를 크게 3가지로 나눠 체계적으로 광학기술을 이용하는 전략을 제시했다.
조 君의 이번 연구는 바이오 이미징 기술을 말라리아 감염질환 연구에 통합 적용하고, 말라리아 연구에 적용 가능한 광학영상 방법들을 소개함으로써, 다 학제 간 융합 연구시대에 경쟁력을 갖는 광학-의학연구 전략을 체계적으로 제시한 것으로 높이 평가받고 있다.
조상연 학생은 “고등학교 시절 SEE-KAIST 과제에 출품해 수상하면서 연구에 대한 재미를 느꼈고, 2학년 1학기까지 특정한 학과가 없는 무학과 제도를 운영해 다양한 분야의 융합연구를 할 수 있는 조건을 갖춘 국내 최고의 연구중심대학 KAIST로 진학을 결심했다”며 “특히, 학부생에게 관련분야 최고 교수와 연구기회를 주는 URP 및 개별연구제도로 인해 뛰어난 교수들의 지도와 학교의 충분한 재정적 지원 덕분에 큰 어려움 없이 마음껏 연구를 펼칠 수 있었다”고 말했다.
조 君은 이와 함께 “앞으로 목표는 세상에서 제일 재미있는 융합연구를 하는 과학자가 되는 것”이라며 “제가 하는 연구를 통해 전 세계 어려운 상황에 놓인 많은 사람들을 도우는 데 노력할 것”이라고 말했다.
조 君은 바쁜 학업생활 속에서도 지역사회를 위해 저소득층 중학생들을 위한 봉사단체인 ‘배움을 나누는 사람들’에서 2년간 꾸준히 봉사를 해왔으며, KAIST 자연과학 학술동아리인 ‘KINS’를 설립했고, 자연과학대학 소식지인 ‘KAIST Science’ 기자로도 활동해 왔다.
조 君은 현재 해외 대학원 입학을 계획하고 있으며 올 3월 입대해 의무소방요원으로 군복무를 할 예정이다. 조 君의 할아버지는 우리나라 최초의 소방관인 故 조용완 씨로 소방관에 대한 남다른 인연으로 군 생활을 시작할 예정이다.
한편, 이번 연구는 KAIST ‘신임교원정착연구사업‘과 ’광기술연구소연구사업‘의 일환으로 이뤄졌으며 화학과 학사과정 조상연(22, 제1저자) 君을 포함해 물리학과 학사과정 김수민(24, 제2저자) 학생과 물리학과 김영찬 박사(30, 공저자)가 함께 수행했다.(끝)
붙임 : 논문요약, 보충자료, 사진설명
<논문요약>
논문주제 : 말라리아 연구를 위한 광학 영상기술
학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다. 세계 각국은 말라리아 감염을 연구하고, 말라리아를 진단하고 치료하는 장비 개발에 박차를 가하고 있다.
빌게이츠 Microsoft사 전 회장 부부가 설립한 Bill & Melinda Gates 재단에서 말라리아 연구에 막대한 연구비를 지원하기 시작했으며, Apple, Google, Intel사 등이 연합 설립한 Intellectual ventures사에서도 빛을 이용한 말라리아 진단 연구를 진행하고 있는 것이 그 사례들이다.
최근에는 첨단 광학 기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 박 교수 연구팀은 말라리아 연구를 크게 3가지로 나누어 체계적으로 광학기술을 이용하는 전략을 제시했다.
▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하여 체외에서 광학 영상을 측정하는 방법과 ▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하지 않고, 적혈구 자체의 광학적 신호를 이용하여 체외에서 영상을 획득하는 방법 그리고 ▲체내에서 말라리아 기생충이 숙주 세포를 감염시키는 과정의 광학 영상을 획득하는 방법이다.
이 논문에서는 물리학(광학)과 의학(감염질환)의 효과적인 융합 연구를 위한 체계화된 전략을 소개했기 때문에 실제 말라리아를 연구하는 연구자들에게 실질적인 도움이 될 수 있을 것이라고 평가받고 있다.
제1저자로 참여한 조상연 학생은 “이번 논문은 연구팀에서 수행하고 있는 굴절률 차이를 이용한 광학영상기술 및 최신 광학영상 기술들이 말라리아에 어떻게 이용될 수 있는가를 소개함으로써, 말라리아 진단 및 치료 연구에 힘을 실어줄 수 있을 것으로 기대한다”고 말했다.
<보충자료: 용어설명>
○ SEE-KAIST1992년 첫 행사를 시작으로 `Open-KAIST`와 번갈아 격년제로 실시해오는 행사로 KAIST 연구 성과, 과학고 탐구 성과, 산업체 연구개발 제품 등을 직접 보고 체험할 수 있는 KAIST의 대표적인 과학문화 대중화 행사다.
○ 무학과제도학사과정의 우수한 학생들에게 학과선택의 자율성을 보장하기 위해 학과 구 분 없이 입학해 개인의 적성 등을 고려해 2학년 1학기를 마친 후 학과를 선택하는 제도.
○ URP
학사과정 학생들이 지도교수와 지도조교의 지도하에 실질적인 실험 및 연구를 할 수 있도록, 연구비 지원 및 학점 연계를 통해 학부생의 연구를 현실적으로 지원하는 프로그램
① Long-Term URP 프로그램 (연 1회 실시)
가. 연구기간 : 12개월 (2011년 12월 26일~2012년 12월 21일)
나. 지원내역
* 단독 : 장학금 1,500천원+연구비 3,000천원
* 팀 : 1인당 장학금 1,200천원+연구비 4,000천원
② 겨울/봄학기, 여름/가을학기 URP 프로그램
가. 연구기간 : 5개월~6개월
나. 지원내역
* 단독 : 장학금 1,000천원+연구비 1,500천원 * 팀 : 1인당 장학금 800천원+연구비 2,000천원
○ 하이젠베르크
하이젠베르크는 1901년 독일에서 출생했다. 그의 아버지는 의학교수였고 그는 뮌헨대학에서 아놀드 좀머펠트(Arnold Sommerfeld) 밑에서 이론물리를 공부했고, 1923년에 박사학위를 받았다. 같은 해에 그는 괴팅겐대학에서 보른(Max Born)의 조수가 되었으며, 다음해에는 강사가 된다. 다음 3년간 코펜하겐에서 닐스 보어와 함께 일하고, 1927년부터 1941년 까지 라이프치히대학의 이론물리학 교수가 된다.거기서 볼프강 파울리 등과 연구하며 양자 전기 역학과 양자장 이론을 발전 시켰고, 핵 물리학과 고 에너지 물리학의 발전에 넓고도 깊은 영향을 미쳤다. 불확정성 원리로 유명한 하이젠베르크는 양자역학의 탄생에 기여한 공로로 1932년 노벨물리학상을 받았다.
<사진설명>
조상연 학생의 지도교수인 물리학과 박용근 교수
연구자 사진 : 왼쪽부터 김수민 학생, 김영찬 박사, 조상연 학생
Trends in Biotechnology 2012년 2월 호 논문표지
화학과 학부생, 세계적 저널에 표지논문 게재
- 화학과 4학년 조상연, 물리학과 4년 김수민 학생, 말라리아 연구를 위한 광학영상 기술을 분석해 셀(Cell) 자매지 표지논문에 게재 -- 국내최초 소방관인 故 조용완씨 손자, 3월 의무소방요원으로 입대예정 -
“교수님, 하이젠 베르크(Werner Heisenberg) 같은 역사 속 과학자들은 20대 초반에 세계적인 연구 성과를 냈는데 저는 이대로 가다간 늦어버릴 것 같습니다. 교수님 연구실에서 융합연구를 할 수 있게 도와주세요”
우리 학교 화학과 4학년에 재학 중인 조상연(22) 君이 1학년 때 이 대학에서 물리화학 분야 융합연구의 세계적인 석학인 이효철 화학과 교수를 찾아 와 당차게 부탁한 한 마디다.
조상연 학생이 말라리아 연구와 관련해 제1저자로 발표한 논문이 셀(Cell)지가 발행하는 생명공학분야 최고 권위 학술지인 ‘생명공학의 동향(Trends in Biotechnology, IF=9.644)’ 2월호 표지논문으로 선정됐다.
근래 들어 학부생의 연구 참여가 활발해진 까닭에 과학기술논문인용색인(SCI)급 국제학술지에 논문이 실리는 경우가 가끔씩은 있었지만, 셀 자매지와 같은 세계적인 학술지에, 그것도 표지논문으로 실리는 경우는 거의 없었다. 하지만 오랜만에 KAIST 학부재학생인 조상연 君이 큰일을 이뤄내 학교 안팎으로부터 많은 화제를 모으고 있다.
광주과학고를 2년 만에 조기 졸업하고 2008년 KAIST에 입학한 조 군은 평소 연구에 대한 높은 관심으로 신입생 때부터 KAIST내 다양한 학과를 넘나들며 연구거리를 찾아다녔다.
2학년 때는 화학과 이효철 교수의 지도아래 학부생 연구지원 프로그램인 URP에 참여, ‘시간분해회절에 의한 용액 상 구조 동력학 분석’에 관한 탁월한 연구 성과를 거뒀다. 이 연구로 조 君은 2학년 학생으로는 이례적으로 최우수상을 수상하는 한편 후속연구비 1000만원과 해외학회 참가라는 특전을 받으며 두각을 보이기 시작했다.
바이오 및 뇌 공학과 김동섭 교수와 ‘알카인 수화반응을 촉매하는 단백질의 컴퓨터 디자인’에 대한 연구를 진행하는 한편 EEWS대학원 정유성 교수와는 ‘전산모사를 통한 이산화탄소 흡착 촉매 디자인’ 등에 대한 연구를 수행하기도 했었다.
이후 조상연 君은 2011년 2월부터 약 1년간 바이오광학분야 융합 연구에 대한 세계적 학자인 물리학과 및 광기술연구소 박용근(32) 교수의 지도를 받아 왔다. 이번 셀 자매지에 게재한 논문은 박용근 교수의 지도를 받으며 수행한 연구과제 중 하나다. 같은 공동저자 중 한명인 김수민 학생(24, 제2저자) 역시 물리학과 학부생으로 ‘개별연구제도’를 통해 연구에 참여했다.
조상연 학생은 ‘말라리아 연구를 위한 광학 영상기술’이라는 제목의 이번 논문을 통해 “학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 또 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다”며 문제를 제기했다.
이와 함께 첨단 광학기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 말라리아 연구를 크게 3가지로 나눠 체계적으로 광학기술을 이용하는 전략을 제시했다.
조 君의 이번 연구는 바이오 이미징 기술을 말라리아 감염질환 연구에 통합 적용하고, 말라리아 연구에 적용 가능한 광학영상 방법들을 소개함으로써, 다 학제 간 융합 연구시대에 경쟁력을 갖는 광학-의학연구 전략을 체계적으로 제시한 것으로 높이 평가받고 있다.
조상연 학생은 “고등학교 시절 SEE-KAIST 과제에 출품해 수상하면서 연구에 대한 재미를 느꼈고, 2학년 1학기까지 특정한 학과가 없는 무학과 제도를 운영해 다양한 분야의 융합연구를 할 수 있는 조건을 갖춘 국내 최고의 연구중심대학 KAIST로 진학을 결심했다”며 “특히, 학부생에게 관련분야 최고 교수와 연구기회를 주는 URP 및 개별연구제도로 인해 뛰어난 교수들의 지도와 학교의 충분한 재정적 지원 덕분에 큰 어려움 없이 마음껏 연구를 펼칠 수 있었다”고 말했다.
조 君은 이와 함께 “앞으로 목표는 세상에서 제일 재미있는 융합연구를 하는 과학자가 되는 것”이라며 “제가 하는 연구를 통해 전 세계 어려운 상황에 놓인 많은 사람들을 도우는 데 노력할 것”이라고 말했다.
조 君은 바쁜 학업생활 속에서도 지역사회를 위해 저소득층 중학생들을 위한 봉사단체인 ‘배움을 나누는 사람들’에서 2년간 꾸준히 봉사를 해왔으며, KAIST 자연과학 학술동아리인 ‘KINS’를 설립했고, 자연과학대학 소식지인 ‘KAIST Science’ 기자로도 활동해 왔다.
조 君은 현재 해외 대학원 입학을 계획하고 있으며 올 3월 입대해 의무소방요원으로 군복무를 할 예정이다. 조 君의 할아버지는 우리나라 최초의 소방관인 故 조용완 씨로 소방관에 대한 남다른 인연으로 군 생활을 시작할 예정이다.
한편, 이번 연구는 KAIST ‘신임교원정착연구사업‘과 ’광기술연구소연구사업‘의 일환으로 이뤄졌으며 화학과 학사과정 조상연(22, 제1저자) 君을 포함해 물리학과 학사과정 김수민(24, 제2저자) 학생과 물리학과 김영찬 박사(30, 공저자)가 함께 수행했다.(끝)
붙임 : 논문요약, 보충자료, 사진설명
<논문요약>
논문주제 : 말라리아 연구를 위한 광학 영상기술
학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다. 세계 각국은 말라리아 감염을 연구하고, 말라리아를 진단하고 치료하는 장비 개발에 박차를 가하고 있다.
빌게이츠 Microsoft사 전 회장 부부가 설립한 Bill & Melinda Gates 재단에서 말라리아 연구에 막대한 연구비를 지원하기 시작했으며, Apple, Google, Intel사 등이 연합 설립한 Intellectual ventures사에서도 빛을 이용한 말라리아 진단 연구를 진행하고 있는 것이 그 사례들이다.
최근에는 첨단 광학 기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 박 교수 연구팀은 말라리아 연구를 크게 3가지로 나누어 체계적으로 광학기술을 이용하는 전략을 제시했다.
▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하여 체외에서 광학 영상을 측정하는 방법과 ▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하지 않고, 적혈구 자체의 광학적 신호를 이용하여 체외에서 영상을 획득하는 방법 그리고 ▲체내에서 말라리아 기생충이 숙주 세포를 감염시키는 과정의 광학 영상을 획득하는 방법이다.
이 논문에서는 물리학(광학)과 의학(감염질환)의 효과적인 융합 연구를 위한 체계화된 전략을 소개했기 때문에 실제 말라리아를 연구하는 연구자들에게 실질적인 도움이 될 수 있을 것이라고 평가받고 있다.
제1저자로 참여한 조상연 학생은 “이번 논문은 연구팀에서 수행하고 있는 굴절률 차이를 이용한 광학영상기술 및 최신 광학영상 기술들이 말라리아에 어떻게 이용될 수 있는가를 소개함으로써, 말라리아 진단 및 치료 연구에 힘을 실어줄 수 있을 것으로 기대한다”고 말했다.
<보충자료: 용어설명>
○ SEE-KAIST1992년 첫 행사를 시작으로 `Open-KAIST`와 번갈아 격년제로 실시해오는 행사로 KAIST 연구 성과, 과학고 탐구 성과, 산업체 연구개발 제품 등을 직접 보고 체험할 수 있는 KAIST의 대표적인 과학문화 대중화 행사다.
○ 무학과제도학사과정의 우수한 학생들에게 학과선택의 자율성을 보장하기 위해 학과 구 분 없이 입학해 개인의 적성 등을 고려해 2학년 1학기를 마친 후 학과를 선택하는 제도.
○ URP
학사과정 학생들이 지도교수와 지도조교의 지도하에 실질적인 실험 및 연구를 할 수 있도록, 연구비 지원 및 학점 연계를 통해 학부생의 연구를 현실적으로 지원하는 프로그램
① Long-Term URP 프로그램 (연 1회 실시)
가. 연구기간 : 12개월 (2011년 12월 26일~2012년 12월 21일)
나. 지원내역
* 단독 : 장학금 1,500천원+연구비 3,000천원
* 팀 : 1인당 장학금 1,200천원+연구비 4,000천원
② 겨울/봄학기, 여름/가을학기 URP 프로그램
가. 연구기간 : 5개월~6개월
나. 지원내역
* 단독 : 장학금 1,000천원+연구비 1,500천원 * 팀 : 1인당 장학금 800천원+연구비 2,000천원
○ 하이젠베르크
하이젠베르크는 1901년 독일에서 출생했다. 그의 아버지는 의학교수였고 그는 뮌헨대학에서 아놀드 좀머펠트(Arnold Sommerfeld) 밑에서 이론물리를 공부했고, 1923년에 박사학위를 받았다. 같은 해에 그는 괴팅겐대학에서 보른(Max Born)의 조수가 되었으며, 다음해에는 강사가 된다. 다음 3년간 코펜하겐에서 닐스 보어와 함께 일하고, 1927년부터 1941년 까지 라이프치히대학의 이론물리학 교수가 된다.거기서 볼프강 파울리 등과 연구하며 양자 전기 역학과 양자장 이론을 발전 시켰고, 핵 물리학과 고 에너지 물리학의 발전에 넓고도 깊은 영향을 미쳤다. 불확정성 원리로 유명한 하이젠베르크는 양자역학의 탄생에 기여한 공로로 1932년 노벨물리학상을 받았다.
<사진설명>
조상연 학생의 지도교수인 물리학과 박용근 교수
연구자 사진 : 왼쪽부터 김수민 학생, 김영찬 박사, 조상연 학생
Trends in Biotechnology 2012년 2월 호 논문표지
2012.02.01
조회수 30510
-
 스마트폰 질병진단 원천기술 개발
- 신개념의 생체분자 검출기술로 휴대용 체외진단 분야에 획기적 원천기술- 화학분야 세계적 학술지 ‘앙게반테 케미’ 1월호(16일자) 표지논문 선정
스마트폰으로도 질병을 진단하는 원천기술이 국내 연구진에 의해 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 스마트폰을 비롯한 휴대용 개인기기에 널리 이용되고 있는 정전기방식의 터치스크린을 이용해 생체분자를 검출하는 원천기술을 세계 최초로 개발하는 데 성공했다.
앞으로 병원에 가지 않고도 스마트폰을 가지고 간단한 질병을 진단하는 시대가 열릴 것으로 기대된다.
최근 스마트폰과 같은 휴대용 전자기기에 적용되는 정전기방식의 터치스크린은 일반적으로 손가락의 접촉을 통해 발생하는 터치스크린 표면의 정전용량 변화를 감지해 작업을 수행하도록 설계돼 있다.
연구팀은 DNA가 자체의 정전용량을 가지고 있으며, 농도에 따라 정전용량이 변화한다는 사실에 착안해 정전기방식의 터치스크린을 생체분자 검출에 활용할 수 있을 것이라고 예상했다.
이를 규명하기 위해 연구팀은 대표적인 생체분자인 DNA를 터치스크린 위에 가하고 정전용량 변화량을 감지했다. 실험결과 터치스크린을 이용해 DNA의 유무와 농도를 정확하게 검출할 수 있었다.이 결과에 따라 DNA뿐만 아니라 세포, 단백질, 핵산, 등 대부분의 생체분자가 정전용량을 갖고 있기 때문에 다양한 생체물질의 검출에도 활용될 수 있다는 가능성을 제시했다는 게 이 기술의 큰 특징이다.
박현규 교수는 “모바일 기기 등에 입력장치로만 이용해 왔던 터치스크린으로 생체 분자 등의 분석에 이용할 수 있음을 세계 최초로 입증한 결과”라며 “이 원천기술을 이용해 앞으로 터치스크린 기반의 스마트폰 또는 태블릿 PC 등을 이용해 개인이 질병을 진단하는 시대가 올 것”이라고 말했다.
이와 함께 논문의 제1저자인 원병연 연구조교수는 “현재는 생체분자의 유무 또는 농도만 측정 가능한 단계이며, 앞으로 특정 생체분자를 선택적으로 검출할 수 있는 기술을 개발해 가까운 시일 내에 상용화에 주력할 것”이라고 덧붙였다.
한편, 이번 연구는 지식경제부가 시행하는 ‘산업원천기술개발사업’으로 수행됐으며, 연구의 중요성을 인정받아 화학 분야의 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 1월호(16일자) 표지논문으로 선정됐다.
그림1. 터치스크린을 이용한 생체 분자 검출 시스템 모식도 (앙게반테 케미 논문 표지). 휴대용 모바일 기기의 입력장치인 터치스크린 위에서 세포, 단백실, 핵산, 소분자 등의 생체 분자를 검출할 수 있다.
그림2. 정전용량 터치스크린 방식의 한가지인 surface capacitive touchscreen을 이용한 시스템 모식도. 여러 지점을 동시에 접촉했을 때 접촉점의 시료 농도에 따라 터치 신호의 위치가 변하는 원리를 이용한 방법. 동시에 두 개의 미지 시료의 농도를 측정할 수 있다.
그림3. 정전용량 터치스크린 방식의 한가지인 projected capacitive touchscreen을 이용한 시스템 모식도. 현재 스마트폰 등에 쓰이는 터치스크린 방식으로서, 터치스크린 표면 내부에 여러 라인의 전극이 패턴되어 있어, 각 전극의 정전용량 변화를 각각 측정함으로써 여러 접촉 시료의 농도를 동시에 검출할 수 있다.
스마트폰 질병진단 원천기술 개발
- 신개념의 생체분자 검출기술로 휴대용 체외진단 분야에 획기적 원천기술- 화학분야 세계적 학술지 ‘앙게반테 케미’ 1월호(16일자) 표지논문 선정
스마트폰으로도 질병을 진단하는 원천기술이 국내 연구진에 의해 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 스마트폰을 비롯한 휴대용 개인기기에 널리 이용되고 있는 정전기방식의 터치스크린을 이용해 생체분자를 검출하는 원천기술을 세계 최초로 개발하는 데 성공했다.
앞으로 병원에 가지 않고도 스마트폰을 가지고 간단한 질병을 진단하는 시대가 열릴 것으로 기대된다.
최근 스마트폰과 같은 휴대용 전자기기에 적용되는 정전기방식의 터치스크린은 일반적으로 손가락의 접촉을 통해 발생하는 터치스크린 표면의 정전용량 변화를 감지해 작업을 수행하도록 설계돼 있다.
연구팀은 DNA가 자체의 정전용량을 가지고 있으며, 농도에 따라 정전용량이 변화한다는 사실에 착안해 정전기방식의 터치스크린을 생체분자 검출에 활용할 수 있을 것이라고 예상했다.
이를 규명하기 위해 연구팀은 대표적인 생체분자인 DNA를 터치스크린 위에 가하고 정전용량 변화량을 감지했다. 실험결과 터치스크린을 이용해 DNA의 유무와 농도를 정확하게 검출할 수 있었다.이 결과에 따라 DNA뿐만 아니라 세포, 단백질, 핵산, 등 대부분의 생체분자가 정전용량을 갖고 있기 때문에 다양한 생체물질의 검출에도 활용될 수 있다는 가능성을 제시했다는 게 이 기술의 큰 특징이다.
박현규 교수는 “모바일 기기 등에 입력장치로만 이용해 왔던 터치스크린으로 생체 분자 등의 분석에 이용할 수 있음을 세계 최초로 입증한 결과”라며 “이 원천기술을 이용해 앞으로 터치스크린 기반의 스마트폰 또는 태블릿 PC 등을 이용해 개인이 질병을 진단하는 시대가 올 것”이라고 말했다.
이와 함께 논문의 제1저자인 원병연 연구조교수는 “현재는 생체분자의 유무 또는 농도만 측정 가능한 단계이며, 앞으로 특정 생체분자를 선택적으로 검출할 수 있는 기술을 개발해 가까운 시일 내에 상용화에 주력할 것”이라고 덧붙였다.
한편, 이번 연구는 지식경제부가 시행하는 ‘산업원천기술개발사업’으로 수행됐으며, 연구의 중요성을 인정받아 화학 분야의 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 1월호(16일자) 표지논문으로 선정됐다.
그림1. 터치스크린을 이용한 생체 분자 검출 시스템 모식도 (앙게반테 케미 논문 표지). 휴대용 모바일 기기의 입력장치인 터치스크린 위에서 세포, 단백실, 핵산, 소분자 등의 생체 분자를 검출할 수 있다.
그림2. 정전용량 터치스크린 방식의 한가지인 surface capacitive touchscreen을 이용한 시스템 모식도. 여러 지점을 동시에 접촉했을 때 접촉점의 시료 농도에 따라 터치 신호의 위치가 변하는 원리를 이용한 방법. 동시에 두 개의 미지 시료의 농도를 측정할 수 있다.
그림3. 정전용량 터치스크린 방식의 한가지인 projected capacitive touchscreen을 이용한 시스템 모식도. 현재 스마트폰 등에 쓰이는 터치스크린 방식으로서, 터치스크린 표면 내부에 여러 라인의 전극이 패턴되어 있어, 각 전극의 정전용량 변화를 각각 측정함으로써 여러 접촉 시료의 농도를 동시에 검출할 수 있다.
2012.01.16
조회수 21488
 달걀 모방한 세포보호 및 분해기술 개발
특정 미생물은 영양분이 부족한 환경에서 생존이 불리해지면 DNA 보존을 위해 세포외벽에 단단한 보호막인 내생포자를 형성한다. 이렇게 만들어진 내생포자가 생존에 적합한 환경을 만나면 다시 세포증식이 가능한 원래 상태로 돌아간다.
이 현상을 인공적으로 조절하는 기술이 국제 공동연구진에 의해 개발됐다. 달걀껍질처럼 하나의 세포를 감싸서 보존했다가 원하는 시기에 분해할 수 있어 세포기반 바이오센서·세포 치료제·바이오촉매 등에 활용될 것으로 기대된다.
우리 학교 화학과 최인성·이영훈 교수는 호주 멜버른대학교 화학공학과 프랭크 카루소(Frank Caruso) 교수와 공동으로 나노미터 스케일의 필름으로 단일 세포를 코팅해 세포의 생존을 유지하다가 원하는 시간에 분해할 수 있는 기술을 개발했다.
연구결과는 화학분야 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition) 11월 10일자 속표지(frontispiece) 논문으로 소개됐다.
세포피포화(細胞被包化)는 세포의 생존을 최대한 유지하면서 각각의 세포를 단단한 캡슐로 포획하는 기술이다. 세포를 기반으로 한 응용 분야에서 당면한 문제인 세포 안정도 유지와 세포분열제어를 위해 중요성이 높아지고 있다.
기존 세포피포화 방법은 유기박막 혹은 유기박막을 주형으로 만들어진 무기물 캡슐을 이용했다. 이들은 세포표면에 단단하게 형성됐으나 잘 분해되지 않아 활용하기가 어려웠다.
연구팀은 효모세포를 가지고 탄닌산 수용액과 철이온 수용액을 섞어 세포를 하나씩 금속-폴리페놀박막으로 감싸는 데 세계 최초로 성공했다.
탄닌산은 참나무껍질이나 포도껍질에서 추출한 천연물질로 세포친화도가 높아 철이온과 만나면 10초 이내로 금속-폴리페놀박막이 만들어진다. 이 박막으로 피포화된 세포들은 높은 생존율을 보였으며 박막 형성시간이 짧고 간단해 효율적으로 많은 양의 피포화 세포를 얻을 수 있었다.
이와 함께 연구팀은 금속-폴리페놀박막이 중성 pH(수소이온지수)에서는 안정하지만 약한 산성조건에서 빠르게 분해되는 특성을 이용해 원하는 시간에 세포를 피포화 전 상태로 복구해 세포분열을 조절할 수 있음을 밝혔다.
달걀껍질처럼 외부환경으로부터 내부 세포를 보호해주는 금속-폴리페놀박막은 △세포에 손상을 줄 수 있는 분해효소 △장시간의 자외선 처리 △은나노입자에 대한 방어기작을 가져 세포가 극한의 외부환경에 노출되더라도 높은 세포 생존도를 유지하는 결과를 나타냈다.
이영훈 교수는 이번 연구에 대해 “이 기술을 통해 피포화과정에서의 세포생존도를 유지함은 물론 극한의 외부환경에 대항하여 세포를 보호할 수 있다”며 “나아가 응답형 분해기작으로 원하는 때에 피포화된 세포의 분열시기를 조절할 수 있는 차세대 세포피포화기술”이라고 말했다.
최인성 교수는 “세포피포화기술은 아직 걸음마 단계지만 기술이 성숙함에 따라 세포조작기술의 응용가능성이 현실화될 것”이라며 “세포기반 응용분야에서 현실적으로 당면한 문제들을 해결할 맞춤형 대안이 될 것”이라고 덧붙였다.
미래창조과학부와 한국연구재단이 추진하는 리더연구자지원사업과 글로벌연구실지원사업의 지원으로 수행된 이번 연구는 KAIST와 호주 멜버른대학교 국제 공동 교수진의 지도아래 KAIST 화학과 박지훈·김경환 석사과정 학생이 주도했다.
그림 1. 앙게반테 케미 속표지
배경 : 금속-폴리페놀박막(붉은색으로 염색)이 형성된 효모세포가 생존을 유지하고 있음(초록색으로 염색-생존도를 가지고 효소활성을 나타냄)을 보여줌.
앞쪽그림 : 각 피포화 단계의 효모세포 왼쪽아래 : 세포는 피포화하기전 상태, 붉은색 화살표를 따라가면 보라색 금속-폴리페놀박막이 형성되어 보라색으로 나타나는 효모세포, 초록색 화살표를 따라가면 약 산성 pH에서 금속-폴리페놀박막이 표면에서 분해되는 것을 형상화했다.
그림 2. 금속-폴리페놀박막을 이용한 세포피포화(細胞被包化) 모식도
(위)피포화하기전 효모세포
(중간) 금속-폴리페놀 나노캡슐(Tannic Acid-Fe(III) Nanoshell)으로 피포화된 효모세포-피포화된 효모세포는 세포분열이 pH에 따라 조절(Cell-Division Control)되고, UV-C, 분해효소와 은나노입자에 대한 저항성을 가진다. (아래) 원하는 시간에 pH 조절로 금속-폴리페놀박막이 분해되는 것을 형상화
2014.11.18 조회수 17511
달걀 모방한 세포보호 및 분해기술 개발
특정 미생물은 영양분이 부족한 환경에서 생존이 불리해지면 DNA 보존을 위해 세포외벽에 단단한 보호막인 내생포자를 형성한다. 이렇게 만들어진 내생포자가 생존에 적합한 환경을 만나면 다시 세포증식이 가능한 원래 상태로 돌아간다.
이 현상을 인공적으로 조절하는 기술이 국제 공동연구진에 의해 개발됐다. 달걀껍질처럼 하나의 세포를 감싸서 보존했다가 원하는 시기에 분해할 수 있어 세포기반 바이오센서·세포 치료제·바이오촉매 등에 활용될 것으로 기대된다.
우리 학교 화학과 최인성·이영훈 교수는 호주 멜버른대학교 화학공학과 프랭크 카루소(Frank Caruso) 교수와 공동으로 나노미터 스케일의 필름으로 단일 세포를 코팅해 세포의 생존을 유지하다가 원하는 시간에 분해할 수 있는 기술을 개발했다.
연구결과는 화학분야 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition) 11월 10일자 속표지(frontispiece) 논문으로 소개됐다.
세포피포화(細胞被包化)는 세포의 생존을 최대한 유지하면서 각각의 세포를 단단한 캡슐로 포획하는 기술이다. 세포를 기반으로 한 응용 분야에서 당면한 문제인 세포 안정도 유지와 세포분열제어를 위해 중요성이 높아지고 있다.
기존 세포피포화 방법은 유기박막 혹은 유기박막을 주형으로 만들어진 무기물 캡슐을 이용했다. 이들은 세포표면에 단단하게 형성됐으나 잘 분해되지 않아 활용하기가 어려웠다.
연구팀은 효모세포를 가지고 탄닌산 수용액과 철이온 수용액을 섞어 세포를 하나씩 금속-폴리페놀박막으로 감싸는 데 세계 최초로 성공했다.
탄닌산은 참나무껍질이나 포도껍질에서 추출한 천연물질로 세포친화도가 높아 철이온과 만나면 10초 이내로 금속-폴리페놀박막이 만들어진다. 이 박막으로 피포화된 세포들은 높은 생존율을 보였으며 박막 형성시간이 짧고 간단해 효율적으로 많은 양의 피포화 세포를 얻을 수 있었다.
이와 함께 연구팀은 금속-폴리페놀박막이 중성 pH(수소이온지수)에서는 안정하지만 약한 산성조건에서 빠르게 분해되는 특성을 이용해 원하는 시간에 세포를 피포화 전 상태로 복구해 세포분열을 조절할 수 있음을 밝혔다.
달걀껍질처럼 외부환경으로부터 내부 세포를 보호해주는 금속-폴리페놀박막은 △세포에 손상을 줄 수 있는 분해효소 △장시간의 자외선 처리 △은나노입자에 대한 방어기작을 가져 세포가 극한의 외부환경에 노출되더라도 높은 세포 생존도를 유지하는 결과를 나타냈다.
이영훈 교수는 이번 연구에 대해 “이 기술을 통해 피포화과정에서의 세포생존도를 유지함은 물론 극한의 외부환경에 대항하여 세포를 보호할 수 있다”며 “나아가 응답형 분해기작으로 원하는 때에 피포화된 세포의 분열시기를 조절할 수 있는 차세대 세포피포화기술”이라고 말했다.
최인성 교수는 “세포피포화기술은 아직 걸음마 단계지만 기술이 성숙함에 따라 세포조작기술의 응용가능성이 현실화될 것”이라며 “세포기반 응용분야에서 현실적으로 당면한 문제들을 해결할 맞춤형 대안이 될 것”이라고 덧붙였다.
미래창조과학부와 한국연구재단이 추진하는 리더연구자지원사업과 글로벌연구실지원사업의 지원으로 수행된 이번 연구는 KAIST와 호주 멜버른대학교 국제 공동 교수진의 지도아래 KAIST 화학과 박지훈·김경환 석사과정 학생이 주도했다.
그림 1. 앙게반테 케미 속표지
배경 : 금속-폴리페놀박막(붉은색으로 염색)이 형성된 효모세포가 생존을 유지하고 있음(초록색으로 염색-생존도를 가지고 효소활성을 나타냄)을 보여줌.
앞쪽그림 : 각 피포화 단계의 효모세포 왼쪽아래 : 세포는 피포화하기전 상태, 붉은색 화살표를 따라가면 보라색 금속-폴리페놀박막이 형성되어 보라색으로 나타나는 효모세포, 초록색 화살표를 따라가면 약 산성 pH에서 금속-폴리페놀박막이 표면에서 분해되는 것을 형상화했다.
그림 2. 금속-폴리페놀박막을 이용한 세포피포화(細胞被包化) 모식도
(위)피포화하기전 효모세포
(중간) 금속-폴리페놀 나노캡슐(Tannic Acid-Fe(III) Nanoshell)으로 피포화된 효모세포-피포화된 효모세포는 세포분열이 pH에 따라 조절(Cell-Division Control)되고, UV-C, 분해효소와 은나노입자에 대한 저항성을 가진다. (아래) 원하는 시간에 pH 조절로 금속-폴리페놀박막이 분해되는 것을 형상화
2014.11.18 조회수 17511 신기루 현상 착안해 테라헤르츠파 광학렌즈 개발
무더운 여름, 아스팔트 도로에 물웅덩이가 보이다가 가까이 다가가면 사라지고 좀 가다보면 또 물웅덩이가 나타난다. ‘신기루’라고 불리는 이 현상은 지표면 가까운 공기층의 큰 온도차로 인한 공기밀도 변화로 빛이 굴절되기 때문이다.
우리 학교 바이오및뇌공학과 정기훈 교수는 물리학과 안재욱 교수와 신기루 현상에서 착안한 물리적 효과를 이용해 테라헤르츠파 굴절률 분포형 렌즈를 세계 최초로 개발했다.
실리콘 소재를 곡면으로 가공해 만드는 카메라렌즈에 사용되는 기존방식과는 달리 이번에 개발된 렌즈는 평평한 실리콘 웨이퍼를 소재로 반도체 양산공정으로 제작해 비용을 최대 1/100 수준으로 낮출 수 있으며 제작시간도 훨씬 단축시킬 수 있다. 광원 추출효율은 4배 이상 향상시켰다.
테라헤르츠파는 0.1THz~30THz(테라헤르츠, 1조헤르츠) 대역의 전자기파로 가시광선이나 적외선보다 파장이 길어 X선처럼 물체의 내부를 높은 해상도로 정확히 식별할 수 있어 보안검색, 의료영상기술 등 비파괴 검사 도구나 의료용 진단기구의 성능을 획기적으로 향상시킬 수 있을 것으로 전망된다.
그러나 넓은 대역의 주파수 특성으로 인해 손실되는 전자기파의 비율이 높아 테라헤르츠파를 높은 효율로 집중시킬 수 있는 광학소자 개발이 요구됐다.
정 교수 연구팀은 평평한 실리콘에 테라헤르츠파 파장(약 300㎛) 보다 작은 80~120㎛ 크기의 구멍을 반도체 양산방법인 광식각공정으로 만들었다. 렌즈 가장자리로 갈수록 홀 사이즈는 크게 만들었다.
테라헤르츠파를 쪼이자 공기와 실리콘 중 공기 비율이 높은 가장자리는 굴절률이 낮았으며, 상대적으로 공기의 비율이 낮은 가운데는 굴절률이 높았다. 평평한 소재를 광학특성을 공학적으로 설계해 빛을 모으는 볼록렌즈와 같은 기능을 한 것으로 신기루 현상과 같은 물리적 효과와 같다.
이번 연구를 주도한 정기훈 교수는 “자연현상에서 착안해 자연계에 존재하지 않는 다양한 광학특성을 띄는 메타물질을 인공적으로 만든 것”이라며 “물질적 제약으로 인해 다양한 광학소자개발이 더딘 테라헤르츠파 기술 진보에 상당한 도움이 될 것”이라고 연구의의를 밝혔다.
미래창조과학부가 지원하는 한국연구재단의 도약연구자지원사업, 그린나노기술개발사업, 글로벌프론티어사업의 일환으로 수행된 이번 연구는 미국물리협회에서 발간하는 귄위 있는 국제학술지인 ‘어플라이드 피직스 레터(Applied Physics Letter)’에 9월자 특집논문 및 표지논문(제1저자 박상길 박사과정)으로 게재됐다.
그림1. 유전체 메타물질을 이용한 실리콘 굴절률 분포형 렌즈. 머리카락 굵기(80~120µm) 수준의 구멍이 실리콘 기판에 서로 다른 크기로 형성돼 있다.
그림2. 굴절률 분포형 렌즈 원리
그림3. 신기루 현상신기루는 아스팔트 도로 위에서 흔하게 나타나는 대기 굴절 현상이다. 이 현상은 도로면이 물체를 반사하는 것처럼 보이게 하는데 이 때문에 도로면에 물웅덩이가 있는 것처럼 착각하게 된다. 아래 사진에는 멀리서 다가오는 차의 상이 도로면을 통해 보인다. <사진 : 경기북과학고등학교 조영우 선생님 제공>
그림4. 논문표지
2014.09.24 조회수 24747
신기루 현상 착안해 테라헤르츠파 광학렌즈 개발
무더운 여름, 아스팔트 도로에 물웅덩이가 보이다가 가까이 다가가면 사라지고 좀 가다보면 또 물웅덩이가 나타난다. ‘신기루’라고 불리는 이 현상은 지표면 가까운 공기층의 큰 온도차로 인한 공기밀도 변화로 빛이 굴절되기 때문이다.
우리 학교 바이오및뇌공학과 정기훈 교수는 물리학과 안재욱 교수와 신기루 현상에서 착안한 물리적 효과를 이용해 테라헤르츠파 굴절률 분포형 렌즈를 세계 최초로 개발했다.
실리콘 소재를 곡면으로 가공해 만드는 카메라렌즈에 사용되는 기존방식과는 달리 이번에 개발된 렌즈는 평평한 실리콘 웨이퍼를 소재로 반도체 양산공정으로 제작해 비용을 최대 1/100 수준으로 낮출 수 있으며 제작시간도 훨씬 단축시킬 수 있다. 광원 추출효율은 4배 이상 향상시켰다.
테라헤르츠파는 0.1THz~30THz(테라헤르츠, 1조헤르츠) 대역의 전자기파로 가시광선이나 적외선보다 파장이 길어 X선처럼 물체의 내부를 높은 해상도로 정확히 식별할 수 있어 보안검색, 의료영상기술 등 비파괴 검사 도구나 의료용 진단기구의 성능을 획기적으로 향상시킬 수 있을 것으로 전망된다.
그러나 넓은 대역의 주파수 특성으로 인해 손실되는 전자기파의 비율이 높아 테라헤르츠파를 높은 효율로 집중시킬 수 있는 광학소자 개발이 요구됐다.
정 교수 연구팀은 평평한 실리콘에 테라헤르츠파 파장(약 300㎛) 보다 작은 80~120㎛ 크기의 구멍을 반도체 양산방법인 광식각공정으로 만들었다. 렌즈 가장자리로 갈수록 홀 사이즈는 크게 만들었다.
테라헤르츠파를 쪼이자 공기와 실리콘 중 공기 비율이 높은 가장자리는 굴절률이 낮았으며, 상대적으로 공기의 비율이 낮은 가운데는 굴절률이 높았다. 평평한 소재를 광학특성을 공학적으로 설계해 빛을 모으는 볼록렌즈와 같은 기능을 한 것으로 신기루 현상과 같은 물리적 효과와 같다.
이번 연구를 주도한 정기훈 교수는 “자연현상에서 착안해 자연계에 존재하지 않는 다양한 광학특성을 띄는 메타물질을 인공적으로 만든 것”이라며 “물질적 제약으로 인해 다양한 광학소자개발이 더딘 테라헤르츠파 기술 진보에 상당한 도움이 될 것”이라고 연구의의를 밝혔다.
미래창조과학부가 지원하는 한국연구재단의 도약연구자지원사업, 그린나노기술개발사업, 글로벌프론티어사업의 일환으로 수행된 이번 연구는 미국물리협회에서 발간하는 귄위 있는 국제학술지인 ‘어플라이드 피직스 레터(Applied Physics Letter)’에 9월자 특집논문 및 표지논문(제1저자 박상길 박사과정)으로 게재됐다.
그림1. 유전체 메타물질을 이용한 실리콘 굴절률 분포형 렌즈. 머리카락 굵기(80~120µm) 수준의 구멍이 실리콘 기판에 서로 다른 크기로 형성돼 있다.
그림2. 굴절률 분포형 렌즈 원리
그림3. 신기루 현상신기루는 아스팔트 도로 위에서 흔하게 나타나는 대기 굴절 현상이다. 이 현상은 도로면이 물체를 반사하는 것처럼 보이게 하는데 이 때문에 도로면에 물웅덩이가 있는 것처럼 착각하게 된다. 아래 사진에는 멀리서 다가오는 차의 상이 도로면을 통해 보인다. <사진 : 경기북과학고등학교 조영우 선생님 제공>
그림4. 논문표지
2014.09.24 조회수 24747 종이 한 장으로 구제역 조기 진단 가능해진다
지난 2010년 11월 말 경북 안동에서 시작돼 이듬해 4월 초까지 전국으로 퍼졌던 구제역파동은 직접적인 피해액만 3조원으로 추산되며 경제 전반에 미친 파급효과는 5조원 이상이라는 분석도 있다.
구제역과 같은 전염성 강한 질병을 현장에서 즉시 진단할 수 없기 때문에 피해가 확산될 가능성이 높다. 의심신고가 들어오면 시료를 채취해 전문기관에서 분석하는 데만 2~3일 걸린다. 그 사이 바이러스는 걷잡을 수 없이 퍼진다.
구제역, 조류독감, 신종플루 등 전염성이 강한 질병 진단을 위한 바이오센서를 저렴한 가격에 만들 수 있게 됐다.
우리 학교 생명화학공학과 정기준·임성갑(41) 교수 공동연구팀은 종이나 비닐 등 다양한 물질에 항체를 고정하는데 성공해 보급형 바이오센서개발에 필요한 원천기술을 확보했다.
연구결과는 세계적 학술지 ‘폴리머 케미스트리(Polymer Chemistry)’ 후면 표지논문(7월 7일자)으로 게재됐다.
바이오센서의 기판은 안정성이 높은 금이나 유리를 주로 사용한다. 그러나 가격이 비싸고 휴대성이 떨어지기 때문에 현장에서 쓰기 어렵다.
게다가 항원 진단을 위해 사용되는 항체의 높은 생산 단가로 인해 진단시스템의 가격이 비싸 축산농가 등에 보급이 어려웠다.
연구팀은 기존에 있던 두 가지 핵심기술을 보급형 바이오센서 개발에 활용했다.
연구팀은 바이오센서의 제조단가를 획기적으로 줄이는 동시에 휴대성을 높이기 위해 초기 화학적 진공증착법(iCVD, Initiated chemical vapour deposition)으로 종이나 비닐에 고분자 박막을 증착했다. 또 박막과의 화학적 반응을 통해 항체 단백질을 안정적으로 고정하는데도 성공했다.
이와 함께 가격이 비싸고 고온에 견디지 못했던 기존의 항체 대신, 미생물을 기반으로 만들어 저렴하면서도 70℃의 높은 온도에서도 뛰어난 안정성을 보여주는 ‘크링글도메인’이라는 유사항체를 활용했다.
그 결과 연구팀은 기존 진단시스템의 고비용·불안정성 문제를 동시에 해결했다.
이번 연구를 주도한 정기준 교수는 “기판을 종이나 비닐로 대체하고 유사항체를 활용해 지금보다 훨씬 저렴하면서도 안정성 높은 바이오센서를 만드는 것이 핵심기술”이라고 설명했다.
이와 함께 “최근 국내에서 발병해 국민경제에 커다란 피해를 유발했던 구제역처럼 급속한 전파력을 갖는 바이러스성 질병을 현장에서 신속하게 진단할 수 있을 것”이라며 “향후 포스트잇 또는 책자 형태로 바이오센서를 만들어 축산농가에 보급되면 전수조사가 가능해져 무조건적인 살처분을 막고 샘플링검사로 인한 부정확성을 줄일 수 있을 것”이라고 말했다.
한편, 이번 연구는 미래창조과학부 신기술융합형 성장동력사업(바이오제약) 및 글로벌프론티어사업(차세대바이오매스연구단)의 지원을 받아 수행됐다.
그림1. 종이 비닐 등 다양한 표면 물질 위에 단백질을 고정화하는 기술의 모식도
그림2. 비닐(a)과 종이(b)에 고정화된 비항체 단백질 골격을 이용한 바이오센서
그림3. 고분자 박막 증착 기술에 기반한 단백질 고정화 시스템 이미지
2014.07.16 조회수 17083
종이 한 장으로 구제역 조기 진단 가능해진다
지난 2010년 11월 말 경북 안동에서 시작돼 이듬해 4월 초까지 전국으로 퍼졌던 구제역파동은 직접적인 피해액만 3조원으로 추산되며 경제 전반에 미친 파급효과는 5조원 이상이라는 분석도 있다.
구제역과 같은 전염성 강한 질병을 현장에서 즉시 진단할 수 없기 때문에 피해가 확산될 가능성이 높다. 의심신고가 들어오면 시료를 채취해 전문기관에서 분석하는 데만 2~3일 걸린다. 그 사이 바이러스는 걷잡을 수 없이 퍼진다.
구제역, 조류독감, 신종플루 등 전염성이 강한 질병 진단을 위한 바이오센서를 저렴한 가격에 만들 수 있게 됐다.
우리 학교 생명화학공학과 정기준·임성갑(41) 교수 공동연구팀은 종이나 비닐 등 다양한 물질에 항체를 고정하는데 성공해 보급형 바이오센서개발에 필요한 원천기술을 확보했다.
연구결과는 세계적 학술지 ‘폴리머 케미스트리(Polymer Chemistry)’ 후면 표지논문(7월 7일자)으로 게재됐다.
바이오센서의 기판은 안정성이 높은 금이나 유리를 주로 사용한다. 그러나 가격이 비싸고 휴대성이 떨어지기 때문에 현장에서 쓰기 어렵다.
게다가 항원 진단을 위해 사용되는 항체의 높은 생산 단가로 인해 진단시스템의 가격이 비싸 축산농가 등에 보급이 어려웠다.
연구팀은 기존에 있던 두 가지 핵심기술을 보급형 바이오센서 개발에 활용했다.
연구팀은 바이오센서의 제조단가를 획기적으로 줄이는 동시에 휴대성을 높이기 위해 초기 화학적 진공증착법(iCVD, Initiated chemical vapour deposition)으로 종이나 비닐에 고분자 박막을 증착했다. 또 박막과의 화학적 반응을 통해 항체 단백질을 안정적으로 고정하는데도 성공했다.
이와 함께 가격이 비싸고 고온에 견디지 못했던 기존의 항체 대신, 미생물을 기반으로 만들어 저렴하면서도 70℃의 높은 온도에서도 뛰어난 안정성을 보여주는 ‘크링글도메인’이라는 유사항체를 활용했다.
그 결과 연구팀은 기존 진단시스템의 고비용·불안정성 문제를 동시에 해결했다.
이번 연구를 주도한 정기준 교수는 “기판을 종이나 비닐로 대체하고 유사항체를 활용해 지금보다 훨씬 저렴하면서도 안정성 높은 바이오센서를 만드는 것이 핵심기술”이라고 설명했다.
이와 함께 “최근 국내에서 발병해 국민경제에 커다란 피해를 유발했던 구제역처럼 급속한 전파력을 갖는 바이러스성 질병을 현장에서 신속하게 진단할 수 있을 것”이라며 “향후 포스트잇 또는 책자 형태로 바이오센서를 만들어 축산농가에 보급되면 전수조사가 가능해져 무조건적인 살처분을 막고 샘플링검사로 인한 부정확성을 줄일 수 있을 것”이라고 말했다.
한편, 이번 연구는 미래창조과학부 신기술융합형 성장동력사업(바이오제약) 및 글로벌프론티어사업(차세대바이오매스연구단)의 지원을 받아 수행됐다.
그림1. 종이 비닐 등 다양한 표면 물질 위에 단백질을 고정화하는 기술의 모식도
그림2. 비닐(a)과 종이(b)에 고정화된 비항체 단백질 골격을 이용한 바이오센서
그림3. 고분자 박막 증착 기술에 기반한 단백질 고정화 시스템 이미지
2014.07.16 조회수 17083 고효율 나노발전기 상용화길 열어
아주 작은 움직임으로도 전기를 생산하는 나노발전기가 개발됐다. 몸에 붙이고 다니면 충전되는 웨어러블 전자기기 전력원 등 다양한 활용이 기대된다.
우리 학교 신소재공학과 이건재 교수팀은 레이저 박리 전사기술과 유연한 압전박막 소재를 활용해 기존보다 약 40배 높은 효율을 갖는 나노발전기 개발에 성공했다.
연구결과는 세계적 학술지 ‘어드밴스드 머티리얼스(Advanced Materials)’ 4월 23일자 표지논문으로 게재됐다.
나노발전기는 유연한 나노소재에 미세한 압력이나 구부러짐이 가해질 때 전기 에너지가 생성되는 기술이다. 전선과 배터리 없이도 에너지공급이 가능하기 때문에 휘어지는 전자제품은 물론 심장 박동기와 같이 몸속에 집어넣는 기기나 로봇의 에너지원으로도 활용 가능하다. 그러나 지금까지는 에너지 효율이 낮고 제작공정이 복잡해 상용화가 어려웠다.
이 교수 연구팀은 고온에서 결정화된 고효율 압전박막물질을 현재 상용화된 레이저 박리기술을 이용해 딱딱한 기판에서 플라스틱 기판으로 전사, 효율을 크게 향상시키면서도 대면적으로 양산 가능성을 높였다.
이번에 개발된 유연한 기판(2cm × 2cm)에 만들어진 나노발전기는 미세한 구부림에 의해 생성된 에너지(250V, 8㎂)로 105개의 LED를 작동시키는데 성공했다.
이 교수는 “이번에 개발된 고효율의 나노발전기술은 자연에서 발생하는 바람, 진동, 소리와 같은 미세한 에너지는 물론 심장박동, 혈액흐름, 근육수축·이완 등 사람 몸에서 발생되는 생체역학적 힘을 이용해 전기를 생산할 수 있는 무한 에너지원으로 사용될 수 있다”고 응용가능성에 대해 설명했다.
이와 함께 “발전효율이 세계최고기록보다 40여배 높고 대량 양산이 가능한 레이저 박리기술을 활용해 그동안 상용화를 가로막았던 저효율과 복잡한 제조공정의 문제점을 해결했다는데 큰 의의가 있다”고 말했다.
이 교수팀은 향후 압전박막물질을 삼차원으로 적층해 생성전력을 더욱 높이고 이를 동물에 이식하는 생체실험을 수행할 계획이다.
이번 연구결과는 미래창조과학부 도약연구사업과 ‘코오롱-카이스트 라이프스타일 이노베이션센터(KOLON-KAIST LifeStyle Innovation Center)’의 지원으로 수행됐다.
그림1. 레이저 박리 기술로 제작된 대면적 형태의 나노발전기 이미지(논문표지)
그림2. 플라스틱에 제작된 나노발전기에서 생성된 전력을 이용해 105개의 LED를 작동하는 모습
2014.05.15 조회수 21469
고효율 나노발전기 상용화길 열어
아주 작은 움직임으로도 전기를 생산하는 나노발전기가 개발됐다. 몸에 붙이고 다니면 충전되는 웨어러블 전자기기 전력원 등 다양한 활용이 기대된다.
우리 학교 신소재공학과 이건재 교수팀은 레이저 박리 전사기술과 유연한 압전박막 소재를 활용해 기존보다 약 40배 높은 효율을 갖는 나노발전기 개발에 성공했다.
연구결과는 세계적 학술지 ‘어드밴스드 머티리얼스(Advanced Materials)’ 4월 23일자 표지논문으로 게재됐다.
나노발전기는 유연한 나노소재에 미세한 압력이나 구부러짐이 가해질 때 전기 에너지가 생성되는 기술이다. 전선과 배터리 없이도 에너지공급이 가능하기 때문에 휘어지는 전자제품은 물론 심장 박동기와 같이 몸속에 집어넣는 기기나 로봇의 에너지원으로도 활용 가능하다. 그러나 지금까지는 에너지 효율이 낮고 제작공정이 복잡해 상용화가 어려웠다.
이 교수 연구팀은 고온에서 결정화된 고효율 압전박막물질을 현재 상용화된 레이저 박리기술을 이용해 딱딱한 기판에서 플라스틱 기판으로 전사, 효율을 크게 향상시키면서도 대면적으로 양산 가능성을 높였다.
이번에 개발된 유연한 기판(2cm × 2cm)에 만들어진 나노발전기는 미세한 구부림에 의해 생성된 에너지(250V, 8㎂)로 105개의 LED를 작동시키는데 성공했다.
이 교수는 “이번에 개발된 고효율의 나노발전기술은 자연에서 발생하는 바람, 진동, 소리와 같은 미세한 에너지는 물론 심장박동, 혈액흐름, 근육수축·이완 등 사람 몸에서 발생되는 생체역학적 힘을 이용해 전기를 생산할 수 있는 무한 에너지원으로 사용될 수 있다”고 응용가능성에 대해 설명했다.
이와 함께 “발전효율이 세계최고기록보다 40여배 높고 대량 양산이 가능한 레이저 박리기술을 활용해 그동안 상용화를 가로막았던 저효율과 복잡한 제조공정의 문제점을 해결했다는데 큰 의의가 있다”고 말했다.
이 교수팀은 향후 압전박막물질을 삼차원으로 적층해 생성전력을 더욱 높이고 이를 동물에 이식하는 생체실험을 수행할 계획이다.
이번 연구결과는 미래창조과학부 도약연구사업과 ‘코오롱-카이스트 라이프스타일 이노베이션센터(KOLON-KAIST LifeStyle Innovation Center)’의 지원으로 수행됐다.
그림1. 레이저 박리 기술로 제작된 대면적 형태의 나노발전기 이미지(논문표지)
그림2. 플라스틱에 제작된 나노발전기에서 생성된 전력을 이용해 105개의 LED를 작동하는 모습
2014.05.15 조회수 21469 건강한 망막혈관 생성을 유도하는 치료방법 개발
- 향후 당뇨망막병증 치료방법으로 적용 기대
우리 학교 연구진이 실명으로 이어질 수 있는 망막혈관 질환치료의 실마리를 찾아냈다. 혈액공급이 잘되지 않는 망막 부위로 건강한 망막혈관이 생성되도록 하여 망막신경을 보호하는 혈관생성단백질을 찾아낸 것. 향후 당뇨망막병증*과 미숙아망막병증**의 치료방법 개선을 위한 연구의 단초가 될 것으로 기대된다.
이번 연구결과는 국내에서 전문적인 기초과학 교육을 받고 있는 안과 전문의 연구원에 의해 이루어진 대표적인 중개연구의 결과여서 더욱 주목받고 있다.
* 미숙아망막병증 : 망막 혈관의 발달이 완성되지 않은 시기에 출생한 미숙아에서 발생하는 망막 혈관질환으로 소아실명의 가장 흔한 원인 질환이다.
* 당뇨망막병증 : 당뇨병의 합병증으로 망막조직으로의 불충분한 혈액공급으로 생기는 망막 혈관질환으로 성인실명의 중요한 원인 질환이다.
우리 학교 의과학대학원 이준엽 연구원이(안과 전문의, 지도교수: 고규영,유욱준) 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)의 지원으로 수행되었고, 연구결과는 사이언스 중개의학(Science Translational Medicine) 표지논문(9월 18일자)으로 소개되었다. 이 학술지는 임상의학과 기초과학을 연계하는 중개의학 분야 권위지로 사이언스지 자매지이다.
(논문명 : Angiopoietin-1 Guides Directional Angiogenesis Through Integrin αvβ5 Signaling for Recovery of Ischemic Retinopathy)
당뇨망막병증의 치료에는 망막조직을 파괴하는 레이저광응고술이나혈관증식과 혈액누출을 억제하는 항체치료제*가 적용되고 있다.
항체치료제는 망막신경을 파괴하지 않는 장점이 있지만 한시적으로 혈관증식을 억제할 뿐, 근본적인 해결이 아니어서 반복적인 치료가 필요하다는 한계가 있었다.
* 항체치료제 : 비정상적인 혈관증식과 혈액누출을 선택적으로 억제하기 위하여 개발된 항체로서, 현재 혈관내피세포성장인자 (VEGF)를 저해하는 아바스틴 (Avastin) 과 루센티스 (Lucentis) 가 대표적인 항체치료제이다.
연구팀은 개체의 발달과정에서 혈관의 생성과 안정화에 필수적이라고 알려진 안지오포이에틴-1* 단백질이 망막혈관의 생성과정에도 중요한 역할을 함을 동물실험을 통해 규명해냈다.
망막출혈에 의한 시력상실의 근본 원인이 되는 망막허혈**을 개선하고 망막신경을 보호하는 단백질을 알아낸 것이다.
망막조직으로 충분한 혈액을 공급해 망막신경의 기능을 보존하는 방식의 근본적인 치료방법 개발의 실마리가 될 것으로 기대된다.
* 망막허혈 : 망막 조직에 충분한 혈액 공급이 되지 않는 상태
* 안지오포이에틴-1(Angiopoietin-1) : 건강한 혈관의 생성을 유도하고 생성된 혈관의 안정화를 유지하는 데 중요한 성장인자.
실제 안지오포이에틴-1을 망막병증 생쥐모델의 안구에 투약한 결과 건강한 망막혈관의 생성이 촉진되어, 망막허혈에 따르는 비정상적인 혈관증식이나 망막출혈, 시력상실이 예방되었다.
이준엽 연구원은 “이번 연구는 안지오포이에틴-1이 망막혈관의 생성과 안정화에 중요한 인자라는 사실을 새롭게 규명함으로써 혈관생성을 억제하는 현재의 치료법에서 건강한 혈관을 생성하고 혈관의 기능을 강화하는 방식의 치료법으로 패러다임이 전환될 것을 기대한다”고 연구 의의를 밝혔다.
그림 1. 망막병증 생쥐모델에서의 안구 내 투여한 Angiopoietin-1의 역할 대조군에 비해 VEGF-Trap 치료군과 Angiopoietin-1 (Ang1) 치료군은 병적인 혈관의 증식을 유의하게 억제함 (아래), 추가적으로 Ang1 치료군은 망막 중심부의 무혈관부위(망막허혈)를 향하여 혈관이 생성되었고, 이러한 현상은 VEGF-Trap 치료군에서는 관찰되지 않음 (위).
그림 2. Angiopoietin-1에 의한 망막허혈과 망막 출혈의 감소 및 혈관의 정상화 (좌) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막허혈부위 면적(화살표)을 유의하게 감소시켰으며, 망막 출혈의 양도 Ang1 치료에 의해 감소함. (우) Ang1 에 의해 새롭게 형성된 혈관은 정상 망막 혈관과 같이 혈관주위세포에 의한 지지를 받는 구조적으로 안정된 혈관임.
그림 3. Angiopoietin-1에 의한 망막 신경 보호 효과 (위) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막 중앙부 와 주변부의 신경세포의 세포자멸사를 유의하게 억제함. (아래) 이러한 Ang1에 의한 망막 신경 보호 효과는 전기 생리학적 검사인 망막전위도 검사를 통해 확인됨.
그림 4. Angiopoietin-1 이 망막 혈관 생성을 유도하는 기전 Angiopoietin-1은 망막 혈관의 내피세포 (Endothelial cell) 에 작용하여 혈관의 안정성 유지에 중요한 역할을 할 뿐만 아니라 망막의 별아교세포 (Astrocyte) 의 integrin 수용체를 통하여 fibronectin 이라는 세포외기질의 생성을 증가시켜 망막 조직 내로의 혈관 생성의 경로를 안내하는 역할을 함.
2013.09.22 조회수 22612
건강한 망막혈관 생성을 유도하는 치료방법 개발
- 향후 당뇨망막병증 치료방법으로 적용 기대
우리 학교 연구진이 실명으로 이어질 수 있는 망막혈관 질환치료의 실마리를 찾아냈다. 혈액공급이 잘되지 않는 망막 부위로 건강한 망막혈관이 생성되도록 하여 망막신경을 보호하는 혈관생성단백질을 찾아낸 것. 향후 당뇨망막병증*과 미숙아망막병증**의 치료방법 개선을 위한 연구의 단초가 될 것으로 기대된다.
이번 연구결과는 국내에서 전문적인 기초과학 교육을 받고 있는 안과 전문의 연구원에 의해 이루어진 대표적인 중개연구의 결과여서 더욱 주목받고 있다.
* 미숙아망막병증 : 망막 혈관의 발달이 완성되지 않은 시기에 출생한 미숙아에서 발생하는 망막 혈관질환으로 소아실명의 가장 흔한 원인 질환이다.
* 당뇨망막병증 : 당뇨병의 합병증으로 망막조직으로의 불충분한 혈액공급으로 생기는 망막 혈관질환으로 성인실명의 중요한 원인 질환이다.
우리 학교 의과학대학원 이준엽 연구원이(안과 전문의, 지도교수: 고규영,유욱준) 수행한 이번 연구는 미래창조과학부와 한국연구재단이 추진하는 중견연구자지원사업(도약)의 지원으로 수행되었고, 연구결과는 사이언스 중개의학(Science Translational Medicine) 표지논문(9월 18일자)으로 소개되었다. 이 학술지는 임상의학과 기초과학을 연계하는 중개의학 분야 권위지로 사이언스지 자매지이다.
(논문명 : Angiopoietin-1 Guides Directional Angiogenesis Through Integrin αvβ5 Signaling for Recovery of Ischemic Retinopathy)
당뇨망막병증의 치료에는 망막조직을 파괴하는 레이저광응고술이나혈관증식과 혈액누출을 억제하는 항체치료제*가 적용되고 있다.
항체치료제는 망막신경을 파괴하지 않는 장점이 있지만 한시적으로 혈관증식을 억제할 뿐, 근본적인 해결이 아니어서 반복적인 치료가 필요하다는 한계가 있었다.
* 항체치료제 : 비정상적인 혈관증식과 혈액누출을 선택적으로 억제하기 위하여 개발된 항체로서, 현재 혈관내피세포성장인자 (VEGF)를 저해하는 아바스틴 (Avastin) 과 루센티스 (Lucentis) 가 대표적인 항체치료제이다.
연구팀은 개체의 발달과정에서 혈관의 생성과 안정화에 필수적이라고 알려진 안지오포이에틴-1* 단백질이 망막혈관의 생성과정에도 중요한 역할을 함을 동물실험을 통해 규명해냈다.
망막출혈에 의한 시력상실의 근본 원인이 되는 망막허혈**을 개선하고 망막신경을 보호하는 단백질을 알아낸 것이다.
망막조직으로 충분한 혈액을 공급해 망막신경의 기능을 보존하는 방식의 근본적인 치료방법 개발의 실마리가 될 것으로 기대된다.
* 망막허혈 : 망막 조직에 충분한 혈액 공급이 되지 않는 상태
* 안지오포이에틴-1(Angiopoietin-1) : 건강한 혈관의 생성을 유도하고 생성된 혈관의 안정화를 유지하는 데 중요한 성장인자.
실제 안지오포이에틴-1을 망막병증 생쥐모델의 안구에 투약한 결과 건강한 망막혈관의 생성이 촉진되어, 망막허혈에 따르는 비정상적인 혈관증식이나 망막출혈, 시력상실이 예방되었다.
이준엽 연구원은 “이번 연구는 안지오포이에틴-1이 망막혈관의 생성과 안정화에 중요한 인자라는 사실을 새롭게 규명함으로써 혈관생성을 억제하는 현재의 치료법에서 건강한 혈관을 생성하고 혈관의 기능을 강화하는 방식의 치료법으로 패러다임이 전환될 것을 기대한다”고 연구 의의를 밝혔다.
그림 1. 망막병증 생쥐모델에서의 안구 내 투여한 Angiopoietin-1의 역할 대조군에 비해 VEGF-Trap 치료군과 Angiopoietin-1 (Ang1) 치료군은 병적인 혈관의 증식을 유의하게 억제함 (아래), 추가적으로 Ang1 치료군은 망막 중심부의 무혈관부위(망막허혈)를 향하여 혈관이 생성되었고, 이러한 현상은 VEGF-Trap 치료군에서는 관찰되지 않음 (위).
그림 2. Angiopoietin-1에 의한 망막허혈과 망막 출혈의 감소 및 혈관의 정상화 (좌) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막허혈부위 면적(화살표)을 유의하게 감소시켰으며, 망막 출혈의 양도 Ang1 치료에 의해 감소함. (우) Ang1 에 의해 새롭게 형성된 혈관은 정상 망막 혈관과 같이 혈관주위세포에 의한 지지를 받는 구조적으로 안정된 혈관임.
그림 3. Angiopoietin-1에 의한 망막 신경 보호 효과 (위) 대조군에 비해 Angiopoietin-1 (Ang1) 치료군은 망막 중앙부 와 주변부의 신경세포의 세포자멸사를 유의하게 억제함. (아래) 이러한 Ang1에 의한 망막 신경 보호 효과는 전기 생리학적 검사인 망막전위도 검사를 통해 확인됨.
그림 4. Angiopoietin-1 이 망막 혈관 생성을 유도하는 기전 Angiopoietin-1은 망막 혈관의 내피세포 (Endothelial cell) 에 작용하여 혈관의 안정성 유지에 중요한 역할을 할 뿐만 아니라 망막의 별아교세포 (Astrocyte) 의 integrin 수용체를 통하여 fibronectin 이라는 세포외기질의 생성을 증가시켜 망막 조직 내로의 혈관 생성의 경로를 안내하는 역할을 함.
2013.09.22 조회수 22612순수한 그래핀의 양자점 개발 성공 - 수 나노미터 직경의 완전히 순수한 그래핀 양자점 개발 -- “바이오센서, 광센서, 바이오 이미징 등 다양한 분야로 응용 가능” - 우리 학교 생명화학공학과 서태석(42) 교수와 물리학과 조용훈(48) 교수 공동 연구팀은 흑연 나노입자를 이용해 순수한 그래핀 양자점을 개발하는데 성공하고 그래핀 양자점에서의 방출되는 형광 빛의 원인을 밝혔다. 연구결과는 나노분야의 권위 있는 학술지 ‘어드밴스드 머티리얼스(Advanced Materials)’ 7월 19일자 표지논문(Back Cover)으로 게재됐다. 이번에 개발된 그래핀 양자점은 흑연으로 제작돼 인체에 무해한 친환경 소재라는 점에서 바이오센서, 광센서, 바이오 이미징 등 다양한 응용 분야에 적용할 수 있을 것으로 기대된다. 그래핀 양자점은 수 나노미터 이하의 직경을 갖고 있으며, 가시광 영역의 형광을 방출하는 특징이 있다. 기존 그래핀 양자점은 대부분 산화된 그래핀 양자점을 다시 환원하는 방식으로 제작했다. 따라서 그래핀 양자점 구조에 존재하는 순수한 탄소 결합과 산소 결합에 의한 형광 특성이 혼합돼 있어 발광의 근원을 정확하게 구분하기 어려웠다. 또 복잡한 화학적 방법으로 제작해 생산성이 떨어졌다. 연구팀은 그래핀 양자점의 정확한 발광 원인을 규명하기 위해 수 나노미터 크기의 흑연 나노입자를 이용해 순수한 그래핀 양자점을 산화반응 과정 없이 제작했다. 또 일반적으로 사용되고 있는 산화 과정을 흑연 나노입자에 적용해 산화 그래핀 양자점을 간단하게 제작하는 방법도 개발했다. 연구팀은 개발된 순수한 그래핀 양자점과 산화 그래핀 양자점으로부터 각각 파란색과 녹색 형광의 빛을 방출하는 것을 확인했는데, 이 두 종류의 양자점들은 산소 결합의 유무에 근본적 차이가 있다는 것을 밝혔다. 이와 함께 다양한 광분석 기법을 이용해 순수한 그래핀 양자점의 파란색 형광 현상이 벤젠 형태의 탄소 결합에 의한 것임을 규명하고, 산화 그래핀 양자점의 녹색 발광이 그래핀에 결합된 다양한 산소 기능기에 의한 것임을 규명했다. 서태석 교수는 “순수한 그래핀 양자점의 개발과 발광 특성 분석을 통해 기존에 뚜렷하게 설명되지 않았던 그래핀 양자점에서의 파란색 형광 빛의 원인을 밝혀냈다”고 이번 연구의 의의를 밝혔다. KAIST 생명화학공학과 페이 리우(Fei Liu), 물리학과 장민호(제1저자) 박사과정 학생이 서태석, 조용훈 교수의 지도를 받아 수행한 이번 연구는 환경융합 신기술개발사업과 KAIST 나노융합연구소의 그래핀 연구센터 지원으로 수행됐다. 서태석 교수(왼쪽), 조용훈 교수(오른쪽)
2013.08.07 조회수 18152 유방암 세포의 자살을 유도하는 최적의 약물조합 발견
조광현 교수
- Science 자매지 표지논문 발표,“IT와 BT의 융합연구로 세포내 분자조절네트워크 제어를 통해 가능”-
국내 연구진이 대다수 암 발생에 직접 관여하는 것으로 알려진 암억제 유전자(p53)의 분자조절네트워크를 제어하여 유방암 세포의 사멸을 유도하는 최적의 약물조합을 찾아내, 향후 신개념 암치료제 개발에 새로운 단초를 열었다. 특히 이번 연구는 IT와 BT의 융합연구인 시스템 생물학 연구로 가능했다는 점에서 의미가 크다.
우리 학교 바이오및뇌공학과 조광현 석좌교수가 주도하고 최민수 박사과정생, 주시 박사, 정성훈 교수 및 시첸 박사과정생이 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약/도전연구)과 기초연구실사업의 지원으로 수행되었다.
연구결과는 세계 최고 과학전문지인 ‘사이언스’의 첫 번째 자매지로서 세포신호전달분야의 권위지인 ‘Science Signaling’지 최신호(11월 20일자) 표지논문으로 선정되었고, 사이언스지의 ‘편집자의 선택(Editor"s Choice)’에 하이라이트 특집기사로 소개되는 영예를 얻었다. (논문명: Attractor Landscape Analysis Reveals Feedback Loops in the p53 Network That Control the Cellular Response to DNA Damage)
유방암은 미국이나 유럽 등 선진국에서 발병하는 여성암 중 가장 흔한 암으로, 40~55세 미국 여성의 사망원인 1위를 차지한다.
지난 10월 15일에는 영국 일간지 ‘데일리메일’이 2040년까지 유방암 환자 수가 현재의 3배가 넘는 168만 명으로 늘어나 일명 “유방암 대란”이 일어날 수도 있다는 충격적인 연구결과를 보도하기도 하였다.
우리나라 보건복지부 자료에 따르면, 국내에서도 미국 등과 같이 유방암 발병빈도가 매년 증가하는 추세인데, 이것은 서구식 식습관과 저출산, 모유수유 기피 등 생활패턴의 변화에 기인한 것으로 알려져 있다.
p53은 ‘유전자의 수호자’로도 잘 알려진 암 억제 단백질로서 33년 전 처음 발견된 후 지금까지 암 치료를 위해 집중적으로 연구되는 분자이다.
p53은 세포의 증식 조절과 사멸 촉진 등 세포의 운명을 결정하는데 중요한 역할을 한다. 우리 몸의 세포가 손상되거나 오작동하면, p53은 세포주기의 진행을 중단시켜 손상된 DNA의 복제를 억제하고, 손상된 세포의 복구를 시도한다. 이 때 만일 세포가 복구될 수 없다고 판단되면, p53은 세포가 스스로 자살하도록 유도한다.
그러나 암세포는 이러한 p53의 기능이 정상적으로 작동되지 않아 이를 인위적으로 조절하여 암 치료에 응용하려는 시도가 꾸준히 이어져왔다. 그러나 지금까지 임상실험에서는 기대와는 달리 효과가 미미하거나 부작용이 발생하는 등 여러 문제점들이 나타났다.
이는 p53이 단독으로 작동하는 것이 아니라 복잡한 신호전달 네트워크 속에서 다수의 양성과 음성 피드백(positive and negative feedbacks)에 의해 조절되고 있었으나, 지금까지 p53만을 단독으로 집중 연구했기 때문이다. 즉, 다양한 피드백 조절에 의해 p53의 동역학적(dynamics) 변화와 기능이 결정되므로, 네트워크 전체를 이해하고 제어하는 시스템 생물학적 접근이 반드시 필요하다.
조광현 교수가 이끈 융합 연구팀은 p53을 중심으로 관련된 모든 실험 데이터를 집대성하여 p53의 조절 네트워크에 대한 수학모형을 구축하였다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 p53의 동역학적 변화 특성에 따른 세포의 운명(증식 또는 사멸) 조절과정을 밝혀내고 이를 효과적으로 제어할 수 있는 방법을 찾아냈다. 그리고 이 방법을 적용한 시뮬레이션 결과를 단일세포실험으로 검증하였다.
조광현 교수팀은 수많은 피드백으로 복잡하게 얽혀 있는 p53 조절 네트워크의 다양한 변이조건에 따른 컴퓨터 시뮬레이션 분석과 세포생물학실험으로, p53의 동역학적 특성과 기능을 결정하는 핵심 조절회로를 발견하고, 이와 같은 p53의 동역학적 특성 변화에 따라 세포의 운명이 달라질 수 있음을 규명하였다.
또한 유방암 세포의 네트워크 모형에서, 위의 분석결과로부터 찾아낸 핵심회로를 억제하는 표적약물(Wip1 억제제)과 기존의 표적항암약물(뉴트린, nutlin-3)을 조합하면 유방암 세포의 사멸을 매우 효율적으로 유도할 수 있음을 발견하였다. 그리고 실제 유방암 세포(MCF7)를 이용한 세포실험을 통해 직접 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 시스템 생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암세포의 조절과정을 네트워크 차원에서 분석하여 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 연구의의를 밝혔다.
한편, 조 교수의 이번 연구 논문은 23일자 사이언스 편집자의 선택(Editors" Choice)으로 선정되는 영예를 얻기도 했다.
여러 양성 및 음성 피드백으로 복잡하게 구성된 p53 조절네트워크
2012.11.23 조회수 18740
유방암 세포의 자살을 유도하는 최적의 약물조합 발견
조광현 교수
- Science 자매지 표지논문 발표,“IT와 BT의 융합연구로 세포내 분자조절네트워크 제어를 통해 가능”-
국내 연구진이 대다수 암 발생에 직접 관여하는 것으로 알려진 암억제 유전자(p53)의 분자조절네트워크를 제어하여 유방암 세포의 사멸을 유도하는 최적의 약물조합을 찾아내, 향후 신개념 암치료제 개발에 새로운 단초를 열었다. 특히 이번 연구는 IT와 BT의 융합연구인 시스템 생물학 연구로 가능했다는 점에서 의미가 크다.
우리 학교 바이오및뇌공학과 조광현 석좌교수가 주도하고 최민수 박사과정생, 주시 박사, 정성훈 교수 및 시첸 박사과정생이 참여한 이번 연구는 교육과학기술부(장관 이주호)와 한국연구재단(이사장 이승종)이 추진하는 중견연구자지원사업(도약/도전연구)과 기초연구실사업의 지원으로 수행되었다.
연구결과는 세계 최고 과학전문지인 ‘사이언스’의 첫 번째 자매지로서 세포신호전달분야의 권위지인 ‘Science Signaling’지 최신호(11월 20일자) 표지논문으로 선정되었고, 사이언스지의 ‘편집자의 선택(Editor"s Choice)’에 하이라이트 특집기사로 소개되는 영예를 얻었다. (논문명: Attractor Landscape Analysis Reveals Feedback Loops in the p53 Network That Control the Cellular Response to DNA Damage)
유방암은 미국이나 유럽 등 선진국에서 발병하는 여성암 중 가장 흔한 암으로, 40~55세 미국 여성의 사망원인 1위를 차지한다.
지난 10월 15일에는 영국 일간지 ‘데일리메일’이 2040년까지 유방암 환자 수가 현재의 3배가 넘는 168만 명으로 늘어나 일명 “유방암 대란”이 일어날 수도 있다는 충격적인 연구결과를 보도하기도 하였다.
우리나라 보건복지부 자료에 따르면, 국내에서도 미국 등과 같이 유방암 발병빈도가 매년 증가하는 추세인데, 이것은 서구식 식습관과 저출산, 모유수유 기피 등 생활패턴의 변화에 기인한 것으로 알려져 있다.
p53은 ‘유전자의 수호자’로도 잘 알려진 암 억제 단백질로서 33년 전 처음 발견된 후 지금까지 암 치료를 위해 집중적으로 연구되는 분자이다.
p53은 세포의 증식 조절과 사멸 촉진 등 세포의 운명을 결정하는데 중요한 역할을 한다. 우리 몸의 세포가 손상되거나 오작동하면, p53은 세포주기의 진행을 중단시켜 손상된 DNA의 복제를 억제하고, 손상된 세포의 복구를 시도한다. 이 때 만일 세포가 복구될 수 없다고 판단되면, p53은 세포가 스스로 자살하도록 유도한다.
그러나 암세포는 이러한 p53의 기능이 정상적으로 작동되지 않아 이를 인위적으로 조절하여 암 치료에 응용하려는 시도가 꾸준히 이어져왔다. 그러나 지금까지 임상실험에서는 기대와는 달리 효과가 미미하거나 부작용이 발생하는 등 여러 문제점들이 나타났다.
이는 p53이 단독으로 작동하는 것이 아니라 복잡한 신호전달 네트워크 속에서 다수의 양성과 음성 피드백(positive and negative feedbacks)에 의해 조절되고 있었으나, 지금까지 p53만을 단독으로 집중 연구했기 때문이다. 즉, 다양한 피드백 조절에 의해 p53의 동역학적(dynamics) 변화와 기능이 결정되므로, 네트워크 전체를 이해하고 제어하는 시스템 생물학적 접근이 반드시 필요하다.
조광현 교수가 이끈 융합 연구팀은 p53을 중심으로 관련된 모든 실험 데이터를 집대성하여 p53의 조절 네트워크에 대한 수학모형을 구축하였다.
또한 대규모 컴퓨터 시뮬레이션 분석을 통해 p53의 동역학적 변화 특성에 따른 세포의 운명(증식 또는 사멸) 조절과정을 밝혀내고 이를 효과적으로 제어할 수 있는 방법을 찾아냈다. 그리고 이 방법을 적용한 시뮬레이션 결과를 단일세포실험으로 검증하였다.
조광현 교수팀은 수많은 피드백으로 복잡하게 얽혀 있는 p53 조절 네트워크의 다양한 변이조건에 따른 컴퓨터 시뮬레이션 분석과 세포생물학실험으로, p53의 동역학적 특성과 기능을 결정하는 핵심 조절회로를 발견하고, 이와 같은 p53의 동역학적 특성 변화에 따라 세포의 운명이 달라질 수 있음을 규명하였다.
또한 유방암 세포의 네트워크 모형에서, 위의 분석결과로부터 찾아낸 핵심회로를 억제하는 표적약물(Wip1 억제제)과 기존의 표적항암약물(뉴트린, nutlin-3)을 조합하면 유방암 세포의 사멸을 매우 효율적으로 유도할 수 있음을 발견하였다. 그리고 실제 유방암 세포(MCF7)를 이용한 세포실험을 통해 직접 확인하였다.
조광현 교수는 “세포내 중요한 역할을 담당하는 분자들은 대부분 복잡한 조절관계 속에 놓여있기 때문에 기존의 직관적인 생물학 연구로 그 원리를 밝히는 것은 근본적인 한계가 있다. 이번 연구는 시스템 생물학으로 그 한계를 극복할 수 있음을 보여주는 대표적인 사례로, 특히 암세포의 조절과정을 네트워크 차원에서 분석하여 새로운 치료법을 개발할 수 있는 가능성을 제시하였다”고 연구의의를 밝혔다.
한편, 조 교수의 이번 연구 논문은 23일자 사이언스 편집자의 선택(Editors" Choice)으로 선정되는 영예를 얻기도 했다.
여러 양성 및 음성 피드백으로 복잡하게 구성된 p53 조절네트워크
2012.11.23 조회수 18740 곤충 눈을 모사한 무반사 미세렌즈 개발
정기훈 교수
- KAIST 정기훈 교수 연구팀, 세계적 물리학회지에 표지논문으로 게재돼, 국내외 특허출원 중 -
- 반도체 양산공정 그대로 활용할 수 있어 상용화 기대 커 -- 빛 반사율 1%이하로 낮춰 값비싼 무반사 코팅 대체 가능 -
국내 연구진이 곤충의 눈을 모사해 빛의 반사를 최소화한 무반사 미세렌즈를 개발하는데 성공했다. 이 렌즈는 특히 휴대폰, 디지털카메라 등에 적용된 이미지센서에 활용할 수 있는 데다, 기존 반도체 양산 공정을 그대로 활용할 수 있다는 점에서 상용화에 대한 기대가 크다.
우리 학교 바이오및뇌공학과 정기훈 교수 연구팀이 곤충의 눈 표면에 형성된 나노구조를 모사해 저렴하면서도 빛 반사율을 1%이하로 낮춘 무반사 미세렌즈 양산기술을 개발하는 데 성공했다.
KAIST는 정 교수 연구팀이 개발한 이번 기술을 카메라 이미지센서용 미세렌즈에 적용할 경우 집광효율이 높기 때문에 대조 효과와 밝기에 대한 특성이 우수한 고감도 카메라를 만들 수 있다는 점에서 국내외로부터 많은 관심을 받을 것으로 예상된다고 설명했다.
특히 정 교수팀이 개발한 공정은 이미 상용화 중에 있는 기존의 반도체공정을 그대로 활용할 수 있다. 따라서 렌즈 표면에 굴절률이 낮은 막을 여러 번 입히는 기존의 무반사 코팅보다 제품 제작비용이 훨씬 줄어들 것으로 기대된다고 강조했다.
나비, 잠자리 등 곤충의 눈은 대부분 겹눈 2개로 구성돼 있다. 이들 곤충은 겹눈을 형성하는 벌집모양의 낱눈을 약 1만~3만 개를 가지고 있는데, 낱눈에는 수많은 나노 돌기가 빛의 투과를 돕는 역할을 한다.
연구팀은 이 같은 특성을 갖는 곤충의 눈이 오랜 진화를 통해 최적의 조건을 만들어 온 것으로 판단해, 컴퓨터 시뮬레이션을 거쳐 빛이 가장 잘 투과되는 나노 구조라는 것을 알아냈다.
이후 이 구조를 모사해 수십 마이크로미터(㎛) 크기의 카메라 미세렌즈에 적용한 결과 반사율이 기존 10%에서 1%이하로 현격히 감소하는 특성을 확인했다.
정 교수 연구팀은 곤충에서 착안한 무반사 구조를 만들기 위해 기존 반도체 생산에 쓰이는 식각공정을 활용했다.
미세렌즈에 은 박막 코팅을 한 후 저온열처리를 통해 은나노 입자를 미세렌즈 표면에 형성시켰다. 이를 마스크로 삼아 렌즈표면을 건식 식각해 무반사 특성을 갖는 나노구조를 렌즈 곡면에 구현하는 데 성공했다.
정기훈 교수는 “곡면 구조의 카메라 미세렌즈 표면에서 빛의 반사가 심해 집광효율이 감소하는 문제가 있었는데, 몰포나비의 눈에 형성된 나노 구조에 착안해 기술개발에 성공했다”며 “기존 반도체공정을 그대로 이용할 수 있기 때문에 고가의 무 반사 코팅보다 훨씬 저렴한 단가로 카메라 이미지센서용 무반사 미세렌즈에 즉시 적용할 수 있다”고 말했다.
한편, 정기훈 교수가 주도하고 정혁진 박사과정 학생이 참여한 이번 연구는 세계적인 물리학회지 ‘어플라이드 피직스 레터스(Applied Physics Letters)’ 최신호(11월 12일자)에 표지논문으로 게재됐으며 현재 국내외 특허 출원중이다.
그림1. 곤충 겹눈(좌), 곤충의 낱눈(우)을 확대한 현미경 사진
그림2. 곤충 겹눈의 나노돌기 구조를 모사한 고효율 미세렌즈 배열. 무반사 렌즈는 일반 렌즈에 비해 표면 반사를 현격히 감소시켜 무반사 렌즈를 통해 맺힌 이미지의 선명도를 증가시킨다.
그림3. 카메라 이미지센서용 미세렌즈 개발 공정
1) 고분자 미세렌즈 배열 전면에 은 박막을 코팅
2) 가열을 통해 은 박막을 은 나노입자로 변형
3) 은 나노입자를 마스크로 삼아 렌즈 식각
4) 은 나노입자 제거하여 무반사 미세렌즈 배열 완성
그림4. 논문표지
2012.11.21 조회수 17097
곤충 눈을 모사한 무반사 미세렌즈 개발
정기훈 교수
- KAIST 정기훈 교수 연구팀, 세계적 물리학회지에 표지논문으로 게재돼, 국내외 특허출원 중 -
- 반도체 양산공정 그대로 활용할 수 있어 상용화 기대 커 -- 빛 반사율 1%이하로 낮춰 값비싼 무반사 코팅 대체 가능 -
국내 연구진이 곤충의 눈을 모사해 빛의 반사를 최소화한 무반사 미세렌즈를 개발하는데 성공했다. 이 렌즈는 특히 휴대폰, 디지털카메라 등에 적용된 이미지센서에 활용할 수 있는 데다, 기존 반도체 양산 공정을 그대로 활용할 수 있다는 점에서 상용화에 대한 기대가 크다.
우리 학교 바이오및뇌공학과 정기훈 교수 연구팀이 곤충의 눈 표면에 형성된 나노구조를 모사해 저렴하면서도 빛 반사율을 1%이하로 낮춘 무반사 미세렌즈 양산기술을 개발하는 데 성공했다.
KAIST는 정 교수 연구팀이 개발한 이번 기술을 카메라 이미지센서용 미세렌즈에 적용할 경우 집광효율이 높기 때문에 대조 효과와 밝기에 대한 특성이 우수한 고감도 카메라를 만들 수 있다는 점에서 국내외로부터 많은 관심을 받을 것으로 예상된다고 설명했다.
특히 정 교수팀이 개발한 공정은 이미 상용화 중에 있는 기존의 반도체공정을 그대로 활용할 수 있다. 따라서 렌즈 표면에 굴절률이 낮은 막을 여러 번 입히는 기존의 무반사 코팅보다 제품 제작비용이 훨씬 줄어들 것으로 기대된다고 강조했다.
나비, 잠자리 등 곤충의 눈은 대부분 겹눈 2개로 구성돼 있다. 이들 곤충은 겹눈을 형성하는 벌집모양의 낱눈을 약 1만~3만 개를 가지고 있는데, 낱눈에는 수많은 나노 돌기가 빛의 투과를 돕는 역할을 한다.
연구팀은 이 같은 특성을 갖는 곤충의 눈이 오랜 진화를 통해 최적의 조건을 만들어 온 것으로 판단해, 컴퓨터 시뮬레이션을 거쳐 빛이 가장 잘 투과되는 나노 구조라는 것을 알아냈다.
이후 이 구조를 모사해 수십 마이크로미터(㎛) 크기의 카메라 미세렌즈에 적용한 결과 반사율이 기존 10%에서 1%이하로 현격히 감소하는 특성을 확인했다.
정 교수 연구팀은 곤충에서 착안한 무반사 구조를 만들기 위해 기존 반도체 생산에 쓰이는 식각공정을 활용했다.
미세렌즈에 은 박막 코팅을 한 후 저온열처리를 통해 은나노 입자를 미세렌즈 표면에 형성시켰다. 이를 마스크로 삼아 렌즈표면을 건식 식각해 무반사 특성을 갖는 나노구조를 렌즈 곡면에 구현하는 데 성공했다.
정기훈 교수는 “곡면 구조의 카메라 미세렌즈 표면에서 빛의 반사가 심해 집광효율이 감소하는 문제가 있었는데, 몰포나비의 눈에 형성된 나노 구조에 착안해 기술개발에 성공했다”며 “기존 반도체공정을 그대로 이용할 수 있기 때문에 고가의 무 반사 코팅보다 훨씬 저렴한 단가로 카메라 이미지센서용 무반사 미세렌즈에 즉시 적용할 수 있다”고 말했다.
한편, 정기훈 교수가 주도하고 정혁진 박사과정 학생이 참여한 이번 연구는 세계적인 물리학회지 ‘어플라이드 피직스 레터스(Applied Physics Letters)’ 최신호(11월 12일자)에 표지논문으로 게재됐으며 현재 국내외 특허 출원중이다.
그림1. 곤충 겹눈(좌), 곤충의 낱눈(우)을 확대한 현미경 사진
그림2. 곤충 겹눈의 나노돌기 구조를 모사한 고효율 미세렌즈 배열. 무반사 렌즈는 일반 렌즈에 비해 표면 반사를 현격히 감소시켜 무반사 렌즈를 통해 맺힌 이미지의 선명도를 증가시킨다.
그림3. 카메라 이미지센서용 미세렌즈 개발 공정
1) 고분자 미세렌즈 배열 전면에 은 박막을 코팅
2) 가열을 통해 은 박막을 은 나노입자로 변형
3) 은 나노입자를 마스크로 삼아 렌즈 식각
4) 은 나노입자 제거하여 무반사 미세렌즈 배열 완성
그림4. 논문표지
2012.11.21 조회수 17097 DNA 기반 반도체 핵심 원천기술 개발
박현규 교수
- 분자 비콘을 이용해 모든(8가지) 논리게이트 구현하는 데 성공 -- 스몰(Small)誌 7월호 표지논문으로 실려 -
초소형 미래 바이오전자기기를 구현하기 위한 핵심기술 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 DNA를 이용해 모든 논리게이트를 구현하는 데 성공, 나노분야의 세계적 학술지 ‘스몰(Small)’ 7월호(23일자) 표지논문으로 실렸다.
현재 최첨단 기술로도 10nm(나노미터) 이하의 실리콘 기반 반도체 제작은 불가능한 것으로 알려져 있지만, DNA는 굵기가 2nm 정도로 가늘기 때문에 보다 저렴하면서도 획기적인 집적도를 가진 반도체를 만들 수 있을 것으로 기대된다.
2나노급 반도체가 개발되면 우표 크기의 메모리 반도체에 고화질 영화 10000편을 저장하는 등 현재 상용화중인 20나노급 반도체보다 약 100배의 용량을 담을 수 있게 된다.
DNA는 네 종류의 염기인 아데닌(adenine, A), 시토신(cytosine, C), 구아닌(guanin, G), 티민(thymine, T)이 연속적으로 연결돼 있는데 A는 T와, G는 C와 각각 특이적으로 결합하는 특성을 갖고 있다.
특정 DNA는 특이적으로 결합하는 염기서열을 지닌 또 다른 DNA와 결합해 이중나선 구조를 형성하는 데, 연구팀은 이러한 DNA의 특이적 결합 특성과 구조 변화에 따른 형광신호 특성이 있는 고리모양의 분자 비콘을 이용했다.
연구팀은 생체 DNA물질을 디지털 회로에서 사용되는 논리게이트와 같은 역할을 담당하도록 입력신호로 사용해 고리모양의 DNA가 열리거나 닫히도록 했다.
고리모양 DNA가 열린 형태에서는 형광신호가 증가하고 닫힌 상태에서는 형광 신호가 감소하며 이로 인해 발생하는 형광신호의 변화를 출력신호로 사용했다.
연구팀은 제한적인 시스템만을 구현하는 기존의 논리게이트의 문제점을 극복, 8가지 모든 논리게이트(AND, OR, XOR, INHIBIT, NAND, NOR, XNOR, IMPlCATION)를 구현하는 데 성공해 반도체 기술로써의 적용 가능성을 높였다.
이와 함께, 각각의 논리게이트의 연결을 통한 다중 논리게이트(Multilevel circuits)와 논리게이트의 재생성을 보여주는 데도 성공했다.
박현규 교수는 “하나의 분자 비콘을 모든 게이트 구성을 위한 보편적인 요소로 사용해 저렴하면서도 초고집적 바이오 전자기기의 가능성을 높였다”며 “앞으로 분자 수준의 전자 소자 연구에 큰 변화가 있을 것으로 예상된다”고 말했다.
이번 연구를 주도한 박기수 박사과정 학생(제1저자)은 “DNA는 10개의 염기서열 길이가 3.4nm이고 굵기가 2nm밖에 되지 않는 매우 작은 물질이기 때문에 이를 이용해 전자 소자를 구현하면 획기적인 집적도 향상을 이룰 수 있다”며 “간단한 시스템 디자인을 통해 정확한 논리게이트를 구현해 내 DNA 반도체를 탑재한 바이오컴퓨터가 곧 현실로 다가올 것”이라고 말했다.XOR 게이트 : 입력 DNA A(input A)와 입력 DNA B(input B) 둘 중 하나만 있을 때는 고리모양 DNA가 열려서 형광 신호가 나오고(출력신호 1), DNA A와 B가 모두 없을 경우와 모두 있는 경우에는 고리모양 DNA가 고리모양을 유지하여 형광을 발생하지 않게 함으로써 XOR 논리게이트를 정확하게 구현했다.
2012.09.18 조회수 16893
DNA 기반 반도체 핵심 원천기술 개발
박현규 교수
- 분자 비콘을 이용해 모든(8가지) 논리게이트 구현하는 데 성공 -- 스몰(Small)誌 7월호 표지논문으로 실려 -
초소형 미래 바이오전자기기를 구현하기 위한 핵심기술 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 DNA를 이용해 모든 논리게이트를 구현하는 데 성공, 나노분야의 세계적 학술지 ‘스몰(Small)’ 7월호(23일자) 표지논문으로 실렸다.
현재 최첨단 기술로도 10nm(나노미터) 이하의 실리콘 기반 반도체 제작은 불가능한 것으로 알려져 있지만, DNA는 굵기가 2nm 정도로 가늘기 때문에 보다 저렴하면서도 획기적인 집적도를 가진 반도체를 만들 수 있을 것으로 기대된다.
2나노급 반도체가 개발되면 우표 크기의 메모리 반도체에 고화질 영화 10000편을 저장하는 등 현재 상용화중인 20나노급 반도체보다 약 100배의 용량을 담을 수 있게 된다.
DNA는 네 종류의 염기인 아데닌(adenine, A), 시토신(cytosine, C), 구아닌(guanin, G), 티민(thymine, T)이 연속적으로 연결돼 있는데 A는 T와, G는 C와 각각 특이적으로 결합하는 특성을 갖고 있다.
특정 DNA는 특이적으로 결합하는 염기서열을 지닌 또 다른 DNA와 결합해 이중나선 구조를 형성하는 데, 연구팀은 이러한 DNA의 특이적 결합 특성과 구조 변화에 따른 형광신호 특성이 있는 고리모양의 분자 비콘을 이용했다.
연구팀은 생체 DNA물질을 디지털 회로에서 사용되는 논리게이트와 같은 역할을 담당하도록 입력신호로 사용해 고리모양의 DNA가 열리거나 닫히도록 했다.
고리모양 DNA가 열린 형태에서는 형광신호가 증가하고 닫힌 상태에서는 형광 신호가 감소하며 이로 인해 발생하는 형광신호의 변화를 출력신호로 사용했다.
연구팀은 제한적인 시스템만을 구현하는 기존의 논리게이트의 문제점을 극복, 8가지 모든 논리게이트(AND, OR, XOR, INHIBIT, NAND, NOR, XNOR, IMPlCATION)를 구현하는 데 성공해 반도체 기술로써의 적용 가능성을 높였다.
이와 함께, 각각의 논리게이트의 연결을 통한 다중 논리게이트(Multilevel circuits)와 논리게이트의 재생성을 보여주는 데도 성공했다.
박현규 교수는 “하나의 분자 비콘을 모든 게이트 구성을 위한 보편적인 요소로 사용해 저렴하면서도 초고집적 바이오 전자기기의 가능성을 높였다”며 “앞으로 분자 수준의 전자 소자 연구에 큰 변화가 있을 것으로 예상된다”고 말했다.
이번 연구를 주도한 박기수 박사과정 학생(제1저자)은 “DNA는 10개의 염기서열 길이가 3.4nm이고 굵기가 2nm밖에 되지 않는 매우 작은 물질이기 때문에 이를 이용해 전자 소자를 구현하면 획기적인 집적도 향상을 이룰 수 있다”며 “간단한 시스템 디자인을 통해 정확한 논리게이트를 구현해 내 DNA 반도체를 탑재한 바이오컴퓨터가 곧 현실로 다가올 것”이라고 말했다.XOR 게이트 : 입력 DNA A(input A)와 입력 DNA B(input B) 둘 중 하나만 있을 때는 고리모양 DNA가 열려서 형광 신호가 나오고(출력신호 1), DNA A와 B가 모두 없을 경우와 모두 있는 경우에는 고리모양 DNA가 고리모양을 유지하여 형광을 발생하지 않게 함으로써 XOR 논리게이트를 정확하게 구현했다.
2012.09.18 조회수 16893 C형 간염 바이러스의 간 손상 메카니즘 규명
- 부작용 없이 간세포 손상 억제하는 치료제 개발 길 열어 -- 의학분야 세계 최고수준 학술지 ‘헤파톨로지’ 9월호 표지논문 장식 -
의사출신으로 구성된 KAIST 연구진이 C형 간염 바이러스 기전을 밝혀내 치료제 개발에 탄력을 받게 됐다.
우리 학교 바이오및뇌공학과 최철희 교수와 의과학대학원 신의철 교수팀이 공동으로 C형 간염 바이러스에 감염된 환자의 간 손상에 대한 메카니즘을 세계 최초로 규명했다.
이번 연구결과로 앞으로 부작용이 없으면서도 간세포 손상이 적은 C형 간염 바이러스 치료제가 개발될 수 있을 것으로 기대된다.
C형 간염은 C형 간염 바이러스(HCV, Hepatitis C virus)에 감염되었을 때 이에 대응하기 위한 신체의 면역반응으로 인해 간에 염증이 생기는 질환이다.
C형 간염 바이러스는 전 세계적으로 약 1억 7천만 명, 그리고 우리나라에서도 1%정도가 감염되어 있는 것으로 추정된다. 감염되면 대부분 만성으로 변하며, 간경변증이나 간암을 유발해 사망할 수 있는 무서운 질병이다.
하지만 2005년 시험관 내 세포에서 C형 간염 바이러스의 감염이 성공하기 전까지는 세포실험이 불가능했고, 침팬지 이외에는 감염시키는 동물이 없어 동물실험이 어려워 연구에 한계가 있었다.
연구팀은 C형 간염 바이러스에 감염시킨 세포주를 이용해 바이러스가 면역을 담당하는 세포에 의해 분비되는 단백질인 종양괴사인자(TNF-α)에 의한 세포의 사멸이 크게 증가하는 메카니즘을 세계 최초로 밝혀냈다.
이와 함께 이러한 작용을 일으키는 바이러스 구성 단백질도 규명에도 성공했다.
기존에는 C형 간염 바이러스가 간 손상을 일으키는 기전을 밝혀내지 못해 주로 바이러스의 증식을 억제하는 데 초점을 맞춰 신약이 개발돼 부작용이 많았다.
이번 연구결과를 통해 바이러스에 의한 간세포 손상을 억제하는 부작용 없는 신약개발이 가능하게 될 것으로 전망된다.
최철희 교수는 “이번 연구를 통해 C형 간염 바이러스가 숙주의 간세포와 어떤 상호 작용을 하는지 밝혀내 감염 환자의 치료법을 획기적으로 개선할 수 있을 것”이라고 말했다.
신의철 교수는 “이번 연구는 기초의학과 응용의학의 융합연구가 성공한 대표적 사례”라며 “앞으로도 다학제간 융합연구를 실시하면 그동안 풀지 못했던 난제들을 효율적으로 해결할 수 있을 것”이라고 강조했다.
한편, 교육과학기술부 미래기반기술개발사업(신약타겟검증연구사업)의 지원을 받아 수행된 이번 연구 결과는 의학 분야의 세계적 학술지인 헤파톨로지(Hepatolog, Impact Factor=11.665) 9월호 표지 논문으로 선정됐다.
□ 연구 세부사항 설명
TNF-α(종양괴사인자)는 면역을 담당하는 세포에 의해 분비되는 단백질이다. HCV에 감염되면 바이러스의 증식을 억제하기 위해 체내의 면역작용이 활발해지고 TNF-α의 분비도 늘어난다.
TNF-α는 세포의 생존을 담당하는 NF-κB 신호전달과 세포의 죽음을 담당하는 JNK 신호 전달을 동시에 활성화시킨다. HCV에 감염되면, 세포의 생존을 담당하는 NF-κB 쪽 신호전달 경로만 선택적으로 활성을 억제하게 되고, TNF-α의 역할은 세포의 죽음 쪽으로 균형이 기울게 된다.
바이러스의 증식을 억제하기 위해 분비된 TNF-α가 오히려 간세포를 죽이게 되는 것이다. 이는 곧 간 손상을 뜻하며, HCV를 구성하는 10가지의 단백질 중 core, NF4B, NS5B 라는 단백질이 이러한 작용을 한다고 규명해냈다.
2012.09.04 조회수 18913
C형 간염 바이러스의 간 손상 메카니즘 규명
- 부작용 없이 간세포 손상 억제하는 치료제 개발 길 열어 -- 의학분야 세계 최고수준 학술지 ‘헤파톨로지’ 9월호 표지논문 장식 -
의사출신으로 구성된 KAIST 연구진이 C형 간염 바이러스 기전을 밝혀내 치료제 개발에 탄력을 받게 됐다.
우리 학교 바이오및뇌공학과 최철희 교수와 의과학대학원 신의철 교수팀이 공동으로 C형 간염 바이러스에 감염된 환자의 간 손상에 대한 메카니즘을 세계 최초로 규명했다.
이번 연구결과로 앞으로 부작용이 없으면서도 간세포 손상이 적은 C형 간염 바이러스 치료제가 개발될 수 있을 것으로 기대된다.
C형 간염은 C형 간염 바이러스(HCV, Hepatitis C virus)에 감염되었을 때 이에 대응하기 위한 신체의 면역반응으로 인해 간에 염증이 생기는 질환이다.
C형 간염 바이러스는 전 세계적으로 약 1억 7천만 명, 그리고 우리나라에서도 1%정도가 감염되어 있는 것으로 추정된다. 감염되면 대부분 만성으로 변하며, 간경변증이나 간암을 유발해 사망할 수 있는 무서운 질병이다.
하지만 2005년 시험관 내 세포에서 C형 간염 바이러스의 감염이 성공하기 전까지는 세포실험이 불가능했고, 침팬지 이외에는 감염시키는 동물이 없어 동물실험이 어려워 연구에 한계가 있었다.
연구팀은 C형 간염 바이러스에 감염시킨 세포주를 이용해 바이러스가 면역을 담당하는 세포에 의해 분비되는 단백질인 종양괴사인자(TNF-α)에 의한 세포의 사멸이 크게 증가하는 메카니즘을 세계 최초로 밝혀냈다.
이와 함께 이러한 작용을 일으키는 바이러스 구성 단백질도 규명에도 성공했다.
기존에는 C형 간염 바이러스가 간 손상을 일으키는 기전을 밝혀내지 못해 주로 바이러스의 증식을 억제하는 데 초점을 맞춰 신약이 개발돼 부작용이 많았다.
이번 연구결과를 통해 바이러스에 의한 간세포 손상을 억제하는 부작용 없는 신약개발이 가능하게 될 것으로 전망된다.
최철희 교수는 “이번 연구를 통해 C형 간염 바이러스가 숙주의 간세포와 어떤 상호 작용을 하는지 밝혀내 감염 환자의 치료법을 획기적으로 개선할 수 있을 것”이라고 말했다.
신의철 교수는 “이번 연구는 기초의학과 응용의학의 융합연구가 성공한 대표적 사례”라며 “앞으로도 다학제간 융합연구를 실시하면 그동안 풀지 못했던 난제들을 효율적으로 해결할 수 있을 것”이라고 강조했다.
한편, 교육과학기술부 미래기반기술개발사업(신약타겟검증연구사업)의 지원을 받아 수행된 이번 연구 결과는 의학 분야의 세계적 학술지인 헤파톨로지(Hepatolog, Impact Factor=11.665) 9월호 표지 논문으로 선정됐다.
□ 연구 세부사항 설명
TNF-α(종양괴사인자)는 면역을 담당하는 세포에 의해 분비되는 단백질이다. HCV에 감염되면 바이러스의 증식을 억제하기 위해 체내의 면역작용이 활발해지고 TNF-α의 분비도 늘어난다.
TNF-α는 세포의 생존을 담당하는 NF-κB 신호전달과 세포의 죽음을 담당하는 JNK 신호 전달을 동시에 활성화시킨다. HCV에 감염되면, 세포의 생존을 담당하는 NF-κB 쪽 신호전달 경로만 선택적으로 활성을 억제하게 되고, TNF-α의 역할은 세포의 죽음 쪽으로 균형이 기울게 된다.
바이러스의 증식을 억제하기 위해 분비된 TNF-α가 오히려 간세포를 죽이게 되는 것이다. 이는 곧 간 손상을 뜻하며, HCV를 구성하는 10가지의 단백질 중 core, NF4B, NS5B 라는 단백질이 이러한 작용을 한다고 규명해냈다.
2012.09.04 조회수 18913 화학과 학부생, 세계적 저널에 표지논문 게재
- 화학과 4학년 조상연, 물리학과 4년 김수민 학생, 말라리아 연구를 위한 광학영상 기술을 분석해 셀(Cell) 자매지 표지논문에 게재 -- 국내최초 소방관인 故 조용완씨 손자, 3월 의무소방요원으로 입대예정 -
“교수님, 하이젠 베르크(Werner Heisenberg) 같은 역사 속 과학자들은 20대 초반에 세계적인 연구 성과를 냈는데 저는 이대로 가다간 늦어버릴 것 같습니다. 교수님 연구실에서 융합연구를 할 수 있게 도와주세요”
우리 학교 화학과 4학년에 재학 중인 조상연(22) 君이 1학년 때 이 대학에서 물리화학 분야 융합연구의 세계적인 석학인 이효철 화학과 교수를 찾아 와 당차게 부탁한 한 마디다.
조상연 학생이 말라리아 연구와 관련해 제1저자로 발표한 논문이 셀(Cell)지가 발행하는 생명공학분야 최고 권위 학술지인 ‘생명공학의 동향(Trends in Biotechnology, IF=9.644)’ 2월호 표지논문으로 선정됐다.
근래 들어 학부생의 연구 참여가 활발해진 까닭에 과학기술논문인용색인(SCI)급 국제학술지에 논문이 실리는 경우가 가끔씩은 있었지만, 셀 자매지와 같은 세계적인 학술지에, 그것도 표지논문으로 실리는 경우는 거의 없었다. 하지만 오랜만에 KAIST 학부재학생인 조상연 君이 큰일을 이뤄내 학교 안팎으로부터 많은 화제를 모으고 있다.
광주과학고를 2년 만에 조기 졸업하고 2008년 KAIST에 입학한 조 군은 평소 연구에 대한 높은 관심으로 신입생 때부터 KAIST내 다양한 학과를 넘나들며 연구거리를 찾아다녔다.
2학년 때는 화학과 이효철 교수의 지도아래 학부생 연구지원 프로그램인 URP에 참여, ‘시간분해회절에 의한 용액 상 구조 동력학 분석’에 관한 탁월한 연구 성과를 거뒀다. 이 연구로 조 君은 2학년 학생으로는 이례적으로 최우수상을 수상하는 한편 후속연구비 1000만원과 해외학회 참가라는 특전을 받으며 두각을 보이기 시작했다.
바이오 및 뇌 공학과 김동섭 교수와 ‘알카인 수화반응을 촉매하는 단백질의 컴퓨터 디자인’에 대한 연구를 진행하는 한편 EEWS대학원 정유성 교수와는 ‘전산모사를 통한 이산화탄소 흡착 촉매 디자인’ 등에 대한 연구를 수행하기도 했었다.
이후 조상연 君은 2011년 2월부터 약 1년간 바이오광학분야 융합 연구에 대한 세계적 학자인 물리학과 및 광기술연구소 박용근(32) 교수의 지도를 받아 왔다. 이번 셀 자매지에 게재한 논문은 박용근 교수의 지도를 받으며 수행한 연구과제 중 하나다. 같은 공동저자 중 한명인 김수민 학생(24, 제2저자) 역시 물리학과 학부생으로 ‘개별연구제도’를 통해 연구에 참여했다.
조상연 학생은 ‘말라리아 연구를 위한 광학 영상기술’이라는 제목의 이번 논문을 통해 “학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 또 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다”며 문제를 제기했다.
이와 함께 첨단 광학기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 말라리아 연구를 크게 3가지로 나눠 체계적으로 광학기술을 이용하는 전략을 제시했다.
조 君의 이번 연구는 바이오 이미징 기술을 말라리아 감염질환 연구에 통합 적용하고, 말라리아 연구에 적용 가능한 광학영상 방법들을 소개함으로써, 다 학제 간 융합 연구시대에 경쟁력을 갖는 광학-의학연구 전략을 체계적으로 제시한 것으로 높이 평가받고 있다.
조상연 학생은 “고등학교 시절 SEE-KAIST 과제에 출품해 수상하면서 연구에 대한 재미를 느꼈고, 2학년 1학기까지 특정한 학과가 없는 무학과 제도를 운영해 다양한 분야의 융합연구를 할 수 있는 조건을 갖춘 국내 최고의 연구중심대학 KAIST로 진학을 결심했다”며 “특히, 학부생에게 관련분야 최고 교수와 연구기회를 주는 URP 및 개별연구제도로 인해 뛰어난 교수들의 지도와 학교의 충분한 재정적 지원 덕분에 큰 어려움 없이 마음껏 연구를 펼칠 수 있었다”고 말했다.
조 君은 이와 함께 “앞으로 목표는 세상에서 제일 재미있는 융합연구를 하는 과학자가 되는 것”이라며 “제가 하는 연구를 통해 전 세계 어려운 상황에 놓인 많은 사람들을 도우는 데 노력할 것”이라고 말했다.
조 君은 바쁜 학업생활 속에서도 지역사회를 위해 저소득층 중학생들을 위한 봉사단체인 ‘배움을 나누는 사람들’에서 2년간 꾸준히 봉사를 해왔으며, KAIST 자연과학 학술동아리인 ‘KINS’를 설립했고, 자연과학대학 소식지인 ‘KAIST Science’ 기자로도 활동해 왔다.
조 君은 현재 해외 대학원 입학을 계획하고 있으며 올 3월 입대해 의무소방요원으로 군복무를 할 예정이다. 조 君의 할아버지는 우리나라 최초의 소방관인 故 조용완 씨로 소방관에 대한 남다른 인연으로 군 생활을 시작할 예정이다.
한편, 이번 연구는 KAIST ‘신임교원정착연구사업‘과 ’광기술연구소연구사업‘의 일환으로 이뤄졌으며 화학과 학사과정 조상연(22, 제1저자) 君을 포함해 물리학과 학사과정 김수민(24, 제2저자) 학생과 물리학과 김영찬 박사(30, 공저자)가 함께 수행했다.(끝)
붙임 : 논문요약, 보충자료, 사진설명
<논문요약>
논문주제 : 말라리아 연구를 위한 광학 영상기술
학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다. 세계 각국은 말라리아 감염을 연구하고, 말라리아를 진단하고 치료하는 장비 개발에 박차를 가하고 있다.
빌게이츠 Microsoft사 전 회장 부부가 설립한 Bill & Melinda Gates 재단에서 말라리아 연구에 막대한 연구비를 지원하기 시작했으며, Apple, Google, Intel사 등이 연합 설립한 Intellectual ventures사에서도 빛을 이용한 말라리아 진단 연구를 진행하고 있는 것이 그 사례들이다.
최근에는 첨단 광학 기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 박 교수 연구팀은 말라리아 연구를 크게 3가지로 나누어 체계적으로 광학기술을 이용하는 전략을 제시했다.
▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하여 체외에서 광학 영상을 측정하는 방법과 ▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하지 않고, 적혈구 자체의 광학적 신호를 이용하여 체외에서 영상을 획득하는 방법 그리고 ▲체내에서 말라리아 기생충이 숙주 세포를 감염시키는 과정의 광학 영상을 획득하는 방법이다.
이 논문에서는 물리학(광학)과 의학(감염질환)의 효과적인 융합 연구를 위한 체계화된 전략을 소개했기 때문에 실제 말라리아를 연구하는 연구자들에게 실질적인 도움이 될 수 있을 것이라고 평가받고 있다.
제1저자로 참여한 조상연 학생은 “이번 논문은 연구팀에서 수행하고 있는 굴절률 차이를 이용한 광학영상기술 및 최신 광학영상 기술들이 말라리아에 어떻게 이용될 수 있는가를 소개함으로써, 말라리아 진단 및 치료 연구에 힘을 실어줄 수 있을 것으로 기대한다”고 말했다.
<보충자료: 용어설명>
○ SEE-KAIST1992년 첫 행사를 시작으로 `Open-KAIST`와 번갈아 격년제로 실시해오는 행사로 KAIST 연구 성과, 과학고 탐구 성과, 산업체 연구개발 제품 등을 직접 보고 체험할 수 있는 KAIST의 대표적인 과학문화 대중화 행사다.
○ 무학과제도학사과정의 우수한 학생들에게 학과선택의 자율성을 보장하기 위해 학과 구 분 없이 입학해 개인의 적성 등을 고려해 2학년 1학기를 마친 후 학과를 선택하는 제도.
○ URP
학사과정 학생들이 지도교수와 지도조교의 지도하에 실질적인 실험 및 연구를 할 수 있도록, 연구비 지원 및 학점 연계를 통해 학부생의 연구를 현실적으로 지원하는 프로그램
① Long-Term URP 프로그램 (연 1회 실시)
가. 연구기간 : 12개월 (2011년 12월 26일~2012년 12월 21일)
나. 지원내역
* 단독 : 장학금 1,500천원+연구비 3,000천원
* 팀 : 1인당 장학금 1,200천원+연구비 4,000천원
② 겨울/봄학기, 여름/가을학기 URP 프로그램
가. 연구기간 : 5개월~6개월
나. 지원내역
* 단독 : 장학금 1,000천원+연구비 1,500천원 * 팀 : 1인당 장학금 800천원+연구비 2,000천원
○ 하이젠베르크
하이젠베르크는 1901년 독일에서 출생했다. 그의 아버지는 의학교수였고 그는 뮌헨대학에서 아놀드 좀머펠트(Arnold Sommerfeld) 밑에서 이론물리를 공부했고, 1923년에 박사학위를 받았다. 같은 해에 그는 괴팅겐대학에서 보른(Max Born)의 조수가 되었으며, 다음해에는 강사가 된다. 다음 3년간 코펜하겐에서 닐스 보어와 함께 일하고, 1927년부터 1941년 까지 라이프치히대학의 이론물리학 교수가 된다.거기서 볼프강 파울리 등과 연구하며 양자 전기 역학과 양자장 이론을 발전 시켰고, 핵 물리학과 고 에너지 물리학의 발전에 넓고도 깊은 영향을 미쳤다. 불확정성 원리로 유명한 하이젠베르크는 양자역학의 탄생에 기여한 공로로 1932년 노벨물리학상을 받았다.
<사진설명>
조상연 학생의 지도교수인 물리학과 박용근 교수
연구자 사진 : 왼쪽부터 김수민 학생, 김영찬 박사, 조상연 학생
Trends in Biotechnology 2012년 2월 호 논문표지
2012.02.01 조회수 30510
화학과 학부생, 세계적 저널에 표지논문 게재
- 화학과 4학년 조상연, 물리학과 4년 김수민 학생, 말라리아 연구를 위한 광학영상 기술을 분석해 셀(Cell) 자매지 표지논문에 게재 -- 국내최초 소방관인 故 조용완씨 손자, 3월 의무소방요원으로 입대예정 -
“교수님, 하이젠 베르크(Werner Heisenberg) 같은 역사 속 과학자들은 20대 초반에 세계적인 연구 성과를 냈는데 저는 이대로 가다간 늦어버릴 것 같습니다. 교수님 연구실에서 융합연구를 할 수 있게 도와주세요”
우리 학교 화학과 4학년에 재학 중인 조상연(22) 君이 1학년 때 이 대학에서 물리화학 분야 융합연구의 세계적인 석학인 이효철 화학과 교수를 찾아 와 당차게 부탁한 한 마디다.
조상연 학생이 말라리아 연구와 관련해 제1저자로 발표한 논문이 셀(Cell)지가 발행하는 생명공학분야 최고 권위 학술지인 ‘생명공학의 동향(Trends in Biotechnology, IF=9.644)’ 2월호 표지논문으로 선정됐다.
근래 들어 학부생의 연구 참여가 활발해진 까닭에 과학기술논문인용색인(SCI)급 국제학술지에 논문이 실리는 경우가 가끔씩은 있었지만, 셀 자매지와 같은 세계적인 학술지에, 그것도 표지논문으로 실리는 경우는 거의 없었다. 하지만 오랜만에 KAIST 학부재학생인 조상연 君이 큰일을 이뤄내 학교 안팎으로부터 많은 화제를 모으고 있다.
광주과학고를 2년 만에 조기 졸업하고 2008년 KAIST에 입학한 조 군은 평소 연구에 대한 높은 관심으로 신입생 때부터 KAIST내 다양한 학과를 넘나들며 연구거리를 찾아다녔다.
2학년 때는 화학과 이효철 교수의 지도아래 학부생 연구지원 프로그램인 URP에 참여, ‘시간분해회절에 의한 용액 상 구조 동력학 분석’에 관한 탁월한 연구 성과를 거뒀다. 이 연구로 조 君은 2학년 학생으로는 이례적으로 최우수상을 수상하는 한편 후속연구비 1000만원과 해외학회 참가라는 특전을 받으며 두각을 보이기 시작했다.
바이오 및 뇌 공학과 김동섭 교수와 ‘알카인 수화반응을 촉매하는 단백질의 컴퓨터 디자인’에 대한 연구를 진행하는 한편 EEWS대학원 정유성 교수와는 ‘전산모사를 통한 이산화탄소 흡착 촉매 디자인’ 등에 대한 연구를 수행하기도 했었다.
이후 조상연 君은 2011년 2월부터 약 1년간 바이오광학분야 융합 연구에 대한 세계적 학자인 물리학과 및 광기술연구소 박용근(32) 교수의 지도를 받아 왔다. 이번 셀 자매지에 게재한 논문은 박용근 교수의 지도를 받으며 수행한 연구과제 중 하나다. 같은 공동저자 중 한명인 김수민 학생(24, 제2저자) 역시 물리학과 학부생으로 ‘개별연구제도’를 통해 연구에 참여했다.
조상연 학생은 ‘말라리아 연구를 위한 광학 영상기술’이라는 제목의 이번 논문을 통해 “학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 또 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다”며 문제를 제기했다.
이와 함께 첨단 광학기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 말라리아 연구를 크게 3가지로 나눠 체계적으로 광학기술을 이용하는 전략을 제시했다.
조 君의 이번 연구는 바이오 이미징 기술을 말라리아 감염질환 연구에 통합 적용하고, 말라리아 연구에 적용 가능한 광학영상 방법들을 소개함으로써, 다 학제 간 융합 연구시대에 경쟁력을 갖는 광학-의학연구 전략을 체계적으로 제시한 것으로 높이 평가받고 있다.
조상연 학생은 “고등학교 시절 SEE-KAIST 과제에 출품해 수상하면서 연구에 대한 재미를 느꼈고, 2학년 1학기까지 특정한 학과가 없는 무학과 제도를 운영해 다양한 분야의 융합연구를 할 수 있는 조건을 갖춘 국내 최고의 연구중심대학 KAIST로 진학을 결심했다”며 “특히, 학부생에게 관련분야 최고 교수와 연구기회를 주는 URP 및 개별연구제도로 인해 뛰어난 교수들의 지도와 학교의 충분한 재정적 지원 덕분에 큰 어려움 없이 마음껏 연구를 펼칠 수 있었다”고 말했다.
조 君은 이와 함께 “앞으로 목표는 세상에서 제일 재미있는 융합연구를 하는 과학자가 되는 것”이라며 “제가 하는 연구를 통해 전 세계 어려운 상황에 놓인 많은 사람들을 도우는 데 노력할 것”이라고 말했다.
조 君은 바쁜 학업생활 속에서도 지역사회를 위해 저소득층 중학생들을 위한 봉사단체인 ‘배움을 나누는 사람들’에서 2년간 꾸준히 봉사를 해왔으며, KAIST 자연과학 학술동아리인 ‘KINS’를 설립했고, 자연과학대학 소식지인 ‘KAIST Science’ 기자로도 활동해 왔다.
조 君은 현재 해외 대학원 입학을 계획하고 있으며 올 3월 입대해 의무소방요원으로 군복무를 할 예정이다. 조 君의 할아버지는 우리나라 최초의 소방관인 故 조용완 씨로 소방관에 대한 남다른 인연으로 군 생활을 시작할 예정이다.
한편, 이번 연구는 KAIST ‘신임교원정착연구사업‘과 ’광기술연구소연구사업‘의 일환으로 이뤄졌으며 화학과 학사과정 조상연(22, 제1저자) 君을 포함해 물리학과 학사과정 김수민(24, 제2저자) 학생과 물리학과 김영찬 박사(30, 공저자)가 함께 수행했다.(끝)
붙임 : 논문요약, 보충자료, 사진설명
<논문요약>
논문주제 : 말라리아 연구를 위한 광학 영상기술
학질모기에 의해 전염되는 말라리아에 전 세계적으로 매년 약 3억 명이 감염되고 수백만 명이 사망하고 있지만, 아직도 말라리아 질병의 많은 부분이 알려져 있지 않다. 세계 각국은 말라리아 감염을 연구하고, 말라리아를 진단하고 치료하는 장비 개발에 박차를 가하고 있다.
빌게이츠 Microsoft사 전 회장 부부가 설립한 Bill & Melinda Gates 재단에서 말라리아 연구에 막대한 연구비를 지원하기 시작했으며, Apple, Google, Intel사 등이 연합 설립한 Intellectual ventures사에서도 빛을 이용한 말라리아 진단 연구를 진행하고 있는 것이 그 사례들이다.
최근에는 첨단 광학 기술을 말라리아 연구에 적용하려는 노력이 최근 많은 주목을 받고 있는데, 박 교수 연구팀은 말라리아 연구를 크게 3가지로 나누어 체계적으로 광학기술을 이용하는 전략을 제시했다.
▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하여 체외에서 광학 영상을 측정하는 방법과 ▲말라리아에 감염된 적혈구를 외부 염색 물질을 사용하지 않고, 적혈구 자체의 광학적 신호를 이용하여 체외에서 영상을 획득하는 방법 그리고 ▲체내에서 말라리아 기생충이 숙주 세포를 감염시키는 과정의 광학 영상을 획득하는 방법이다.
이 논문에서는 물리학(광학)과 의학(감염질환)의 효과적인 융합 연구를 위한 체계화된 전략을 소개했기 때문에 실제 말라리아를 연구하는 연구자들에게 실질적인 도움이 될 수 있을 것이라고 평가받고 있다.
제1저자로 참여한 조상연 학생은 “이번 논문은 연구팀에서 수행하고 있는 굴절률 차이를 이용한 광학영상기술 및 최신 광학영상 기술들이 말라리아에 어떻게 이용될 수 있는가를 소개함으로써, 말라리아 진단 및 치료 연구에 힘을 실어줄 수 있을 것으로 기대한다”고 말했다.
<보충자료: 용어설명>
○ SEE-KAIST1992년 첫 행사를 시작으로 `Open-KAIST`와 번갈아 격년제로 실시해오는 행사로 KAIST 연구 성과, 과학고 탐구 성과, 산업체 연구개발 제품 등을 직접 보고 체험할 수 있는 KAIST의 대표적인 과학문화 대중화 행사다.
○ 무학과제도학사과정의 우수한 학생들에게 학과선택의 자율성을 보장하기 위해 학과 구 분 없이 입학해 개인의 적성 등을 고려해 2학년 1학기를 마친 후 학과를 선택하는 제도.
○ URP
학사과정 학생들이 지도교수와 지도조교의 지도하에 실질적인 실험 및 연구를 할 수 있도록, 연구비 지원 및 학점 연계를 통해 학부생의 연구를 현실적으로 지원하는 프로그램
① Long-Term URP 프로그램 (연 1회 실시)
가. 연구기간 : 12개월 (2011년 12월 26일~2012년 12월 21일)
나. 지원내역
* 단독 : 장학금 1,500천원+연구비 3,000천원
* 팀 : 1인당 장학금 1,200천원+연구비 4,000천원
② 겨울/봄학기, 여름/가을학기 URP 프로그램
가. 연구기간 : 5개월~6개월
나. 지원내역
* 단독 : 장학금 1,000천원+연구비 1,500천원 * 팀 : 1인당 장학금 800천원+연구비 2,000천원
○ 하이젠베르크
하이젠베르크는 1901년 독일에서 출생했다. 그의 아버지는 의학교수였고 그는 뮌헨대학에서 아놀드 좀머펠트(Arnold Sommerfeld) 밑에서 이론물리를 공부했고, 1923년에 박사학위를 받았다. 같은 해에 그는 괴팅겐대학에서 보른(Max Born)의 조수가 되었으며, 다음해에는 강사가 된다. 다음 3년간 코펜하겐에서 닐스 보어와 함께 일하고, 1927년부터 1941년 까지 라이프치히대학의 이론물리학 교수가 된다.거기서 볼프강 파울리 등과 연구하며 양자 전기 역학과 양자장 이론을 발전 시켰고, 핵 물리학과 고 에너지 물리학의 발전에 넓고도 깊은 영향을 미쳤다. 불확정성 원리로 유명한 하이젠베르크는 양자역학의 탄생에 기여한 공로로 1932년 노벨물리학상을 받았다.
<사진설명>
조상연 학생의 지도교수인 물리학과 박용근 교수
연구자 사진 : 왼쪽부터 김수민 학생, 김영찬 박사, 조상연 학생
Trends in Biotechnology 2012년 2월 호 논문표지
2012.02.01 조회수 30510 스마트폰 질병진단 원천기술 개발
- 신개념의 생체분자 검출기술로 휴대용 체외진단 분야에 획기적 원천기술- 화학분야 세계적 학술지 ‘앙게반테 케미’ 1월호(16일자) 표지논문 선정
스마트폰으로도 질병을 진단하는 원천기술이 국내 연구진에 의해 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 스마트폰을 비롯한 휴대용 개인기기에 널리 이용되고 있는 정전기방식의 터치스크린을 이용해 생체분자를 검출하는 원천기술을 세계 최초로 개발하는 데 성공했다.
앞으로 병원에 가지 않고도 스마트폰을 가지고 간단한 질병을 진단하는 시대가 열릴 것으로 기대된다.
최근 스마트폰과 같은 휴대용 전자기기에 적용되는 정전기방식의 터치스크린은 일반적으로 손가락의 접촉을 통해 발생하는 터치스크린 표면의 정전용량 변화를 감지해 작업을 수행하도록 설계돼 있다.
연구팀은 DNA가 자체의 정전용량을 가지고 있으며, 농도에 따라 정전용량이 변화한다는 사실에 착안해 정전기방식의 터치스크린을 생체분자 검출에 활용할 수 있을 것이라고 예상했다.
이를 규명하기 위해 연구팀은 대표적인 생체분자인 DNA를 터치스크린 위에 가하고 정전용량 변화량을 감지했다. 실험결과 터치스크린을 이용해 DNA의 유무와 농도를 정확하게 검출할 수 있었다.이 결과에 따라 DNA뿐만 아니라 세포, 단백질, 핵산, 등 대부분의 생체분자가 정전용량을 갖고 있기 때문에 다양한 생체물질의 검출에도 활용될 수 있다는 가능성을 제시했다는 게 이 기술의 큰 특징이다.
박현규 교수는 “모바일 기기 등에 입력장치로만 이용해 왔던 터치스크린으로 생체 분자 등의 분석에 이용할 수 있음을 세계 최초로 입증한 결과”라며 “이 원천기술을 이용해 앞으로 터치스크린 기반의 스마트폰 또는 태블릿 PC 등을 이용해 개인이 질병을 진단하는 시대가 올 것”이라고 말했다.
이와 함께 논문의 제1저자인 원병연 연구조교수는 “현재는 생체분자의 유무 또는 농도만 측정 가능한 단계이며, 앞으로 특정 생체분자를 선택적으로 검출할 수 있는 기술을 개발해 가까운 시일 내에 상용화에 주력할 것”이라고 덧붙였다.
한편, 이번 연구는 지식경제부가 시행하는 ‘산업원천기술개발사업’으로 수행됐으며, 연구의 중요성을 인정받아 화학 분야의 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 1월호(16일자) 표지논문으로 선정됐다.
그림1. 터치스크린을 이용한 생체 분자 검출 시스템 모식도 (앙게반테 케미 논문 표지). 휴대용 모바일 기기의 입력장치인 터치스크린 위에서 세포, 단백실, 핵산, 소분자 등의 생체 분자를 검출할 수 있다.
그림2. 정전용량 터치스크린 방식의 한가지인 surface capacitive touchscreen을 이용한 시스템 모식도. 여러 지점을 동시에 접촉했을 때 접촉점의 시료 농도에 따라 터치 신호의 위치가 변하는 원리를 이용한 방법. 동시에 두 개의 미지 시료의 농도를 측정할 수 있다.
그림3. 정전용량 터치스크린 방식의 한가지인 projected capacitive touchscreen을 이용한 시스템 모식도. 현재 스마트폰 등에 쓰이는 터치스크린 방식으로서, 터치스크린 표면 내부에 여러 라인의 전극이 패턴되어 있어, 각 전극의 정전용량 변화를 각각 측정함으로써 여러 접촉 시료의 농도를 동시에 검출할 수 있다.
2012.01.16 조회수 21488
스마트폰 질병진단 원천기술 개발
- 신개념의 생체분자 검출기술로 휴대용 체외진단 분야에 획기적 원천기술- 화학분야 세계적 학술지 ‘앙게반테 케미’ 1월호(16일자) 표지논문 선정
스마트폰으로도 질병을 진단하는 원천기술이 국내 연구진에 의해 개발됐다.
우리 학교 생명화학공학과 박현규 교수 연구팀이 스마트폰을 비롯한 휴대용 개인기기에 널리 이용되고 있는 정전기방식의 터치스크린을 이용해 생체분자를 검출하는 원천기술을 세계 최초로 개발하는 데 성공했다.
앞으로 병원에 가지 않고도 스마트폰을 가지고 간단한 질병을 진단하는 시대가 열릴 것으로 기대된다.
최근 스마트폰과 같은 휴대용 전자기기에 적용되는 정전기방식의 터치스크린은 일반적으로 손가락의 접촉을 통해 발생하는 터치스크린 표면의 정전용량 변화를 감지해 작업을 수행하도록 설계돼 있다.
연구팀은 DNA가 자체의 정전용량을 가지고 있으며, 농도에 따라 정전용량이 변화한다는 사실에 착안해 정전기방식의 터치스크린을 생체분자 검출에 활용할 수 있을 것이라고 예상했다.
이를 규명하기 위해 연구팀은 대표적인 생체분자인 DNA를 터치스크린 위에 가하고 정전용량 변화량을 감지했다. 실험결과 터치스크린을 이용해 DNA의 유무와 농도를 정확하게 검출할 수 있었다.이 결과에 따라 DNA뿐만 아니라 세포, 단백질, 핵산, 등 대부분의 생체분자가 정전용량을 갖고 있기 때문에 다양한 생체물질의 검출에도 활용될 수 있다는 가능성을 제시했다는 게 이 기술의 큰 특징이다.
박현규 교수는 “모바일 기기 등에 입력장치로만 이용해 왔던 터치스크린으로 생체 분자 등의 분석에 이용할 수 있음을 세계 최초로 입증한 결과”라며 “이 원천기술을 이용해 앞으로 터치스크린 기반의 스마트폰 또는 태블릿 PC 등을 이용해 개인이 질병을 진단하는 시대가 올 것”이라고 말했다.
이와 함께 논문의 제1저자인 원병연 연구조교수는 “현재는 생체분자의 유무 또는 농도만 측정 가능한 단계이며, 앞으로 특정 생체분자를 선택적으로 검출할 수 있는 기술을 개발해 가까운 시일 내에 상용화에 주력할 것”이라고 덧붙였다.
한편, 이번 연구는 지식경제부가 시행하는 ‘산업원천기술개발사업’으로 수행됐으며, 연구의 중요성을 인정받아 화학 분야의 세계적 학술지 ‘앙게반테 케미(Angewandte Chemie International Edition)’ 1월호(16일자) 표지논문으로 선정됐다.
그림1. 터치스크린을 이용한 생체 분자 검출 시스템 모식도 (앙게반테 케미 논문 표지). 휴대용 모바일 기기의 입력장치인 터치스크린 위에서 세포, 단백실, 핵산, 소분자 등의 생체 분자를 검출할 수 있다.
그림2. 정전용량 터치스크린 방식의 한가지인 surface capacitive touchscreen을 이용한 시스템 모식도. 여러 지점을 동시에 접촉했을 때 접촉점의 시료 농도에 따라 터치 신호의 위치가 변하는 원리를 이용한 방법. 동시에 두 개의 미지 시료의 농도를 측정할 수 있다.
그림3. 정전용량 터치스크린 방식의 한가지인 projected capacitive touchscreen을 이용한 시스템 모식도. 현재 스마트폰 등에 쓰이는 터치스크린 방식으로서, 터치스크린 표면 내부에 여러 라인의 전극이 패턴되어 있어, 각 전극의 정전용량 변화를 각각 측정함으로써 여러 접촉 시료의 농도를 동시에 검출할 수 있다.
2012.01.16 조회수 21488