-
 윤태영 교수팀, 생체막 단백질 기능 첫 규명
우리대학 윤태영 물리학과 교수 주도하에 생체막 단백질인 시냅토태그민1(Synaptotagmin1)이 신경세포 통신을 능동적으로 제어한다는 사실을 세계 최초로 규명하였다.
시냅토태그민1은 신경전달물질 분출을 조절하는 양대 핵심 단백질로서, 지금까지 학계는 단순히 칼슘 이온이 유입되면 시냅토태크민1이 신경전달물질을 분출하는 것으로 추정해 왔지만, 명확히 그 기능을 밝혀내지 못했다.
△카이스트 윤태영 물리학과 교수, △이한기 박사 △신연균 교수(포항공대, 아이오와주립대) △권대혁 교수(성균관대) △현창봉 교수 (고등과학원) 등이 참여한 이번 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 ‘기초연구실육성사업(BRL)"과 ‘세계 수준의 연구중심대학(WCU)육성사업’의 지원을 받아 수행되었고, 연구결과는 세계 최고 권위의 과학저널인 ‘사이언스(Science)’誌 5월 7일자에 게재된다. 이번 연구결과는 젊은 국내 토종박사들이 주축이 되어 불굴의 도전정신으로 일궈낸 값진 연구성과이다.
총 9명으로 구성된 연구팀에서 8명이 국내 연구자들로, 이중 7명이 만 40세를 넘지 않은 신진 연구자이다.
특히 연구를 주도한 윤태영 교수는 만 34세로 2004년 서울대에서, 이한기 박사는 만 33세로 명지대에서, 권대혁 교수는 만 38세로 서울대에서 박사학위를 받은 토종박사들이다.
또한 이번 연구성과는 정부의 대표적인 연구지원사업(BRL)과 인력 양성사업(WCU)의 지원을 받아 시너지 효과를 발휘하여, 세계 최고의 과학저널에 발표했다는 점에서 의의가 있다.
[그림1. 신경전달물질 분출에 있어서 시냅토태그민1의 동적제어 스위치 모델]
윤태영 교수 연구팀은 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어하는 스위치 역할을 한다는 새로운 사실을 밝혀냈다.
연구팀은 신경세포 내에 적정농도(10μmol/L, 1리터당 10마이크로 몰)의 칼슘 이온이 유입되면 시냅토태그민1은 신경전달물질을 빠르게 분출하지만, 적정농도 이상의 칼슘이 유입되면 오히려 그 기능이 감소된다는 사실을 최초로 확인하였다. 이것은 시냅토태그민1이 신경세포에서 나오는 칼슘 농도에 따라 다양하게 반응한다는 사실을 의미하는 것으로, 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어할 수 있다는 사실을 새롭게 규명한 것이다.
윤태영 교수팀의 이번 연구는 지난 10년간 학계의 풀리지 않은 수수께끼인 시냅토태그민1의 기능에 대한 명쾌한 해답을 제시하였다. 이번 연구는 낮은 농도의 칼슘에서 시냅토태그민1이 가장 활발히 활동한다는 사실을 최초로 발견하여, 기존 연구가 밝히지 못한 시냅토태그민1의 기능을 정확히 설명하였다.
특히 연구팀은 시냅토태그민1을 생체막으로부터 분리하면, 제어 스위치 기능이 상실된다는 사실도 확인하여, 시냅토태그민1의 생체막 부착 여부가 그 기능에 핵심인 것을 밝혀냈다.
또한 윤 교수팀은 차세대 신약개발의 주요 타깃인 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발하는데 성공하였다.
생체막 단백질은 물질 수송 등 세포내 필수적인 역할을 하는데, 암, 당뇨, 비만 등 각종 질병과 밀접하게 관련되어 있어, 차세대 신약개발 표적 단백질의 최대 70%를 차지하는 것으로 알려져 있다.
연구팀은 ‘단소포체 형광 기법(single-vesicle fluorescence detection)’을 개발하는데 성공하여, 생체막 단백질의 기능을 단분자 혹은 수개 분자 수준에서 관찰할 수 있는 세계 최고 수준의 기술을 보유하게 되었다.
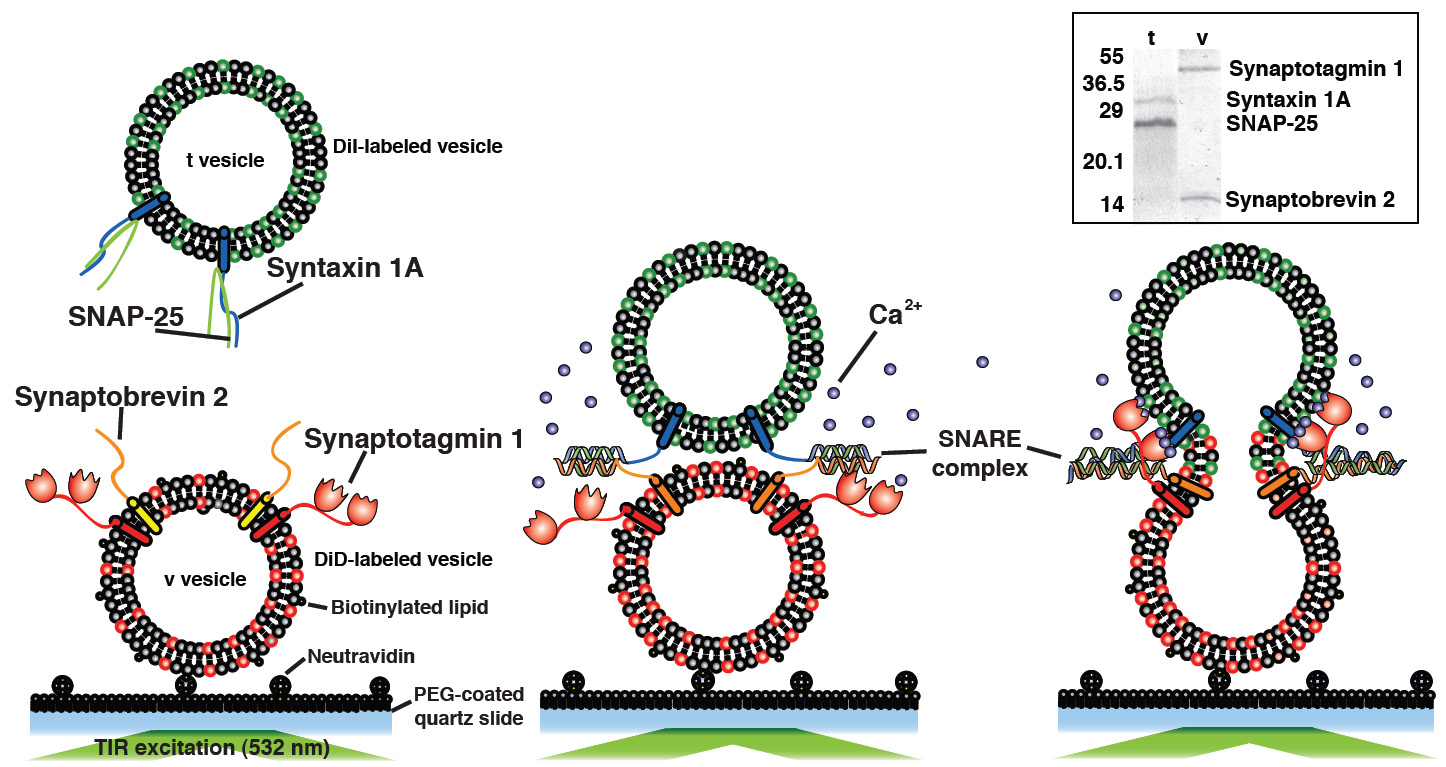
[그림2. 단소포체 형광기법]
윤 교수는 “이번 연구결과는 지난 10년간 학계가 밝혀내지 못한 시냅토태그민1의 기능을 명쾌히 밝혀내고, 복잡한 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발한 것이다. 이번 연구로 생체막 단백질을 활용하여, 암, 당뇨, 비만 등 현대인의 질병에 대한 신약을 개발할 수 있는 가능성을 열었다“라고 연구 의의를 밝혔다.
윤태영 교수팀, 생체막 단백질 기능 첫 규명
우리대학 윤태영 물리학과 교수 주도하에 생체막 단백질인 시냅토태그민1(Synaptotagmin1)이 신경세포 통신을 능동적으로 제어한다는 사실을 세계 최초로 규명하였다.
시냅토태그민1은 신경전달물질 분출을 조절하는 양대 핵심 단백질로서, 지금까지 학계는 단순히 칼슘 이온이 유입되면 시냅토태크민1이 신경전달물질을 분출하는 것으로 추정해 왔지만, 명확히 그 기능을 밝혀내지 못했다.
△카이스트 윤태영 물리학과 교수, △이한기 박사 △신연균 교수(포항공대, 아이오와주립대) △권대혁 교수(성균관대) △현창봉 교수 (고등과학원) 등이 참여한 이번 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 ‘기초연구실육성사업(BRL)"과 ‘세계 수준의 연구중심대학(WCU)육성사업’의 지원을 받아 수행되었고, 연구결과는 세계 최고 권위의 과학저널인 ‘사이언스(Science)’誌 5월 7일자에 게재된다. 이번 연구결과는 젊은 국내 토종박사들이 주축이 되어 불굴의 도전정신으로 일궈낸 값진 연구성과이다.
총 9명으로 구성된 연구팀에서 8명이 국내 연구자들로, 이중 7명이 만 40세를 넘지 않은 신진 연구자이다.
특히 연구를 주도한 윤태영 교수는 만 34세로 2004년 서울대에서, 이한기 박사는 만 33세로 명지대에서, 권대혁 교수는 만 38세로 서울대에서 박사학위를 받은 토종박사들이다.
또한 이번 연구성과는 정부의 대표적인 연구지원사업(BRL)과 인력 양성사업(WCU)의 지원을 받아 시너지 효과를 발휘하여, 세계 최고의 과학저널에 발표했다는 점에서 의의가 있다.
[그림1. 신경전달물질 분출에 있어서 시냅토태그민1의 동적제어 스위치 모델]
윤태영 교수 연구팀은 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어하는 스위치 역할을 한다는 새로운 사실을 밝혀냈다.
연구팀은 신경세포 내에 적정농도(10μmol/L, 1리터당 10마이크로 몰)의 칼슘 이온이 유입되면 시냅토태그민1은 신경전달물질을 빠르게 분출하지만, 적정농도 이상의 칼슘이 유입되면 오히려 그 기능이 감소된다는 사실을 최초로 확인하였다. 이것은 시냅토태그민1이 신경세포에서 나오는 칼슘 농도에 따라 다양하게 반응한다는 사실을 의미하는 것으로, 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어할 수 있다는 사실을 새롭게 규명한 것이다.
윤태영 교수팀의 이번 연구는 지난 10년간 학계의 풀리지 않은 수수께끼인 시냅토태그민1의 기능에 대한 명쾌한 해답을 제시하였다. 이번 연구는 낮은 농도의 칼슘에서 시냅토태그민1이 가장 활발히 활동한다는 사실을 최초로 발견하여, 기존 연구가 밝히지 못한 시냅토태그민1의 기능을 정확히 설명하였다.
특히 연구팀은 시냅토태그민1을 생체막으로부터 분리하면, 제어 스위치 기능이 상실된다는 사실도 확인하여, 시냅토태그민1의 생체막 부착 여부가 그 기능에 핵심인 것을 밝혀냈다.
또한 윤 교수팀은 차세대 신약개발의 주요 타깃인 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발하는데 성공하였다.
생체막 단백질은 물질 수송 등 세포내 필수적인 역할을 하는데, 암, 당뇨, 비만 등 각종 질병과 밀접하게 관련되어 있어, 차세대 신약개발 표적 단백질의 최대 70%를 차지하는 것으로 알려져 있다.
연구팀은 ‘단소포체 형광 기법(single-vesicle fluorescence detection)’을 개발하는데 성공하여, 생체막 단백질의 기능을 단분자 혹은 수개 분자 수준에서 관찰할 수 있는 세계 최고 수준의 기술을 보유하게 되었다.
[그림2. 단소포체 형광기법]
윤 교수는 “이번 연구결과는 지난 10년간 학계가 밝혀내지 못한 시냅토태그민1의 기능을 명쾌히 밝혀내고, 복잡한 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발한 것이다. 이번 연구로 생체막 단백질을 활용하여, 암, 당뇨, 비만 등 현대인의 질병에 대한 신약을 개발할 수 있는 가능성을 열었다“라고 연구 의의를 밝혔다.
2010.05.07
조회수 30239
-
 신소재공학과 김상욱 교수팀, 생체분자 이용한 액정성 펩타이드 나노선 개발
- 어드밴스드 머티리얼즈誌 19일(월)자 발표, 표지 논문으로 선정- 순수 국내연구진에 의해 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 연구 성과
우리 학교 신소재공학과 김상욱(金尙郁, 35) 교수팀이 생체분자(biomolecule)를 이용한 액정성 펩타이드 나노선(nanowire) 개발에 성공했다.
이 연구결과는 재료분야의 세계적 학술지인 어드밴스드 머티리얼즈(Advanced Materials)誌에 19일(월)자로 발표되고 그 중요성을 인정받아 표지 논문으로 선정됐다.
金 교수팀은 생체소재 나노제작기술(bionanofabrication)을 이용, 두 개의 아미노산이 연결된 생체 분자인 디펩타이드(dipeptide)로부터 액정성 나노선을 제조하고 그 분자 구조 및 액정상을 규명했다. (그림참조)
환경오염 등의 문제를 극복하기 위해 전 세계적으로 생체물질을 이용한 새로운 나노소재 연구가 큰 관심을 끌고 있다. 이번 액정성 나노선 개발은 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 중요한 연구 성과다. 또한, 이 분야의 연구 기반이 거의 없는 국내에서 순수 국내연구진에 의해 새로운 분야를 개척한 것으로도 큰 의미가 있다.
金 교수팀은 그동안 ‘고분자 자기조립현상을 이용한 수십 나노미터 크기의 패턴 제조 연구’ 논문을 사이언스誌, 네이처誌 등 주요 학술지에 발표해 왔다. 이번 연구 결과로 합성 고분자 소재 뿐 아니라 생체 소재의 자기조립 관련 분야 연구에도 우수한 역량을 보여주었다.
이 연구는 金 교수의 지도하에 박사과정 한태희씨가 진행하고, 화학과 김장배(지도교수 이효철 교수, 박사과정)씨가 엑스선회절을 이용한 분자 구조 규명에 참여했다.
<용어설명>
- 액정상 : 액정은 결정과 액체의 중간 상태로 입자가 갖는 방향성에 따라 네마틱, 스메틱, 콜레스테릭 등으로 구분하기도 한다. 네마틱은 일정 방향으로 향하는 성질을 갖는 것으로 액정 표시 장치 (LCD)에 많이 쓰이고 있으며 보통 막대형 (rod/wire) 또는 판형 (disk) 분자로 이루어져 있다. 본 연구에서 개발된 펩타이드 나노선은 네마틱을 나타내고 있다.
- 팹타이드(Peptide) : 펩타이드는 몇 개의 아미노산이 펩타이드 결합을 통해 연결된 형태를 말한다. 많은 아미노산이 연결되면 단백질이 된다. 두 개의 아미노산이 연결된 형태를 디펩타이드라고 하며, 본 연구에서는 두 개의 페닐알라닌이 연결된 디펩타이드가 사용되었다.
- 나노선(nanowire) : 나노미터 단위의 크기를 가지는 일차원적 구조체로 금속성과 반도체, 절연성의 많은 종류의 나노선이 존재한다. 전 세계적으로 초미세/고효율 소자의 부품으로 활용하기 위한 연구가 활발하게 진행되고 있다.
신소재공학과 김상욱 교수팀, 생체분자 이용한 액정성 펩타이드 나노선 개발
- 어드밴스드 머티리얼즈誌 19일(월)자 발표, 표지 논문으로 선정- 순수 국내연구진에 의해 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 연구 성과
우리 학교 신소재공학과 김상욱(金尙郁, 35) 교수팀이 생체분자(biomolecule)를 이용한 액정성 펩타이드 나노선(nanowire) 개발에 성공했다.
이 연구결과는 재료분야의 세계적 학술지인 어드밴스드 머티리얼즈(Advanced Materials)誌에 19일(월)자로 발표되고 그 중요성을 인정받아 표지 논문으로 선정됐다.
金 교수팀은 생체소재 나노제작기술(bionanofabrication)을 이용, 두 개의 아미노산이 연결된 생체 분자인 디펩타이드(dipeptide)로부터 액정성 나노선을 제조하고 그 분자 구조 및 액정상을 규명했다. (그림참조)
환경오염 등의 문제를 극복하기 위해 전 세계적으로 생체물질을 이용한 새로운 나노소재 연구가 큰 관심을 끌고 있다. 이번 액정성 나노선 개발은 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 중요한 연구 성과다. 또한, 이 분야의 연구 기반이 거의 없는 국내에서 순수 국내연구진에 의해 새로운 분야를 개척한 것으로도 큰 의미가 있다.
金 교수팀은 그동안 ‘고분자 자기조립현상을 이용한 수십 나노미터 크기의 패턴 제조 연구’ 논문을 사이언스誌, 네이처誌 등 주요 학술지에 발표해 왔다. 이번 연구 결과로 합성 고분자 소재 뿐 아니라 생체 소재의 자기조립 관련 분야 연구에도 우수한 역량을 보여주었다.
이 연구는 金 교수의 지도하에 박사과정 한태희씨가 진행하고, 화학과 김장배(지도교수 이효철 교수, 박사과정)씨가 엑스선회절을 이용한 분자 구조 규명에 참여했다.
<용어설명>
- 액정상 : 액정은 결정과 액체의 중간 상태로 입자가 갖는 방향성에 따라 네마틱, 스메틱, 콜레스테릭 등으로 구분하기도 한다. 네마틱은 일정 방향으로 향하는 성질을 갖는 것으로 액정 표시 장치 (LCD)에 많이 쓰이고 있으며 보통 막대형 (rod/wire) 또는 판형 (disk) 분자로 이루어져 있다. 본 연구에서 개발된 펩타이드 나노선은 네마틱을 나타내고 있다.
- 팹타이드(Peptide) : 펩타이드는 몇 개의 아미노산이 펩타이드 결합을 통해 연결된 형태를 말한다. 많은 아미노산이 연결되면 단백질이 된다. 두 개의 아미노산이 연결된 형태를 디펩타이드라고 하며, 본 연구에서는 두 개의 페닐알라닌이 연결된 디펩타이드가 사용되었다.
- 나노선(nanowire) : 나노미터 단위의 크기를 가지는 일차원적 구조체로 금속성과 반도체, 절연성의 많은 종류의 나노선이 존재한다. 전 세계적으로 초미세/고효율 소자의 부품으로 활용하기 위한 연구가 활발하게 진행되고 있다.
2007.11.20
조회수 21574
-
 생명과학과 김재섭 교수팀, '생체시계 뇌신경망 교신 유전자'세계최초로 밝혀
2만5천여 종의 형질전환 초파리 이용, 새로운 생체시계 유전자 발견
수면장애, 생체리듬 장애로 인한 각종 생리질환 치료법 개발 활로 열어
우리 몸은 하루 24시간의 시각 주기를 기억해서 현재 시각이 아침인지 저녁인지 혹은 낮인지 밤인지를 스스로 아는 능력이 있다. 한국에 살던 사람이 미국에 가면 한국에서 기억된 시각주기 때문에 처음 며칠 동안은 밤에는 깨어 있다가 낮이 되면 졸리고 하는 것이 그 일예이다. 우리 몸이 이렇게 하루 24시간 주기의 시간 흐름을 아는 것은 대뇌 아래 시상하부에 존재하는 일부 신경세포가 시계의 기능을 하기 때문인데, 이 시계를 “생체시계”라고 부른다. 정상적으로 생활하던 사람을 하루 종일 어두운 곳에 두어도 아침 시간이 되면 잠에서 깨고, 끼니마다 배가 고파지며, 또 밤 시간이 되면 잠을 자는 이유도 이 생체시계 때문이다.
생체시계의 역할은 시상하부에 위치한 수십 개의 신경세포가 담당한다. 이 생체시계 신경세포 각각의 내부에서 작동하는 유전자들은 그 동안 잘 알려져 있었다. 그러나 정작 각각의 생체시계 신경세포가 어떻게 서로 교신하여 하나의 완벽하고 정교한 생체시계 신경망을 이루어 우리 몸의 시간을 지배하는 지는 베일에 쌓여 있었다. KAIST 생명과학과 김재섭(金在燮, 42) 교수팀이 바이오벤처 제넥셀과의 공동연구로 이번에 그 베일을 세계 최초로 벗겼다.
金 교수팀은 제넥셀이 구축한 2만5천여 종의 형질전환 초파리를 이용, 새로운 생체시계 유전자를 발견하였으며, 그 이름을 “한(Han)"이라고 명명하였다. 金 교수팀에 따르면 “한” 유전자로부터 만들어지는 단백질은 "피디에프(PDF)"라는 리간드 단백질의 수용체로 작용하며, 생체시계 신경 세포들의 표면에 존재한다. 생체시계 신경세포 중에서 마스터(master) 생체시계 신경세포가 하루 24시간의 주기에 따라 각기 다른 양의 “피디에프”를 분비한다. 그러면 뇌의 다른 부위에 존재하는 생체시계 신경세포들은 표면에 있는 “한” 수용체 단백질을 통해 이 신호를 받아서 자기의 생체시계 작동을 마스터 신경세포의 생체시계 시각과 동조화 시킨다. 이렇게 해서 생체시계 신경망을 담당하는 모든 신경세포들 안에 있는 생체시계는 동일한 시각으로 맞춰지게 된다. 즉, “피디에프”와 “한” 단백질을 이용한 생체시계 신경세포들 사이의 교신이 정확하게 이뤄져 생체시계의 시각 결정을 담당하는 모든 신경세포가 특정 시간을 모두 동일한 시간으로 인식하여 일사 분란하게 몸을 조절하는 것이다. 金 교수팀의 이번 연구결과는 뉴론(Neuron)誌 10월호(10.20 발행)에 게재된다. 뉴론誌는 셀지의 자매지로서 네이처 뉴로사이언스와 쌍벽을 이루는 신경과학 분야의 최고 권위지다.
김재섭 교수는 "학문적으로는 생체시계를 담당하는 뇌신경들이 어떻게 서로 교신 하는 지를 알 수 있게 되었으며, 의학적으로는 수면 장애와 생체리듬 장애로 인한 각종 생리 질환 치료법 개발에 새로운 길을 열게 되었다"고 이번 연구 성과의 의의를 밝혔다.
생명과학과 김재섭 교수팀, '생체시계 뇌신경망 교신 유전자'세계최초로 밝혀
2만5천여 종의 형질전환 초파리 이용, 새로운 생체시계 유전자 발견
수면장애, 생체리듬 장애로 인한 각종 생리질환 치료법 개발 활로 열어
우리 몸은 하루 24시간의 시각 주기를 기억해서 현재 시각이 아침인지 저녁인지 혹은 낮인지 밤인지를 스스로 아는 능력이 있다. 한국에 살던 사람이 미국에 가면 한국에서 기억된 시각주기 때문에 처음 며칠 동안은 밤에는 깨어 있다가 낮이 되면 졸리고 하는 것이 그 일예이다. 우리 몸이 이렇게 하루 24시간 주기의 시간 흐름을 아는 것은 대뇌 아래 시상하부에 존재하는 일부 신경세포가 시계의 기능을 하기 때문인데, 이 시계를 “생체시계”라고 부른다. 정상적으로 생활하던 사람을 하루 종일 어두운 곳에 두어도 아침 시간이 되면 잠에서 깨고, 끼니마다 배가 고파지며, 또 밤 시간이 되면 잠을 자는 이유도 이 생체시계 때문이다.
생체시계의 역할은 시상하부에 위치한 수십 개의 신경세포가 담당한다. 이 생체시계 신경세포 각각의 내부에서 작동하는 유전자들은 그 동안 잘 알려져 있었다. 그러나 정작 각각의 생체시계 신경세포가 어떻게 서로 교신하여 하나의 완벽하고 정교한 생체시계 신경망을 이루어 우리 몸의 시간을 지배하는 지는 베일에 쌓여 있었다. KAIST 생명과학과 김재섭(金在燮, 42) 교수팀이 바이오벤처 제넥셀과의 공동연구로 이번에 그 베일을 세계 최초로 벗겼다.
金 교수팀은 제넥셀이 구축한 2만5천여 종의 형질전환 초파리를 이용, 새로운 생체시계 유전자를 발견하였으며, 그 이름을 “한(Han)"이라고 명명하였다. 金 교수팀에 따르면 “한” 유전자로부터 만들어지는 단백질은 "피디에프(PDF)"라는 리간드 단백질의 수용체로 작용하며, 생체시계 신경 세포들의 표면에 존재한다. 생체시계 신경세포 중에서 마스터(master) 생체시계 신경세포가 하루 24시간의 주기에 따라 각기 다른 양의 “피디에프”를 분비한다. 그러면 뇌의 다른 부위에 존재하는 생체시계 신경세포들은 표면에 있는 “한” 수용체 단백질을 통해 이 신호를 받아서 자기의 생체시계 작동을 마스터 신경세포의 생체시계 시각과 동조화 시킨다. 이렇게 해서 생체시계 신경망을 담당하는 모든 신경세포들 안에 있는 생체시계는 동일한 시각으로 맞춰지게 된다. 즉, “피디에프”와 “한” 단백질을 이용한 생체시계 신경세포들 사이의 교신이 정확하게 이뤄져 생체시계의 시각 결정을 담당하는 모든 신경세포가 특정 시간을 모두 동일한 시간으로 인식하여 일사 분란하게 몸을 조절하는 것이다. 金 교수팀의 이번 연구결과는 뉴론(Neuron)誌 10월호(10.20 발행)에 게재된다. 뉴론誌는 셀지의 자매지로서 네이처 뉴로사이언스와 쌍벽을 이루는 신경과학 분야의 최고 권위지다.
김재섭 교수는 "학문적으로는 생체시계를 담당하는 뇌신경들이 어떻게 서로 교신 하는 지를 알 수 있게 되었으며, 의학적으로는 수면 장애와 생체리듬 장애로 인한 각종 생리 질환 치료법 개발에 새로운 길을 열게 되었다"고 이번 연구 성과의 의의를 밝혔다.
2005.10.20
조회수 21273
-
 초고감도 나노바이오센서 원천기술 개발
KAIST 바이오시스템학과 박제균(朴濟均, 42) 교수팀이 나노자성입자를 이용 단백질, DNA 등의 생체분자(生體分子)를 초고감도로 검출할 수 있는 바이오센서 기술 개발에 성공했다.
이 기술은 나노(10억분의 일)그램 이하 수준으로 존재하는 극미량 물질을 검출할 수 있는 새로운 센서기술로 특정 자기장(磁氣場)하에서 생체분자의 정량적 및 고감도 분석이 가능하다.
황사 알레르기 등 많은 질환의 표지가 되는 생체분자들은 일반적으로 극미량 만으로도 인체에 심각한 영향을 미치기 때문에 이를 검출할 수 있는 센서기술은 차세대 나노바이오기술의 핵심분야에 속한다.
기존의 바이오센서 기술은 극미량 검출에는 본질적인 한계가 있는데 이번에 개발된 나노입자를 이용한 극미량 검출기술은 그러한 한계를 뛰어넘은 새로운 원천기술로서 향후 바이오센서, 랩온어칩(Lab on a chip, 손톱만한 크기의 칩으로 실험실에서 할 수 있는 연구를 수행할 수 있도록 만든 장치)개발 등에 크게 기여할 것으로 보인다.
이 연구결과는 최근 나노바이오분야의 세계적인 학술지인“랩온어칩”誌 인터넷 판에 발표되었고, 관련기술은 현재 특허 출원중에 있다.
초고감도 나노바이오센서 원천기술 개발
KAIST 바이오시스템학과 박제균(朴濟均, 42) 교수팀이 나노자성입자를 이용 단백질, DNA 등의 생체분자(生體分子)를 초고감도로 검출할 수 있는 바이오센서 기술 개발에 성공했다.
이 기술은 나노(10억분의 일)그램 이하 수준으로 존재하는 극미량 물질을 검출할 수 있는 새로운 센서기술로 특정 자기장(磁氣場)하에서 생체분자의 정량적 및 고감도 분석이 가능하다.
황사 알레르기 등 많은 질환의 표지가 되는 생체분자들은 일반적으로 극미량 만으로도 인체에 심각한 영향을 미치기 때문에 이를 검출할 수 있는 센서기술은 차세대 나노바이오기술의 핵심분야에 속한다.
기존의 바이오센서 기술은 극미량 검출에는 본질적인 한계가 있는데 이번에 개발된 나노입자를 이용한 극미량 검출기술은 그러한 한계를 뛰어넘은 새로운 원천기술로서 향후 바이오센서, 랩온어칩(Lab on a chip, 손톱만한 크기의 칩으로 실험실에서 할 수 있는 연구를 수행할 수 있도록 만든 장치)개발 등에 크게 기여할 것으로 보인다.
이 연구결과는 최근 나노바이오분야의 세계적인 학술지인“랩온어칩”誌 인터넷 판에 발표되었고, 관련기술은 현재 특허 출원중에 있다.
2005.05.20
조회수 23879
 윤태영 교수팀, 생체막 단백질 기능 첫 규명
우리대학 윤태영 물리학과 교수 주도하에 생체막 단백질인 시냅토태그민1(Synaptotagmin1)이 신경세포 통신을 능동적으로 제어한다는 사실을 세계 최초로 규명하였다.
시냅토태그민1은 신경전달물질 분출을 조절하는 양대 핵심 단백질로서, 지금까지 학계는 단순히 칼슘 이온이 유입되면 시냅토태크민1이 신경전달물질을 분출하는 것으로 추정해 왔지만, 명확히 그 기능을 밝혀내지 못했다.
△카이스트 윤태영 물리학과 교수, △이한기 박사 △신연균 교수(포항공대, 아이오와주립대) △권대혁 교수(성균관대) △현창봉 교수 (고등과학원) 등이 참여한 이번 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 ‘기초연구실육성사업(BRL)"과 ‘세계 수준의 연구중심대학(WCU)육성사업’의 지원을 받아 수행되었고, 연구결과는 세계 최고 권위의 과학저널인 ‘사이언스(Science)’誌 5월 7일자에 게재된다. 이번 연구결과는 젊은 국내 토종박사들이 주축이 되어 불굴의 도전정신으로 일궈낸 값진 연구성과이다.
총 9명으로 구성된 연구팀에서 8명이 국내 연구자들로, 이중 7명이 만 40세를 넘지 않은 신진 연구자이다.
특히 연구를 주도한 윤태영 교수는 만 34세로 2004년 서울대에서, 이한기 박사는 만 33세로 명지대에서, 권대혁 교수는 만 38세로 서울대에서 박사학위를 받은 토종박사들이다.
또한 이번 연구성과는 정부의 대표적인 연구지원사업(BRL)과 인력 양성사업(WCU)의 지원을 받아 시너지 효과를 발휘하여, 세계 최고의 과학저널에 발표했다는 점에서 의의가 있다.
[그림1. 신경전달물질 분출에 있어서 시냅토태그민1의 동적제어 스위치 모델]
윤태영 교수 연구팀은 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어하는 스위치 역할을 한다는 새로운 사실을 밝혀냈다.
연구팀은 신경세포 내에 적정농도(10μmol/L, 1리터당 10마이크로 몰)의 칼슘 이온이 유입되면 시냅토태그민1은 신경전달물질을 빠르게 분출하지만, 적정농도 이상의 칼슘이 유입되면 오히려 그 기능이 감소된다는 사실을 최초로 확인하였다. 이것은 시냅토태그민1이 신경세포에서 나오는 칼슘 농도에 따라 다양하게 반응한다는 사실을 의미하는 것으로, 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어할 수 있다는 사실을 새롭게 규명한 것이다.
윤태영 교수팀의 이번 연구는 지난 10년간 학계의 풀리지 않은 수수께끼인 시냅토태그민1의 기능에 대한 명쾌한 해답을 제시하였다. 이번 연구는 낮은 농도의 칼슘에서 시냅토태그민1이 가장 활발히 활동한다는 사실을 최초로 발견하여, 기존 연구가 밝히지 못한 시냅토태그민1의 기능을 정확히 설명하였다.
특히 연구팀은 시냅토태그민1을 생체막으로부터 분리하면, 제어 스위치 기능이 상실된다는 사실도 확인하여, 시냅토태그민1의 생체막 부착 여부가 그 기능에 핵심인 것을 밝혀냈다.
또한 윤 교수팀은 차세대 신약개발의 주요 타깃인 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발하는데 성공하였다.
생체막 단백질은 물질 수송 등 세포내 필수적인 역할을 하는데, 암, 당뇨, 비만 등 각종 질병과 밀접하게 관련되어 있어, 차세대 신약개발 표적 단백질의 최대 70%를 차지하는 것으로 알려져 있다.
연구팀은 ‘단소포체 형광 기법(single-vesicle fluorescence detection)’을 개발하는데 성공하여, 생체막 단백질의 기능을 단분자 혹은 수개 분자 수준에서 관찰할 수 있는 세계 최고 수준의 기술을 보유하게 되었다.
[그림2. 단소포체 형광기법]
윤 교수는 “이번 연구결과는 지난 10년간 학계가 밝혀내지 못한 시냅토태그민1의 기능을 명쾌히 밝혀내고, 복잡한 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발한 것이다. 이번 연구로 생체막 단백질을 활용하여, 암, 당뇨, 비만 등 현대인의 질병에 대한 신약을 개발할 수 있는 가능성을 열었다“라고 연구 의의를 밝혔다.
2010.05.07 조회수 30239
윤태영 교수팀, 생체막 단백질 기능 첫 규명
우리대학 윤태영 물리학과 교수 주도하에 생체막 단백질인 시냅토태그민1(Synaptotagmin1)이 신경세포 통신을 능동적으로 제어한다는 사실을 세계 최초로 규명하였다.
시냅토태그민1은 신경전달물질 분출을 조절하는 양대 핵심 단백질로서, 지금까지 학계는 단순히 칼슘 이온이 유입되면 시냅토태크민1이 신경전달물질을 분출하는 것으로 추정해 왔지만, 명확히 그 기능을 밝혀내지 못했다.
△카이스트 윤태영 물리학과 교수, △이한기 박사 △신연균 교수(포항공대, 아이오와주립대) △권대혁 교수(성균관대) △현창봉 교수 (고등과학원) 등이 참여한 이번 연구는 교육과학기술부(장관 안병만)와 한국연구재단(이사장 박찬모)이 추진하는 ‘기초연구실육성사업(BRL)"과 ‘세계 수준의 연구중심대학(WCU)육성사업’의 지원을 받아 수행되었고, 연구결과는 세계 최고 권위의 과학저널인 ‘사이언스(Science)’誌 5월 7일자에 게재된다. 이번 연구결과는 젊은 국내 토종박사들이 주축이 되어 불굴의 도전정신으로 일궈낸 값진 연구성과이다.
총 9명으로 구성된 연구팀에서 8명이 국내 연구자들로, 이중 7명이 만 40세를 넘지 않은 신진 연구자이다.
특히 연구를 주도한 윤태영 교수는 만 34세로 2004년 서울대에서, 이한기 박사는 만 33세로 명지대에서, 권대혁 교수는 만 38세로 서울대에서 박사학위를 받은 토종박사들이다.
또한 이번 연구성과는 정부의 대표적인 연구지원사업(BRL)과 인력 양성사업(WCU)의 지원을 받아 시너지 효과를 발휘하여, 세계 최고의 과학저널에 발표했다는 점에서 의의가 있다.
[그림1. 신경전달물질 분출에 있어서 시냅토태그민1의 동적제어 스위치 모델]
윤태영 교수 연구팀은 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어하는 스위치 역할을 한다는 새로운 사실을 밝혀냈다.
연구팀은 신경세포 내에 적정농도(10μmol/L, 1리터당 10마이크로 몰)의 칼슘 이온이 유입되면 시냅토태그민1은 신경전달물질을 빠르게 분출하지만, 적정농도 이상의 칼슘이 유입되면 오히려 그 기능이 감소된다는 사실을 최초로 확인하였다. 이것은 시냅토태그민1이 신경세포에서 나오는 칼슘 농도에 따라 다양하게 반응한다는 사실을 의미하는 것으로, 시냅토태그민1이 신경세포 통신의 강약을 자유자재로 제어할 수 있다는 사실을 새롭게 규명한 것이다.
윤태영 교수팀의 이번 연구는 지난 10년간 학계의 풀리지 않은 수수께끼인 시냅토태그민1의 기능에 대한 명쾌한 해답을 제시하였다. 이번 연구는 낮은 농도의 칼슘에서 시냅토태그민1이 가장 활발히 활동한다는 사실을 최초로 발견하여, 기존 연구가 밝히지 못한 시냅토태그민1의 기능을 정확히 설명하였다.
특히 연구팀은 시냅토태그민1을 생체막으로부터 분리하면, 제어 스위치 기능이 상실된다는 사실도 확인하여, 시냅토태그민1의 생체막 부착 여부가 그 기능에 핵심인 것을 밝혀냈다.
또한 윤 교수팀은 차세대 신약개발의 주요 타깃인 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발하는데 성공하였다.
생체막 단백질은 물질 수송 등 세포내 필수적인 역할을 하는데, 암, 당뇨, 비만 등 각종 질병과 밀접하게 관련되어 있어, 차세대 신약개발 표적 단백질의 최대 70%를 차지하는 것으로 알려져 있다.
연구팀은 ‘단소포체 형광 기법(single-vesicle fluorescence detection)’을 개발하는데 성공하여, 생체막 단백질의 기능을 단분자 혹은 수개 분자 수준에서 관찰할 수 있는 세계 최고 수준의 기술을 보유하게 되었다.
[그림2. 단소포체 형광기법]
윤 교수는 “이번 연구결과는 지난 10년간 학계가 밝혀내지 못한 시냅토태그민1의 기능을 명쾌히 밝혀내고, 복잡한 생체막 단백질의 기능을 분자수준에서 관찰할 수 있는 신기술을 개발한 것이다. 이번 연구로 생체막 단백질을 활용하여, 암, 당뇨, 비만 등 현대인의 질병에 대한 신약을 개발할 수 있는 가능성을 열었다“라고 연구 의의를 밝혔다.
2010.05.07 조회수 30239 신소재공학과 김상욱 교수팀, 생체분자 이용한 액정성 펩타이드 나노선 개발
- 어드밴스드 머티리얼즈誌 19일(월)자 발표, 표지 논문으로 선정- 순수 국내연구진에 의해 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 연구 성과
우리 학교 신소재공학과 김상욱(金尙郁, 35) 교수팀이 생체분자(biomolecule)를 이용한 액정성 펩타이드 나노선(nanowire) 개발에 성공했다.
이 연구결과는 재료분야의 세계적 학술지인 어드밴스드 머티리얼즈(Advanced Materials)誌에 19일(월)자로 발표되고 그 중요성을 인정받아 표지 논문으로 선정됐다.
金 교수팀은 생체소재 나노제작기술(bionanofabrication)을 이용, 두 개의 아미노산이 연결된 생체 분자인 디펩타이드(dipeptide)로부터 액정성 나노선을 제조하고 그 분자 구조 및 액정상을 규명했다. (그림참조)
환경오염 등의 문제를 극복하기 위해 전 세계적으로 생체물질을 이용한 새로운 나노소재 연구가 큰 관심을 끌고 있다. 이번 액정성 나노선 개발은 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 중요한 연구 성과다. 또한, 이 분야의 연구 기반이 거의 없는 국내에서 순수 국내연구진에 의해 새로운 분야를 개척한 것으로도 큰 의미가 있다.
金 교수팀은 그동안 ‘고분자 자기조립현상을 이용한 수십 나노미터 크기의 패턴 제조 연구’ 논문을 사이언스誌, 네이처誌 등 주요 학술지에 발표해 왔다. 이번 연구 결과로 합성 고분자 소재 뿐 아니라 생체 소재의 자기조립 관련 분야 연구에도 우수한 역량을 보여주었다.
이 연구는 金 교수의 지도하에 박사과정 한태희씨가 진행하고, 화학과 김장배(지도교수 이효철 교수, 박사과정)씨가 엑스선회절을 이용한 분자 구조 규명에 참여했다.
<용어설명>
- 액정상 : 액정은 결정과 액체의 중간 상태로 입자가 갖는 방향성에 따라 네마틱, 스메틱, 콜레스테릭 등으로 구분하기도 한다. 네마틱은 일정 방향으로 향하는 성질을 갖는 것으로 액정 표시 장치 (LCD)에 많이 쓰이고 있으며 보통 막대형 (rod/wire) 또는 판형 (disk) 분자로 이루어져 있다. 본 연구에서 개발된 펩타이드 나노선은 네마틱을 나타내고 있다.
- 팹타이드(Peptide) : 펩타이드는 몇 개의 아미노산이 펩타이드 결합을 통해 연결된 형태를 말한다. 많은 아미노산이 연결되면 단백질이 된다. 두 개의 아미노산이 연결된 형태를 디펩타이드라고 하며, 본 연구에서는 두 개의 페닐알라닌이 연결된 디펩타이드가 사용되었다.
- 나노선(nanowire) : 나노미터 단위의 크기를 가지는 일차원적 구조체로 금속성과 반도체, 절연성의 많은 종류의 나노선이 존재한다. 전 세계적으로 초미세/고효율 소자의 부품으로 활용하기 위한 연구가 활발하게 진행되고 있다.
2007.11.20 조회수 21574
신소재공학과 김상욱 교수팀, 생체분자 이용한 액정성 펩타이드 나노선 개발
- 어드밴스드 머티리얼즈誌 19일(월)자 발표, 표지 논문으로 선정- 순수 국내연구진에 의해 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 연구 성과
우리 학교 신소재공학과 김상욱(金尙郁, 35) 교수팀이 생체분자(biomolecule)를 이용한 액정성 펩타이드 나노선(nanowire) 개발에 성공했다.
이 연구결과는 재료분야의 세계적 학술지인 어드밴스드 머티리얼즈(Advanced Materials)誌에 19일(월)자로 발표되고 그 중요성을 인정받아 표지 논문으로 선정됐다.
金 교수팀은 생체소재 나노제작기술(bionanofabrication)을 이용, 두 개의 아미노산이 연결된 생체 분자인 디펩타이드(dipeptide)로부터 액정성 나노선을 제조하고 그 분자 구조 및 액정상을 규명했다. (그림참조)
환경오염 등의 문제를 극복하기 위해 전 세계적으로 생체물질을 이용한 새로운 나노소재 연구가 큰 관심을 끌고 있다. 이번 액정성 나노선 개발은 새로운 개념의 생체 소재 나노소자 개발 가능성을 한 단계 높인 중요한 연구 성과다. 또한, 이 분야의 연구 기반이 거의 없는 국내에서 순수 국내연구진에 의해 새로운 분야를 개척한 것으로도 큰 의미가 있다.
金 교수팀은 그동안 ‘고분자 자기조립현상을 이용한 수십 나노미터 크기의 패턴 제조 연구’ 논문을 사이언스誌, 네이처誌 등 주요 학술지에 발표해 왔다. 이번 연구 결과로 합성 고분자 소재 뿐 아니라 생체 소재의 자기조립 관련 분야 연구에도 우수한 역량을 보여주었다.
이 연구는 金 교수의 지도하에 박사과정 한태희씨가 진행하고, 화학과 김장배(지도교수 이효철 교수, 박사과정)씨가 엑스선회절을 이용한 분자 구조 규명에 참여했다.
<용어설명>
- 액정상 : 액정은 결정과 액체의 중간 상태로 입자가 갖는 방향성에 따라 네마틱, 스메틱, 콜레스테릭 등으로 구분하기도 한다. 네마틱은 일정 방향으로 향하는 성질을 갖는 것으로 액정 표시 장치 (LCD)에 많이 쓰이고 있으며 보통 막대형 (rod/wire) 또는 판형 (disk) 분자로 이루어져 있다. 본 연구에서 개발된 펩타이드 나노선은 네마틱을 나타내고 있다.
- 팹타이드(Peptide) : 펩타이드는 몇 개의 아미노산이 펩타이드 결합을 통해 연결된 형태를 말한다. 많은 아미노산이 연결되면 단백질이 된다. 두 개의 아미노산이 연결된 형태를 디펩타이드라고 하며, 본 연구에서는 두 개의 페닐알라닌이 연결된 디펩타이드가 사용되었다.
- 나노선(nanowire) : 나노미터 단위의 크기를 가지는 일차원적 구조체로 금속성과 반도체, 절연성의 많은 종류의 나노선이 존재한다. 전 세계적으로 초미세/고효율 소자의 부품으로 활용하기 위한 연구가 활발하게 진행되고 있다.
2007.11.20 조회수 21574 생명과학과 김재섭 교수팀, '생체시계 뇌신경망 교신 유전자'세계최초로 밝혀
2만5천여 종의 형질전환 초파리 이용, 새로운 생체시계 유전자 발견
수면장애, 생체리듬 장애로 인한 각종 생리질환 치료법 개발 활로 열어
우리 몸은 하루 24시간의 시각 주기를 기억해서 현재 시각이 아침인지 저녁인지 혹은 낮인지 밤인지를 스스로 아는 능력이 있다. 한국에 살던 사람이 미국에 가면 한국에서 기억된 시각주기 때문에 처음 며칠 동안은 밤에는 깨어 있다가 낮이 되면 졸리고 하는 것이 그 일예이다. 우리 몸이 이렇게 하루 24시간 주기의 시간 흐름을 아는 것은 대뇌 아래 시상하부에 존재하는 일부 신경세포가 시계의 기능을 하기 때문인데, 이 시계를 “생체시계”라고 부른다. 정상적으로 생활하던 사람을 하루 종일 어두운 곳에 두어도 아침 시간이 되면 잠에서 깨고, 끼니마다 배가 고파지며, 또 밤 시간이 되면 잠을 자는 이유도 이 생체시계 때문이다.
생체시계의 역할은 시상하부에 위치한 수십 개의 신경세포가 담당한다. 이 생체시계 신경세포 각각의 내부에서 작동하는 유전자들은 그 동안 잘 알려져 있었다. 그러나 정작 각각의 생체시계 신경세포가 어떻게 서로 교신하여 하나의 완벽하고 정교한 생체시계 신경망을 이루어 우리 몸의 시간을 지배하는 지는 베일에 쌓여 있었다. KAIST 생명과학과 김재섭(金在燮, 42) 교수팀이 바이오벤처 제넥셀과의 공동연구로 이번에 그 베일을 세계 최초로 벗겼다.
金 교수팀은 제넥셀이 구축한 2만5천여 종의 형질전환 초파리를 이용, 새로운 생체시계 유전자를 발견하였으며, 그 이름을 “한(Han)"이라고 명명하였다. 金 교수팀에 따르면 “한” 유전자로부터 만들어지는 단백질은 "피디에프(PDF)"라는 리간드 단백질의 수용체로 작용하며, 생체시계 신경 세포들의 표면에 존재한다. 생체시계 신경세포 중에서 마스터(master) 생체시계 신경세포가 하루 24시간의 주기에 따라 각기 다른 양의 “피디에프”를 분비한다. 그러면 뇌의 다른 부위에 존재하는 생체시계 신경세포들은 표면에 있는 “한” 수용체 단백질을 통해 이 신호를 받아서 자기의 생체시계 작동을 마스터 신경세포의 생체시계 시각과 동조화 시킨다. 이렇게 해서 생체시계 신경망을 담당하는 모든 신경세포들 안에 있는 생체시계는 동일한 시각으로 맞춰지게 된다. 즉, “피디에프”와 “한” 단백질을 이용한 생체시계 신경세포들 사이의 교신이 정확하게 이뤄져 생체시계의 시각 결정을 담당하는 모든 신경세포가 특정 시간을 모두 동일한 시간으로 인식하여 일사 분란하게 몸을 조절하는 것이다. 金 교수팀의 이번 연구결과는 뉴론(Neuron)誌 10월호(10.20 발행)에 게재된다. 뉴론誌는 셀지의 자매지로서 네이처 뉴로사이언스와 쌍벽을 이루는 신경과학 분야의 최고 권위지다.
김재섭 교수는 "학문적으로는 생체시계를 담당하는 뇌신경들이 어떻게 서로 교신 하는 지를 알 수 있게 되었으며, 의학적으로는 수면 장애와 생체리듬 장애로 인한 각종 생리 질환 치료법 개발에 새로운 길을 열게 되었다"고 이번 연구 성과의 의의를 밝혔다.
2005.10.20 조회수 21273
생명과학과 김재섭 교수팀, '생체시계 뇌신경망 교신 유전자'세계최초로 밝혀
2만5천여 종의 형질전환 초파리 이용, 새로운 생체시계 유전자 발견
수면장애, 생체리듬 장애로 인한 각종 생리질환 치료법 개발 활로 열어
우리 몸은 하루 24시간의 시각 주기를 기억해서 현재 시각이 아침인지 저녁인지 혹은 낮인지 밤인지를 스스로 아는 능력이 있다. 한국에 살던 사람이 미국에 가면 한국에서 기억된 시각주기 때문에 처음 며칠 동안은 밤에는 깨어 있다가 낮이 되면 졸리고 하는 것이 그 일예이다. 우리 몸이 이렇게 하루 24시간 주기의 시간 흐름을 아는 것은 대뇌 아래 시상하부에 존재하는 일부 신경세포가 시계의 기능을 하기 때문인데, 이 시계를 “생체시계”라고 부른다. 정상적으로 생활하던 사람을 하루 종일 어두운 곳에 두어도 아침 시간이 되면 잠에서 깨고, 끼니마다 배가 고파지며, 또 밤 시간이 되면 잠을 자는 이유도 이 생체시계 때문이다.
생체시계의 역할은 시상하부에 위치한 수십 개의 신경세포가 담당한다. 이 생체시계 신경세포 각각의 내부에서 작동하는 유전자들은 그 동안 잘 알려져 있었다. 그러나 정작 각각의 생체시계 신경세포가 어떻게 서로 교신하여 하나의 완벽하고 정교한 생체시계 신경망을 이루어 우리 몸의 시간을 지배하는 지는 베일에 쌓여 있었다. KAIST 생명과학과 김재섭(金在燮, 42) 교수팀이 바이오벤처 제넥셀과의 공동연구로 이번에 그 베일을 세계 최초로 벗겼다.
金 교수팀은 제넥셀이 구축한 2만5천여 종의 형질전환 초파리를 이용, 새로운 생체시계 유전자를 발견하였으며, 그 이름을 “한(Han)"이라고 명명하였다. 金 교수팀에 따르면 “한” 유전자로부터 만들어지는 단백질은 "피디에프(PDF)"라는 리간드 단백질의 수용체로 작용하며, 생체시계 신경 세포들의 표면에 존재한다. 생체시계 신경세포 중에서 마스터(master) 생체시계 신경세포가 하루 24시간의 주기에 따라 각기 다른 양의 “피디에프”를 분비한다. 그러면 뇌의 다른 부위에 존재하는 생체시계 신경세포들은 표면에 있는 “한” 수용체 단백질을 통해 이 신호를 받아서 자기의 생체시계 작동을 마스터 신경세포의 생체시계 시각과 동조화 시킨다. 이렇게 해서 생체시계 신경망을 담당하는 모든 신경세포들 안에 있는 생체시계는 동일한 시각으로 맞춰지게 된다. 즉, “피디에프”와 “한” 단백질을 이용한 생체시계 신경세포들 사이의 교신이 정확하게 이뤄져 생체시계의 시각 결정을 담당하는 모든 신경세포가 특정 시간을 모두 동일한 시간으로 인식하여 일사 분란하게 몸을 조절하는 것이다. 金 교수팀의 이번 연구결과는 뉴론(Neuron)誌 10월호(10.20 발행)에 게재된다. 뉴론誌는 셀지의 자매지로서 네이처 뉴로사이언스와 쌍벽을 이루는 신경과학 분야의 최고 권위지다.
김재섭 교수는 "학문적으로는 생체시계를 담당하는 뇌신경들이 어떻게 서로 교신 하는 지를 알 수 있게 되었으며, 의학적으로는 수면 장애와 생체리듬 장애로 인한 각종 생리 질환 치료법 개발에 새로운 길을 열게 되었다"고 이번 연구 성과의 의의를 밝혔다.
2005.10.20 조회수 21273 초고감도 나노바이오센서 원천기술 개발
KAIST 바이오시스템학과 박제균(朴濟均, 42) 교수팀이 나노자성입자를 이용 단백질, DNA 등의 생체분자(生體分子)를 초고감도로 검출할 수 있는 바이오센서 기술 개발에 성공했다.
이 기술은 나노(10억분의 일)그램 이하 수준으로 존재하는 극미량 물질을 검출할 수 있는 새로운 센서기술로 특정 자기장(磁氣場)하에서 생체분자의 정량적 및 고감도 분석이 가능하다.
황사 알레르기 등 많은 질환의 표지가 되는 생체분자들은 일반적으로 극미량 만으로도 인체에 심각한 영향을 미치기 때문에 이를 검출할 수 있는 센서기술은 차세대 나노바이오기술의 핵심분야에 속한다.
기존의 바이오센서 기술은 극미량 검출에는 본질적인 한계가 있는데 이번에 개발된 나노입자를 이용한 극미량 검출기술은 그러한 한계를 뛰어넘은 새로운 원천기술로서 향후 바이오센서, 랩온어칩(Lab on a chip, 손톱만한 크기의 칩으로 실험실에서 할 수 있는 연구를 수행할 수 있도록 만든 장치)개발 등에 크게 기여할 것으로 보인다.
이 연구결과는 최근 나노바이오분야의 세계적인 학술지인“랩온어칩”誌 인터넷 판에 발표되었고, 관련기술은 현재 특허 출원중에 있다.
2005.05.20 조회수 23879
초고감도 나노바이오센서 원천기술 개발
KAIST 바이오시스템학과 박제균(朴濟均, 42) 교수팀이 나노자성입자를 이용 단백질, DNA 등의 생체분자(生體分子)를 초고감도로 검출할 수 있는 바이오센서 기술 개발에 성공했다.
이 기술은 나노(10억분의 일)그램 이하 수준으로 존재하는 극미량 물질을 검출할 수 있는 새로운 센서기술로 특정 자기장(磁氣場)하에서 생체분자의 정량적 및 고감도 분석이 가능하다.
황사 알레르기 등 많은 질환의 표지가 되는 생체분자들은 일반적으로 극미량 만으로도 인체에 심각한 영향을 미치기 때문에 이를 검출할 수 있는 센서기술은 차세대 나노바이오기술의 핵심분야에 속한다.
기존의 바이오센서 기술은 극미량 검출에는 본질적인 한계가 있는데 이번에 개발된 나노입자를 이용한 극미량 검출기술은 그러한 한계를 뛰어넘은 새로운 원천기술로서 향후 바이오센서, 랩온어칩(Lab on a chip, 손톱만한 크기의 칩으로 실험실에서 할 수 있는 연구를 수행할 수 있도록 만든 장치)개발 등에 크게 기여할 것으로 보인다.
이 연구결과는 최근 나노바이오분야의 세계적인 학술지인“랩온어칩”誌 인터넷 판에 발표되었고, 관련기술은 현재 특허 출원중에 있다.
2005.05.20 조회수 23879