%EB%AF%B8%EA%B5%AD%EA%B5%AD%EB%A6%BD%EA%B3%BC%ED%95%99%EC%9B%90%ED%9A%8C%EB%B3%B4
-
 친환경을 위한 숙신산 세계 최고 수준 생산 성공
지구 온난화 등의 심각한 환경 문제로 인해 화석 연료를 대체할 수 있는 친환경 기반 화학물질 생산 기술개발의 필요성이 지속적으로 증가하고 있다. 우리 연구진이 화학적인 공정이 아닌 시스템 대사공학을 활용, 플라스틱의 원료와 식품, 의약품 등의 합성에 사용되는 매우 중요한 산업 기반 화학물질인 숙신산을 세계 최고 수준으로 생산하는 데 성공해 화제다.
우리 대학 생명화학공학과 김지연 박사과정생과 이종언 박사를 포함한 이상엽 특훈교수 연구팀이 마그네슘(Mg2+) 수송 시스템을 최적화함으로써 고효율 숙신산 생산 균주를 개발했다고 11일 밝혔다.
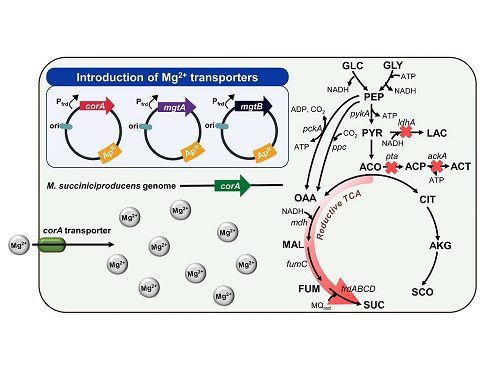
이상엽 특훈교수 연구팀은 한우의 반추위에서 분리한 미생물인 ‘맨하이미아 (Mannheimia)’의 대사회로를 조작하고 마그네슘 수송 시스템을 최적화해 세계 최고 수준의 생산성을 갖는 숙신산 생산 기술을 개발했다.
연구팀은 미생물 발효 과정 중 pH 조절을 위해 사용되는 다양한 알칼리성 중화제가 숙신산 생산에 미치는 영향을 파악하고, 최적화된 중화제를 선정했다. 특히 수산화마그네슘(Mg(OH)2)이 포함된 중화제를 사용, 마그네슘이 미치는 생리학적 영향을 분석해 세포 성장과 숙신산 생산에 중요한 역할을 한다는 사실을 확인했다.
또한, 맨하이미아 내 존재하는 마그네슘 수송체인 corA 유전자를 규명하고, 다양한 마그네슘 수송체를 도입해 마그네슘의 수송을 더욱 향상했다. 그중 살모넬라 엔테리카(Salmonella enterica) 균에서 유래한 고효율 마그네슘 수송체를 도입해 시스템을 최적화한 결과 152.23 g/L의 숙신산을 생산했으며, 최대 생산성은 39.64 g/L/h를 달성했다.
이는 기존 대비 약 2배 향상된, 현재까지 보고된 세계 최고의 숙신산 생산성 수치로, 연구팀은 이 과정에서 계속해서 세계 기록을 세우며 자체 기록을 경신하고 있다. 이는 생물학적 플랫폼을 통해 화학물질 생산을 극대화한 중요한 발전으로 의의를 지닌다.
이번 논문의 공동 제1 저자인 김지연 박사과정생은 “마그네슘 수송 시스템을 최적화해 고농도의 숙신산을 생산했다는 점에 의의가 있다”며, “이 기술이 향후 중요한 화학물질들을 생물학적으로 생산하는 미생물 균주 개발의 전략으로 작용할 것으로 기대된다”고 밝혔다. 또한, 이상엽 특훈교수는 “이번 연구는 숙신산 생산의 새로운 표준을 제시했으며 생물 기반 화학물질의 경제성을 크게 높일 수 있는 잠재력을 가지고 있으며, 지속 가능한 바이오화학 산업의 발전에도 크게 기여할 것으로 기대된다”고 말했다.
해당 연구 결과는 국제 학술지인 `미국 국립과학원 회보(PNAS)'에 9월 6일(현지시간) 자 게재됐다.
※ 논문명 : High-level succinic acid production by overexpressing a magnesium transporter in Mannheimia succiniciproducens
※ 저자 정보 : 김지연(한국과학기술원, 공동 제1 저자), 이종언(한국과학기술원, 공동 제1 저자), 안정호(한국과학기술원), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
한편, 이번 연구는 과기정통부가 지원하는 석유대체 친환경 화학기술개발사업의 ‘바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발’ 과제(과제 책임자 KAIST 이상엽 특훈교수)의 지원을 받아 수행됐다.
2024.09.11 조회수 4931
친환경을 위한 숙신산 세계 최고 수준 생산 성공
지구 온난화 등의 심각한 환경 문제로 인해 화석 연료를 대체할 수 있는 친환경 기반 화학물질 생산 기술개발의 필요성이 지속적으로 증가하고 있다. 우리 연구진이 화학적인 공정이 아닌 시스템 대사공학을 활용, 플라스틱의 원료와 식품, 의약품 등의 합성에 사용되는 매우 중요한 산업 기반 화학물질인 숙신산을 세계 최고 수준으로 생산하는 데 성공해 화제다.
우리 대학 생명화학공학과 김지연 박사과정생과 이종언 박사를 포함한 이상엽 특훈교수 연구팀이 마그네슘(Mg2+) 수송 시스템을 최적화함으로써 고효율 숙신산 생산 균주를 개발했다고 11일 밝혔다.
이상엽 특훈교수 연구팀은 한우의 반추위에서 분리한 미생물인 ‘맨하이미아 (Mannheimia)’의 대사회로를 조작하고 마그네슘 수송 시스템을 최적화해 세계 최고 수준의 생산성을 갖는 숙신산 생산 기술을 개발했다.
연구팀은 미생물 발효 과정 중 pH 조절을 위해 사용되는 다양한 알칼리성 중화제가 숙신산 생산에 미치는 영향을 파악하고, 최적화된 중화제를 선정했다. 특히 수산화마그네슘(Mg(OH)2)이 포함된 중화제를 사용, 마그네슘이 미치는 생리학적 영향을 분석해 세포 성장과 숙신산 생산에 중요한 역할을 한다는 사실을 확인했다.
또한, 맨하이미아 내 존재하는 마그네슘 수송체인 corA 유전자를 규명하고, 다양한 마그네슘 수송체를 도입해 마그네슘의 수송을 더욱 향상했다. 그중 살모넬라 엔테리카(Salmonella enterica) 균에서 유래한 고효율 마그네슘 수송체를 도입해 시스템을 최적화한 결과 152.23 g/L의 숙신산을 생산했으며, 최대 생산성은 39.64 g/L/h를 달성했다.
이는 기존 대비 약 2배 향상된, 현재까지 보고된 세계 최고의 숙신산 생산성 수치로, 연구팀은 이 과정에서 계속해서 세계 기록을 세우며 자체 기록을 경신하고 있다. 이는 생물학적 플랫폼을 통해 화학물질 생산을 극대화한 중요한 발전으로 의의를 지닌다.
이번 논문의 공동 제1 저자인 김지연 박사과정생은 “마그네슘 수송 시스템을 최적화해 고농도의 숙신산을 생산했다는 점에 의의가 있다”며, “이 기술이 향후 중요한 화학물질들을 생물학적으로 생산하는 미생물 균주 개발의 전략으로 작용할 것으로 기대된다”고 밝혔다. 또한, 이상엽 특훈교수는 “이번 연구는 숙신산 생산의 새로운 표준을 제시했으며 생물 기반 화학물질의 경제성을 크게 높일 수 있는 잠재력을 가지고 있으며, 지속 가능한 바이오화학 산업의 발전에도 크게 기여할 것으로 기대된다”고 말했다.
해당 연구 결과는 국제 학술지인 `미국 국립과학원 회보(PNAS)'에 9월 6일(현지시간) 자 게재됐다.
※ 논문명 : High-level succinic acid production by overexpressing a magnesium transporter in Mannheimia succiniciproducens
※ 저자 정보 : 김지연(한국과학기술원, 공동 제1 저자), 이종언(한국과학기술원, 공동 제1 저자), 안정호(한국과학기술원), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
한편, 이번 연구는 과기정통부가 지원하는 석유대체 친환경 화학기술개발사업의 ‘바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발’ 과제(과제 책임자 KAIST 이상엽 특훈교수)의 지원을 받아 수행됐다.
2024.09.11 조회수 4931 -
 수술 후 방광 기능은 전자센서로 모니터링하세요
방광절제술을 받은 환자들의 성공적인 재활을 위해 카테터* 삽입없이 방광 기능을 안전하게 모니터링하는 생체전자 시스템이 개발되어 화제다.
*카테터: 방광에 삽입하는 고무 또는 금속제의 가는 관
우리 대학 전기및전자공학부 권경하 교수팀이 미국 노스웨스턴대 김지혜 박사와 공동연구를 통해 방광의 크기 및 압력 변화를 정확하게 측정하는 디지털 헬스케어 기술을 개발했다고 16일 밝혔다.
부분적 방광절제술*은 긴 회복 기간이 필요하며, 이 기간에 요로 동역학 검사**(이하 UDS)를 통해 몸 밖으로 소변을 배출하는 기능을 간헐적으로 평가한다. 그러나 UDS는 환자 친화적이지 않으며 사용자마다 결과에 변동성이 있고, 연속적인 데이터 수집 능력이 제한된다. 또한 카테터 관련 요로 감염의 위험을 초래하며, 고위험 환자에게서는 상행성 신우신염으로 진행되기도 한다. 이러한 UDS의 적절한 대안으로, 요로에 카테터를 삽입하지 않고 방광의 상태를 연속적이고 실시간으로 모니터링할 수 있는 기술이 필요하다.
*부분적 방광절제술: 방광에 종양이 있는 부위를 잘라내고 나머지 방광을 이어 붙여주는 수술
**요로 동역학 검사: 방광과 요도의 전반적인 기능을 확인하여 치료 계획을 세우기 위한 진단적 검사
이에 연구팀은 방광의 충전 및 배뇨와 관련된 기계적 변형 변화를 무선 원격 측정할 수 있는 이식형 방광 플랫폼을 개발했다. 이 시스템은 생분해성 스트레인 센서를 이용해 방광의 크기와 압력 변화를 실시간으로 측정하고, 회복 기간이 끝나면 해당 센서가 신체 내에서 자연스럽게 용해돼 사라지는 것이 특징이다. 모니터링 장비 제거를 위한 추가 수술이 필요 없고 합병증 위험을 줄이는 것은 물론 환자의 편안함과 회복 시간을 개선한다.
연구팀은 이 플랫폼을 이식 후 최대 30일까지 실시간 변화를 재현적으로 측정할 수 있음을 쥐 모델에서 입증했다. 또한 개코원숭이 실험을 통해, 해당 기술이 전통적인 UDS와 비교해 최대 8주까지 압력 측정의 일치성을 보였다. 이러한 결과는 해당 시스템이 장기간 수술 후 방광 회복 모니터링을 위한 UDS의 적절한 대안으로 사용될 수 있음을 시사한다.
권경하 교수는 "비인간 영장류(개코원숭이)를 활용한 광범위한 실험을 통해 방광 기능에 대한 정확하고 신뢰할 수 있는 데이터를 제공하는 장치의 효능을 입증했다ˮ면서 "환자들의 회복 시간을 단축하고 전반적인 수술 결과를 개선하는데 활용할 수 있을 것ˮ이라고 말했다.
이번 연구 결과는 국제 학술지 `미국 국립 과학원 회보 (Proceedings of the National Academy of Sciences; PNAS)'에 지난 4월 2일 발표됐다. (논문명 : A wireless, implantable bioelectronic system for monitoring urinary bladder function following surgical recovery, 링크: https://www.pnas.org/doi/abs/10.1073/pnas.2400868121?af=R)
한편, 이번 연구는 과학기술정보통신부 한국연구재단의 기초연구사업, 지역혁신선도연구센터사업 및 BK21의 지원을 받아 수행됐다.
2024.04.16 조회수 6683
수술 후 방광 기능은 전자센서로 모니터링하세요
방광절제술을 받은 환자들의 성공적인 재활을 위해 카테터* 삽입없이 방광 기능을 안전하게 모니터링하는 생체전자 시스템이 개발되어 화제다.
*카테터: 방광에 삽입하는 고무 또는 금속제의 가는 관
우리 대학 전기및전자공학부 권경하 교수팀이 미국 노스웨스턴대 김지혜 박사와 공동연구를 통해 방광의 크기 및 압력 변화를 정확하게 측정하는 디지털 헬스케어 기술을 개발했다고 16일 밝혔다.
부분적 방광절제술*은 긴 회복 기간이 필요하며, 이 기간에 요로 동역학 검사**(이하 UDS)를 통해 몸 밖으로 소변을 배출하는 기능을 간헐적으로 평가한다. 그러나 UDS는 환자 친화적이지 않으며 사용자마다 결과에 변동성이 있고, 연속적인 데이터 수집 능력이 제한된다. 또한 카테터 관련 요로 감염의 위험을 초래하며, 고위험 환자에게서는 상행성 신우신염으로 진행되기도 한다. 이러한 UDS의 적절한 대안으로, 요로에 카테터를 삽입하지 않고 방광의 상태를 연속적이고 실시간으로 모니터링할 수 있는 기술이 필요하다.
*부분적 방광절제술: 방광에 종양이 있는 부위를 잘라내고 나머지 방광을 이어 붙여주는 수술
**요로 동역학 검사: 방광과 요도의 전반적인 기능을 확인하여 치료 계획을 세우기 위한 진단적 검사
이에 연구팀은 방광의 충전 및 배뇨와 관련된 기계적 변형 변화를 무선 원격 측정할 수 있는 이식형 방광 플랫폼을 개발했다. 이 시스템은 생분해성 스트레인 센서를 이용해 방광의 크기와 압력 변화를 실시간으로 측정하고, 회복 기간이 끝나면 해당 센서가 신체 내에서 자연스럽게 용해돼 사라지는 것이 특징이다. 모니터링 장비 제거를 위한 추가 수술이 필요 없고 합병증 위험을 줄이는 것은 물론 환자의 편안함과 회복 시간을 개선한다.
연구팀은 이 플랫폼을 이식 후 최대 30일까지 실시간 변화를 재현적으로 측정할 수 있음을 쥐 모델에서 입증했다. 또한 개코원숭이 실험을 통해, 해당 기술이 전통적인 UDS와 비교해 최대 8주까지 압력 측정의 일치성을 보였다. 이러한 결과는 해당 시스템이 장기간 수술 후 방광 회복 모니터링을 위한 UDS의 적절한 대안으로 사용될 수 있음을 시사한다.
권경하 교수는 "비인간 영장류(개코원숭이)를 활용한 광범위한 실험을 통해 방광 기능에 대한 정확하고 신뢰할 수 있는 데이터를 제공하는 장치의 효능을 입증했다ˮ면서 "환자들의 회복 시간을 단축하고 전반적인 수술 결과를 개선하는데 활용할 수 있을 것ˮ이라고 말했다.
이번 연구 결과는 국제 학술지 `미국 국립 과학원 회보 (Proceedings of the National Academy of Sciences; PNAS)'에 지난 4월 2일 발표됐다. (논문명 : A wireless, implantable bioelectronic system for monitoring urinary bladder function following surgical recovery, 링크: https://www.pnas.org/doi/abs/10.1073/pnas.2400868121?af=R)
한편, 이번 연구는 과학기술정보통신부 한국연구재단의 기초연구사업, 지역혁신선도연구센터사업 및 BK21의 지원을 받아 수행됐다.
2024.04.16 조회수 6683 -
 이산화탄소에서 바이오 플라스틱 20배 이상 뽑아내다
전 세계적으로 기후변화 문제가 심각해짐에 따라 이를 기후 위기로 인식하고 이에 대응하는 적극적인 관심과 노력이 요구되고 있다. 그중 이산화탄소를 활용해 재자원화하는 여러 방법 중에서 전기화학적 이산화탄소 전환 기술은 전기에너지를 이용해 이산화탄소를 유용한 화학물질로 전환할 수 있는 기술이다. 이는 설비 운용이 용이하고, 태양 전지나 풍력에 의해 생산된 재생 가능한 전기에너지를 이용할 수 있으므로 온실가스 감축 및 탄소 중립 달성에 기여하는 친환경 기술로 많은 관심을 받고 있다.
우리 대학 생명화학공학과 이현주 교수와 이상엽 특훈교수 공동연구팀이 전기화학적 이산화탄소 전환과 미생물 기반의 바이오 전환을 연계한 하이브리드 시스템을 개발해 이산화탄소로부터 높은 효율로 바이오 플라스틱을 생산하는 기술 개발에 성공했다고 30일 밝혔다. 유사한 시스템 대비 20배 이상의 세계 최고 생산성을 보여준 해당 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 3월 27일 字 온라인 게재됐다.
※ 논문명 : Biohybrid CO2 electrolysis for the direct synthesis of polyesters from CO2
※ 저자 정보 : 이현주 (한국과학기술원, 교신저자), 이상엽(한국과학기술원, 교신저자), 임진규(한국과학기술원, 현 소속 기관 Stanford Linear Accelerator Center, 공동 제1저자), 최소영(한국과학기술원, 공동 제1저자), 이재원(한국과학기술원, 공동 제1저자) - 총 5명
이산화탄소의 효율적인 전환을 위해 고효율 전극 촉매 및 시스템 개발이 활발히 진행되고 있는데, 전환생성물로는 주로 탄소 1~3개의 화합물만이 제한적으로 생산되고 있다. 일산화탄소, 포름산, 에틸렌과 같은 탄소 1개의 화합물이 비교적 높은 효율로 생산되며, 이 밖에 에탄올, 아세트산, 프로판올과 같은 여러 개 탄소의 액상 화합물도 만들어질 수 있으나 이는 더 많은 전자를 필요로 하는 화학반응 특성상 전환 효율 및 생성물 선택성이 크게 낮다는 한계점이 있다.
이에 우리 대학 생명화학공학과 이현주 교수와 이상엽 특훈교수 공동연구팀은 전기화학적 이산화탄소 전환 기술과 미생물을 이용한 바이오 전환 기술을 연계해 이산화탄소로부터 바이오 플라스틱을 생산하는 기술을 개발했다. 이 전기화학-바이오 하이브리드 시스템은 전기화학 전환반응이 일어나는 전해조와 미생물 배양이 이루어지는 발효조가 연결된 형태로, 전해조에서 이산화탄소가 포름산으로 전환되면, 이 포름산을 발효조에 공급해 커프리아비더스 네케이터(Cupriavidus necator)라는 미생물이 탄소원으로 섭취해 미생물 유래 바이오 플라스틱인 폴리하이드록시알카노에이트(polyhydroxyalkanoate, PHA)를 생산한다.
기존 이러한 하이브리드 콘셉트의 연구 결과에 따르면, 전기화학 반응의 낮은 효율 및 미생물 배양 조건과의 차이 등의 문제로 생산성이 매우 낮거나 비연속적 공정에 그친다는 단점이 있었다.
이를 극복하기 위해 공동연구팀은 기체 상태의 이산화탄소를 이용한 기체 확산 전극(gas diffusion electrode)으로 포름산을 만들었다. 그리고 미생물의 생장을 저해하지 않으면서도 전기화학 반응이 충분히 잘 일어나도록 하는 전해액이자 동시에 미생물 배양 배지로 이용할 수 있는 ‘생리적 호환 가능한 양극 전해액(physiologically compatible catholyte)’을 개발하여 별도의 분리 및 정제과정 없이 바로 미생물에게 공급하도록 했다. 이를 통해 이산화탄소로부터 만들어진 포름산을 포함하고 있는 전해액이 발효조로 들어가 미생물 배양에 쓰이고, 전해조로 들어가 순환되도록 하여 전해액과 남은 포름산의 활용을 극대화했다. 또한, 이 과정에서 필터를 설치해 전극 반응에 영향을 줄 수 있는 미생물이 걸러진 전해액만이 전해조로 공급되고 미생물은 발효조 안에만 존재하도록 하는 두 시스템이 잘 연계되면서도 효율적으로 작동되도록 설계했다.
개발한 하이브리드 시스템을 통해 이산화탄소로부터 세포 건조 중량의 83%에 달하는 높은 함량의 바이오 플라스틱(PHB)를 생산했으며, 이는 4 cm2 전극에서 1.38g의 PHB를 생산한 결과로 세계 최초 그램(g) 수준의 생산이며 기존 연구 대비 20배 이상의 생산성이다. 또한 해당 하이브리드 시스템은 연속 배양(continuous culture)의 가능성을 보여줌으로써 추후 다양한 산업공정으로의 응용 또한 기대된다.
교신저자인 이현주 교수와 이상엽 특훈교수는 “이번 연구 결과는 바이오 플라스틱뿐만 아니라 다양한 화학물질 생산에 응용될 수 있는 기술로서 앞으로 탄소 중립을 위한 핵심 기술로 많은 활용이 기대된다”라고 밝혔다.
한편, 이번 연구는 과기정통부가 지원하는 이산화탄소 저감 촉매 및 에너지 소자 기술 개발 과제, 불균일계 원자 촉매 제어 과제와 석유대체 친환경 화학기술개발사업의 바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발 과제의 지원을 받아 수행됐다.
2023.03.30 조회수 11743
이산화탄소에서 바이오 플라스틱 20배 이상 뽑아내다
전 세계적으로 기후변화 문제가 심각해짐에 따라 이를 기후 위기로 인식하고 이에 대응하는 적극적인 관심과 노력이 요구되고 있다. 그중 이산화탄소를 활용해 재자원화하는 여러 방법 중에서 전기화학적 이산화탄소 전환 기술은 전기에너지를 이용해 이산화탄소를 유용한 화학물질로 전환할 수 있는 기술이다. 이는 설비 운용이 용이하고, 태양 전지나 풍력에 의해 생산된 재생 가능한 전기에너지를 이용할 수 있으므로 온실가스 감축 및 탄소 중립 달성에 기여하는 친환경 기술로 많은 관심을 받고 있다.
우리 대학 생명화학공학과 이현주 교수와 이상엽 특훈교수 공동연구팀이 전기화학적 이산화탄소 전환과 미생물 기반의 바이오 전환을 연계한 하이브리드 시스템을 개발해 이산화탄소로부터 높은 효율로 바이오 플라스틱을 생산하는 기술 개발에 성공했다고 30일 밝혔다. 유사한 시스템 대비 20배 이상의 세계 최고 생산성을 보여준 해당 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 3월 27일 字 온라인 게재됐다.
※ 논문명 : Biohybrid CO2 electrolysis for the direct synthesis of polyesters from CO2
※ 저자 정보 : 이현주 (한국과학기술원, 교신저자), 이상엽(한국과학기술원, 교신저자), 임진규(한국과학기술원, 현 소속 기관 Stanford Linear Accelerator Center, 공동 제1저자), 최소영(한국과학기술원, 공동 제1저자), 이재원(한국과학기술원, 공동 제1저자) - 총 5명
이산화탄소의 효율적인 전환을 위해 고효율 전극 촉매 및 시스템 개발이 활발히 진행되고 있는데, 전환생성물로는 주로 탄소 1~3개의 화합물만이 제한적으로 생산되고 있다. 일산화탄소, 포름산, 에틸렌과 같은 탄소 1개의 화합물이 비교적 높은 효율로 생산되며, 이 밖에 에탄올, 아세트산, 프로판올과 같은 여러 개 탄소의 액상 화합물도 만들어질 수 있으나 이는 더 많은 전자를 필요로 하는 화학반응 특성상 전환 효율 및 생성물 선택성이 크게 낮다는 한계점이 있다.
이에 우리 대학 생명화학공학과 이현주 교수와 이상엽 특훈교수 공동연구팀은 전기화학적 이산화탄소 전환 기술과 미생물을 이용한 바이오 전환 기술을 연계해 이산화탄소로부터 바이오 플라스틱을 생산하는 기술을 개발했다. 이 전기화학-바이오 하이브리드 시스템은 전기화학 전환반응이 일어나는 전해조와 미생물 배양이 이루어지는 발효조가 연결된 형태로, 전해조에서 이산화탄소가 포름산으로 전환되면, 이 포름산을 발효조에 공급해 커프리아비더스 네케이터(Cupriavidus necator)라는 미생물이 탄소원으로 섭취해 미생물 유래 바이오 플라스틱인 폴리하이드록시알카노에이트(polyhydroxyalkanoate, PHA)를 생산한다.
기존 이러한 하이브리드 콘셉트의 연구 결과에 따르면, 전기화학 반응의 낮은 효율 및 미생물 배양 조건과의 차이 등의 문제로 생산성이 매우 낮거나 비연속적 공정에 그친다는 단점이 있었다.
이를 극복하기 위해 공동연구팀은 기체 상태의 이산화탄소를 이용한 기체 확산 전극(gas diffusion electrode)으로 포름산을 만들었다. 그리고 미생물의 생장을 저해하지 않으면서도 전기화학 반응이 충분히 잘 일어나도록 하는 전해액이자 동시에 미생물 배양 배지로 이용할 수 있는 ‘생리적 호환 가능한 양극 전해액(physiologically compatible catholyte)’을 개발하여 별도의 분리 및 정제과정 없이 바로 미생물에게 공급하도록 했다. 이를 통해 이산화탄소로부터 만들어진 포름산을 포함하고 있는 전해액이 발효조로 들어가 미생물 배양에 쓰이고, 전해조로 들어가 순환되도록 하여 전해액과 남은 포름산의 활용을 극대화했다. 또한, 이 과정에서 필터를 설치해 전극 반응에 영향을 줄 수 있는 미생물이 걸러진 전해액만이 전해조로 공급되고 미생물은 발효조 안에만 존재하도록 하는 두 시스템이 잘 연계되면서도 효율적으로 작동되도록 설계했다.
개발한 하이브리드 시스템을 통해 이산화탄소로부터 세포 건조 중량의 83%에 달하는 높은 함량의 바이오 플라스틱(PHB)를 생산했으며, 이는 4 cm2 전극에서 1.38g의 PHB를 생산한 결과로 세계 최초 그램(g) 수준의 생산이며 기존 연구 대비 20배 이상의 생산성이다. 또한 해당 하이브리드 시스템은 연속 배양(continuous culture)의 가능성을 보여줌으로써 추후 다양한 산업공정으로의 응용 또한 기대된다.
교신저자인 이현주 교수와 이상엽 특훈교수는 “이번 연구 결과는 바이오 플라스틱뿐만 아니라 다양한 화학물질 생산에 응용될 수 있는 기술로서 앞으로 탄소 중립을 위한 핵심 기술로 많은 활용이 기대된다”라고 밝혔다.
한편, 이번 연구는 과기정통부가 지원하는 이산화탄소 저감 촉매 및 에너지 소자 기술 개발 과제, 불균일계 원자 촉매 제어 과제와 석유대체 친환경 화학기술개발사업의 바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발 과제의 지원을 받아 수행됐다.
2023.03.30 조회수 11743 -
 인공지능으로 코로나19 치료제 팍스로비드와 기존 약물간 반응 예측 고도화
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 인공지능 기반 약물 상호작용 예측 기술을 고도화해, 코로나19 치료제로 사용되는 팍스로비드(PaxlovidTM) 성분과 기존 승인된 약물 간의 상호작용 분석 결과를 논문으로 발표했다고 16일 밝혔다. 이번 논문은 국제저명학술지인 「미국국립과학원회보 (PNAS)」誌’ 3월 13일자 온라인판에 게재됐다.
※ 논문명 : Computational prediction of interactions between Paxlovid and prescription drugs
※ 저자 정보 : 김예지(한국과학기술원, 공동 제1 저자), 류재용(덕성여자대학교, 공동 제1 저자), 김현욱(한국과학기술원, 공동 제1 저자), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
연구팀은 이번 연구에서 2018년에 개발한 인공지능 기반의 약물 상호작용 예측 모델인 딥디디아이(DeepDDI)를 고도화한 딥디디아이2(DeepDDI2)를 개발했다. 딥디디아이2는 기존 딥디디아이가 예측하는 86가지 약물 상호작용 종류보다 더 많은, 총 113가지의 약물 상호작용 종류를 예측한다.
연구팀은 딥디디아이2를 이용하여 코로나19 치료제인 팍스로비드*의 성분(리토나비르, 니르마트렐비르)과 기존에 승인된 약물 간의 상호작용 가능성을 예측하였다. 연구팀은 코로나19 환자 중 고위험군인 고혈압, 당뇨병 등을 앓고 있는 만성질환자가 이미 약물을 복용하고 있어, 약물 상호작용 및 약물 이상 반응이 충분히 분석되지 않은 팍스로비드를 복용 시 문제가 될 수 있다는 점에 착안해 이번 연구를 수행했다.
* 팍스로비드 : 팍스로비드는 미국 제약사인 화이자가 개발한 코로나19 치료제로, 2021년 12월 미국 식품의약국(FDA)의 긴급사용승인을 받았다.
연구팀은 팍스로비드의 성분인 리토나비르와 니르마트렐비르가 2,248개의 승인된 약물과 어떤 상호작용을 하는지, 딥디디아이2를 이용해 예측했다. 예측 결과 리토나비르는 1,403개의 승인된 약물과, 니르마트렐비르는 673개의 승인된 약물과 상호작용이 있을 것으로 예측됐다.
또한, 연구팀은 예측 결과를 활용해, 약물 상호작용 가능성이 높은 승인 약물에 대해, 동일 기전을 갖되 약물 상호작용 가능성이 낮은 대체 약물들을 제안했다. 이에 따라, 리토나비르와의 약물 상호작용 가능성을 낮출 수 있는 대체 약물 124개와 니르마트렐비르와의 약물 상호작용 가능성을 낮출 수 있는 대체 약물 239개를 제안했다.
이번 연구 성과를 통해 약물 상호작용을 정확하게 예측할 수 있는 인공지능 모델을 활용하는 것이 가능해졌으며, 이는 신약 개발 및 약물 처방 시 유용한 정보를 제공함으로써, 디지털 헬스케어, 정밀의료 산업 및 제약 산업에서 중요한 역할을 할 것으로 기대된다.
이상엽 특훈교수는 "이번 연구 결과는 실험과 임상을 통해 검증된 것은 아니므로 100% 의존해서는 안된다“고 강조하면서 ”팬데믹과 같이 긴급한 상황에서 신속하게 개발된 약물을 사용할 때, 예측된 약물 상호작용 유래 약물 이상 반응결과를 전문의가 미리 검토하여 약을 처방할 때 도움을 줄 수 있다는 점에서 의미가 있다"고 말했다.
한편 이번 연구는 과기정통부가 지원하는 KAIST 코로나대응 과학기술 뉴딜사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2023.03.16 조회수 9395
인공지능으로 코로나19 치료제 팍스로비드와 기존 약물간 반응 예측 고도화
우리 대학 생명화학공학과 이상엽 특훈교수 연구팀이 인공지능 기반 약물 상호작용 예측 기술을 고도화해, 코로나19 치료제로 사용되는 팍스로비드(PaxlovidTM) 성분과 기존 승인된 약물 간의 상호작용 분석 결과를 논문으로 발표했다고 16일 밝혔다. 이번 논문은 국제저명학술지인 「미국국립과학원회보 (PNAS)」誌’ 3월 13일자 온라인판에 게재됐다.
※ 논문명 : Computational prediction of interactions between Paxlovid and prescription drugs
※ 저자 정보 : 김예지(한국과학기술원, 공동 제1 저자), 류재용(덕성여자대학교, 공동 제1 저자), 김현욱(한국과학기술원, 공동 제1 저자), 이상엽(한국과학기술원, 교신저자) 포함 총 4명
연구팀은 이번 연구에서 2018년에 개발한 인공지능 기반의 약물 상호작용 예측 모델인 딥디디아이(DeepDDI)를 고도화한 딥디디아이2(DeepDDI2)를 개발했다. 딥디디아이2는 기존 딥디디아이가 예측하는 86가지 약물 상호작용 종류보다 더 많은, 총 113가지의 약물 상호작용 종류를 예측한다.
연구팀은 딥디디아이2를 이용하여 코로나19 치료제인 팍스로비드*의 성분(리토나비르, 니르마트렐비르)과 기존에 승인된 약물 간의 상호작용 가능성을 예측하였다. 연구팀은 코로나19 환자 중 고위험군인 고혈압, 당뇨병 등을 앓고 있는 만성질환자가 이미 약물을 복용하고 있어, 약물 상호작용 및 약물 이상 반응이 충분히 분석되지 않은 팍스로비드를 복용 시 문제가 될 수 있다는 점에 착안해 이번 연구를 수행했다.
* 팍스로비드 : 팍스로비드는 미국 제약사인 화이자가 개발한 코로나19 치료제로, 2021년 12월 미국 식품의약국(FDA)의 긴급사용승인을 받았다.
연구팀은 팍스로비드의 성분인 리토나비르와 니르마트렐비르가 2,248개의 승인된 약물과 어떤 상호작용을 하는지, 딥디디아이2를 이용해 예측했다. 예측 결과 리토나비르는 1,403개의 승인된 약물과, 니르마트렐비르는 673개의 승인된 약물과 상호작용이 있을 것으로 예측됐다.
또한, 연구팀은 예측 결과를 활용해, 약물 상호작용 가능성이 높은 승인 약물에 대해, 동일 기전을 갖되 약물 상호작용 가능성이 낮은 대체 약물들을 제안했다. 이에 따라, 리토나비르와의 약물 상호작용 가능성을 낮출 수 있는 대체 약물 124개와 니르마트렐비르와의 약물 상호작용 가능성을 낮출 수 있는 대체 약물 239개를 제안했다.
이번 연구 성과를 통해 약물 상호작용을 정확하게 예측할 수 있는 인공지능 모델을 활용하는 것이 가능해졌으며, 이는 신약 개발 및 약물 처방 시 유용한 정보를 제공함으로써, 디지털 헬스케어, 정밀의료 산업 및 제약 산업에서 중요한 역할을 할 것으로 기대된다.
이상엽 특훈교수는 "이번 연구 결과는 실험과 임상을 통해 검증된 것은 아니므로 100% 의존해서는 안된다“고 강조하면서 ”팬데믹과 같이 긴급한 상황에서 신속하게 개발된 약물을 사용할 때, 예측된 약물 상호작용 유래 약물 이상 반응결과를 전문의가 미리 검토하여 약을 처방할 때 도움을 줄 수 있다는 점에서 의미가 있다"고 말했다.
한편 이번 연구는 과기정통부가 지원하는 KAIST 코로나대응 과학기술 뉴딜사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2023.03.16 조회수 9395 -
 수학과 실험을 결합하여 생체시계의 역설 규명
수학과 실험을 결합한 융합연구를 통해 생체시계가 안정적 리듬을 유지하면서도 환경변화에 쉽게 적응할 수 있는 원리가 밝혀졌다. 우리 대학 수리과학과 김재경 교수가 이끄는 기초과학연구원(IBS) 수리 및 계산과학 연구단 의생명 수학 그룹과 우리 대학 수리과학과 연구팀, 그리고 아주대 의과대학 뇌과학과 김은영 교수 연구팀은 공동연구를 통해 초파리 뇌의 생체시계 뉴런들의 생체시계 작동원리를 분석했다.
생체시계(Circadian clock)는 생명체가 24시간 주기에 맞춰 살아갈 수 있도록 행동과 생리 작용을 조절하는 역할을 한다. 예를 들어, 생체시계는 밤 9시경이 되면 뇌에서 멜라토닌 호르몬 분비를 유발해 일정 시간이 되면 수면을 취할 수 있도록 하는 등 우리 운동 능력이나 학습 능력에 이르는 거의 모든 생리 작용에 관여한다. 따라서, 평소에는 일정한 시간을 안정적으로 몸에 제시하면서, 동시에 계절 변화에 따른 낮밤의 길이 변화나 해외여행으로 인한 시차 등 환경변화가 생겼을 때는 새로운 환경에 유연하게 적응해서 변화한 시간을 몸에 제시해주어야 한다. 이러한 안정성과 유연성을 동시에 유지하는 생체시계의 역설적인 성질의 원리는 지금까지 알려져 있지 않았다.
초파리 생체시계 뉴런들의 경우, 마스터 뉴런(master neuron)이 외부로부터 들어오는 빛 정보를 취합하여 시간 정보를 슬레이브 뉴런(slave neuron)에 전달하면, 이에 맞춰 슬레이브 뉴런이 일주기 행동을 조절하는 계층구조를 형성하고 있다. 이러한 역할 차이에도 불구하고, 두 뉴런의 생체시계는 동일한 원리로 작동한다고 알려져 있었다. 2017년 노벨 생리의학상을 수상한 마이클 영, 제프리 홀 그리고 마이클 로스바쉬 교수는 PER 단백질이 매일 일정한 시간에 세포핵 안으로 들어가 PER 유전자의 전사를 일정 시간에 스스로 억제하는 음성피드백 루프를 통해 24시간 주기의 리듬을 만드는 것이 생체시계의 핵심 원리임을 밝혔다.
연구진은 초파리에서 CLK에 변이가 생겼을 때 마스터 뉴런과 슬레이브 뉴런에서 서로 다른 PER변화 양상이 나타나는 것에 착안하여 마스터 뉴런과 슬레이브 뉴런이 만들어내는 PER 단백질의 변화 양상을 1000여 개 수리 모델을 개발하여 분석한 결과, 마스터 뉴런의 PER이 슬레이브 뉴런의 PER에 비해 빠르게 합성되었다 분해되고 있음을 예측하였다. 이러한 마스터 뉴런의 독특한 성질 덕분에, 평소에 강한 PER 리듬을 생성해서 안정적인 시계 역할을 하다가 외부 환경에 변화가 일어났을 때 빠르게 적응할 수 있음 역시 가상 시뮬레이션을 통해 예측하였다. 이러한 마스터 뉴런에 관한 수리모델링 예측은 초파리 생체 실험을 통해서도 검증되었다.
김재경 교수는 “모든 세포의 생체시계는 당연히 비슷한 방식으로 작동될 것이란 오래된 믿음이 수학을 이용한 분석 덕분에 틀렸음을 알게 되었다”며 “수학과 실험을 융합한 방식으로 문제에 접근하였기 때문에 문제를 해결할 수 있었다”고 말했다. 또한, 김은영 교수는 “마스터 뉴런 생체시계의 독특한 성질 덕분에 생체시계가 안정성과 유연성이라는 역설적인 성질을 모두 가질 수 있었다”며 “모든 세포의 생체시계가 천편일률적으로 작동하는 대신 자신의 역할에 맞게 다른 작동 방식을 취한다는 점이 놀라웠다”고 말했다.
생체시계가 안정성과 유연성을 동시에 유지하지 못하면 다양한 환경에서 일정한 수면패턴을 유지할 수 없고, 일주기 리듬 수면장애가 발생한다. 이번 연구결과는 일주기 리듬 수면장애의 원인을 규명하고 치료법을 찾는 새로운 패러다임을 제시할 수 있을 것으로 예상된다.
정의민, 권미리, 조은주 박사가 공동 제 1저자로 참여한 이번 연구결과는 2월 15일 오후 5시(한국시간) 자연과학 분야의 저명 국제학술지인 미국국립과학원회보(Proceedings Of The National Academy Of Sciences, PNAS, IF 11.205)에 게재됐다.
* 논문명: Systematic modeling-driven experiments identify distinct molecular clockworks underlying hierarchically organized pacemaker neurons
2022.02.16 조회수 15297
수학과 실험을 결합하여 생체시계의 역설 규명
수학과 실험을 결합한 융합연구를 통해 생체시계가 안정적 리듬을 유지하면서도 환경변화에 쉽게 적응할 수 있는 원리가 밝혀졌다. 우리 대학 수리과학과 김재경 교수가 이끄는 기초과학연구원(IBS) 수리 및 계산과학 연구단 의생명 수학 그룹과 우리 대학 수리과학과 연구팀, 그리고 아주대 의과대학 뇌과학과 김은영 교수 연구팀은 공동연구를 통해 초파리 뇌의 생체시계 뉴런들의 생체시계 작동원리를 분석했다.
생체시계(Circadian clock)는 생명체가 24시간 주기에 맞춰 살아갈 수 있도록 행동과 생리 작용을 조절하는 역할을 한다. 예를 들어, 생체시계는 밤 9시경이 되면 뇌에서 멜라토닌 호르몬 분비를 유발해 일정 시간이 되면 수면을 취할 수 있도록 하는 등 우리 운동 능력이나 학습 능력에 이르는 거의 모든 생리 작용에 관여한다. 따라서, 평소에는 일정한 시간을 안정적으로 몸에 제시하면서, 동시에 계절 변화에 따른 낮밤의 길이 변화나 해외여행으로 인한 시차 등 환경변화가 생겼을 때는 새로운 환경에 유연하게 적응해서 변화한 시간을 몸에 제시해주어야 한다. 이러한 안정성과 유연성을 동시에 유지하는 생체시계의 역설적인 성질의 원리는 지금까지 알려져 있지 않았다.
초파리 생체시계 뉴런들의 경우, 마스터 뉴런(master neuron)이 외부로부터 들어오는 빛 정보를 취합하여 시간 정보를 슬레이브 뉴런(slave neuron)에 전달하면, 이에 맞춰 슬레이브 뉴런이 일주기 행동을 조절하는 계층구조를 형성하고 있다. 이러한 역할 차이에도 불구하고, 두 뉴런의 생체시계는 동일한 원리로 작동한다고 알려져 있었다. 2017년 노벨 생리의학상을 수상한 마이클 영, 제프리 홀 그리고 마이클 로스바쉬 교수는 PER 단백질이 매일 일정한 시간에 세포핵 안으로 들어가 PER 유전자의 전사를 일정 시간에 스스로 억제하는 음성피드백 루프를 통해 24시간 주기의 리듬을 만드는 것이 생체시계의 핵심 원리임을 밝혔다.
연구진은 초파리에서 CLK에 변이가 생겼을 때 마스터 뉴런과 슬레이브 뉴런에서 서로 다른 PER변화 양상이 나타나는 것에 착안하여 마스터 뉴런과 슬레이브 뉴런이 만들어내는 PER 단백질의 변화 양상을 1000여 개 수리 모델을 개발하여 분석한 결과, 마스터 뉴런의 PER이 슬레이브 뉴런의 PER에 비해 빠르게 합성되었다 분해되고 있음을 예측하였다. 이러한 마스터 뉴런의 독특한 성질 덕분에, 평소에 강한 PER 리듬을 생성해서 안정적인 시계 역할을 하다가 외부 환경에 변화가 일어났을 때 빠르게 적응할 수 있음 역시 가상 시뮬레이션을 통해 예측하였다. 이러한 마스터 뉴런에 관한 수리모델링 예측은 초파리 생체 실험을 통해서도 검증되었다.
김재경 교수는 “모든 세포의 생체시계는 당연히 비슷한 방식으로 작동될 것이란 오래된 믿음이 수학을 이용한 분석 덕분에 틀렸음을 알게 되었다”며 “수학과 실험을 융합한 방식으로 문제에 접근하였기 때문에 문제를 해결할 수 있었다”고 말했다. 또한, 김은영 교수는 “마스터 뉴런 생체시계의 독특한 성질 덕분에 생체시계가 안정성과 유연성이라는 역설적인 성질을 모두 가질 수 있었다”며 “모든 세포의 생체시계가 천편일률적으로 작동하는 대신 자신의 역할에 맞게 다른 작동 방식을 취한다는 점이 놀라웠다”고 말했다.
생체시계가 안정성과 유연성을 동시에 유지하지 못하면 다양한 환경에서 일정한 수면패턴을 유지할 수 없고, 일주기 리듬 수면장애가 발생한다. 이번 연구결과는 일주기 리듬 수면장애의 원인을 규명하고 치료법을 찾는 새로운 패러다임을 제시할 수 있을 것으로 예상된다.
정의민, 권미리, 조은주 박사가 공동 제 1저자로 참여한 이번 연구결과는 2월 15일 오후 5시(한국시간) 자연과학 분야의 저명 국제학술지인 미국국립과학원회보(Proceedings Of The National Academy Of Sciences, PNAS, IF 11.205)에 게재됐다.
* 논문명: Systematic modeling-driven experiments identify distinct molecular clockworks underlying hierarchically organized pacemaker neurons
2022.02.16 조회수 15297 -
 아동의 다언어 사용이 뇌 전체 연결망 향상에 미치는 영향 확인
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 미국 예일대학교(Yale University) 심리학과 마빈 천(Marvin M. Chun) 교수 연구팀과 공동연구를 통해 아동기의 외국어 구사 여부가 인지능력을 향상하고 뇌 연결망에 변화를 가져온다고 10일 밝혔다.
연구팀은 미국 국립 보건원(National Institutes of Health, NIH)의 청소년 뇌 인지 발달 연구(the Adolescent Brain Cognitive Development, ABCD Study) 데이터를 사용해 발달단계에 있는 9-10세 아이들의 인지기능 점수와 기능적 자기공명영상(functional magnetic resonance imaging, fMRI)을 분석했다. 모국어 외 다른 언어를 추가로 사용하는 아이들은 모국어만 사용하는 아이들에 비해 기억을 측정하는 인지 과제에서 높은 점수를 보였다. 또한 다언어 사용은 아이들의 뇌 전체 연결망에도 영향을 주는 것으로 확인됐다.
바이오및뇌공학과 권영혜 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `미국국립과학원회보(Proceedings of the National Academy of Sciences of the United States of America, PNAS)' 11월 118권 49호에 출판됐다. (논문명 : Predicting multilingual effects on executive function and individual connectomes in children: an ABCD Study).
뇌는 과제를 수행할 뿐만 아니라 쉬고 있을 때도 특정 영역들이 활성화된다. 기능적 자기공명영상(fMRI)을 통해 활성화되는 각 영역을 관찰할 수 있고, 이 영역들이 서로 어떻게 연결이 돼 있는지 기능적 뇌 연결망(functional connectivity)을 계산할 수 있다.
뇌 모든 영역 간의 연결 패턴을 나타내는 뇌 전체 연결망(whole-brain functional connectivity, connectome)은 사람마다 다르고, 그 사람의 나이, 지능, 인지기능 등 그 사람만의 고유한 특성을 내포하고 있다고 알려져 최근 뇌 과학 분야에서 활발히 연구되고 있다.
연구팀은 뇌의 특정 영역에 국한하지 않고 뇌 전체의 연결망에 초점을 맞춰, 여러 언어를 하는 아이들과 하나의 언어만 사용하는 아이들이 서로 다른 뇌 전체 연결망을 가지는 것을 관찰했다. 기억 관련 과제를 수행할 때 다언어 사용 아이들은 단일언어 사용 아이들에 비해 뇌 후두엽(occipital lobe)과 피질하 영역(subcortical area)간 강한 연결망을 보였다. 아이들이 아무 과제를 수행하지 않는 휴지기(resting state)에도 두 그룹 간 차이가 관찰됐는데, 다언어 사용 아이들에게서 뇌 후두엽과 전전두엽(prefrontal cortex)간 강한 연결성을 보였다.
더 나아가 연구팀은 기계학습을 통해 아이들이 기억 관련 과제를 수행할 때와 휴지기일 때 나타나는 뇌 전체 연결망만으로 그 아이가 여러 언어를 사용하는지 한 언어를 사용하는지를 성공적으로 예측할 수 있었다. 또한 다언어 사용 아이들이 기억 관련 과제를 수행할 때 관찰되는 기억 관련 연결망만으로 그 아이들이 해당 과제에서 어떤 점수를 얻었는지 예측할 수 있었다. 단일 언어사용 아이들에게서는 이러한 현상이 발견되지 않았는데, 이는 다언어 사용 아이들의 뇌 전체 연결망이 그들의 행동과 더 밀접한 관계를 맺고 있다는 것을 시사한다.
연구팀은 이번 연구를 통해 발달단계에 있는 9-10세 아이들의 다언어 사용 여부가 뇌 전체 연결망에 변화를 주는 것을 확인했다. 이 연구를 바탕으로 다언어 사용의 영향이 발달단계를 거치며 성인이 될 때까지 어떻게 변화하는지 이해하는 데 도움이 될 것으로 기대한다. 더 나아가 다언어 사용은 알츠하이머와 같은 퇴행성 뇌질환에 동반되는 인지기능 저하를 방어하는 뇌인지 예비능(cognitive reserve)을 가져오는데, 이 현상을 연구하는 데 도움이 될 것으로 기대된다.
제1 저자인 권영혜 박사과정은 "성인보다 언어사용 기간이 짧은 9-10세 아이들에게서도 여러 언어의 사용이 인지기능과 뇌 연결 패턴에 영향을 주는 것을 확인하였다ˮ 라며 "어렸을 때부터 형성된 이러한 차이가 시간이 흐르면서 어떠한 형태로 자리 잡아 성인이 되었을 때 그리고 노인이 되어서까지 영향을 주는지를 이해하는 데 도움이 되길 바란다ˮ 라고 말했다.
이번 연구는 한국연구재단, 산업통상자원부, 미국 국립 보건원 지원을 받아 수행됐다.
2021.12.10 조회수 11656
아동의 다언어 사용이 뇌 전체 연결망 향상에 미치는 영향 확인
우리 대학 바이오및뇌공학과 정용 교수 연구팀이 미국 예일대학교(Yale University) 심리학과 마빈 천(Marvin M. Chun) 교수 연구팀과 공동연구를 통해 아동기의 외국어 구사 여부가 인지능력을 향상하고 뇌 연결망에 변화를 가져온다고 10일 밝혔다.
연구팀은 미국 국립 보건원(National Institutes of Health, NIH)의 청소년 뇌 인지 발달 연구(the Adolescent Brain Cognitive Development, ABCD Study) 데이터를 사용해 발달단계에 있는 9-10세 아이들의 인지기능 점수와 기능적 자기공명영상(functional magnetic resonance imaging, fMRI)을 분석했다. 모국어 외 다른 언어를 추가로 사용하는 아이들은 모국어만 사용하는 아이들에 비해 기억을 측정하는 인지 과제에서 높은 점수를 보였다. 또한 다언어 사용은 아이들의 뇌 전체 연결망에도 영향을 주는 것으로 확인됐다.
바이오및뇌공학과 권영혜 박사과정이 제1 저자로 참여한 이번 연구는 국제 학술지 `미국국립과학원회보(Proceedings of the National Academy of Sciences of the United States of America, PNAS)' 11월 118권 49호에 출판됐다. (논문명 : Predicting multilingual effects on executive function and individual connectomes in children: an ABCD Study).
뇌는 과제를 수행할 뿐만 아니라 쉬고 있을 때도 특정 영역들이 활성화된다. 기능적 자기공명영상(fMRI)을 통해 활성화되는 각 영역을 관찰할 수 있고, 이 영역들이 서로 어떻게 연결이 돼 있는지 기능적 뇌 연결망(functional connectivity)을 계산할 수 있다.
뇌 모든 영역 간의 연결 패턴을 나타내는 뇌 전체 연결망(whole-brain functional connectivity, connectome)은 사람마다 다르고, 그 사람의 나이, 지능, 인지기능 등 그 사람만의 고유한 특성을 내포하고 있다고 알려져 최근 뇌 과학 분야에서 활발히 연구되고 있다.
연구팀은 뇌의 특정 영역에 국한하지 않고 뇌 전체의 연결망에 초점을 맞춰, 여러 언어를 하는 아이들과 하나의 언어만 사용하는 아이들이 서로 다른 뇌 전체 연결망을 가지는 것을 관찰했다. 기억 관련 과제를 수행할 때 다언어 사용 아이들은 단일언어 사용 아이들에 비해 뇌 후두엽(occipital lobe)과 피질하 영역(subcortical area)간 강한 연결망을 보였다. 아이들이 아무 과제를 수행하지 않는 휴지기(resting state)에도 두 그룹 간 차이가 관찰됐는데, 다언어 사용 아이들에게서 뇌 후두엽과 전전두엽(prefrontal cortex)간 강한 연결성을 보였다.
더 나아가 연구팀은 기계학습을 통해 아이들이 기억 관련 과제를 수행할 때와 휴지기일 때 나타나는 뇌 전체 연결망만으로 그 아이가 여러 언어를 사용하는지 한 언어를 사용하는지를 성공적으로 예측할 수 있었다. 또한 다언어 사용 아이들이 기억 관련 과제를 수행할 때 관찰되는 기억 관련 연결망만으로 그 아이들이 해당 과제에서 어떤 점수를 얻었는지 예측할 수 있었다. 단일 언어사용 아이들에게서는 이러한 현상이 발견되지 않았는데, 이는 다언어 사용 아이들의 뇌 전체 연결망이 그들의 행동과 더 밀접한 관계를 맺고 있다는 것을 시사한다.
연구팀은 이번 연구를 통해 발달단계에 있는 9-10세 아이들의 다언어 사용 여부가 뇌 전체 연결망에 변화를 주는 것을 확인했다. 이 연구를 바탕으로 다언어 사용의 영향이 발달단계를 거치며 성인이 될 때까지 어떻게 변화하는지 이해하는 데 도움이 될 것으로 기대한다. 더 나아가 다언어 사용은 알츠하이머와 같은 퇴행성 뇌질환에 동반되는 인지기능 저하를 방어하는 뇌인지 예비능(cognitive reserve)을 가져오는데, 이 현상을 연구하는 데 도움이 될 것으로 기대된다.
제1 저자인 권영혜 박사과정은 "성인보다 언어사용 기간이 짧은 9-10세 아이들에게서도 여러 언어의 사용이 인지기능과 뇌 연결 패턴에 영향을 주는 것을 확인하였다ˮ 라며 "어렸을 때부터 형성된 이러한 차이가 시간이 흐르면서 어떠한 형태로 자리 잡아 성인이 되었을 때 그리고 노인이 되어서까지 영향을 주는지를 이해하는 데 도움이 되길 바란다ˮ 라고 말했다.
이번 연구는 한국연구재단, 산업통상자원부, 미국 국립 보건원 지원을 받아 수행됐다.
2021.12.10 조회수 11656 -
 살아있는 미생물 내 바이오 플라스틱 생성 관찰 최초 성공
우리 대학 생명화학공학과 이상엽 특훈교수(연구부총장)와 물리학과 박용근 석좌교수 공동연구팀이 ‘3차원 홀로그래픽 현미경 기술을 통한 미생물의 바이오 플라스틱 과립 생산 특징 규명’에 성공했다고 27일 밝혔다.
이번 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 7월 27일 字 온라인 게재됐다.
※ 논문명 : Three-dimensional label-free visualization and quantification of polyhydroxyalkanoates in individual bacterial cell in its native state
※ 저자 정보 : 이상엽(KAIST, 교신저자), 박용근(KAIST, 교신저자), 최소영(KAIST, 공동 제1 저자), 오정훈(KAIST, 공동 제1저자), 정재황(KAIST, 공동 제1저자) - 총 5명
전 세계적으로 폐플라스틱으로 인한 환경오염 및 생태계 파괴, 미세 플라스틱의 인류 보건 위협 등의 문제가 심각해짐에 따라 다양한 규제 및 대안 기술들이 연구되고 있다. 그중 미생물로부터 만들어지는 폴리에스테르인 폴리하이드록시알카노에이트 (polyhydroxyalkanoate, 이하 PHA)가 기존 합성 플라스틱을 대체할 친환경 바이오 플라스틱으로 많은 관심을 받고 있다.
PHA는 폴리에틸렌이나 폴리프로필렌과 같은 범용 플라스틱과 유사한 물성을 가지고 있어 용기 포장재, 비닐, 일회용품 등의 다양한 활용이 가능하며, 토양이나 해양 환경에서 생분해가 가능한 고분자라는 가장 중요한 장점을 갖고 있다.
PHA는 몇몇 미생물 내에 불용성의 과립(granule) 형태로 발견되는 고분자 물질로, 미생물이 환경 변화 및 세포 상태에 따라 탄소원, 에너지원으로 세포 내에 축적하게 된다. PHA가 세포 내에 축적되는 원리를 관찰하기 위해 여러 연구가 진행돼왔다.
형광 현미경, 투과전자현미경, 전자 저온 촬영 등의 기술이 이용됐는데, 이는 2차원상의 이미지만을 제시하거나 형광 물질과 같은 별도의 표식이나 세포의 고정/절편 제작 과정이 있어야 하여, 세포 원래 그대로의 상태에서의 관측이 어려웠다. 따라서 기술적 한계로 인해 세포 내에서 PHA 과립 형성에 대한 완전한 이해가 어려웠고, 관측 결과에 기반을 둔 여러 형성 메커니즘 모델만이 제안돼왔다.
이에 이상엽 특훈교수와 박용근 석좌교수 공동연구팀은 최근 떠오르고 있는 *3차원 홀로그래픽 현미경 기술을 통해 PHA 생산 박테리아의 심층 관찰 및 정량/정성 분석 연구를 수행했다.
*3차원 홀로그래픽 현미경 기술은 물질의 굴절률(refractive index)을 활용하는 이미징 방법으로, 염색 등 준비 과정을 필요로 하지 않기 때문에 살아 있는 세포의 3차원 정보를 정량적으로 측정 가능하다.
연구팀은 PHA의 한 종류인 *PHB 생산 미생물로 잘 알려진 쿠프리아비두스 네카토르(Cupriavidus necator)와 이 미생물의 PHB 합성 대사회로 유전자를 가진 재조합 대장균을 이용해 비교·분석을 수행했다.
*PHA는 현재까지 약 150여 가지의 하이드록시산 화합물들이 단량체로 보고되었으며, PHA 중 가장 대표적이며 많은 연구가 이루어진 것이 poly(3-hydroxybutyrate) [PHB]임
연구팀은 재구성된 세포의 3차원 굴절률 분포로 단일세포 수준에서 세포와 세포 내 과립의 3차원 시각화 및 이를 통한 부피, 질량, 밀도, 분포 등의 정량 분석에 성공했다. 수백 개의 단일 세포들과 세포 내의 PHA 과립에 대한 정량 및 이의 통계 분석을 통해 두 미생물에서의 PHA 과립 형성의 차이점을 도출해냈다.
특히, 단일세포 내의 PHA 과립의 밀도의 개념을 새롭게 제시했으며, 두 미생물에서의 PHA 과립의 밀도의 차이 및 세포 내 분포 형태 및 위치에 대한 특이적인 차이를 발견했다. 더 나아가서, 두 미생물의 PHA 과립 형성의 차이를 나타내게 하는 핵심 단백질을 규명해, 재조합 대장균의 PHA 과립 형성의 양상을 쿠프리아비두스 네카토르와 유사하게 변화시킬 수 있었다.
또한, 실시간 모니터링을 통해 최대 약 8시간 동안의 세포와 세포 내 PHA 과립의 성장 과정을 보여주는 3차원 영상을 제작할 수 있었다. 이는 미생물이 살아있는 상태에서 별도의 처리 과정이 없는 자연 상태 조건 하에, 세포 내 PHA 과립의 형성과 세포 분열과 연계된 이동을 3차원에서 실시간으로 관측한 세계 최초의 결과라는 데 큰 의의가 있다.
이상엽 특훈교수는 “이번 연구를 통해 미생물의 PHA 생산 원리에 대해 더욱 깊은 이해가 가능해졌고, 이는 생물학과 물리학의 융합 연구로서 이뤄진 성과라는 데에 큰 의의가 있으며, 향후 다양한 바이오 플라스틱 생산 공정 개발에 큰 도움이 될 것”이라고 말했다.
한편 이번 연구는 과기정통부가 지원하는 기후변화대응기술개발사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2021.07.28 조회수 16626
살아있는 미생물 내 바이오 플라스틱 생성 관찰 최초 성공
우리 대학 생명화학공학과 이상엽 특훈교수(연구부총장)와 물리학과 박용근 석좌교수 공동연구팀이 ‘3차원 홀로그래픽 현미경 기술을 통한 미생물의 바이오 플라스틱 과립 생산 특징 규명’에 성공했다고 27일 밝혔다.
이번 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 7월 27일 字 온라인 게재됐다.
※ 논문명 : Three-dimensional label-free visualization and quantification of polyhydroxyalkanoates in individual bacterial cell in its native state
※ 저자 정보 : 이상엽(KAIST, 교신저자), 박용근(KAIST, 교신저자), 최소영(KAIST, 공동 제1 저자), 오정훈(KAIST, 공동 제1저자), 정재황(KAIST, 공동 제1저자) - 총 5명
전 세계적으로 폐플라스틱으로 인한 환경오염 및 생태계 파괴, 미세 플라스틱의 인류 보건 위협 등의 문제가 심각해짐에 따라 다양한 규제 및 대안 기술들이 연구되고 있다. 그중 미생물로부터 만들어지는 폴리에스테르인 폴리하이드록시알카노에이트 (polyhydroxyalkanoate, 이하 PHA)가 기존 합성 플라스틱을 대체할 친환경 바이오 플라스틱으로 많은 관심을 받고 있다.
PHA는 폴리에틸렌이나 폴리프로필렌과 같은 범용 플라스틱과 유사한 물성을 가지고 있어 용기 포장재, 비닐, 일회용품 등의 다양한 활용이 가능하며, 토양이나 해양 환경에서 생분해가 가능한 고분자라는 가장 중요한 장점을 갖고 있다.
PHA는 몇몇 미생물 내에 불용성의 과립(granule) 형태로 발견되는 고분자 물질로, 미생물이 환경 변화 및 세포 상태에 따라 탄소원, 에너지원으로 세포 내에 축적하게 된다. PHA가 세포 내에 축적되는 원리를 관찰하기 위해 여러 연구가 진행돼왔다.
형광 현미경, 투과전자현미경, 전자 저온 촬영 등의 기술이 이용됐는데, 이는 2차원상의 이미지만을 제시하거나 형광 물질과 같은 별도의 표식이나 세포의 고정/절편 제작 과정이 있어야 하여, 세포 원래 그대로의 상태에서의 관측이 어려웠다. 따라서 기술적 한계로 인해 세포 내에서 PHA 과립 형성에 대한 완전한 이해가 어려웠고, 관측 결과에 기반을 둔 여러 형성 메커니즘 모델만이 제안돼왔다.
이에 이상엽 특훈교수와 박용근 석좌교수 공동연구팀은 최근 떠오르고 있는 *3차원 홀로그래픽 현미경 기술을 통해 PHA 생산 박테리아의 심층 관찰 및 정량/정성 분석 연구를 수행했다.
*3차원 홀로그래픽 현미경 기술은 물질의 굴절률(refractive index)을 활용하는 이미징 방법으로, 염색 등 준비 과정을 필요로 하지 않기 때문에 살아 있는 세포의 3차원 정보를 정량적으로 측정 가능하다.
연구팀은 PHA의 한 종류인 *PHB 생산 미생물로 잘 알려진 쿠프리아비두스 네카토르(Cupriavidus necator)와 이 미생물의 PHB 합성 대사회로 유전자를 가진 재조합 대장균을 이용해 비교·분석을 수행했다.
*PHA는 현재까지 약 150여 가지의 하이드록시산 화합물들이 단량체로 보고되었으며, PHA 중 가장 대표적이며 많은 연구가 이루어진 것이 poly(3-hydroxybutyrate) [PHB]임
연구팀은 재구성된 세포의 3차원 굴절률 분포로 단일세포 수준에서 세포와 세포 내 과립의 3차원 시각화 및 이를 통한 부피, 질량, 밀도, 분포 등의 정량 분석에 성공했다. 수백 개의 단일 세포들과 세포 내의 PHA 과립에 대한 정량 및 이의 통계 분석을 통해 두 미생물에서의 PHA 과립 형성의 차이점을 도출해냈다.
특히, 단일세포 내의 PHA 과립의 밀도의 개념을 새롭게 제시했으며, 두 미생물에서의 PHA 과립의 밀도의 차이 및 세포 내 분포 형태 및 위치에 대한 특이적인 차이를 발견했다. 더 나아가서, 두 미생물의 PHA 과립 형성의 차이를 나타내게 하는 핵심 단백질을 규명해, 재조합 대장균의 PHA 과립 형성의 양상을 쿠프리아비두스 네카토르와 유사하게 변화시킬 수 있었다.
또한, 실시간 모니터링을 통해 최대 약 8시간 동안의 세포와 세포 내 PHA 과립의 성장 과정을 보여주는 3차원 영상을 제작할 수 있었다. 이는 미생물이 살아있는 상태에서 별도의 처리 과정이 없는 자연 상태 조건 하에, 세포 내 PHA 과립의 형성과 세포 분열과 연계된 이동을 3차원에서 실시간으로 관측한 세계 최초의 결과라는 데 큰 의의가 있다.
이상엽 특훈교수는 “이번 연구를 통해 미생물의 PHA 생산 원리에 대해 더욱 깊은 이해가 가능해졌고, 이는 생물학과 물리학의 융합 연구로서 이뤄진 성과라는 데에 큰 의의가 있으며, 향후 다양한 바이오 플라스틱 생산 공정 개발에 큰 도움이 될 것”이라고 말했다.
한편 이번 연구는 과기정통부가 지원하는 기후변화대응기술개발사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2021.07.28 조회수 16626 -
 약물 가상 스크리닝 기술로 코로나19 치료제 후보 발굴
우리 대학 생명화학공학과 이상엽 특훈교수(연구부총장)와 한국파스퇴르연구소 김승택 박사 공동연구팀이 ‘약물 가상 스크리닝 기술을 이용한 코로나19 치료제 개발’에 성공했다고 8일 밝혔다.
이번 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 7월 7일 字 온라인 게재됐다.
※ 논문명 : Drugs repurposed for COVID-19 by virtual screening of 6,218 drugs and cell-based assay
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), 김승택(한국파스퇴르연구소, 교신저자), 장우대(한국과학기술원, 제1저자), 전상은(한국파스퇴르연구소, 제2저자), 포함 총 4명
코로나바이러스감염증-19(이하 코로나19)는 글로벌 팬데믹으로 전개되고 있으며 현재 인류 보건을 심각하게 위협하는 상황이다. 코로나19 치료 목적으로 미국식품의약국(FDA)에서 정식 승인을 받은 렘데시비르(상품명 베클러리)가 현재 임상에서 사용 중이지만, 사망률은 감소시키지 못하고 회복 기간을 5일 정도 단축함으로써 치료 효과가 기대에 미치지 못하는 것으로 알려졌다. 또한 렘데시비르는 정맥 주사제여서 의료기관에서 입원을 통해 수일 동안 투여받아야 하므로 팬데믹 상황에 적합하지 않은 약물이다. 따라서 코로나19로 인한 사망률을 획기적으로 감소시키고, 치료 기간을 단축시키는 경구용 치료제 개발이 시급한 상황이었다.
이에 이상엽 특훈교수와 한국파스퇴르연구소 김승택 박사 공동연구팀은 약물 가상 스크리닝 기술을 이용한 약물 재창출 전략으로 코로나19 치료제 개발 연구를 수행했다.
연구팀은 팬데믹 상황에 대응한 신속한 치료제 개발을 위해 가상 스크리닝 기술을 이용한 약물 재창출 전략을 수립했다. 약물 재창출은 이미 안전성이 검증된 FDA 승인 약물 또는 임상 진행 중인 약물을 대상으로 새로운 적응증을 찾는 방식이다. 이 전략은 신약 개발 과정에 소요되는 시간을 단축시킬 수 있어 코로나19와 같은 팬데믹 상황에 적합한 신약 개발 전략이다.
우리 대학 생명화학공학과 장우대 박사는 우선 FDA 승인 약물 또는 임상 진행 중인 약물을 데이터베이스에서 수집해 6,218종의 약물 가상 라이브러리를 구축했다. 실험으로 이 약물들을 모두 검증하기에는 시간과 비용이 많이 소요되기 때문에 바이러스 치료제로 가능성이 있는 약물만 신속하게 선별할 수 있는 컴퓨터 기반 가상 스크리닝 기술을 도입했다.
기존의 도킹 시뮬레이션 기반의 가상 스크리닝 기술은 높은 위양성률(false positive rate)로 인해 유효물질 도출 비율(hit rate)이 매우 낮은 것이 문제점인 상황이었다. 연구팀은 구조 유사도 분석 모듈과 상호작용 유사도 분석 모듈을 도킹 전후에 도입하여 가상 스크리닝의 정확도를 높이는 데 성공했다. 이번 연구를 통해 개발된 가상 스크리닝 기술은 단백질-약물 복합체 구조 정보를 이용하여 다양한 후보 약물을 빠르고 정확하게 스크리닝할 수 있는 것이 특징이다.
연구팀은 또한 바이러스 치료제로 주로 사용되는 핵산 유사체(nucleotide analogues) 기반 전구약물(prodrug)의 활성형 구조를 자동으로 생성하는 알고리즘을 개발했다. 전구약물은 그 자체로는 약효가 없고 체내 대사를 통해 활성형 구조로 변환되어야만 약효를 나타낸다. 따라서 전구약물은 활성형으로 구조변환 후, 도킹 시뮬레이션을 수행하는 것이 중요하다. 연구팀은 렘데시비르를 포함한 여러 핵산유사체 기반 전구약물들의 활성형 구조를 자동으로 생성하는 데 성공하였고, 도킹 시뮬레이션의 정확도를 향상시킬 수 있었다.
연구팀은 가상 스크리닝 플랫폼으로 사스-코로나바이러스-2(SARS-CoV-2)의 복제와 증식에 필수적인 역할을 하는 단백질 가수분해 효소(3CL hydrolase, Mpro)와 RNA 중합효소(RNA-dependent RNA polymerase, RdRp)를 저해할 수 있는 후보 화합물을 15종과 23종으로 각각 선별했다.
그 후, 가상 스크리닝으로 선별된 38종의 약물에 대해 한국파스퇴르연구소의 생물안전 3등급(BSL-3) 실험실에서 세포 이미지 기반 항바이러스 활성 분석 플랫폼을 활용해 약효를 검증했다.
먼저 사스-코로나바이러스-2를 감염시킨 원숭이 신장세포(Vero cell)를 이용한 시험관 내(in vitro) 실험을 수행한 결과, 38종의 약물 중 7종의 약물에서 항바이러스 활성이 확인됐다.
또한, 검증된 7종의 약물에 대해 인간 폐 세포(Calu-3 cell)에서 추가적인 검증 실험을 수행했고, 3종의 약물에서 항바이러스 활성이 확인됐다. 후보 약물에는 암 및 특발성 폐섬유증(idiopathic pulmonary fibrosis)으로 임상이 진행 중인 오미팔리십(omipalisib), 암 및 조로증(progeria)으로 임상이 진행 중인 티피파닙(tipifarnib), 식물 추출물로써 항암제로 임상이 진행 중인 에모딘(emodin)이 있다. 특히 오미팔리십은 현재 코로나19 표준 치료제인 렘데시비르 대비 항바이러스 활성이 약 200배 이상 높은 것으로 확인됐고, 티피파닙은 렘데시비르와 유사한 수준으로 항바이러스 활성이 확인됐다.
세포 수준에서 항바이러스 효과가 확인된 약물은 바이러스 감염 동물모델을 이용한 전임상시험이 필요하다. 이에 연구팀은 과기정통부의 코로나 치료제 전임상 지원사업을 통해 후보 약물 중 하나의 약물에 대해 약효를 평가했다. 그러나 이 과정에서 동물에 대한 약물 독성이 나타났다. 약물의 독성을 최소화하면서 치료 유효 농도에 도달할 수 있는 최적의 약물 농도를 찾기 위해 추가적인 전임상시험을 진행할 예정이다. 또한, 나머지 후보 약물들에 대해서도 전임상시험을 계획 중이다.
연구팀 관계자는 이번 연구를 통해 예측 성능이 우수한 약물 가상 스크리닝 플랫폼을 구축했고, 이를 통해 코로나19 치료제로 유망한 후보물질을 단기간에 발견할 수 있었다고 설명했다.
이상엽 특훈교수는 “이번 연구를 통해 신종 바이러스 출현 시 신속하게 대응할 수 있는 기반 기술을 마련했다는 데에 의의가 있으며, 이를 통해 향후 코로나바이러스 계열의 유사한 바이러스나 신종 바이러스 출현 시에도 적용할 수 있는 기술을 개발하고자 한다”라고 밝혔다.
한편 이번 연구는 과기정통부가 지원하는 KAIST 코로나대응 과학기술 뉴딜사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2021.07.08 조회수 17523
약물 가상 스크리닝 기술로 코로나19 치료제 후보 발굴
우리 대학 생명화학공학과 이상엽 특훈교수(연구부총장)와 한국파스퇴르연구소 김승택 박사 공동연구팀이 ‘약물 가상 스크리닝 기술을 이용한 코로나19 치료제 개발’에 성공했다고 8일 밝혔다.
이번 연구 결과는 국제 학술지인 ‘미국국립과학원회보(PNAS)'에 7월 7일 字 온라인 게재됐다.
※ 논문명 : Drugs repurposed for COVID-19 by virtual screening of 6,218 drugs and cell-based assay
※ 저자 정보 : 이상엽(한국과학기술원, 교신저자), 김승택(한국파스퇴르연구소, 교신저자), 장우대(한국과학기술원, 제1저자), 전상은(한국파스퇴르연구소, 제2저자), 포함 총 4명
코로나바이러스감염증-19(이하 코로나19)는 글로벌 팬데믹으로 전개되고 있으며 현재 인류 보건을 심각하게 위협하는 상황이다. 코로나19 치료 목적으로 미국식품의약국(FDA)에서 정식 승인을 받은 렘데시비르(상품명 베클러리)가 현재 임상에서 사용 중이지만, 사망률은 감소시키지 못하고 회복 기간을 5일 정도 단축함으로써 치료 효과가 기대에 미치지 못하는 것으로 알려졌다. 또한 렘데시비르는 정맥 주사제여서 의료기관에서 입원을 통해 수일 동안 투여받아야 하므로 팬데믹 상황에 적합하지 않은 약물이다. 따라서 코로나19로 인한 사망률을 획기적으로 감소시키고, 치료 기간을 단축시키는 경구용 치료제 개발이 시급한 상황이었다.
이에 이상엽 특훈교수와 한국파스퇴르연구소 김승택 박사 공동연구팀은 약물 가상 스크리닝 기술을 이용한 약물 재창출 전략으로 코로나19 치료제 개발 연구를 수행했다.
연구팀은 팬데믹 상황에 대응한 신속한 치료제 개발을 위해 가상 스크리닝 기술을 이용한 약물 재창출 전략을 수립했다. 약물 재창출은 이미 안전성이 검증된 FDA 승인 약물 또는 임상 진행 중인 약물을 대상으로 새로운 적응증을 찾는 방식이다. 이 전략은 신약 개발 과정에 소요되는 시간을 단축시킬 수 있어 코로나19와 같은 팬데믹 상황에 적합한 신약 개발 전략이다.
우리 대학 생명화학공학과 장우대 박사는 우선 FDA 승인 약물 또는 임상 진행 중인 약물을 데이터베이스에서 수집해 6,218종의 약물 가상 라이브러리를 구축했다. 실험으로 이 약물들을 모두 검증하기에는 시간과 비용이 많이 소요되기 때문에 바이러스 치료제로 가능성이 있는 약물만 신속하게 선별할 수 있는 컴퓨터 기반 가상 스크리닝 기술을 도입했다.
기존의 도킹 시뮬레이션 기반의 가상 스크리닝 기술은 높은 위양성률(false positive rate)로 인해 유효물질 도출 비율(hit rate)이 매우 낮은 것이 문제점인 상황이었다. 연구팀은 구조 유사도 분석 모듈과 상호작용 유사도 분석 모듈을 도킹 전후에 도입하여 가상 스크리닝의 정확도를 높이는 데 성공했다. 이번 연구를 통해 개발된 가상 스크리닝 기술은 단백질-약물 복합체 구조 정보를 이용하여 다양한 후보 약물을 빠르고 정확하게 스크리닝할 수 있는 것이 특징이다.
연구팀은 또한 바이러스 치료제로 주로 사용되는 핵산 유사체(nucleotide analogues) 기반 전구약물(prodrug)의 활성형 구조를 자동으로 생성하는 알고리즘을 개발했다. 전구약물은 그 자체로는 약효가 없고 체내 대사를 통해 활성형 구조로 변환되어야만 약효를 나타낸다. 따라서 전구약물은 활성형으로 구조변환 후, 도킹 시뮬레이션을 수행하는 것이 중요하다. 연구팀은 렘데시비르를 포함한 여러 핵산유사체 기반 전구약물들의 활성형 구조를 자동으로 생성하는 데 성공하였고, 도킹 시뮬레이션의 정확도를 향상시킬 수 있었다.
연구팀은 가상 스크리닝 플랫폼으로 사스-코로나바이러스-2(SARS-CoV-2)의 복제와 증식에 필수적인 역할을 하는 단백질 가수분해 효소(3CL hydrolase, Mpro)와 RNA 중합효소(RNA-dependent RNA polymerase, RdRp)를 저해할 수 있는 후보 화합물을 15종과 23종으로 각각 선별했다.
그 후, 가상 스크리닝으로 선별된 38종의 약물에 대해 한국파스퇴르연구소의 생물안전 3등급(BSL-3) 실험실에서 세포 이미지 기반 항바이러스 활성 분석 플랫폼을 활용해 약효를 검증했다.
먼저 사스-코로나바이러스-2를 감염시킨 원숭이 신장세포(Vero cell)를 이용한 시험관 내(in vitro) 실험을 수행한 결과, 38종의 약물 중 7종의 약물에서 항바이러스 활성이 확인됐다.
또한, 검증된 7종의 약물에 대해 인간 폐 세포(Calu-3 cell)에서 추가적인 검증 실험을 수행했고, 3종의 약물에서 항바이러스 활성이 확인됐다. 후보 약물에는 암 및 특발성 폐섬유증(idiopathic pulmonary fibrosis)으로 임상이 진행 중인 오미팔리십(omipalisib), 암 및 조로증(progeria)으로 임상이 진행 중인 티피파닙(tipifarnib), 식물 추출물로써 항암제로 임상이 진행 중인 에모딘(emodin)이 있다. 특히 오미팔리십은 현재 코로나19 표준 치료제인 렘데시비르 대비 항바이러스 활성이 약 200배 이상 높은 것으로 확인됐고, 티피파닙은 렘데시비르와 유사한 수준으로 항바이러스 활성이 확인됐다.
세포 수준에서 항바이러스 효과가 확인된 약물은 바이러스 감염 동물모델을 이용한 전임상시험이 필요하다. 이에 연구팀은 과기정통부의 코로나 치료제 전임상 지원사업을 통해 후보 약물 중 하나의 약물에 대해 약효를 평가했다. 그러나 이 과정에서 동물에 대한 약물 독성이 나타났다. 약물의 독성을 최소화하면서 치료 유효 농도에 도달할 수 있는 최적의 약물 농도를 찾기 위해 추가적인 전임상시험을 진행할 예정이다. 또한, 나머지 후보 약물들에 대해서도 전임상시험을 계획 중이다.
연구팀 관계자는 이번 연구를 통해 예측 성능이 우수한 약물 가상 스크리닝 플랫폼을 구축했고, 이를 통해 코로나19 치료제로 유망한 후보물질을 단기간에 발견할 수 있었다고 설명했다.
이상엽 특훈교수는 “이번 연구를 통해 신종 바이러스 출현 시 신속하게 대응할 수 있는 기반 기술을 마련했다는 데에 의의가 있으며, 이를 통해 향후 코로나바이러스 계열의 유사한 바이러스나 신종 바이러스 출현 시에도 적용할 수 있는 기술을 개발하고자 한다”라고 밝혔다.
한편 이번 연구는 과기정통부가 지원하는 KAIST 코로나대응 과학기술 뉴딜사업과 바이오·의료기술개발사업의 지원을 받아 수행됐다.
2021.07.08 조회수 17523 -
 개인 맞춤형 암 치료에 한 발짝 다가서
우리 연구진이 급성골수성백혈병(Acute myeloid leukemia)과 골수이형성증후군(Myelodysplastic syndromes) 치료에 사용되는 항암 화학 치료제 중 하나인 데시타빈(decitabine)의 인체 내 작용 메커니즘을 규명해 항암제 효과가 있는 환자와 없는 환자를 구별해 낼 수 있는 유전자 발굴에 성공했다.
이번 연구를 통해 환자별로 적합한 치료를 받을 수 있게 되면 환자들이 치료에 드는 경제적 지출과 시간적 소비 또한 확연하게 줄일 수 있을 것으로 기대된다.
우리 대학 생명화학공학과 김유식 교수와 서울대병원 혈액암센터 홍준식 교수 공동 연구팀이 항암 화학치료에서 작용하는 주요 인자를 찾아냈다고 7일 밝혔다.
생명화학공학과 박사과정에 재학 중인 구용석 학생, 서울대병원 박주환 연구원 그리고 우리 대학 조령은 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `미국국립과학원회보(PNAS)' 3월 30일 字에 게재됐다. (논문명: Noncanonical immune response to the inhibition of DNA methylation via stabilization of endogenous retrovirus dsRNAs)
데시타빈과 같은 DNA 탈메틸화제(DNA demethylating agent)는 DNA 복제과정에 참여하고 DNA상에 존재하는 메틸기(-CH₃)를 제거해 유전자 발현을 조절한다. 특히 암세포에는 일반 세포보다 많은 양의 DNA가 메틸화돼 있으며, 이는 DNA에서 RNA를 생성하는 전사 과정을 억제하는 역할을 한다. 세포에 탈메틸화제 처리를 하면 DNA상에 메틸기가 제거돼 세포 내에 수많은 종류의 RNA들이 생성된다.
이렇게 데시타빈에 의해 조절되는 RNA 중에는 이중나선 RNA (double-stranded RNA, 이하 dsRNA)가 있다. 원래 dsRNA는 바이러스에 감염된 세포에서 많이 생산되며, 인간 세포는 바이러스에서 유래된 dsRNA를 외부 물질로 인지해 면역반응을 일으킨다.
특이하게도 dsRNA를 인지하는 인간의 선천성 면역반응 시스템은 핵산 서열 정보를 무시한 채 dsRNA의 길이나 말단 형태와 같은 구조적 특징을 이용해 dsRNA와 반응한다. 이와 같은 특징 때문에 꼭 바이러스에서 유래된 dsRNA가 아니라 체내에서 생성된 dsRNA 또한 외부 물질로 오인돼 비정상적인 면역반응을 일으킬 수 있다. 암 치료에서는 DNA 탈메틸화제 처리로 dsRNA의 발현량을 증가시키고 이는 dsRNA에 의한 면역 활성으로 이어져 암세포만의 세포사멸이 일어나게 된다.
연구팀은 이러한 데시타빈에 의한 dsRNA 발현증가 그리고 dsRNA에 의한 세포사멸을 조절하는 유전자를 연구했다. 특히, DNA 탈메틸화제를 투여받은 환자 중 많은 수의 환자가 약물의 효과를 보지 못한다는 점에 착안해 dsRNA와 상호작용하는 다양한 dsRNA 결합 단백질을 분석했다.
그 결과로 dsRNA와 직접 결합해 dsRNA의 안정성을 조절하는 단백질인 `스타우펜1(이하 Staufen1)'이 데시타빈에 의한 세포 반응에 중요한 기능을 한다는 것을 최초로 규명했다. Staufen1의 발현이 억제된 세포에서는 dsRNA가 빠르게 제거돼 하위 면역반응이 일어나지 않았으며 암세포의 사멸도 관찰되지 않았다.
연구팀은 데시타빈 뿐만 아니라 아자시티딘(azacitidine)과 같은 DNA 탈메틸화제를 투여받은 급성골수성백혈병과 골수이형성증후군 환자 46명의 골수추출액에서 Staufen1 유전자의 발현양상을 분석했고, 그 결과 약물의 효과를 보지 못한 환자에게서는 Staufen1의 발현이 유의미하게 감소해 있다는 것을 확인했다. 또한, Staufen1의 발현이 낮은 환자는 생존율(overall survival)과 무진행 생존율(progression-free survival)이 모두 낮아 환자의 예후가 좋지 않다는 것을 확인했다.
생명화학공학과 김유식 교수는 "이번 연구에서는 단순 데시타빈 항암제의 작용기전 규명을 넘어서 실제 데시타빈을 투여받은 환자의 검체에서도 그 효과를 검증했다ˮ면서 "추후 이번에 찾은 유전자의 바이오마커화를 통해 데시타빈과 아자시티딘과 같은 DNA 탈메틸화제의 효과를 예측할 수 있어 효과적인 맞춤형 암 치료전략을 마련하는데 유용할 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원을 받아 수행됐다.
2021.04.07 조회수 80222
개인 맞춤형 암 치료에 한 발짝 다가서
우리 연구진이 급성골수성백혈병(Acute myeloid leukemia)과 골수이형성증후군(Myelodysplastic syndromes) 치료에 사용되는 항암 화학 치료제 중 하나인 데시타빈(decitabine)의 인체 내 작용 메커니즘을 규명해 항암제 효과가 있는 환자와 없는 환자를 구별해 낼 수 있는 유전자 발굴에 성공했다.
이번 연구를 통해 환자별로 적합한 치료를 받을 수 있게 되면 환자들이 치료에 드는 경제적 지출과 시간적 소비 또한 확연하게 줄일 수 있을 것으로 기대된다.
우리 대학 생명화학공학과 김유식 교수와 서울대병원 혈액암센터 홍준식 교수 공동 연구팀이 항암 화학치료에서 작용하는 주요 인자를 찾아냈다고 7일 밝혔다.
생명화학공학과 박사과정에 재학 중인 구용석 학생, 서울대병원 박주환 연구원 그리고 우리 대학 조령은 학생이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `미국국립과학원회보(PNAS)' 3월 30일 字에 게재됐다. (논문명: Noncanonical immune response to the inhibition of DNA methylation via stabilization of endogenous retrovirus dsRNAs)
데시타빈과 같은 DNA 탈메틸화제(DNA demethylating agent)는 DNA 복제과정에 참여하고 DNA상에 존재하는 메틸기(-CH₃)를 제거해 유전자 발현을 조절한다. 특히 암세포에는 일반 세포보다 많은 양의 DNA가 메틸화돼 있으며, 이는 DNA에서 RNA를 생성하는 전사 과정을 억제하는 역할을 한다. 세포에 탈메틸화제 처리를 하면 DNA상에 메틸기가 제거돼 세포 내에 수많은 종류의 RNA들이 생성된다.
이렇게 데시타빈에 의해 조절되는 RNA 중에는 이중나선 RNA (double-stranded RNA, 이하 dsRNA)가 있다. 원래 dsRNA는 바이러스에 감염된 세포에서 많이 생산되며, 인간 세포는 바이러스에서 유래된 dsRNA를 외부 물질로 인지해 면역반응을 일으킨다.
특이하게도 dsRNA를 인지하는 인간의 선천성 면역반응 시스템은 핵산 서열 정보를 무시한 채 dsRNA의 길이나 말단 형태와 같은 구조적 특징을 이용해 dsRNA와 반응한다. 이와 같은 특징 때문에 꼭 바이러스에서 유래된 dsRNA가 아니라 체내에서 생성된 dsRNA 또한 외부 물질로 오인돼 비정상적인 면역반응을 일으킬 수 있다. 암 치료에서는 DNA 탈메틸화제 처리로 dsRNA의 발현량을 증가시키고 이는 dsRNA에 의한 면역 활성으로 이어져 암세포만의 세포사멸이 일어나게 된다.
연구팀은 이러한 데시타빈에 의한 dsRNA 발현증가 그리고 dsRNA에 의한 세포사멸을 조절하는 유전자를 연구했다. 특히, DNA 탈메틸화제를 투여받은 환자 중 많은 수의 환자가 약물의 효과를 보지 못한다는 점에 착안해 dsRNA와 상호작용하는 다양한 dsRNA 결합 단백질을 분석했다.
그 결과로 dsRNA와 직접 결합해 dsRNA의 안정성을 조절하는 단백질인 `스타우펜1(이하 Staufen1)'이 데시타빈에 의한 세포 반응에 중요한 기능을 한다는 것을 최초로 규명했다. Staufen1의 발현이 억제된 세포에서는 dsRNA가 빠르게 제거돼 하위 면역반응이 일어나지 않았으며 암세포의 사멸도 관찰되지 않았다.
연구팀은 데시타빈 뿐만 아니라 아자시티딘(azacitidine)과 같은 DNA 탈메틸화제를 투여받은 급성골수성백혈병과 골수이형성증후군 환자 46명의 골수추출액에서 Staufen1 유전자의 발현양상을 분석했고, 그 결과 약물의 효과를 보지 못한 환자에게서는 Staufen1의 발현이 유의미하게 감소해 있다는 것을 확인했다. 또한, Staufen1의 발현이 낮은 환자는 생존율(overall survival)과 무진행 생존율(progression-free survival)이 모두 낮아 환자의 예후가 좋지 않다는 것을 확인했다.
생명화학공학과 김유식 교수는 "이번 연구에서는 단순 데시타빈 항암제의 작용기전 규명을 넘어서 실제 데시타빈을 투여받은 환자의 검체에서도 그 효과를 검증했다ˮ면서 "추후 이번에 찾은 유전자의 바이오마커화를 통해 데시타빈과 아자시티딘과 같은 DNA 탈메틸화제의 효과를 예측할 수 있어 효과적인 맞춤형 암 치료전략을 마련하는데 유용할 것ˮ 이라고 말했다.
한편 이번 연구는 한국연구재단 신진연구자지원사업과 KAIST 미래형 시스템 헬스케어 연구개발사업의 지원을 받아 수행됐다.
2021.04.07 조회수 80222 -
 탄소중립 인공 광합성 기술 개발
우리 대학 생명과학과 조병관 교수 연구팀이 기후변화의 주된 요인인 C1 가스(이산화탄소, 일산화탄소 등 탄소 1개로 구성된 가스)를 고부가가치 바이오 화학물질로 전환하는 기술을 개발했다고 9일 밝혔다.
조 교수 연구팀은 광 나노입자가 빛을 받으면 내놓는 전자를 미생물이 에너지원으로 이용할 수 있도록 고효율 광 나노입자가 표면에 부착된 미생물-광 나노입자 인공광합성 시스템을 개발했다. 이 기술은 빛을 유일한 에너지원으로 활용해 미생물이 C1 가스를 다양한 바이오 화학물질로 전환하는 친환경 C1 가스 리파이너리 기술로 정부가 선언한 2050 탄소중립 실현을 위한 다양한 응용 가능성을 제시한다.
생명과학과 진상락 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 국제 학술지 `미국국립과학원회보(Proceedings of National Academy of Science, PNAS)'에 2월 23일 字 온라인판에 게재됐다.(논문명: Acetogenic bacteria utilize light-driven electrons as an energy source for autotrophic growth)
아세토젠 미생물은 우드-융달 대사회로를 통해 C1 가스를 아세트산으로 전환할 수 있다. 이에 C1 가스로부터 바이오 화학물질 생산을 위한 바이오 촉매로 활용 가능성이 커 탄소 포집 및 활용 기술로 많은 주목을 받고 있다.
아세토젠 미생물은 C1 가스 대사를 위한 환원 에너지를 당이나 수소를 분해해 얻는다. 당이나 수소를 대체하기 위해 나노입자 크기의 개별 광전극 역할을 하는 광 나노입자를 미생물 표면에 부착시켜 빛에너지를 미생물로 전달시키면 당이나 수소 없이도 C1 가스를 활용할 수 있다.
기존기술은 광 나노입자를 생합성해 세포 표면에 부착시키는 방법으로 광 나노입자의 구조와 크기를 조절하기 어려워 C1 가스 대사 효율을 높이는 데 한계가 있었다. 이는 구조와 크기에 따라 광전도효과의 성능에 차이가 생기는 광 나노입자의 독특한 특성 때문이다.
이와 같은 한계를 극복하기 위해 연구팀은 구조와 크기가 균일하고 우수한 광전도효과를 나타내는 고효율 광 나노입자를 화학적 방법으로 합성하고, 산업적으로 활용 가능한 아세토젠 미생물 중 하나인 `클로스트리디움 오토에타노게놈(Clostridium autoethanogenum)'의 표면에 부착시켰다.
연구팀은 광 나노입자를 부착한 미생물이 C1 가스로부터 아세트산을 생산할 수 있음을 입증해 빛을 이용한 친환경 인공광합성 시스템을 구축하고 구축된 인공광합성 시스템 미생물의 전사체 분석(세포 내 모든 RNA를 분석해 유전자 발현 유무를 규명하는 기술)을 통해 광 나노입자로부터 생성된 전자가 미생물 내로 전달되기 위한 전자수용체를 규명했다.
연구를 주도한 조병관 교수는 "C1 가스 고정과정에서 사용되는 당 또는 수소를 친환경 빛에너지로 대체할 수 있고, 미생물 기반의 생합성 광 나노입자를 활용한 기존 인공광합성 시스템의 한계를 극복했다ˮ며 "고효율 광 나노입자를 사용해 인공광합성 효율을 증대시킬 수 있고, 광 나노입자로부터 생성된 전자를 효율적으로 수용할 수 있는 인공미생물 개발연구에 실마리를 제공했다ˮ 고 의의를 설명했다.
한편 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 C1 가스 리파이너리 사업단 및 지능형바이오시스템 설계 및 합성연구단(글로벌프론티어사업)의 지원을 받아 수행됐다.
2021.03.09 조회수 101044
탄소중립 인공 광합성 기술 개발
우리 대학 생명과학과 조병관 교수 연구팀이 기후변화의 주된 요인인 C1 가스(이산화탄소, 일산화탄소 등 탄소 1개로 구성된 가스)를 고부가가치 바이오 화학물질로 전환하는 기술을 개발했다고 9일 밝혔다.
조 교수 연구팀은 광 나노입자가 빛을 받으면 내놓는 전자를 미생물이 에너지원으로 이용할 수 있도록 고효율 광 나노입자가 표면에 부착된 미생물-광 나노입자 인공광합성 시스템을 개발했다. 이 기술은 빛을 유일한 에너지원으로 활용해 미생물이 C1 가스를 다양한 바이오 화학물질로 전환하는 친환경 C1 가스 리파이너리 기술로 정부가 선언한 2050 탄소중립 실현을 위한 다양한 응용 가능성을 제시한다.
생명과학과 진상락 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 국제 학술지 `미국국립과학원회보(Proceedings of National Academy of Science, PNAS)'에 2월 23일 字 온라인판에 게재됐다.(논문명: Acetogenic bacteria utilize light-driven electrons as an energy source for autotrophic growth)
아세토젠 미생물은 우드-융달 대사회로를 통해 C1 가스를 아세트산으로 전환할 수 있다. 이에 C1 가스로부터 바이오 화학물질 생산을 위한 바이오 촉매로 활용 가능성이 커 탄소 포집 및 활용 기술로 많은 주목을 받고 있다.
아세토젠 미생물은 C1 가스 대사를 위한 환원 에너지를 당이나 수소를 분해해 얻는다. 당이나 수소를 대체하기 위해 나노입자 크기의 개별 광전극 역할을 하는 광 나노입자를 미생물 표면에 부착시켜 빛에너지를 미생물로 전달시키면 당이나 수소 없이도 C1 가스를 활용할 수 있다.
기존기술은 광 나노입자를 생합성해 세포 표면에 부착시키는 방법으로 광 나노입자의 구조와 크기를 조절하기 어려워 C1 가스 대사 효율을 높이는 데 한계가 있었다. 이는 구조와 크기에 따라 광전도효과의 성능에 차이가 생기는 광 나노입자의 독특한 특성 때문이다.
이와 같은 한계를 극복하기 위해 연구팀은 구조와 크기가 균일하고 우수한 광전도효과를 나타내는 고효율 광 나노입자를 화학적 방법으로 합성하고, 산업적으로 활용 가능한 아세토젠 미생물 중 하나인 `클로스트리디움 오토에타노게놈(Clostridium autoethanogenum)'의 표면에 부착시켰다.
연구팀은 광 나노입자를 부착한 미생물이 C1 가스로부터 아세트산을 생산할 수 있음을 입증해 빛을 이용한 친환경 인공광합성 시스템을 구축하고 구축된 인공광합성 시스템 미생물의 전사체 분석(세포 내 모든 RNA를 분석해 유전자 발현 유무를 규명하는 기술)을 통해 광 나노입자로부터 생성된 전자가 미생물 내로 전달되기 위한 전자수용체를 규명했다.
연구를 주도한 조병관 교수는 "C1 가스 고정과정에서 사용되는 당 또는 수소를 친환경 빛에너지로 대체할 수 있고, 미생물 기반의 생합성 광 나노입자를 활용한 기존 인공광합성 시스템의 한계를 극복했다ˮ며 "고효율 광 나노입자를 사용해 인공광합성 효율을 증대시킬 수 있고, 광 나노입자로부터 생성된 전자를 효율적으로 수용할 수 있는 인공미생물 개발연구에 실마리를 제공했다ˮ 고 의의를 설명했다.
한편 이번 연구는 과학기술정보통신부와 한국연구재단이 추진하는 C1 가스 리파이너리 사업단 및 지능형바이오시스템 설계 및 합성연구단(글로벌프론티어사업)의 지원을 받아 수행됐다.
2021.03.09 조회수 101044 -
 인공지능 기술을 이용한 유전자 전사인자 예측 시스템 개발
우리 대학 생명화학공학과 이상엽 특훈교수와 미국 캘리포니아대학교 샌디에이고캠퍼스(UCSD) 생명공학과 버나드 팔슨(Bernhard Palsson) 교수 공동연구팀이 인공지능을 이용해 단백질 서열로부터 *전사인자를 예측하는 시스템인 '딥티팩터(DeepTFactor)'를 개발했다고 29일 밝혔다. 이번 연구는 국제학술지인 '미국국립과학원회보(PNAS)'에 12월 28일 字 게재됐다. (논문명: DeepTFactor: A deep learning-based tool for the prediction of transcription factors)
※ 전사인자 (transcription factor) : 유전자의 전사(유전 정보를 복사하는 과정)를 조절하는 단백질. 특정 DNA 서열에 특이적으로 결합해 유전자의 전사를 조절한다.
※ 저자 정보 : 김기배(한국과학기술원, 제1 저자), 예 가오(Ye Gao) (UCSD, 제2 저자), 버나드 팔슨(Bernhard Palsson) (UCSD, 제3 저자), 이상엽(교신저자) 포함 총 4명
전사인자는 특정한 DNA 서열에 특이적으로 결합해 유전자의 전사(유전 정보를 복사하는 과정)를 조절하는 단백질이다. 전사인자로 인한 유전자 전사를 분석함으로써 유기체가 유전적 또는 환경적 변화에 어떻게 반응해 유전자의 발현을 제어하는지 이해할 수 있다. 이러한 점에서 유기체의 전사인자를 찾는 것은 유기체의 전사 조절 시스템 분석을 위한 첫 단계라고 할 수 있다.
지금까지 새로운 전사인자를 찾기 위해서는 이미 알려진 전사인자와의 상동성(유사한 성질)을 분석하거나, 기계학습(머신러닝)과 같은 데이터 기반의 접근 방식을 이용했다. 기존의 기계학습 모델을 이용하기 위해서는 분자의 물리 화학적 특성을 계산하거나, 생물학적 서열의 상동성을 분석하는 등, 해결하고자 하는 문제에 대한 전문 지식에 의존해 모델의 입력값으로 사용할 특징을 찾아내는 과정이 필요하다.
한편, 심층 학습(딥러닝)은 문제 해결을 위한 잠재적인 특징을 내재적으로 학습할 수 있기에 최근 다양한 생물학 분야에서 활용되고 있다. 하지만, 심층 학습을 이용한 예측 시스템의 경우 시스템 내부의 복잡한 연산 때문에 추론 과정을 직접 확인할 수 없는 `블랙박스(black box)'라는 특징을 가지고 있다.
공동연구팀은 심층 학습 기법을 이용해 주어진 단백질 서열이 전사인자인지 예측할 수 있는 시스템인 딥티팩터(DeepTFactor)를 개발했다. 딥티팩터는 단백질 서열로부터 전사인자를 예측하기 위해 세 개의 병렬적인 합성곱 신경망(convolutional neural network)을 이용한다. 공동연구팀은 딥티팩터를 이용해 대장균(Escherichia coli K-12 MG1655)의 전사인자 332개를 예측했으며, 그중 3개의 전사인자의 게놈 전체 결합 위치(genome-wide binding site)를 실험으로 확인함으로써 딥티팩터의 성능을 검증했다.
공동연구팀은 나아가 딥티팩터의 추론 과정을 이해하기 위해 특징 지도 (saliency map) 기반의 심층 학습 모델 해석 방법론을 사용했다. 이를 통해 딥티팩터의 학습 과정에서 전사인자의 DNA의 결합 영역에 대한 정보가 명시적으로 주어지지 않았지만, 내재적으로 이를 학습해 예측에 활용한다는 사실을 확인했다.
연구팀 관계자에 따르면, 특정 생물군의 단백질 서열만을 위해 개발됐던 이전 예측 방법론들과 달리, 딥티팩터는 모든 생물군의 단백질 서열에서 우수한 성능을 보여 다양한 유기체의 전사 시스템 분석에 활용 가능할 것으로 기대된다.
이상엽 특훈교수는 “이번 연구에서 개발한 딥티팩터를 이용해서 새롭게 발견되는 단백질 서열과 아직 특성화되지 않은 수많은 단백질 서열을 높은 처리 능력으로 분석할 수 있게 됐다”며 “이는 유기체의 전자 조절 네트워크 분석을 위한 기초 기술로써 활용 가능할 것”이라고 밝혔다.
한편, 이번 연구는 과기정통부가 지원하는 기후변화대응기술개발사업의 바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제 지원을 받아 수행됐다.
2020.12.30 조회수 58138
인공지능 기술을 이용한 유전자 전사인자 예측 시스템 개발
우리 대학 생명화학공학과 이상엽 특훈교수와 미국 캘리포니아대학교 샌디에이고캠퍼스(UCSD) 생명공학과 버나드 팔슨(Bernhard Palsson) 교수 공동연구팀이 인공지능을 이용해 단백질 서열로부터 *전사인자를 예측하는 시스템인 '딥티팩터(DeepTFactor)'를 개발했다고 29일 밝혔다. 이번 연구는 국제학술지인 '미국국립과학원회보(PNAS)'에 12월 28일 字 게재됐다. (논문명: DeepTFactor: A deep learning-based tool for the prediction of transcription factors)
※ 전사인자 (transcription factor) : 유전자의 전사(유전 정보를 복사하는 과정)를 조절하는 단백질. 특정 DNA 서열에 특이적으로 결합해 유전자의 전사를 조절한다.
※ 저자 정보 : 김기배(한국과학기술원, 제1 저자), 예 가오(Ye Gao) (UCSD, 제2 저자), 버나드 팔슨(Bernhard Palsson) (UCSD, 제3 저자), 이상엽(교신저자) 포함 총 4명
전사인자는 특정한 DNA 서열에 특이적으로 결합해 유전자의 전사(유전 정보를 복사하는 과정)를 조절하는 단백질이다. 전사인자로 인한 유전자 전사를 분석함으로써 유기체가 유전적 또는 환경적 변화에 어떻게 반응해 유전자의 발현을 제어하는지 이해할 수 있다. 이러한 점에서 유기체의 전사인자를 찾는 것은 유기체의 전사 조절 시스템 분석을 위한 첫 단계라고 할 수 있다.
지금까지 새로운 전사인자를 찾기 위해서는 이미 알려진 전사인자와의 상동성(유사한 성질)을 분석하거나, 기계학습(머신러닝)과 같은 데이터 기반의 접근 방식을 이용했다. 기존의 기계학습 모델을 이용하기 위해서는 분자의 물리 화학적 특성을 계산하거나, 생물학적 서열의 상동성을 분석하는 등, 해결하고자 하는 문제에 대한 전문 지식에 의존해 모델의 입력값으로 사용할 특징을 찾아내는 과정이 필요하다.
한편, 심층 학습(딥러닝)은 문제 해결을 위한 잠재적인 특징을 내재적으로 학습할 수 있기에 최근 다양한 생물학 분야에서 활용되고 있다. 하지만, 심층 학습을 이용한 예측 시스템의 경우 시스템 내부의 복잡한 연산 때문에 추론 과정을 직접 확인할 수 없는 `블랙박스(black box)'라는 특징을 가지고 있다.
공동연구팀은 심층 학습 기법을 이용해 주어진 단백질 서열이 전사인자인지 예측할 수 있는 시스템인 딥티팩터(DeepTFactor)를 개발했다. 딥티팩터는 단백질 서열로부터 전사인자를 예측하기 위해 세 개의 병렬적인 합성곱 신경망(convolutional neural network)을 이용한다. 공동연구팀은 딥티팩터를 이용해 대장균(Escherichia coli K-12 MG1655)의 전사인자 332개를 예측했으며, 그중 3개의 전사인자의 게놈 전체 결합 위치(genome-wide binding site)를 실험으로 확인함으로써 딥티팩터의 성능을 검증했다.
공동연구팀은 나아가 딥티팩터의 추론 과정을 이해하기 위해 특징 지도 (saliency map) 기반의 심층 학습 모델 해석 방법론을 사용했다. 이를 통해 딥티팩터의 학습 과정에서 전사인자의 DNA의 결합 영역에 대한 정보가 명시적으로 주어지지 않았지만, 내재적으로 이를 학습해 예측에 활용한다는 사실을 확인했다.
연구팀 관계자에 따르면, 특정 생물군의 단백질 서열만을 위해 개발됐던 이전 예측 방법론들과 달리, 딥티팩터는 모든 생물군의 단백질 서열에서 우수한 성능을 보여 다양한 유기체의 전사 시스템 분석에 활용 가능할 것으로 기대된다.
이상엽 특훈교수는 “이번 연구에서 개발한 딥티팩터를 이용해서 새롭게 발견되는 단백질 서열과 아직 특성화되지 않은 수많은 단백질 서열을 높은 처리 능력으로 분석할 수 있게 됐다”며 “이는 유기체의 전자 조절 네트워크 분석을 위한 기초 기술로써 활용 가능할 것”이라고 밝혔다.
한편, 이번 연구는 과기정통부가 지원하는 기후변화대응기술개발사업의 바이오리파이너리를 위한 시스템대사공학 원천기술개발 과제 지원을 받아 수행됐다.
2020.12.30 조회수 58138 -
 노화된 세포를 젊은 세포로 되돌리는 초기 원천기술 개발
우리 연구진이 노화된 세포를 젊은 세포로 되돌리는 역 노화 원천기술을 개발했다. 이를 활용하면 노화 현상을 막고 각종 노인성 질환을 사전 억제할 수 있는 치료제를 개발할 단서를 찾을 수 있을 것으로 기대된다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌리는 역 노화의 초기 원천기술을 개발했다고 26일 밝혔다.
조광현 교수팀의 이번 연구 결과는 ㈜아모레퍼시픽 기술연구원과의 산학 공동연구를 통해 최초로 개발된 노화 인공피부 모델에서 이 기술을 적용함으로써 입증하는 데 성공했다.
조 교수팀은 이번 연구를 위해 인간 진피 섬유아세포의 세포노화 신호전달 네트워크의 컴퓨터 모델을 개발한 후 시뮬레이션 분석을 통해 노화된 인간 진피 섬유아세포를 젊은 세포로 되돌리는데 필요한 핵심 인자를 찾아냈다. 이후 노화 인공피부 모델에서 핵심 인자를 조절함으로써 노화된 피부조직에서 감소된 콜라겐의 합성을 증가시키고 재생 능력을 회복시켜 젊은 피부조직의 특성을 보이게 하는 역 노화 기술을 개발했다.
연구팀 관계자는 이러한 역 노화 기술은 노화된 피부 등을 포함한 노화 현상 및 많은 노인성 질환의 발생을 사전에 억제할 수 있도록 근본적인 치료전략을 제시한 것으로 건강 수명을 오랫동안 유지하고 싶은 인류의 꿈을 실현하는데 한 걸음 다가선 결과라고 의미를 부여했다.
바이오및뇌공학과 안수균 박사과정 학생, 강준수 연구원, 이수범 연구원과 ㈜아모레퍼시픽의 바이오사이언스랩이 참여한 이번 연구 결과는 국제저명학술지인 `미국국립과학원회보(PNAS)'에 게재됐다.(논문명: Inhibition of 3-phosphoinositide-dependent protein kinase 1 (PDK1) can revert cellular senescence in human dermal fibroblasts)
현재 널리 연구되고 있는 회춘 전략은 이미 분화된 세포를 역분화시키는 4개의 `OSKM(Oct4, Sox2, Klf4, c-Myc) 야마나카 전사인자'를 일시적으로 발현시켜 후성유전학적 리모델링(epigenetic remodeling)을 일으킴으로써 노화된 세포를 젊은 상태로 되돌리는 부분적 역분화(partial reprogramming) 전략이다.
이 기술은 노화된 세포가 젊은 세포로 되돌아갈 수 있다는 것을 증명했지만 종양의 형성과 암의 진행을 유발하는 부작용이 생긴다. 따라서 이와 같은 부작용을 배제할 수 있는 정교한 제어 전략이 과학 난제로 남아있었다.
조 교수팀은 이러한 난제 해결을 위해 시스템생물학 연구 방법을 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌릴 수 있는 핵심 조절인자를 오래전부터 탐구하기 시작했다. 4년에 걸친 연구 끝에 단백질 합성, 세포의 성장 등을 조절하는 mTOR와 면역 물질 사이토카인의 생성에 관여하는 NF-kB를 동시에 제어하고 있는 상위 조절 인자인 `PDK1(3-phosphoinositide-dependent protein kinase 1)'을 찾아냈다.
연구팀은 PDK1을 억제함으로써 노화된 인간 진피 섬유아세포를 다시 정상적인 젊은 세포로 되돌릴 수 있음을 분자 세포실험 및 노화 인공피부 모델 실험을 통해 입증했다. 연구를 통해 노화된 인간 진피 섬유아세포에서 PDK1을 억제했을 때 세포노화 표지 인자들이 사라지고 주변 환경에 적절하게 반응하는 정상 세포로서 기능을 회복하는 현상을 확인했다.
연구 결과 노화된 인간 진피 섬유아세포에서는 PDK1이 mTOR와 NF-kB를 활성화해 노화와 관련된 분비 표현형(SASP: Senescence Associated Secretary Phenotype)을 유발하고 노화 형질을 유지하는 것과 연관돼 있음을 밝혀냈다. 즉, PDK1을 억제함으로써 다시 원래의 정상적인 젊은 세포 상태로 안전하게 되돌릴 수 있음을 증명한 것이다.
조 교수팀이 연구 과정에서 찾아낸 표적 단백질의 활성을 억제할 수 있는 저분자화합물과 관련된 신약개발과 그리고 전임상실험을 통해 노화된 세포의 정상 세포화라는 연구 결과는 새로운 노인성 질환의 치료 기술과 회춘 기술에 관한 연구를 본 궤도에 올려놓은 초석을 다진 획기적인 연구로 평가받고 있다.
실제 ㈜아모레퍼시픽 기술연구원은 이번 연구 결과로부터 동백추출물에서 PDK1 억제 성분을 추출해 노화된 피부의 주름을 개선하는 화장품을 개발중이다.
조광현 교수는 "그동안 비가역적 생명현상이라고 인식돼왔던 노화를 가역화할 가능성을 보여줬다ˮ라며 "이번 연구는 노화를 가역적 생명현상으로 인식하고 이에 적극적으로 대처해 건강 수명을 연장하는 한편 노인성 질환을 예방할 수 있는 새로운 시대의 서막을 열었다ˮ라고 의미를 부여했다.
이번 연구는 조광현 교수 연구팀의 시스템생물학 기반 가역화 기술 개발의 일환으로 이뤄졌으며, 연구팀은 지난 1월 같은 기술을 적용해 대장암세포를 다시 정상 대장 세포로 되돌리는 연구에 성공한 바 있다.
한편 이번 연구는 한국연구재단의 중견연구자지원사업과 KAIST 그랜드챌린지 30 (KC30) 프로젝트 및 아모레퍼시픽 R&D 센터의 지원으로 수행됐다.
2020.11.26 조회수 48403
노화된 세포를 젊은 세포로 되돌리는 초기 원천기술 개발
우리 연구진이 노화된 세포를 젊은 세포로 되돌리는 역 노화 원천기술을 개발했다. 이를 활용하면 노화 현상을 막고 각종 노인성 질환을 사전 억제할 수 있는 치료제를 개발할 단서를 찾을 수 있을 것으로 기대된다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 시스템생물학 연구를 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌리는 역 노화의 초기 원천기술을 개발했다고 26일 밝혔다.
조광현 교수팀의 이번 연구 결과는 ㈜아모레퍼시픽 기술연구원과의 산학 공동연구를 통해 최초로 개발된 노화 인공피부 모델에서 이 기술을 적용함으로써 입증하는 데 성공했다.
조 교수팀은 이번 연구를 위해 인간 진피 섬유아세포의 세포노화 신호전달 네트워크의 컴퓨터 모델을 개발한 후 시뮬레이션 분석을 통해 노화된 인간 진피 섬유아세포를 젊은 세포로 되돌리는데 필요한 핵심 인자를 찾아냈다. 이후 노화 인공피부 모델에서 핵심 인자를 조절함으로써 노화된 피부조직에서 감소된 콜라겐의 합성을 증가시키고 재생 능력을 회복시켜 젊은 피부조직의 특성을 보이게 하는 역 노화 기술을 개발했다.
연구팀 관계자는 이러한 역 노화 기술은 노화된 피부 등을 포함한 노화 현상 및 많은 노인성 질환의 발생을 사전에 억제할 수 있도록 근본적인 치료전략을 제시한 것으로 건강 수명을 오랫동안 유지하고 싶은 인류의 꿈을 실현하는데 한 걸음 다가선 결과라고 의미를 부여했다.
바이오및뇌공학과 안수균 박사과정 학생, 강준수 연구원, 이수범 연구원과 ㈜아모레퍼시픽의 바이오사이언스랩이 참여한 이번 연구 결과는 국제저명학술지인 `미국국립과학원회보(PNAS)'에 게재됐다.(논문명: Inhibition of 3-phosphoinositide-dependent protein kinase 1 (PDK1) can revert cellular senescence in human dermal fibroblasts)
현재 널리 연구되고 있는 회춘 전략은 이미 분화된 세포를 역분화시키는 4개의 `OSKM(Oct4, Sox2, Klf4, c-Myc) 야마나카 전사인자'를 일시적으로 발현시켜 후성유전학적 리모델링(epigenetic remodeling)을 일으킴으로써 노화된 세포를 젊은 상태로 되돌리는 부분적 역분화(partial reprogramming) 전략이다.
이 기술은 노화된 세포가 젊은 세포로 되돌아갈 수 있다는 것을 증명했지만 종양의 형성과 암의 진행을 유발하는 부작용이 생긴다. 따라서 이와 같은 부작용을 배제할 수 있는 정교한 제어 전략이 과학 난제로 남아있었다.
조 교수팀은 이러한 난제 해결을 위해 시스템생물학 연구 방법을 통해 노화된 인간 진피 섬유아세포를 정상적인 젊은 세포로 되돌릴 수 있는 핵심 조절인자를 오래전부터 탐구하기 시작했다. 4년에 걸친 연구 끝에 단백질 합성, 세포의 성장 등을 조절하는 mTOR와 면역 물질 사이토카인의 생성에 관여하는 NF-kB를 동시에 제어하고 있는 상위 조절 인자인 `PDK1(3-phosphoinositide-dependent protein kinase 1)'을 찾아냈다.
연구팀은 PDK1을 억제함으로써 노화된 인간 진피 섬유아세포를 다시 정상적인 젊은 세포로 되돌릴 수 있음을 분자 세포실험 및 노화 인공피부 모델 실험을 통해 입증했다. 연구를 통해 노화된 인간 진피 섬유아세포에서 PDK1을 억제했을 때 세포노화 표지 인자들이 사라지고 주변 환경에 적절하게 반응하는 정상 세포로서 기능을 회복하는 현상을 확인했다.
연구 결과 노화된 인간 진피 섬유아세포에서는 PDK1이 mTOR와 NF-kB를 활성화해 노화와 관련된 분비 표현형(SASP: Senescence Associated Secretary Phenotype)을 유발하고 노화 형질을 유지하는 것과 연관돼 있음을 밝혀냈다. 즉, PDK1을 억제함으로써 다시 원래의 정상적인 젊은 세포 상태로 안전하게 되돌릴 수 있음을 증명한 것이다.
조 교수팀이 연구 과정에서 찾아낸 표적 단백질의 활성을 억제할 수 있는 저분자화합물과 관련된 신약개발과 그리고 전임상실험을 통해 노화된 세포의 정상 세포화라는 연구 결과는 새로운 노인성 질환의 치료 기술과 회춘 기술에 관한 연구를 본 궤도에 올려놓은 초석을 다진 획기적인 연구로 평가받고 있다.
실제 ㈜아모레퍼시픽 기술연구원은 이번 연구 결과로부터 동백추출물에서 PDK1 억제 성분을 추출해 노화된 피부의 주름을 개선하는 화장품을 개발중이다.
조광현 교수는 "그동안 비가역적 생명현상이라고 인식돼왔던 노화를 가역화할 가능성을 보여줬다ˮ라며 "이번 연구는 노화를 가역적 생명현상으로 인식하고 이에 적극적으로 대처해 건강 수명을 연장하는 한편 노인성 질환을 예방할 수 있는 새로운 시대의 서막을 열었다ˮ라고 의미를 부여했다.
이번 연구는 조광현 교수 연구팀의 시스템생물학 기반 가역화 기술 개발의 일환으로 이뤄졌으며, 연구팀은 지난 1월 같은 기술을 적용해 대장암세포를 다시 정상 대장 세포로 되돌리는 연구에 성공한 바 있다.
한편 이번 연구는 한국연구재단의 중견연구자지원사업과 KAIST 그랜드챌린지 30 (KC30) 프로젝트 및 아모레퍼시픽 R&D 센터의 지원으로 수행됐다.
2020.11.26 조회수 48403