%EB%B0%94%EC%9D%B4%EC%98%A4%EB%A6%AC%ED%8C%8C%EC%9D%B4%EB%84%88%EB%A6%AC%EB%A5%BC+%EC%9C%84%ED%95%9C+%EC%8B%9C%EC%8A%A4%ED%85%9C%EB%8C%80%EC%82%AC%EA%B3%B5%ED%95%99+%EC%97%B0%EA%B5%AC%EC%82%AC%EC%97%85
-
 이상엽, 김현욱 교수, 약물 상호작용 예측기술 DeepDDI 개발
우리 대학 생명화학공학과 이상엽 특훈교수와 김현욱 교수 공동 연구팀이 약물-약물 및 약물-음식 간 상호작용을 정확하게 예측하기 위해 딥 러닝(deep learning)을 이용해 약물 상호작용 예측 방법론인 딥디디아이 (DeepDDI)를 개발했다.
김현욱 교수, 류재용 연구원이 공동 1저자로 참여한 이번 연구는 국제학술지 ‘미국 국립과학원 회보(PNAS)’ 4월 16일자 온라인판에 게재됐다.
기존의 약물 상호작용 예측 방법론은 약물-약물 간의 상호작용 가능성만을 예측할 뿐, 두 약물 간의 구체적인 약리작용에 대한 정보는 제공하지 못했다. 이러한 이유로 맞춤형 약물 처방, 식이요법 등 응용 연구에서 체계적인 근거를 제시하거나 가설을 세우는 데에 한계가 있었다.
연구팀은 딥 러닝(deep learning) 기술을 적용해 19만 2천 284개의 약물-약물 상호작용을 아우르는 86가지의 약물 상호작용을 92.4%의 정확도로 예측하는 시스템 딥디디아이 (DeepDDI)를 개발했다.
딥디디아이는 두 약물 A, B 간의 상호작용에 대한 예측 결과를 다음과 같이 사람이 읽을 수 있는 영문 문장으로 출력한다 : “The metabolism of Drug B can be decreased when combined with Drug A (약물 A를 약물 B와 함께 복용 시 약물 B의 약물 대사가 감소 될 수 있다)”
연구팀은 딥디디아이를 이용해 두 약물 복용 시 일어날 수 있는 유해반응의 원인, 보고된 인체 부작용을 최소화시킬 수 있는 대체 약물, 특정 약물의 약효를 떨어뜨릴 수 있는 음식 및 음식 성분, 지금껏 알려지지 않은 음식 성분의 활성 등을 예측했다.
이번 연구성과로 약물-약물 및 약물-음식 상호작용을 정확하게 예측할 수 있는 시스템을 활용하는 것이 가능해졌으며 이는 신약개발, 복합적 약의 처방, 투약시의 음식조절 등을 포함해 헬스케어, 정밀의료 산업 및 제약 산업에 중요한 역할을 할 것으로 기대된다.
이상엽 특훈교수는 “이번 연구결과는 4차 산업혁명 시대의 정밀의료를 선도할 수 있는 기반 기술을 개발한 것이다”며, “복합 투여되는 약물들의 부작용을 낮추고 환자 맞춤형 약물 처방과 식이요법 제안을 통한 효과적인 약물치료 전략을 수립할 수 있다. 특히 고령화 사회에서 건강한 삶을 유지하는데 필요한 약-음식 궁합에 대한 제안을 해 줄 수 있는 시스템으로 발전해 나갈 것이다”고 말했다.
이 연구성과는 과학기술정보통신부의 바이오리파이너리를 위한 시스템대사공학 연구사업, KAIST의 4차 산업혁명 인공지능 플래그십 이니셔티브 연구사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 딥디디아이 (DeepDDI)의 모식도 및 예측된다양한 약물-음식성분의 상호작용들의 시각화
2018.04.18 조회수 21577
이상엽, 김현욱 교수, 약물 상호작용 예측기술 DeepDDI 개발
우리 대학 생명화학공학과 이상엽 특훈교수와 김현욱 교수 공동 연구팀이 약물-약물 및 약물-음식 간 상호작용을 정확하게 예측하기 위해 딥 러닝(deep learning)을 이용해 약물 상호작용 예측 방법론인 딥디디아이 (DeepDDI)를 개발했다.
김현욱 교수, 류재용 연구원이 공동 1저자로 참여한 이번 연구는 국제학술지 ‘미국 국립과학원 회보(PNAS)’ 4월 16일자 온라인판에 게재됐다.
기존의 약물 상호작용 예측 방법론은 약물-약물 간의 상호작용 가능성만을 예측할 뿐, 두 약물 간의 구체적인 약리작용에 대한 정보는 제공하지 못했다. 이러한 이유로 맞춤형 약물 처방, 식이요법 등 응용 연구에서 체계적인 근거를 제시하거나 가설을 세우는 데에 한계가 있었다.
연구팀은 딥 러닝(deep learning) 기술을 적용해 19만 2천 284개의 약물-약물 상호작용을 아우르는 86가지의 약물 상호작용을 92.4%의 정확도로 예측하는 시스템 딥디디아이 (DeepDDI)를 개발했다.
딥디디아이는 두 약물 A, B 간의 상호작용에 대한 예측 결과를 다음과 같이 사람이 읽을 수 있는 영문 문장으로 출력한다 : “The metabolism of Drug B can be decreased when combined with Drug A (약물 A를 약물 B와 함께 복용 시 약물 B의 약물 대사가 감소 될 수 있다)”
연구팀은 딥디디아이를 이용해 두 약물 복용 시 일어날 수 있는 유해반응의 원인, 보고된 인체 부작용을 최소화시킬 수 있는 대체 약물, 특정 약물의 약효를 떨어뜨릴 수 있는 음식 및 음식 성분, 지금껏 알려지지 않은 음식 성분의 활성 등을 예측했다.
이번 연구성과로 약물-약물 및 약물-음식 상호작용을 정확하게 예측할 수 있는 시스템을 활용하는 것이 가능해졌으며 이는 신약개발, 복합적 약의 처방, 투약시의 음식조절 등을 포함해 헬스케어, 정밀의료 산업 및 제약 산업에 중요한 역할을 할 것으로 기대된다.
이상엽 특훈교수는 “이번 연구결과는 4차 산업혁명 시대의 정밀의료를 선도할 수 있는 기반 기술을 개발한 것이다”며, “복합 투여되는 약물들의 부작용을 낮추고 환자 맞춤형 약물 처방과 식이요법 제안을 통한 효과적인 약물치료 전략을 수립할 수 있다. 특히 고령화 사회에서 건강한 삶을 유지하는데 필요한 약-음식 궁합에 대한 제안을 해 줄 수 있는 시스템으로 발전해 나갈 것이다”고 말했다.
이 연구성과는 과학기술정보통신부의 바이오리파이너리를 위한 시스템대사공학 연구사업, KAIST의 4차 산업혁명 인공지능 플래그십 이니셔티브 연구사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 딥디디아이 (DeepDDI)의 모식도 및 예측된다양한 약물-음식성분의 상호작용들의 시각화
2018.04.18 조회수 21577 -
 이상엽 특훈교수, 병원균이 항생제에 내성을 갖는 원리 규명
〈 이 상 엽 교수 〉
우리 대학 생명화학공학과 이상엽 교수와 덴마크 공대(DTU) 노보 노르디스크 바이오지속가능센터(Novo Nordist Foundation Center for Biosustainability) 공동 연구팀이 박테리아 병원균이 항생제에 대한 내성을 획득하는 작동 원리를 밝혔다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 7일자 온라인 판에 게재됐다.
항생제 남용 등으로 인해 항생제 내성균이 점점 더 늘어나고 있다. 이는 인류의 생존을 위협하는 문제로 그 심각성이 전 세계적으로 점점 커지고 있다.
인체 감염균이 항생제 내성을 갖는 방식에는 항생제를 분해하는 효소를 갖거나 다시 뱉어내는 등 다양한 방식이 있다. 그 중 대표적인 것은 항생제 내성 유전자를 획득해 항생제를 무용지물로 만드는 것이다.
내성 유전자는 보통 항생제를 생산하는 곰팡이나 악티노박테리아에서 발견된다. 이는 해당 항생제를 만드는 곰팡이와 박테리아가 자기 스스로를 항생제로부터 보호하기 위해 갖고 있는 것이다.
이 내성 유전자를 인체 감염균이 획득하면 항생제 내성을 갖게 된다. 이러한 사실은 게놈 정보 등을 통해 이미 알려져 있는 사실이다.
그러나 어떤 방식으로 항생제 내성 유전자들이 인체 감염균에 전달되는지는 밝혀지지 않았다.
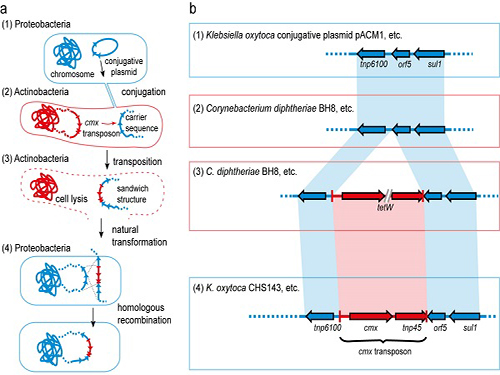
이상엽 교수와 덴마크 공대 공동 연구팀은 항생제 내성 유전자가 직접적으로 인체 감염균에 전달되는 것이 아니라 연구팀이 캐리백(carry-back)이라고 이름 지은 복잡한 과정을 통해 이뤄지는 것을 규명했다.
우선 인체 감염균과 방선균이 박테리아간의 성교에 해당하는 접합(conjugation)에 의해 인체 감염균의 DNA 일부가 방선균으로 들어간다.
그 와중에 항생제 내성 유전자 양쪽 주위에도 감염균의 DNA가 들어가는경우가 생긴다. 이 상태에서 방선균이 죽어 세포가 깨지면 항생제 내성 유전자와 감염균의 DNA 조각이 포함된 DNA들도 함께 나오게 된다.
이렇게 배출된 항생제 내성 유전자에는 인체 감염균의 일부 DNA가 양쪽에 공존하고 있다. 이 때문에 인체 감염균은 자신의 게놈에 재삽입이 가능해지고 이를 통해 항생제 내성을 획득한다.
연구팀은 생물정보학적 분석과 실제 실험을 통해 이를 증명했다.
이 교수는 “이번 연구결과는 인체 감염 유해균들이 항생제 내성을 획득하는 방식 중 한 가지를 제시한 것이다”며 “병원 내, 외부의 감염과 예방 관리시스템, 항생제의 올바른 사용에 대해 다시 한 번 생각할 수 있는 기회를 제공할 것이다”고 말했다.
이번 연구는 노보 노르디스크 재단과 미래창조과학부 원천기술과(바이오리파이너리를 위한 시스템대사공학 연구사업)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 항생제 내성 유전자가 전달되는 캐리백 현상의 모식도
2017.06.19 조회수 24332
이상엽 특훈교수, 병원균이 항생제에 내성을 갖는 원리 규명
〈 이 상 엽 교수 〉
우리 대학 생명화학공학과 이상엽 교수와 덴마크 공대(DTU) 노보 노르디스크 바이오지속가능센터(Novo Nordist Foundation Center for Biosustainability) 공동 연구팀이 박테리아 병원균이 항생제에 대한 내성을 획득하는 작동 원리를 밝혔다.
이번 연구결과는 국제 학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 7일자 온라인 판에 게재됐다.
항생제 남용 등으로 인해 항생제 내성균이 점점 더 늘어나고 있다. 이는 인류의 생존을 위협하는 문제로 그 심각성이 전 세계적으로 점점 커지고 있다.
인체 감염균이 항생제 내성을 갖는 방식에는 항생제를 분해하는 효소를 갖거나 다시 뱉어내는 등 다양한 방식이 있다. 그 중 대표적인 것은 항생제 내성 유전자를 획득해 항생제를 무용지물로 만드는 것이다.
내성 유전자는 보통 항생제를 생산하는 곰팡이나 악티노박테리아에서 발견된다. 이는 해당 항생제를 만드는 곰팡이와 박테리아가 자기 스스로를 항생제로부터 보호하기 위해 갖고 있는 것이다.
이 내성 유전자를 인체 감염균이 획득하면 항생제 내성을 갖게 된다. 이러한 사실은 게놈 정보 등을 통해 이미 알려져 있는 사실이다.
그러나 어떤 방식으로 항생제 내성 유전자들이 인체 감염균에 전달되는지는 밝혀지지 않았다.
이상엽 교수와 덴마크 공대 공동 연구팀은 항생제 내성 유전자가 직접적으로 인체 감염균에 전달되는 것이 아니라 연구팀이 캐리백(carry-back)이라고 이름 지은 복잡한 과정을 통해 이뤄지는 것을 규명했다.
우선 인체 감염균과 방선균이 박테리아간의 성교에 해당하는 접합(conjugation)에 의해 인체 감염균의 DNA 일부가 방선균으로 들어간다.
그 와중에 항생제 내성 유전자 양쪽 주위에도 감염균의 DNA가 들어가는경우가 생긴다. 이 상태에서 방선균이 죽어 세포가 깨지면 항생제 내성 유전자와 감염균의 DNA 조각이 포함된 DNA들도 함께 나오게 된다.
이렇게 배출된 항생제 내성 유전자에는 인체 감염균의 일부 DNA가 양쪽에 공존하고 있다. 이 때문에 인체 감염균은 자신의 게놈에 재삽입이 가능해지고 이를 통해 항생제 내성을 획득한다.
연구팀은 생물정보학적 분석과 실제 실험을 통해 이를 증명했다.
이 교수는 “이번 연구결과는 인체 감염 유해균들이 항생제 내성을 획득하는 방식 중 한 가지를 제시한 것이다”며 “병원 내, 외부의 감염과 예방 관리시스템, 항생제의 올바른 사용에 대해 다시 한 번 생각할 수 있는 기회를 제공할 것이다”고 말했다.
이번 연구는 노보 노르디스크 재단과 미래창조과학부 원천기술과(바이오리파이너리를 위한 시스템대사공학 연구사업)의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 항생제 내성 유전자가 전달되는 캐리백 현상의 모식도
2017.06.19 조회수 24332