%EB%B6%84%EC%9E%90%EC%8A%A4%EC%9C%84%EC%B9%98
-
 암세포 발생 순간 되돌리는 분자스위치 발견
조광현 교수 연구팀은 암세포를 죽이지 않고 그 상태만을 변환시켜 정상 세포와 유사한 상태로 되돌리는 암 가역 치료 원천기술을 개발한 바 있다. 이번에는 정상세포가 암세포로 변화되는 순간의 유전자 네트워크에 암 가역화를 유도할 수 있는 분자스위치가 숨겨져 있음을 최초로 밝히는데 성공하였다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 정상세포에서 암세포로 변화하는 순간의 임계 전이(臨界轉移, critical transition) 현상을 포착하고 이를 분석해 암세포를 다시 정상세포로 되돌릴 수 있는 분자스위치를 발굴하는 기술 개발에 성공했다고 5일 밝혔다.
임계 전이란 물이 섭씨 100도에서 증기로 변하는 것처럼 특정 시점에 갑작스러운 상태변화가 일어나는 현상을 말한다. 정상세포가 유전적, 후성유전적 변화의 축적으로 인해 특정 시점에 암세포로 변화되는 과정에도 이러한 임계 전이 현상이 나타난다.
연구팀은 암 발생 과정에서 정상세포가 암세포로 전환되기 직전, 정상세포와 암세포들이 공존하는 불안정한 임계 전이 상태에 놓일 수 있음을 발견하고 이러한 임계 전이 상태를 시스템생물학 방법으로 분석해 암화 과정을 역전시킬 수 있는 암 가역화 분자스위치 발굴 기술을 개발했다. 그리고 이를 대장암세포에 적용해 암세포가 정상세포의 특징을 회복할 수 있음을 분자세포실험으로 확인했다.
암 발생의 임계 전이를 관장하는 유전자 네트워크의 컴퓨터 모델을 단일세포 유전자 발현 데이터로부터 자동 추론해내고 이를 시뮬레이션 분석해 암 가역화 분자스위치를 체계적으로 찾아내는 원천기술을 개발한 것이어서 향후 다른 암종의 가역 치료제 개발에도 응용될 수 있을 것으로 기대된다.
조광현 교수는 "정상세포가 되돌릴 수 없는 암세포 상태로 변화되기 직전의 임계 전이 순간을 포착해 암세포의 운명을 다시 정상세포 상태로 되돌릴 수 있는 분자스위치를 발굴해 낸 것이다ˮ라고 말했다.
이어 “특히 이번 연구에서는 그동안 수수께끼로 여겨졌던 암 발생 과정 이면의 세포 내에 어떠한 변화가 일어나는지를 유전자 네트워크 차원에서 상세히 밝혀냈다”며 “암세포의 운명을 다시 정상세포로 되돌릴 수 있는 중요한 단서가 바로 이러한 변화의 순간에 숨어있다는 것을 처음으로 규명한 연구다”라고 강조했다.
우리 대학 신동관 박사(現 국립암센터), 공정렬 박사, 정서윤 박사과정 학생 등이 참여했으며 서울대학교 연구팀이 대장암 환자 오가노이드(체외배양조직)를 제공해 진행된 이번 연구 결과는 와일리(Wiley)에서 출간하는 국제저널 `어드밴스드 사이언스(Advanced Science)' 1월 22일 字 온라인판 논문으로 출판됐다. (논문명: Attractor landscape analysis reveals a reversion switch in the transition of colorectal tumorigenesis) (DOI: https://doi.org/10.1002/advs.202412503)
한편 이번 연구는 과학기술정보통신부 한국연구재단의 중견연구사업과 기초연구실사업, 그리고 보건복지부 한국보건산업진흥원의 질병중심 중개연구사업의 지원을 통해 수행됐다.
2025.02.05 조회수 8171
암세포 발생 순간 되돌리는 분자스위치 발견
조광현 교수 연구팀은 암세포를 죽이지 않고 그 상태만을 변환시켜 정상 세포와 유사한 상태로 되돌리는 암 가역 치료 원천기술을 개발한 바 있다. 이번에는 정상세포가 암세포로 변화되는 순간의 유전자 네트워크에 암 가역화를 유도할 수 있는 분자스위치가 숨겨져 있음을 최초로 밝히는데 성공하였다.
우리 대학 바이오및뇌공학과 조광현 교수 연구팀이 정상세포에서 암세포로 변화하는 순간의 임계 전이(臨界轉移, critical transition) 현상을 포착하고 이를 분석해 암세포를 다시 정상세포로 되돌릴 수 있는 분자스위치를 발굴하는 기술 개발에 성공했다고 5일 밝혔다.
임계 전이란 물이 섭씨 100도에서 증기로 변하는 것처럼 특정 시점에 갑작스러운 상태변화가 일어나는 현상을 말한다. 정상세포가 유전적, 후성유전적 변화의 축적으로 인해 특정 시점에 암세포로 변화되는 과정에도 이러한 임계 전이 현상이 나타난다.
연구팀은 암 발생 과정에서 정상세포가 암세포로 전환되기 직전, 정상세포와 암세포들이 공존하는 불안정한 임계 전이 상태에 놓일 수 있음을 발견하고 이러한 임계 전이 상태를 시스템생물학 방법으로 분석해 암화 과정을 역전시킬 수 있는 암 가역화 분자스위치 발굴 기술을 개발했다. 그리고 이를 대장암세포에 적용해 암세포가 정상세포의 특징을 회복할 수 있음을 분자세포실험으로 확인했다.
암 발생의 임계 전이를 관장하는 유전자 네트워크의 컴퓨터 모델을 단일세포 유전자 발현 데이터로부터 자동 추론해내고 이를 시뮬레이션 분석해 암 가역화 분자스위치를 체계적으로 찾아내는 원천기술을 개발한 것이어서 향후 다른 암종의 가역 치료제 개발에도 응용될 수 있을 것으로 기대된다.
조광현 교수는 "정상세포가 되돌릴 수 없는 암세포 상태로 변화되기 직전의 임계 전이 순간을 포착해 암세포의 운명을 다시 정상세포 상태로 되돌릴 수 있는 분자스위치를 발굴해 낸 것이다ˮ라고 말했다.
이어 “특히 이번 연구에서는 그동안 수수께끼로 여겨졌던 암 발생 과정 이면의 세포 내에 어떠한 변화가 일어나는지를 유전자 네트워크 차원에서 상세히 밝혀냈다”며 “암세포의 운명을 다시 정상세포로 되돌릴 수 있는 중요한 단서가 바로 이러한 변화의 순간에 숨어있다는 것을 처음으로 규명한 연구다”라고 강조했다.
우리 대학 신동관 박사(現 국립암센터), 공정렬 박사, 정서윤 박사과정 학생 등이 참여했으며 서울대학교 연구팀이 대장암 환자 오가노이드(체외배양조직)를 제공해 진행된 이번 연구 결과는 와일리(Wiley)에서 출간하는 국제저널 `어드밴스드 사이언스(Advanced Science)' 1월 22일 字 온라인판 논문으로 출판됐다. (논문명: Attractor landscape analysis reveals a reversion switch in the transition of colorectal tumorigenesis) (DOI: https://doi.org/10.1002/advs.202412503)
한편 이번 연구는 과학기술정보통신부 한국연구재단의 중견연구사업과 기초연구실사업, 그리고 보건복지부 한국보건산업진흥원의 질병중심 중개연구사업의 지원을 통해 수행됐다.
2025.02.05 조회수 8171 -
 천연물 최초 합성으로부터 신개념 광스위치 개발
자연에서 일어나는 대부분의 화학 반응은 에너지적으로 안정한 형태를 취하는 방향으로 진행된다. 그렇기에 상대적으로 불안정한 구조를 가진 세큐린진 B의 합성은 매우 도전적인 과제다. 우리 연구진이 천연물 합성 원리를 바탕으로 빛으로 on/off가 가능한 분자 스위치 신소재 원천기술을 확보했다.
우리 대학 화학과 한순규 교수와 윤동기 교수 공동연구팀이 항암 및 퇴행성 뇌 질환 치료 효과로 학계의 꾸준한 관심을 받고있는 세큐리네가 알칼로이드 천연물 군에 속하는 세큐린진(securingine) B의 합성 방법을 세계 최초로 밝혀내고, 이 과정에서 발견한 화학적 반응성을 응용해 새로운 타입의 분자 광스위치를 개발했다고 11일 밝혔다.
한 교수 연구팀은 천연물 합성에 머무르지 않고 이 분자 재배열 원리를 바탕으로 서로 다른 파장의 빛을 통해 가역적으로 형태와 성질이 바뀌는 분자 광스위치를 고안했다.
천연물에 전자주개 치환기*를 달자 가시광선 영역의 빛을 흡수하면서, 무색인 기본 천연물과 달리 신물질은 노란색을 띠었다. 이렇게 새로 만든 천연물 유래 소재에 파란색 빛을 쬐었더니 수 초 뒤 색이 없어졌다. 빛에 의해 분자구조가 변형되면서 물질의 성질이 바뀌어 더 이상 색을 띄지 않게 된 것이다. 게다가 이 변형된 구조의 물질에 310나노미터(nm) 파장의 자외선을 쬐었더니 다시 구조가 원래대로 돌아오면서 노란색이 됐다.
*전자주개 치환기: 상대적으로 전자밀도가 풍부하여 전자가 부족한 시스템을 안정화시킬 수 있는 탄화수소의 모체 사슬 상의 한 개 이상의 수소 원자를 대체하는 원자 또는 원자단
한 교수 연구팀은 새로이 개발한 광 감응 물질을 고분자에도 적용했다. 연구팀은 PDMS(polydimethylsiloxane, 연성고분자의 일종) 고분자에 분자 광스위치 물질을 혼합하고 굳혀서 427 nm 파장의 파란색 가시광선을 쬐어쬐어주면 무색이 되고 310 nm 파장의 자외선을 쬐어주면 노란색으로 변하는 젤리 물질을 개발하였다.
연구팀은 새로 개발한 광스위치 소재를 광학재료 분야에 접목하고자 같은 학과 윤동기 교수 연구팀과 광 감응 카이랄* 혼입제 개발에 착수했다. 디스플레이 분야에 적용하기 위해 액정 물질에 파란색 빛을 쬐었을 때 카이랄 액정의 꼬임 주기가 변하면서 광스위치의 성질도 여전히 가지는 것을 관찰했다.
*카이랄: 왼손과 오른손처럼 서로 거울 쌍을 이루지만, 둘이 서로 겹쳐지지 않는 성질로 화학의 핵심 개념이자 물질의 광학적 특성을 결정하는 근본 요소 중 하나.
이번에 개발한 광스위치는 분자 내에서 결합이 이동해 분자구조가 바뀌는 혁신적인 작동 원리에 기반해 분자 광스위치 관련 분야 연구자의 눈길을 끌었다. 파장에 따른 색 변화뿐 아니라 형광의 on/off도 가능하기 때문에 형광 탐침자로써 생물학 분야에도 응용가능하다.
한 교수는 “이번 성과는 천연물 합성이라는 기초과학 연구 과정에서 발견한 원리를 다양하게 응용 가능한 새로운 분자 광스위치 개발로 연결한 사례”라며 “새로운 기술의 개발을 위해서는 자연현상의 작동 원리를 탐구하는 기초과학 연구가 굉장히 중요하다는 것을 다시 한번 일깨워준 계기가 되었다”라고 밝혔다.
화학과 박상빈 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 ‘셀 프레스(Cell Press)’에서 발간하는 국제 학술지 ‘켐(Chem)’에 10월 31일 字 게재됐다. (논문명: Synthesis of securingine B enables photoresponsive materials design)
이번 연구는 한국연구재단이 지원하는 선도연구센터인 KAIST 멀티스케일 카이랄 구조체 연구센터에(센터장: 이희승 교수) 속한 한순규-윤동기 교수 연구팀의 공동연구로 진행됐다.
이 밖에도 이번 연구는 한국연구재단의 개인기초연구사업과 KAIST의 도약연구(UP) 사업, KC30 사업, 그리고 초세대 협업연구실 프로젝트의 지원을 받아 수행됐다.
2024.11.11 조회수 4132
천연물 최초 합성으로부터 신개념 광스위치 개발
자연에서 일어나는 대부분의 화학 반응은 에너지적으로 안정한 형태를 취하는 방향으로 진행된다. 그렇기에 상대적으로 불안정한 구조를 가진 세큐린진 B의 합성은 매우 도전적인 과제다. 우리 연구진이 천연물 합성 원리를 바탕으로 빛으로 on/off가 가능한 분자 스위치 신소재 원천기술을 확보했다.
우리 대학 화학과 한순규 교수와 윤동기 교수 공동연구팀이 항암 및 퇴행성 뇌 질환 치료 효과로 학계의 꾸준한 관심을 받고있는 세큐리네가 알칼로이드 천연물 군에 속하는 세큐린진(securingine) B의 합성 방법을 세계 최초로 밝혀내고, 이 과정에서 발견한 화학적 반응성을 응용해 새로운 타입의 분자 광스위치를 개발했다고 11일 밝혔다.
한 교수 연구팀은 천연물 합성에 머무르지 않고 이 분자 재배열 원리를 바탕으로 서로 다른 파장의 빛을 통해 가역적으로 형태와 성질이 바뀌는 분자 광스위치를 고안했다.
천연물에 전자주개 치환기*를 달자 가시광선 영역의 빛을 흡수하면서, 무색인 기본 천연물과 달리 신물질은 노란색을 띠었다. 이렇게 새로 만든 천연물 유래 소재에 파란색 빛을 쬐었더니 수 초 뒤 색이 없어졌다. 빛에 의해 분자구조가 변형되면서 물질의 성질이 바뀌어 더 이상 색을 띄지 않게 된 것이다. 게다가 이 변형된 구조의 물질에 310나노미터(nm) 파장의 자외선을 쬐었더니 다시 구조가 원래대로 돌아오면서 노란색이 됐다.
*전자주개 치환기: 상대적으로 전자밀도가 풍부하여 전자가 부족한 시스템을 안정화시킬 수 있는 탄화수소의 모체 사슬 상의 한 개 이상의 수소 원자를 대체하는 원자 또는 원자단
한 교수 연구팀은 새로이 개발한 광 감응 물질을 고분자에도 적용했다. 연구팀은 PDMS(polydimethylsiloxane, 연성고분자의 일종) 고분자에 분자 광스위치 물질을 혼합하고 굳혀서 427 nm 파장의 파란색 가시광선을 쬐어쬐어주면 무색이 되고 310 nm 파장의 자외선을 쬐어주면 노란색으로 변하는 젤리 물질을 개발하였다.
연구팀은 새로 개발한 광스위치 소재를 광학재료 분야에 접목하고자 같은 학과 윤동기 교수 연구팀과 광 감응 카이랄* 혼입제 개발에 착수했다. 디스플레이 분야에 적용하기 위해 액정 물질에 파란색 빛을 쬐었을 때 카이랄 액정의 꼬임 주기가 변하면서 광스위치의 성질도 여전히 가지는 것을 관찰했다.
*카이랄: 왼손과 오른손처럼 서로 거울 쌍을 이루지만, 둘이 서로 겹쳐지지 않는 성질로 화학의 핵심 개념이자 물질의 광학적 특성을 결정하는 근본 요소 중 하나.
이번에 개발한 광스위치는 분자 내에서 결합이 이동해 분자구조가 바뀌는 혁신적인 작동 원리에 기반해 분자 광스위치 관련 분야 연구자의 눈길을 끌었다. 파장에 따른 색 변화뿐 아니라 형광의 on/off도 가능하기 때문에 형광 탐침자로써 생물학 분야에도 응용가능하다.
한 교수는 “이번 성과는 천연물 합성이라는 기초과학 연구 과정에서 발견한 원리를 다양하게 응용 가능한 새로운 분자 광스위치 개발로 연결한 사례”라며 “새로운 기술의 개발을 위해서는 자연현상의 작동 원리를 탐구하는 기초과학 연구가 굉장히 중요하다는 것을 다시 한번 일깨워준 계기가 되었다”라고 밝혔다.
화학과 박상빈 석박사통합과정 학생이 제1 저자로 참여한 이번 연구는 ‘셀 프레스(Cell Press)’에서 발간하는 국제 학술지 ‘켐(Chem)’에 10월 31일 字 게재됐다. (논문명: Synthesis of securingine B enables photoresponsive materials design)
이번 연구는 한국연구재단이 지원하는 선도연구센터인 KAIST 멀티스케일 카이랄 구조체 연구센터에(센터장: 이희승 교수) 속한 한순규-윤동기 교수 연구팀의 공동연구로 진행됐다.
이 밖에도 이번 연구는 한국연구재단의 개인기초연구사업과 KAIST의 도약연구(UP) 사업, KC30 사업, 그리고 초세대 협업연구실 프로젝트의 지원을 받아 수행됐다.
2024.11.11 조회수 4132 -
 단백질 나노튜브의 자기조립 분자스위치 발견
- 한국, 미국, 이스라엘 국제 공동 연구 성과 -
- 암 치료와 뇌 질환 메커니즘 단서 -
우리 학교 바이오및뇌공학과 최명철 교수와 송채연 연구교수는 미국
산타바바라 캘리포니아대학교, 이스라엘 히브리대학교와 공동으로 세포분열과 세포간 물질수송에 열쇠가 되는 단백질 나노튜브의 자기조립
구조를 제어하는 분자스위치를 발견했다.
연구 결과는 세계적 학술지 ‘네이처 머티리얼즈(Nature Materials, IF=35.7)’ 19일자에 게재됐다.
마이크로튜불(microtubule, 미세소관)은 사람의 몸속에서 세포분열·세포골격·세포간 물질수송 도구로 사용되는 튜브 형태의 단백질로 굵기가 25나노미터(1나노미터는 머리카락 굵기의 10만분의 1)에 불과하다.
대부분의 암 치료 약물은 마이크로튜불의 형성을 교란해 암세포 분열을
억제하는 것으로 작용 메커니즘이 알려져 있다. 알츠하이머병은 세포간 물질수송을 담당하는 마이크로튜불의 구조적 안정성이 떨어지면서
신경세포에서의 신호전달이 제대로 이루어지지 않아 생기는 대표적 뇌질환이다.
연구팀은 싱크로트론 X선 산란장치(synchrotron x-ray
scattering: 전자를 빛의 속도에 가깝게 가속시켜 강력한 X선을 발생시키는 장치)와 투과전자현미경을 이용해 단백질
나노튜브의 자기조립 구조를 서브나노미터(1나노미터 미만)의 정확도로 측정했다.
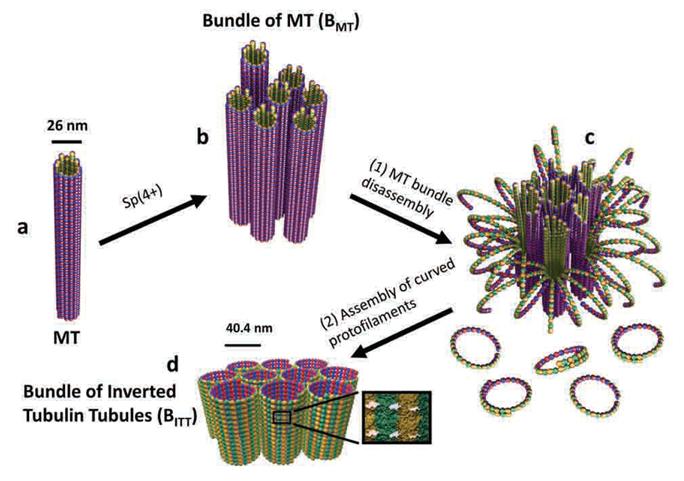
연구팀은 이번 연구를 분자 레벨에서 레고 블록을 쌓아 올리는 것에 비유해
가로×세로×폭이 각각 4×5×8 나노미터인 단백질 블록을 쌓아 올려 25나노미터 굵기의 튜브를 형성하는 메커니즘을 추적했다. 이
과정에서 연구팀은 레고 블록의 형태를 제어하는 분자스위치를 발견했다. 또 지금까지 보고된 바 없는 전혀 새로운 크기와 형태의
단백질 튜브 구조를 만들어 내는데 성공했다.
최명철 교수는 “인간의 생명 시스템은 고도의 자기조립 구조체를 형성해 복잡한 생물학적 기능을 하고 있지만 한편으로는 극히 단순한 물리학적 원리에 의해 제어가 가능하다는 새로운 패러다임을 제시했다”고 이 연구의 의의를 밝혔다.
또 “이번 연구는 암 치료와 뇌질환 메커니즘을 규명하고자하는 작은 발걸음이며 앞으로 바이오 나노튜브를 이용한 공학적 응용이 무궁무진할 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 국제협력사업, 신진연구자지원사업, 학문후속세대양성사업, KAIST 고위험 고수익 프로젝트(High Risk High Return Project)의 지원으로 수행됐다.
2014.01.21 조회수 25144
단백질 나노튜브의 자기조립 분자스위치 발견
- 한국, 미국, 이스라엘 국제 공동 연구 성과 -
- 암 치료와 뇌 질환 메커니즘 단서 -
우리 학교 바이오및뇌공학과 최명철 교수와 송채연 연구교수는 미국
산타바바라 캘리포니아대학교, 이스라엘 히브리대학교와 공동으로 세포분열과 세포간 물질수송에 열쇠가 되는 단백질 나노튜브의 자기조립
구조를 제어하는 분자스위치를 발견했다.
연구 결과는 세계적 학술지 ‘네이처 머티리얼즈(Nature Materials, IF=35.7)’ 19일자에 게재됐다.
마이크로튜불(microtubule, 미세소관)은 사람의 몸속에서 세포분열·세포골격·세포간 물질수송 도구로 사용되는 튜브 형태의 단백질로 굵기가 25나노미터(1나노미터는 머리카락 굵기의 10만분의 1)에 불과하다.
대부분의 암 치료 약물은 마이크로튜불의 형성을 교란해 암세포 분열을
억제하는 것으로 작용 메커니즘이 알려져 있다. 알츠하이머병은 세포간 물질수송을 담당하는 마이크로튜불의 구조적 안정성이 떨어지면서
신경세포에서의 신호전달이 제대로 이루어지지 않아 생기는 대표적 뇌질환이다.
연구팀은 싱크로트론 X선 산란장치(synchrotron x-ray
scattering: 전자를 빛의 속도에 가깝게 가속시켜 강력한 X선을 발생시키는 장치)와 투과전자현미경을 이용해 단백질
나노튜브의 자기조립 구조를 서브나노미터(1나노미터 미만)의 정확도로 측정했다.
연구팀은 이번 연구를 분자 레벨에서 레고 블록을 쌓아 올리는 것에 비유해
가로×세로×폭이 각각 4×5×8 나노미터인 단백질 블록을 쌓아 올려 25나노미터 굵기의 튜브를 형성하는 메커니즘을 추적했다. 이
과정에서 연구팀은 레고 블록의 형태를 제어하는 분자스위치를 발견했다. 또 지금까지 보고된 바 없는 전혀 새로운 크기와 형태의
단백질 튜브 구조를 만들어 내는데 성공했다.
최명철 교수는 “인간의 생명 시스템은 고도의 자기조립 구조체를 형성해 복잡한 생물학적 기능을 하고 있지만 한편으로는 극히 단순한 물리학적 원리에 의해 제어가 가능하다는 새로운 패러다임을 제시했다”고 이 연구의 의의를 밝혔다.
또 “이번 연구는 암 치료와 뇌질환 메커니즘을 규명하고자하는 작은 발걸음이며 앞으로 바이오 나노튜브를 이용한 공학적 응용이 무궁무진할 것으로 기대한다”고 말했다.
이번 연구는 한국연구재단의 국제협력사업, 신진연구자지원사업, 학문후속세대양성사업, KAIST 고위험 고수익 프로젝트(High Risk High Return Project)의 지원으로 수행됐다.
2014.01.21 조회수 25144