%EC%88%98%EC%9A%A9%EC%B2%B4
-
 뉴로모픽 반도체로 통증도 느낀다
최근 인간의 뇌를 모방한 뉴로모픽 반도체 소자 연구가 주목받고 있다. 이에서 더 나아가 최근에는 뇌를 넘어 첨단 센서와 휴머노이드 분야에 적용가능한 감각신경계 모사에 관한 연구가 활발하게 진행되고 있다.
우리 대학 신소재공학과 김경민 교수 연구팀이 새로운 메모리 소자인 멤리스터를 사용하여 통증자극 민감도 조절 기능을 갖는 뉴로모픽 통각수용체 소자를 최초로 구현했다고 15일 밝혔다.
※ 멤리스터(memristor): 메모리(memory)와 저항(resistor)의 합성어로, 전류의 흐름에 따라 저항이 변화하는 전자소자
감각신경계의 핵심적인 역할 중 하나는 유해한 자극을 감지해 위험한 상황을 회피하는 것이다. 특히 통각수용체는 자극이 민감도의 임계치를 넘으면 통증 신호를 발생하여 인체가 자극에서 회피할 수 있도록 한다. 이를 위해 통각수용체의 신호 전달에는 통증 신호를 전달하는 흥분성 신경전달물질(Excitatory Neurotransmitter)과 외부 자극에 대한 임계치를 조절하는 억제성 신경전달물질(Inhibitory Neurotransmitter)이 관여하는 것으로 알려져 있다. 특히 억제성 신경전달물질은 흥분 작용과 역균형을 이뤄 신경의 과도한 활성화를 방지하고, 다양한 외부 자극에 적절하게 반응하기 위한 핵심적인 역할을 가지게 된다. <그림 1> 그동안 이러한 복잡한 감각신경계의 동작을 모사하는 전자 소자를 개발하는 연구가 활발히 진행되었는데, 기존의 연구에서는 흥분성 신경전달물질의 특성은 쉽게 구현할 수 있었으나, 억제성 신경전달물질에 의한 임계치 조절 특성까지 동시에 구현하는데 한계가 있었다.
김경민 교수 연구팀은 이중 전하 저장층 구조를 통해 외부에서의 자극에 대한 임계치를 조절할 수 있는 뉴로모픽 통각수용체 소자를 최초로 개발했다. <그림 2> 두 종류의 서로 다른 전하 저장층은 각각 전도성을 조절하는 흥분성 신경전달물질의 역할과 임계치를 조절하는 억제성 신경전달물질의 역할을 맡아 통각수용체의 필수적인 기능들인 통증 전달 특성(threshold triggering), 통증 완화(Relaxation), 통증 민감화(Sensitization) 등의 특성을 조절할 수 있음을 확인했다. <그림 3> 이는 신경계의 복잡한 기능을 신경계의 동작 원리를 모방하여 단순한 구조의 전자 소자로 구현하는 새로운 방법을 제시한 의의가 있다.
또한, 이 소자는 온도 자극에도 반응하는 온도수용체 특성을 보였으며, 특히 억제성 상태를 제어하여 단일 소자가 고온 범위와 저온 범위를 모두 감지할 수 있는 가변적인 온도수용체 특성을 구현할 수 있었다. <그림 4> 이러한 통각수용체, 온도수용체 소자는 인간을 모방하는 휴머노이드 피부에 적용하여 인간과 같은 방식으로 자극을 감지하는 센서로 활용될 수 있다.
김경민 교수는 "이번 연구는 흥분성 및 억제성 신호 작용의 특성을 단일 소자에 구현해, 간단한 반도체 기술로 복잡한 생물학적 감각신경계의 특성을 모사하는 새로운 방법론을 제시한 것에 큰 의의가 있다ˮ며 "이처럼 임계치를 조절할 수 있는 특성은 감각신경계 모사뿐 아니라 임계 스위칭 특성을 활용하는 보안 소자나 차세대 컴퓨팅 소자에도 활용될 수 있을 것으로 기대된다ˮ고 밝혔다.
한편 이번 연구는 신소재공학과 김근영 석박사통합과정 학생이 제1 저자로 참여했으며, 국제 학술지 `어드밴스드 머티리얼즈(Advanced Materials, Impact Factor: 29.4)'에 10월 21일 字 온라인 게재됐다.
이번 연구는 한국연구재단, 나노종합기술원, KAIST, 그리고 SK 하이닉스의 지원을 받아 수행됐다. (논문명: Threshold Modulative Artificial GABAergic Nociceptor, 논문링크: https://doi.org/10.1002/adma.202304148)
2023.11.15 조회수 8620
뉴로모픽 반도체로 통증도 느낀다
최근 인간의 뇌를 모방한 뉴로모픽 반도체 소자 연구가 주목받고 있다. 이에서 더 나아가 최근에는 뇌를 넘어 첨단 센서와 휴머노이드 분야에 적용가능한 감각신경계 모사에 관한 연구가 활발하게 진행되고 있다.
우리 대학 신소재공학과 김경민 교수 연구팀이 새로운 메모리 소자인 멤리스터를 사용하여 통증자극 민감도 조절 기능을 갖는 뉴로모픽 통각수용체 소자를 최초로 구현했다고 15일 밝혔다.
※ 멤리스터(memristor): 메모리(memory)와 저항(resistor)의 합성어로, 전류의 흐름에 따라 저항이 변화하는 전자소자
감각신경계의 핵심적인 역할 중 하나는 유해한 자극을 감지해 위험한 상황을 회피하는 것이다. 특히 통각수용체는 자극이 민감도의 임계치를 넘으면 통증 신호를 발생하여 인체가 자극에서 회피할 수 있도록 한다. 이를 위해 통각수용체의 신호 전달에는 통증 신호를 전달하는 흥분성 신경전달물질(Excitatory Neurotransmitter)과 외부 자극에 대한 임계치를 조절하는 억제성 신경전달물질(Inhibitory Neurotransmitter)이 관여하는 것으로 알려져 있다. 특히 억제성 신경전달물질은 흥분 작용과 역균형을 이뤄 신경의 과도한 활성화를 방지하고, 다양한 외부 자극에 적절하게 반응하기 위한 핵심적인 역할을 가지게 된다. <그림 1> 그동안 이러한 복잡한 감각신경계의 동작을 모사하는 전자 소자를 개발하는 연구가 활발히 진행되었는데, 기존의 연구에서는 흥분성 신경전달물질의 특성은 쉽게 구현할 수 있었으나, 억제성 신경전달물질에 의한 임계치 조절 특성까지 동시에 구현하는데 한계가 있었다.
김경민 교수 연구팀은 이중 전하 저장층 구조를 통해 외부에서의 자극에 대한 임계치를 조절할 수 있는 뉴로모픽 통각수용체 소자를 최초로 개발했다. <그림 2> 두 종류의 서로 다른 전하 저장층은 각각 전도성을 조절하는 흥분성 신경전달물질의 역할과 임계치를 조절하는 억제성 신경전달물질의 역할을 맡아 통각수용체의 필수적인 기능들인 통증 전달 특성(threshold triggering), 통증 완화(Relaxation), 통증 민감화(Sensitization) 등의 특성을 조절할 수 있음을 확인했다. <그림 3> 이는 신경계의 복잡한 기능을 신경계의 동작 원리를 모방하여 단순한 구조의 전자 소자로 구현하는 새로운 방법을 제시한 의의가 있다.
또한, 이 소자는 온도 자극에도 반응하는 온도수용체 특성을 보였으며, 특히 억제성 상태를 제어하여 단일 소자가 고온 범위와 저온 범위를 모두 감지할 수 있는 가변적인 온도수용체 특성을 구현할 수 있었다. <그림 4> 이러한 통각수용체, 온도수용체 소자는 인간을 모방하는 휴머노이드 피부에 적용하여 인간과 같은 방식으로 자극을 감지하는 센서로 활용될 수 있다.
김경민 교수는 "이번 연구는 흥분성 및 억제성 신호 작용의 특성을 단일 소자에 구현해, 간단한 반도체 기술로 복잡한 생물학적 감각신경계의 특성을 모사하는 새로운 방법론을 제시한 것에 큰 의의가 있다ˮ며 "이처럼 임계치를 조절할 수 있는 특성은 감각신경계 모사뿐 아니라 임계 스위칭 특성을 활용하는 보안 소자나 차세대 컴퓨팅 소자에도 활용될 수 있을 것으로 기대된다ˮ고 밝혔다.
한편 이번 연구는 신소재공학과 김근영 석박사통합과정 학생이 제1 저자로 참여했으며, 국제 학술지 `어드밴스드 머티리얼즈(Advanced Materials, Impact Factor: 29.4)'에 10월 21일 字 온라인 게재됐다.
이번 연구는 한국연구재단, 나노종합기술원, KAIST, 그리고 SK 하이닉스의 지원을 받아 수행됐다. (논문명: Threshold Modulative Artificial GABAergic Nociceptor, 논문링크: https://doi.org/10.1002/adma.202304148)
2023.11.15 조회수 8620 -
 암세포만 공략하는 스마트 면역세포 시스템 개발
우리 대학 바이오및뇌공학과 최정균 교수와 의과학대학원 박종은 교수 공동연구팀이 인공지능과 빅데이터 분석을 기반으로 스마트 면역세포를 통한 암 치료의 핵심 기술을 개발했다고 밝혔다. 이 기술은 키메라 항원 수용체(Chimeric antigen receptor, CAR)가 논리회로를 통해 작동하게 함으로써 정확하게 암세포만 공략할 수 있도록 하는 차세대 면역항암 치료법으로 기대가 모아진다. 이번 연구는 분당차병원 안희정 교수와 가톨릭의대 이혜옥 교수가 공동연구로 참여했다.
최정균 교수 연구팀은 수백만개의 세포에 대한 유전자 발현 데이터베이스를 구축하고 이를 이용해 종양세포와 정상세포 간의 유전자 발현 양상 차이를 논리회로 기반으로 찾아낼 수 있는 딥러닝 알고리즘을 개발하고 검증하는 데 성공했다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용없이 암세포만 정확하게 공략하는 것이 가능하다.
바이오및뇌공학과 권준하 박사, 의과학대학원 강준호 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 '네이처 바이오테크놀로지(Nature Biotechnology)'에 지난 2월 16일 출판됐다. (논문명: Single-cell mapping of combinatorial target antigens for CAR switches using logic gates)
최근의 암 연구에서 가장 많은 시도와 진전이 있었던 분야는 바로 면역항암치료이다. 암환자가 갖고 있는 면역체계를 활용하여 암을 극복하는 이 치료 분야에는 몇 가지 방법이 있는데, 면역관문억제제 및 암백신과 더불어 세포치료 또한 해당된다. 특히, 키메라 항원 수용체를 장착한 CAR-T 혹은 CAR-NK라고 하는 면역세포들은 암항원을 인식하여 암세포를 직접 파괴할 수 있다.
CAR 세포치료는 현재 혈액암에서의 성공을 시작으로 고형암으로 그 적용 범위를 넓히고자 하는 중인데, 혈액암과 달리 고형암에서는 부작용을 최소화하면서 효과적인 암 살상 능력을 보유하는 CAR 세포 개발에 어려움이 있었다. 이에 따라 최근에는 한 단계 진보된 CAR 엔지니어링 기술, 즉 AND, OR, NOT 과 같은 컴퓨터 연산 논리회로를 활용해 효과적으로 암세포를 공략할 수 있는 스마트 면역세포 개발이 활발히 진행되고 있다.
이러한 시점에서, 연구진은 세포 단위에서 정확히 암세포들에서만 발현하는 유전자들을 발굴하기 위해 대규모 암 및 정상 단일세포 데이터베이스를 구축했다. 이어서 연구진은 암세포들과 정상세포들을 가장 잘 구별할 수 있는 유전자 조합을 검색하는 인공지능 알고리즘을 개발했다. 특히 이 알고리즘은, 모든 유전자 조합에 대한 세포 단위 시뮬레이션을 통해 암세포만을 특이적으로 공략할 수 있는 논리회로를 찾아내는데 사용되었다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용은 최소화하면서도 항암치료의 효과는 극대화시킬 수 있을 것으로 기대된다.
제1 저자인 권준하 박사는 "이번 연구는 이전에 시도된 적이 없는 방법론을 제시했는데, 특히 주목할 점은 수백만개의 개별 암세포 및 정상세포들에 대한 시뮬레이션을 통해 최적의 CAR 세포용 회로들을 찾아낸 과정이다ˮ라며 "인공지능과 컴퓨터 논리회로를 면역세포 엔지니어링에 적용하는 획기적인 기술로서 혈액암에서 성공적으로 사용되고 있는 CAR 세포치료가 고형암으로 확대되는데 중요한 역할을 할 것으로 기대된다"고 설명했다.ᅠ
이번 연구는 한국연구재단 원천기술개발사업-차세대응용오믹스사업의 지원을 받아 수행됐다.
2023.03.02 조회수 14460
암세포만 공략하는 스마트 면역세포 시스템 개발
우리 대학 바이오및뇌공학과 최정균 교수와 의과학대학원 박종은 교수 공동연구팀이 인공지능과 빅데이터 분석을 기반으로 스마트 면역세포를 통한 암 치료의 핵심 기술을 개발했다고 밝혔다. 이 기술은 키메라 항원 수용체(Chimeric antigen receptor, CAR)가 논리회로를 통해 작동하게 함으로써 정확하게 암세포만 공략할 수 있도록 하는 차세대 면역항암 치료법으로 기대가 모아진다. 이번 연구는 분당차병원 안희정 교수와 가톨릭의대 이혜옥 교수가 공동연구로 참여했다.
최정균 교수 연구팀은 수백만개의 세포에 대한 유전자 발현 데이터베이스를 구축하고 이를 이용해 종양세포와 정상세포 간의 유전자 발현 양상 차이를 논리회로 기반으로 찾아낼 수 있는 딥러닝 알고리즘을 개발하고 검증하는 데 성공했다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용없이 암세포만 정확하게 공략하는 것이 가능하다.
바이오및뇌공학과 권준하 박사, 의과학대학원 강준호 박사과정 학생이 공동 제1 저자로 참여한 이번 연구는 국제 학술지 '네이처 바이오테크놀로지(Nature Biotechnology)'에 지난 2월 16일 출판됐다. (논문명: Single-cell mapping of combinatorial target antigens for CAR switches using logic gates)
최근의 암 연구에서 가장 많은 시도와 진전이 있었던 분야는 바로 면역항암치료이다. 암환자가 갖고 있는 면역체계를 활용하여 암을 극복하는 이 치료 분야에는 몇 가지 방법이 있는데, 면역관문억제제 및 암백신과 더불어 세포치료 또한 해당된다. 특히, 키메라 항원 수용체를 장착한 CAR-T 혹은 CAR-NK라고 하는 면역세포들은 암항원을 인식하여 암세포를 직접 파괴할 수 있다.
CAR 세포치료는 현재 혈액암에서의 성공을 시작으로 고형암으로 그 적용 범위를 넓히고자 하는 중인데, 혈액암과 달리 고형암에서는 부작용을 최소화하면서 효과적인 암 살상 능력을 보유하는 CAR 세포 개발에 어려움이 있었다. 이에 따라 최근에는 한 단계 진보된 CAR 엔지니어링 기술, 즉 AND, OR, NOT 과 같은 컴퓨터 연산 논리회로를 활용해 효과적으로 암세포를 공략할 수 있는 스마트 면역세포 개발이 활발히 진행되고 있다.
이러한 시점에서, 연구진은 세포 단위에서 정확히 암세포들에서만 발현하는 유전자들을 발굴하기 위해 대규모 암 및 정상 단일세포 데이터베이스를 구축했다. 이어서 연구진은 암세포들과 정상세포들을 가장 잘 구별할 수 있는 유전자 조합을 검색하는 인공지능 알고리즘을 개발했다. 특히 이 알고리즘은, 모든 유전자 조합에 대한 세포 단위 시뮬레이션을 통해 암세포만을 특이적으로 공략할 수 있는 논리회로를 찾아내는데 사용되었다. 이 방법론으로 찾아진 논리회로를 장착한 CAR 면역세포는 마치 컴퓨터처럼 암과 정상 세포를 구별하여 작동함으로써 부작용은 최소화하면서도 항암치료의 효과는 극대화시킬 수 있을 것으로 기대된다.
제1 저자인 권준하 박사는 "이번 연구는 이전에 시도된 적이 없는 방법론을 제시했는데, 특히 주목할 점은 수백만개의 개별 암세포 및 정상세포들에 대한 시뮬레이션을 통해 최적의 CAR 세포용 회로들을 찾아낸 과정이다ˮ라며 "인공지능과 컴퓨터 논리회로를 면역세포 엔지니어링에 적용하는 획기적인 기술로서 혈액암에서 성공적으로 사용되고 있는 CAR 세포치료가 고형암으로 확대되는데 중요한 역할을 할 것으로 기대된다"고 설명했다.ᅠ
이번 연구는 한국연구재단 원천기술개발사업-차세대응용오믹스사업의 지원을 받아 수행됐다.
2023.03.02 조회수 14460 -
 유방암 환자의 면역 항암치료 원리 발견해 효과적인 치료 전략 제시
우리 대학 의과학대학원 신의철 교수 연구팀이 연세대학교 의과대학 김승일 교수, 가톨릭대 의과대학 박우찬 교수 연구팀과 공동 연구를 통해 유방암 환자의 면역 항암치료 핵심 원리를 발견했다고 14일 밝혔다.
이번 연구를 통해, 최근 유행하는 면역 항암치료에 좋은 반응을 보일 것으로 예상되는 유방암 환자들을 선별해 효과적인 암 치료 전략을 제시할 것으로 기대된다.
연세대학교 의과대학 외과학 교실 이용준 강사, 김지예 임상 조교수가 공동 제1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 `사이언스 면역학(Science Immunology)' 8월 26일 字 온라인판에 게재됐다. (논문명 : CD39+ tissue-resident memory CD8+ T cells with a clonal overlap across compartments mediate anti-tumor immunity in breast cancer)
암 환자는 암세포에 대항해 이를 제거하는 역할을 하는 세포독성 T세포의 기능이 현저히 약해져 암세포에 대한 효과적인 면역반응을 나타내지 못한다. 이러한 세포독성 T세포 약화의 주된 이유는 PD-1이라는 세포독성 T세포의 기능을 저하하는 억제 수용체가 종양 조직 내 세포독성 T세포에 과다하게 발현되기 때문으로 알려져 있다.
최근 유행하고 있는 면역항암제의 기본원리는 바로 이 PD-1 억제 수용체의 기능을 차단해 약화돼 있던 세포독성 T세포의 기능을 회복시키는 것이다. 이러한 면역항암제는 유방암 환자에게서 기존의 치료를 대체할 수 있는 표준치료로 자리 잡아 가고 있지만, 투여받은 유방암 환자 중 일부에서만 치료 효과가 나타나며 이에 대한 이유를 알지 못하고 있다. 따라서, 많은 연구자가 유방암에서 면역 항암치료의 기전을 이해하고 치료에 효과를 보이는 환자를 선별하고자 하는 연구를 활발히 수행하고 있다.
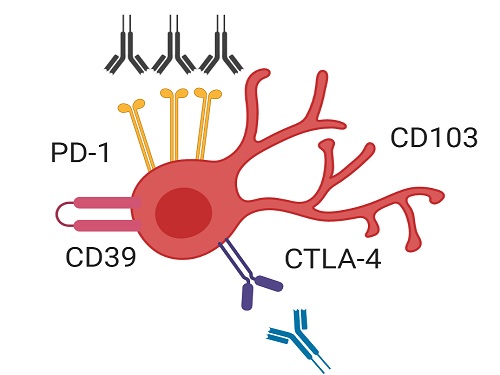
이번 연구에서 공동 연구팀은 종양 조직에 존재하는 세포독성 T세포 중에서도 CD39 단백질과 조직 상주 마커 단백질을 동시에 발현하는 조직 상주 기억 T세포(CD39+ tissue-resident memory CD8+ T cell)가 유방암 환자에서 효과적인 항암 면역반응을 매개하는 핵심 면역세포임을 새롭게 밝혔다.
종양 조직에 존재하는 세포독성 T세포 중에는 항암 면역반응에 영향을 주지 않는 방관자(bystander) 세포들이 존재한다는 사실은 이미 잘 알려져 있었다. 이렇게 항암 면역반응과는 상관없는 방관자 세포들도 종양 조직에 있기 때문에 암 환자의 항암 면역반응을 정확히 측정하고 분석하는 데 어려움이 있었다. 연구팀은 CD39 단백질과 조직 상주 마커 단백질의 발현을 측정해 항암 면역반응과 관련이 있는 세포독성 T세포들만 분리해 개별 환자의 항암 면역반응을 정확히 측정할 수 있음을 새롭게 밝혔다.
그리고 유방암 환자에서 CD39를 발현하는 조직 상주 기억 세포독성 T세포는 특징적으로 삼중음성유방암(triple-negative breast cancer) 환자에게서 증가해 있었고, CD39를 발현하는 조직 상주 기억 세포독성 T세포가 증가해 있는 유방암 환자들은 수술 이후에도 재발이 적게 나타나는 등 좋은 예후를 보였다.
이번 연구에서 연구팀은 유방암 환자에서 면역항암제 치료 효율을 높이는 전략을 제시했다. 구체적으로, CD39를 발현하는 조직 상주 기억 세포독성 T세포들이 PD-1을 차단하는 면역항암제 처리에 반응해 그 기능이 효과적으로 회복됐다. 그리고 CTLA-4라는 다른 억제 수용체까지 함께 차단하자 세포독성 T세포의 기능 회복은 더욱 크게 나타났다. 따라서 이러한 면역항암제의 병용요법을 CD39 발현 조직 상주 기억 세포독성 T세포가 증가해 있는 환자들에게 선별적으로 사용한다면 치료 효과를 극대화할 수 있을 것으로 기대할 수 있다.
이번 연구는 연세대학교 및 가톨릭대 의과대학 외과 연구팀과 KAIST 의과학대학원이 유방암 환자의 항암 면역반응 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로서 중개 연구(translational research)의 주요 성과로 평가받는다.
신의철 교수는 "이번 연구는 항암 면역반응의 메커니즘과 측정에 대해 상세히 연구함으로써 유방암에서 새로운 임상 치료 전략을 제시하게 된 중요한 연구ˮ라며 "향후 암 환자의 생존율을 보다 높일 수 있도록 항암 면역반응 연구 및 면역 항암치료의 *적응증에 관한 연구를 계속하겠다ˮ라고 말했다.
☞ 적응증(indication): 어떠한 약제나 수술 따위에 의하여 치료 효과가 기대되는 병이나 증상
2022.09.14 조회수 9644
유방암 환자의 면역 항암치료 원리 발견해 효과적인 치료 전략 제시
우리 대학 의과학대학원 신의철 교수 연구팀이 연세대학교 의과대학 김승일 교수, 가톨릭대 의과대학 박우찬 교수 연구팀과 공동 연구를 통해 유방암 환자의 면역 항암치료 핵심 원리를 발견했다고 14일 밝혔다.
이번 연구를 통해, 최근 유행하는 면역 항암치료에 좋은 반응을 보일 것으로 예상되는 유방암 환자들을 선별해 효과적인 암 치료 전략을 제시할 것으로 기대된다.
연세대학교 의과대학 외과학 교실 이용준 강사, 김지예 임상 조교수가 공동 제1 저자로 참여한 이번 연구 결과는 면역학 분야 국제 학술지 `사이언스 면역학(Science Immunology)' 8월 26일 字 온라인판에 게재됐다. (논문명 : CD39+ tissue-resident memory CD8+ T cells with a clonal overlap across compartments mediate anti-tumor immunity in breast cancer)
암 환자는 암세포에 대항해 이를 제거하는 역할을 하는 세포독성 T세포의 기능이 현저히 약해져 암세포에 대한 효과적인 면역반응을 나타내지 못한다. 이러한 세포독성 T세포 약화의 주된 이유는 PD-1이라는 세포독성 T세포의 기능을 저하하는 억제 수용체가 종양 조직 내 세포독성 T세포에 과다하게 발현되기 때문으로 알려져 있다.
최근 유행하고 있는 면역항암제의 기본원리는 바로 이 PD-1 억제 수용체의 기능을 차단해 약화돼 있던 세포독성 T세포의 기능을 회복시키는 것이다. 이러한 면역항암제는 유방암 환자에게서 기존의 치료를 대체할 수 있는 표준치료로 자리 잡아 가고 있지만, 투여받은 유방암 환자 중 일부에서만 치료 효과가 나타나며 이에 대한 이유를 알지 못하고 있다. 따라서, 많은 연구자가 유방암에서 면역 항암치료의 기전을 이해하고 치료에 효과를 보이는 환자를 선별하고자 하는 연구를 활발히 수행하고 있다.
이번 연구에서 공동 연구팀은 종양 조직에 존재하는 세포독성 T세포 중에서도 CD39 단백질과 조직 상주 마커 단백질을 동시에 발현하는 조직 상주 기억 T세포(CD39+ tissue-resident memory CD8+ T cell)가 유방암 환자에서 효과적인 항암 면역반응을 매개하는 핵심 면역세포임을 새롭게 밝혔다.
종양 조직에 존재하는 세포독성 T세포 중에는 항암 면역반응에 영향을 주지 않는 방관자(bystander) 세포들이 존재한다는 사실은 이미 잘 알려져 있었다. 이렇게 항암 면역반응과는 상관없는 방관자 세포들도 종양 조직에 있기 때문에 암 환자의 항암 면역반응을 정확히 측정하고 분석하는 데 어려움이 있었다. 연구팀은 CD39 단백질과 조직 상주 마커 단백질의 발현을 측정해 항암 면역반응과 관련이 있는 세포독성 T세포들만 분리해 개별 환자의 항암 면역반응을 정확히 측정할 수 있음을 새롭게 밝혔다.
그리고 유방암 환자에서 CD39를 발현하는 조직 상주 기억 세포독성 T세포는 특징적으로 삼중음성유방암(triple-negative breast cancer) 환자에게서 증가해 있었고, CD39를 발현하는 조직 상주 기억 세포독성 T세포가 증가해 있는 유방암 환자들은 수술 이후에도 재발이 적게 나타나는 등 좋은 예후를 보였다.
이번 연구에서 연구팀은 유방암 환자에서 면역항암제 치료 효율을 높이는 전략을 제시했다. 구체적으로, CD39를 발현하는 조직 상주 기억 세포독성 T세포들이 PD-1을 차단하는 면역항암제 처리에 반응해 그 기능이 효과적으로 회복됐다. 그리고 CTLA-4라는 다른 억제 수용체까지 함께 차단하자 세포독성 T세포의 기능 회복은 더욱 크게 나타났다. 따라서 이러한 면역항암제의 병용요법을 CD39 발현 조직 상주 기억 세포독성 T세포가 증가해 있는 환자들에게 선별적으로 사용한다면 치료 효과를 극대화할 수 있을 것으로 기대할 수 있다.
이번 연구는 연세대학교 및 가톨릭대 의과대학 외과 연구팀과 KAIST 의과학대학원이 유방암 환자의 항암 면역반응 원리를 밝히고 새로운 치료 전략을 제시하기 위해 협동 연구를 한 것으로서 중개 연구(translational research)의 주요 성과로 평가받는다.
신의철 교수는 "이번 연구는 항암 면역반응의 메커니즘과 측정에 대해 상세히 연구함으로써 유방암에서 새로운 임상 치료 전략을 제시하게 된 중요한 연구ˮ라며 "향후 암 환자의 생존율을 보다 높일 수 있도록 항암 면역반응 연구 및 면역 항암치료의 *적응증에 관한 연구를 계속하겠다ˮ라고 말했다.
☞ 적응증(indication): 어떠한 약제나 수술 따위에 의하여 치료 효과가 기대되는 병이나 증상
2022.09.14 조회수 9644 -
 호르몬 조절 수용체 구조와 작용 메커니즘 규명으로 뇌기능 향상 물질 개발 가속
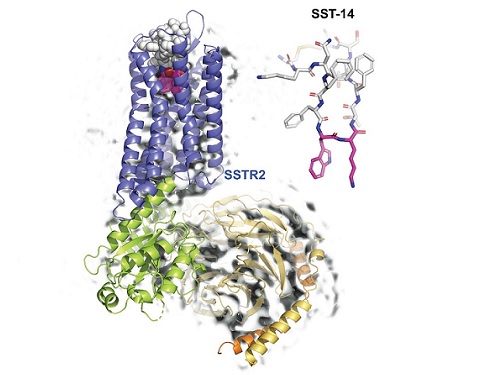
우리 대학 생명과학과 송지준 교수 연구팀이 초저온 전자 현미경(cryo-Electron Microscopy)을 이용해 호르몬 조절 물질인 소마토스타틴(somatostatin)과 그 수용체인 소마토스타틴 리셉터 2(Somatostatin Receptor 2, 이하 SSTR2) 복합체의 3차원 원자 해상도 구조를 규명해 호르몬 조절 메커니즘을 밝혔다고 6일 밝혔다.
소마토스타틴은 성장호르몬의 분비를 억제하는 작용이 있는 호르몬으로 내장과 뇌에 관련된 호르몬이며, 호르몬 분비 조절, 세포의 증식, 뇌 신경 물질 전달에 관한 작용을 한다.
송 교수 연구팀은 연세대학교 이원태 교수 연구팀, 피씨지-바이오텍 연구팀과의 공동연구를 통해, 소마토스타틴과 결합해 다양한 호르몬의 분비를 억제하는 SSTR2 복합체 구조를 3차원 원자 해상도로 초저온 전자현미경을 이용해 규명하고, 소마토스타틴이 SSTR2를 통해 호르몬 분비를 억제하는 메커니즘을 규명했다. 이러한 연구 결과는 호르몬 분비의 이상에서 유발되는 말단비대증, 신경 뇌분비 종양을 제어하는 방법을 개발하는데 적용될 수 있을 것으로 기대된다.
생명과학과 윤어진 박사과정이 공동 제1 저자로 참여한 이번 연구는 국제 저명 학술지 `이라이프(eLife)' 에 4월 22일에 출판됐다. (논문명 : Cryo-EM structure of the human somatostatin receptor 2 complex with its agonist somatostatin delineates the ligand binding specificity)
SSTR2은 세포막에 존재하는 막 단백질로, 세포 밖의 소마토스타틴을 신호로 인식해 세포 내로 전달하는 역할을 한다. 최근 생명과학과 이승희 교수 연구팀에서도 소마토스타틴이 인지기능 향상에 기여한다 것을 밝힌 바 있다. 이렇게 소마토스타틴의 생체 내 기능 및 질병에 역할의 중요성에도 불구하고, 소마토스타틴이 세포막에 존재하는 수용체와 결합하는 자세한 메커니즘에 대해서는 알려지지 않았고, 신약 개발에 필수적인 역할을 하는, 3차원 원자구조는 알려지지 않았다.
송지준 교수 연구팀은 소마토스타틴이 수용체인 SSTR2와 결합하는 원리를 규명하기 위해, 초저온 전자현미경을 이용해 소마토스타틴이 결합된 SSTR2 복합체의 원자 3차원 구조를 규명했다. 또한 연구팀은 소마토스타틴과 수용체가 결합한 3차원 구조를 바탕으로 소마토스타틴과 결합하는데 중요한 아미노산들을 발견하고, 이들의 기능성을 세포 내에서 확인했다.
연구팀은 더 나아가 인공지능을 이용한 구조예측 프로그램인 알파폴드(AlphaFold)를 이용해 소마토스타틴 수용체의 이성질 형태(같은 분자식을 갖는 화합물이지만 분자 구조가 다른 형태)인 SSTR1, SSTR3, SSTR4, SSTR5의 구조를 예측해 이성질 형태 각각의 소마토스타틴 결합 메커니즘을 밝혀냈다.
이번 연구 결과는 소마토스타틴 수용체의 작용 메커니즘을 이용해 말단비대증, 신경뇌분비 종양의 제어 및 뇌기능을 향상할 수 있는 물질 개발에 이용될 수 있을 것으로 기대된다.
한편 이번 연구는 한국연구재단 바이오-의료기술개발사업의 지원을 받아 수행됐다.
2022.05.09 조회수 9364
호르몬 조절 수용체 구조와 작용 메커니즘 규명으로 뇌기능 향상 물질 개발 가속
우리 대학 생명과학과 송지준 교수 연구팀이 초저온 전자 현미경(cryo-Electron Microscopy)을 이용해 호르몬 조절 물질인 소마토스타틴(somatostatin)과 그 수용체인 소마토스타틴 리셉터 2(Somatostatin Receptor 2, 이하 SSTR2) 복합체의 3차원 원자 해상도 구조를 규명해 호르몬 조절 메커니즘을 밝혔다고 6일 밝혔다.
소마토스타틴은 성장호르몬의 분비를 억제하는 작용이 있는 호르몬으로 내장과 뇌에 관련된 호르몬이며, 호르몬 분비 조절, 세포의 증식, 뇌 신경 물질 전달에 관한 작용을 한다.
송 교수 연구팀은 연세대학교 이원태 교수 연구팀, 피씨지-바이오텍 연구팀과의 공동연구를 통해, 소마토스타틴과 결합해 다양한 호르몬의 분비를 억제하는 SSTR2 복합체 구조를 3차원 원자 해상도로 초저온 전자현미경을 이용해 규명하고, 소마토스타틴이 SSTR2를 통해 호르몬 분비를 억제하는 메커니즘을 규명했다. 이러한 연구 결과는 호르몬 분비의 이상에서 유발되는 말단비대증, 신경 뇌분비 종양을 제어하는 방법을 개발하는데 적용될 수 있을 것으로 기대된다.
생명과학과 윤어진 박사과정이 공동 제1 저자로 참여한 이번 연구는 국제 저명 학술지 `이라이프(eLife)' 에 4월 22일에 출판됐다. (논문명 : Cryo-EM structure of the human somatostatin receptor 2 complex with its agonist somatostatin delineates the ligand binding specificity)
SSTR2은 세포막에 존재하는 막 단백질로, 세포 밖의 소마토스타틴을 신호로 인식해 세포 내로 전달하는 역할을 한다. 최근 생명과학과 이승희 교수 연구팀에서도 소마토스타틴이 인지기능 향상에 기여한다 것을 밝힌 바 있다. 이렇게 소마토스타틴의 생체 내 기능 및 질병에 역할의 중요성에도 불구하고, 소마토스타틴이 세포막에 존재하는 수용체와 결합하는 자세한 메커니즘에 대해서는 알려지지 않았고, 신약 개발에 필수적인 역할을 하는, 3차원 원자구조는 알려지지 않았다.
송지준 교수 연구팀은 소마토스타틴이 수용체인 SSTR2와 결합하는 원리를 규명하기 위해, 초저온 전자현미경을 이용해 소마토스타틴이 결합된 SSTR2 복합체의 원자 3차원 구조를 규명했다. 또한 연구팀은 소마토스타틴과 수용체가 결합한 3차원 구조를 바탕으로 소마토스타틴과 결합하는데 중요한 아미노산들을 발견하고, 이들의 기능성을 세포 내에서 확인했다.
연구팀은 더 나아가 인공지능을 이용한 구조예측 프로그램인 알파폴드(AlphaFold)를 이용해 소마토스타틴 수용체의 이성질 형태(같은 분자식을 갖는 화합물이지만 분자 구조가 다른 형태)인 SSTR1, SSTR3, SSTR4, SSTR5의 구조를 예측해 이성질 형태 각각의 소마토스타틴 결합 메커니즘을 밝혀냈다.
이번 연구 결과는 소마토스타틴 수용체의 작용 메커니즘을 이용해 말단비대증, 신경뇌분비 종양의 제어 및 뇌기능을 향상할 수 있는 물질 개발에 이용될 수 있을 것으로 기대된다.
한편 이번 연구는 한국연구재단 바이오-의료기술개발사업의 지원을 받아 수행됐다.
2022.05.09 조회수 9364 -
 췌장 내 미토콘드리아 기능 장애, 췌장염에 이어 췌장암 위험성 높여
우리 대학 의과학대학원 서재명 교수 연구팀은 Salk 연구소 로날드 에반스(Ronald M. Evans) 교수, Harbor-UCLA 병원 에이지 요시하라(Eiji Yoshihara) 교수와 국제공동 연구를 통해 에너지 대사 및 생리기능 조절에 중요한 에스트로겐 관련 수용체 감마(ERRγ)의 기능부전이 췌장염 및 췌장 외분비선 질환을 유발할 수 있음을 22일 밝혔다.
췌장조직에서는 하루 동안 한 컵 정도의 소화액을 생산하고 분비한다. 그러나 소화액이 장으로 이동하기 전에 활성화되면 췌장조직 자체에 심각한 손상이 일어나며, 이로 인해 췌장염이 발생하게 된다. 대표적인 췌장염의 원인은 담석이 담췌관을 막아 소화액이 역류하거나 과도한 음주로 인해 췌장 세포의 에너지 항상성이 무너지면서 세포사멸을 유발함으로써 발병한다고 알려져 있다. 만성적인 췌장염은 극심한 고통을 수반함과 더불어 치사율 높은 췌장암의 원인이 될 수도 있어서 학계에서는 주목하고 있는 분야다.
연구팀은 “다량의 소화액을 분비하는 췌장 세포는 많은 양의 에너지를 소모하기 때문에, 에너지대사 기능이 저하되면 췌장염을 비롯한 다양한 췌장 질환에 노출될 수 있다. 건강한 췌장기능을 유지하기 위해 강력한 미토콘드리아의 에너지 생산 체계가 필요하다고 알려져 있었으나 췌장 미토콘드리아 에너지대사의 핵심 조절인자는 알려져 있지 않았다. 본 연구 결과는 ERRγ가 췌장 에너지 생성에 필수적일 뿐만 아니라 ERRγ의 기능이상이 췌장염과 췌장암 초기 발병기전에 관여한다는 점을 보여준다”고 밝혔다.
연구진은 췌장염 환자의 췌장 세포가 정상세포에 비해 ERRγ 유전자 활성이 감소하여 있음을 밝혀 임상적 연결고리를 보여주었으며, 이러한 발견은 ERRγ의 유전자 활성 조절을 통해 췌장염과 췌장암을 예방하거나 치료할 새로운 가능성을 열었다.
현재 연구팀은 미토콘드리아 조절 장애 및 췌장염이 초래하는 초기 췌장암을 예방하거나 치료하는 데 있어 ERRγ 활성 조절을 활용한 후속 연구를 이어가고 있다고 전했다.
우리 대학 의과학대학원 최진혁 박사와 Salk 연구소 오태규 박사가 공동 제1저자로 참여한 이번 연구는 4월 21일 소화기분야 최고 권위 저널인 ‘가스트로엔터롤로지 (Gastroenterology, IF 22.682)’ 온라인판에 게재됐다. (논문명: Estrogen-Related Receptor γ maintains pancreatic acinar cell function and identity by regulating cellular metabolism).
이번 연구는 과학기술정보통신부와 대구경북첨단의료산업진흥재단 원천기술개발사업, 과학기술정보통신부 글로벌연구실사업 및 한국과학기술원 국제공동연구지원사업의 지원을 받아 수행됐다.
2022.04.22 조회수 9352
췌장 내 미토콘드리아 기능 장애, 췌장염에 이어 췌장암 위험성 높여
우리 대학 의과학대학원 서재명 교수 연구팀은 Salk 연구소 로날드 에반스(Ronald M. Evans) 교수, Harbor-UCLA 병원 에이지 요시하라(Eiji Yoshihara) 교수와 국제공동 연구를 통해 에너지 대사 및 생리기능 조절에 중요한 에스트로겐 관련 수용체 감마(ERRγ)의 기능부전이 췌장염 및 췌장 외분비선 질환을 유발할 수 있음을 22일 밝혔다.
췌장조직에서는 하루 동안 한 컵 정도의 소화액을 생산하고 분비한다. 그러나 소화액이 장으로 이동하기 전에 활성화되면 췌장조직 자체에 심각한 손상이 일어나며, 이로 인해 췌장염이 발생하게 된다. 대표적인 췌장염의 원인은 담석이 담췌관을 막아 소화액이 역류하거나 과도한 음주로 인해 췌장 세포의 에너지 항상성이 무너지면서 세포사멸을 유발함으로써 발병한다고 알려져 있다. 만성적인 췌장염은 극심한 고통을 수반함과 더불어 치사율 높은 췌장암의 원인이 될 수도 있어서 학계에서는 주목하고 있는 분야다.
연구팀은 “다량의 소화액을 분비하는 췌장 세포는 많은 양의 에너지를 소모하기 때문에, 에너지대사 기능이 저하되면 췌장염을 비롯한 다양한 췌장 질환에 노출될 수 있다. 건강한 췌장기능을 유지하기 위해 강력한 미토콘드리아의 에너지 생산 체계가 필요하다고 알려져 있었으나 췌장 미토콘드리아 에너지대사의 핵심 조절인자는 알려져 있지 않았다. 본 연구 결과는 ERRγ가 췌장 에너지 생성에 필수적일 뿐만 아니라 ERRγ의 기능이상이 췌장염과 췌장암 초기 발병기전에 관여한다는 점을 보여준다”고 밝혔다.
연구진은 췌장염 환자의 췌장 세포가 정상세포에 비해 ERRγ 유전자 활성이 감소하여 있음을 밝혀 임상적 연결고리를 보여주었으며, 이러한 발견은 ERRγ의 유전자 활성 조절을 통해 췌장염과 췌장암을 예방하거나 치료할 새로운 가능성을 열었다.
현재 연구팀은 미토콘드리아 조절 장애 및 췌장염이 초래하는 초기 췌장암을 예방하거나 치료하는 데 있어 ERRγ 활성 조절을 활용한 후속 연구를 이어가고 있다고 전했다.
우리 대학 의과학대학원 최진혁 박사와 Salk 연구소 오태규 박사가 공동 제1저자로 참여한 이번 연구는 4월 21일 소화기분야 최고 권위 저널인 ‘가스트로엔터롤로지 (Gastroenterology, IF 22.682)’ 온라인판에 게재됐다. (논문명: Estrogen-Related Receptor γ maintains pancreatic acinar cell function and identity by regulating cellular metabolism).
이번 연구는 과학기술정보통신부와 대구경북첨단의료산업진흥재단 원천기술개발사업, 과학기술정보통신부 글로벌연구실사업 및 한국과학기술원 국제공동연구지원사업의 지원을 받아 수행됐다.
2022.04.22 조회수 9352 -
 면역관문 신호 극복하는 차세대 CAR-T 세포 치료제 개발
우리 대학 생명과학과 김찬혁 교수 연구팀이 면역관문 신호를 극복하는 차세대 `키메라 항원 수용체 T(chimeric antigen receptor T, 이하 CAR-T) 세포' 치료제를 개발했다고 20일 밝혔다.
CAR-T 세포 치료제는 우리 몸에서 항암 및 항바이러스 기능에 중요한 역할을 하는 면역세포인 T 세포에 CAR 유전자를 도입해 항암 기능을 증가시킨 유전자 세포 치료제로서, 기존의 모든 항암 치료에 불응한 말기 백혈병 환자들을 대상으로 한 임상 시험에서 80% 이상의 높은 치료 효과를 보이며 `기적의 항암제'로 불리고 있는 항암 치료제다.
김 교수 연구팀은 CAR-T 세포 치료제 제작에 사용되는 렌티바이러스 벡터를 2종류의 짧은 헤어핀 RNA(short hairpin RNA, 이하 shRNA)가 CAR 유전자와 함께 발현하도록 개량했다. 이들 shRNA를 통해 T 세포의 기능 저하를 유도하는 2종의 면역관문 수용체인 `PD-1'과 `TIGIT'의 발현을 동시에 억제했을 때, 생쥐를 이용한 백혈병과 림프종 모델에서 CAR-T 세포의 향상된 항암 기능을 확인했다.
우리 대학 생명과학과 이영호 박사후연구원이 제1 저자 및 공동교신 저자로 참여한 이번 연구는 미국 유전자 세포 치료제 학회(American Society of Gene & Cell Therapy, ASGCT) 공식 학술지인 `분자 치료(Molecular Therapy)' 10월 온라인 판에 출판됐다. (논문명 : PD-1 and TIGIT downregulation distinctly affect the effector and early memory phenotypes of CD19-targeting CAR T cells).
해당 기술은 김 교수가 공동 창업한 CAR-T 세포 치료제 전문 개발 벤처인 ㈜큐로셀에 기술이전되어 올해 3월부터 삼성서울병원에서 기존 항암 치료 후 재발 및 불응하는 미만성 거대 B 세포 림프종 (diffuse large B cell lymphoma, DLBCL) 환자를 대상으로 1b/2a 단계 임상 시험이 진행중이며, 이는 국내에서 국내기술로 시도된 최초의 CAR-T 임상시험이다.
높은 항암 효과로 미국에서는 2017년 최초 2종의 CAR-T 치료제가 허가를 받았고, 산학계의 활발한 연구를 바탕으로 현재까지 총 5종의 CAR-T 치료제가 허가를 받았다. 최근에는 중국이 대규모 투자와 공격적인 임상 연구를 진행하며 CAR-T 치료제 분야의 새로운 강국으로 급부상해, 현재 전 세계적으로 진행 중인 500여 건의 CAR-T 임상 시험 중 절반 이상이 중국에서 진행되고 있다. 반면 현재 국내에서는 1건의 임상 시험 만이 진행 중이다.
이처럼 높은 치료 효과로 많은 관심을 받는 CAR-T 치료제이지만 지금까지 임상에서 극적인 효과를 보인 암종이 B 세포성 급성 백혈병과 다발 골수종 같은 혈액암에 국한돼 있으며, 혈액암 중에서도 B 세포성 만성 백혈병과 림프종에서는 상대적으로 치료 효과가 낮다는 점, 그리고 무엇보다 고형암에서 높은 효과를 보이는 CAR-T 치료제가 아직 없다는 것이 중요하게 해결해야 할 과제로 대두되고 있다.
연구팀은 CAR-T 세포의 효능을 제한할 수 있는 잠재적인 요소 중, T 세포의 활성을 억제하는 기능을 갖는 면역관문 수용체에 주목했다. T 세포에 발현하는 다양한 면역관문 수용체들은 본래 T 세포가 지속해서 활성화될 때 생기는 부작용을 방지하는 기능을 하고 있으나, 암세포가 이를 악용해 T 세포의 활성을 떨어뜨림으로써 면역계의 작용을 회피하는 메커니즘이 잘 알려져 있다.
연구팀은 2종의 shRNA를 동시에 발현하는 플랫폼을 기반으로 다양한 조합의 면역관문 수용체들의 발현을 억제해 보았고, 흥미롭게도 PD-1과 TIGIT의 조합이 유독 CAR-T 세포의 기능을 높게 향상하는 것을 발견했다. 이후 연구팀은 전사체 분석 및 세포 기능 시험을 통해 흥미롭게도 PD-1의 발현 억제는 CAR-T 세포의 작용 기능(effector function)을 향상하는 데 비해 TIGIT의 발현 억제는 분화를 지연시켜 생체 내에서 CAR-T 세포의 증식 및 지속성을 향상하는 것을 밝혔다.
제1 저자이자 공동교신 저자인 이영호 박사후연구원은 "PD-1과 TIGIT 신호 차단은 CAR-T 세포가 면역억제 현상을 극복할 수 있도록 고안된 새로운 기술 전략으로 기존 치료제의 효과를 기대하기 힘든 림프종 환자분들에게 꼭 필요한 치료제로 여겨질 것으로 기대한다ˮ라며 "CAR-T 치료제 개발 경험은 고형암을 포함하는 새로운 치료제 개발에 큰 자양분이 될 것이다ˮ라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자 지원사업 및 과학기술정보통신부 신약개발지원센터 R&D 지원 사업의 지원을 받아 수행됐다.
2021.10.21 조회수 13184
면역관문 신호 극복하는 차세대 CAR-T 세포 치료제 개발
우리 대학 생명과학과 김찬혁 교수 연구팀이 면역관문 신호를 극복하는 차세대 `키메라 항원 수용체 T(chimeric antigen receptor T, 이하 CAR-T) 세포' 치료제를 개발했다고 20일 밝혔다.
CAR-T 세포 치료제는 우리 몸에서 항암 및 항바이러스 기능에 중요한 역할을 하는 면역세포인 T 세포에 CAR 유전자를 도입해 항암 기능을 증가시킨 유전자 세포 치료제로서, 기존의 모든 항암 치료에 불응한 말기 백혈병 환자들을 대상으로 한 임상 시험에서 80% 이상의 높은 치료 효과를 보이며 `기적의 항암제'로 불리고 있는 항암 치료제다.
김 교수 연구팀은 CAR-T 세포 치료제 제작에 사용되는 렌티바이러스 벡터를 2종류의 짧은 헤어핀 RNA(short hairpin RNA, 이하 shRNA)가 CAR 유전자와 함께 발현하도록 개량했다. 이들 shRNA를 통해 T 세포의 기능 저하를 유도하는 2종의 면역관문 수용체인 `PD-1'과 `TIGIT'의 발현을 동시에 억제했을 때, 생쥐를 이용한 백혈병과 림프종 모델에서 CAR-T 세포의 향상된 항암 기능을 확인했다.
우리 대학 생명과학과 이영호 박사후연구원이 제1 저자 및 공동교신 저자로 참여한 이번 연구는 미국 유전자 세포 치료제 학회(American Society of Gene & Cell Therapy, ASGCT) 공식 학술지인 `분자 치료(Molecular Therapy)' 10월 온라인 판에 출판됐다. (논문명 : PD-1 and TIGIT downregulation distinctly affect the effector and early memory phenotypes of CD19-targeting CAR T cells).
해당 기술은 김 교수가 공동 창업한 CAR-T 세포 치료제 전문 개발 벤처인 ㈜큐로셀에 기술이전되어 올해 3월부터 삼성서울병원에서 기존 항암 치료 후 재발 및 불응하는 미만성 거대 B 세포 림프종 (diffuse large B cell lymphoma, DLBCL) 환자를 대상으로 1b/2a 단계 임상 시험이 진행중이며, 이는 국내에서 국내기술로 시도된 최초의 CAR-T 임상시험이다.
높은 항암 효과로 미국에서는 2017년 최초 2종의 CAR-T 치료제가 허가를 받았고, 산학계의 활발한 연구를 바탕으로 현재까지 총 5종의 CAR-T 치료제가 허가를 받았다. 최근에는 중국이 대규모 투자와 공격적인 임상 연구를 진행하며 CAR-T 치료제 분야의 새로운 강국으로 급부상해, 현재 전 세계적으로 진행 중인 500여 건의 CAR-T 임상 시험 중 절반 이상이 중국에서 진행되고 있다. 반면 현재 국내에서는 1건의 임상 시험 만이 진행 중이다.
이처럼 높은 치료 효과로 많은 관심을 받는 CAR-T 치료제이지만 지금까지 임상에서 극적인 효과를 보인 암종이 B 세포성 급성 백혈병과 다발 골수종 같은 혈액암에 국한돼 있으며, 혈액암 중에서도 B 세포성 만성 백혈병과 림프종에서는 상대적으로 치료 효과가 낮다는 점, 그리고 무엇보다 고형암에서 높은 효과를 보이는 CAR-T 치료제가 아직 없다는 것이 중요하게 해결해야 할 과제로 대두되고 있다.
연구팀은 CAR-T 세포의 효능을 제한할 수 있는 잠재적인 요소 중, T 세포의 활성을 억제하는 기능을 갖는 면역관문 수용체에 주목했다. T 세포에 발현하는 다양한 면역관문 수용체들은 본래 T 세포가 지속해서 활성화될 때 생기는 부작용을 방지하는 기능을 하고 있으나, 암세포가 이를 악용해 T 세포의 활성을 떨어뜨림으로써 면역계의 작용을 회피하는 메커니즘이 잘 알려져 있다.
연구팀은 2종의 shRNA를 동시에 발현하는 플랫폼을 기반으로 다양한 조합의 면역관문 수용체들의 발현을 억제해 보았고, 흥미롭게도 PD-1과 TIGIT의 조합이 유독 CAR-T 세포의 기능을 높게 향상하는 것을 발견했다. 이후 연구팀은 전사체 분석 및 세포 기능 시험을 통해 흥미롭게도 PD-1의 발현 억제는 CAR-T 세포의 작용 기능(effector function)을 향상하는 데 비해 TIGIT의 발현 억제는 분화를 지연시켜 생체 내에서 CAR-T 세포의 증식 및 지속성을 향상하는 것을 밝혔다.
제1 저자이자 공동교신 저자인 이영호 박사후연구원은 "PD-1과 TIGIT 신호 차단은 CAR-T 세포가 면역억제 현상을 극복할 수 있도록 고안된 새로운 기술 전략으로 기존 치료제의 효과를 기대하기 힘든 림프종 환자분들에게 꼭 필요한 치료제로 여겨질 것으로 기대한다ˮ라며 "CAR-T 치료제 개발 경험은 고형암을 포함하는 새로운 치료제 개발에 큰 자양분이 될 것이다ˮ라고 말했다.
한편 이번 연구는 한국연구재단 중견연구자 지원사업 및 과학기술정보통신부 신약개발지원센터 R&D 지원 사업의 지원을 받아 수행됐다.
2021.10.21 조회수 13184 -
 서성배 교수 연구팀, 동물의 식습관을 조절하는 원리 규명해 네이처 게재
우리 대학 생명과학과 서성배 교수 연구팀이 서울대학교 생명과학부 이원재 교수 연구팀과 공동연구를 통해 체내 단백질, 필수아미노산 부족을 감지하는 장 세포와 필수아미노산을 섭취하도록 섭식행동을 조절하는 구체적인 원리를 규명했다고 7일 밝혔다. 그뿐만 아니라, 공동연구팀은 필수아미노산을 생산하는 장내미생물이 이러한 메커니즘에 어떠한 영향을 미치는 지도 규명했다.
사람이든 동물이든 수분이 부족하면 갈증을 느끼고 물을 마시고, 혈당량이 떨어지면 당을 찾아 먹는다. 필수 영양소가 부족하면 자연스럽게 이를 섭취하기 위한 행동 변화가 있다는 것은 누구나 경험적으로 쉽게 알 수 있는 사실이다. 과학자들은 수분이나 당분뿐만 아니라 필수아미노산과 같은 영양소에 대해서도 동물들이 결핍을 인지하여 항상성을 유지하는 메커니즘을 가지고 있을 것이라 오랫동안 예상해 왔지만, 그동안 이를 구체적으로 밝힌 연구는 없었다.
필수아미노산 항상성은 수분 항상성보다 복잡한 메커니즘을 가질 수밖에 없다. 장내미생물의 종류에 따라 반드시 섭취해야 하는 필수아미노산의 종류가 달라지기 때문이다. 예를 들면, 코알라의 경우 주된 먹이가 되는 나뭇잎의 섬유질을 직접 소화하지 못하고, 장내미생물이 나뭇잎을 분해하여 흡수 가능한 영양소를 만들어 내면 이를 흡수한다. 그런데 장내미생물의 종류에 따라 분해할 수 있는 나뭇잎의 종류가 달라지고, 이에 따라 코알라의 식성도 달라진다. 이는 필수아미노산과 같이 미생물을 통해 합성이 가능한 영양소의 경우, 똑같은 종의 동물들이라 해도, 동일한 필수아미노산이 부족한 상황에서 각 개체가 보유하고 있는 장내미생물의 종류에 따라 다른 식성을 보일 수 있다는 것을 의미한다.
공동연구팀은 이번 연구에서 어떤 유전자가 체내 필수아미노산 부족을 감지하는지 찾아내고, 어떤 신호를 통해 부족한 아미노산을 섭취하도록 섭식행동을 조절하는지 규명했으며, 필수아미노산을 생산하는 장내미생물이 이러한 메커니즘에 어떠한 영향을 미치는지 확인하기 위한 실험을 진행했다.
연구진은 초파리에 필수아미노산이 결핍된 먹이를 제공하거나 유전적 결핍 혹은 유전자 조작을 이용해 필수아미노산을 생산하지 못하는 장내미생물을 초파리에 도입하면, 초파리의 장 호르몬 중 하나인 CNMa 호르몬의 발현이 유도됨을 확인했다. 흥미롭게도, 이 호르몬은 그동안 장 호르몬이 발현된다고 알려진 내분비세포 (enteroendocrine cells)가 아닌 장 상피세포(enterocytes)에서 발현되는데 이는 장 상피세포가 필수아미노산 결핍을 직접 인지한다는 것을 의미한다. 또한 공동연구팀은 CNMa 호르몬이 발현되는 과정에서 기존에 세포 내 아미노산 센서로 잘 알려진 Gcn2와 Tor 분자들이 관여한다는 사실도 증명했다. CNMa 호르몬의 수용체는 두뇌와 장 신경세포(enteric neuron)에서 발현하는데 CNMa 수용체를 발현하는 신경세포가 활성화되는지 여부에 따라 필수아미노산을 섭취하려는 섭식행동이 증가하거나 감소한다.
이번 논문은 동물이 필수아미노산의 부족을 인지한 후 필수아미노산이 풍부한 음식을 섭취하는 행동을 장내미생물-장-뇌 축(microbiome-gut-brain axis)을 통해 분자적 수준에서 설명한 최초의 논문이다.
제 1저자인 우리 대학 김보람 연구원은 “이번 연구 결과는 장내미생물에서 동물의 장 그리고 뇌로 이어지는 장내미생물-장-뇌 축을 통해 아미노산 결핍이 일어난다는 사실을 처음으로 밝혔다는데 큰 의미가 있으며, 초파리뿐만 아니라, 사람을 포함한 척추동물에서도 이런 경로를 통해 장내미생물이 동물의 식성을 조절할 가능성을 제기한다. 만약 장내미생물과 동물의 식습관이 장뇌 축을 통해 조절된다면, 미생물 섭취라는 방법을 통해 현대인의 불균형한 식습관으로 인한 만성 질병을 개선할 수도 있을 것이며, 그런 점에서 이 논문의 가치를 찾을 수 있다”라고 말했다.
최근 10여 년간 탄수화물 영양소를 감지하는 체내의 센서나 센싱세포를 두뇌나 다른 기관에서 규명했고 이번 공동연구를 통해 장 세포에서 필수아미노산 결핍을 인지하는 원리를 밝힌 서성배 교수는 “여러 영양소가 미각에 의해 피상적으로 1차 감지되지만 어떻게 체내에서 인지되고 섭식행동을 유도하는 연구는 그의 중요성에 비해 아직 매우 제한적이다. 그 이유는 체내의 영양소 센서를 마우스나 복잡한 포유류에서 발견하기는 쉽지 않기에 유전자 조작이 용이한 초파리를 이용해서 영양소 센서를 초파리에서 규명한 후에 쥐나 인간에서 그의 대응체를 찾는 방법을 선택했다. 영양소 센서는 모든 개체에 중요하고 진화적으로도 보존이 돼 있을 것 같아 초파리에서 밝힌 센서들이 포유류에서도 비슷한 역할을 할 것이라고 추측된다. 영양소에는 탄수화물, 단백질, 지방 같은 거대영양소뿐 아니라 비타민, 아연, 소금 등 소량영양소가 존재하는데 그 센서들을 규명하고 섭식행동에 미치는 영향이나 대사 질환, 성인병에 관련성 연구는 더욱 증폭될 것이라 예상된다.”고 말했다.
김보람 박사가 제1 저자로 참여하고 우리 대학 서성배 교수, 서울대학교 이원재 교수가 공동교신저자로 참여한 이번 연구 결과는 국제학술지 ‘네이처(Nature)’ 5월 5일 자 온라인판에 게재됐다 (논문명 : Response of the Drosophila microbiome-gut-brain axis to amino acid deficit).
2021.05.07 조회수 28570
서성배 교수 연구팀, 동물의 식습관을 조절하는 원리 규명해 네이처 게재
우리 대학 생명과학과 서성배 교수 연구팀이 서울대학교 생명과학부 이원재 교수 연구팀과 공동연구를 통해 체내 단백질, 필수아미노산 부족을 감지하는 장 세포와 필수아미노산을 섭취하도록 섭식행동을 조절하는 구체적인 원리를 규명했다고 7일 밝혔다. 그뿐만 아니라, 공동연구팀은 필수아미노산을 생산하는 장내미생물이 이러한 메커니즘에 어떠한 영향을 미치는 지도 규명했다.
사람이든 동물이든 수분이 부족하면 갈증을 느끼고 물을 마시고, 혈당량이 떨어지면 당을 찾아 먹는다. 필수 영양소가 부족하면 자연스럽게 이를 섭취하기 위한 행동 변화가 있다는 것은 누구나 경험적으로 쉽게 알 수 있는 사실이다. 과학자들은 수분이나 당분뿐만 아니라 필수아미노산과 같은 영양소에 대해서도 동물들이 결핍을 인지하여 항상성을 유지하는 메커니즘을 가지고 있을 것이라 오랫동안 예상해 왔지만, 그동안 이를 구체적으로 밝힌 연구는 없었다.
필수아미노산 항상성은 수분 항상성보다 복잡한 메커니즘을 가질 수밖에 없다. 장내미생물의 종류에 따라 반드시 섭취해야 하는 필수아미노산의 종류가 달라지기 때문이다. 예를 들면, 코알라의 경우 주된 먹이가 되는 나뭇잎의 섬유질을 직접 소화하지 못하고, 장내미생물이 나뭇잎을 분해하여 흡수 가능한 영양소를 만들어 내면 이를 흡수한다. 그런데 장내미생물의 종류에 따라 분해할 수 있는 나뭇잎의 종류가 달라지고, 이에 따라 코알라의 식성도 달라진다. 이는 필수아미노산과 같이 미생물을 통해 합성이 가능한 영양소의 경우, 똑같은 종의 동물들이라 해도, 동일한 필수아미노산이 부족한 상황에서 각 개체가 보유하고 있는 장내미생물의 종류에 따라 다른 식성을 보일 수 있다는 것을 의미한다.
공동연구팀은 이번 연구에서 어떤 유전자가 체내 필수아미노산 부족을 감지하는지 찾아내고, 어떤 신호를 통해 부족한 아미노산을 섭취하도록 섭식행동을 조절하는지 규명했으며, 필수아미노산을 생산하는 장내미생물이 이러한 메커니즘에 어떠한 영향을 미치는지 확인하기 위한 실험을 진행했다.
연구진은 초파리에 필수아미노산이 결핍된 먹이를 제공하거나 유전적 결핍 혹은 유전자 조작을 이용해 필수아미노산을 생산하지 못하는 장내미생물을 초파리에 도입하면, 초파리의 장 호르몬 중 하나인 CNMa 호르몬의 발현이 유도됨을 확인했다. 흥미롭게도, 이 호르몬은 그동안 장 호르몬이 발현된다고 알려진 내분비세포 (enteroendocrine cells)가 아닌 장 상피세포(enterocytes)에서 발현되는데 이는 장 상피세포가 필수아미노산 결핍을 직접 인지한다는 것을 의미한다. 또한 공동연구팀은 CNMa 호르몬이 발현되는 과정에서 기존에 세포 내 아미노산 센서로 잘 알려진 Gcn2와 Tor 분자들이 관여한다는 사실도 증명했다. CNMa 호르몬의 수용체는 두뇌와 장 신경세포(enteric neuron)에서 발현하는데 CNMa 수용체를 발현하는 신경세포가 활성화되는지 여부에 따라 필수아미노산을 섭취하려는 섭식행동이 증가하거나 감소한다.
이번 논문은 동물이 필수아미노산의 부족을 인지한 후 필수아미노산이 풍부한 음식을 섭취하는 행동을 장내미생물-장-뇌 축(microbiome-gut-brain axis)을 통해 분자적 수준에서 설명한 최초의 논문이다.
제 1저자인 우리 대학 김보람 연구원은 “이번 연구 결과는 장내미생물에서 동물의 장 그리고 뇌로 이어지는 장내미생물-장-뇌 축을 통해 아미노산 결핍이 일어난다는 사실을 처음으로 밝혔다는데 큰 의미가 있으며, 초파리뿐만 아니라, 사람을 포함한 척추동물에서도 이런 경로를 통해 장내미생물이 동물의 식성을 조절할 가능성을 제기한다. 만약 장내미생물과 동물의 식습관이 장뇌 축을 통해 조절된다면, 미생물 섭취라는 방법을 통해 현대인의 불균형한 식습관으로 인한 만성 질병을 개선할 수도 있을 것이며, 그런 점에서 이 논문의 가치를 찾을 수 있다”라고 말했다.
최근 10여 년간 탄수화물 영양소를 감지하는 체내의 센서나 센싱세포를 두뇌나 다른 기관에서 규명했고 이번 공동연구를 통해 장 세포에서 필수아미노산 결핍을 인지하는 원리를 밝힌 서성배 교수는 “여러 영양소가 미각에 의해 피상적으로 1차 감지되지만 어떻게 체내에서 인지되고 섭식행동을 유도하는 연구는 그의 중요성에 비해 아직 매우 제한적이다. 그 이유는 체내의 영양소 센서를 마우스나 복잡한 포유류에서 발견하기는 쉽지 않기에 유전자 조작이 용이한 초파리를 이용해서 영양소 센서를 초파리에서 규명한 후에 쥐나 인간에서 그의 대응체를 찾는 방법을 선택했다. 영양소 센서는 모든 개체에 중요하고 진화적으로도 보존이 돼 있을 것 같아 초파리에서 밝힌 센서들이 포유류에서도 비슷한 역할을 할 것이라고 추측된다. 영양소에는 탄수화물, 단백질, 지방 같은 거대영양소뿐 아니라 비타민, 아연, 소금 등 소량영양소가 존재하는데 그 센서들을 규명하고 섭식행동에 미치는 영향이나 대사 질환, 성인병에 관련성 연구는 더욱 증폭될 것이라 예상된다.”고 말했다.
김보람 박사가 제1 저자로 참여하고 우리 대학 서성배 교수, 서울대학교 이원재 교수가 공동교신저자로 참여한 이번 연구 결과는 국제학술지 ‘네이처(Nature)’ 5월 5일 자 온라인판에 게재됐다 (논문명 : Response of the Drosophila microbiome-gut-brain axis to amino acid deficit).
2021.05.07 조회수 28570 -
 김대수 교수, 근긴장이상증 억제 신약 개발
우리 대학 생명과학과 김대수 교수 연구팀이 신경전달물질인 세로토닌을 억제하는 물질을 성분으로 포함해 근긴장이상증을 효율적으로 치료할 수 있는 신규 약물을 개발했다고 10일 밝혔다.
근긴장이상증은 의지와 무관하게 근육의 긴장이 증가해 통증과 함께 몸의 일부 또는 전신이 뒤틀리는 세계 3대 운동 질환 중 하나이며 스트레스가 많은 현대사회에서 환자 수가 증가하고 있다. 우리나라에서 2010년 2만 8 천여 명이던 환자가 2017년 통계로는 3만 5천여 명으로 약 25% 증가했다.
근긴장이상증은 발병 원인이 밝혀져 있지 않고 효과적인 치료약물이 없는 상황이다. 유일한 치료 방법으로는 보톡스 주사 혹은 수술로 해당 근육을 긴장시키는 신경 신호를 차단하거나 뇌를 전기로 자극하는 뇌 심부 전기자극 수술(DBS)을 받는 것이다.
김대수 교수 연구팀은 근긴장이상증 환자들이 스트레스 상황에서 증상이 심해지는 것에 주목했다. 스트레스를 받으면 전신에서 근긴장이상증을 나타내는 동물모델을 활용해 어떻게 스트레스가 근긴장이상증을 유발하는지를 연구했다. 연구 결과 스트레스를 받으면 세로토닌 신경의 활성이 증가해 세로토닌 분비가 늘어나며 늘어난 세로토닌은 5HT2A 라는 세로토닌 수용체에 작용해 근육을 긴장시킴을 밝혔다. 따라서 세로토닌 신경을 차단하거나 5HT2A 수용체를 억제하면 근긴장이상증을 치료할 수 있게 된다. 연구팀은 또한 5HT2A 수용체를 효과적으로 억제할 수 있는 약물을 개발해 근긴장이상증 치료에 기반을 마련했다.
김대수 교수가 주도하고 김정은 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `사이언스 어드밴시스(Science Advances)' 저널 3월 4일 字 온라인판에 게재됐다. (논문명 : Cerebellar 5HT-2A receptor mediates stress-induced onset of dystonia)
기존 치료법으로 알려진 보톡스 주사의 경우는 국소적인 근긴장이상에 적용할 수 있어 부위가 넓을 때 적용이 어려우며 내성이 생기면 투여량을 증가시켜야 한다. 또 다른 치료법인 뇌 심부 전기자극 수술(DBS)은 일부 환자들에게만 적용 가능하며 뇌수술의 위험을 감수해야 한다. 따라서 수술 없는 약물치료가 가능하다면 환자들의 증상 관리와 치료에 획기적인 전기를 마련하게 된다.
김대수 교수는 "이번 연구를 통해 개발된 근긴장이상증 치료제가 환자들의 삶의 질을 높이는 데 이바지하기를 바란다ˮ라며 "근긴장이상증뿐 아니라 근육 통증 등 스트레스에 의해 유발되는 다양한 운동 질환에도 적용할 수 있을 것이라 기대된다ˮ라고 말했다.
연구팀은 이번 연구성과를 바탕으로 설립된 신약 개발 회사인 ㈜뉴로토브(CEO 김대수)를 통해 근긴장이상증 치료제 개발을 위한 임상 연구를 준비 중이다.
이번 연구는 한국연구재단 초 융합 AI 원천기술개발 인프라, KAIST G-core 연구사업 및 글로벌특이점 과제의 지원을 통해 수행됐다.
2021.03.10 조회수 102965
김대수 교수, 근긴장이상증 억제 신약 개발
우리 대학 생명과학과 김대수 교수 연구팀이 신경전달물질인 세로토닌을 억제하는 물질을 성분으로 포함해 근긴장이상증을 효율적으로 치료할 수 있는 신규 약물을 개발했다고 10일 밝혔다.
근긴장이상증은 의지와 무관하게 근육의 긴장이 증가해 통증과 함께 몸의 일부 또는 전신이 뒤틀리는 세계 3대 운동 질환 중 하나이며 스트레스가 많은 현대사회에서 환자 수가 증가하고 있다. 우리나라에서 2010년 2만 8 천여 명이던 환자가 2017년 통계로는 3만 5천여 명으로 약 25% 증가했다.
근긴장이상증은 발병 원인이 밝혀져 있지 않고 효과적인 치료약물이 없는 상황이다. 유일한 치료 방법으로는 보톡스 주사 혹은 수술로 해당 근육을 긴장시키는 신경 신호를 차단하거나 뇌를 전기로 자극하는 뇌 심부 전기자극 수술(DBS)을 받는 것이다.
김대수 교수 연구팀은 근긴장이상증 환자들이 스트레스 상황에서 증상이 심해지는 것에 주목했다. 스트레스를 받으면 전신에서 근긴장이상증을 나타내는 동물모델을 활용해 어떻게 스트레스가 근긴장이상증을 유발하는지를 연구했다. 연구 결과 스트레스를 받으면 세로토닌 신경의 활성이 증가해 세로토닌 분비가 늘어나며 늘어난 세로토닌은 5HT2A 라는 세로토닌 수용체에 작용해 근육을 긴장시킴을 밝혔다. 따라서 세로토닌 신경을 차단하거나 5HT2A 수용체를 억제하면 근긴장이상증을 치료할 수 있게 된다. 연구팀은 또한 5HT2A 수용체를 효과적으로 억제할 수 있는 약물을 개발해 근긴장이상증 치료에 기반을 마련했다.
김대수 교수가 주도하고 김정은 박사가 제1 저자로 참여한 이번 연구 결과는 국제 학술지 `사이언스 어드밴시스(Science Advances)' 저널 3월 4일 字 온라인판에 게재됐다. (논문명 : Cerebellar 5HT-2A receptor mediates stress-induced onset of dystonia)
기존 치료법으로 알려진 보톡스 주사의 경우는 국소적인 근긴장이상에 적용할 수 있어 부위가 넓을 때 적용이 어려우며 내성이 생기면 투여량을 증가시켜야 한다. 또 다른 치료법인 뇌 심부 전기자극 수술(DBS)은 일부 환자들에게만 적용 가능하며 뇌수술의 위험을 감수해야 한다. 따라서 수술 없는 약물치료가 가능하다면 환자들의 증상 관리와 치료에 획기적인 전기를 마련하게 된다.
김대수 교수는 "이번 연구를 통해 개발된 근긴장이상증 치료제가 환자들의 삶의 질을 높이는 데 이바지하기를 바란다ˮ라며 "근긴장이상증뿐 아니라 근육 통증 등 스트레스에 의해 유발되는 다양한 운동 질환에도 적용할 수 있을 것이라 기대된다ˮ라고 말했다.
연구팀은 이번 연구성과를 바탕으로 설립된 신약 개발 회사인 ㈜뉴로토브(CEO 김대수)를 통해 근긴장이상증 치료제 개발을 위한 임상 연구를 준비 중이다.
이번 연구는 한국연구재단 초 융합 AI 원천기술개발 인프라, KAIST G-core 연구사업 및 글로벌특이점 과제의 지원을 통해 수행됐다.
2021.03.10 조회수 102965 -
 머리에 빛을 비춰 신경세포 재생과 공간기억 향상
뇌질환 상태에서 신경재생으로 일시적인 기억향상이 일어나는 기전이 밝혀졌다.
우리 대학 생명과학과 허원도 교수 연구팀은 머리에 빛을 비춰 뇌신경세포 내 Fas 수용체의 활성을 조절함으로써 신경재생과 공간기억 능력이 향상됨을 보였다.
Fas 수용체는 허혈성 뇌질환, 염증성 뇌질환, 퇴행성 신경질환 등 다양한 대뇌질환에 걸린 경우 발현이 유도되는 단백질이다. 일반적으로는 세포를 죽음에 이르게 하지만, 신경계의 다양한 세포들에서는 세포증식 관련 신호전달 경로를 활성화시켜 세포를 재생시킨다. 특히, 뇌질환에 걸린 경우 대뇌 해마의 신경재생에 Fas 수용체가 관련되어 있다는 사실이 알려져 왔으나, 연구방법의 한계로 세부적인 기전에 대해서는 아직 자세히 알려진 바가 없다. 또한, 질환이 있는 뇌에서 해마가 관장하는 공간기억이 Fas 단백질에 의해 어떻게 영향받는지에 대해서도 논란이 되어 왔다.
연구팀은 광수용체 단백질의 유전자에 Fas 수용체 단백질의 유전자를 결합시킴으로써 청색광을 쬐어주면 Fas 단백질의 활성이 유도되는 옵토파스(OptoFAS) 기술을 개발했다. 살아있는 생쥐 대뇌에 다양한 시간동안 빛을 쬐어주면서 시공간적으로 Fas 수용체 단백질의 활성을 조절함으로써 대뇌 해마에서 여러 신호전달 경로들이 순차적으로 활성화되고, 그 결과로 신경재생과 공간기억 능력이 향상된다는 것을 확인했다.
옵토파스(OptoFAS) 기술은 빛을 이용하여 세포의 기능을 조절하는 광유전학(Optogenetics) 기술이다. 배양시킨 세포나 살아있는 생쥐 머리에 청색광을 쬐어주면 광수용체 단백질 여러 개가 결합되며, 이 단백질 복합체가 하위 신호전달경로들을 활성화시킨다. 생체 내에 광섬유를 삽입하여 원하는 시간에 빛을 뇌 조직 내로 전달하는 방식으로 선택적으로 단백질을 활성화시킬 수 있다.
연구팀은 빛을 이용해 대뇌 해마의 치아이랑에 존재하는 미성숙신경세포에서 옵토파스를 활성화시키고, 빛을 쬐어주는 시간에 따라 미성숙신경세포와 신경줄기세포에서 각각 서로 다른 하위 신호전달경로가 활성화됨을 관찰했다. 또한 이 현상에 특정 뇌유래 신경성장인자가 관여함을 밝혀내었다. 반복적으로 충분한 시간동안 빛을 쬐어주면 해마 치아이랑의 신경줄기세포가 증식하는 성체 신경재생이 관찰되었으며, 실험 대상 쥐에서는 일시적으로 공간기억 능력이 향상됨을 밝혔다.
옵토파스 기술을 이용하면 약물을 처리하거나 유전자변형 쥐를 사용하였을 때 발생하는 여러 부작용이 없이 빛 자극만으로 쥐의 생리현상에 지장을 주지 않으면서 뇌신경세포에서 Fas 단백질의 활성을 실시간으로 조절할 수 있다. 질환이 있는 뇌에서 Fas 단백질이 활성화되어 질병에 맞서 대뇌의 기능을 보호하는 여러 가지 역할을 한다는 사실을 생각해볼 때, 향후 세포 수준을 물론 개체 수준까지 뇌질환 상태에서의 신경행동적인 변화를 규명하는 연구에 활용될 것으로 기대한다.
허원도 교수는 “옵토파스(OptoFAS) 기술을 이용하면 빛만으로 살아있는 개체의 신경세포 내에서 단백질의 활성과 신호전달 경로를 쉽게 조절할 수 있다”며 “이 기술이 뇌인지 과학 연구를 비롯해 향후 대뇌질환 치료제 개발 등에 다양하게 적용되길 바란다”고 말했다.
이번 연구결과는 국제 학술지 사이언스 어드밴시즈(Science Advances, IF 12.80)에 4월 23일 오전 3시(한국시간) 온라인 게재됐다.
2020.04.27 조회수 15970
머리에 빛을 비춰 신경세포 재생과 공간기억 향상
뇌질환 상태에서 신경재생으로 일시적인 기억향상이 일어나는 기전이 밝혀졌다.
우리 대학 생명과학과 허원도 교수 연구팀은 머리에 빛을 비춰 뇌신경세포 내 Fas 수용체의 활성을 조절함으로써 신경재생과 공간기억 능력이 향상됨을 보였다.
Fas 수용체는 허혈성 뇌질환, 염증성 뇌질환, 퇴행성 신경질환 등 다양한 대뇌질환에 걸린 경우 발현이 유도되는 단백질이다. 일반적으로는 세포를 죽음에 이르게 하지만, 신경계의 다양한 세포들에서는 세포증식 관련 신호전달 경로를 활성화시켜 세포를 재생시킨다. 특히, 뇌질환에 걸린 경우 대뇌 해마의 신경재생에 Fas 수용체가 관련되어 있다는 사실이 알려져 왔으나, 연구방법의 한계로 세부적인 기전에 대해서는 아직 자세히 알려진 바가 없다. 또한, 질환이 있는 뇌에서 해마가 관장하는 공간기억이 Fas 단백질에 의해 어떻게 영향받는지에 대해서도 논란이 되어 왔다.
연구팀은 광수용체 단백질의 유전자에 Fas 수용체 단백질의 유전자를 결합시킴으로써 청색광을 쬐어주면 Fas 단백질의 활성이 유도되는 옵토파스(OptoFAS) 기술을 개발했다. 살아있는 생쥐 대뇌에 다양한 시간동안 빛을 쬐어주면서 시공간적으로 Fas 수용체 단백질의 활성을 조절함으로써 대뇌 해마에서 여러 신호전달 경로들이 순차적으로 활성화되고, 그 결과로 신경재생과 공간기억 능력이 향상된다는 것을 확인했다.
옵토파스(OptoFAS) 기술은 빛을 이용하여 세포의 기능을 조절하는 광유전학(Optogenetics) 기술이다. 배양시킨 세포나 살아있는 생쥐 머리에 청색광을 쬐어주면 광수용체 단백질 여러 개가 결합되며, 이 단백질 복합체가 하위 신호전달경로들을 활성화시킨다. 생체 내에 광섬유를 삽입하여 원하는 시간에 빛을 뇌 조직 내로 전달하는 방식으로 선택적으로 단백질을 활성화시킬 수 있다.
연구팀은 빛을 이용해 대뇌 해마의 치아이랑에 존재하는 미성숙신경세포에서 옵토파스를 활성화시키고, 빛을 쬐어주는 시간에 따라 미성숙신경세포와 신경줄기세포에서 각각 서로 다른 하위 신호전달경로가 활성화됨을 관찰했다. 또한 이 현상에 특정 뇌유래 신경성장인자가 관여함을 밝혀내었다. 반복적으로 충분한 시간동안 빛을 쬐어주면 해마 치아이랑의 신경줄기세포가 증식하는 성체 신경재생이 관찰되었으며, 실험 대상 쥐에서는 일시적으로 공간기억 능력이 향상됨을 밝혔다.
옵토파스 기술을 이용하면 약물을 처리하거나 유전자변형 쥐를 사용하였을 때 발생하는 여러 부작용이 없이 빛 자극만으로 쥐의 생리현상에 지장을 주지 않으면서 뇌신경세포에서 Fas 단백질의 활성을 실시간으로 조절할 수 있다. 질환이 있는 뇌에서 Fas 단백질이 활성화되어 질병에 맞서 대뇌의 기능을 보호하는 여러 가지 역할을 한다는 사실을 생각해볼 때, 향후 세포 수준을 물론 개체 수준까지 뇌질환 상태에서의 신경행동적인 변화를 규명하는 연구에 활용될 것으로 기대한다.
허원도 교수는 “옵토파스(OptoFAS) 기술을 이용하면 빛만으로 살아있는 개체의 신경세포 내에서 단백질의 활성과 신호전달 경로를 쉽게 조절할 수 있다”며 “이 기술이 뇌인지 과학 연구를 비롯해 향후 대뇌질환 치료제 개발 등에 다양하게 적용되길 바란다”고 말했다.
이번 연구결과는 국제 학술지 사이언스 어드밴시즈(Science Advances, IF 12.80)에 4월 23일 오전 3시(한국시간) 온라인 게재됐다.
2020.04.27 조회수 15970 -
 이흥규 교수, 수지상세포 자식작용의 역할 규명
〈 이흥규 교수 〉
세포 항상성을 유지해주는 ‘자식작용’의 또 다른 기능이 보고됐다. 우리 대학 의과학대학원 이흥규 교수 연구팀이 T세포의 항암 활성이 유도되는 과정에서 수지상세포 자식작용이 기여함을 규명했다.
이번 연구결과는 국제학술지 ‘오토파지(Autophagy)’ 3월 22일 자에 게재됐다.
자식작용은 세포 내 노폐물 및 손상된 세포 소기관을 제거해 세포의 항상성을 유지하는 과정이다.
수지상세포는 병원균이나 암 항원을 인지해 T세포의 면역반응을 유도하는 세포이다. 방사선이나 항암제에 의해 암세포가 사멸하면 수지상세포가 이를 흡수‧제거하고, 자신의 표면에 항원을 제시해 T세포에 전달해주는 기능을 한다.
연구팀은 수지상세포의 자식작용이 T세포 활성화에서 핵심 역할을 한다는 것을 밝히고 항암 효과를 높일 수 있는 원리를 제시했다.
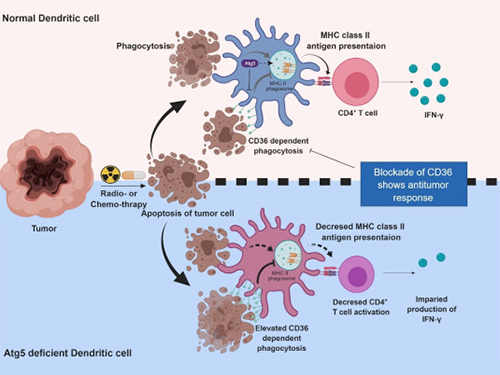
실험결과 자식작용을 일으키는 Atg5 유전자가 결손될 때 수지상세포의 T세포 활성화 기능이 떨어지고 항암 면역반응이 감소했다.
Atg5가 결손되면 수지상세포 표면의 CD36 수용체가 월등히 증가하는데, 이로 인해 식세포작용(암 항원의 흡수)만 과활성되고 항원 제시를 통한 T세포 활성화가 정상적으로 이뤄지지 않는다.
이때 항체를 도입해 CD36 수용체를 다시 억제하면 T세포 면역반응이 많이 증가하고 암의 성장이 억제됐다.
이흥규 교수는 “이번 연구를 통해 자식작용이 T세포의 항암 면역반응에 관여하는 기능을 새롭게 규명했다”라 “향후 CD36 수용체를 활용한 표적 항암치료제 개발의 단초가 되길 기대한다”라고 밝혔다.
이 연구성과는 과학기술정보통신부·한국연구재단 바이오‧의료기술개발사업의 지원으로 수행됐다.
□ 그림 설명
그림1. 수지상세포 자식작용의 기전
그림2. 항원제시에서 수지상세포 자식작용의 기능
2019.04.02 조회수 17767
이흥규 교수, 수지상세포 자식작용의 역할 규명
〈 이흥규 교수 〉
세포 항상성을 유지해주는 ‘자식작용’의 또 다른 기능이 보고됐다. 우리 대학 의과학대학원 이흥규 교수 연구팀이 T세포의 항암 활성이 유도되는 과정에서 수지상세포 자식작용이 기여함을 규명했다.
이번 연구결과는 국제학술지 ‘오토파지(Autophagy)’ 3월 22일 자에 게재됐다.
자식작용은 세포 내 노폐물 및 손상된 세포 소기관을 제거해 세포의 항상성을 유지하는 과정이다.
수지상세포는 병원균이나 암 항원을 인지해 T세포의 면역반응을 유도하는 세포이다. 방사선이나 항암제에 의해 암세포가 사멸하면 수지상세포가 이를 흡수‧제거하고, 자신의 표면에 항원을 제시해 T세포에 전달해주는 기능을 한다.
연구팀은 수지상세포의 자식작용이 T세포 활성화에서 핵심 역할을 한다는 것을 밝히고 항암 효과를 높일 수 있는 원리를 제시했다.
실험결과 자식작용을 일으키는 Atg5 유전자가 결손될 때 수지상세포의 T세포 활성화 기능이 떨어지고 항암 면역반응이 감소했다.
Atg5가 결손되면 수지상세포 표면의 CD36 수용체가 월등히 증가하는데, 이로 인해 식세포작용(암 항원의 흡수)만 과활성되고 항원 제시를 통한 T세포 활성화가 정상적으로 이뤄지지 않는다.
이때 항체를 도입해 CD36 수용체를 다시 억제하면 T세포 면역반응이 많이 증가하고 암의 성장이 억제됐다.
이흥규 교수는 “이번 연구를 통해 자식작용이 T세포의 항암 면역반응에 관여하는 기능을 새롭게 규명했다”라 “향후 CD36 수용체를 활용한 표적 항암치료제 개발의 단초가 되길 기대한다”라고 밝혔다.
이 연구성과는 과학기술정보통신부·한국연구재단 바이오‧의료기술개발사업의 지원으로 수행됐다.
□ 그림 설명
그림1. 수지상세포 자식작용의 기전
그림2. 항원제시에서 수지상세포 자식작용의 기능
2019.04.02 조회수 17767 -
 김필한 교수, 패혈증 환자의 폐 손상 원인 밝혀
〈 김필한 교수 〉
우리 대학 의과학대학원/나노과학기술대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 패혈증 폐에서 모세혈관과 혈액 내 순환 세포를 고해상도 촬영하는 데 성공했다.
연구팀은 패혈증 폐의 모세혈관 내부에서 백혈구의 일종인 호중구(好中球, neutrophil)들이 서로 응집하며 혈액 미세순환의 저해를 유발하고, 나아가 피가 통하지 않는 사강(死腔, dead space)을 형성함을 규명했다.
연구팀은 이 현상이 패혈증 모델의 폐손상으로 이어지는 조직 저산소증 유발의 원인이 되며, 호중구 응집을 해소하면 미세순환이 개선되며 저산소증도 함께 호전됨을 증명했다.
박인원 박사(현 분당서울대학교병원 응급의학과)가 주도한 이번 연구결과는 의학 분야 국제 학술지 ‘유럽호흡기학회지(European Respiratory Journal)’에 3월 28일 자에 게재됐다.
폐는 호흡을 통해 생명 유지의 필수 작용인 산소와 이산화탄소 간 가스 교환을 하는 기관으로 이는 적혈구들이 순환하는 수많은 모세혈관으로 둘러싸인 폐포(肺胞)에서 이뤄진다.
폐포의 미세순환 관찰을 위해 연구자들이 지속적인 노력을 하고 있으나 호흡을 위해 항상 움직이는 폐 안의 모세혈관과 적혈구의 미세순환을 고해상도로 촬영하는 것은 매우 어려웠다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 폐의 호흡 상태를 보존하면서 움직임을 최소화할 수 있는 영상 챔버를 새롭게 제작했다. 이를 통해 패혈증 동물모델의 폐에서 모세혈관 내부의 적혈구 순환 촬영에 성공했다.
이 과정에서 패혈증 모델의 폐에서 적혈구들이 순환하지 않는 공간인 사강이 증가하며 이곳에서 저산소증이 유발되는 것을 발견했다. 이는 혈액 내부의 호중구들이 모세혈관과 세동맥 내부에서 서로 응집하며 갇히는 현상으로 인해 발생함을 밝혔다. 갇힌 호중구들은 미세순환 저해, 활성산소의 다량 생산 등 패혈증 모델의 폐 조직 손상을 유발하는 것도 확인했다.
연구팀은 추가 연구를 통해 폐혈관 내부의 응집한 호중구가 전신을 순환하는 호중구에 비해 세포 간 부착에 관여하는 Mac-1 수용체(CD11b/CD18)가 높게 발현함을 증명했다. 이어 Mac-1 저해제를 패혈증 모델에 사용하여 호중구 응집으로 저해된 미세순환을 개선하고 저산소증의 호전과 폐부종 감소를 증명했다.
연구팀이 독자 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 폐 안 세포들의 실시간 영상촬영이 가능해 패혈증을 포함한 여러 폐 질환의 연구에 다양하게 활용될 것으로 기대된다.
연구팀의 폐 미세순환 영상촬영 및 정밀 분석 기법은 향후 미세순환과 연관된 다양한 질환들의 연구뿐 아니라 새로운 진단기술 개발 및 치료제의 평가를 위한 원천기술로 활용될 것으로 보인다.
김 교수 연구팀의 3차원 생체현미경 기술은 KAIST 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올인원 생체현미경 모델 ‘IVM-CM’과 ‘IVM-C’로 출시됐으며 여러 인간 질환의 복잡한 발생 과정을 밝히기 위한 기초 의․생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장에 핵심 장비로 활용될 예정이다.
김 교수는 “패혈증으로 인한 급성 폐손상 모델에서 폐 미세순환의 저해가 호중구로 인하여 발생하며, 이를 제어하면 미세순환 개선을 통해 저산소증 및 폐부종을 해소할 수 있어 패혈증 환자를 치료하는 새로운 전략이 될 수 있음을 새롭게 밝혀냈다.”고 말했다.
이번 연구는 의과학대학원 졸업생 박인원 박사가 1저자로 참여했고 유한재단 보건장학회, 교육부 글로벌박사펠로우쉽사업, 과학기술정보통신부의 글로벌프론티어사업과 이공분야기초연구사업, 그리고 보건복지부의 질환극복기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 초고속 레이저주사 3차원 생체현미경 시스템
그림2. 생체 내 폐 이미징 기술 개념도 및 사진
2019.04.01 조회수 23555
김필한 교수, 패혈증 환자의 폐 손상 원인 밝혀
〈 김필한 교수 〉
우리 대학 의과학대학원/나노과학기술대학원 김필한 교수 연구팀이 3차원 생체현미경 기술을 통해 패혈증 폐에서 모세혈관과 혈액 내 순환 세포를 고해상도 촬영하는 데 성공했다.
연구팀은 패혈증 폐의 모세혈관 내부에서 백혈구의 일종인 호중구(好中球, neutrophil)들이 서로 응집하며 혈액 미세순환의 저해를 유발하고, 나아가 피가 통하지 않는 사강(死腔, dead space)을 형성함을 규명했다.
연구팀은 이 현상이 패혈증 모델의 폐손상으로 이어지는 조직 저산소증 유발의 원인이 되며, 호중구 응집을 해소하면 미세순환이 개선되며 저산소증도 함께 호전됨을 증명했다.
박인원 박사(현 분당서울대학교병원 응급의학과)가 주도한 이번 연구결과는 의학 분야 국제 학술지 ‘유럽호흡기학회지(European Respiratory Journal)’에 3월 28일 자에 게재됐다.
폐는 호흡을 통해 생명 유지의 필수 작용인 산소와 이산화탄소 간 가스 교환을 하는 기관으로 이는 적혈구들이 순환하는 수많은 모세혈관으로 둘러싸인 폐포(肺胞)에서 이뤄진다.
폐포의 미세순환 관찰을 위해 연구자들이 지속적인 노력을 하고 있으나 호흡을 위해 항상 움직이는 폐 안의 모세혈관과 적혈구의 미세순환을 고해상도로 촬영하는 것은 매우 어려웠다.
연구팀은 자체 개발한 초고속 레이저 스캐닝 공초점 현미경과 폐의 호흡 상태를 보존하면서 움직임을 최소화할 수 있는 영상 챔버를 새롭게 제작했다. 이를 통해 패혈증 동물모델의 폐에서 모세혈관 내부의 적혈구 순환 촬영에 성공했다.
이 과정에서 패혈증 모델의 폐에서 적혈구들이 순환하지 않는 공간인 사강이 증가하며 이곳에서 저산소증이 유발되는 것을 발견했다. 이는 혈액 내부의 호중구들이 모세혈관과 세동맥 내부에서 서로 응집하며 갇히는 현상으로 인해 발생함을 밝혔다. 갇힌 호중구들은 미세순환 저해, 활성산소의 다량 생산 등 패혈증 모델의 폐 조직 손상을 유발하는 것도 확인했다.
연구팀은 추가 연구를 통해 폐혈관 내부의 응집한 호중구가 전신을 순환하는 호중구에 비해 세포 간 부착에 관여하는 Mac-1 수용체(CD11b/CD18)가 높게 발현함을 증명했다. 이어 Mac-1 저해제를 패혈증 모델에 사용하여 호중구 응집으로 저해된 미세순환을 개선하고 저산소증의 호전과 폐부종 감소를 증명했다.
연구팀이 독자 개발한 최첨단 고해상도 3차원 생체현미경 기술은 살아있는 폐 안 세포들의 실시간 영상촬영이 가능해 패혈증을 포함한 여러 폐 질환의 연구에 다양하게 활용될 것으로 기대된다.
연구팀의 폐 미세순환 영상촬영 및 정밀 분석 기법은 향후 미세순환과 연관된 다양한 질환들의 연구뿐 아니라 새로운 진단기술 개발 및 치료제의 평가를 위한 원천기술로 활용될 것으로 보인다.
김 교수 연구팀의 3차원 생체현미경 기술은 KAIST 교원창업기업인 아이빔테크놀로지(IVIM Technology, Inc)를 통해 상용화돼 올인원 생체현미경 모델 ‘IVM-CM’과 ‘IVM-C’로 출시됐으며 여러 인간 질환의 복잡한 발생 과정을 밝히기 위한 기초 의․생명 연구의 차세대 첨단 영상장비로서 미래 글로벌 바이오헬스 시장에 핵심 장비로 활용될 예정이다.
김 교수는 “패혈증으로 인한 급성 폐손상 모델에서 폐 미세순환의 저해가 호중구로 인하여 발생하며, 이를 제어하면 미세순환 개선을 통해 저산소증 및 폐부종을 해소할 수 있어 패혈증 환자를 치료하는 새로운 전략이 될 수 있음을 새롭게 밝혀냈다.”고 말했다.
이번 연구는 의과학대학원 졸업생 박인원 박사가 1저자로 참여했고 유한재단 보건장학회, 교육부 글로벌박사펠로우쉽사업, 과학기술정보통신부의 글로벌프론티어사업과 이공분야기초연구사업, 그리고 보건복지부의 질환극복기술개발사업의 지원을 받아 수행됐다.
□ 그림 설명
그림1. 초고속 레이저주사 3차원 생체현미경 시스템
그림2. 생체 내 폐 이미징 기술 개념도 및 사진
2019.04.01 조회수 23555 -
 고규영 교수, 녹내장 발생에 관여하는 신호전달체계 규명
우리 대학 의과학대학원 고규영 교수가 녹내장(Glaucoma)이 발생하고 진행되는 근본적 원인을 규명하고 새로운 치료방법을 제시했다.
김재령 박사과정이 1저자로 참여한 이번 연구는 미국 임상연구학회에서 발간하는 임상연구학회지(The Journal of Clinical Investigation) 9월 19일자 온라인 판에 게재됐다. 또한 10월 발간되는 인쇄본의 표지 및 커버스토리로 실린다.
녹내장은 안압이 상승해 시신경이 눌리거나 혈액 공급에 문제가 생겨 시신경이 망가지고 실명에 이르는 병이다. 증상이 나타날 땐 이미 시신경이 크게 손상된 상태라 완치가 어렵다. 전 세계 40세 이상 성인 인구의 3.5%가 녹내장을 앓고 있으며 국내에서도 환자가 빠르게 증가하는 추세다. 특히 전체 환자의 약 75% 이상을 차지하는 원발개방각녹내장의 경우 원인을 분자적 수준에서 밝히기 어려워 근본적인 치료법 마련에 한계가 있었다.
원발개방각녹내장 발병 기전의 이해를 넓힌 이번 연구로 그간 더뎠던 치료법 개발에 속도가 날 것으로 기대된다.
연구진은 안압이 안정적으로 유지되는 작동원리와 신호전달체계를 규명했다. 안압 조절에 중요한 기관인 쉴렘관의 항상성 유지를 Angiopoietin-TIE2 수용체 신호전달체계(이하 ANG-TIE2 신호전달체계)가 수행함을 밝혔다.
녹내장은 방수배출장치가 고장 나면서 발생한다. 눈 내부에서 생성된 방수는 섬유주를 지나 쉴렘관을 거쳐 혈관으로 배출된다. 안압은 방수가 생성되는 만큼 배출되어야 일정하게 유지되는데 방수배출장치에 문제가 생기면 안압이 상승한다. 원발개방각녹내장의 경우, 방수유출경로의 저항이 커지면서 방수가 제대로 빠져나가지 않아 발생하는 것으로 알려져 있으나 어떤 이유 때문에 저항이 커지는지는 알 수 없었다.
김재령 연구원과 박대영 연구원(박사후연구원/안과 전문의)은 혈관 성숙과 안정화에 필수적인 ANG 단백질과 TIE2 수용체가 각각 쉴렘관 주변부와 내피세포에 두드러지게 발현되는 것을 발견했다. 연구진은 ANG-TIE2 신호전달체계가 생후 초기 쉴렘관의 발달뿐만 아니라 성체가 된 이후에도 항상성 유지에 필수적일 것으로 예상했다.
실험 결과, 연구진은 쉴렘관 형성과 유지, 안압 조절에 있어 ANG-TIE2 신호전달체계가 핵심적인 역할을 수행함을 확인했다. ANG-TIE2 신호전달체계는 쉴렘관을 형성하고 내강을 유지해 방수 유출을 가능케 한다.
쉴렘관이 형성되는 동안에는 Prox1 전사인자 발현을 촉진하고 성체가 된 이후에는 적절한 양의 방수, 거대액포, Prox1 전사인자 발현을 유지하여 쉴렘관의 항상성을 지킨다.
연구진은 녹내장이 유발된 상황에서 ANG-TIE2 신호전달체계의 활성화가 어떤 효과가 있는지 추가 실험을 진행했다. TIE2 수용체를 활성화하는 실험적 항체(ABTAA)가 쉴렘관의 내피세포에 작용하여 방수 유출을 증가시키고 안압을 낮출 수 있는지가 관건이었다. 쉴렘관이 망가져 안압 상승으로 녹내장이 유발된 실험군의 눈 속에 항체를 투여한 결과, 쉴렘관이 회복되면서 안압이 내려가는 것을 확인했다. 결국 ANG-TIE2 신호전달체계가 쉴렘관의 항상성을 유지함으로써 안압을 조절해 녹내장이 발병하지 않도록 하는 것이다.
이번 연구는 녹내장을 근본적으로 해결할 수 있는 치료법 개발에 큰 도움이 될 것으로 보인다. 특히 녹내장을 재현한 질병 모델에 TIE2 활성 항체를 주사해 안압 하강 효과를 얻은 만큼 추후 임상 연구로의 확장이 기대된다. 연구진은 방수배출장치의 또 다른 요소인 섬유주와 ANG-TIE2 신호전달체계의 관계를 밝히는 실험과 실제 환자에게 TIE2 활성 항체를 사용할 수 있을지 전임상 실험을 계획 중이다.
연구를 이끈 고규영 교수는 “이번 논문에는 이십여 개에 달하는 연구 이미지 세트가 실렸다. 일반적인 경우의 두 배에 달한다”며 “쉴렘관 항상성 유지의 기전을 자세히 밝히는 방대한 양의 연구를 수행했음을 보여준다”라고 말했다.
□ 그림 설명
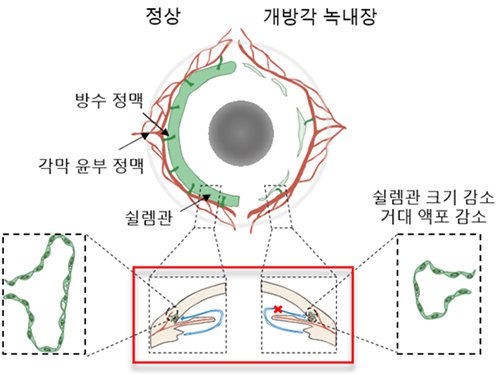
그림1. 녹내장의 증상과 원인
그림2. ANG-TIE2 신호전달체계의 역할
그림3. ANG-TIE2 신호전달체계 억제 시 쉴렘관 항상성 저해 현상
2017.09.20 조회수 19336
고규영 교수, 녹내장 발생에 관여하는 신호전달체계 규명
우리 대학 의과학대학원 고규영 교수가 녹내장(Glaucoma)이 발생하고 진행되는 근본적 원인을 규명하고 새로운 치료방법을 제시했다.
김재령 박사과정이 1저자로 참여한 이번 연구는 미국 임상연구학회에서 발간하는 임상연구학회지(The Journal of Clinical Investigation) 9월 19일자 온라인 판에 게재됐다. 또한 10월 발간되는 인쇄본의 표지 및 커버스토리로 실린다.
녹내장은 안압이 상승해 시신경이 눌리거나 혈액 공급에 문제가 생겨 시신경이 망가지고 실명에 이르는 병이다. 증상이 나타날 땐 이미 시신경이 크게 손상된 상태라 완치가 어렵다. 전 세계 40세 이상 성인 인구의 3.5%가 녹내장을 앓고 있으며 국내에서도 환자가 빠르게 증가하는 추세다. 특히 전체 환자의 약 75% 이상을 차지하는 원발개방각녹내장의 경우 원인을 분자적 수준에서 밝히기 어려워 근본적인 치료법 마련에 한계가 있었다.
원발개방각녹내장 발병 기전의 이해를 넓힌 이번 연구로 그간 더뎠던 치료법 개발에 속도가 날 것으로 기대된다.
연구진은 안압이 안정적으로 유지되는 작동원리와 신호전달체계를 규명했다. 안압 조절에 중요한 기관인 쉴렘관의 항상성 유지를 Angiopoietin-TIE2 수용체 신호전달체계(이하 ANG-TIE2 신호전달체계)가 수행함을 밝혔다.
녹내장은 방수배출장치가 고장 나면서 발생한다. 눈 내부에서 생성된 방수는 섬유주를 지나 쉴렘관을 거쳐 혈관으로 배출된다. 안압은 방수가 생성되는 만큼 배출되어야 일정하게 유지되는데 방수배출장치에 문제가 생기면 안압이 상승한다. 원발개방각녹내장의 경우, 방수유출경로의 저항이 커지면서 방수가 제대로 빠져나가지 않아 발생하는 것으로 알려져 있으나 어떤 이유 때문에 저항이 커지는지는 알 수 없었다.
김재령 연구원과 박대영 연구원(박사후연구원/안과 전문의)은 혈관 성숙과 안정화에 필수적인 ANG 단백질과 TIE2 수용체가 각각 쉴렘관 주변부와 내피세포에 두드러지게 발현되는 것을 발견했다. 연구진은 ANG-TIE2 신호전달체계가 생후 초기 쉴렘관의 발달뿐만 아니라 성체가 된 이후에도 항상성 유지에 필수적일 것으로 예상했다.
실험 결과, 연구진은 쉴렘관 형성과 유지, 안압 조절에 있어 ANG-TIE2 신호전달체계가 핵심적인 역할을 수행함을 확인했다. ANG-TIE2 신호전달체계는 쉴렘관을 형성하고 내강을 유지해 방수 유출을 가능케 한다.
쉴렘관이 형성되는 동안에는 Prox1 전사인자 발현을 촉진하고 성체가 된 이후에는 적절한 양의 방수, 거대액포, Prox1 전사인자 발현을 유지하여 쉴렘관의 항상성을 지킨다.
연구진은 녹내장이 유발된 상황에서 ANG-TIE2 신호전달체계의 활성화가 어떤 효과가 있는지 추가 실험을 진행했다. TIE2 수용체를 활성화하는 실험적 항체(ABTAA)가 쉴렘관의 내피세포에 작용하여 방수 유출을 증가시키고 안압을 낮출 수 있는지가 관건이었다. 쉴렘관이 망가져 안압 상승으로 녹내장이 유발된 실험군의 눈 속에 항체를 투여한 결과, 쉴렘관이 회복되면서 안압이 내려가는 것을 확인했다. 결국 ANG-TIE2 신호전달체계가 쉴렘관의 항상성을 유지함으로써 안압을 조절해 녹내장이 발병하지 않도록 하는 것이다.
이번 연구는 녹내장을 근본적으로 해결할 수 있는 치료법 개발에 큰 도움이 될 것으로 보인다. 특히 녹내장을 재현한 질병 모델에 TIE2 활성 항체를 주사해 안압 하강 효과를 얻은 만큼 추후 임상 연구로의 확장이 기대된다. 연구진은 방수배출장치의 또 다른 요소인 섬유주와 ANG-TIE2 신호전달체계의 관계를 밝히는 실험과 실제 환자에게 TIE2 활성 항체를 사용할 수 있을지 전임상 실험을 계획 중이다.
연구를 이끈 고규영 교수는 “이번 논문에는 이십여 개에 달하는 연구 이미지 세트가 실렸다. 일반적인 경우의 두 배에 달한다”며 “쉴렘관 항상성 유지의 기전을 자세히 밝히는 방대한 양의 연구를 수행했음을 보여준다”라고 말했다.
□ 그림 설명
그림1. 녹내장의 증상과 원인
그림2. ANG-TIE2 신호전달체계의 역할
그림3. ANG-TIE2 신호전달체계 억제 시 쉴렘관 항상성 저해 현상
2017.09.20 조회수 19336