%EC%9D%B8%EC%8A%90%EB%A6%B0
-
 성장 조절하는 인슐린 유사성장 인자의 비밀을 밝히다
인슐린유사성장인자(Insulin-like Growth Factor, IGF)는 인슐린과 유사한 분자구조를 가진 호르몬으로, 신체의 유지와 신진대사에 관여하며, 특히 태아 및 소아·청소년기 성장에 중요한 역할을 한다. 인슐린유사성장인자의 결핍은 느린 성장, 작은 체구, 지연된 발육과 같은 성장기 발달 장애, 그리고 성인에게는 골밀도와 근육강도 저하 등의 증상으로 나타난다. 인슐린유사성장인자의 과잉은 거인증 혹은 말단 비대증을 유발하고 다양한 성인병 위험도를 증가시킨다. 인슐린유사성장인자는 신체의 발달을 촉진시키는 작용 외에도 인슐린과 협동하여 혈당을 조절하는 작용도 하며, 종양의 발생에도 관여함이 알려져 있어, 인슐린유사성장인자의 작동 원리를 밝히기 위한 다양한 연구가 국내외에서 활발하게 진행 중이다.
우리 대학 의과학대학원 김호민 교수(기초과학연구원 (IBS), 바이오분자 및 세포구조연구단, Chief Investigator)는 인슐린유사성장인자 복합체의 3차원 분자구조를 규명하고, 인슐린유사성장인자 복합체의 조립과정 및 인슐린유사성장인자 활성화 메커니즘을 제시했다. 본 연구 결과는 성장과 대사에 관련된 다양한 질병에 대한 이해를 높이고 진단·치료제 개발에도 기여할 것으로 기대된다.
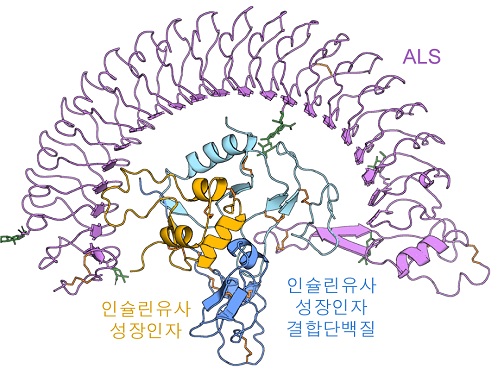
인슐린유사성장인자는 다양한 조직 세포막에 분포하는 인슐린유사성장인자 수용체를 활성화시켜 세포분열, 세포 증식·분화와 생존을 조절한다. 하지만 인슐린유사성장인자는 단독으로는 매우 불안정하여 체내반감기가 10분이 채 되지 않는다. 이 때문에 혈중 인슐린유사성장인자의 70% 이상은 체내에서 12시간 이상 머무를 수 있도록 인슐린유사성장인자 결합단백질들인 IGFBP 단백질(IGF Binding Protein), ALS 단백질(Acid labile subunit)과 결합하여 안정한 삼중복합체 형태로 존재한다.
IGFBP 단백질과 ALS 단백질은 인슐린유사성장인자와 결합하는 운반체 역할 뿐만 아니라 인슐린유사성장인자의 생물학적 작용을 조절하는 중요한 기능도 수행한다. 즉, 인슐린유사성장인자 삼중복합체(IGF1/IGFBP3/ALS)는 생체 내에서 아주 정교하게 조립되고, 필요시에만 활성화되어 적절하게 성장조절 효과를 나타낼 수 있게 된다. 이 때문에 인슐린유사성장인자와 이들 결합단백질의 혈중 농도는 성장호르몬결핍증, ALS 결핍증과 같은 성장관련 질환을 평가하는데 검사항목으로도 이용되고 있다.
연구진은 인슐린유사성장인자 삼중복합체의 3차원 분자구조를 초저온투과전자현미경(cryo-EM)을 활용하여 규명하고, 각 구성요소 간의 상호작용을 밝혀냈다. 특히, 인슐린유사성장인자가 IGFBP 단백질에 둘러쌓여 이중복합체를 이루고 있으며, 말발굽 모양의 ALS 단백질이 이중복합체를 한번 더 감싸는 안정된 구조로 인해 인슐린유사성장인자가 체내에서 쉽게 분해되지 않는 것을 발견했다.
또한, 다양한 생화학적 실험 방법을 통해 인슐린유사성장인자 삼중복합체의 순차적 조립과정과 삼중복합체로부터 인슐린유사성장인자가 분리되어 인슐린유사성장인자 수용체를 활성화시키는 분자 메커니즘을 규명했다. 인슐린유사성장인자 삼중복합체에 포함된 IGFBP 단백질이 생체 내 단백질분해효소에 의해 잘리면, IGFBP 단백질의 C-말단이 떨어져나가면서 불안정한 중간 삼중복합체가 형성된다. 이 과정이 인슐린유사성장인자가 활성을 나타내게 하는 핵심 과정임을 새롭게 발견했다.
김호민 교수는 “첨단 초저온투과전자현미경을 활용하여 고해상도 분자구조를 규명한 연구성과”라며, “인슐린유사성장인자 삼중복합체의 분자구조와 활성화 메커니즘은 향후 청소년기 성장 관련 연구 또는 인슐린유사성장인자 관련 질환의 진단 및 치료제 개발에 크게 기여할 것으로 기대한다.”라고 말했다.
이번 연구는 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications, IF 17.69)’ 온라인 판 7월 30일 자에 게재되었다.
2022.08.04 조회수 16961
성장 조절하는 인슐린 유사성장 인자의 비밀을 밝히다
인슐린유사성장인자(Insulin-like Growth Factor, IGF)는 인슐린과 유사한 분자구조를 가진 호르몬으로, 신체의 유지와 신진대사에 관여하며, 특히 태아 및 소아·청소년기 성장에 중요한 역할을 한다. 인슐린유사성장인자의 결핍은 느린 성장, 작은 체구, 지연된 발육과 같은 성장기 발달 장애, 그리고 성인에게는 골밀도와 근육강도 저하 등의 증상으로 나타난다. 인슐린유사성장인자의 과잉은 거인증 혹은 말단 비대증을 유발하고 다양한 성인병 위험도를 증가시킨다. 인슐린유사성장인자는 신체의 발달을 촉진시키는 작용 외에도 인슐린과 협동하여 혈당을 조절하는 작용도 하며, 종양의 발생에도 관여함이 알려져 있어, 인슐린유사성장인자의 작동 원리를 밝히기 위한 다양한 연구가 국내외에서 활발하게 진행 중이다.
우리 대학 의과학대학원 김호민 교수(기초과학연구원 (IBS), 바이오분자 및 세포구조연구단, Chief Investigator)는 인슐린유사성장인자 복합체의 3차원 분자구조를 규명하고, 인슐린유사성장인자 복합체의 조립과정 및 인슐린유사성장인자 활성화 메커니즘을 제시했다. 본 연구 결과는 성장과 대사에 관련된 다양한 질병에 대한 이해를 높이고 진단·치료제 개발에도 기여할 것으로 기대된다.
인슐린유사성장인자는 다양한 조직 세포막에 분포하는 인슐린유사성장인자 수용체를 활성화시켜 세포분열, 세포 증식·분화와 생존을 조절한다. 하지만 인슐린유사성장인자는 단독으로는 매우 불안정하여 체내반감기가 10분이 채 되지 않는다. 이 때문에 혈중 인슐린유사성장인자의 70% 이상은 체내에서 12시간 이상 머무를 수 있도록 인슐린유사성장인자 결합단백질들인 IGFBP 단백질(IGF Binding Protein), ALS 단백질(Acid labile subunit)과 결합하여 안정한 삼중복합체 형태로 존재한다.
IGFBP 단백질과 ALS 단백질은 인슐린유사성장인자와 결합하는 운반체 역할 뿐만 아니라 인슐린유사성장인자의 생물학적 작용을 조절하는 중요한 기능도 수행한다. 즉, 인슐린유사성장인자 삼중복합체(IGF1/IGFBP3/ALS)는 생체 내에서 아주 정교하게 조립되고, 필요시에만 활성화되어 적절하게 성장조절 효과를 나타낼 수 있게 된다. 이 때문에 인슐린유사성장인자와 이들 결합단백질의 혈중 농도는 성장호르몬결핍증, ALS 결핍증과 같은 성장관련 질환을 평가하는데 검사항목으로도 이용되고 있다.
연구진은 인슐린유사성장인자 삼중복합체의 3차원 분자구조를 초저온투과전자현미경(cryo-EM)을 활용하여 규명하고, 각 구성요소 간의 상호작용을 밝혀냈다. 특히, 인슐린유사성장인자가 IGFBP 단백질에 둘러쌓여 이중복합체를 이루고 있으며, 말발굽 모양의 ALS 단백질이 이중복합체를 한번 더 감싸는 안정된 구조로 인해 인슐린유사성장인자가 체내에서 쉽게 분해되지 않는 것을 발견했다.
또한, 다양한 생화학적 실험 방법을 통해 인슐린유사성장인자 삼중복합체의 순차적 조립과정과 삼중복합체로부터 인슐린유사성장인자가 분리되어 인슐린유사성장인자 수용체를 활성화시키는 분자 메커니즘을 규명했다. 인슐린유사성장인자 삼중복합체에 포함된 IGFBP 단백질이 생체 내 단백질분해효소에 의해 잘리면, IGFBP 단백질의 C-말단이 떨어져나가면서 불안정한 중간 삼중복합체가 형성된다. 이 과정이 인슐린유사성장인자가 활성을 나타내게 하는 핵심 과정임을 새롭게 발견했다.
김호민 교수는 “첨단 초저온투과전자현미경을 활용하여 고해상도 분자구조를 규명한 연구성과”라며, “인슐린유사성장인자 삼중복합체의 분자구조와 활성화 메커니즘은 향후 청소년기 성장 관련 연구 또는 인슐린유사성장인자 관련 질환의 진단 및 치료제 개발에 크게 기여할 것으로 기대한다.”라고 말했다.
이번 연구는 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications, IF 17.69)’ 온라인 판 7월 30일 자에 게재되었다.
2022.08.04 조회수 16961 -
 고규영 특훈교수 연구팀, 대사적으로 건강한 비만을 유도하는 원리 밝혔다
대사적으로 건강한 비만을 유도하는 원리가 밝혀졌다. 기초과학연구원(IBS, 원장 노도영) 혈관연구단 고규영 단장(우리 대학 의과학대학원 특훈교수) 연구팀은 혈관 생성을 촉진하는 단백질 ‘안지오포이에틴-2(Angiopoietin-2)’가 건강한 지방 축적 작용의 핵심요소임을 규명했다. 대사 기능에 대한 혈관의 역할과 지방 축적 기전을 이해함으로써 비만, 당뇨병, 고혈압 등 대사질환 치료에 새길을 열 것으로 기대된다.
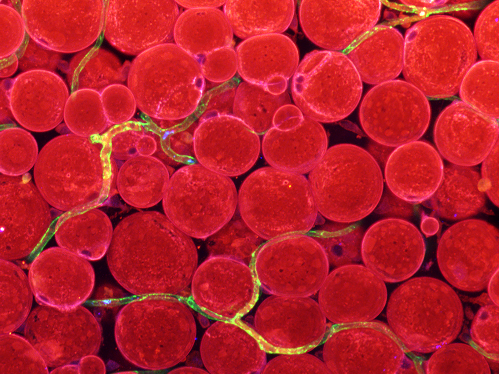
대사적으로 건강한 비만은 일반 비만에 비해 내장지방 축적이 적으며, 인슐린 저항성 수치, 혈압, 심혈관 질환 발병 위험이 낮다. 비만으로 인해 당 대사기능을 하는 간, 근육 등에 지방이 비정상적으로 축적되면 대사합병증 발병 위험이 높아지는데, 건강한 비만의 경우 혈중 지방이 주로 피하지방으로 축적되기 때문이다.
지방의 축적에는 모세혈관이 관여한다고 알려져 있다. 지방산전달인자들이 모세혈관에서 발현하고, 이들 인자는 모세혈관을 통해 지방의 주구성원인 지방산을 전달하여 지방세포로 축적시킨다. 모세혈관이 지방 축적을 위한 지방산의 전달자이자 이동통로인 셈이다. 그러나 이렇게 비만에 중요한 역할을 하는 모세혈관의 기능을 관장하는 요인과 기전은 밝혀지지 않았다.
이번 연구에서는 안지오포이에틴-2가 피하지방 모세혈관 내 지방산전달인자를 조절하여 건강한 비만을 유도하는 원리를 밝혀 기존의 한계를 극복했다. 연구팀은 피하지방 혈관에 특정 지방산전달인자들이 분포한다는 사실에 주목했다. 우선 건강한 비만환자의 피하지방에만 발현하는 물질을 찾기 위해 건강한 비만 환자군과 일반적인 비만 환자군을 비교분석했다. 그 결과 안지오포이에틴-2가 건강한 비만 환자의 피하지방에만 발현하는 유일한 분비 물질임을 발견했다. 안지오포이에틴-2가 건강한 지방 축적에 핵심 역할을 한다는 의미다. 실제로 안지오포이에틴-2를 지방세포에서 비활성화시킨 생쥐 모델에서 혈중 지방의 피하지방 축적이 감소하는 한편, 간‧골격근‧갈색지방 등에 비정상적으로 축적되어 인슐린 기능과 신진대사에 이상이 생겼다.
나아가 안지오포이에틴-2와 결합하는 ‘인테그린(Integrin)’수용체가 피하지방 혈관에 한해 발현함을 확인했다. 이어 혈관내피세포에서 수용체를 활성화시킨 결과 안지오포이에틴-2에 의한 지방산 전달이 크게 증가했다. 요컨대 인테그린 수용체에 안지오포이에틴-2가 결합하여 지방산전달인자들을 조절함으로써 피하지방으로만 지방을 전달하고 축적시키는 것이다.
배호성 선임연구원은 “혈관의 대사기능을 조절하여 피하지방에 선택적으로 혈중 지방이 축적될 수 있음을 밝혔다”며 “비만, 당뇨병 등 대사질환 치료에 새로운 접근법을 제시할 수 있을 것”이라고 전했다.
이번 연구결과는 국제 학술지 네이처 커뮤니케이션즈(Nature Communications, IF 11.878) 온라인판에 6월 12일 오후 7시(한국시간) 게재됐다.
2020.06.25 조회수 19766
고규영 특훈교수 연구팀, 대사적으로 건강한 비만을 유도하는 원리 밝혔다
대사적으로 건강한 비만을 유도하는 원리가 밝혀졌다. 기초과학연구원(IBS, 원장 노도영) 혈관연구단 고규영 단장(우리 대학 의과학대학원 특훈교수) 연구팀은 혈관 생성을 촉진하는 단백질 ‘안지오포이에틴-2(Angiopoietin-2)’가 건강한 지방 축적 작용의 핵심요소임을 규명했다. 대사 기능에 대한 혈관의 역할과 지방 축적 기전을 이해함으로써 비만, 당뇨병, 고혈압 등 대사질환 치료에 새길을 열 것으로 기대된다.
대사적으로 건강한 비만은 일반 비만에 비해 내장지방 축적이 적으며, 인슐린 저항성 수치, 혈압, 심혈관 질환 발병 위험이 낮다. 비만으로 인해 당 대사기능을 하는 간, 근육 등에 지방이 비정상적으로 축적되면 대사합병증 발병 위험이 높아지는데, 건강한 비만의 경우 혈중 지방이 주로 피하지방으로 축적되기 때문이다.
지방의 축적에는 모세혈관이 관여한다고 알려져 있다. 지방산전달인자들이 모세혈관에서 발현하고, 이들 인자는 모세혈관을 통해 지방의 주구성원인 지방산을 전달하여 지방세포로 축적시킨다. 모세혈관이 지방 축적을 위한 지방산의 전달자이자 이동통로인 셈이다. 그러나 이렇게 비만에 중요한 역할을 하는 모세혈관의 기능을 관장하는 요인과 기전은 밝혀지지 않았다.
이번 연구에서는 안지오포이에틴-2가 피하지방 모세혈관 내 지방산전달인자를 조절하여 건강한 비만을 유도하는 원리를 밝혀 기존의 한계를 극복했다. 연구팀은 피하지방 혈관에 특정 지방산전달인자들이 분포한다는 사실에 주목했다. 우선 건강한 비만환자의 피하지방에만 발현하는 물질을 찾기 위해 건강한 비만 환자군과 일반적인 비만 환자군을 비교분석했다. 그 결과 안지오포이에틴-2가 건강한 비만 환자의 피하지방에만 발현하는 유일한 분비 물질임을 발견했다. 안지오포이에틴-2가 건강한 지방 축적에 핵심 역할을 한다는 의미다. 실제로 안지오포이에틴-2를 지방세포에서 비활성화시킨 생쥐 모델에서 혈중 지방의 피하지방 축적이 감소하는 한편, 간‧골격근‧갈색지방 등에 비정상적으로 축적되어 인슐린 기능과 신진대사에 이상이 생겼다.
나아가 안지오포이에틴-2와 결합하는 ‘인테그린(Integrin)’수용체가 피하지방 혈관에 한해 발현함을 확인했다. 이어 혈관내피세포에서 수용체를 활성화시킨 결과 안지오포이에틴-2에 의한 지방산 전달이 크게 증가했다. 요컨대 인테그린 수용체에 안지오포이에틴-2가 결합하여 지방산전달인자들을 조절함으로써 피하지방으로만 지방을 전달하고 축적시키는 것이다.
배호성 선임연구원은 “혈관의 대사기능을 조절하여 피하지방에 선택적으로 혈중 지방이 축적될 수 있음을 밝혔다”며 “비만, 당뇨병 등 대사질환 치료에 새로운 접근법을 제시할 수 있을 것”이라고 전했다.
이번 연구결과는 국제 학술지 네이처 커뮤니케이션즈(Nature Communications, IF 11.878) 온라인판에 6월 12일 오후 7시(한국시간) 게재됐다.
2020.06.25 조회수 19766