%EC%BC%80%EB%AA%A8%EC%B9%B4%EC%9D%B8
-
 암세포 사멸과 연관된 대사를 관장하는 최상위인자 규명
우리 대학 생명과학과 강석조 교수 연구팀이 3차원 종양미세환경에서 성장한 암세포에서 유래한 케모카인(Chemokine) CXCL5가 암세포의 대사 리프로그래밍(reprogramming)을 조절하며 이를 통하여 지질 과산화물의 축적으로 인해 유도되는 세포 사멸인 페롭토시스(ferroptosis)에 대한 저항성을 획득한다고 7일 밝혔다.
CXCL5는 수용체인 CXCR2와의 결합을 통해 세포의 이동(migration) 및 침습(invasion)을 촉진하는 역할을 하는 케모카인으로, 종양미세환경에서 면역세포들의 침윤에 관여함이 알려져왔다. CXCL5는 여러 암종에서 발현이 증가되어 있음이 보고되었으나 실제 3차원 종양미세환경 내 암세포에서 유래한 CXCL5의 역할에 대해서는 밝혀진 바가 없다.
강 교수 연구팀은 세포외기질의 침착과 대식세포의 침투가 특징적인 암 미세환경을 모사하는 3차원 배양 시스템을 구축해 세포 간, 세포와 세포외기질 간 상호작용 뿐 아니라 종양미세환경 내 암세포의 위치에 따라 생장에 필요한 산소와 영양분의 접근성 차이로 인한 비세포적 요소가 형성될 수 있도록 유도하였다. 연구팀은 IFNγ자극을 받은 대식세포의 분비물이 3차원 환경 특이적으로 암세포의 CXCL5 발현을 증가시킴을 확인하였고, 야생형 암세포와 CXCL5 결손 암세포의 성장을 2차원, 3차원에서 비교한 결과 암세포의 CXCL5의 발현은 3차원 성장에만 필수적임을 확인하였다.
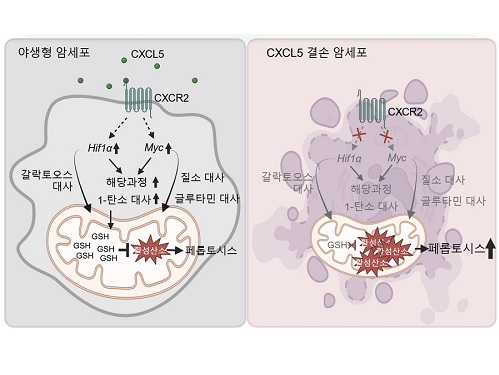
연구팀은 2차원 배양 암세포와 3차원 배양 암세포의 유전자 발현과 대사체를 비교하여 3차원에서 광범위한 대사 과정의 리프로그래밍이 일어남을 확인하였고, CXCL5가 이런 3차원 특이적 대사 리프로그래밍을 관장하는 핵심적 역할을 수행함을 보였다. 기전적으로 CXCL5는 전사인자 HIF-1a와 MYC의 발현을 유도하여 대사 리프로그래밍을 조절하며, 특히 여러 대사 과정 중 해당과정과 1-탄소 대사과정에 영향을 주는 것을 확인하였다.
또한, 연구팀은 저해된 해당과정과 1-탄소 대사과정이 산화-환원 항상성 조절에 중요한 역할을 한다는 이전 연구결과를 바탕으로, 세포 내 산화손상 정도를 측정한 결과 CXCL5 결손 시 미토콘드리아 활성산소와 철분에 의존하여 페롭토시스를 유발하는 지질 과산화물이 증가한 것을 확인하였다. 흥미롭게도 세포자멸사(apoptosis), 염증성 세포사멸인 파이롭토시스(pyroptosis), 그리고 구리 의존적 세포사멸인 큐프롭티시스(cuproptosis)는 CXCL5 결손에 의해 영향을 받지 않는 것을 밝혔다. 또한, HIF-1a와 MYC의 과발현은 CXCL5 결손 세포에서 보이는 활성산소와 지질 과산화물의 증가를 감소시키고 효과적으로 페롭토시스를 억제함을 확인하였다. CXCL5 수용체인 CXCR2를 결손시켰을 경우 동일하게 HIF-1a와 MYC의 발현이 저해되는 것을 확인함으로써, 암세포의 CXCL5-CXCR2 경로 억제를 통한 페롭토시스의 유도는 현재 개발 중인 세포자멸사 유도제의 한계를 극복할 새로운 전략이 될 수 있음을 시사하였다.
강석조 교수는 “본 연구는 3차원 종양미세환경 특이적인 암세포 대사를 보다 광범위하게 밝히고, 암세포에서 유래한 CXCL5가 HIF-1a와 MYC의 발현을 유도하여 3차원 성장을 위한 암대사 리프로그래밍을 총괄하는 지휘자적인 역할을 수행함을 새롭게 밝힌 연구”라고 언급하면서, “본 연구 성과는 암세포 대사 과정과 세포사멸 저항성 획득의 연결고리를 끊을 수 있는 차별적인 기전을 제시함으로써 혁신적인 치료 전략을 제공할 것으로 기대한다”고 전했다.
이번 연구 결과는 세포사멸의 권위있는 국제 학술지 `셀 데쓰 앤 디퍼런시에이션(Cell Death and Differentiation)’에 3월 7일 字 온라인판으로 게재됐다 (논문명: Cancer-intrinsic Cxcl5 orchestrates a global metabolic reprogramming for resistance to oxidative cell death in 3D). KAIST 생명과학과 서라민 박사가 제 1저자로 연구를 주도하였고, 서울대학교 Arvie Camille V. de Guzman 박사와 박성혁 교수, 그리고 한국표준과학연구원의 이지연 박사가 함께 연구에 참여하였다.
이번 연구는 한국연구재단의 바이오∙의료기술개발사업과 개인기초연구사업(중견연구) 지원을 받아 수행됐다.
2025.03.07 조회수 3166
암세포 사멸과 연관된 대사를 관장하는 최상위인자 규명
우리 대학 생명과학과 강석조 교수 연구팀이 3차원 종양미세환경에서 성장한 암세포에서 유래한 케모카인(Chemokine) CXCL5가 암세포의 대사 리프로그래밍(reprogramming)을 조절하며 이를 통하여 지질 과산화물의 축적으로 인해 유도되는 세포 사멸인 페롭토시스(ferroptosis)에 대한 저항성을 획득한다고 7일 밝혔다.
CXCL5는 수용체인 CXCR2와의 결합을 통해 세포의 이동(migration) 및 침습(invasion)을 촉진하는 역할을 하는 케모카인으로, 종양미세환경에서 면역세포들의 침윤에 관여함이 알려져왔다. CXCL5는 여러 암종에서 발현이 증가되어 있음이 보고되었으나 실제 3차원 종양미세환경 내 암세포에서 유래한 CXCL5의 역할에 대해서는 밝혀진 바가 없다.
강 교수 연구팀은 세포외기질의 침착과 대식세포의 침투가 특징적인 암 미세환경을 모사하는 3차원 배양 시스템을 구축해 세포 간, 세포와 세포외기질 간 상호작용 뿐 아니라 종양미세환경 내 암세포의 위치에 따라 생장에 필요한 산소와 영양분의 접근성 차이로 인한 비세포적 요소가 형성될 수 있도록 유도하였다. 연구팀은 IFNγ자극을 받은 대식세포의 분비물이 3차원 환경 특이적으로 암세포의 CXCL5 발현을 증가시킴을 확인하였고, 야생형 암세포와 CXCL5 결손 암세포의 성장을 2차원, 3차원에서 비교한 결과 암세포의 CXCL5의 발현은 3차원 성장에만 필수적임을 확인하였다.
연구팀은 2차원 배양 암세포와 3차원 배양 암세포의 유전자 발현과 대사체를 비교하여 3차원에서 광범위한 대사 과정의 리프로그래밍이 일어남을 확인하였고, CXCL5가 이런 3차원 특이적 대사 리프로그래밍을 관장하는 핵심적 역할을 수행함을 보였다. 기전적으로 CXCL5는 전사인자 HIF-1a와 MYC의 발현을 유도하여 대사 리프로그래밍을 조절하며, 특히 여러 대사 과정 중 해당과정과 1-탄소 대사과정에 영향을 주는 것을 확인하였다.
또한, 연구팀은 저해된 해당과정과 1-탄소 대사과정이 산화-환원 항상성 조절에 중요한 역할을 한다는 이전 연구결과를 바탕으로, 세포 내 산화손상 정도를 측정한 결과 CXCL5 결손 시 미토콘드리아 활성산소와 철분에 의존하여 페롭토시스를 유발하는 지질 과산화물이 증가한 것을 확인하였다. 흥미롭게도 세포자멸사(apoptosis), 염증성 세포사멸인 파이롭토시스(pyroptosis), 그리고 구리 의존적 세포사멸인 큐프롭티시스(cuproptosis)는 CXCL5 결손에 의해 영향을 받지 않는 것을 밝혔다. 또한, HIF-1a와 MYC의 과발현은 CXCL5 결손 세포에서 보이는 활성산소와 지질 과산화물의 증가를 감소시키고 효과적으로 페롭토시스를 억제함을 확인하였다. CXCL5 수용체인 CXCR2를 결손시켰을 경우 동일하게 HIF-1a와 MYC의 발현이 저해되는 것을 확인함으로써, 암세포의 CXCL5-CXCR2 경로 억제를 통한 페롭토시스의 유도는 현재 개발 중인 세포자멸사 유도제의 한계를 극복할 새로운 전략이 될 수 있음을 시사하였다.
강석조 교수는 “본 연구는 3차원 종양미세환경 특이적인 암세포 대사를 보다 광범위하게 밝히고, 암세포에서 유래한 CXCL5가 HIF-1a와 MYC의 발현을 유도하여 3차원 성장을 위한 암대사 리프로그래밍을 총괄하는 지휘자적인 역할을 수행함을 새롭게 밝힌 연구”라고 언급하면서, “본 연구 성과는 암세포 대사 과정과 세포사멸 저항성 획득의 연결고리를 끊을 수 있는 차별적인 기전을 제시함으로써 혁신적인 치료 전략을 제공할 것으로 기대한다”고 전했다.
이번 연구 결과는 세포사멸의 권위있는 국제 학술지 `셀 데쓰 앤 디퍼런시에이션(Cell Death and Differentiation)’에 3월 7일 字 온라인판으로 게재됐다 (논문명: Cancer-intrinsic Cxcl5 orchestrates a global metabolic reprogramming for resistance to oxidative cell death in 3D). KAIST 생명과학과 서라민 박사가 제 1저자로 연구를 주도하였고, 서울대학교 Arvie Camille V. de Guzman 박사와 박성혁 교수, 그리고 한국표준과학연구원의 이지연 박사가 함께 연구에 참여하였다.
이번 연구는 한국연구재단의 바이오∙의료기술개발사업과 개인기초연구사업(중견연구) 지원을 받아 수행됐다.
2025.03.07 조회수 3166 -
 코로나19 감염 중증도 결정하는 인자 발견
코로나19로 위중, 중증 상태인 중환자가 6일 0시 기준 163명을 기록했다. 지난달 19일 12명이었던 위중, 중증 환자는 20여일 만에 13배 넘게 늘어났다. 이러한 심각한 상황에서 우리 연구진이 코로나19 중증 환자와 경증 환자를 쉽게 판별할 수 있는 바이오 마커(표시물)를 발견해 중증 코로나19에 대한 치료제 개발에 기대감을 높였다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 *'호중구'와 *'당질코르티코이드'의 연관성을 밝혀 코로나19의 중증도를 결정짓는 인자를 발견했다고 7일 밝혔다.
☞ 호중구(neutrophil) : 혈액의 전체 백혈구 중 50~70%를 차지하는 선천 면역세포로, 세균이나 곰팡이 감염 등에 대응하는 면역세포이다.
☞ 당질코르티코이드(glucocorticoid) : 글루코코르티코이드라고도 하며 콩팥 근처 부신의 부신 겉질에서 생성되는 호르몬으로, 다양한 신체 기능 조절에 관여한다. 특히, 면역반응을 억제하는 호르몬으로도 알려져 있다.
WHO에 의해 세계적 대유행(팬데믹)으로 지정된 코로나바이러스감염증(COVID-19)은 사람마다 증상이 판이하다. 따라서, 환자의 중증도를 예상 및 판별하기 위해서는 확실한 바이오 마커의 활용이 중요하며, 이들을 선별적으로 치료할 수 있는 표적 치료제가 매우 중요하다.
중증 코로나19 환자들은 급성 호흡곤란 증후군의 증상을 보이고 특히 폐 조직의 심한 손상이 관찰된다. 이에 대응해 호중구 등 다양한 면역세포들이 바이러스 감염으로부터 숙주를 보호하기 위해 면역반응을 보이지만 사이토카인 폭풍(과잉 염증반응)처럼 과도한 면역반응으로 오히려 장기를 손상시킬 수도 있다.
이 교수 연구팀은 유전자 발현 옴니버스(GEO)에 공개된 코로나19 감염 경증 및 중증 환자의 기관지 폐포 세척액에 존재하는 단일세포 유전 정보를 분석했다. 그 결과, 그동안 곰팡이나 세균 감염에서만 중요성이 알려졌고 바이러스 감염 시에는 상대적으로 중요성이 알려지지 않았던 호중구의 과활성화로 인해 중증 코로나19가 발생함을 밝혔다.
특히 연구팀은 대식세포 등의 골수 유래 면역세포 내에서 발현하는 CXCL8과 같은 *케모카인에 의해 호중구 유입이 증가함을 밝혔다. 연구팀은 골수에서 유래한 면역세포 내의 당질코르티코이드 수용체 발현에 따라 CXCL8의 생성이 조절받으며, 이것이 결과적으로 호중구의 유입 및 활성도와 연관됨을 밝혔다.
☞ 케모카인(chemokine): 백혈구유주작용, 활성화작용을 하는 염기성헤파린 결합성 저분자 단백질
이 교수는 "이번 연구 결과는 코로나19의 중증도를 결정하는 바이오 마커를 발굴한 것 뿐만 아니라, 덱사메타손 등의 당질코르티코이드 억제제를 활용해 중증도를 개선할 치료제 개발에 단초를 제공할 수 있을 것으로 기대한다"고 밝혔다.
의과학대학원 박장현 석박사통합과정 대학원생이 제1 저자로 참여한 이번 연구는 국제면역학회연합에서 발간하는 면역학 전문 학술지인 '프론티어스 인 이뮤놀로지(Frontiers in Immunology)' 8월 28일 字 온라인판에 게재됐다. (논문명: Re-analysis of Single Cell Transcriptome Reveals That the NR3C1-CXCL8-Neutrophil Axis Determines the Severity of COVID-19)
한편 이번 연구는 과학기술정보통신부의 코리아 바이오 그랜드 챌린지사업, 신약타겟발굴 및 검증사업 및 KAIST 코로나 대응 과학기술 뉴딜사업을 받아 수행됐다.
2020.09.07 조회수 29290
코로나19 감염 중증도 결정하는 인자 발견
코로나19로 위중, 중증 상태인 중환자가 6일 0시 기준 163명을 기록했다. 지난달 19일 12명이었던 위중, 중증 환자는 20여일 만에 13배 넘게 늘어났다. 이러한 심각한 상황에서 우리 연구진이 코로나19 중증 환자와 경증 환자를 쉽게 판별할 수 있는 바이오 마커(표시물)를 발견해 중증 코로나19에 대한 치료제 개발에 기대감을 높였다.
우리 대학 의과학대학원 이흥규 교수 연구팀이 *'호중구'와 *'당질코르티코이드'의 연관성을 밝혀 코로나19의 중증도를 결정짓는 인자를 발견했다고 7일 밝혔다.
☞ 호중구(neutrophil) : 혈액의 전체 백혈구 중 50~70%를 차지하는 선천 면역세포로, 세균이나 곰팡이 감염 등에 대응하는 면역세포이다.
☞ 당질코르티코이드(glucocorticoid) : 글루코코르티코이드라고도 하며 콩팥 근처 부신의 부신 겉질에서 생성되는 호르몬으로, 다양한 신체 기능 조절에 관여한다. 특히, 면역반응을 억제하는 호르몬으로도 알려져 있다.
WHO에 의해 세계적 대유행(팬데믹)으로 지정된 코로나바이러스감염증(COVID-19)은 사람마다 증상이 판이하다. 따라서, 환자의 중증도를 예상 및 판별하기 위해서는 확실한 바이오 마커의 활용이 중요하며, 이들을 선별적으로 치료할 수 있는 표적 치료제가 매우 중요하다.
중증 코로나19 환자들은 급성 호흡곤란 증후군의 증상을 보이고 특히 폐 조직의 심한 손상이 관찰된다. 이에 대응해 호중구 등 다양한 면역세포들이 바이러스 감염으로부터 숙주를 보호하기 위해 면역반응을 보이지만 사이토카인 폭풍(과잉 염증반응)처럼 과도한 면역반응으로 오히려 장기를 손상시킬 수도 있다.
이 교수 연구팀은 유전자 발현 옴니버스(GEO)에 공개된 코로나19 감염 경증 및 중증 환자의 기관지 폐포 세척액에 존재하는 단일세포 유전 정보를 분석했다. 그 결과, 그동안 곰팡이나 세균 감염에서만 중요성이 알려졌고 바이러스 감염 시에는 상대적으로 중요성이 알려지지 않았던 호중구의 과활성화로 인해 중증 코로나19가 발생함을 밝혔다.
특히 연구팀은 대식세포 등의 골수 유래 면역세포 내에서 발현하는 CXCL8과 같은 *케모카인에 의해 호중구 유입이 증가함을 밝혔다. 연구팀은 골수에서 유래한 면역세포 내의 당질코르티코이드 수용체 발현에 따라 CXCL8의 생성이 조절받으며, 이것이 결과적으로 호중구의 유입 및 활성도와 연관됨을 밝혔다.
☞ 케모카인(chemokine): 백혈구유주작용, 활성화작용을 하는 염기성헤파린 결합성 저분자 단백질
이 교수는 "이번 연구 결과는 코로나19의 중증도를 결정하는 바이오 마커를 발굴한 것 뿐만 아니라, 덱사메타손 등의 당질코르티코이드 억제제를 활용해 중증도를 개선할 치료제 개발에 단초를 제공할 수 있을 것으로 기대한다"고 밝혔다.
의과학대학원 박장현 석박사통합과정 대학원생이 제1 저자로 참여한 이번 연구는 국제면역학회연합에서 발간하는 면역학 전문 학술지인 '프론티어스 인 이뮤놀로지(Frontiers in Immunology)' 8월 28일 字 온라인판에 게재됐다. (논문명: Re-analysis of Single Cell Transcriptome Reveals That the NR3C1-CXCL8-Neutrophil Axis Determines the Severity of COVID-19)
한편 이번 연구는 과학기술정보통신부의 코리아 바이오 그랜드 챌린지사업, 신약타겟발굴 및 검증사업 및 KAIST 코로나 대응 과학기술 뉴딜사업을 받아 수행됐다.
2020.09.07 조회수 29290